Похожие презентации:
Получение меламина из карбамида
1. Получение меламина из карбамида
12. Меламин
Мелами́н (1, 3, 5-триазин-2, 4, 6-триамин) — бесцветные кристаллы,малорастворимые в воде. Объём мирового производства в 2007 году
составил более 1 млн тонн.
Для обнаружения используется хроматография. Гравиметрически
меламин определяют в виде солей с циануровой или пикриновой
кислотой, а также фотометрически в слабокислой среде по поглощению
при длине волны 236 нм.
2
3. Применение
Меламин широко применяется в промышленном органическом синтезе, втом числе ионообменных смол, дубителей, гексахлормеламина,
используемого в производстве красителей и гербицидов. Меламин,
наряду c мочевиной, также применялся в качестве небелкового
источника азота для домашнего скота, однако в 1978 году был сделан
вывод о «неприемлемости меламина как небелкового источника азота,
так как он медленнее и недостаточно полно гидролизуется по
сравнению с другими — например, мочевиной».
Большая часть производимого меламина используется в производстве
меламин-формальдегидных смол, относимых к группе аминопластов,
которые получают поликонденсацией меламина с формальдегидом в
слабощелочной среде (рН 7,8—8,5), при этом на начальной стадии
происходит гидроксиметилирование меламина по аминогруппам, с
образованием метилольных производных различной степени замещения
(вплоть до гексаметилолмеламина):
3
4.
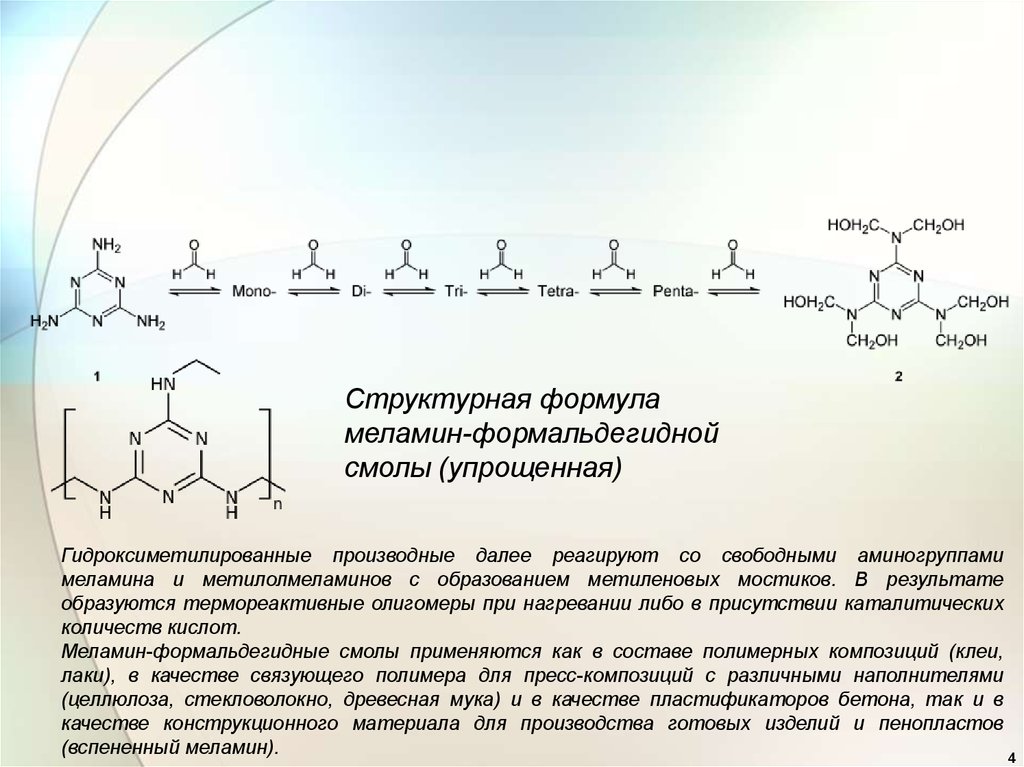
Структурная формуламеламин-формальдегидной
смолы (упрощенная)
Гидроксиметилированные производные далее реагируют со свободными аминогруппами
меламина и метилолмеламинов с образованием метиленовых мостиков. В результате
образуются термореактивные олигомеры при нагревании либо в присутствии каталитических
количеств кислот.
Меламин-формальдегидные смолы применяются как в составе полимерных композиций (клеи,
лаки), в качестве связующего полимера для пресс-композиций с различными наполнителями
(целлюлоза, стекловолокно, древесная мука) и в качестве пластификаторов бетона, так и в
качестве конструкционного материала для производства готовых изделий и пенопластов
(вспененный меламин).
4
5. Свойства и синтез
tпл =364 °C (с разложением); Растворим в воде (0,5 % по массе при 20 °C, 4 % при 90 °C), не растворим в органическихрастворителях. Меламин — основание, с кислотами образует соли (C3H6N6×HCl и др.), разлагающиеся при
нагревании. В жидком аммиаке с амидами щелочных металлов меламин образует как продукты присоединения
C3H6N6•MNH2 так и соли, M3C3H3N6 (M — металл).
При нагревании до 354 °С и выше меламин отщепляет аммиак с образованием мелема (2,6,10-триамино-симгептазина).
Характерным свойством меламина является замещение аминогрупп под действием нуклеофилов. Так, в водных
растворах щелочей при повышенных температурах и давлениях меламин гидролизуется, отщепляя аммиак, при
этом происходит последовательное замещение аминогрупп на гидроксильные группы с образованием аммелина (2гидрокси-4,6-диамино-сим-триазина), аммелида (2,4-дигидрокси-6-диамино-сим-триазина) и циануровой кислоты
(2,4,6-тригидрокси-сим-триазина). Под действием алкиламинов или их солей аминогруппы меламина замещаются
аминоалкильными группами с образованием N-алкилмеламинов, степень замещения (от одного до трех)
определяется степенью избытка амина.
Под действием электрофильных агентов происходит замещение атомов водорода аминогрупп меламина:
нитрование азотной кислотой в уксусной кислоте ведет к образованию моно- и ди-N-нитромеламинов.
Галогенирование ведет к образованию N-галогенмеламинов различной степени замещения, при хлорировании может
быть получен гексахлормеламин, являющийся энергичным хлорирующим агентом и применяющийся в составе
композиций для дегазации отравляющих веществ.
В лабораторных условиях простейшим методом синтеза меламина является взаимодействие цианурхлорида с
аммиаком при 100 °C, другими методами являются синтезы меламина нагреванием гуанидина и тримеризацией
цианамида.
В промышленности применяется два основных метода синтеза меламина — пиролиз мочевины и синтез из
дициандиамида.
При пиролизе мочевины применяются катализаторы (на онове Al2O3 и др.) при 350—450 °C и давлении 50—200 МПа,
при этом на первой стадии мочевина отщепляет аммиак с образованием циановой кислоты:
5
6. Свойства и синтез
(NH2)2CO → HCNO + NH3 которая затем с отщеплением углекислого газа образует меламин:6 HCNO → C3H6N6 + 3 CO2
Другим методом является синтез из дициандиамида (NH2CN)2 в жидком аммиаке или растворе аммиака в этаноле
при температуре 180—500 °C и давлении 4—20 МПа (40—200 кг/см²). Исторически первым промышленным методом
стало производство меламина из дициандиамида, получаемого, в свою очередь, из карбида кальция, однако по мере
роста крупнотоннажного производства мочевины дициандиамидный процесс был вытеснен процессом пиролиза
мочевины.
25 мая 2012 года в Невинномысске (Ставропольский край) на ОАО «Невинномысский Азот» была запущена первая в
России установка по производству меламина и был получен первый отечественный меламин. Годовой объём
производства составляет 50 тысяч тонн.
6
7. Получение из карбамида
Меламин является ценным химическим соединением, которое применяют для получения меламиноформальдегидных полимеров, обладающих высокой механической прочностью, стойкостью в горячей воде иорганических растворителях, малой электропроводностью и высокой термостойкостью. Продукты,
синтезируемые на основе меламино-формальдегидных полимеров, используют в различных отраслях
промышленности: в электротехнической - для изготовления изоляторов, в текстильной – для производства
безусадочных и не мнущихся тканей и для придания им блеска, в бумажной – для получения водонепроницаемой
бумаги, в мебельной – для изготовления лаков, клеев, а также для приготовления дубителей, ионообменных смол,
дезинфицирующих веществ, медицинских препаратов, негорючих составов и др.
Меламин образуется из карбамида по реакции
6СО(NН2)2 = С3Н6N6 + 6NН3 + 3СО2.
Реакция протекает при ~600 К с образованием в качестве промежуточного продукта циануровой кислоты.
Зависимость равновесного выхода меламина от давления и температуры. С возрастанием давления при
постоянной температуре выход меламина уменьшается, так как равновесие реакции смещается в сторону
образования карбамида. Наоборот, при повышении температуры и постоянном давлении выход меламина
увеличивается. В зависимости от условий реакции можно добиться выхода меламина более 95%.
7
8. Получение
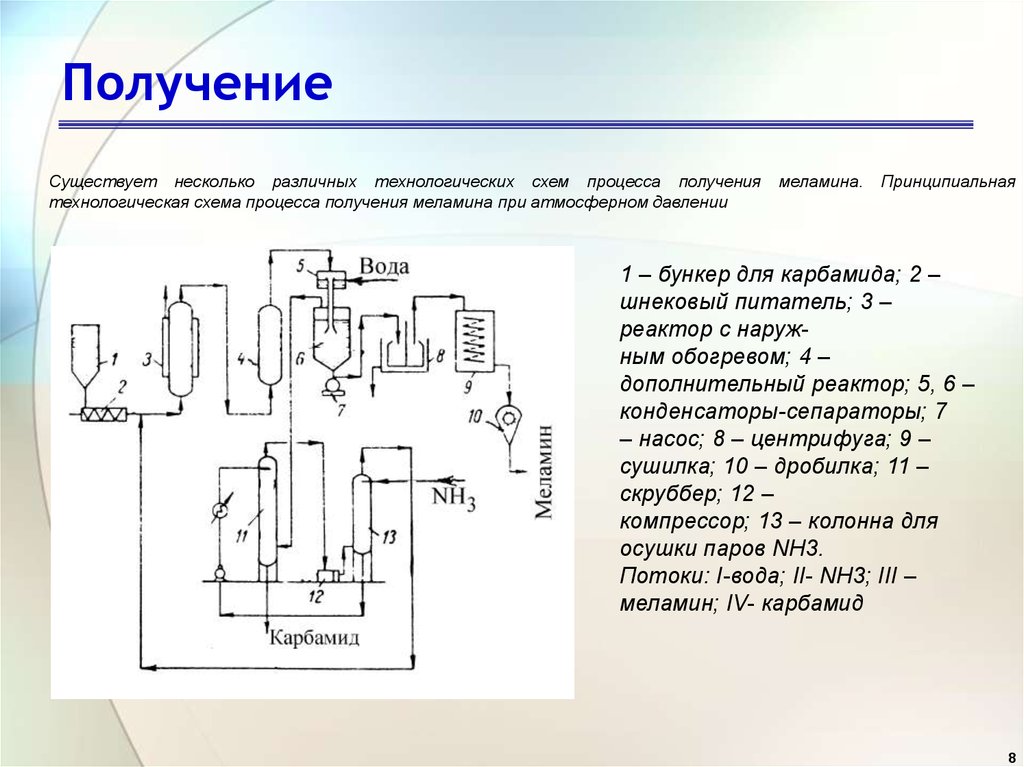
Существует несколько различных технологических схем процесса получениятехнологическая схема процесса получения меламина при атмосферном давлении
меламина.
Принципиальная
1 – бункер для карбамида; 2 –
шнековый питатель; 3 –
реактор с наружным обогревом; 4 –
дополнительный реактор; 5, 6 –
конденсаторы-сепараторы; 7
– насос; 8 – центрифуга; 9 –
сушилка; 10 – дробилка; 11 –
скруббер; 12 –
компрессор; 13 – колонна для
осушки паров NH3.
Потоки: I-вода; II- NH3; III –
меламин; IV- карбамид
8
9. Получение
По этой технологии синтез проводится в газовой фазе на катализаторе споследующим быстрым выделением меламина при охлаждении газов. Вначале
при сильном нагревании карбамид превращается в циановую кислоту,
которая затем, отщепляя диоксид углерода, образует меламин:
СО(NН2)2 = НNСО + NН3,
6НNСО = С3Н6N6 + 3СО2.
Карбамид из бункера 1 шнеком 2 подается в реактор 3 с внешним
подогревом, в котором при ~600 К он разлагается в "кипящем слое" с
образованием циановой кислоты и аммиака. Образовавшаяся смесь паров
циановой кислоты и аммиака направляется в реактор 4, в котором
происходит образование меламина. Выход меламина составляет 95%.
Меламин вследствие быстрого охлаждения выпадает в осадок в
конденсаторе 5 и далее через сепаратор 6 и центрифугу 8 направляется на
сушку и упаковку.
9








 Химия
Химия








