Похожие презентации:
Ядерные методы анализа
1. Ядерные методы анализа
Метод радиоактивных индикаторов(метод изотопных меток)
Метод широко применяется для контроля потерь на стадии
предварительного концентрирования микропримесей.
Перед проведением предварительного концентрирования к исходной
пробе добавляют радиоактивный изотоп в той же химической форме, что
и предполагаемый для определения химический элемент. Полнота
выделения микроэлемента легко контролируется измерением активности
концентрата или раствора, оставшегося после выделения микроэлемента.
Примесь, попадающая в образец в процессе пробоподготовки снижает
удельную активность добавляемого изотопа. По величине удельной
активности можно определить количество примеси, попавшей в образец
со стороны.
Пример. Выделение Ва из его смеси с Со и Sr. Используя радиоактивные
изотопы Sr89 и Ва140 было установлено, что в осадок ВаSO4 попадает
около 7% Sr, а 13% Ва остается в растворе (растворимость при 20 С:
BaSO4 – 2,3 10-4 г/(100 г раствора), а SrSO4 – 132 10-4 г/(100 г раствора)).
2.
Пример. Определим уровень концентрации, который можно почувствоватьметодом изотопных меток.
1 Ки=3,7 1010 Бк 2,2 1012 расп/мин.
Imin=100 имп/мин.
Amin
100имп / мин
1Ки 4,5 10 11 Ки
12
2,2 10 имп / мин
Введем изотопную метку трития. 1 г Т2 имеет активность А 104 Ки.
При Imin=100 имп/мин
4,5 10 11 Ки
15
mT2 min
4
,
5
10
г
4
10 Ки / г
Возьмем какое-либо вещество с молярной массой М=100 г/моль и введем в
него всего 1% трития. Тогда в 1 г смеси можно почувствовать примесь этого
вещества в количестве
4,5 10 15 100
1гсмеси
100 4,5 10 11 масс.%
Достоинства и недостатки:
Высокий предел обнаружения.
Для определения удельной активности требуется знание весового
количества вещества.
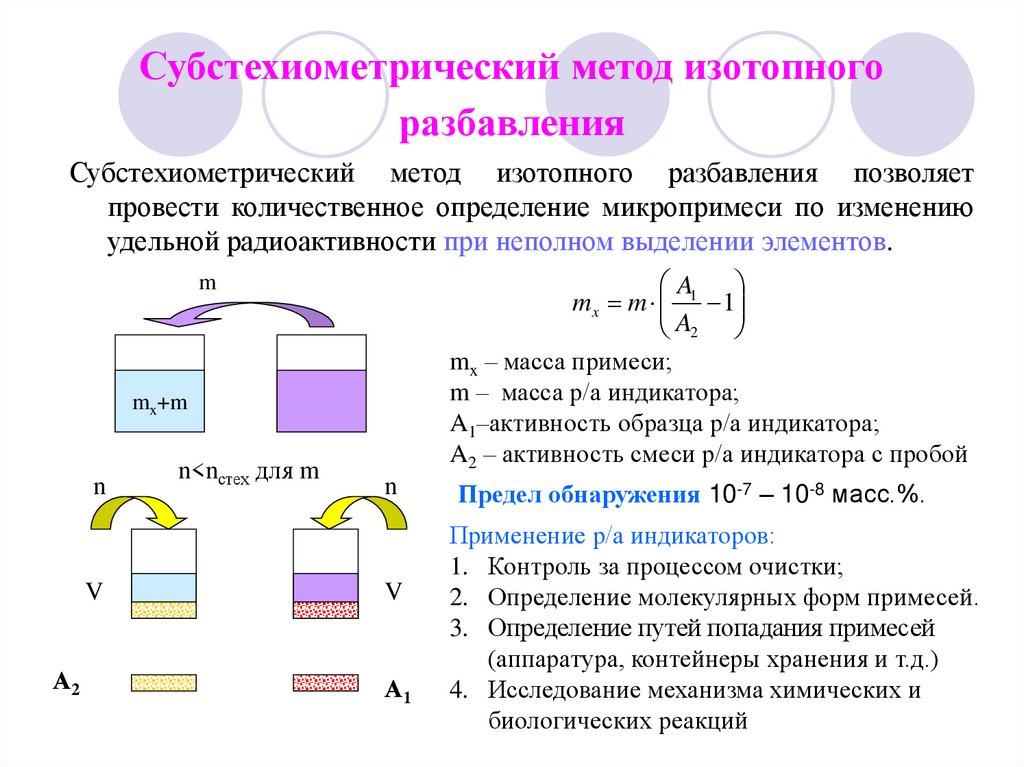
3. Субстехиометрический метод изотопного разбавления
Субстехиометрический метод изотопного разбавления позволяетпровести количественное определение микропримеси по изменению
удельной радиоактивности при неполном выделении элементов.
A
mx m 1 1
A2
mx – масса примеси;
m – масса р/а индикатора;
A1–активность образца р/а индикатора;
A2 – активность смеси р/а индикатора с пробой
m
mm
x
x+m
n
V
А2
n<nстех для m
n
V
А1
Предел обнаружения 10-7 – 10-8 масс.%.
Применение р/а индикаторов:
1. Контроль за процессом очистки;
2. Определение молекулярных форм примесей.
3. Определение путей попадания примесей
(аппаратура, контейнеры хранения и т.д.)
4. Исследование механизма химических и
биологических реакций
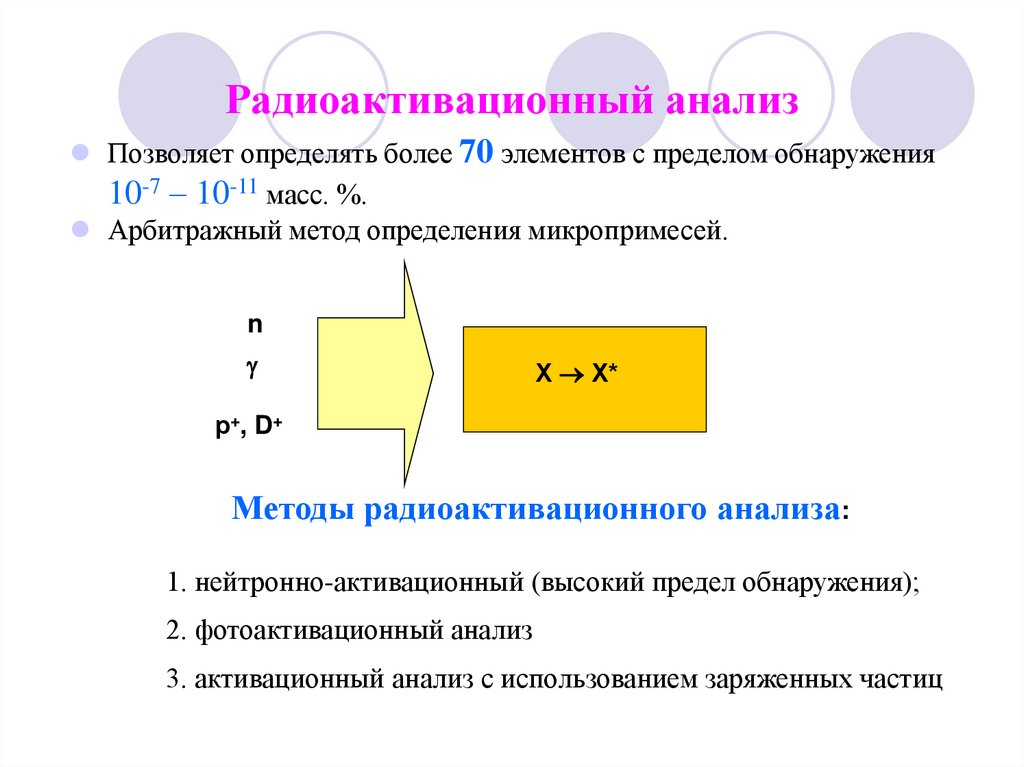
4. Радиоактивационный анализ
Позволяет определять более 70 элементов с пределом обнаружения10-7 – 10-11 масс. %.
Арбитражный метод определения микропримесей.
n
Х Х*
Х
р+, D+
Методы радиоактивационного анализа:
1. нейтронно-активационный (высокий предел обнаружения);
2. фотоактивационный анализ
3. активационный анализ с использованием заряженных частиц
5.
Скорость накопления радиоактивных ядер определяется двумя процессами– образования и распада.
*
dN
f N N *
d
f – поток ядерных частиц;
- сечение захвата частиц (эффективное сечение ядерной реакции);
N – число атомов активируемого элемента;
N* - число образующихся радиоактивных ядер;
- константа распада, которая равна 0,693 , Т – период полураспада;
T
- время облучения.
Если кроме р/а распада образующиеся N* ядра взаимодействуют с потоком
ядерных частиц, то в правую часть уравнения нужно добавить член
(-f 1 N*).
Принимая
f=const, =const и N=const
dN *
d
f N N
6.
Вводим граничные условия =0, N*=0 и интегрируем:N*
0
f N N* f N e
dN *
d
f N N *
0
N*
f N
1 e
• Измеренная активность образца после облучения : A N * f N 1 e
• Если между облучением и измерением прошло A f N 1 e e
время 1, то активность равна:
• Количество облучаемых атомов:
1
1
N 6,02 10 23
g
M
g – количество определяемого элемента; М – атомная масса определяемого
элемента; - доля активированного изотопа в определяемом элементе
(природный изотопный состав).
• Количество примеси:
g
M A 1
M N
6,02 1023 6,02 1023 f (1 e ) e 1
Это – абсолютный метод радиоактивационного анализа.
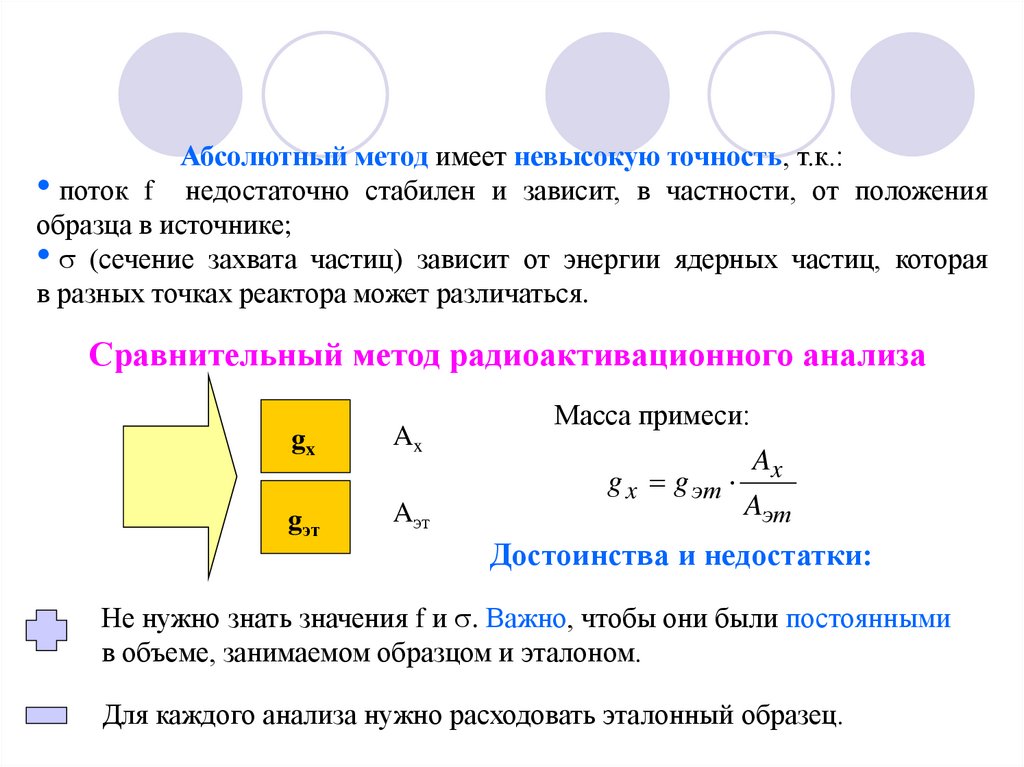
7.
Абсолютный метод имеет невысокую точность, т.к.:• поток f недостаточно стабилен и зависит, в частности, от положения
образца в источнике;
• (сечение захвата частиц) зависит от энергии ядерных частиц, которая
в разных точках реактора может различаться.
Сравнительный метод радиоактивационного анализа
gx
Ax
gэт
Aэт
Масса примеси:
Ax
g x g эт
Aэт
Достоинства и недостатки:
Не нужно знать значения f и . Важно, чтобы они были постоянными
в объеме, занимаемом образцом и эталоном.
Для каждого анализа нужно расходовать эталонный образец.