Похожие презентации:
Иммунологическая реактивность и ее нарушения у детей. Лекция №5
1.
Иммунологическая реактивностьи ее нарушения у детей
Шабалов Николай Павлович
Военно-медицинская академия
Кафедра детских болезней
им. М.С. Маслова
2. Иммунитет
Иммунитет способ обеспечения иподдержания антигенного гомеостаза.
Антигенное постоянство внутренней
среды, то есть присутствие в организме
лишь “своего”, необходимо для
регуляции функции собственных клеток
(чужое “ускользает” от контроля)
3.
ПРИОБРЕТЕННЫЙ ИММУНИТЕТ(профессор Михаил Николаевич Ярцев – заведующий отделением
иммунопатологии детей, ГНЦ Институт Иммунологии ФМБА)
• Память иммунная, так же, как и память
нейронная не наследуются, а приобретается с
возрастом ребенка.
• Процесс «обучения» иммунокомпетентных
клеток продолжается многие годы и
характеризуется постепенным нарастанием
объема информации об антигенах окружающей
среды и соответственно связан с расширением
спектра специфических антител и клеточных
популяций, несущих иммунную память.
• Кто же «учитель» иммунитета новорожденного?
4.
Материнский микрохимеризм (А.Г. Румянцев, 2016)− Поступление материнских клеток в плод документировано 55 лет назад
(Grenn I. et al, Hodgkin’s disease: a matuernal-to fetal lymphocyte chimegera,
Lancet, 1960)
− Диагностика/скрининг – пуповинная кровь
− Доказан перенос клеток с материнским молоком
− Изучен клеточный состав ММХ: макрофаги, Т-клетки, В-клетки,
естественные киллеры
− Материнские клетки обнаружены у детей не только в виде
циркулирующих в крови клеток, но и как дифференцированные тканевые
клетки кожи, тимуса, сердца, легких, поджелудочной железы, селезенки,
почки, мышц и костного мозга
5.
Доказательства межклеточных взаимодействий всистеме мать-плод
(А.Г. Румянцев, 2016)
• Клетки плода обнаруживаются на 6 неделе гестации и частота их обнаружения
нарастает с ростом гестационного возраста, достигая 100% к 36 неделе
гестации
• При нормальной беременности во втором триместре беременности число
клеток плода в венозной крови матери составляет 1-6 клеток/мл (т.е., от 5 до
30х103 клеток)
• При аномалиях плаценты и плода, эклампсии, проблемах тканевой
совместимости, невынашивании, самопроизвольных абортах в сроки от 20и
недель, число циркулирующих клеток плода возрастает до 20-1500 клеток в
мл.
• Специальные исследования послеродового микрохимеризма обнаруживают
его более чем у 40% здоровых женщин, перенесших беременность
6. «Твои клетки –мои клетки» Дж. Ли Нельсон В мире науки («Scientific American»), 2008, № 5, стр. 54-61)
• «Согласно последним данным, каждый из нас несет в себенекоторое количество клеток, принадлежавшим ранее другим
людям. Этот феномен называется микрохимеризмом. Наш
организм хранит материнские клетки, полученные в период
внутриутробного развития, организм беременной женщины –
клетки плода.
• Новоприобретенные клетки могут находиться в организме
десятилетиями и «приживаться» в разных тканях, становясь
неотъемлимой их частью.
• В одних случаях микрохимеризм бывает причастен к развитию
аутоиммунных заболеваний, в других – помогает организму
преодолеть ту или иную болезнь».
Дополнительная информация: Marcia Barinaga, Science, vol. 296, 21 June 2002,
p. 2169 – 2172,”Cells exchanged during pregnancy live on”
7.
8.
9.
Другие источники материнскогомикрохимеризма (А.Г. Румянцев, 2016)
− Клетки исчезнувшего близнеца (5% беременностей)
− Клетки сибсов при многоплодной беременности
(фетофетальная трансфузия)
− Клетки, сохранившиеся у матери от плода предыдущей
беременности
− Клетки сохранившиеся у матери со времени когда она
была плодом/ребенком (бабушки, тетки и дяди матери и
т.д.)
10. «Твои клетки –мои клетки» Дж. Ли Нельсон В мире науки («Scientific American»), 2008, № 5, стр. 54-61)
11. «Твои клетки –мои клетки» Дж. Ли Нельсон В мире науки («Scientific American»), 2008, № 5, стр. 54-61)
12.
«Твои клетки –мои клетки»Дж. Ли Нельсон В мире науки («Scientific American»), 2008, № 5, стр. 5461)
13. «Твои клетки –мои клетки» Дж. Ли Нельсон В мире науки («Scientific American»), 2008, № 5, стр. 54-61)
14. «Твои клетки –мои клетки» Дж. Ли Нельсон В мире науки («Scientific American»), 2008, № 5, стр. 54-61)
ЧТО ДАЛЬШЕ?• «Могут ли клетки, полученные от матери или плода,
преодолевать гематоэнцефалический барьер и влиять на работу
костного и спинного мозга? Если да, то влияют ли
материнские клетки на развитие головного мозга ребенка?
• Можно ли использовать фетальный микрохимеризм для
лечения нейродегенеративных расстройств?
• И, наконец, уместно ли говорить о психологической
индивидуальности человека, если головной мозг – не совсем
его?»
15. (Immune Mediated Inflammatory Disorders)- группа болезней, характеризующихся нарушением иммунной регуляции, хроническим
Иммуноопосредованные воспалительныезаболевания
(ИОВЗ)
(Immune Mediated
Inflammatory Disorders)группа болезней,
характеризующихся
нарушением иммунной
регуляции, хроническим
воспалением и
повреждением тканей
16. Патология иммунной системы
• Аллергические заболевания• Аутоиммунные заболевания
• Иммунодефициты (первичные,
вторичные)
• Транзиторные вторичные
иммунодефициты (иммунокомпрометированность)
17. Иммунодефицитные состояния у детей
Иммунодефициты (ИД) – снижениефункциональной активности основных
компонентов системы иммунитета ведущие к
нарушению антигенного гомеостаза организма и,
прежде всего, снижению способности организма
защищаться от микробов и проявляющееся в
повышенной инфекционной заболеваемости.
Практическое значение имеют прежде всего
патология клеточного и гуморального иммунитета
(Т, В и стволовые клетки), дефекты фагоцитоза и
нарушение функций комплементарной системы.
ИД делят на первичные (ПИД) и вторичные
(ВтИД).
18.
ИММУНОДЕФИЦИТНЫЕ СОСТОЯНИЯПЕРВИЧНЫЕ
(врожденные нарушения
системы иммунитета,
связанные с генетическими
дефектами -клеточного,
гуморального иммунитета,
фагоцитоза, комплемента)
>200 видов
ВТОРИЧНЫЕ
(нарушения иммунитета, не
являющиеся результатом
генетического дефекта)
Идиопатические
(«Спонтанные»)
ПРИОБРЕТЕННЫЕ
(СПИД)
Клинически проявляется в виде
хронических рецидивирующих
инфекционно-воспалительных
процессах легких, ЖКТ,
урогенитального тракта и т.д.
Индуцированные
1. При наличии конкретной причины: рентгеновское облучение, действие
кортикостероидов, цитостатиков, травм, хирургических вмешательств.
2. Развиваются вторично по отношению к основному заболеванию (диабет,
заболевания почек, печени, злокачественные новообразования и др.)
Транзиторные – устраняются при ликвидации причины
19. Иммунодефицитные состояния у детей
Первичные иммунодефицитныесостояния (ИДС) - врожденные
нарушения системы иммунитета,
связанные с генетическими дефектами
одного или нескольких ее компонентов:
клеточного и гуморального иммунитета,
фагоцитоза, комплемента. К первичным
ИДС относят случаи стойкого нарушения
конечной эффекторной функции
поврежденного звена, характеризующиеся
стабильностью и воспроизводимыми
лабораторными характеристиками.
20.
21. Первичные иммунодефициты: 10 настораживающих признаков (Комитет экспертов ВОЗ, 1990)
22.
8 и более отитов в течениегода
2 и более месяцев а/б
терапии
Задержка роста и развития
2 и более серьезных синуситов в
течение года
2 и более пневмонии в течение года
Рецидивирующие абсцессы
23.
Грибковые инфекциисохраняющиеся после года
2 и более серьезных
инфекционных бактериальных
заболевания в течение года
Необходимость применения в/в
а/б для разрешения инфекций
Наличие в семейной анамнезе
истории первичных ИДС
24. Распространенность
По данным ведущего иммунолога страны академика Р.В.Петрова средняя частота первичных ИДС (включая дефекты
комплемента и фагоцитоза) в разных странах составляет 2 на 1000
новорождённых.
Считается, что 50-75% общего количества больных с ПИД - дети
с дефектом В-лимфоидной системы (наиболее част селективный
дефицит IgA его распространение 1:200 – 1:1000;
агаммаглобулинемия Брутона – 1:1 000 000), 5-10% - Т-клеточного
иммунитета, а остальные - имеют комбинированную
иммунологическую недостаточность (частота 1:66 000).
Наследственные дефекты неспецифических факторов защиты
имеют следующую популяционную частоту: фагоцитоза 1:10000;
комплемента 1: 1500-3000 .
Частота минорных (малых) транзиторных ИДС не установлена.
По мнению некоторых авторов, транзиторная
гипогаммаглобулинемия может быть выявлена у 5-8% детей
раннего возраста.
25. Распространенность в США (Braithwaite K.A., Cairo M.S., 2004)
При исключении дефицита IgA частотапервичных иммунодефицитов составляет примерно
1 : 10 000, т.е. в США регистрируется примерно 400
новых случаев ежегодно и общее число больных в
пределах 5 000 – 10 000. Для сравнения это
примерно четверть от количества детей с
муковисцидозом (1 : 2 500) и немного больше, чем
больных фенилкетонурией (1 : 14 000).
26. Клиническими проявлениями ИДС могут быть сочетания:
1.2.
3.
4.
5.
6.
7.
8.
Рецидивирующие инфекционные, в том числе грибковые процессы в
дыхательных путях, отиты, синуситы, кожные абсцессы, инфекции
мочевыводящих путей и пиелонефрит, воспалительные заболевания
кишечника, септицемии с гнойными поражениями кожи, менингитом,
артритом и остеомиелитом.
Гематологические дефициты (лимфоцитопения, нейтропения, иногда
тромбоцитопения, мегалобластная анемия).
Необычные реакции (системные) на вакцины, содержащие живых
ослабленных возбудителей, вплоть до развития сепсиса.
Расстройства пищеварения, диарейный синдром и синдром
мальабсорбции.
Аутоиммунные и другие иммунопатологические процессы (артриты,
склеродермия, красная волчанка, тиреоидит и др.).
Аллергические реакции 1 типа в виде экземы, отека Квинке,
аллергическими реакциями на введение лекарственных препаратов,
иммуноглобулинов, препаратов крови.
Опухоли и лимфопролиферативные заболевания (при ИДС встречаются в
1000 раз чаще, чем без ИДС);
Первичные иммунодефицитные состояния часто сочетаются с пороками
развития, прежде всего с гипоплазией клеточных элементов хряща и волос.
Кардиоваскулярные пороки описаны, главным образом, при синдроме Ди
Джорджи.
27. Фенотипическая классификация ПИДС (рабочая классификация экспертов ВОЗ, 1971)
1.2.
3.
4.
5.
6.
Синдромы недостаточности антител
(гуморальные иммунодефициты)
Преимущественно клеточные
(лимфоидные) дефекты иммунитета
Синдромы тяжелой комбинированной
иммунной недостаточности (ТКИН)
Дефекты фагоцитоза
Дефициты комплемента
ПИДС, ассоциированные с другими
главными дефектами (другие четко
очерченные ПИДС)
28. Основные лабораторные исследования при диагностике ИД
Общий анализ крови позволяет выявить анемию,лейкопению или тромбоцитопению. Поскольку Тлимфоциты составляют 75% всех лимфоцитов крови,
лимфоцитопения почти всегда свидетельствует о
снижении числа Т-лимфоцитов. У больных с
недостаточностью клеточного иммунитета часто
наблюдается эозинофилия. Нарушение адгезии
лейкоцитов сопровождается стойким лимфоцитозом.
Для синдрома Вискотта-Олдрича характерно
уменьшение числа и размеров тромбоцитов. При
некоторых иммунодефицитах, например, синдроме
гиперпродукции IgM и тяжелом комбинированном
иммунодефиците, наблюдается аутоиммунная
тромбоцитопения.
29. Основные лабораторные исследования при диагностике ИД
Количественное определение IgG, IgM, IgA.Нормальным считается уровень
иммуноглобулинов, находящийся в пределах 2
стандартных отклонений от среднего значения
для данного возраста. При снижении уровня
иммуноглобулинов более чем на 2
стандартных отклонения от возрастной нормы
ставят диагноз гипогаммаглобилинемии.
Очень высокий уровень иммуноглобулинов
позволяет заподозрить СПИД.
30. Основные лабораторные исследования при диагностике ИД
Оценку клеточного иммунитета проводят и спомощью кожных проб, основанных на
аллергических реакциях замедленного типа с
использованием столбнячного, дифтерийного
анатоксинов, Сandida albicans. Папула должна
появиться через 48-72 часа. Положительная
реакция при проведении кожных проб исключает
тяжелую недостаточность клеточного иммунитета,
тогда как отрицательная реакция не имеет
диагностического значения.
Обязательным является и учет субпопуляций
лимфоцитов и других клеток крови в соответствии
с CD-рецепторами.
31. Исследование фагоцитов
Исследование фагоцитоза включает тествосстановления нитросинего тетразолия,
исследование хемотаксиса и адгезии
лейкоцитов (в частности, тест кожного окна),
УЗИ селезенки, стернальную пункцию (при
стойкой лейкопении или лейкоцитозе),
изменении морфологии лейкоцитов,
выявлении бластных форм в крови,
выявление антинейтрофильных антител,
определение числа клеток с антигенным
маркером CD11/ CD18
32. Исследование комплемента
Включает количественное определение ифункциональную оценку компонентов
комплемента, исследование альтернативного
пути активации комплемента, определение
опсонинов и факторов хемотаксиса в
сыворотке. О дефиците опсонинов в
исследуемой сыворотке свидетельствует ее
неспособность усиливать фагоцитоз бактерий
и дрожжевых грибов нормальными
лейкоцитами.
33.
Генетика первичных иммунодефицитов(Р.Х. Бакли, 2009)
Хромосома
и участок
Продукт гена
Дефект
Функциональная недостаточность
Первичные нарушения продукции антител
2р11*
κ-цепь
Недостаточность к-цепи
Отсутствие иммуноглобули6нов с κцепями
6р21.3
Неизвестен
Избирательная недостаточность
IgA, ОВИН
Низкий уровень или отсутствие IgA, при
ОВИН низкая концентрация всех
иммуноглоюулинов
12р13*
Индуцируемая при
активации
цитидиндезаминаа
Аутосомно-рецессивный
синдром гиперпродукции IgМ
Отсутствие продукции антител классов
IgG, IgA и IgE
14q32.3*
Тяжелые цепи
иммуноглобулино
в
В-негативная
агаммаглобулинемия (μ) или
избирательные дефициты
других изотипов
Отсутствие продукции антител и Влимфоцитов при мутациях гена μ-цепи; в
других случаях – отсутствие подклассов
иммуноглобулинов, но наличие Влимфоцитов
CD40
Аутосомно-рецессивный
синдром гиперпродукции IgМ
Отсутствие продукции антител классов
IgG, IgA и IgE
Xq22*
Брутоновская
тирозинкиназа
Х-сцепленная
агаммаглобулинемия
Отсутствие продукции антител и Влимфоцитов
Xq23*
SLAMассоциированный
белок (SH2D1A)
Х-сцепленная
лимфопролиферативная
болезнь (болезнь Дункана)
Отсутствие антител к ядерному антигену
вируса Эпстейна-Барр и долговременного
Т-клеточного иммунитета; низкий уровень
иммуноглобулинов
Xq26*
CD154 (лиганд
CD40)
Х-сцепленный синдром
гиперпродукции IgМ
Отсутствие продукции антител классов
IgG, IgA и IgE
Xq28*
NF-κB NEMO
Ангидротическая эктодермальная дисплазия с иммунодефици-
Гиперпродукции IgМ или подклассов IgG и
антител к полисахаридным антигенам
20*
34.
Генетика первичных иммунодефицитов(Р.Х. Бакли, 2009)
Первичные нарушения клеточного иммунитета
2q12
10р13
11
22q11.22
ZAP-70
CD8-лимфоцитопения
Отсутствие ответа CD8 Т-лимфоцитов на
обычные сигналы
Неизвестен
Гипоплазия тимуса (синдром
Ди Джорджи)/
велокардиофациальный
синдром
Низкое число Т-лимфоцитов и нарушение их
функции
CD3γ* или ε*
Недостаточность CD3
Слабый ответь Т-лимфоцитов на митогены;
дефицит подклассов IgG
Неизвестен
Гипоплазия тимуса (синдром
Ди Джорджи)/
велокардиофациальный
синдром
Низкое число Т-лимфоцитов и нарушение их
функции
35.
Первичные комбинированные нарушения иммунитета1q*
RFX5
Дефицит HLA класса II
Низкий уровень иммуноглобулинов, отсутствие ответа Тлимфоцитов на антигены, дефицит CD4
5р13*
ИЛ-7Rα
ТКИД, Т-, В+, NK+
Отсутствие функции Т- и В-лимфоцитов
6р21.3*
ТАР1, ТАР2
Дефицит HLA класса I
Резкий дефицит CD8 Т-лимфоцитов, комбинированные
дефекты Т- и В-лимфоцитов
6q22-q23*
ИНФ-γR1
Диссеминированные
микобактериальные
инфекции
Неспособность макрофагов и других клеток продуцировать
ФНО-α при действии ИНФ-γ
9р21-р23
Эндорибонуклеаз
а РНКаза MRP
Метафизарная
хондродисплазия , тип МакКьюсика
Комбинированные дефекты Т- и В-лимфоцитов различной
тяжести (включая нарушения гуморального иммунитета,
КИД и ТКИД)
!0р13*
Artemis
ТКИД, Т-, В-, NK+
Отсутствие функции Т- и В-лимфоцитов
!0р14-р15*
ИЛ-2Rα
Лимфопролиферативный
синдром
Отсутствие ответов Т-лимфоцитов; нарушение апоптоза;
повышенный уровень bcl-2: аутоиммунные заболевания
11р13*
RAG1 или RAG2
ТКИД, Т-, В-, NK+
Отсутствие функции Т- и В-лимфоцитов
11q22/3*
ДНК-зависимая
киназа
Атаксия-телеангиоэктазия
Избирательный дефицит IgA; дефицит Т-лимфоцитов
13q*
RFXAP
Дефицит HLA класса II
Низкий уровень иммуноглобулинов, отсутствие ответа Тлимфоцитов на антигены, дефицит CD4
14q13.1*
Пуриннуклеозида
за
Недостаточность
пуриннуклеозидфосфорилазы
Резкий дефицит Т-лимфоцитов; возможно присутствие
иммуноглобулинов
16р13*
CIITA
Дефицит HLA класса II
Низкий уровень иммуноглобулинов, отсутствие ответа Тлимфоцитов на антигены, дефицит CD4
19р13.1*
Jak3
ТКИД, Т-, В+, NK-
Отсутствие функции Т- и В-лимфоцитов и NK-клеток
20q13.11*
Аденозиндезамин
аза
ТКИД, Т-, В-, NK+
Отсутствие функции Т- и В-лимфоцитов
Хр1.23*
WASP
Синдром Вискотта-Олдрича
Тромбоцитопения, нарушение продукции
антиполисахаридных антител
36. ИДС с преимущественным дефектом продукции антител
Врожденная агаммаглобулинемия с дефицитом Вклеток (болезнь Брутона)Агаммаглобулинемия с гипер-IgМ
Транзиторная младенческая гипогаммаглобулинемия
(ТМГ)
Общая вариабельная гипогаммаглобулинемия (ОВГ)
Селективный дефицит IgA (CД IgA)
37.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
38. В-клеточные дефициты у детей
ЗаболеваниеТип наследования
Клинические особенности
Лечение
Болезнь
Брутона
(первичная
агаммаглобу
линемия)
Рециссивный,
сцепленный с Ххромосомой (85%).
Ген локализован на
Xq21.3-22
Рецидивирующие гнойные заболевания;
инфекционные заболевания легких, околоносовых
пазух, среднего уха, кожи, ЦНС; аутоиммунные
заболевания- полиартриты, дерматомиозит; высока
частота аллергических заболеваний. Уровень в крови
IgG < 2 г/л, отсутствуют IgM, IgA,IgE, IgD. Глубокий
дефицит В-клеток ( CD19< 2%) при нормальном уровне
преВ-клеток в костном мозге), мутация в Btk, отсутствие
Btk в нейтрофилах, моноцитах, тромбоцитах. Btk – Вклеточная тирозинкиназа
Сывороточный Ig в
начале в дозе 0,2-0,3
г/кг 1 раз в 5-7 дней и
далее 0,4-0,5 г/кг 1 раз
в 3-4 недели,
поддерживая уровень
IgG 5 г/л,
антибиотики
парентерально
Транзиторная
младенческа
я
гипогаммагло
булинемия
Неизвестный.
Часто в семьях с
различными
комбинированным
и
иммунодефицитам
и
Рецидивирующие бактериальные кожные,легочные и
ЛОР- инфекции, астроэнтероколит., гемоцитопении.
Стойкое снижение суммарной концентрации
иммуноглобулинов ниже 3 г/л при нормальном или
умеренно сниженном уровне В-клеток
Антибиотики,
некоторым
пациентам –
сывороточный Ig
(при уровне IgG в
крови менее 2 г/л)
Селективный
дефицит Ig А
Аутосомнорецессивный или
аутосомнодоминантный
Рецидивирующие нетяжелые инфекционные
заболевания легких; болезни ЖКТ, хроническая
диарея; при наличии В8 и DR3 HLA - ревматоидный
артрит, СКВ, дерматомиозит, склонность к
анафилактическим реакциям; у 50% - бессимптомное
течение.
Снижение уровне IgA < 0,07 г/л у детей старше 4-х лет при
нормальном уровнях других иммуноглобулинов, хотя у
части больных выявлен сопутствующий дефицит IgG2, и у
22% гипер-IgE
Антибиотики,
сывороточный Ig
при дефиците IgG
(но не при
изолированном
дефиците IgA, т.к.
высок риск
анафилактического
шока,
обусловленного
выработкой IgE
против экзогенного
IgA).
39. Билобэктомия у ребенка с врожденной агаммаглобулинемией выполнена по поводу хронической бронхоэктатической болезни до
врожденнВрожденная агаммаглобулинемия
ой с
дефицитом В-клеток
агаммагл
обулинем
ией
выполнен
а по
поводу
хроничес
кой
бронхоэк
татическ
ой
Наблюдение М.Н. Ярцева
болезни
40. Сердечный горб и scapula alatae (крыловидные лопатки) у ребенка с хроническим гнойным бронхитом и септическим эндокардитом на
Врожденная агаммаглобулинемия сдефицитом В-клеток
Сердечный горб и
scapula alatae
(крыловидные лопатки)
у ребенка с
хроническим гнойным
бронхитом и
септическим
эндокардитом на фоне
врожденной
агаммаглобулинемии.
Наблюдение М.Н. Ярцева
41. В-клеточные дефициты у детей
ЗаболеваниеТип наследования
Клинические особенности
Лечение
Общая
вариабельная
иммунная
недостаточность
(ОВИН)
Различный
(аутосомнорецессивный, Хсцепленный и
неизвестный)
Воспалительные заболевания
желудочно-кишечного тракта,
мальабсорбция, мегалобластическая
анемия, аутоиммунные заболевания,
высока частота лимфоретикулярных
и желудочно-кишечных
злокачественных опухолей Критерии
диагноза: уровень IgG и IgM или IgA<
2SD от возрастной нормы, отсутствие
изогемагглютининов и/или плохой ответ
на вакцины
Сывороточный
Ig, антибиотики
Иммунодефицит
с
гиперпродукцией
IgM, IgD
Различный
(аутосомнорецессивный –
мутация в AID-ген,
сцепленный с Ххромосомой – Xq
26,27 или не
устанавливается)
Тяжелое течение бактериальных
инфекций, рецидивирующие
лихорадочные состояния, лямблиоз,
синдром мальабсорбции,
аутоиммунные цитопении
Критерии диагноза: уровень IgG < 2SD
от возрастной нормы и IgM>2 SD от
возрастной нормы
Сывороточный
Ig, антибиотики
Дефицит
транскобаламина
Аутосомнорецессивный
Рецидивирующие инфекции, атрофия
ворсин кишечника, мальабсорбция,
мегалобластическая анемия,
панцитопения
Сывороточный
Ig, высокие дозы
витамина В12
Х-сцепленная
гипогаммаглобул
инемия с
Сцепление с Ххромосомой
Рецидивирующие гнойные инфекции,
задержка роста
Сывороточный Ig
42.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
43. Распространенное витилиго – одно из аутоиммунных проявлений у девочки с общей вариабельной иммунной недостаточностью.
Общая вариабельная иммуннаянедостаточность
Распростране
ОВИН
нное
витилиго –
одно из
аутоиммунных
проявлений у
девочки с
общей
вариабельной
иммунной
недостаточно
стью.
Наблюдение М.Н. Ярцева
44. Тотальная алопеция (аутоиммунное проявление) и хронический энтероколит (подросток лежит на клеенке из-за неспособности
(аутоиммунное
Гуморальные ПИДС
Общая вариабельная иммунная недостаточность
проявление)
и
ОВИН
хронически
й
энтероколи
т (подросток
лежит на
клеенке изза
неспособно
сти
удерживать
водянистый
Наблюдение М.Н. Ярцева
стул) у
мальчика с
45.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
46. Диана Д.
• Родилась 26.10.2004 года от второйбеременности. Старший брат и родители
здоровы. Беременность протекала на фоне
угрозы выкидыша. Перенесена вирусная
инфекция в 28 недель (заболевание с
лихорадкой и сыпью на теле). Этиология не
уточнена. Роды на 38 неделе, масса 3 400 г.,
длина 52 см. На первом месяце девочка
перенесла пиодермию, стафилококковый
энтероколит.
47. Продолжение
• В 3 месяца госпитализирована в тяжеломсостоянии по легочно–сердечной недостаточности,
интоксикации, неврологической симптоматике в
ОДКБ г.Архангельска.
• Уровень IgM – до 5,2 г/л, IgA – 0,28 г/л, IgG – 10,5
г/л
• Диагностирована ВУИ неуточненной этиологии с
поражением легких, головного мозга и
сопутствующие диагнозы: двусторонний средний
отит, гастроэзофагеальный рефлюкс, ОАП.
• Выявлены особенности заболевания:
рентгенологически преобладание поражения
интерстициальной ткани легких, при отсутствии
аускультативных данных, гепатоспленомегалия,
кальцификаты при рентгенограмме черепа,
лимфоаденопатия, при осмотре окулиста патологии
не выявлено.
48. Продолжение
• КТ головного мозга от 20. 05. 2005: в веществе мозга определяютсямножественные обызвествления, распологающиеся ассиметрично,
вдоль субарахноидальных пространств
• ПЦР ликвора и крови от 20. 05. 2005 на наличие антигенов токсоплазм,
СMV, герпеса 1и 2-го типа, хламидий, микоплазм – результаты
отрицательные
• В дальнейшем неоднократно (впервые в 7 месяцев) больная поступала
в клинику детских болезней ВМА и другие детские больницы СанктПетербурга по поводу резкой задержки психомоторного развития и
неврологических нарушений, рецидивирующих респираторных и
кожных инфекций.
• Уровни иммуноглобулинов при 12-кратном определении до возраста 2,5
лет: IgM от 3,8 г/л до 30 г/л (обычно более 10 г/л), IgA от 0 до 0,5 г/л (5
раз - 0 г/л), IgG от 1,75 г/л до нормы после вливаний Гамимуна Н ).
• МРТ головного мозга в 1,5 года: киста прозрачной перегородки,
наружная гидроцефалия (по атрофическому типу).
49. Диагноз
• Синдром первичного иммунодефицита: гиперIgM синдром.
• Сопутствующие и осложнения:
• Внутриутробная инфекция неуточненной
этиологии (наиболее вероятно - краснуха;
мать краснухой не болела)
• ДЦП, двойная гемиплегия, грубая задержка
психомоторного развития, бульбарный
синдром, симптоматическая эпилепсия.
• Гипотрофия 2 степени смешанного генеза
50. Лечение
• Подбор иммуноглобулина и индивидуальной дозы.Проведение базисной заместительной терапии
Гамимун Н (2,5 г в месяц)
• Лечение ДЦП
• Поддержка трофического статуса, ликвидация
дефицитных состояний
• Мониторирование показателей иммунитета и
аутоиммунных состояний
• Антибактериальная, антимикотическая терапия (по
показаниям)
51. Множественная гиперплазия шейных лимфатических желез и распространенный кариес у девочки с аутосомно-рецессивной формой
Гуморальные ПИДСАгаммаглобулинемия с гипер IgM
Множественная
гиперплазия шейных
лимфатических желез
и распространенный
кариес у девочки с
аутосомнорецессивной формой
агаммаглобулинемии
с гипер-IgM.
Наблюдение М.Н. Ярцева
52. Гипер-IgE синдром (Синдром Иова)
Иов – образцовый праведник. В Ветхом завете «Книга Иова»начинается так : «Был человек в земле Уц, имя его Иов; и был человек
этот непорочен, справедлив и богобоязнен и удалялся от зла». Иов
прожил 210 лет. По разрешению Господа сатана в начале лишает его
овец и другого скота, погонщиков, дочерей и сыновей - ответ Иова
«Господь дал, Господь и взял – благословенно имя Господне!».
Следующим испытанием была страшная болезнь – сатана «поразил
Иова проказою лютою от подошвы ноги его до самого темя его», но
здесь Иов остался верен Господу, за что Господь вернул ему все вдвое
и дал 140 лет жизни, новых семь сыновей и трех дочерей.
При гипер-IgE синдроме у всех детей отмечены повторные
холодные абсцессы мягких тканей, часто встречались гнойные
лимфоадениты (56%), синуситы (22%), повторные гнойные отиты
(50%), тяжелые пневмонии (83%), в том числе деструктивные с
исходом в пневматоцеле (50%), абсцессы печени (11%), кандидозный
стоматит (11%). Частые банальные ОРЗ отсутствовали.
М.Н. Ярцев
53. Семейный случай гипер-IgE синдрома. Характерные черты лица: крупный картофелевидный нос, массивный квадратный подбородок,
Гипер-IgE синдромСемейный случай
гипер-IgE синдрома.
Характерные черты
лица: крупный
картофелевидный нос,
массивный квадратный
подбородок, широкая
переносица.
Наблюдение М.Н. Ярцева
54.
Гипер-IgE синдромХолодный абсцесс
мягких тканей в левой
подмышечной области у
ребенка с гипер-IgE
синдромом. Контуры
абсцесса обведены
маркером. Отсутствует
гиперемия и
болезненность.
Наблюдение М.Н. Ярцева
55. Переразгибание в суставах кисти («гуттаперчивый мальчик») – характерная особенность детей с гипер-IgE синдромом.
Гипер-IgE синдромПереразгибание
в суставах кисти
(«гуттаперчивый
мальчик») –
характерная
особенность
детей с гиперIgE синдромом.
Наблюдение М.Н. Ярцев
56. Рубцы после множественных обширных холодных абсцессов мягких тканей бедра у ребенка с гипер-IgE синдромом.
Гипер-IgE синдромРубцы после
множественных
обширных холодных
абсцессов мягких
тканей бедра у
ребенка с гипер-IgE
синдромом.
Наблюдение М.Н. Ярцев
57. Холодный абсцесс шейного лимфоузла у ребенка с гипер-IgE синдромом.
Гипер-IgE синдромХолодный абсцесс
шейного лимфоузла у
ребенка с гипер-IgE
синдромом.
Наблюдение М.Н. Ярцева
58. ВНИМАНИЕ – вторичное гипер-IgE состояние!
Реально встречается в сотни раз чаще, чемпервичный гипер-IgE синдром, и не имеет с ним ничего
общего.
Употребление
термина
состояние» часто связано
искажением.
«вторичное
гипер-IgE
с грубым смысловым
Никаких прямых пагубных воздействий на иммунитет,
сопоставимых с теми, что наблюдаются при первичном
гипер-IgE синдроме, высокие и сверхвысокие уровни IgE
(наблюдаемые, например, при диффузном атопическом
дерматите, некоторых паразитарных инвазиях) не
оказывают.
М.Н. Ярцев
59. Т-клеточные и комбинированные Т- и В- клеточные иммунодефициты
Т-клеточные и комбинированные Т- и Вклеточные иммунодефицитыЗаболевание
Тип
наследования
Клинические особенности
Лечение
Тяжелый
комбинированный
иммунодефицит –
гетерогенная группа
болезней
Аутосомнорецессивный
В 3-6 месяцев рецидивирующие тяжелые
бактериальные и грибковые заболевания,
сепсис, задержка развития, экзема, могут
отсутствовать тимус, лимфоузлы, миндалины
Лимфоцитопения, обусловленная отсутствием Тлимфоцитов (в циркуляции нет CD3, CD4< CD8лифоцитов), приживление трансплацентарноприобретенных материнских Т-лимфоцитов (!)
Трансплантация
костного мозга,
антибиотики
Дефицит
пуриннуклезидфо
сфорилазы или
аденозиндезаминаз
ы
Аутосомнорецессивный
Рецидивирующие инфекционные, в т.ч.
вирусные, заболевания, анемия
(мегалобластическая, аутоиммунная
гемолитическая или гипопластическая),
неврологические симптомы в виде судорог,
спастической тетраплегии, атаксии,
лимфопролиферативные синдромы
(лимфомы)
Трансплантация
костного мозга,
заместительное
введение ферментов
Синдром ДиДжорджи
(гипоплазия
вилочковой
железы)
В части случаев
дефект делеции
22q11.2
Гипопаратиреоидизм (тетания гипокальциемия), количество CD3-клеток менее
500 в мкл, дисморфия лица, врожденные
пороки сердца, катаракта, рецидивирующие
инфекции легких и кишечника, психические
отклонения (у некоторых больных)
Трансплантация тимуса
плода, гестационный
возраст которого не
превышает 14 нед;
введение гормонов
тимуса
Хронический
слизисто-кожный
кандидоз
Аутосомнорецессивный
Хронический кандидоз с поражением кожи,
ногтей, волосистой части головы, слизистых
оболочек; рецидивирующие вирусные и
бактериальные инфекции; аутоиммунные
эндокринные заболевания (недостаточность
надпочечников, околощитовидных и
щитовидной желез)
Трансплантация
стволовых клеток;
системные и местные
противогрибковые
препараты
60.
Детис
тяжелой
комбинированной
иммунной
недостаточностью
погибали
преимущественно на первом году
жизни
при
развитии
интерстициальной
пневмонии,
истощающего
энтероколита,
генерализованного
кандидоза,
сепсиса
на
фоне
остановки
развития.
О частых ОРЗ в таких случаях
не упоминалось.
М.Н. Ярцев
61. Генерализованная BCG-инфекция у ребенка с ТКИН
Наблюдение М.Н. Ярцева62. Генерализованная BCG-инфекция у ребенка с ТКИН
Наблюдение М.Н. Ярцева63.
64.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
65.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
66.
При комбинированной иммунной недостаточностис атаксией-телеангиэктазией отмечались повторные
затяжные инфекции респираторного тракта (60%), ЛОРорганов (52%), кожи и мягких тканей (22%),
энтероколиты (18%), рецидивирующая герпетическая
инфекция (17%). Из-за прогрессирующих двигательных
нарушений дети не посещали детские учреждения и
банальными ОРЗ болели редко.
М.Н. Ярцев
67. Характерная атаксическая поза («утиная походка», пошатывание, атетоидные движения кистей) у ребенка с
Комбинированная иммунная недостаточность сатаксией-телеангиэктазией
Характерная атаксическая поза
(«утиная походка», пошатывание,
атетоидные движения кистей) у
ребенка с атаксией-телеангиэктазией.
Наблюдение М.Н. Ярцева
68. Телеангиэктазы склер и распространенный кариес у ребенка с атаксией-телеангиэктазией.
распространенныйкариес у ребенка с
атаксиейтелеангиэктазией.
Наблюдение М.Н. Ярцева
69.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
70. Синдром Вискотта-Олдрича (WAS)
• Частота: 1на 100 000 новорождённых.• Альфред Вискотт (A. Wiskott) в 1937 году описал болезнь,
характеризующуюся триадой симптомов: геморрагический
тромбоцитопенический синдром, экзема и частые тяжелые инфекции, у трех
братьев, но ни у одной из сестер. Роберт Олдрич (R. Aldrich) в 1954 г.
установил рецессичный, сцепленный с Х-хромосомой тип наследования.
• Патогенез. Ген, определяющий болезнь, расположен на Xp11.22 и состоит
из 12 экзонов, кодирует белок из 502 аминокислот с молекулярным весом 54
кД – WASP, экпрессирующийся на всех гемопоэтических клетках и
регулирующий полимеризацию актина и ремоделирование цитоскелетона,
которая необходима для установления синапсов между Т-лимфоцитами и
антигенпрезентующими клетками, адгезии и перемещении В-лимфоцитов,
макрофагов, дентритических клеток. Описано более 160 мутациий WASРгена, определяющих особенности клинического течения болезни. При
полном отсутствии WASP (динуклеотидная мутация в WAS-экзоне1)
наиболее тяжелое течение WAS. У девочек носителей нулевого WAS-гена
описаны случаи атипичного течения WAS.
71. Синдром Вискотта-Олдрича (WAS)
Клиника. У мальчиков - тромбоцитопения разной степенивыраженности (80% тромбоцитов имеют диаметр ниже 2 микрон),
отиты, синуситы, пневмония, диарея (нередко «кровавая»), экзема
обычно на первых месяцах жизни.Инфекционные процессы при
WAS обычно вызывают герпетические вирусы, грибы рода
кандида, условнопатогенные и бактерии с полисахаридной
капсулой. Уровни IgA, IgG – нормальны или повышены, IgM и
титр изогемагглютининов – снижены, с возрастом снижается
количество Т-лимфоцитов. Возможны БА, аутоиммунная ГА,
васкулиты, повышена частота опухолевых заболеваний
(неходжкинские лимфомы).
Диагноз подтверждают обнаружением мутации в WAS-гене и/или
отсутствием или аномальным WASP.
Лечение – трансплантация аллогенного костного мозга или
стволовых клеток, переливание тромбопоэтического ростового
фактора, такого как ИЛ-11, паллиативная терапия – антибиотики и
др.
72.
73. Синдром Вискотта-Олдрича: экзематозные поражения с геморрагиями на лице и шее; в левой суборбитальной Синдром Вискотта-Олдрича:
экзематозные поражения сгеморрагиями на лице и шее;
в левой суборбитальной
области – герпетическое
поражение с
геморрагическим экссудатом
Наблюдение М.Н. Ярцева
74. Количественные и качественные дефекты фагоцитов
ЗаболеваниеТип наследования
Клинические
особенности
Лечение
Хроническая
гранулематозная болезнь
(септический гранулематоз)
Дефицит цитохрома b558
Дефект синтеза
цитохрома р558, ген
на Х-хромосоме.
Суммарная частота
генных мутаций
1:2000
Рецидивирующие гнойные процессы
в легких, коже,костях; экзема,
гепатоспленомегалия, множественные
гранулемы в разных органах. Диагноз
основан на отрицательном NBT-тесте.
Антимикробная
терапия,
трансплантация
костного мозга
Дефицит других белков
цитоплазмы нейтрофилов
Аутосомнорецессивный
Рецидивирующие гнойные
процессы, образование множества
гранулем в различных органах;
сплено- и гепатомегалия;
персистирующие диареи
Антибактериальные
препараты, интерферон
Дефицит
миелопероксидазы
Аутосомнорецессивный
Длительные кандидозные инфекции
Антимикробная терапия
Синром Чедиака-Хигаси
Аутосомнорецессивный
(ген картирован на
1-ой хромосоме)
Микробно-воспалительные
заболевания; септические
состояния; альбинизм;
гепатоспленомегалия;
панцитопения; сенсорная и
моторная невропатия
Антимикробная терапия
Нарушение адгезивных
свойств фагоцитов
Описано три типа с
аутосомнорецессивным типом
наследования
Замедление отпадения пупочного
канатика; омфалит; рецидивирующие
инфекционные поражения кожи,
легких и др.; медленное заживление
ран и частые перианальные и
кишечные свищи; при дефекте 2-го
типа – задержка умственного
развития. Снижена экспрессия
Антимикробная
терапия,
трансплантация
костного мозга
75. Количественные и качественные дефекты фагоцитов
ЗаболеваниеТип
наследования
Клинические
особенности
Лечение
Синдром Швахмана
Аутосомнорецессивный
Хроническое расстройство
пищеварения со стеатореей
(недостаточность
экзокринной функции
поджелудочной железы);
малые прибавки в массе
тела; повторные
воспалительные
заболевания легких;
лейкопения с
нейтропенией;
тромбоцитопения; анемия
Антибактериальная
терапия, большие
дозы панкреатина
Циклическая
нейтропения
Аутосомнодоминантный
Склонность к гнойным
процессам, чаще
стафилококковой природы
(поражаются кожа, легкие,
слизистые оболочки
пищеварительного тракта)
Противомикробная
терапия, при
сепсисе–
переливание
нейтрофилов
Болезнь (синдром)
Костмана
Аутосомнорецессивный
Рецидивирующие
бактериальные инфекции
кожи, легких, остеомиелит,
сепсис
76.
77.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
78.
79.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
80.
При хронической гранулематозной болезни у детейотмечались также гнойные инфекции кожи и
подкожной клетчатки (85%), БЦЖ-ит (85%), абсцессы
печени (70%), гнойные лимфоадениты (70%),
легочные инфекции (70%). Серьезные гнойные
инфекции отмечались в анамнезе практически всех
детей с хронической гранулематозной болезнью, хотя
интервалы между отдельными эпизодами гнойных
инфекций могли быть весьма значительными,
составляя иногда годы. Повышенной частоты ОРЗ не
отмечалось.
М.Н. Ярцев
81. Рубец от лапаротомии по поводу абсцесса печени у мальчика с хронической гранулематозной болезнью.
Наблюдение М.Н. Ярцева82. Свищ на шее у ребенка с генерализованным БЦЖ-итом на фоне хронической гранулематозной болезни.
Свищ на шее у ребенка с генерализованным БЦЖитом на фоне хронической гранулематозной болезни.Наблюдение М.Н. Ярцева
83. Система комплемента
Недостаточность системы комплемента может влиять наэлиминацию ЦИК, воспаление, фагоцитоз и бактериолиз. В
частности, дефицит С3 и его рецептора, сопровождается гнойными
инфекциями вследствие дефекта опсонизации. Недостаточность
компонентов мембран-атакующего комплекса ассоциируется с
высокой восприимчивостью к заражению Neisseria meningitidis.
Наследственный дефицит ингибитора С1 сопровождается
периодическим развитием ангионевротического отека. Развитие
отека опосредовано брадикинином и пептидом кинин-С2¸ вследствие
неингибируемой активации не только системы комплемента¸ но и
связанных с ним трех плазменных каскадных протеолитических
систем: кининовой¸ тромбиновой и фибринолитической.
По данным Г.А. Зайцевой (1989) низкие показатели С1-С5 и общей
активности комплемента встречаются у 4-7,7% людей, а частота
мутаций в полиморфной системе С4 достигает в Европе 12,6%. Такие
мутации предрасполагают к развитию аутоиммунных процессов.
84.
Г.-Р. Бурместер, А. Пецутто «Наглядная иммунология»,М.: Бином, 2007
85. Данные анамнеза при недостаточности комплемента
Недостаточностькомплемента
Тип наследования
Сопутствующие заболевания
Clq
Аутосомнорецессивный
Поражение кожи, как при красной волчанке (СКВ-подобный
синдром), рецидивирующие инфекции, агаммаглобулинемия
Clr
Аутосомнорецессивный
СКВ-подобный синдром, хронический гломерулонефрит,
дерматомиозит, рецидивирующие гнойные инфекции
Cls
Аутосомнорецессивный
СКВ-подобный синдром
C2
Аутосомнорецессивный
СКВ-подобный
синдром,
рецидивирующие
гнойные
инфекции,сепсис,
васкулиты,
мезангиокапиллярный
гломерулонефрит,
полимиозит,
лимфогранулематоз,
хронический лимфолейкоз, герпетиформный дерматит
C3
Аутосомнорецессивный
СКВ-подобный синдром, рецидивирующие гнойные инфекции
без
нейтрофилеза,
мембранопролифативный
гломерулонефрит, диффузные липодистрофии
C4
Аутосомнорецессивный
СКВ-подобный синдром, дерматомиозит, васкулиты
C5
Аутосомнорецессивный
СКВ-подобный
синдром,
артрит,
менингококковая и гонококковая инфекции
C6
Аутосомнорецессивный
СКВ-подобный синдром, рецидивирующие нейссериальные
инфекции (гонококковые и менингококковые), васкулиты,
системная
склеродермия,
мембранопролиферативный
гломерулонефрит
рецидивирующая
86. Данные анамнеза при недостаточности комплемента
Недостаточностькомплемента
Тип наследования
Сопутствующие заболевания
C7
Аутосомнорецессивный
СКВ-подобный синдром, рецидивирующие нейссериальные
инфекции (гонококковые и менингококковые) , васкулиты,
синдром Рейно ревматоидный артрит, склеродермия,
анкилозирующий спондилит
C8
Аутосомнорецессивный
СКВ-подобный
синдром,
пигментная ксеродерма
C9
Аутосомнорецессивный
Нейссериальные инфекции
Ингибитор C1
Аутосомнодоминантный
Наследственный ангионевротический отек, СКВ-подобный
синдром, нефрит. Лечение производными андрогенов – даназол,
антифибринолитическими препаратами (Σ-АКК), дапсоном, в остром
периоде – свежезамороженная плазма, концентрат С1-ингибитора
Фактор I
Аутосомнорецессивный
Рецидивирующие гнойные инфекции, крапивница
Фактор H
Аутосомнорецессивный
Рецидивирующие
гнойные
инфекции,
диффузные
липодистрофии, мезангиокапиллярный гломерулонефрит
Фактор D
Аутосомнорецессивный
Нейссериальные инфекции
Сцепленный с Xхромосомой
Менингококковая инфекция
Пропердин
нейссериальные
инфекции,
87. Лечение больных ИДС
Гигиенический режим. Больные с ИДСнуждаются в профилактике инфекций:
гигиенические мероприятия, асептика,
антисептика, закаливание и, иногда, активная
иммунизация по специальной методике; живые
вакцины не применяются в связи с опасностью
сепсиса; в особой чистоте микроклимата, в
ограждении от контакта с больными вирусными
или грибковыми заболеваниями.
При ПИД – гнотобиологическая изоляция.
88. Лечение больных ИДС
Рациональное питание (преждевсего естественное вскармливание).
Диета при наличии желудочнокишечных нарушений должна
удовлетворять потребность в белках,
витаминах, макро- и микроэлементах и
быть достаточно калорийной для
обеспечения нормального роста и
развития. Недостаточное питание при
иммунодефиците может привести к еще
большему угнетению иммунитета.
89. Антибактериальная терапия.
При лихорадке и других проявлениях инфекцииантимикробную терапию начинают немедленно, не
дожидаясь результатов посева и определения
чувствительности возбудителя. Если лечение
неэффективно, по результатам посева и определения
чувствительности возбудителя назначают другой
препарат. При неэффективности антибактериальной
терапии следует заподозрить микобактериальную,
вирусную, протозойную или грибковую инфекцию.
Профилактически антибиотики назначают в период
повышенного риска инфекционных заболеваний.
Разработаны схемы длительной антимикробной
профилактики при некоторых ПИД, обеспечивающей
подавление инфекции и предотвращение появления
устойчивых штаммов микроорганизмов.
90. Заболевания, при которых эффект ВВИГ убедительно доказан (Т.В. Латышева, 2009: Институт Иммунологии ФМБА)
Первичные иммунодефициты (врожденные)
Х-связанная агаммаглобулинемия
Общий вариабельный иммунодефицит
Транзиторная гипогаммаглобулинемия у детей
Иммунодефицит с гиперглобулинемией М у детей
Дефицит подклассов иммуноглобулина G
Дефицит антител с нормальным уровнем
иммуноглобулинов
Тяжелые комбинированные иммудефициты всех типов
Синдром Вискотта-Олдрича
Атаксия-телеангиоэктазия
91. Лечение при гуморальных ПИД Заместительная терапия
Препараты иммуноглобулинов человека нормальные IgGПервичные иммунодефициты (поддерживать уровень IgG крови около 5 г/л)
Иммуноглобулин (Имбио)
Биавен
Гамимун
Сандоглобин
Октагам
Эндобулин
Вигам-ликвид
Габриглобин
Интраглобин
Стандартная доза иммуноглобулинов для внутривенного
введения, содержащих антитела класса IgG, применяемая с
заместительной целью 400 мг/кг 1 раз в 3-4 недели.
Иммуносупрессивная доза, назначаемая при
иммунопатологических болезнях (болезнь Кавасаки, иммуноопосредованные тромбоцитопении, аутоиммунная
гемолитическая анемия, дерматомиозит, полимиозит,
нейропатии и др.) – 3 г/кг на курс в течение 3-х дней.
92.
Т.В. Латышева «Внутривенные иммуноглобулины в клиническойпрактике», М., 2009
93. Лечение при ПИД Пересадка органов, тканей, клеток
• Пересадка эмбриональной вилочковойжелезы при синдромах Ди Джорджи,
Незелофа, а печени при ТКИН
• Трансплантация костного мозга при учете
HLA
• Пересадка стволовых клеток (оптимально
полученных из пуповинной крови). По
данным А.Г. Румянцева выживаемость
больных при ТКИН – 93%.
94. ПИД, при которых доказан положительный эффект ТГСК (Пашанов Е.Д., Фридрих В., Мюллер С., 2006)
• Дефекты развития и дифференцировкилимфоцитов (ТКИН разных вариантов)
• Дефекты МНС II класса
• Функциональные дефекты эффекторных клеток
(дефекты миграции/адгезии, синдром ВискоттаОлдрича)
• Дефекты киллинга внутриклеточных патогенов
(хроническая гранулематозная болезнь и др.)
• Дефекты цитотоксичности/цитолиза
(лимфогистиоцитоз, синдром Чедиака-Хигаси, и
др.)
• Дефекты иммунной регуляции)
95. Трехлетняя выживаемость у пациентов с ПИД после ТГСК (Пашанов Е.Д., Фридрих В., Мюллер С., 2006)
Тип ПИДДефекты фагоцитоза
HLA-идентичный HLAсиблинг (число % неидентичный
выживших)
сиблинг(число %
выживших)
23 (70%)
14 (69%)
Синдром ВискоттаОлдрича
32 (81%)
43 (45%)
Гемофагоцитарные
синдромы
Т-клеточные дефицит
(не ТКИН)
32 (68%)
28 (49%)
47 (63%)
72 (35%)
96. Лечение при ПИД Пересадка генов – генная терапия
• В 1990 году в США осуществлена с помощьюретровируса пересадка гена аденозиндезаминазы
в аутологичные лимфоциты двух больных с ТКИД,
обусловленным отсутствием этого фермента.
Позднее вместо повторных вливаний измененных
аутологичных лимфоцитов сделали
трансплантацию ранних стволовых клеток.
• Положительные результаты зарубежом получены
при пересадке генов у больных с септическим
гранулематозом (введение генов цитохрома
р558,) синдромом «лысых лимфоцитов»
(пересадка гена регуляторного фактора синтеза
молекул HLA), синдромом LAD (пересадка генов
молекул адгезии).
97.
Вторичные иммунодефицитныесостояния или вторичные
иммунодефициты (ВтИД) –
нарушения иммунной системы
развивающиеся в постнеонатальном
периоде у детей или у взрослых и не
являющиеся результатом
генетических дефектов системы
иммунитета.
98. Современная патология человека характеризуется наличием двух взаимосвязанных и взаимообусловленных процессов
• Ростом хронических инфекционныхзаболеваний, вызываемых условнопатогенными или оппортунистическими
возбудителями
• Снижением иммунологической реактивности
населения, наблюдаемое практически во всех
развитых странах
Р.М. Хаитов, Б.В. Пинегин (2006)
99. Часто и длительно болеющие дети (ЧБД)
Критерии включения в группу ЧБД(А.А. Баранов, В.Ю. Альбицкий, 1988)
Возраст
Число эпизодов ОРИ в год
0 –1год
4 и более
1 – 3 года
6 и более
4 – 5 лет
5 и более
Старше 5 лет
4 и более
У детей старше 3 лет используют инфекционный индекс
(ИИ). ИИ= сумма всех случпаев ОРИ в течение года :
возраст ребенка (годы). У детей из группы ЧБД ИИ более
1,0.
В зависимости от возраста, эпидемиологических и
социальных условий удельный вес ЧБД может составлять
от 15 до 50% (на долю ОРИ приходится 67,7-75%).
ЧБД – не нозологическая форма и не диагноз, а группа
диспансерного наблюдения.
100.
• Бенджамин Спок опроблеме (1970):
• “В возрасте от 2 до 6 лет
дети простуживаются
чаще, болеют дольше и с
осложнениями (в среднем
7 раз в год в северных
городах США или даже
больше, если в семье есть
дети, посещающие детский
сад или школу).
• Эти цифры должны
успокоить родителей,
которым кажется, что их
малыш постоянно болеет”
101. Респираторные инфекции в детском саду
http://gazeta.aif.ru/data/mags/aif/1413/pics/67_01_01.jpg102.
Первичныеиммунодефицитные
состояния
Внеиммунные
причины
Причины
частых
заболеваний у
детей
Недостаточность
врожденного
иммунитета
Аллергия
Иммунокомпрометированность
Ярцев М.Н
Вторичные
иммунодефицитные
состояния
103. Иммунокомпрометированный ребенок. Определение.
Иммунокомпрометированность –состояние пациента, у которого можно
заподозрить недостаточно эффективную
работу иммунитета, что проявляется в более
частых, чем у сверстников, заболеваниях
104.
«Иммунокомпрометированный ребенок»и вторичное ИДС.
«иммунокомпрометированный
вторичное ИДC
ребенок»
1. Предположительное суждение, в 1. Утвердительное
суждение:
полноценности иммунитета данного иммунитет пациента безусловно
пациента можно усомниться, однако, страдает, есть ИДС.
может быть, нарушений иммунитета
нет.
2. Не
требует
лабораторного 2. Без лабораторного подтверждения
подтверждения.
остается сомнительным.
3. Не требует поиска первопричины, 3. Необходим поиск первопричины,
достаточен
факт
клинической вследствие которой развился
скомпрометированности.
вторичный ИД и оценка
возможности
устранения
(компенсации)
этой
первопричины.
105. ЭНДОГЕННЫЕ ФАКТОРЫ РИСКА
Перинатальные дефициты и патология
Недоношенность
Гипотрофия
Анемия
Рахит
Ранее искусственное вскармливание
Дисбиозы слизистых и кожи
Вторичная цилиарная дискинезия
106. ЭНДОГЕННЫЕ ФАКТОРЫ РИСКА
• Патология ЦНС и ВНС• Лимфатико-гипопластическая и экссудативнокатаральная аномалии конституции
• Очаги хронической инфекции носоглотки
• Инфицирование микобактериями туберкулеза
107. ЭКЗОГЕННЫЕ ФАКТОРЫ РИСКА
• Высокая контагиозность возбудителейОРЗ
• Низкий материальный и культурный
уровень семьи
• Взрослые и другие дети в семье с
хроническими очагами инфекции
• Раннее (в возрастном аспекте) начало
посещения детских учреждений
108. ЭКЗОГЕННЫЕ ФАКТОРЫ РИСКА
• Пассивное курение• Дефицитное по микронутриентам
питание
• Иатрогенное воздействие на иммунную
систему антибиотиков и других
фармакологических препаратов
• Нарушения экологии окружающей
среды
109. Часто болеющие дети. С чего начинать лечение?
1.Исключить (главным образом, по клиническим
параметрам) пациентов с первичными ИД и аллергией.
2.
Оценить вклад социальных (уровень
гигиены,
контактов)
и
общебиологических
факторов
(наследственность, интеркуррентные заболевания,
возрастной фактор) в частую заболеваемость и строить
программу терапии с первоочередным учетом этих
факторов.
3.
Широко использовать методы воздействия на
врожденный иммунитет (закаливание, выработку
психо-эмоциональной устойчивости, рациональное
питание, физкультура).
Ярцев М.Н., 2009
110. Заболевания, которые следует исключить у ЧБД
Первичные иммунодефициты
Респираторная аллергия
Аспирация инородного тела
Бронхолегочная дисплазия
Рецидивирующий бронхит
Муковисцидоз
Бронхоэктатическая болезнь
Внутриутробные инфекции
111. Изменения лабораторных показателей, отмеченные у часто болеющих детей:
• селективный дефицит IgA и/илиIgG2;
• недостаток секреторного IgA;
• дисиммуноглобулинемия;
• снижение
абсолютного
количества В-лимфоцитов;
• незначительное (менее чем на
20%)
снижение
различных
параметров иммунограммы –
CD3, CD4, CD16;
• сниженный фагоцитоз;
• нарушение
процессов
интерферон-образования;
• сниженный синтез лизоцима;
• снижение функциональной
112. ПРИНЦИПЫ ИММУНОКОРРЕКЦИИ ЧБД
Не лечить «измененные показателииммунитета», а лечить, если это
необходимо, часто болеющего ребенка!
Ярцев М.Н., 2009
113. «Частые ОРЗ» и первичная иммунная недостаточность у детей.
«Частые ОРЗ» выявлены в анамнеземенее, чем у 100 детей с первичной
иммунной недостаточностью и почти
исключительно
с
легкими
селективными
(селективная
недостаточность
IgA,
дефицит
подклассов IgG) или транзиторными
(транзиторная
гипогаммаглобулинемия
раннего
возраста)
формами
иммунной
недостаточности.
За этот период обследовано около
7000 детей с частой заболеваемостью,
не имевших признаков первичной
иммунной недостаточности.
Таким
образом
обследование
детей с частыми не осложненными
«ОРЗ»
крайне
редко
приводит
к
114. Отличительные особенности инфекций при первичных иммунодефицитных состояниях.
~хроническое или рецидивирующее течение, склонность к
прогрессированию;
~
политопность (множественные поражения различных органов
и тканей);
~
полиэтиологичность
(восприимчивость
возбудителям одновременно);
~
неполнота очищения организма от возбудителей или
неполный
эффект
лечения
(отсутствие
нормальной
цикличности здоровье - болезнь - здоровье).
ко
многим
По всем этим параметрам дети с «частыми ОРЗ» имеют другие
особенности инфекций.
115. Оценка иммунного статуса у детей. Как относиться к умеренному снижению отдельных показателей? (М,Н. Ярцев)
• Иммунная система, созданная в ходе эволюционноизвечного противостояния макроорганизма (в т.ч. приматов и
человека) и инфекта столь многократно эшелонирована и
дублирована, что…
… снижение отдельных показателей на 20-30 и даже 50%,
чаще всего никак не проявляется клинически, т.к.
перекрывается множеством других факторов иммунитета.
• Принципиальная особенность адаптивного иммунитета –
многократно усиливаться и приумножаться в ходе развития
иммунного ответа, поэтому совсем небольшое исходное
количество клеток нужного клона может дать достаточное
количество
клеток
потомков
для
контроля
инфекционного процесса.
116. Лечение при ВтИД
При вторичных ИД необходимо лечить тесостояния, которые привели к иммунодефициту.
Кроме этого, показаны санитарноэпидемиологический режим, рациональное
питание, витаминотерапия, коррекция
дисбактериоза, адекватная физическая
нагрузка или массаж, санаторно-курортное
лечение.
Применяется иммунокоррекция при условии
наличия информации об исходном
иммунологическом статусе больного.
117. Основные способы (уровни) противоинфекционной защиты у человека:
покровные ткани (кожа, слизистые); мукоцилиарный аппарат (микроворсинки);
сосудистые реакции, препятствующие попаданию инфектов во внутреннюю
среду;
микробицидные экзосекреты (бактерицидные компоненты слюны и слизи,
соляная кислота желудка, литические пищеварительные ферменты и т. д.);
эндогенные антибиотики (дефенсины, кателицидины, гистатины);
белки острой фазы: С-реактивный протеин и маннансвязывающий лектин,
связывающие широко распространенные бактерии и одноклеточные грибы
(опсонизация);
система Toll-подобных рецепторов (TLR), которые «оповещают о приходе
чужого» нейтрофилы, макрофаги, дендритные, эндотелиальные и эпителиальные
клетки;
система комплемента;
доиммунный фагоцитоз инфекционных агентов нейтрофилами и макрофагами;
специфический адаптивный иммунитет;
ментальная поведенческая защита.
118. Механизмы врожденного иммунитета недостаточно исследуются при оценке иммунного статуса.
• Врожденный иммунитет является преградой для развитиябольшинства инфекций и если он неполноценен – восполнить
этот пробел адаптивный иммунитет сможет не всегда и не
сразу.
• Между тем, большинство показателей оценки иммунного
статуса относятся к адаптивному (приобретенному)
иммунитету.
• Объективная
оценка
врожденного
разработана крайне недостаточно.
М.Н. Ярцев
иммунитета
119. Проблемы иммунотерапии. Можно ли воздействовать на врожденный иммунитет?
• Врожденныйиммунитет,
в
отличие от адаптивного, не
усиливается после перенесенной
инфекции,
однако,
это
не
означает, что он неизменен на
протяжении жизни и остается
таким, каким он дан при
рождении.
• Врожденный
иммунитет
изменяется
естественным
образом в процессе онтогенеза от
младенца до старца и на него
можно воздействовать.
120. Проблемы иммунотерапии. Можно ли воздействовать на врожденный иммунитет?
• Примеры положительного воздействия наврожденный иммунитет:
– закаливание, выработка устойчивости к
холоду (развитие сосудистой реакции и
стрессовой адаптации);
– преодоление
психо-эмоционального
стресса (в период адаптации к детскому
коллективу дети перестают плакать – и
меньше болеют);
– рациональное питание (в противовес
недостаточному и избыточному).
121. Показания для назначения внутривенных иммуноглобулинов, одобренные FDA USA (Red book, 30 издание, 2015)
• Первичные иммунодефициты (поддерживать уровеньIgG крови около 5 г/л)
• Кавасаки болезнь
• ВИЧ-инфекция у детей
• Гипогаммаглобулинемия при хроническом Вклеточном лимфоидном лейкозе
• Трансплантация костного мозга
• Иммуно-опосредованые тромбоцитопении
• Гийена-Барре синдром* и хронические
воспалительные демиелинизирующие полинейропатии
• Синдром токсического шока (при раннем введении)
*симметричные параличи, нарушения
чувствительности и пирамидная симптоматика
122. Титры противовирусных антител в Интраглобине ( 3-е поколение внутривенных иммуноглобулинов с сохраненным Fc-фрагментом и
высоким уровнем IgG3 – противовирусных антител)(Biotest Pharma)
Антиген
Титр
Цитомегаловирус (ЦМВ)
12 ЕД/мл
Ветряной оспы, опоясывающий лишай
5 ЕД/мл
Простого герпеса 1/2
1 : 37 200
Эпштейна-Барра
14 М.Е./мл
Паротита
Корь
1 : 2048-4096
0,5-0,8 М.Е./мл
Краснуха
>1 :128
Парвовирус В19
1 : 1000
Парагрипп (разные штаммы)
1 : 8-32
Полиомиелит (разные штаммы)
Коксаки (разные штаммы)
Аденовирусы
0,2-0,9 М.Е./мл
1 : 8-320
1 : 20
Гепатит В
0,2-0,5 М.Е./мл
Гепатит А
7-15 М.Е./мл
Токсоплазмоз
1 : 256
123. Вирусная безопасность ВВИГ
Названиепрепарата
Контроль
исходной
плазмы на
антитела к ВИЧ1/-2/-), HBsантиген и
гепатиту С
Контроль исходной
плазмы на ДНК
вирусов гепатита В,
парвовирус В19,
РНК вирусов
гепатита С, А и ВИЧ
Количество
степеней
вирусинактивац
ии
Лекарственная
форма
Пентаглобин
Да
Да
4
Готовый к
употреблению 5%
раствор
Интраглобин
Да
Да
4
Тоже
Октагам
Да
ДНК вирусов
гепатита В, РНК
вирусов гепатита С,
А и ВИЧ
3
Тоже
Габриглобин
Да
Нет
1
Тоже
Хумаглобин
Да
Нет
1
Лиофилизат
124.
Иммуноглобулины,обогащённые антителами
класса IgM
Пентаглобин
125.
Пентаглобин обеспечивает не только специфическийпассивный иммунитет (прежде всего к граммотрицательным
бактериям), но за счет повышенного содержания IgM
неспецифически активирует фагоцитоз (в 1000 раз активнее
чем IgG), Т-лимфоциты хелперы (амплифаеры - усилители),
имеющие рецептор FcμR, со всеми последствиями для
продукции цитокинов.
Кроме того, IgM лучше других классов ИГ активирует
систему комплемента по классическому пути. Как пентамер,
он наиболее активно агглютинирует бактерии - одна
молекула IgM способна уничтожить одну бактерию, но для
этого необходимо 2000 молекул IgG. Эти свойства
пентаглобина одновременно с терапевтическим эффектом
служат и профилактике ИДС, т.е. препятствуют
присоединению оппортунистических возбудителей.
126. Титры противобактериальных антител в Пентаглобине (Biotest Pharma)
АнтигенПентаглобин
Интраглобин
Грамотрицательные бактерии
E. coli
640/1280
80
Pseudomonas aeruginosa
640/1280
160
Klebsiella pneumoniae
1280/2560
40-80
Serratia marcesens
64
-
Proteus vulgaris
64
8
Salmonella typhimurium
16
16
Salmonella paratyphi
Грамположительные бактерии
Streptococcus viridans
320
0
Streptococcus pyogenes
320-360
0
640
0
Streptococcus agalactiae
(Streptococcus B)
80 - 160
0
Staphylococcus aureus
160 - 320
10
160
0
Streptococcus faecalis
Staphylococcus epidermidis
Противотоксические антитела
Lipid A
E. Coli J5
2521
Не определяли
2569 (IgM)
640
Способность связывать липосахарид разных штаммов E. Coli у IgM была в 4-20 раз выше, чем у IgG
127. Пентаглобин (Pentaglobin) Biotest Pharma (Германия)
• 5% белки плазмы человека (ампулы по 10 и 20 мл и флаконы по 50 или100 мл), из них (95% - иммуноглобулины) и в 1 мл: IgG – 76% (38 мг), IgM
– 12% (6 мг), IgA – 12% (6 мг).
• Дозировка 5 мл/кг/сутки в течение 3-х дней или через день.
Обязательным условием правильного применения Пентаглобина является
соблюдение рекомендуемой скорости введения препарата.
• Пентаглобин вводят внутривенно со следующей скоростью:
Новорожденные и грудные дети – не более 1 7 мл/кг/час с помощью
инфузионного насоса.
Продолжительность курса терапии:
Необходимость повторного введения зависит от клинического течения болезни
128. Пентаглобин – золотой стандарт лечения при сепсисе и септическом шоке
Пентаглобин является единственным ВВИГ, эффективностькоторого в плане снижения летальности при сепсисе и
септическом шоке подтверждена с позиций доказательной
медицины (надежность доказательств – категория Ia,
рекомендации – категория А).
Обоснованность включения Пентаглобина в комплексную
терапию пациентов с сепсисом и септическим шоком
подтверждена данными мета-анализа, проведенного группой
независимых ученых Соchrane Infection Disease Group, указавшей
что это снижает летальность в 2,1 раза.
(Alejandria M.M. et al. The Cochrane Library, 2005, Issure 3, Oxfort Update
Software)
129.
ИММУНОМОДУЛЯТОРЫ –ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ОБЛАДАЮЩИЕ
ИММУНОТРОПНОЙ АКТИВНОСТЬЮ, КОТОРЫЕ В
ТЕРАПЕВТИЧЕСКИХ ДОЗАХ ВОССТАНАВЛИВАЮТ
ФУНКЦИЮ ИММУННОЙ СИСТЕМЫ
(ЭФФЕКТИВНУЮ ИММУННУЮ ЗАЩИТУ)
130. Фитопрепараты
• Иммунал – препарат эхинацеи пурпурной семейства астровыхрастений. Иммуновит - препарат эхинацеи пурпурной в
сочетании с цинка глюконатом и витамином С
• Хлорофиллипт, эвкаламин, эвкабал С – препараты эвкалипта,
обладающие помимо способности стимулировать
неспецифическую резистентность, бактерицидной и
бактериостатической активностью
• Фитосборы с зверобоем, календулой, ромашкой, алое (сок) и др.
• Зостерин-Ультра получают из морской травы Zosteria marina,
которая произрастает в экологически чистых акваториях
Приморского края. Зостерин-ультра - сложный углеводный
полимер пектиновой природы, состоящий в основной цепи из
блоков полигалактуроновой кислоты, соединенных связями сахара
D-рамнозы.. В состав молекулы Зостерина –Ультра входят также
другие сахара: D- апиоза, D-ксилоза, D-галактоза, L-арабиноза и 20-метил-D-ксилоза.
131.
• Зостерин-Ультра: энтеросорбция - способность захватывать вжелудочно-кишечном тракте вредные вещества и выводить их из
организма
• Зостерин-Ультра: гемосорбция - способность попадать в кровь и
внутренние органы, связывать там вредные вещества и выводить их из
макроорганизма
Зостерин-Ультра 30%:
• Дисбактериоз кишечника
• Инфекционно-воспалительные заболевания желудочно-кишечного тракта
(гастродуодениты, энтероколиты) – 10-15 сут
• Дискинезия желчевыводящих путей и рефлюкс-гастриты
• Профилактика дисбактериоза при длительной антибактериальной терапии
- 10-20 сут
• Затяжные физиологические желтухи и поражения печени различного
генеза
Детям в возрасте до 3 лет - не более 0,25 г/сут
Детям в возрасте от 3 до 12 лет - 0,5 г/сут
Детям старше 12 лет - 1,0 г/сут
132. Рекомендации к дифференцированному применению медикаментов при вторичных иммунодефицитных состояниях (Стандарты диагностики и
лечения «Иммунология и аллергология» 2001)При дефиците функции моноцитарномакрофагальной системы (ММС) применяют:
• Полиоксидоний в дозе от 6 до 12 мг;
• Ликопид в дозе 1 и 10 мг.
При наиболее тяжелых формах лейкопений
используют препараты гранулоциарномакрофагальных колониестимулирующих
факторов
• Молграмостим (Лейкомакс) 150 300 и 400 мкг;
• Филграстим (Нейпоген) 300 и 480 мкг;
• Граноцит (Ленограстим) 105 265 и 365 мкг.
133. Рекомендации к дифференцированному применению медикаментов при иммунодефицитных состояниях (Стандарты диагностики и лечения
«Иммунология и аллергология» 2001)При дефектах клеточного звена иммунитета
назначают один из препаратов:
• Полиоксидоний в дозе от 6 до 12 мг;
• 0 01% раствор Тактивина в дозе 1 мл п/к;
• 0 01% раствор Тимогена в дозе 1 мл в/м;
• Тималин 10 мг;
• Имунофан.
При нарушении синтеза антител Влимфоцитами показаны:
• Миелопид 0 003 г;
• Полиоксидоний в дозе от 6 до 12 мг.
134.
По данным ВОЗ• иммуностимуляторы, относящиеся к тимическим
факторам, такие как естественные (получаемых из
зобной железы крупного рогатого скота) и
синтетические (тимогены) запрещены к продаже в
большинстве стран мира, из-за возможного риска
развития бычьей губковидной энцефалопатии
• использование левамизола ограничено из-за риска
возникновения у пациентов агранулоцитоза
World Health Organization. Fact Sheet 113. (accessed July 20, 2005) 2005
135. Рекомендации к дифференцированному применению медикаментов при иммунодефицитных состояниях (Стандарты диагностики и лечения
«Иммунология и аллергология» 2001)При нарушении синтеза - и интерферонов показано назначение
следующих препаратов:
• Интерфероны:
- природные (Человеческий лейкоцитарный
интерферон Эгиферон Лейкинферон);
- рекомбинантные (Реаферон Роферон
Виферон Реальдирон Интрон А Инрек).
• Индукторы интерферонов (Амиксин
Циклоферон Неовир Полудан);
136. Иммунотерапия у новорождённых
Виферон 1 – отечественный препарат (150000 МЕрекомбинантного интерферона α2β в сочетании с
витаминами Е и С; препарат активирует
макрофаги, усиливая представление антигена, В- и
Т-системы иммунитета) новорождённым
назначают в виде ректальных свечей 2 раза в сутки
в течение 5 дней, далее 5 дней перерыв и вновь
такой же курс, в дальнейшем при вирусных
внутриутробных инфекциях в течение полугода
рекомендуют вводить по две свечи каждые 2-3 дня.
137. Применение Виферона у ЧБД (Г.А. Самсыгина,Педиатрия, 2015, № 4)
Суппозитории ректальные:• Детям в возрасте от 1 мес. до 3 лет по 150 000 МЕ (Виферон 2) 2
раза в день в течение 5 дней, далее по 500 000 МЕ 2 раза в день в
течение 5 дней (Виферон 1)
• Детям в возрасте от 3 до 7 лет по 500 000 МЕ 2 раза в день в
течение 5 дней, далее по 500 000 МЕ 1 раз в день утром и 150 000
МЕ 1 раз в день вечером в течение 5 дней (Виферон 1)
• Детям в возрасте от 7 до 18 лет по 1 000 000 МЕ (Виферон 3)
1 раз в день утром и 500 000 МЕ 1 раз в день вечером в течение 5
дней и далее по 500 000 МЕ 2 раза в день в течение 5 дней
138.
Индукторы интерфероновАрбидол
Циклоферон
Амиксин
Неовир
Дибазол
Пентоксифиллин (трентал)
Курантил (дипиридомол)
139. Арбидол -ЛЭНС
• Противовирусное средство• Препятствует контакту и проникновению
вирусов в клетку
• Обладает интерферон-индуцирущим
действием, повышая устойчивость
организма к вирусным инфекциям
• Дозы: детям 2-6 лет – 0,05 г; 6-12 лет –
0,1 г; старше 12 лет и взрослым - 0,2 г 23 раза в день до еды 10-14 дней.
140.
141.
Принципы воздействия иммуномодуляторовна иммунную систему
Полиоксидоний
Нейтрофилы
МП-3
NKклетки
Макрофаг
Бакт.препараты
Ликопид
Моноцит
МП-1
Интерфероны
Т-клетки
Имунофан
В-клетки
Тактивин
142.
Полиоксидоний -N-оксидированное производное полиэтиленпиперазина
применяется у взрослых в дозе 6 - 12 мг
и детей в дозе 0,1 - 0,15 мг/кг в сутки
Полиоксидоний
для
инъекций
3мг и 6 мг
• внутривенно
капельно
• внутримышечно
• интраназально
• сублингвально
таблетки
12 мг
сублингвально
Полиоксидоний показан
суппозитории
6 мг
• ректально
• интравагинально
при всех вторичных иммунодефицитных состояниях,
проявляющихся в острых и хронических, рецидивирующих
и вялотекущих инфекционно-воспалительных процессах
бактериальной, вирусной и грибковой этиологии
143.
Механизмы фармакологического действияПолиоксидония в организме
1. Иммуномодулирующее действие проявляется в
повышении миграции фагоцитов в воспалительный очаг
усилении поглощения и переваривания микробов фагоцитами
усилении ферментативной активности фагоцитов
повышении функциональной активности Т-лимфоцитов
стимуляции антителообразования
усилении цитотоксичности NK-клеток
повышении устойчивости к бактериальным и вирусным
инфекциям
2. Детоксицирующее действие проявляется в
способности сорбировать экзо- и эндотоксины, находящиеся в
кровяном русле и тканях организма и выводить их из организма
снижении токсичности ряда лекарственных препаратов и
химических веществ
3. Антиоксидантное действие
проявляется в
способности ингибировать в организме свободно-радикальные
реакции
4. Мембранопротекторное действие проявляется в
защите клеток от повреждающего действия токсических веществ
144. Схема терапии полиоксидонием
Сублингвально илиинтраназально, из расчета 0,15
мг на кг веса ежедневно – 10
дней, через месяц курс
повторить
145. Вывод об эффективности лечения часто болеющих детей полиоксидонием
Сублингвальное и интраназальное использованиеПолиоксидония позволяет достичь у часто болеющих
детей удлинения периодов клинической ремиссии и
нормализации измененных лабораторных показателей,
что подтверждает эффективность применения
препарата у ЧБД.
Назначение Полиоксидония курсом 12 инъекций (в/м,
0,15 мг\кг) достоверно уменьшило частоту
интеркуррентных инфекций у 72% больных
бронхиальной астмой, улучшало показатели внешнего
дыхания, снижало уровни IgE, IL-4, IL-6, IL-8 (И.И.
Балаболкин, 2012).
146. Иммуномодуляторы (L03)
Иммуностимуляторы (L 03A)АТХ
МНН / НН
колониестимулирующие
факторы
L 03AA
ленограстим
филграстим
интерфероны
L 03AВ
интерферон альфа
интерферон альфа-2a
интерферон альфа -2b
интерферон бета-1a
интерферон бета-1b
L 03AС
интерлейкин 2
интерлейкин 1-b
L 03AХ
бактериальные
растительные
животного происхождения
интерлейкины
прочие
иммуностимуляторы
147. Механизм действия
• Фактический механизм подавляющего большинства используемыхиммуностимуляторов полностью еще не изучен
• В настоящее время механизм действия известен только для
иммуностимуляторов бактериального происхождения
• Считают, что эти средства стимулируют и активизируют иммунные
клетки макроорганизма (прежде всего Т лимфоциты), используя
рецепторы, расположенные на поверхности иммунных клеток,
которые опознают в организме бактерии
• Не обладая селективным механизмом действия, большинство
бактериальных иммуностимуляторов вызывают «адъювантный»
эффект, оптимизируя презентацию антигена
• Таким образом, бактериальные иммуностимуляторы активируют
оба вида иммунитета – врождённый и приобретённый.
Del-Rio-Navarro B., et al. Cochrane Database Syst Rev. 2006 Oct 18;(4):CD004974.
148. Ликопид
•Синтетический аналог одного из компонентовбактериальной стенки
•Главная мишень –клетки фагоцитарно-макрофагального
звена
•Усиление поглощения и киллинга микроорганизмов
•Стимуляция продукции антител
•Повышение пролиферации Т и В-лимфоцитов
•Показания: хронические фарингит, бронхит, аденоидит,
повторные ОРЗ, рецидивирующий фурункулез, пиодермия.
•Схема приема – по 1 табл. (1мг, 10мг) 1 раз в день
(рассасывать или проглатывать) или по 0,5 табл. 2 раза в
день в течение 10 дней
149. ИМ микробного происхождения (ИММП) Бактериальные лизаты: мировой опыт
ИМ микробного происхождения (ИММП)
Бактериальные лизаты: мировой опыт
Современные бактериальные лизаты
разработаны в 70-х годах и первые
коммерческие продажи – с конца 80-х годов
• Сегодня бактериальные лизаты
зарегистрированы и используются в 65
странах мира, например: BronchoVaxom/Imocur: 63 страны
• Суммарно в мире ежегодно бактериальные
лизаты применяют около 8 млн. пациентов
• С 80-х годов около 130 -180 миллионов
пациентов, пролеченных бактериальными
лизатами
INTERNATIONAL BOARD: BACTERIAL IMMUNOSTIMULANTS IN PREVENTION OF
RECURRENT RESPIRATORY TRACT INFECTIONS, Paris, March 1-2, 2006
150.
Бактериальные лизаты преимущественноместного действия
ИРС – 19
Имудон
151.
I.R.S.фирмы Sarbach)
19
SOLVAY (Бывший препарат
Содержит:
– бактериальные лизаты 18 бактерий
Streptococcus pneumoniae (6x), staphylococcus aureus,haemophilus influenzae
type b, klebsiella pneumoniae, acinetobacter calcoaceticus var baumannii,
moraxella catarrhalis, neisseria subflava (2x) streptococcus pyogenes A,
streptococcus dysgalactiae C, enterococcus faecium, streptococcus gpe G,
enterococcus faecalis
Назальный спрей:
–1 доза в каждый носовой ход, 2 раза в день в течение 2 недель
Преимущества для врача:
–Иммуностимулирующий эффект на неспецифическую иммунную
систему
– Немедленный эффект глицина и ароматических веществ...
152.
Бактериальные лизатыпреимущественно
системного действия
Бронхо-мунал (Бронхо-ваксом)
Рибомунил
Рузам
ВП – 4
Биостим
Иммуфорс
153.
Кохрейновский обзор 20061. В Обзоре включено и
проанализировано 759
сообщений по
иммуностимуляторам.
2. Среди них 34 плацебоконтролируемых исследования,
включенных в мета-анализ, 6 из
которых относятся к уровню
доказательноси класса А
(адекватно рандомизированные,
двойные-слепые).
3. Более 70% исследований класса А
изучали ОМ-85 (Бронхо-мунал)
.
153
154. Бронхо-муналâ
Бронхо-мунал• Лиофилизированный лизат бактерий
Streptococcus pneumoniae
Haemophilus influenzae
Klebsiella pneumoniae
Klebsiella ozaenae
Staphylococcus aureus
Streptococcus viridans
Streptococcus pyogenes
Moraxella catarrhalis
155.
Прием Бронхомунала ®Усиление защиты против
рецидивирующих ИДП
Местная продукция Ig
на
уровне дыхательных путей
Миграция иммунных клеток в
органы и системы (особенно в
дыхательную)
Циркуляция иммунных
На уровне ЖКТ
происходит
инициация процесса , приводящего
к настройке системы врожденного
иммунитета
клеток в кровеносных и
лимфатичеких сосудах
Активация T и B
лимфоцитов (основных
клеток , включенных защиту
организма)
155
156.
Фармакологический профильБронхо-мунала ®
• Врожденный иммунитет: стимуляция
- Моноцитарной и
макрофагальной активности
- Созревания и увеличение
активности дендритных клеток
- Активности гранулоцитов
- Натуральных киллеров
Emmerich 1990, Respiration, 57, 90-99
Wybran 1989, Immunopharmacol and Immunotoxicol, 11, 1, 17-32
Meredith 2007, Int J Biotechnology, 9, ¾, 344-59
Zelle-Rieser 2001, Immunol Letters, 76, 63-67
Lusuardi 1996, Eur Respir Rev, 6, 36, 182-5
and 2002, Eur Resp J, 19, 785-6
156
157.
Фармакологический профильБронхо-мунала ®
• Приобретенный иммунитет: увеличение
- Сывороточных IgA, IgG,
IgM
- Секреторного IgA
- Активности T клеток
- Активности В клеток
Puigdollers 1980, Respiration, 40, 142-9
Byl 1998, J Interferon and cytokines, 18, 817-21
Quezada 1999, J Inv Allergol Clin Immunol, 9, 3, 178- 82
Genel 2003, Cur ther Res, 64, 8, 600-15
Bowman 2001, Infection and Immunity, 69, 6, 3719-27
Lusuardi 1996, Eur. Respir Rev, and 2002 , Eur Resp J, 19, 785-6
Huber 2005, Eur J Med Res, 10, 209-17
157
158. Секреторные антитела
Синтез секреторных Ig A- 2 фрагмента IgA соединяются вместе с
секреторным фрагментом = s IgA
Молекула секреторного
IgA
- s IgA задерживаются на поверхности
J chain
слизистых и присутствуют в секретах
(слюна, отделяемое носа…)
• Ig A фиксируется на мембране
эпителиальной клетки
секреторный
фрагмент
Защита слизистых
•Crotty 2004, Seminars in immunol, 16, 197-203
158
159. Бронхо-муналâ
ПОКАЗАНИЯ• профилактика рецидивирующих
инфекций дыхательных путей (в т.ч.
хронического бронхита и ЛОРинфекций (включая ОСО)
• лечение инфекций дыхательных путей
в комбинации с другими препаратами
160. БРОНХО-МУНАЛâ
«...Назначение не требует специальныхлабораторных иммунологических
исследований, в отличие от
лекарственных препаратов, содержащих
регуляторные пептиды центрального
происхождения (тимического и
костномозгового)...»
Тузанкина И.А., 1998
161. Бронхо-муналâ Дозирование
xxxxxxxxxxxxxxxxxxxx
xxxxxxxxxx
162. ЛОР-инфекции: Бронхо-мунал уменьшает необходимость применения антибиотиков (Paupe G., 1991)
Пациенты (%)50
40
30
20
10
44,0
39,5
16,5
(n=61)
23,5
0
без обострения
инфекций
placebo (n=55)
Broncho-munal
без применения
антибиотиков
163. Бронхо-мунал в лечении бронхиальной астмы
Число ингаляций симпатомиметиковБронхо-мунал в лечении
бронхиальной астмы
160
control
Broncho-munal
140
120
100
80
60
40
20
0
1
2
3
4
5
6
месяцы
164. Таким образом
• Бактериальные лизаты - одна из самых популярныхгрупп иммуномодуляторов
Наиболее часто применяются в педиатрической практике
Бактериальные лизаты влияют на иммунную систему иначе,
чем вакцины (принципиально другая группа по механизму
действия)
Доказанное влияние на оба звена иммунитета (врожденное
и приобретенное)
Накопленный большой опыт использования бактериальных
лизатов подтверждает, что они восполняют недостаток
физиологической иммуностимуляции
«Иммуномодуляторы в педиатрии» Д.Г. Чувиров, М.Н. Ярцев, Педиатрия, 2009,
165.
Профиль безопасности Бронхомунала®* Используется более 30 лет: около 3.5
миллионов пациентов ежегодно в мире
принимают (взрослые и дети).
* В 3-х отчетах по регистрации побочных
эффектов, включавших 100'000 пролеченных
пациентов (взрослые и дети) –
распространенность побочных эффектов
среди детей: 1.43 /100'000 , среди взрослых:
1.09/100'000.
Source : Broncho-Vaxom ® - latest PSURs / Risk management
Plan / DrugWatch database
166. ВЫВОДЫ
• В большинстве случаев иммунокорригирующаятерапия у иммунокомпроментированных детей
назначается по клиническим показаниям, а
выбор препарата осуществляется эмпирически
• Предпочтение следует отдавать наиболее
проверенным иммуномодуляторам с
множественным механизмом действия
Ярцев М.Н. , из доклада проекта «ОЛИМП»
167.
168. А.В. Караулов «Препарат пидотимод – новое эффективное средство в иммунопрофилактике и иммунотерапии респираторных инфекций у
детей»(Вопросы современной педиатрии, 2008, № 1, с.96-100)
•Пидотимод (3-L-пироглютпмат-Lтиазолилин-4карбоксильная кислота) – синтезированный
иммуномодулирующий препарат пептидной
структуры с высокой биодоступностью (4345%)при приеме внутрь
•Эффекты: активирует фагоцитоз и другие
параметры врожденного иммунитета,
восстанавливает активность В- и Т- лимфоцитов,
активизирует синтез провоспалительных
цитокинов и γ-интерферона
•Эффективность изучена в более чем 60
контролируемых исследованиях на более 3200
пациентов с ОРЗ и рецидивирующими РЗ.
•Далее приведены результаты лечения 416
пациентов в от 3 до 14 лет с рецидивирующими
фаринготонзиллярными инфекциями
169. А.В. Караулов «Препарат пидотимод – новое эффективное средство в иммунопрофилактике и иммунотерапии респираторных инфекций у
детей»(Вопросы современной педиатрии, 2008, № 1, с.96-100)
170. А.В. Караулов «Препарат пидотимод – новое эффективное средство в иммунопрофилактике и иммунотерапии респираторных инфекций у
детей»(Вопросы современной педиатрии, 2008, № 1, с.96-100)
171. А.В. Караулов «Препарат пидотимод – новое эффективное средство в иммунопрофилактике и иммунотерапии респираторных инфекций у
детей»(Вопросы современной педиатрии, 2008, № 1, с.96-100)
• В рандомизированном исследовании участвовало 40
пациентов разного возраста (дети и взрослые) с
наличием в анамнезе не менее 5 эпизодов фарингита и
(или) тонзиллита за последний год, протекавших с
фебрильной лихорадкой.
• Пидотимод (Имунорикс) по 800 мг взрослым и 400 мг
детям в течение 2-х месяцев (или капсулованный
лифилизат по 7 мг взрослым и 3.5 мг детям в течение
10 дней в месяц 3 месяца)
• Вывод достоверно снизилась как частота так и
продолжительность инфекций уменьшилась
экспрессия CD30, т.е. препарат изменяет
дифференцировку Th-1/Th-2 в сторону Th-1.
172. Изопринозин (инозин пранобекс, «Гроприноксин» - Гедеон Рихтер
• Инозин пранобенакс – синтетическийиммуномодулятор (соль парааминобензойной кислоты,
NN-диметил-амино-2-пропанол и β-изомер инозина в
соотношении 3:1), обладающий противовирусной
активностью и стимулирующий Т-лимфоциты,
фагоцитарную активность макрофагов. Не
аллергогенен, не токсичен.
• Согласно В.А. Ревякиной (МГ 29.5.2015) назначение
внутрь при ОРВИ в дозе 50-100 мг/кг (на 3 приема
внутрь) в комплексной терапии и профилактике
препарат снижает тяжесть симптомов на 60%,
сокращает продолжительность заболевания на 88%,
снижает частоту развития осложнений в 4 раза,
сокращает частоту применения антибиотиков на 93%,
снижает заболеваемость ОРВИ после
профилактического применения (14-21 день) на 81%.
173.
ПЕРВЫЙ В РОССИИ ПРЕПАРАТ ИНОЗИНА ПРАНОБЕКСДЛЯ ЛЕЧЕНИЯ ЧБД С ОСЛАБЛЕННЫМ ИММУНИТЕТОМ
•ИМЕЕТ ДЕТСКУЮ ЛЕКАРСТВЕННУЮ ФОРМУ
•ДОЗИРУЕТСЯ В СООТВЕТСТВИЕ С ВЕСОМ РЕБЕНКА
у ЧБД С РАЗВИТИЕМ
МЕСТНЫХ/ОБЩИХ ОСЛОЖНЕНИЙ
РУ ЛП-004000 от 06.12.2016г.
Инструкция по медицинскому применению препарата Нормомед.
Производитель:
ABC Фармацойгичи С.п.А., Италия
Виа Кантоне Моретти, 29 (местность Локалита Сан Бернардо)
10090, Ивреа (Турин).
Тел.: 0125/240111 Факс: 0125/240179
174.
ЛЕЧЕНИЕ ОРВИ/ГРИППА у ЧБД С РАЗВИТИЕММЕСТНЫХ/ОБЩИХ ОСЛОЖНЕНИЙ
Иммуномодулятор, обладающий
иммуностимулирующей активностью и
неспецифическим противовирусным действием
стимулирует активность цитотоксических Т-лимфоцитов и
естественных киллеров, функцию Т-супрессоров и Т-хелперов;
повышает продукцию иммуноглобулина (Ig) G, интерферона-гамма,
интерлейкинов (ИЛ-1 и ИЛ-2);
снижает образование провоспалительных цитокинов - ИЛ-4 и ИЛ10;
потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов.
* Хаитов
Р.М., Пинегин Б.В. // Аллергия, астма и клиническая иммунология — 2000. — 1. — 9-16.
Masihi K.N. // Int. J. Antimicrob. Agents. — 2000. — 14, 3. — 181-191.
175. С февраля 2004 по май 2005 года 110 часто болеющих детей привито вакцинами АКТ-ХИБ, ВАКСИГРИП и ПНЕВМО 23 (компания sanofi
pasteur)50
60
акт-хиб + пневмо
23
акт-хиб + пневмо
23 + ваксигрипп
Проф. Т.И. Гаращенко, проф. Л.И. Ильенко, М.В
.Гаращенко
176. Частота обострений и приема антибактериальных препаратов в первой группе детей (АКТ-ХИБ + ПНЕВМО 23)
109
8
7
6
5
4
3
2
1
0
до вакцинации от 5
до 13 раз
после вакцинации
от 2 до 5 раз
частота
обострений
частота
приема
антибиотиков
Проф. Т.И. Гаращенко, проф. Л.И. Ильенко, М.В .Гаращенко
177. Частота обострений и приема антибактериальных препаратов во второй группе детей (Акт-ХИБ + ПНЕВМО 23 + ВАКСИГРИП)
87
6
5
4
3
2
1
0
до вакцинации от 5
до 10 раз в год
после вакцинации
от 1 до 2 раз за 6
мес
частота
обострений
частота
приема
антибиотиков
Проф. Т.И. Гаращенко, проф. Л.И. Ильенко, М.В .Гаращенко
178. Выводы
• Часто и длительно болеющим детям с хронической ирецидивирующей неспецифической инфекционной
патологией различных отделов бронхолегочной
системы показано проведение комбинированной
вакцинации против S. pneumoniae и H. influanzae (тип
b)
• Для снижения числа неспецифических инфекционных
заболеваний верхних и нижних дыхательных путей у
детей, может быть рекомендована активная
иммунизация вакцинами «Пневмо 23», «Акт-ХИБ» и
«Ваксигрип»
Проф. Т.И. Гаращенко, проф. Л.И. Ильенко, М.В .Гаращенко






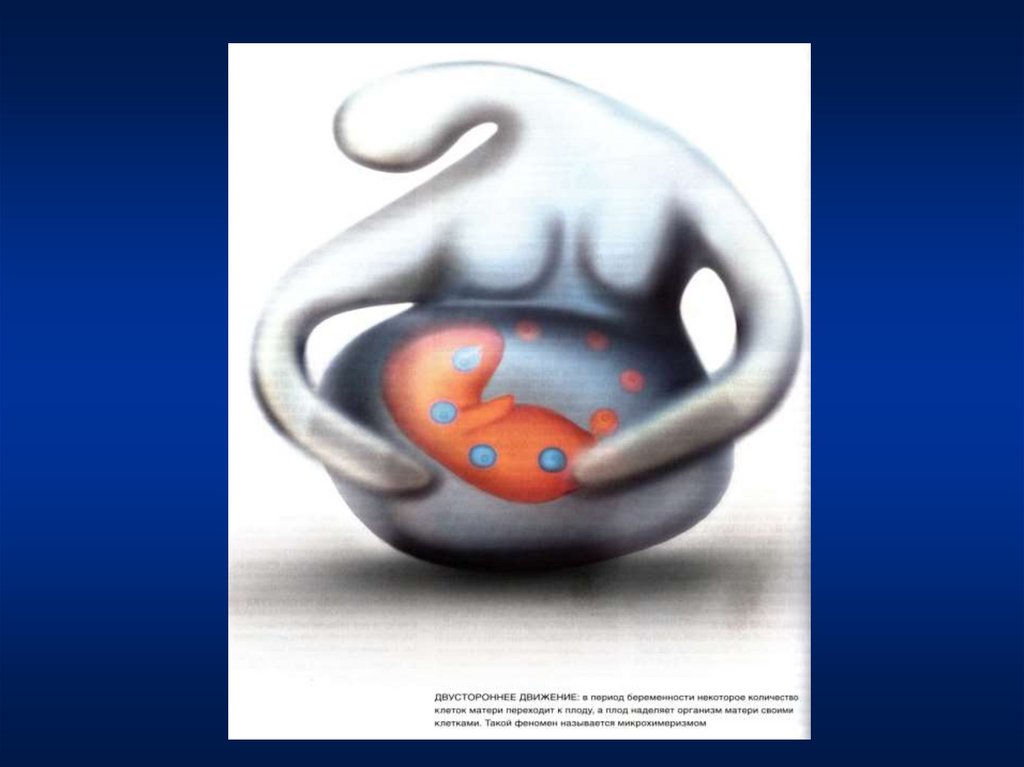









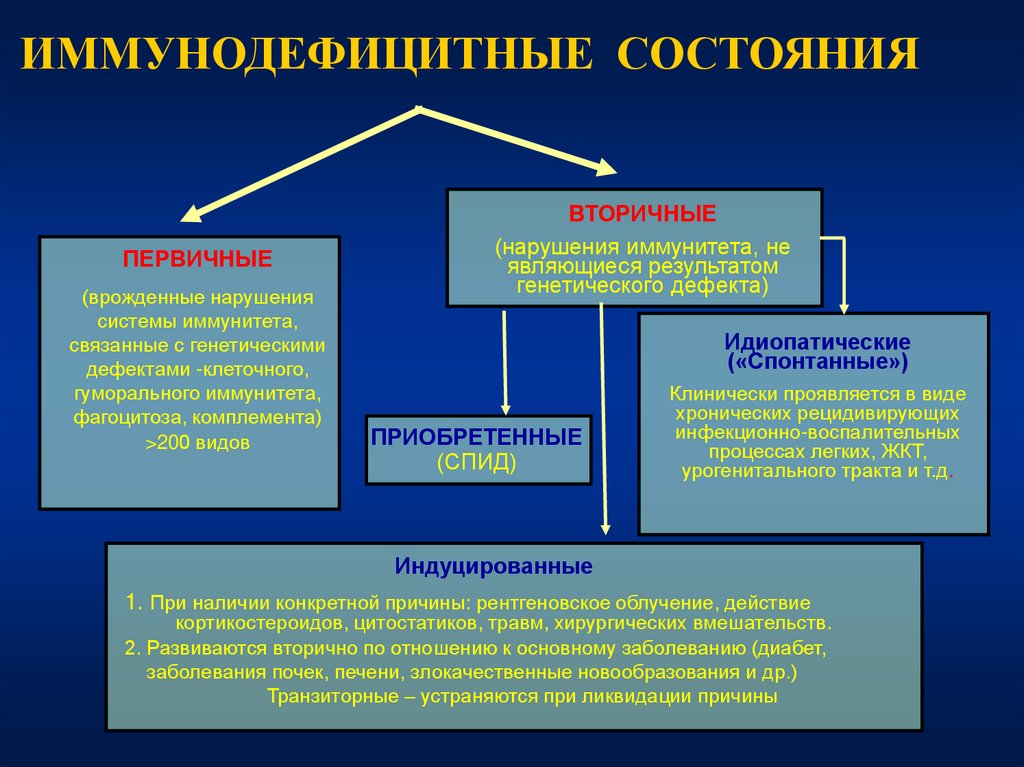




















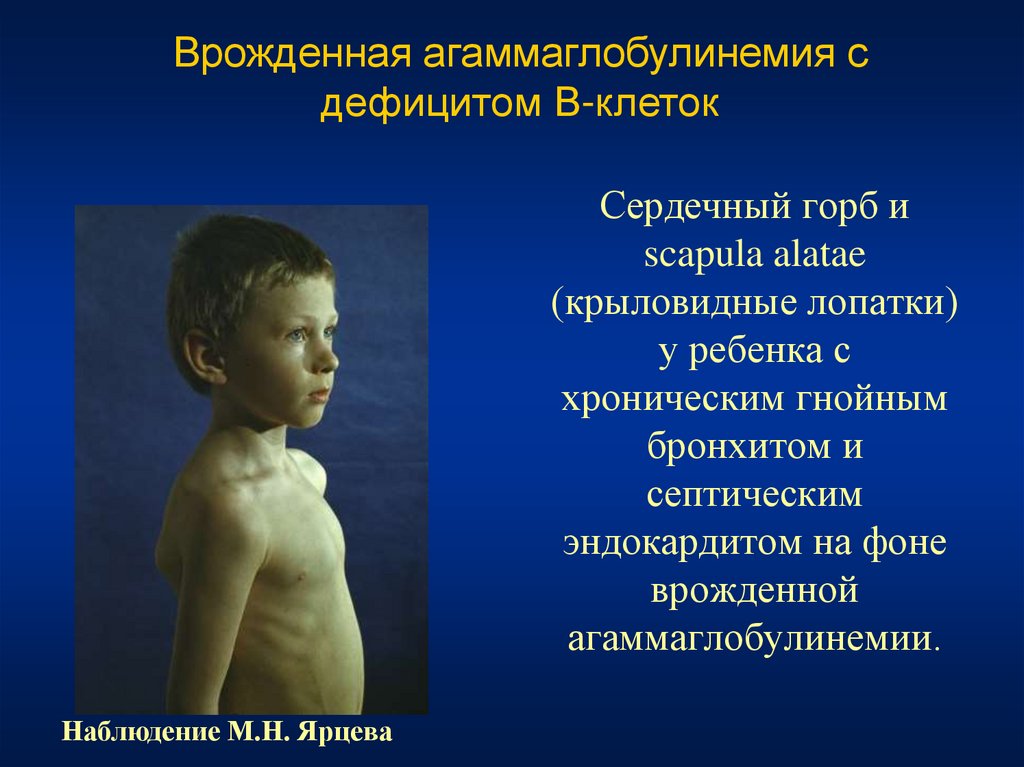
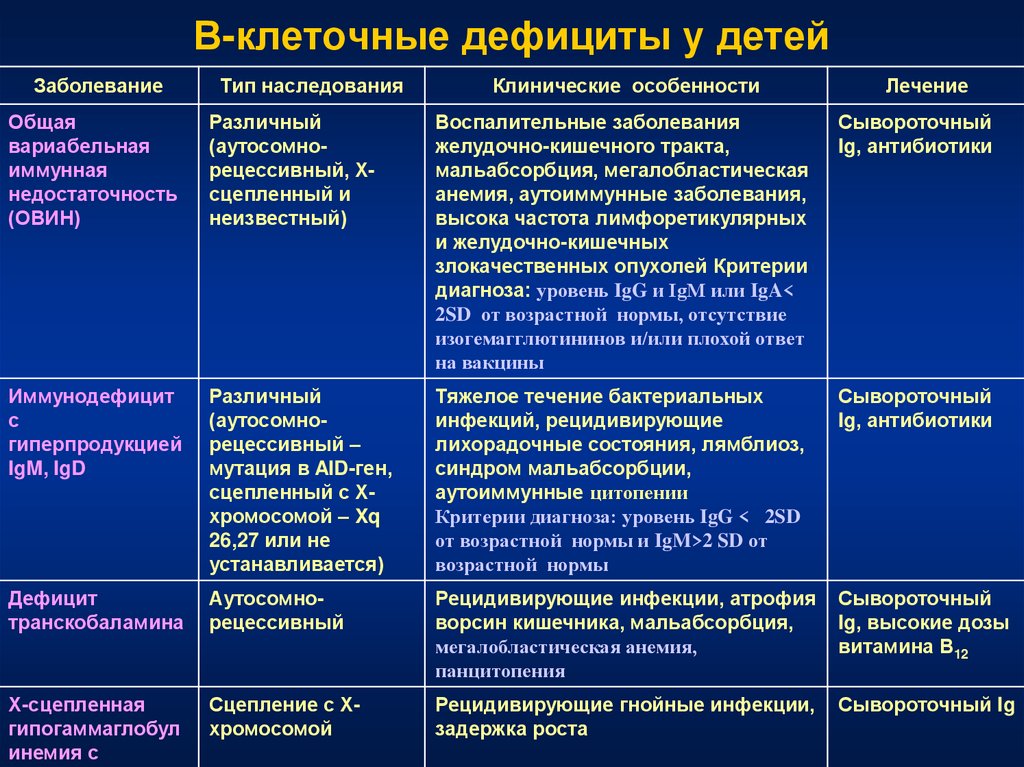
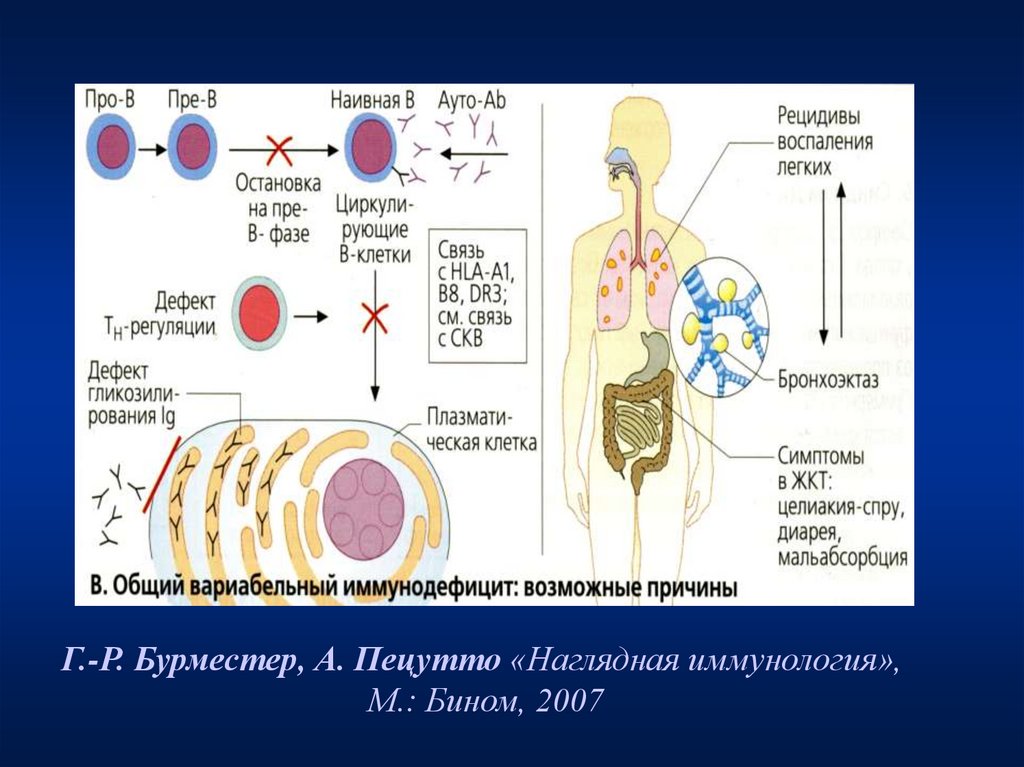


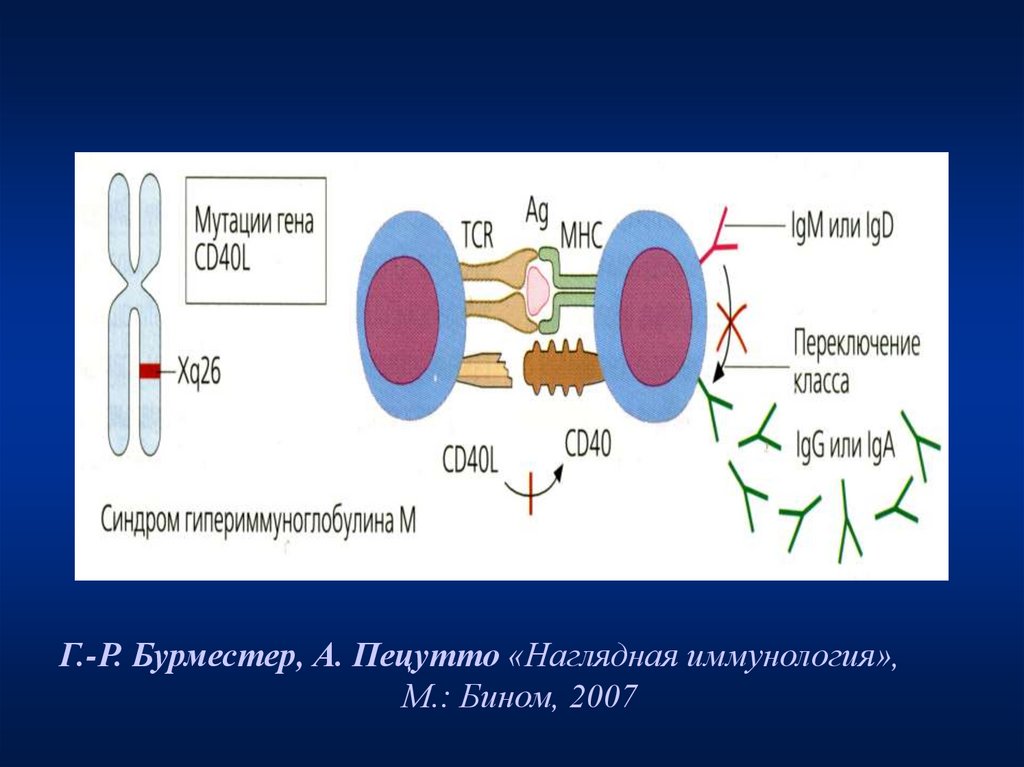








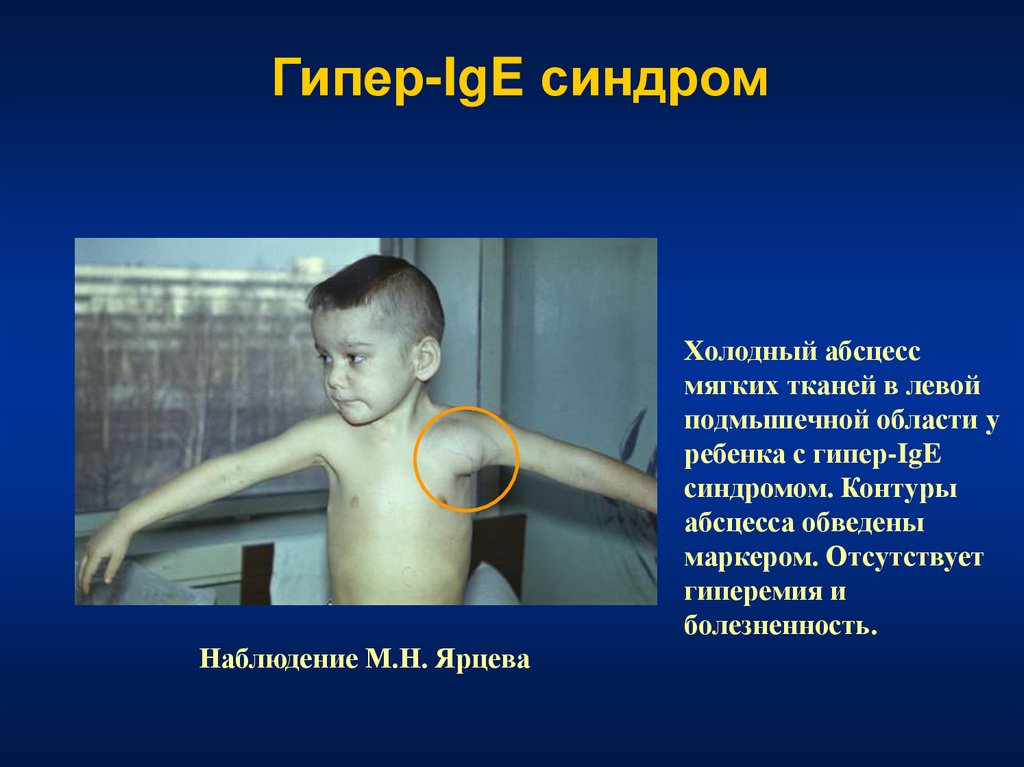




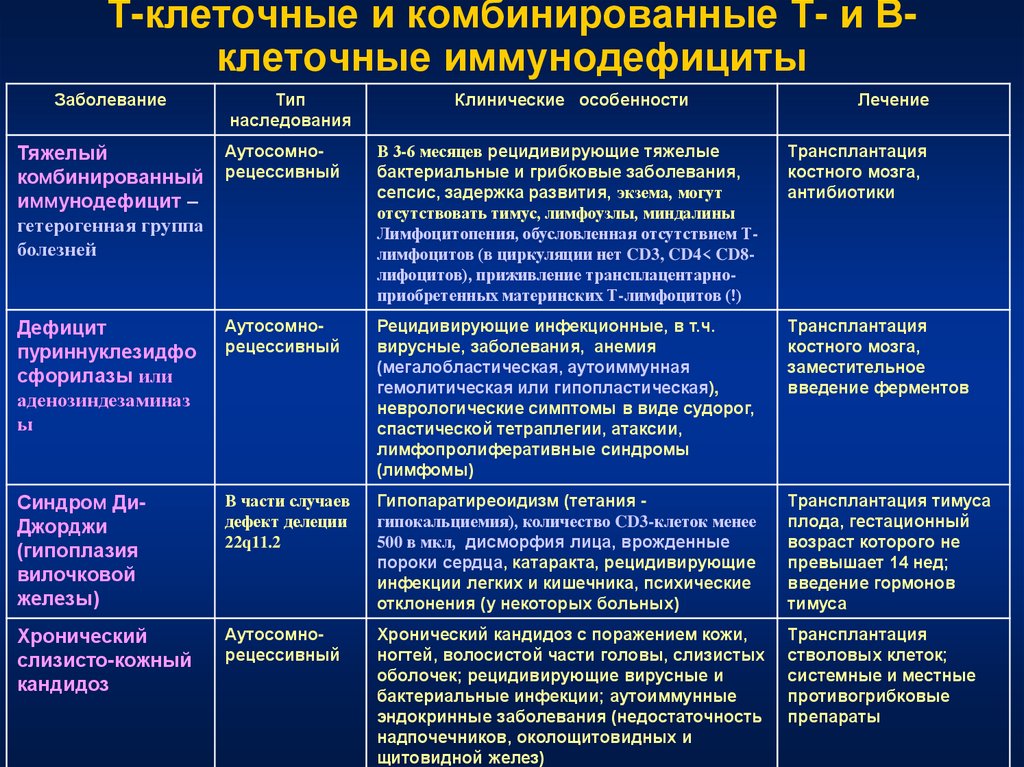



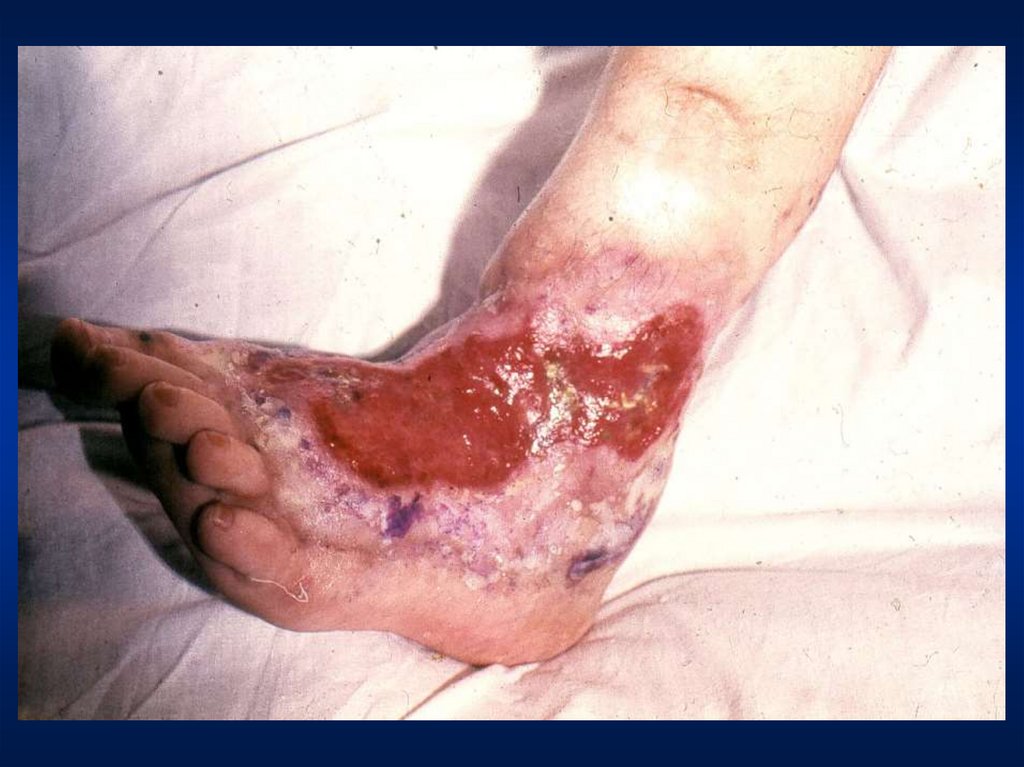
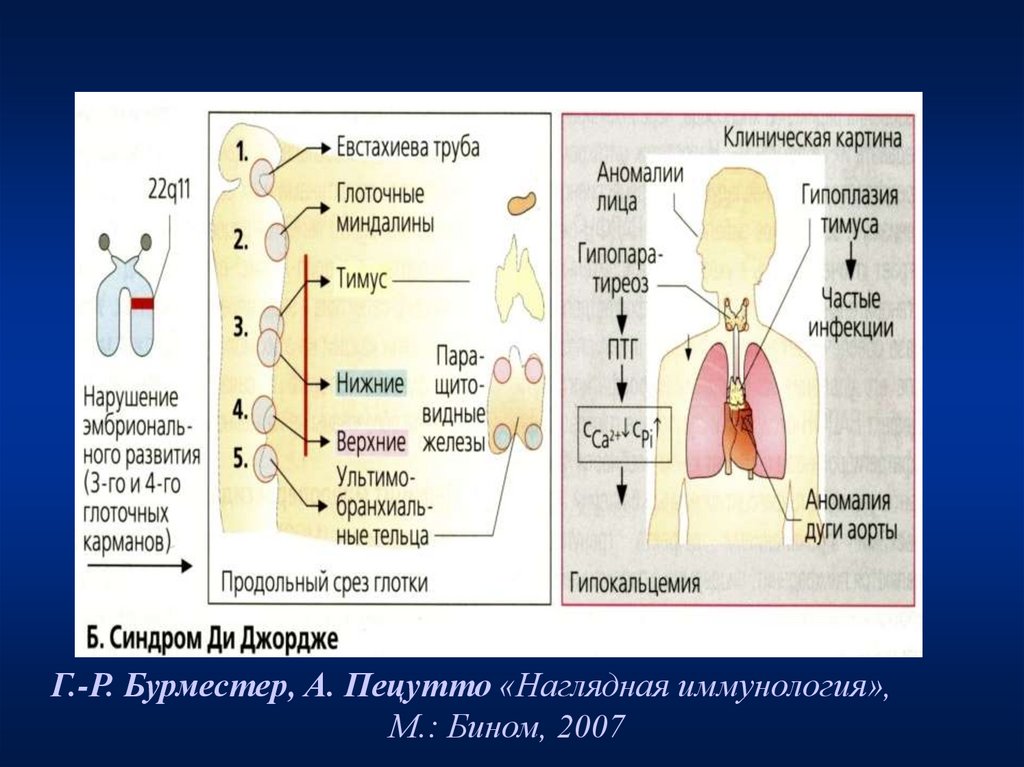



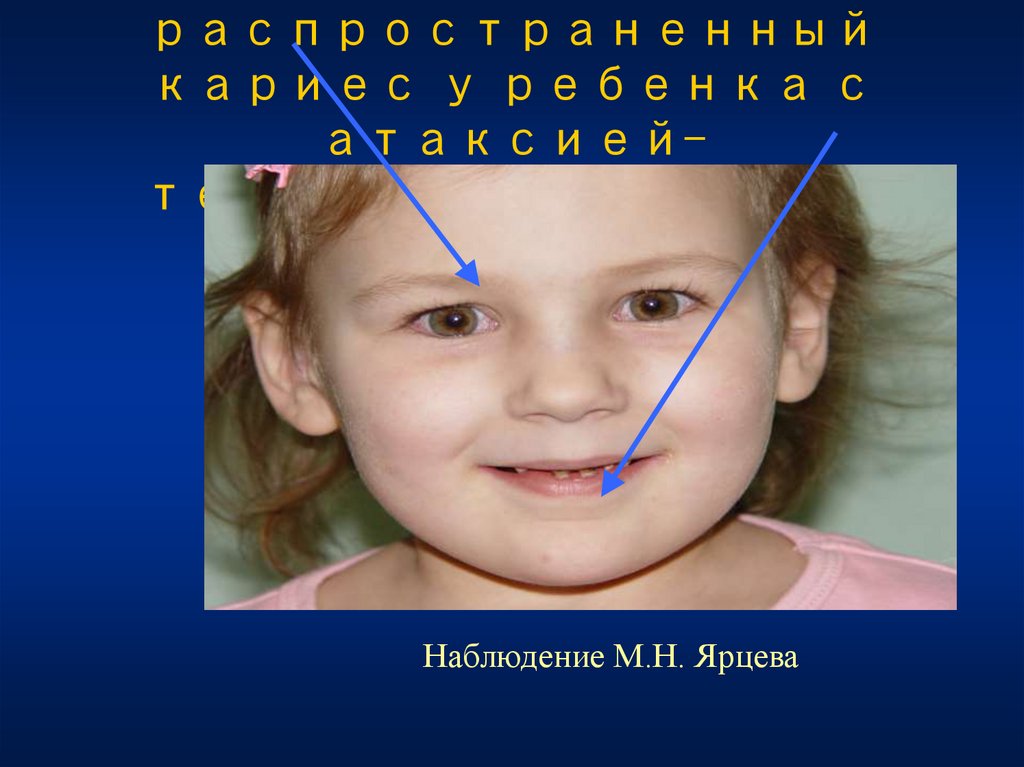
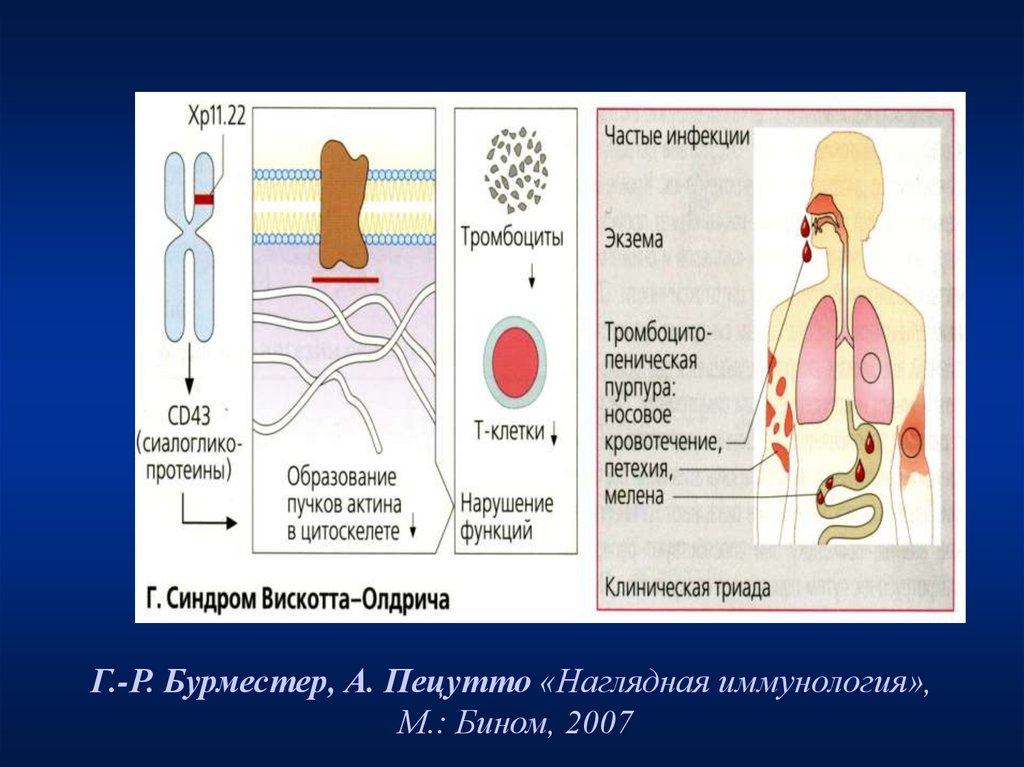



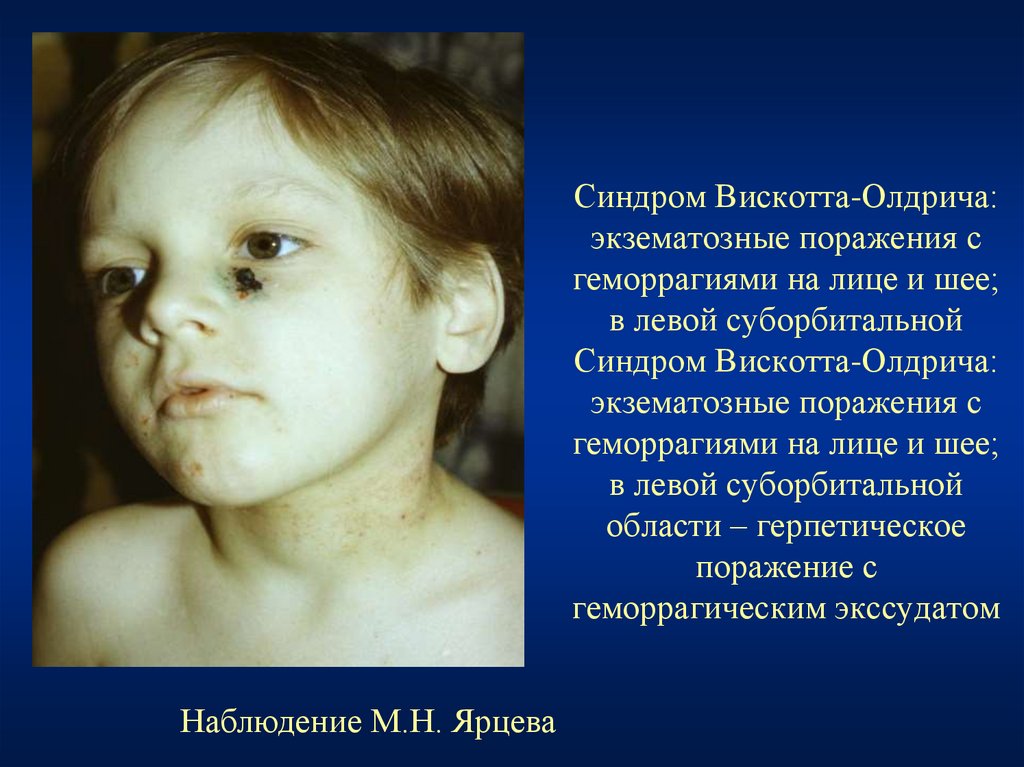
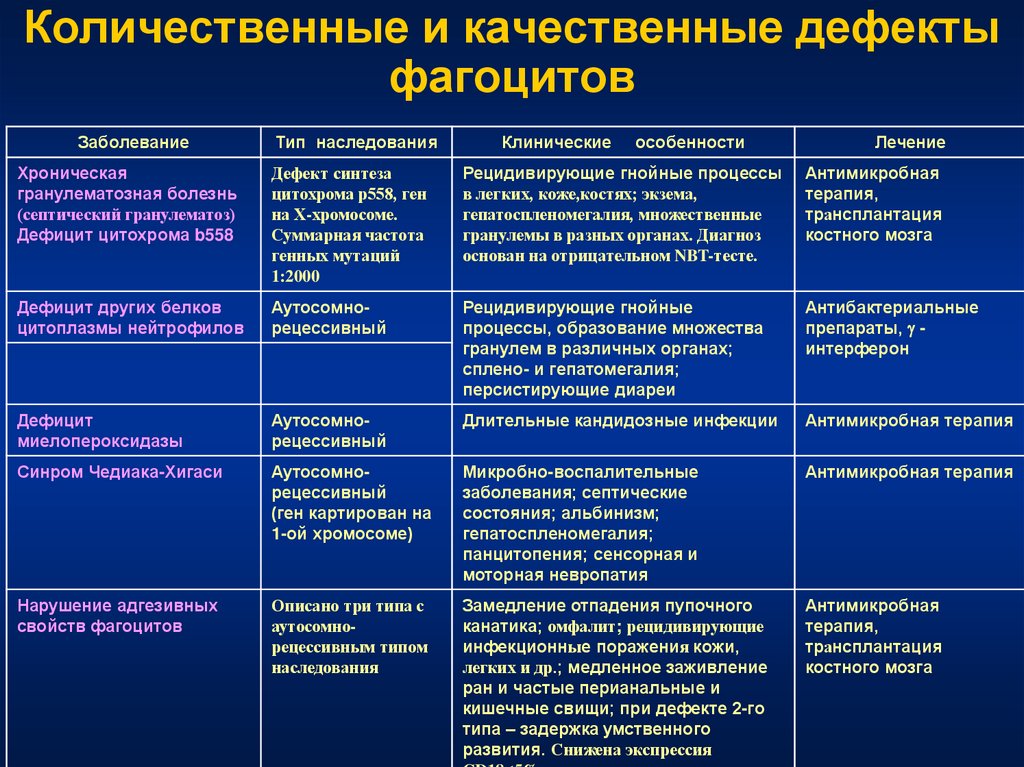


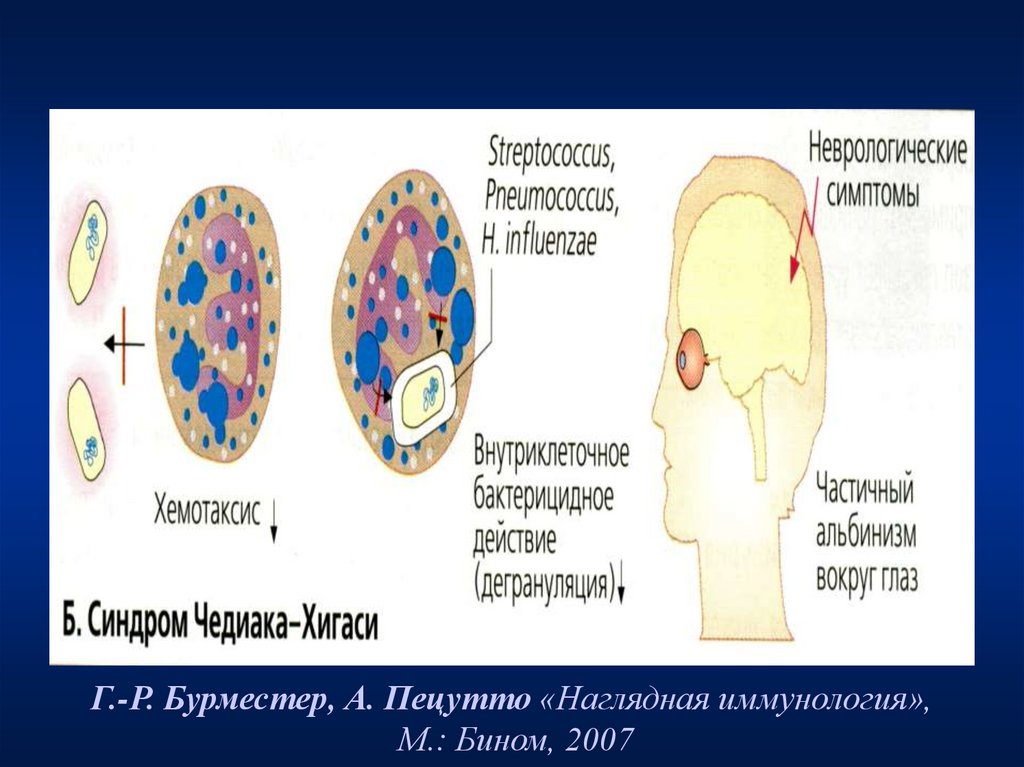







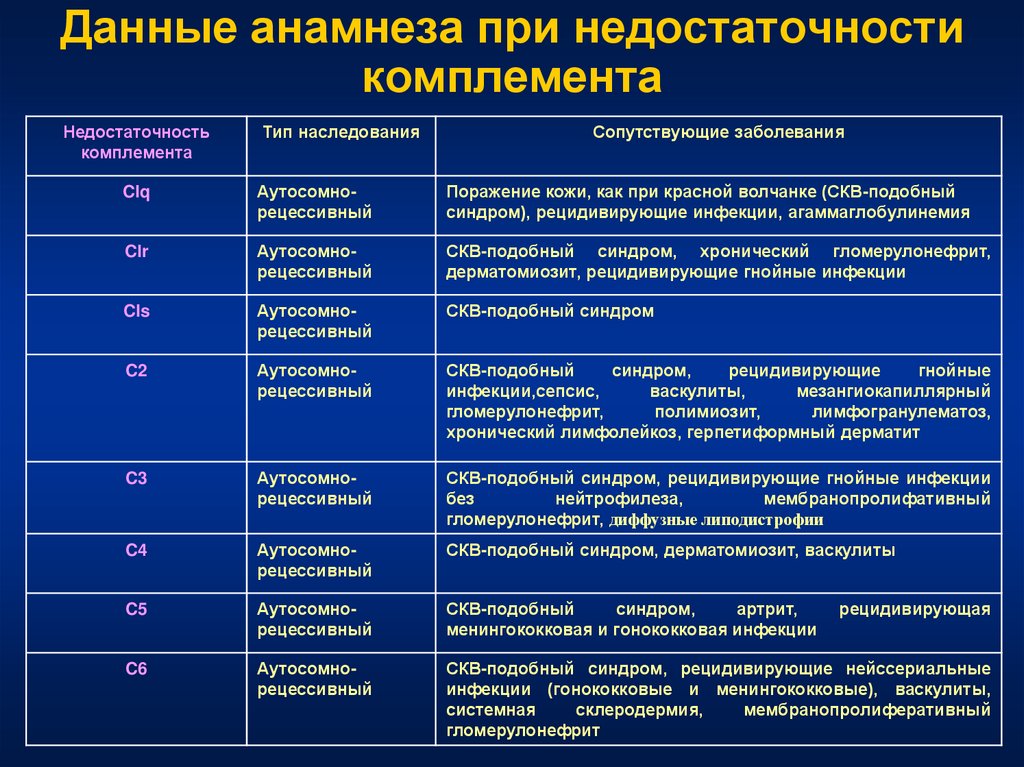
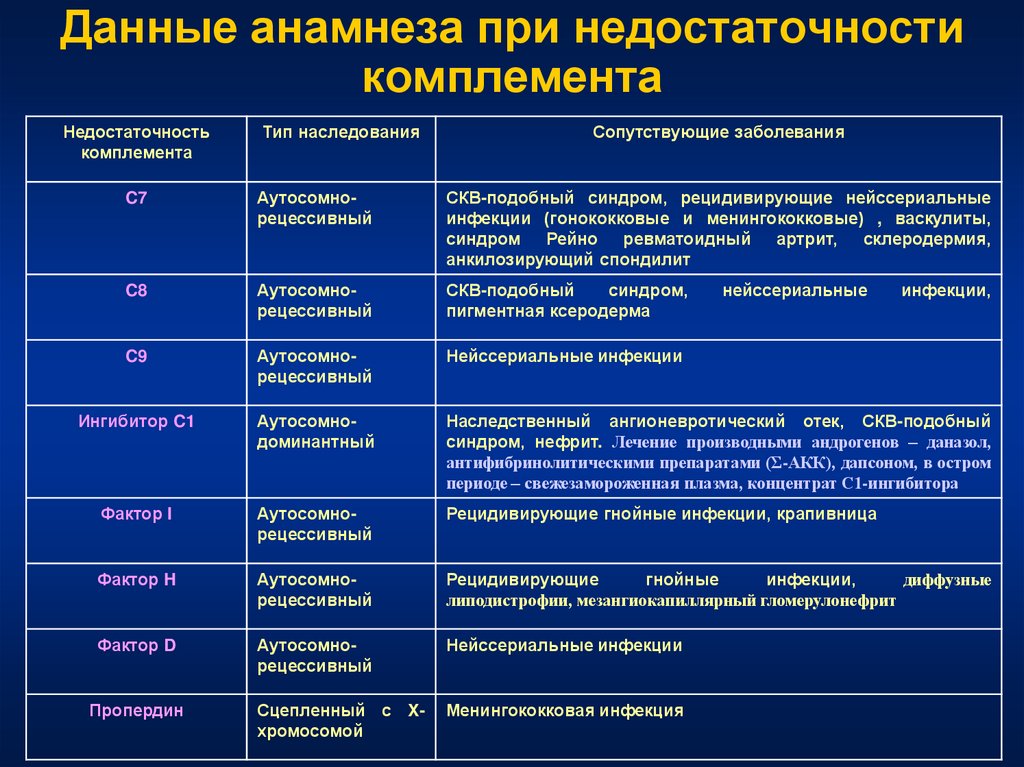








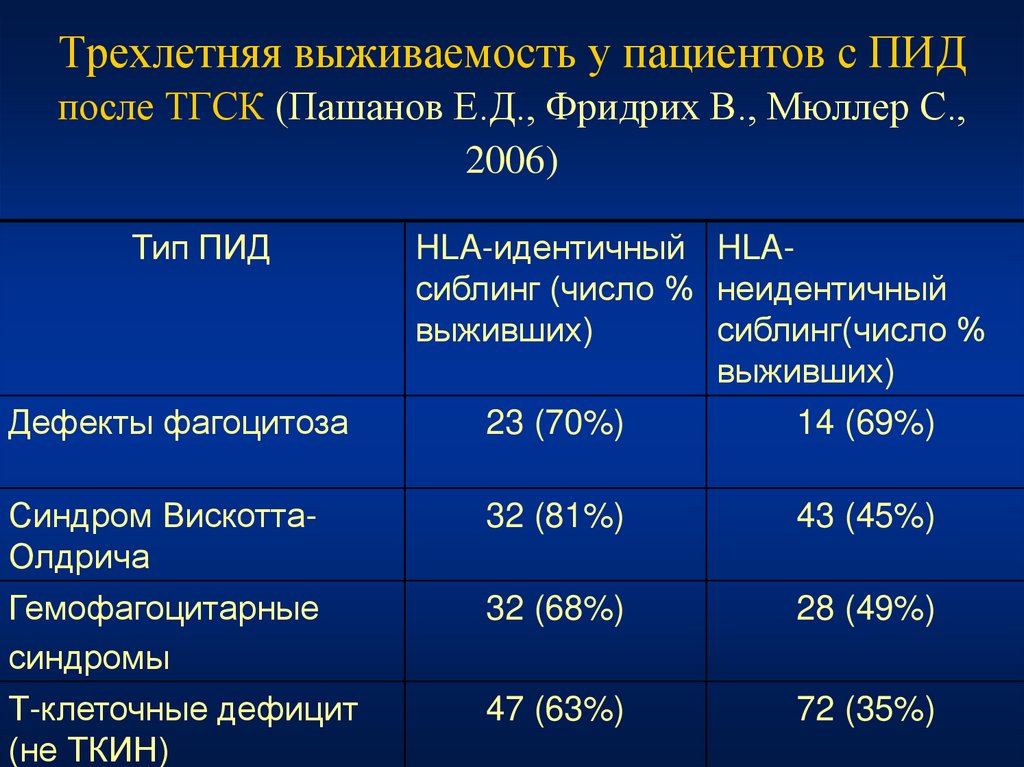






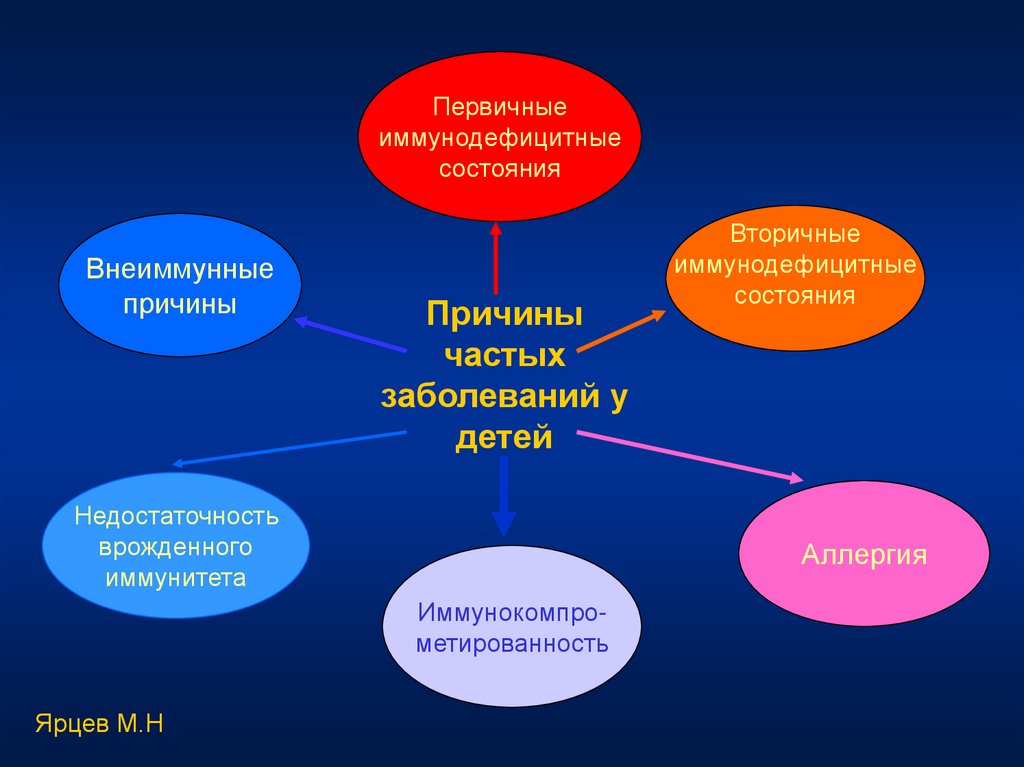

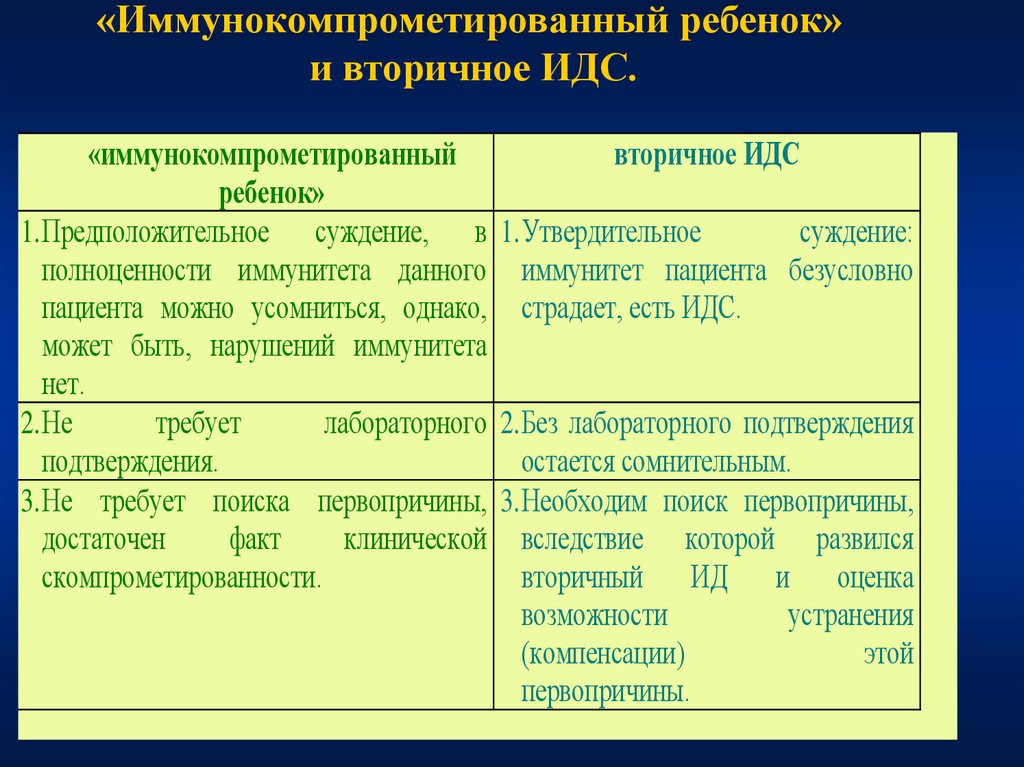


















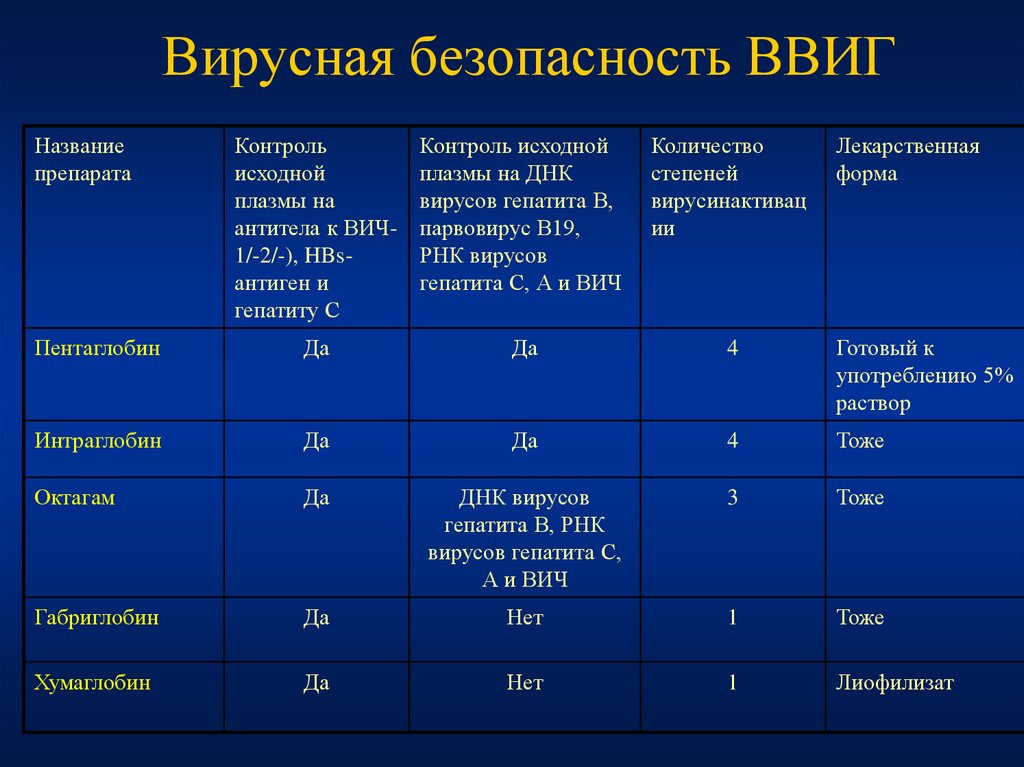

















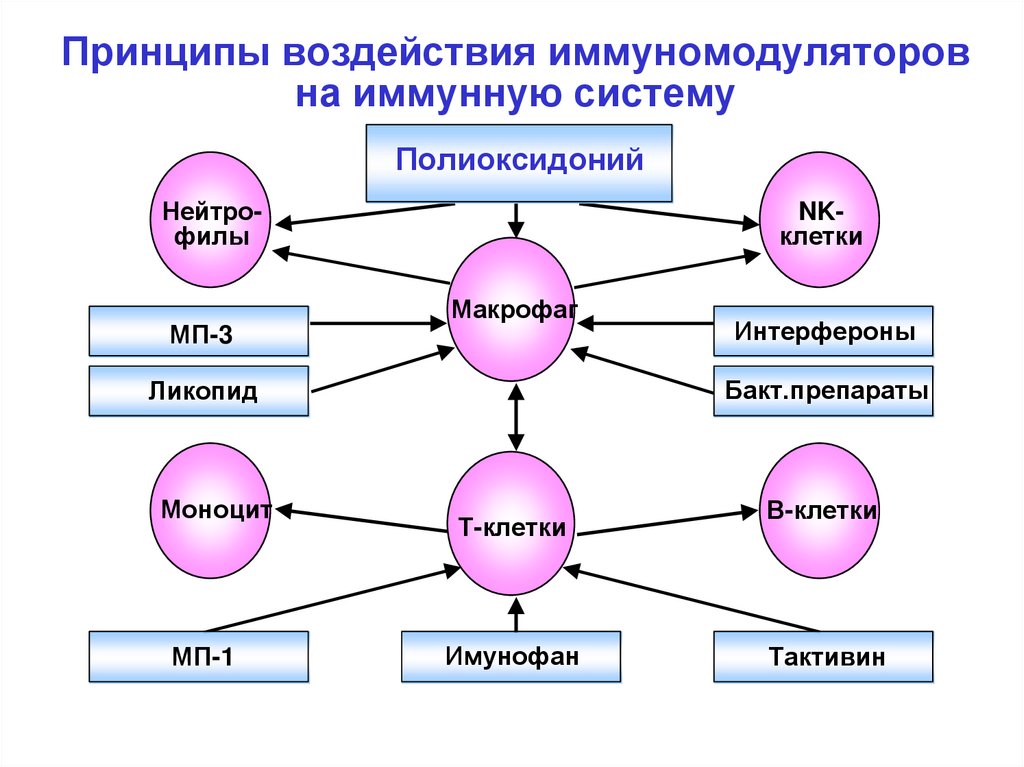
















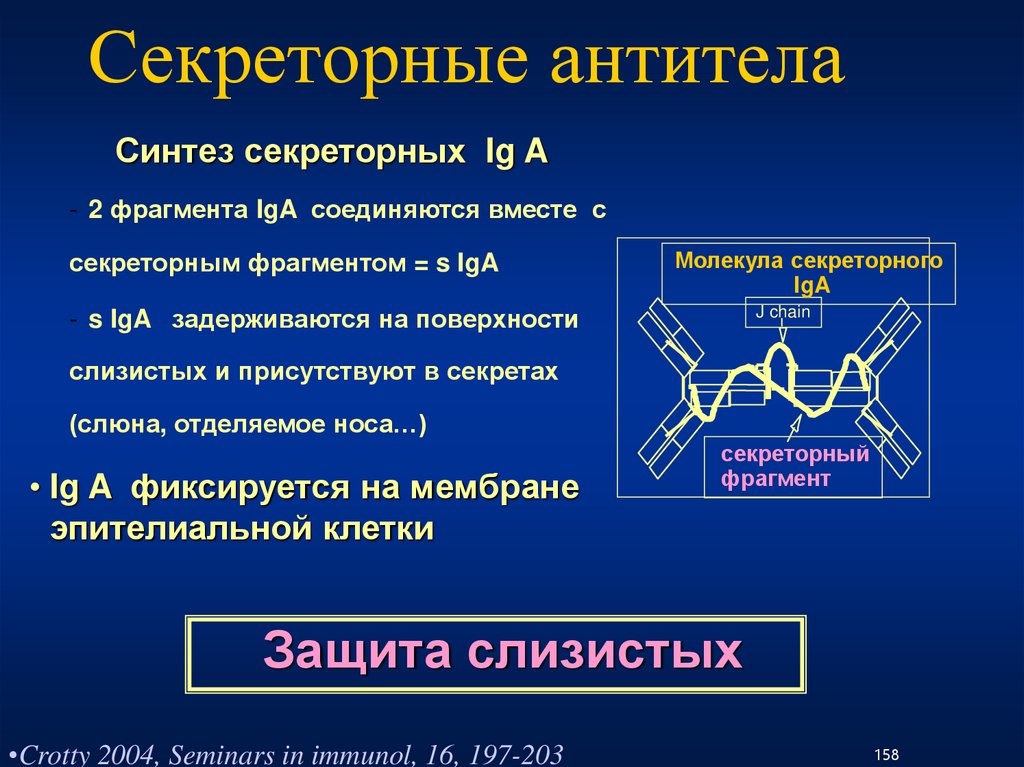



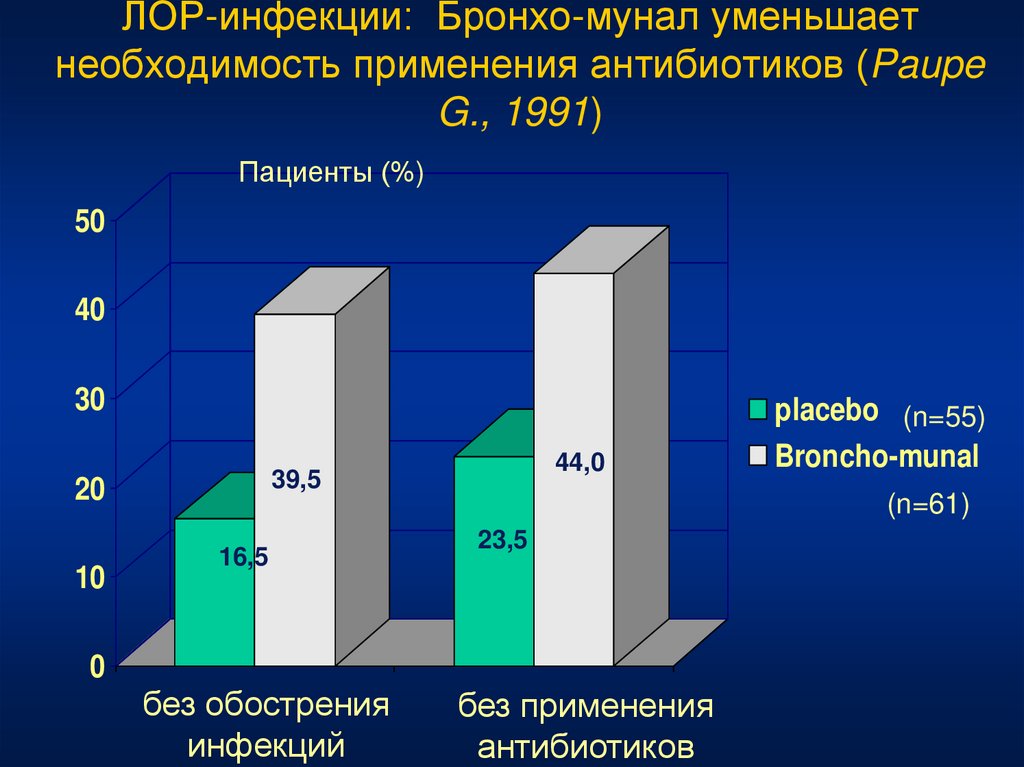
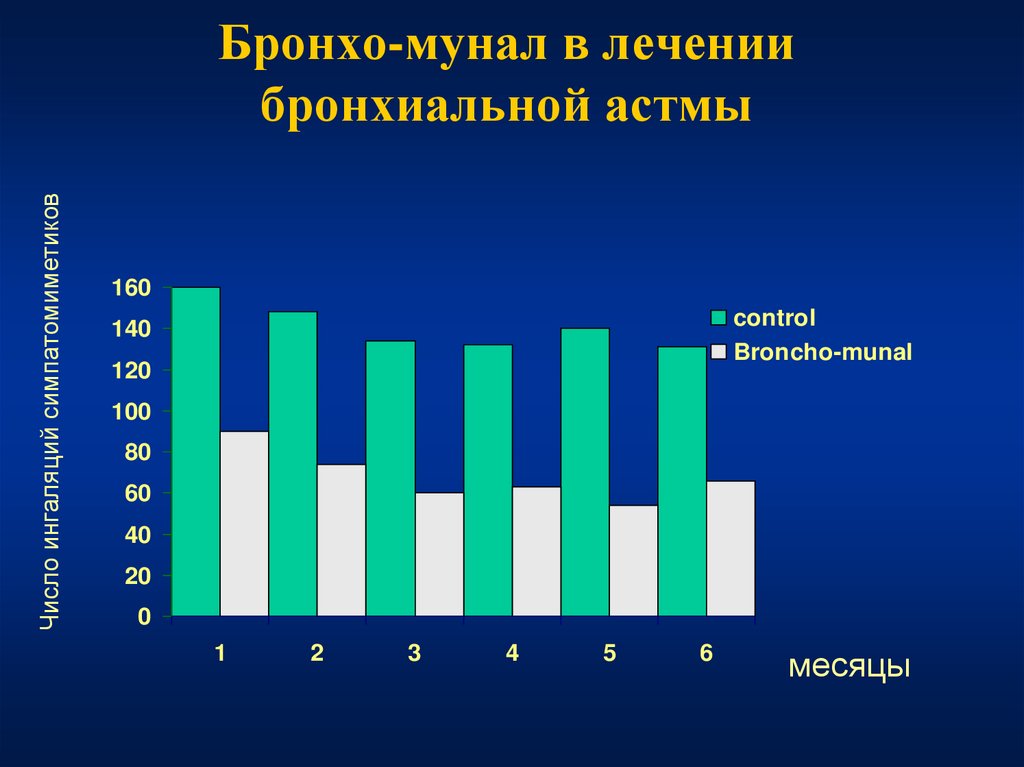






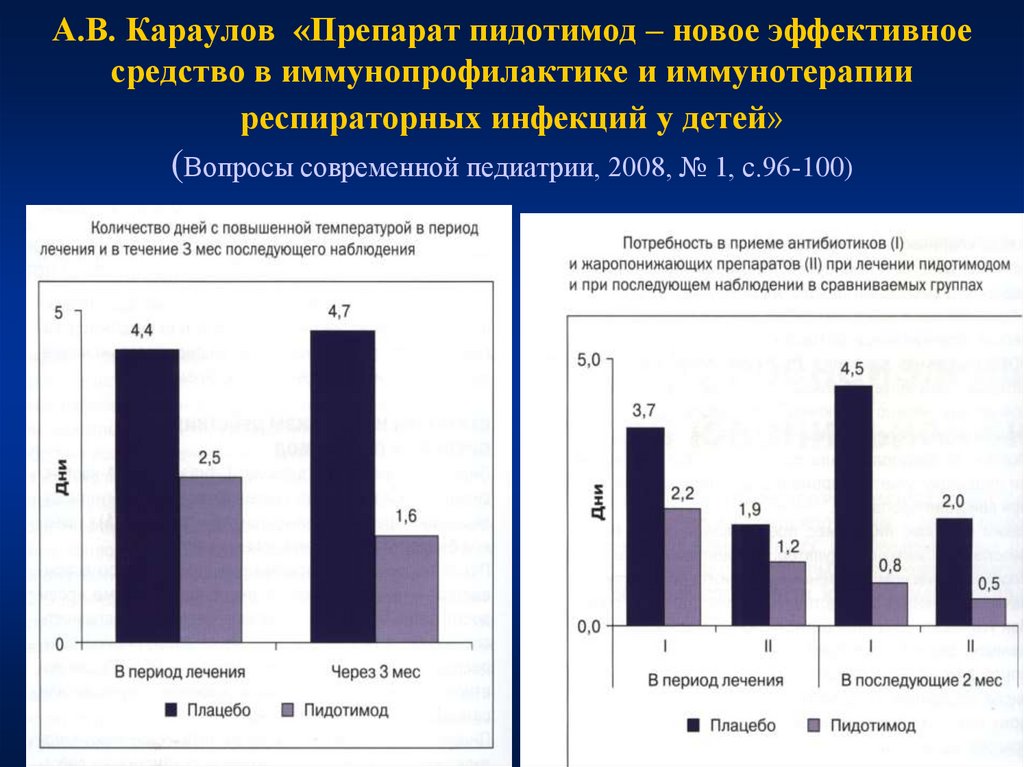





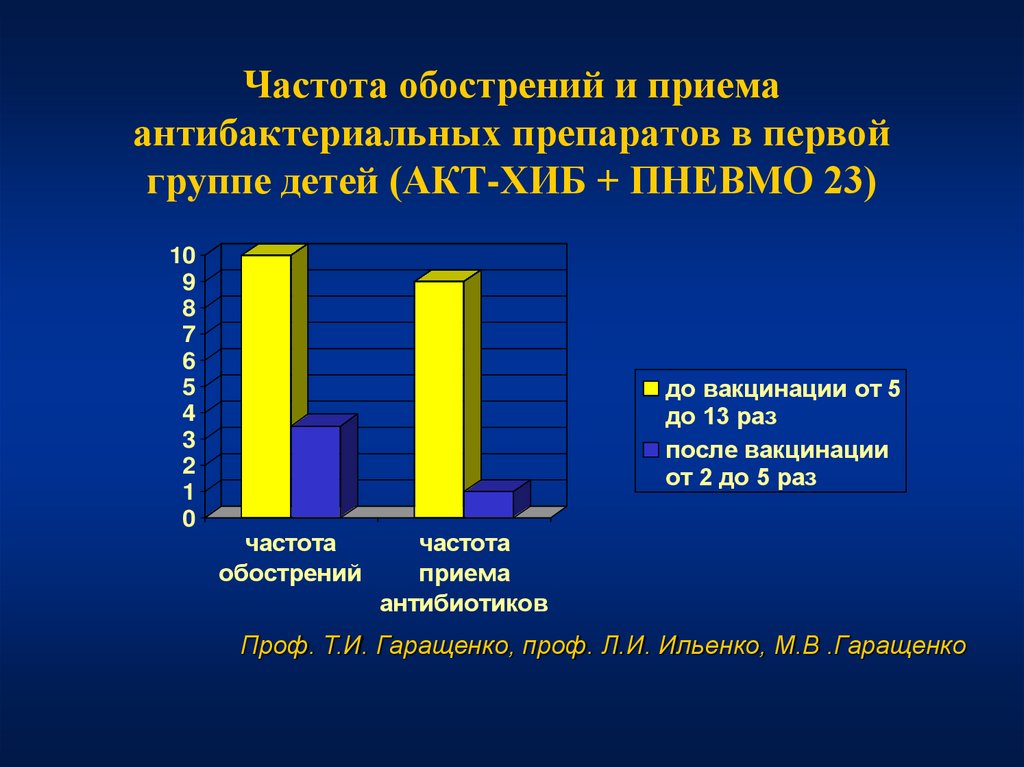



 Медицина
Медицина