Похожие презентации:
Кислоты. Классификация кислот
1. Кислоты
2. Кислоты
• Кислоты - сложные вещества, состоящие из одногоили нескольких атомов водорода, способных
заместиться на атом металла, и кислотного остатка.
• Число атомов водорода определяет основность
кислот.
• Общая формула: Нх(Ас) Ас - кислотный
остаток (от англ. “acid” - кислота).
• Кислоты образуют неметаллы и металлы со
степенью окисления больше, чем +4.
21.06.2022
Кузнецова Екатерина Владимировна
2
3. Классификация по наличию кислорода в кислотном остатке
БескислородныеHCl, HBr, HI, H2S
анион «-ид»
HCl-хлороводородная
(соляная кислота),
Cl- - хлорид
H2S-сероводородная,
S2- - сульфид
21.06.2022
Кислородсодержащие
H2SO4, HNO3, H2CO3,
H3PO4 и другие.
Кузнецова Екатерина Владимировна
3
4. КЛАССИФИКАЦИЯ КИСЛОТ ПО КОЛИЧЕСТВУ АТОМОВ ВОДОРОДА В МОЛЕКУЛЕ
КИСЛОТЫОДНООСНОВНЫЕ
HCl, HNO3
ТРЕХОСНОВНЫЕ
ДВУХОСНОВНЫЕ
H3PO4
H2SO4, H2CO3
21.06.2022
Кузнецова Екатерина Владимировна
4
5. Классификация кислот
СильныеHCl; HBr; HI; H2SO4; HNO3;
HClO4
Слабые
H2S; H2CO3; H2SO3; HCN
Стойкие
H2SO4; H3PO4; HCl
Нестойкие - легко
разлагаются
H2CO3; H2SO3; H2SiO3
Летучие
HCl; HBr; HI; H2S
Нелетучие
H2SO4; H3PO4
21.06.2022
Кузнецова Екатерина Владимировна
5
6. Кислоты отличаются по поведению в ОВР
ОкислителиH2SO4; HNO3 конц.
Окислитель элемент,
образующий
кислоту: S+6; N+5
21.06.2022
Неокислители
Окислитель - ион
водорода H+
Кузнецова Екатерина Владимировна
6
7. Номенклатура
21.06.2022Кузнецова Екатерина Владимировна
7
8. Проверь себя
• 1. Формулы двухосновной и одноосновной кислотсоответственно:
1. HCl и H2CO3
2. HI и H3PO4
3. H2SO4 и HF
4. H2S и H2SO3
2. Формула слабой кислоты:
1. H3PO4,
2. HNO3,
3. HClO4,
4. HCl
21.06.2022
Кузнецова Екатерина Владимировна
8
9. Проверь себя
3. Выберите из списка названия одноосновных кислот:1.
2.
3.
4.
5.
Серная кислота
Соляная кислота
Уксусная кислота
Ортофосфорная кислота
Азотная кислота
21.06.2022
Кузнецова Екатерина Владимировна
9
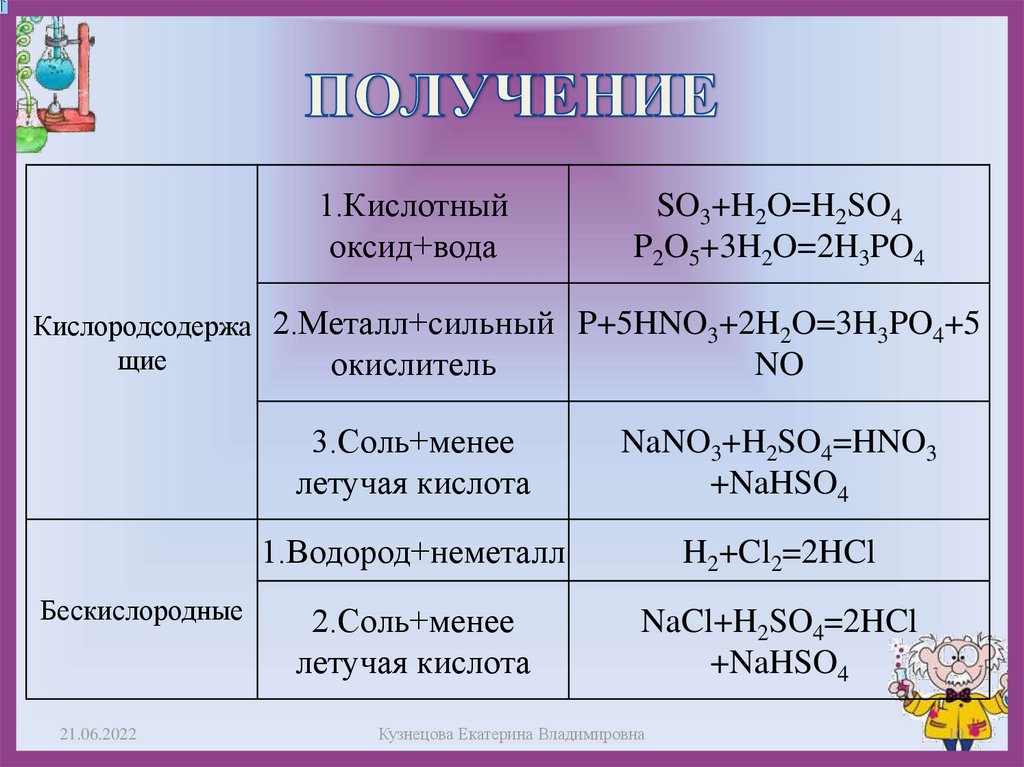
10. ПОЛУЧЕНИЕ
1.Кислотныйоксид+вода
SO3+H2O=H2SO4
P2O5+3H2O=2H3PO4
Кислородсодержа 2.Металл+сильный P+5HNO3+2H2O=3H3PO4+5
щие
окислитель
NO
Бескислородные
21.06.2022
3.Cоль+менее
летучая кислота
NaNO3+H2SO4=HNO3
+NaHSO4
1.Водород+неметалл
H2+Cl2=2HCl
2.Cоль+менее
летучая кислота
NaCl+H2SO4=2HCl
+NaHSO4
Кузнецова Екатерина Владимировна
10
11. Физические свойства кислот
ЖидкостиH2SO4
HClO4 и др.
21.06.2022
Кислоты
Твердые
H3PO4
H2SiO3 и др.
Кузнецова Екатерина Владимировна
Газообразные
HCl
H2S и др.
11
12. Химические свойства
1.Изменяют окраску индикаторов2.Взаимодействие с металлами, стоящими до водорода
H2SO4+Ca=CaSO4+H2
2HCl+Ca=CaCl2+H2
3.Взаимодействие с основными оксидами
H2SO4+CaO=CaSO4+H2O
2HCl+CaO=CaCl2+H2O
4.Взаимодействие с основаниями
H2SO4+Ca(OH)2=CaSO4+2H2O
21.06.2022
2HCl+Ca(OH)2=CaCl2+2H2O
Кузнецова Екатерина Владимировна
12
13. Проверь себя
1.Закончить уравнения реакции:Mg + H2SO4 = …
MgSO4+ H2
Cu + H2CO3 = …
KOH + HCl = …KCl + H2O
Fe(OH)2 + H2SO4 = …FeSO4 + 2H2O
2.Подставьте формулы вместо знака (?) в
схеме реакции:
? + CaO = CaCl2 + H2O
? + MgO = MgSO4 + ?
21.06.2022
Кузнецова Екатерина Владимировна
13
14. Проверь себя
С какими из перечисленных веществ будетвзаимодействовать соляная кислота:
1. CuO
2. Cu
3. Cu(OH)2
4. Al
5. LiOH
6. CO2
21.06.2022
Кузнецова Екатерина Владимировна
14













 Химия
Химия








