Похожие презентации:
Углеводороды нефти. Алканы. Парафины Циклоалканы. Нафтены Ароматические углеводороды. Арены
1. Углеводороды нефти
Алканы. ПарафиныЦиклоалканы. Нафтены
Ароматические углеводороды.
Арены
2. Алканы. Парафины это углеводороды, в молекулах которых имеются только простые (одинарные) связи ациклические или алифатические
–соединения с открытой (незамкнутой)
цепью
Содержание в нефтях в среднем 25-35%
(не считая растворенных газов)
3. Общая формула алканов СnH2n+2
СH4С2H6
С3H8
С4H10
С5H12
С6H14
С7H16
С8H18
С9H20
С10H22
метан
этан
пропан
бутан
пентан
гексан
гептан
октан
нонан
декан
газы
жидкости
4.
C11C12
C15
C16
C20
C21
C22
C30
C40
C50
C99
C100
ундекан
додекан
пентадекан
гексадекан
эйкозан
унэйкозан
докозан
триаконтан
тетаконтан
пентаконтан
нонаннонаконтан
гектан
жидкости
твердые
вещества
5.
Газообразныепарафиновые
углеводороды, входящие в состав
природных углеводородных газов, в
зависимости от условий нахождения
в природе делятся на три типа:
- природные газы;
- газы
газоконденсатных
месторождений;
- попутные газы.
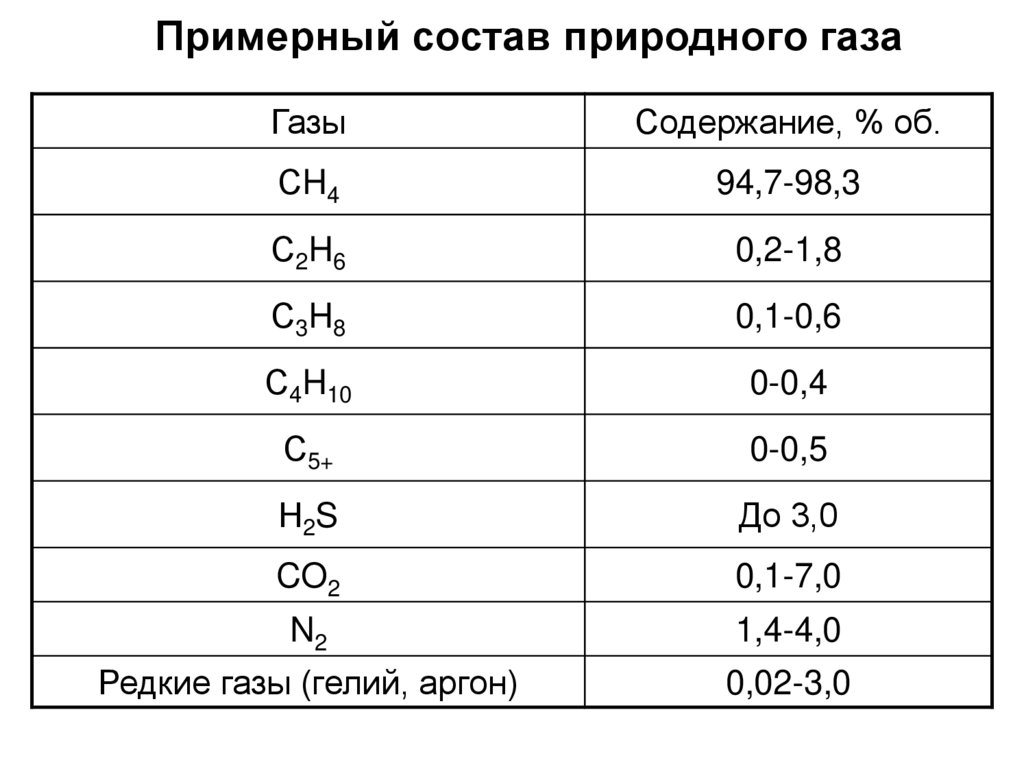
6. Примерный состав природного газа
ГазыСодержание, % об.
СH4
94,7-98,3
С2H6
0,2-1,8
С3H8
0,1-0,6
С4H10
0-0,4
С5+
0-0,5
Н2S
До 3,0
CO2
0,1-7,0
N2
1,4-4,0
Редкие газы (гелий, аргон)
0,02-3,0
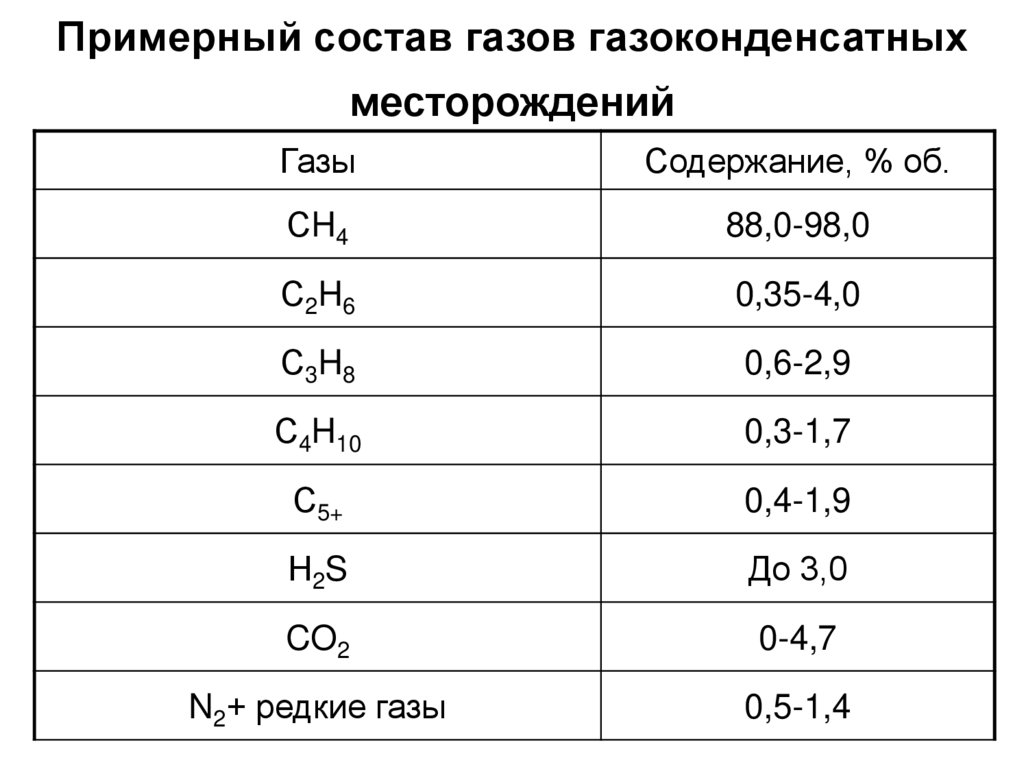
7. Примерный состав газов газоконденсатных месторождений
ГазыСодержание, % об.
СH4
88,0-98,0
С2H6
0,35-4,0
С3H8
0,6-2,9
С4H10
0,3-1,7
С5+
0,4-1,9
Н2S
До 3,0
CO2
0-4,7
N2+ редкие газы
0,5-1,4
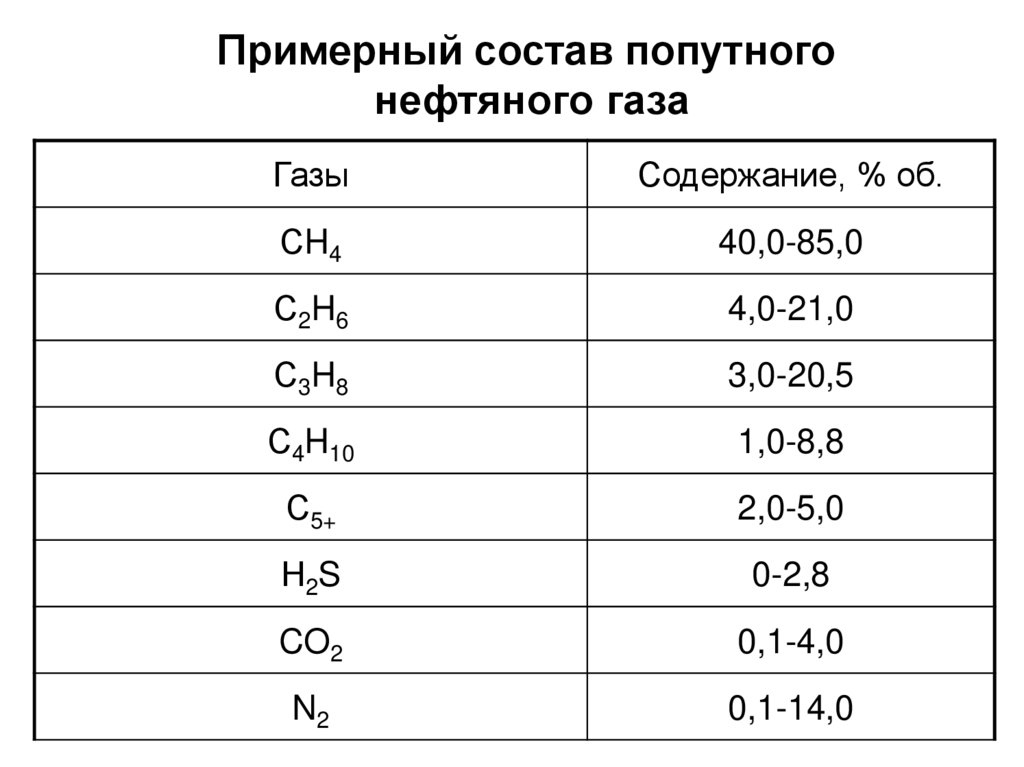
8. Примерный состав попутного нефтяного газа
ГазыСодержание, % об.
СH4
40,0-85,0
С2H6
4,0-21,0
С3H8
3,0-20,5
С4H10
1,0-8,8
С5+
2,0-5,0
Н2S
0-2,8
CO2
0,1-4,0
N2
0,1-14,0
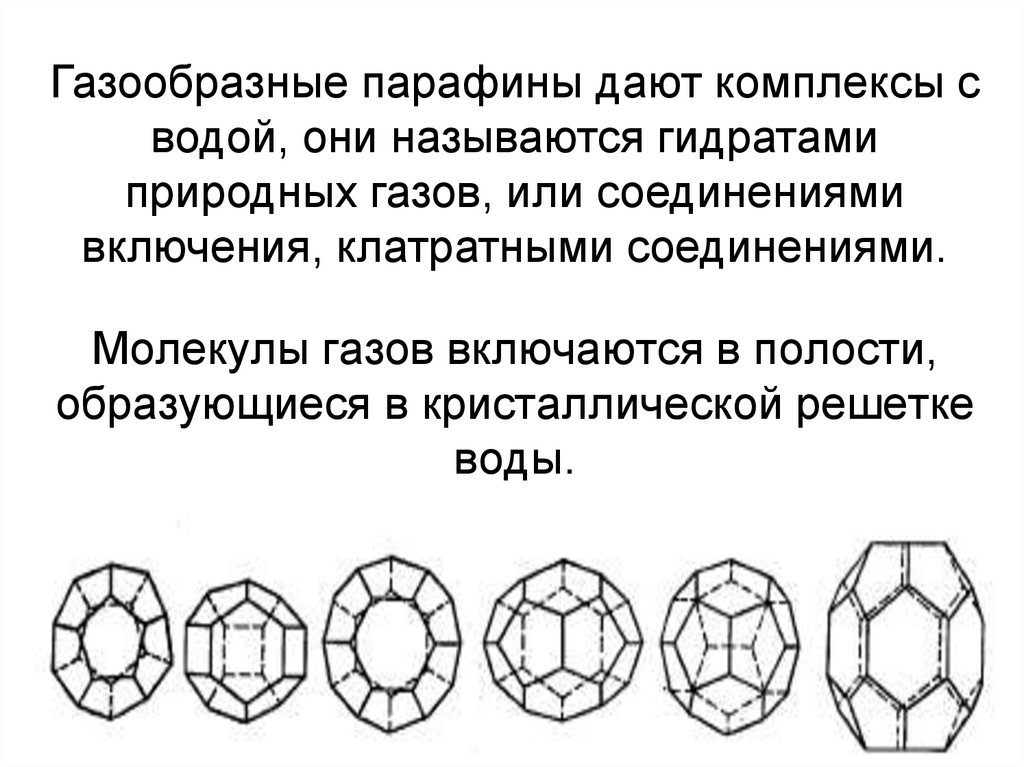
9. Газообразные парафины дают комплексы с водой, они называются гидратами природных газов, или соединениями включения, клатратными
соединениями.Молекулы газов включаются в полости,
образующиеся в кристаллической решетке
воды.
10. Систематическая номенклатура алканов (ИЮПАК; JUPAC; Международный союз теоретической и прикладной химии)
1.Выбирают самую длинную
углеродную цепь
(при одинаковой длине выбирают
наиболее разветвленную)
11.
CH3|
H3C – CH2 – C – CH – CH3
| |
CH3CH3
12.
CH3|
H3C –C– CH2 – CH2 – CH2 – CH3
|
CH2
|
CH3
13. 2. Нумеруют атомы углерода в цепи, с того конца, к которому ближе расположен радикал (одновалентный остаток, получаемый
удалением атома водорода от какоголибо атома углерода).14. Формулы и названия радикалов
ФормулаНазвание
CH3 -
Метил
H3C –CН2-
Этил
H3C –CН2- CН2-
Пропил
H3C –CН- CН3
I
Изопропил
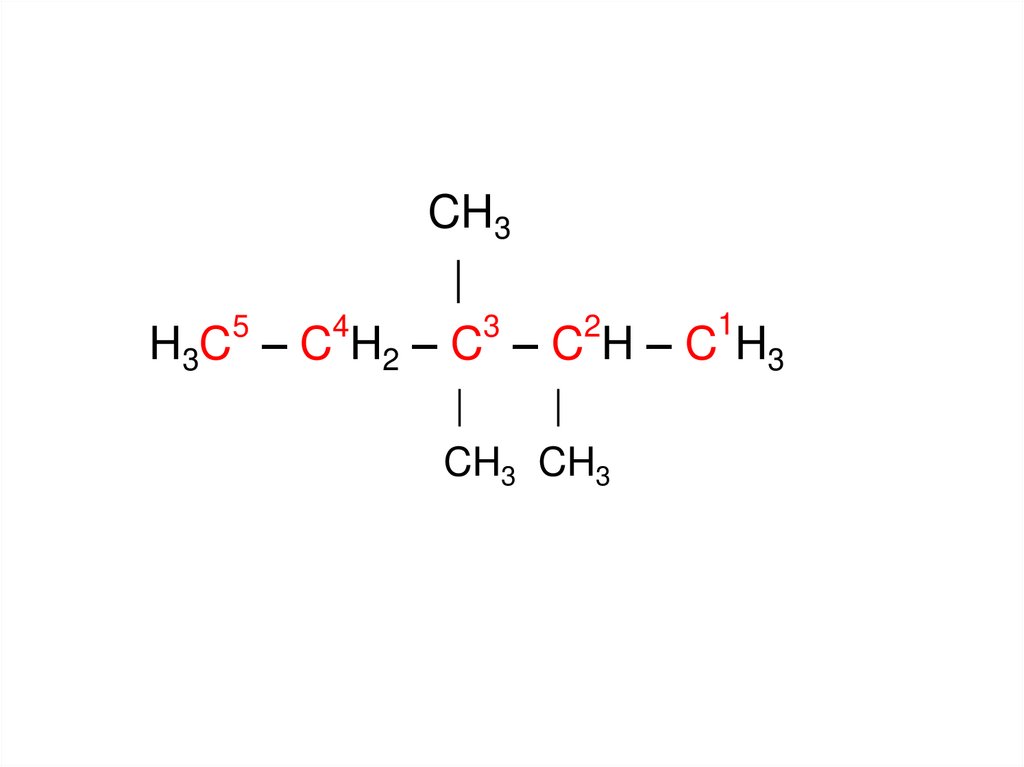
15.
CH3|
1
5
4
3
2
H3C – C H2 – C – C H – C H3
|
|
CH3 CH3
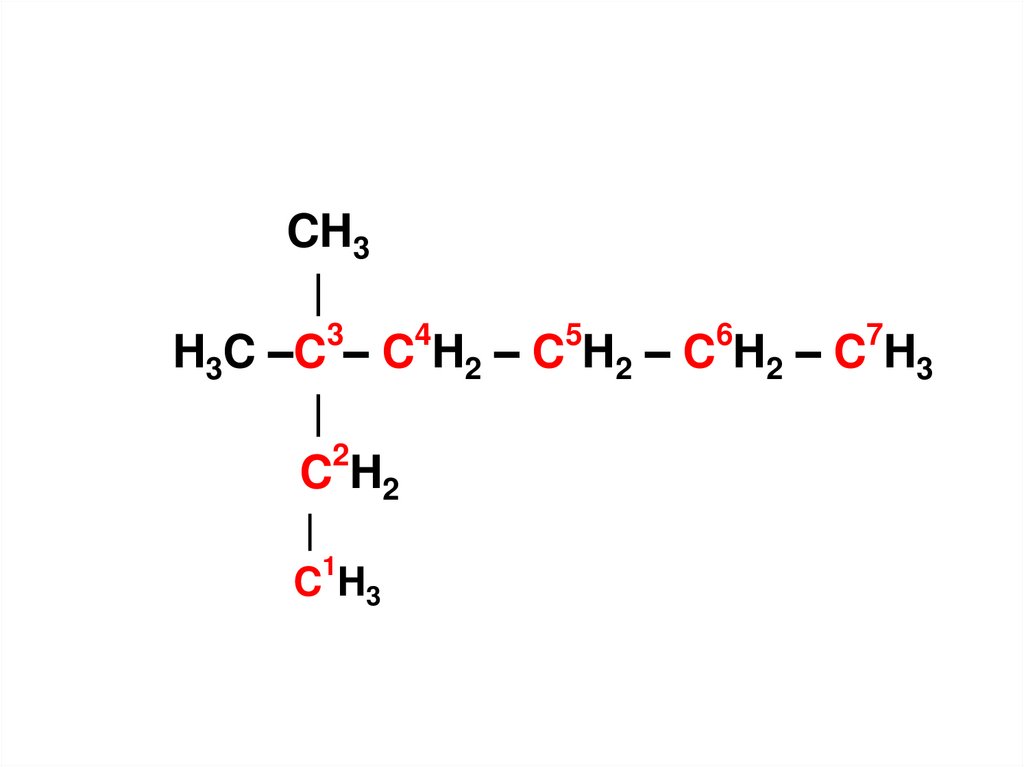
16.
CH3|
3
4
5
6
7
H3C –C – C H2 – C H2 – C H2 – C H3
|
2
C H2
|
1
C H3
17. 3. Перечисляют все радикалы (в порядке возрастания сложности) перед каждым радикалом ставится цифра указывающая номер углерода
укоторого он расположен, при наличии
нескольких одинаковых радикалов их
число обозначают греческими
числительными (ди-, три-, тетра- и т.д.).
18.
CH3|
1
5
4
3
2
H 3C – C H 2 – C – C H – C H 3
|
CH3
|
CH3
2,3,3-триметил-
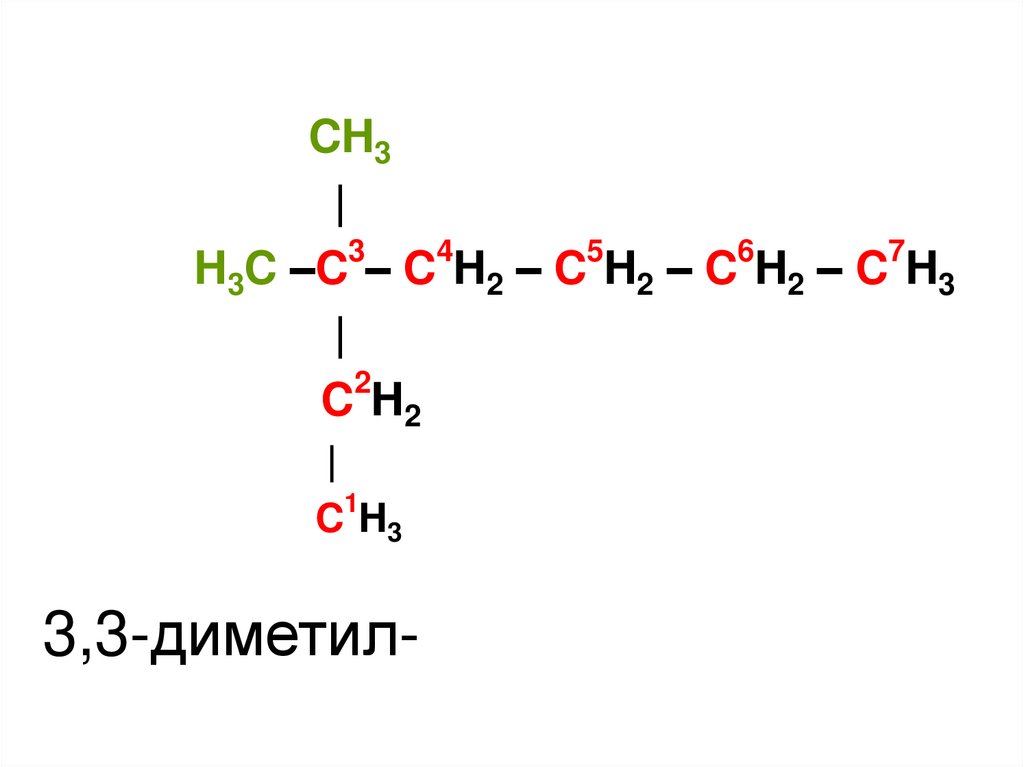
19.
CH3|
3
4
5
6
7
H3C –C – C H2 – C H2 – C H2 – C H3
|
2
C H2
|
1
C H3
3,3-диметил-
20. 4. Дают название пронумерованной цепи, которое соответствует названию нормального алкана, состоящего из такого же числа атомов
углерода21.
CH3|
1
5
4
3
2
H 3C – C H 2 – C – C H – C H 3
|
CH3
|
CH3
2,3,3-триметил-пентан
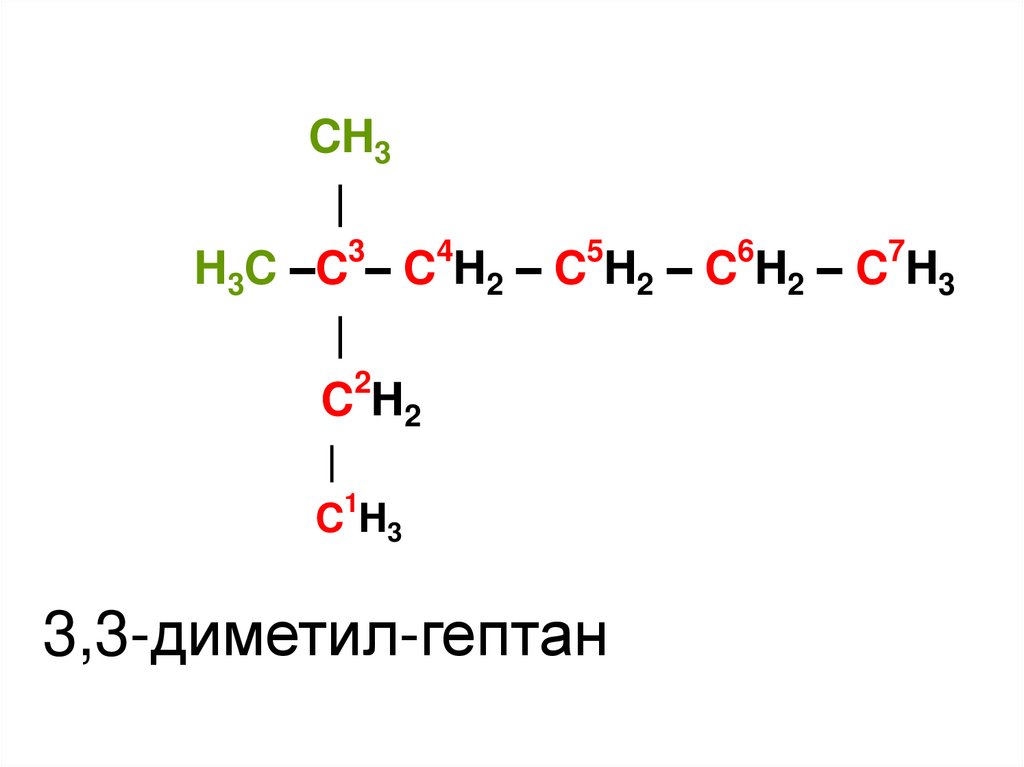
22.
CH3|
3
4
5
6
7
H3C –C – C H2 – C H2 – C H2 – C H3
|
2
C H2
|
1
C H3
3,3-диметил-гептан
23. Физические свойства алканов
Пентан (С5)Гексан (С6)
Гептан (С7)
tкипения
36,08
68,8
98,42
tплавления
-129,7
-94,0
-90,58
плотность
0,6264
0,6594
0,6837
Среди алканов нормального строения с ростом
числа атомов углерода в молекуле растут:
- температура кипения
- температура плавления
- плотность
24. Физические свойства алканов
Пентан (С5)2-метилбутан
(С5)
2,2-диметилпропан
(С5)
tкипения
36,08
27,95
tплавления
-129,7
-159,6
плотность
0,6264
0,6199
9,45
-166,3
0,6130
Среди алканов одинакового состава,
строения минимальными показателями:
температура кипения
температура плавления
плотность
обладают наиболее разветвленные из них
но
разного
25. Циклоалканы. Нафтены циклические насыщенные углеводороды, по химическим свойствам близки к предельным углеводородам
Алициклические (алифатическиециклические) - соединения с замкнутой
цепью
Содержание в нефтях в среднем 2580%
26.
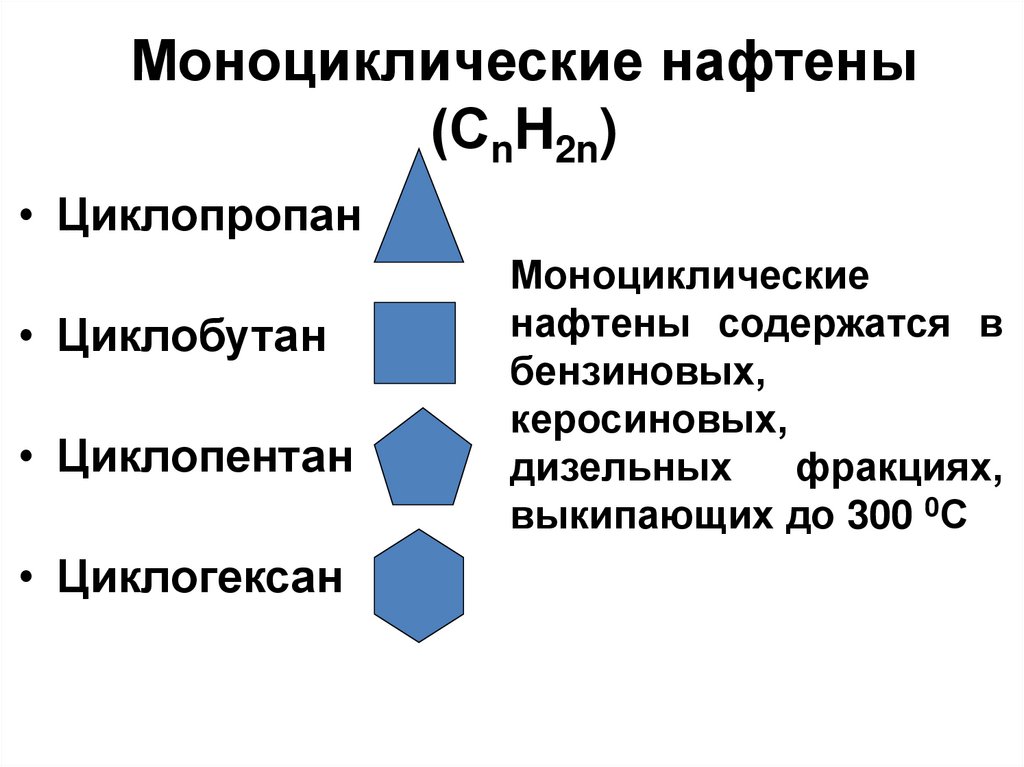
Моноциклические нафтены(СnH2n)
• Циклопропан
• Циклобутан
• Циклопентан
• Циклогексан
Моноциклические
нафтены содержатся в
бензиновых,
керосиновых,
дизельных
фракциях,
выкипающих до 300 0С
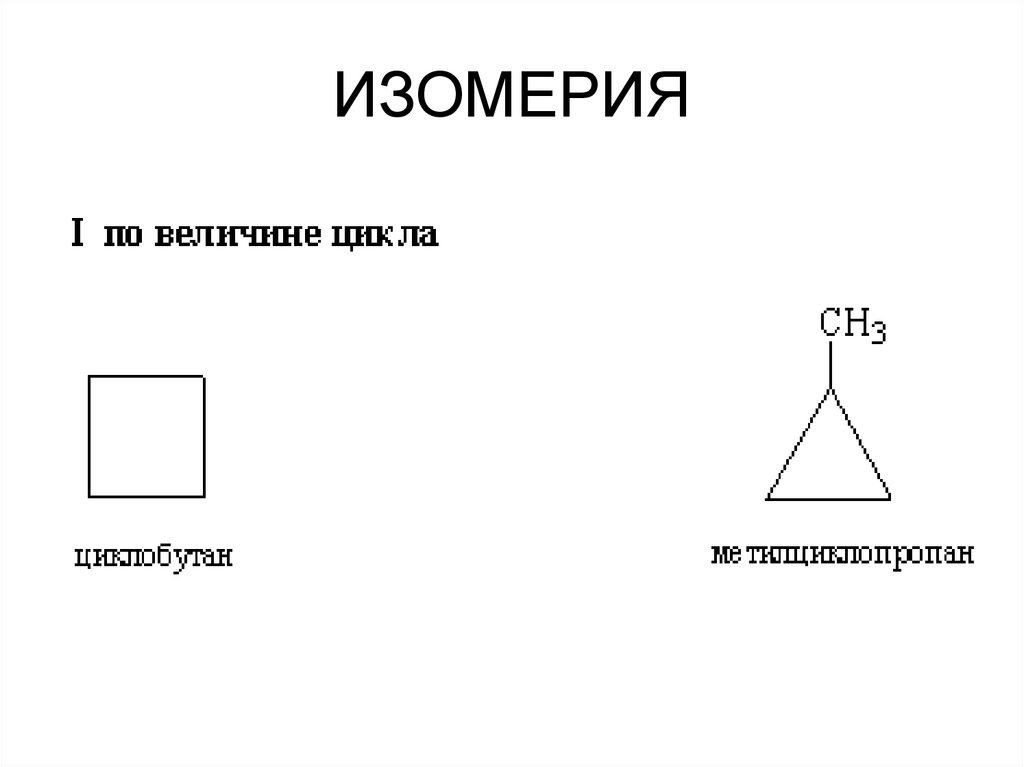
27. ИЗОМЕРИЯ
28.
29.
30.
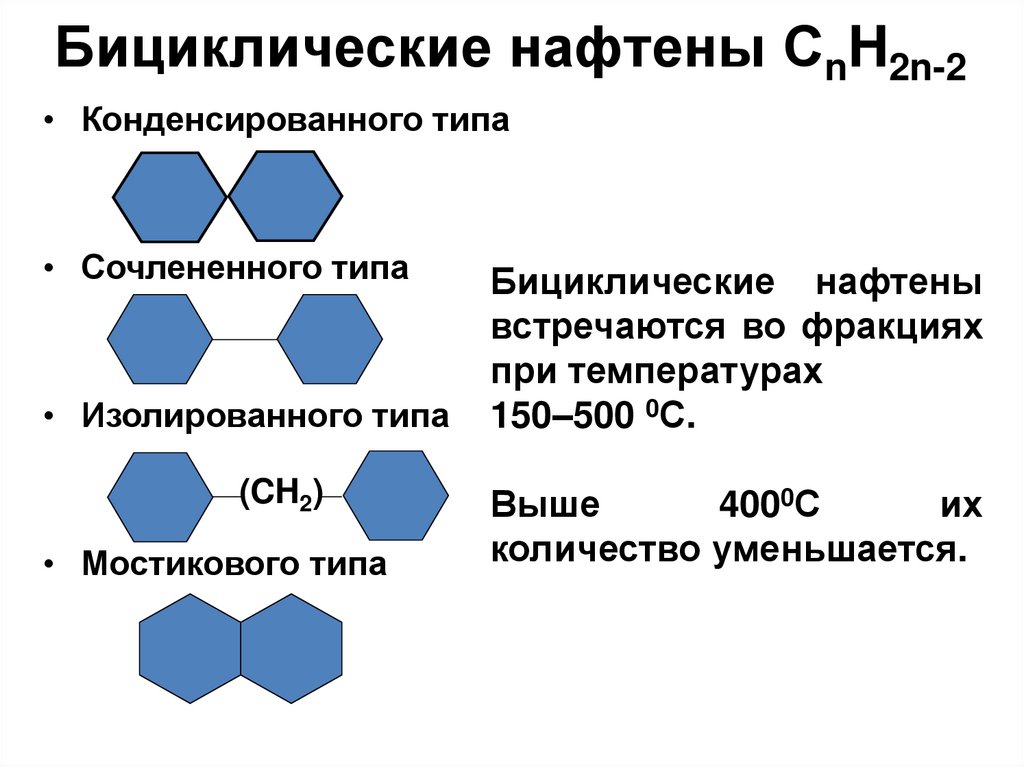
31. Бициклические нафтены СnH2n-2
• Конденсированного типа• Сочлененного типа
• Изолированного типа
(CH2)
• Мостикового типа
Бициклические нафтены
встречаются во фракциях
при температурах
150–500 0С.
Выше
4000С
их
количество уменьшается.
32.
Номенклатура бициклических нафтеновКонденсированного
типа
(спирановые
соединения):
1 Название начинается с приставки «спиро-»
2 В квадратных скобках указывается
количество атомов углерода:
а) сначала меньшего цикла
б) после точки – большего цикла
в) узловой атом в скобках не
указывается.
3
Полная
нумерация
начинается
с
ближайшего к узловому атома углерода в меньшем
цикле и продолжается по периметру молекулы.
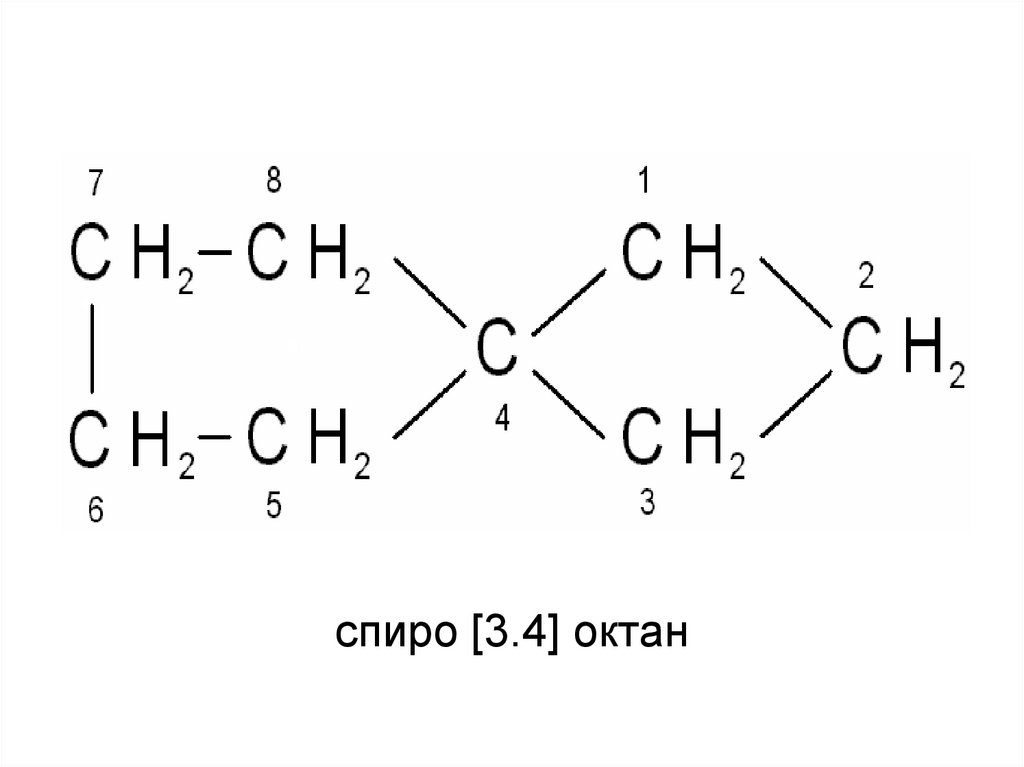
33. Спиро
спиро [3.4] октан34.
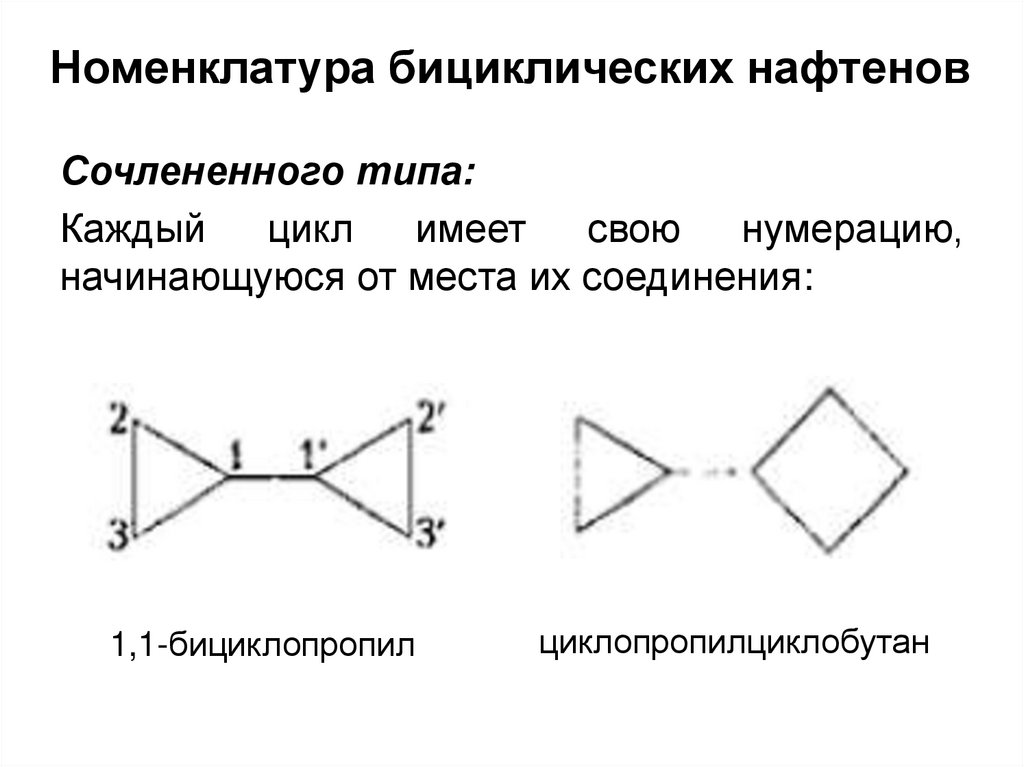
Номенклатура бициклических нафтеновСочлененного типа:
Каждый
цикл
имеет
свою
нумерацию,
начинающуюся от места их соединения:
1,1-бициклопропил
циклопропилциклобутан
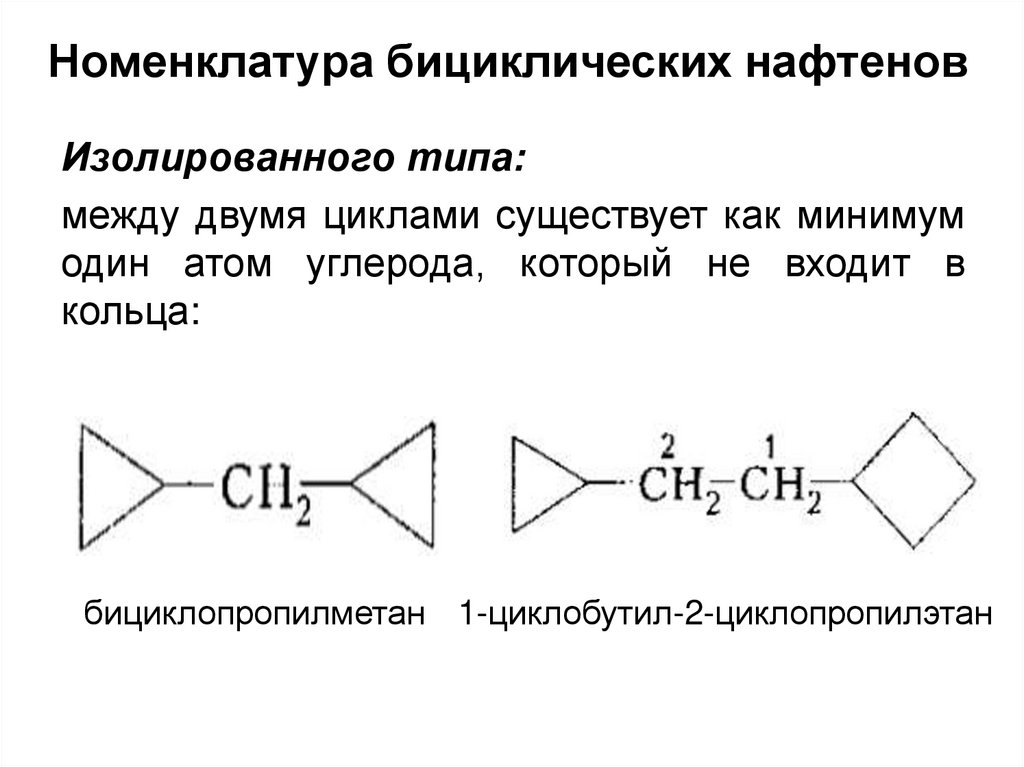
35. Номенклатура бициклических нафтенов
Изолированного типа:между двумя циклами существует как минимум
один атом углерода, который не входит в
кольца:
бициклопропилметан 1-циклобутил-2-циклопропилэтан
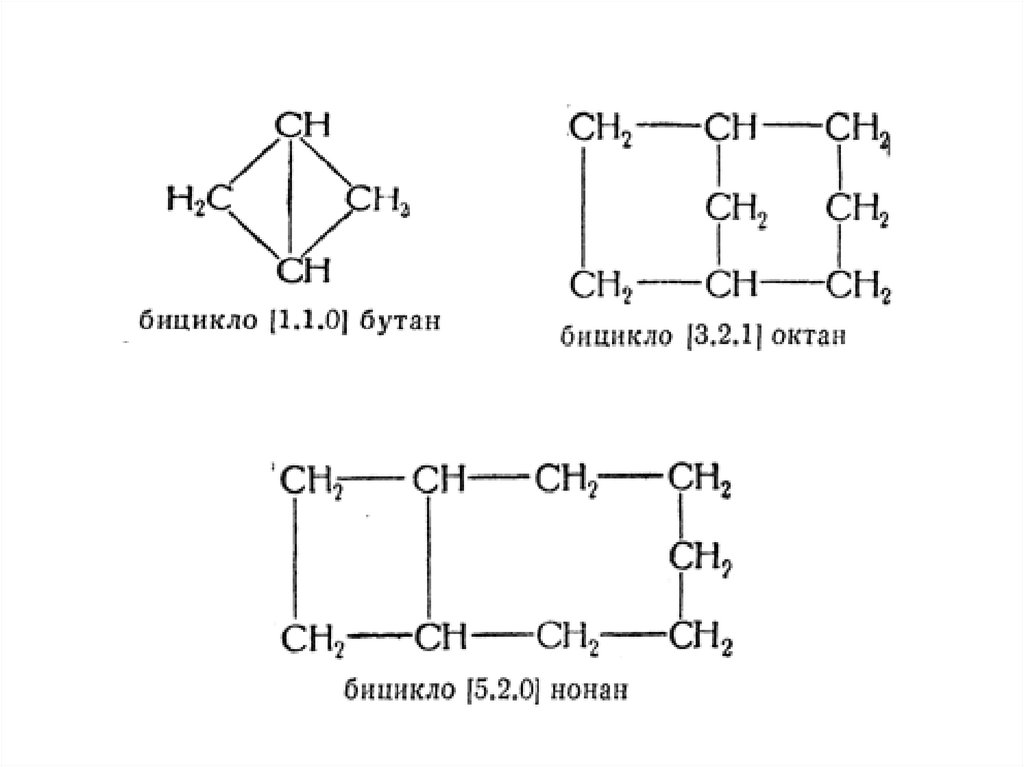
36. Номенклатура бициклических нафтенов
Мостикового типа:Содержат два узловых атома углерода.
1 Название начинается с префикса «бицикло-».
2 Далее в квадратных скобках обозначают цифрами
количество атомов углерода каждого цикла между
узловыми атомами в порядке уменьшения (узловые атомы
не учитываются).
3 За скобкой располагают название углеводорода с
учетом всех атомов углерода. Если мостик между узловыми
атомами не содержит атомов углерода, то в скобках пишут
0 (ноль).
4 Нумерация начинается с большего цикла и
проходит от одного узлового атома углерода к другому
длинным путем.
5 Последними нумеруют узловые атомы.
37.
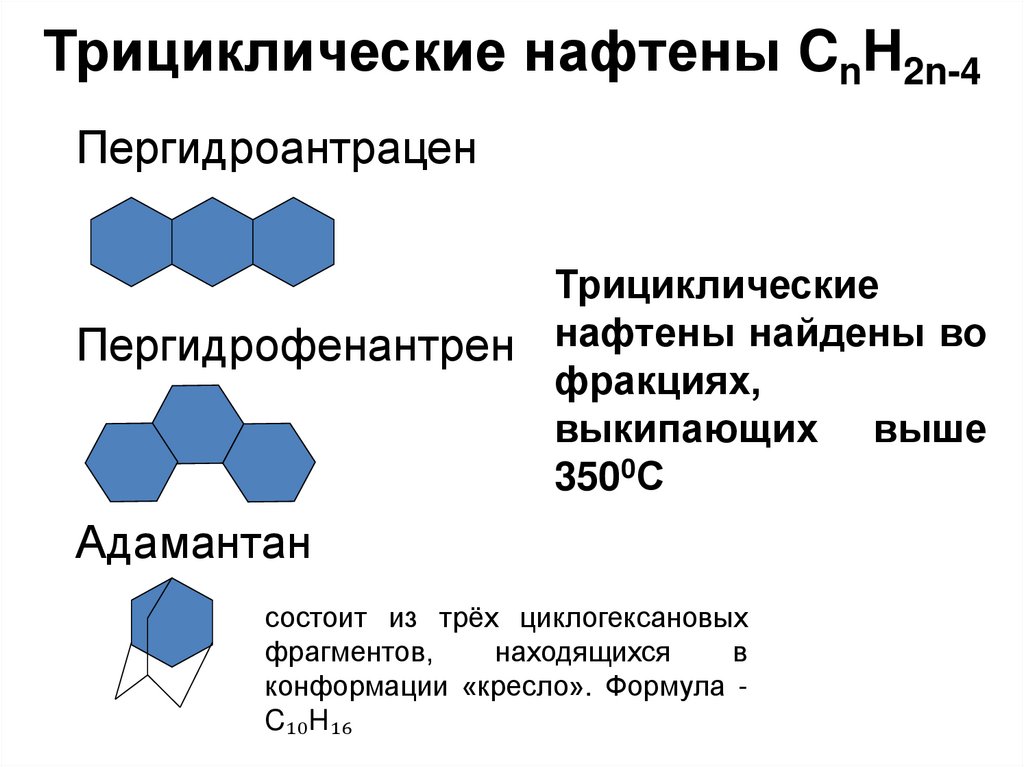
38. Трициклические нафтены CnH2n-4
ПергидроантраценТрициклические
Пергидрофенантрен нафтены найдены во
фракциях,
выкипающих выше
3500С
Адамантан
состоит из трёх циклогексановых
фрагментов,
находящихся
в
конформации «кресло». Формула C₁₀H₁₆
39.
Физические свойства нафтеновПентан (С5)
Циклопентан
(С5)
Гексан (С6)
циклогексан
(С6)
tкипения
36,08
tплавления
-129,7
плотность
0,6264
49,3
-94,4
0,7454
68,8
-94,0
0,6594
80,8
6,5
0,7781
Это объясняется тем, что вследствие более правильной, более
жесткой структуры молекулы нафтенов плотнее упаковываются в
жидком
или
твердом
состоянии,
что
увеличивает
силы
межмолекулярного взаимодействия
40. Введение метильной группы в молекулу нафтена резко нарушает симметрию молекулы, что приводит к уменьшению температуры плавления
Циклопентан (С5)Метилциклопентан (С6)
-940С
-142,70С
Циклогексан (С6)
Метилциклогексан (С7)
+6,50С
-126,30С
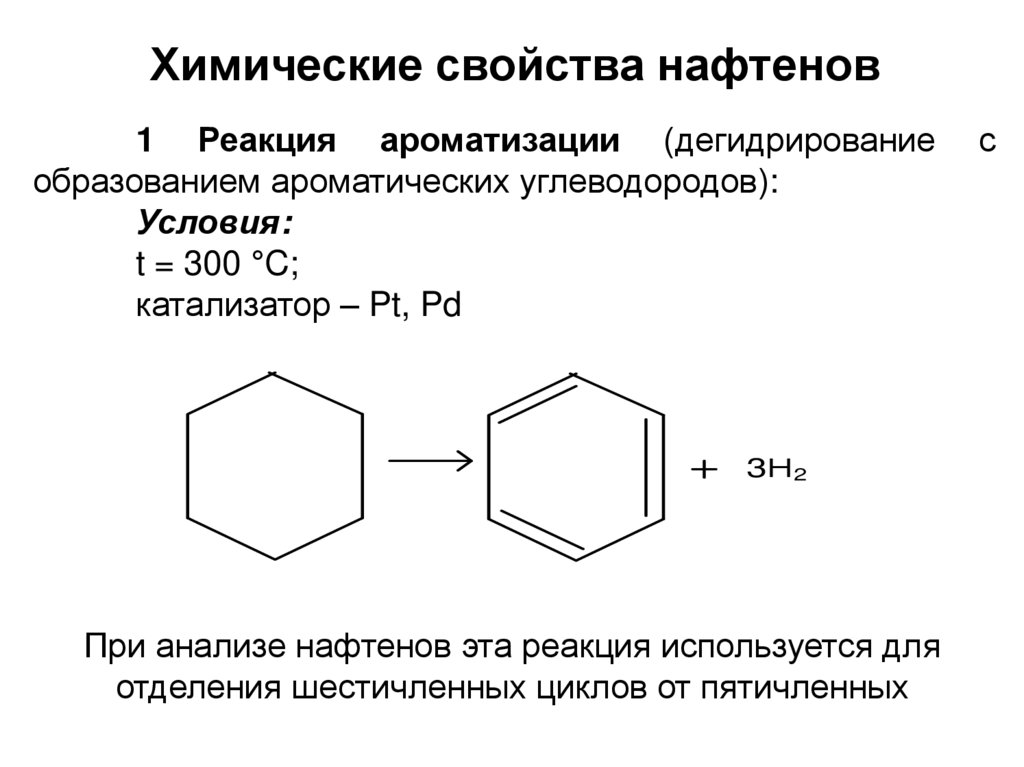
41. Химические свойства нафтенов
1 Реакция ароматизации (дегидрированиеобразованием ароматических углеводородов):
Условия:
t = 300 °C;
катализатор – Pt, Pd
3Н2
При анализе нафтенов эта реакция используется для
отделения шестичленных циклов от пятичленных
с
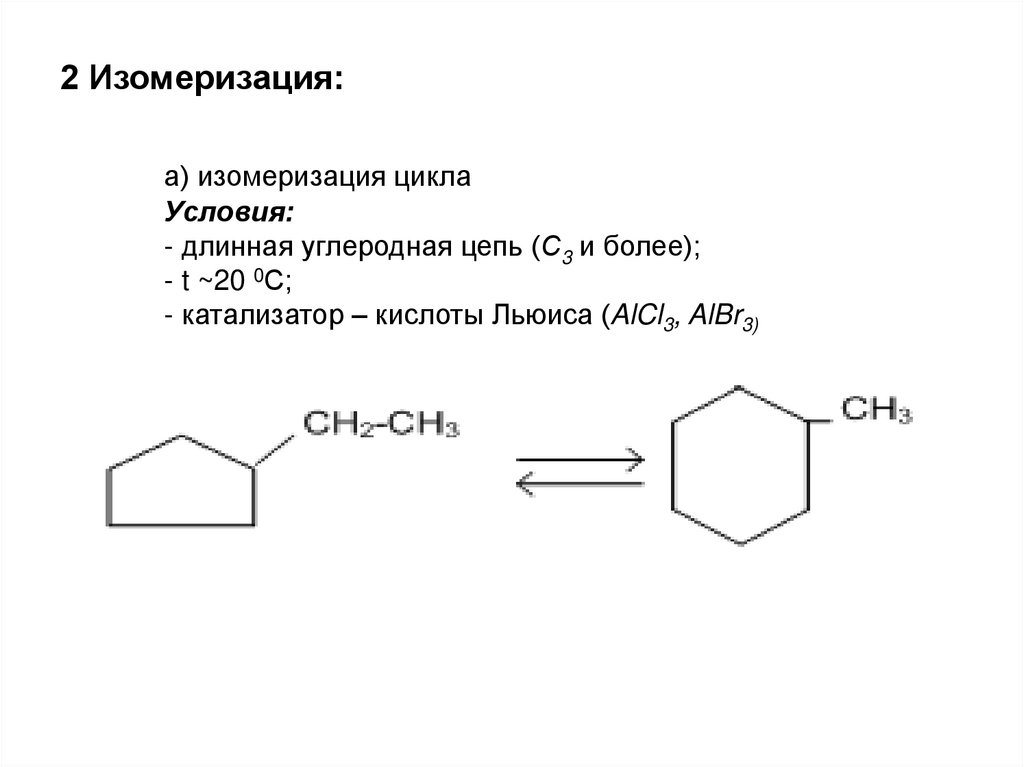
42.
2 Изомеризация:а) изомеризация цикла
Условия:
- длинная углеродная цепь (С3 и более);
- t ~20 0С;
- катализатор – кислоты Льюиса (AlCl3, AlBr3)
43. 3 Реакция окисления
Устойчивость к кислороду у нафтенового цикла ниже,чем у ароматического.
При
окислении
нафтеновых
получаются:
- спирты;
- двухосновные кислоты;
- кетокислоты.
углеводородов
Образующиеся кислоты окисляются в оксикислоты,
которые при дальнейшей конденсации дают смолы.
Пятичленный цикл более устойчив к окислению, чем
шестичленный
44.
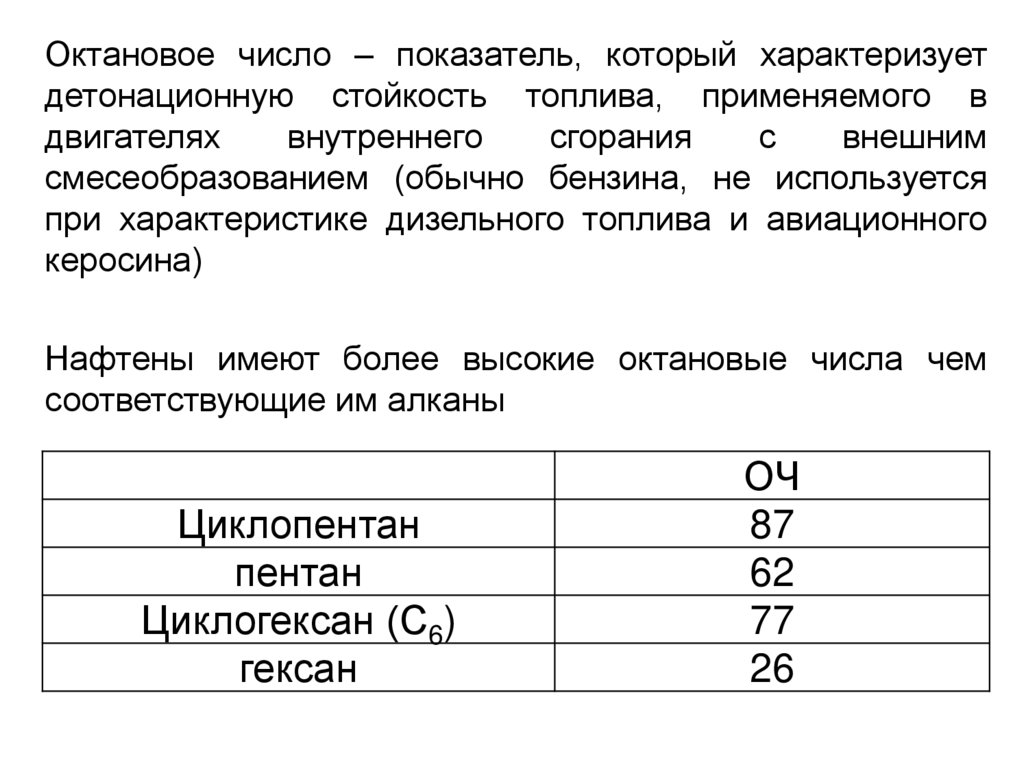
Октановое число – показатель, который характеризуетдетонационную стойкость топлива, применяемого в
двигателях
внутреннего
сгорания
с
внешним
смесеобразованием (обычно бензина, не используется
при характеристике дизельного топлива и авиационного
керосина)
Нафтены имеют более высокие октановые числа чем
соответствующие им алканы
Циклопентан
пентан
Циклогексан (С6)
гексан
ОЧ
87
62
77
26
45.
Ароматические углеводороды. Ареныорганические вещества, характеризующиеся
присутствием в их молекуле бензольного
кольца — циклической группировки из шести
атомов углерода с тремя двойными связями
Содержание в нефтях в среднем 10-20%
46.
Классификацияароматических
углеводородов:
1 одноядерные
2 многоядерные
- двуядерные
- трехядерные
- четырехядерные
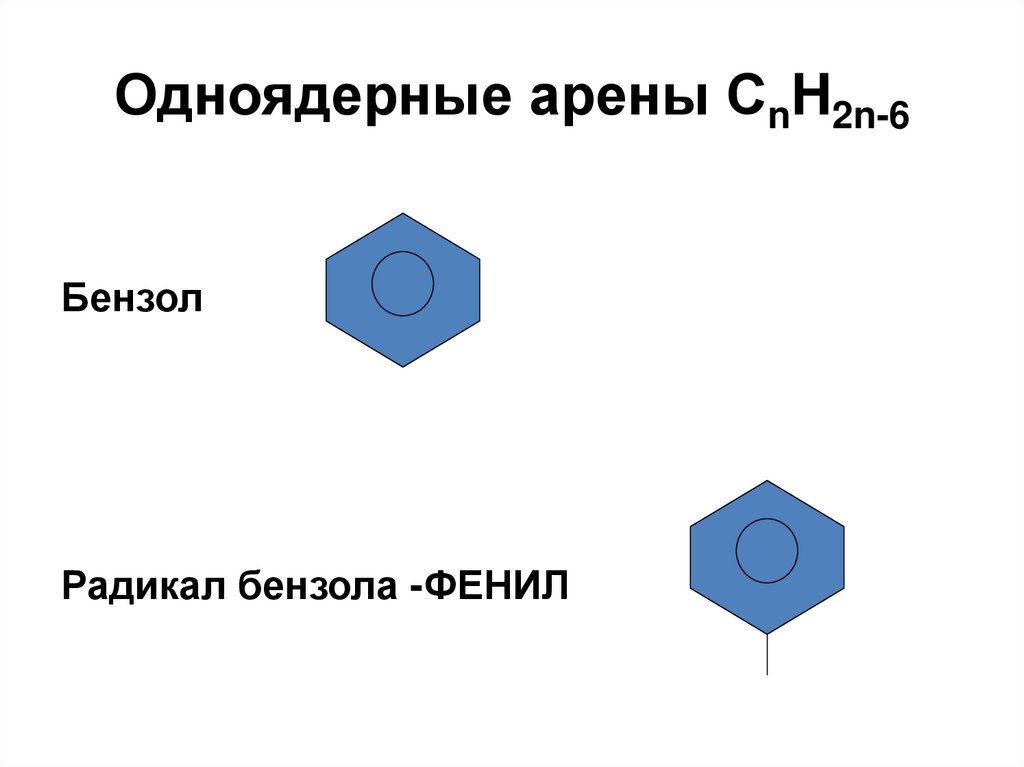
47. Одноядерные арены СnH2n-6
БензолРадикал бензола -ФЕНИЛ
48.
ТолуолМетил-бензол
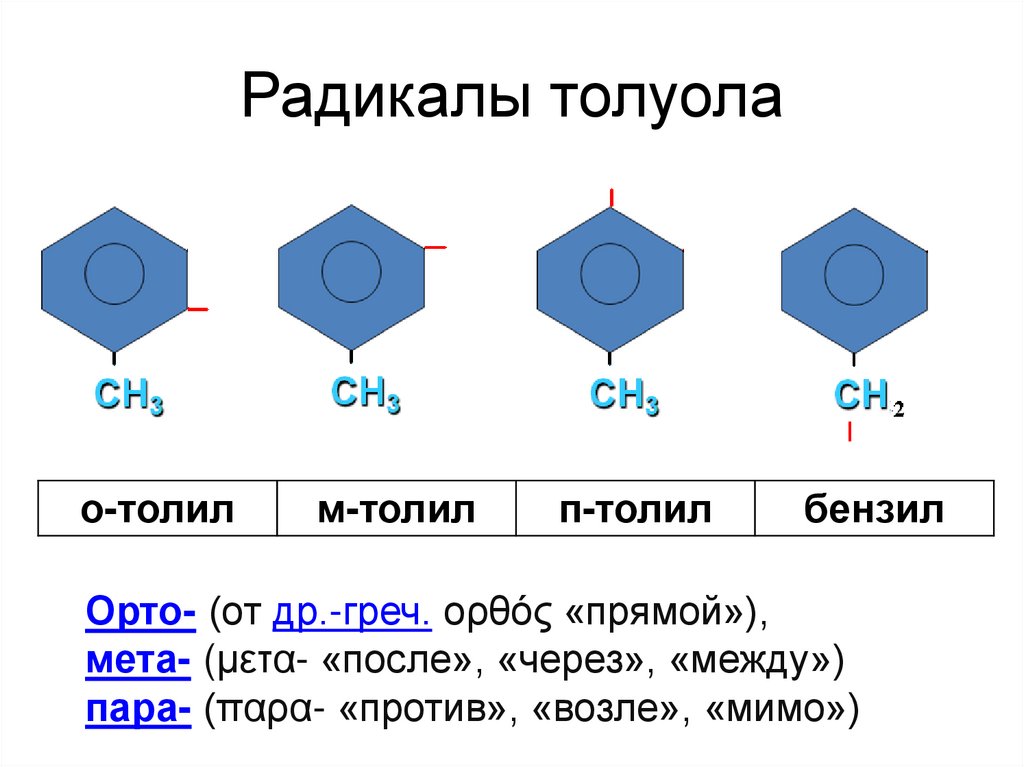
49. Радикалы толуола
о-толилм-толил
п-толил
бензил
Орто- (от др.-греч. ορθός «прямой»),
мета- (μετα- «после», «через», «между»)
пара- (παρα- «против», «возле», «мимо»)
50.
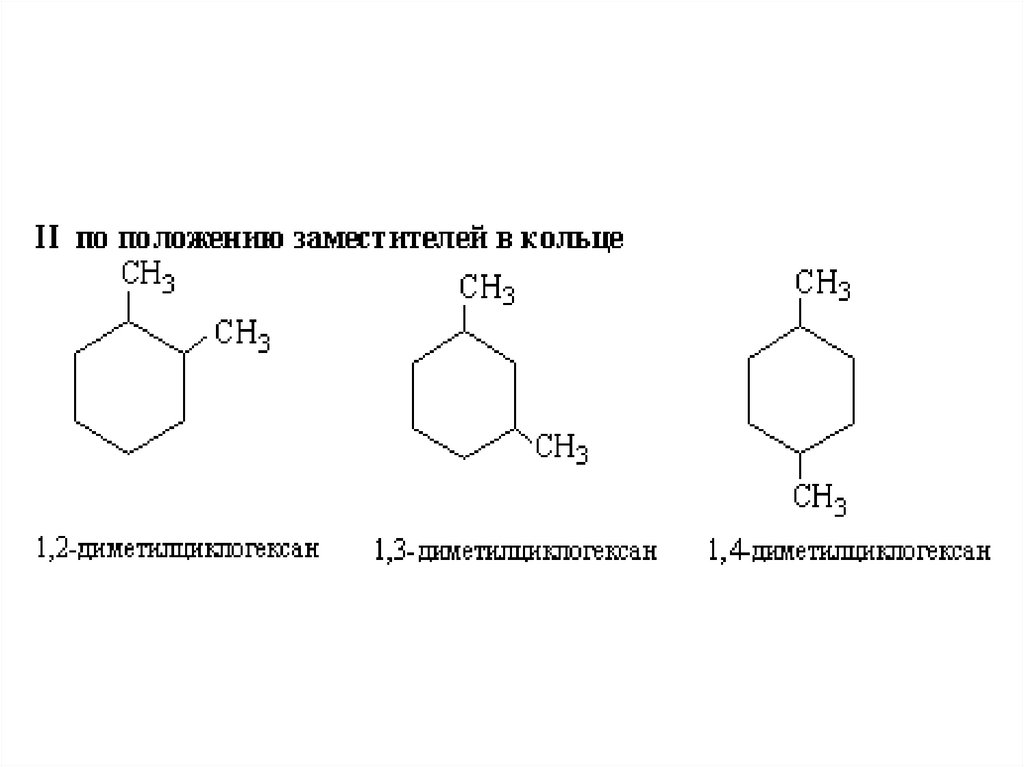
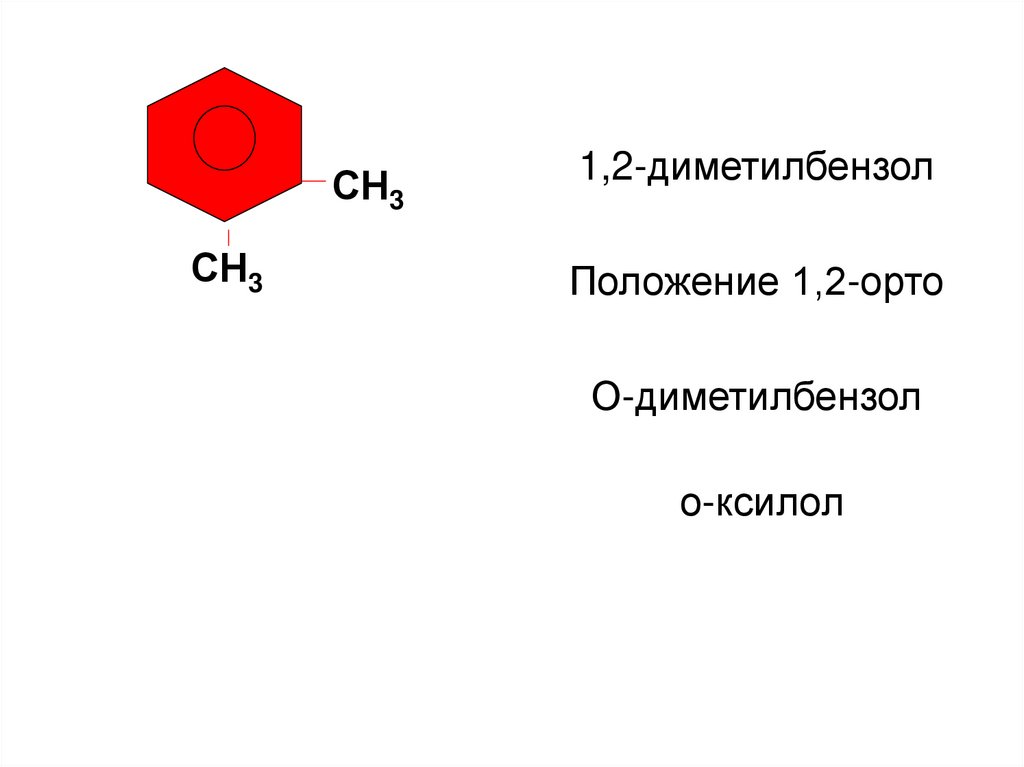
СН3СН3
1,2-диметилбензол
Положение 1,2-орто
О-диметилбензол
о-ксилол
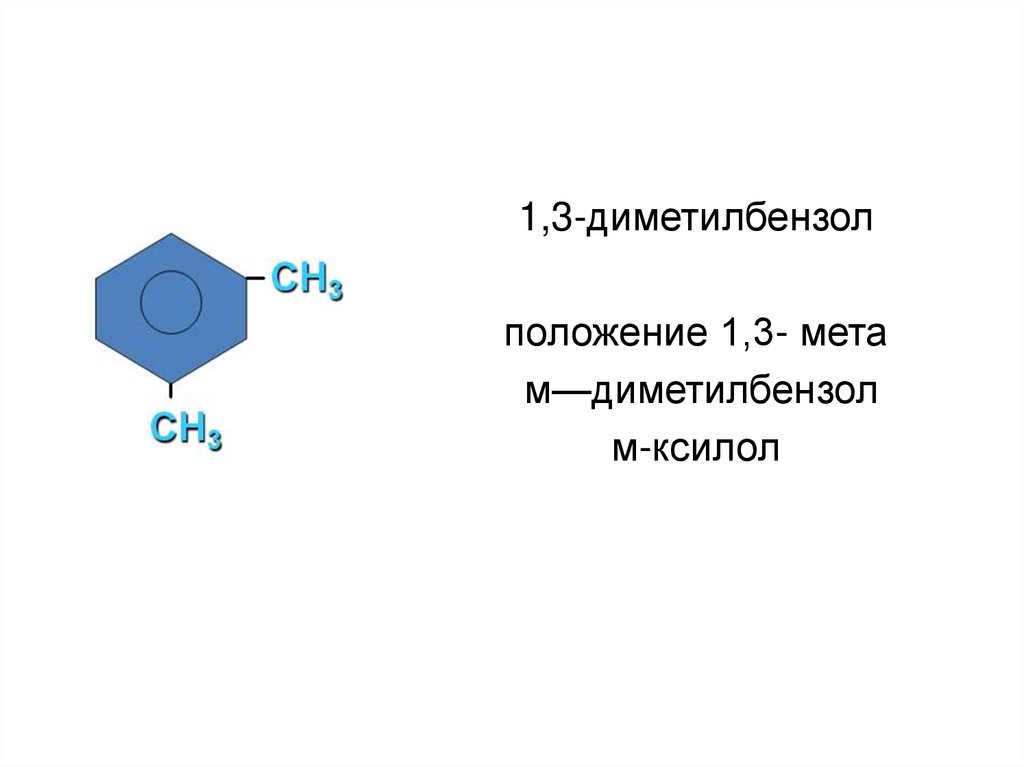
51.
1,3-диметилбензолположение 1,3- мета
м—диметилбензол
м-ксилол
52.
СН31,4-диметилбензол
положение 1,4 –пара
СН3
п-диметилбензол
п-ксилол
53. Многоядерные арены
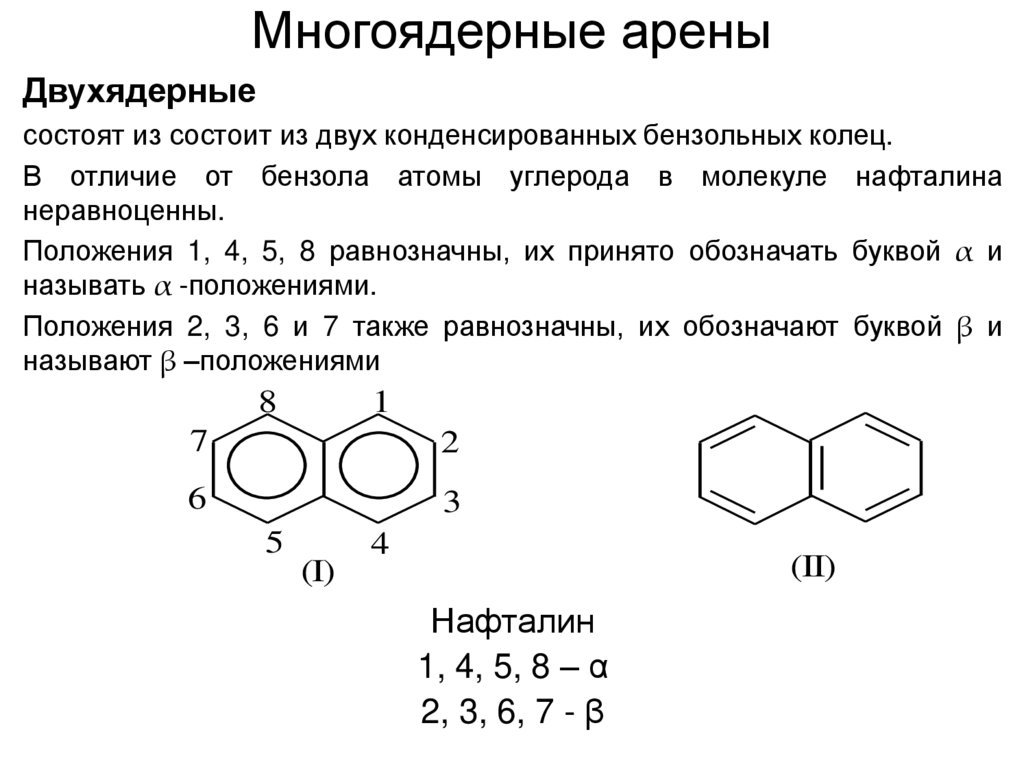
Двухядерныесостоят из состоит из двух конденсированных бензольных колец.
В отличие от бензола атомы углерода в молекуле нафталина
неравноценны.
Положения 1, 4, 5, 8 равнозначны, их принято обозначать буквой α и
называть α -положениями.
Положения 2, 3, 6 и 7 также равнозначны, их обозначают буквой β и
называют β –положениями
8
1
7
2
6
3
5
(I)
4
(II)
Нафталин
1, 4, 5, 8 – α
2, 3, 6, 7 - β
54.
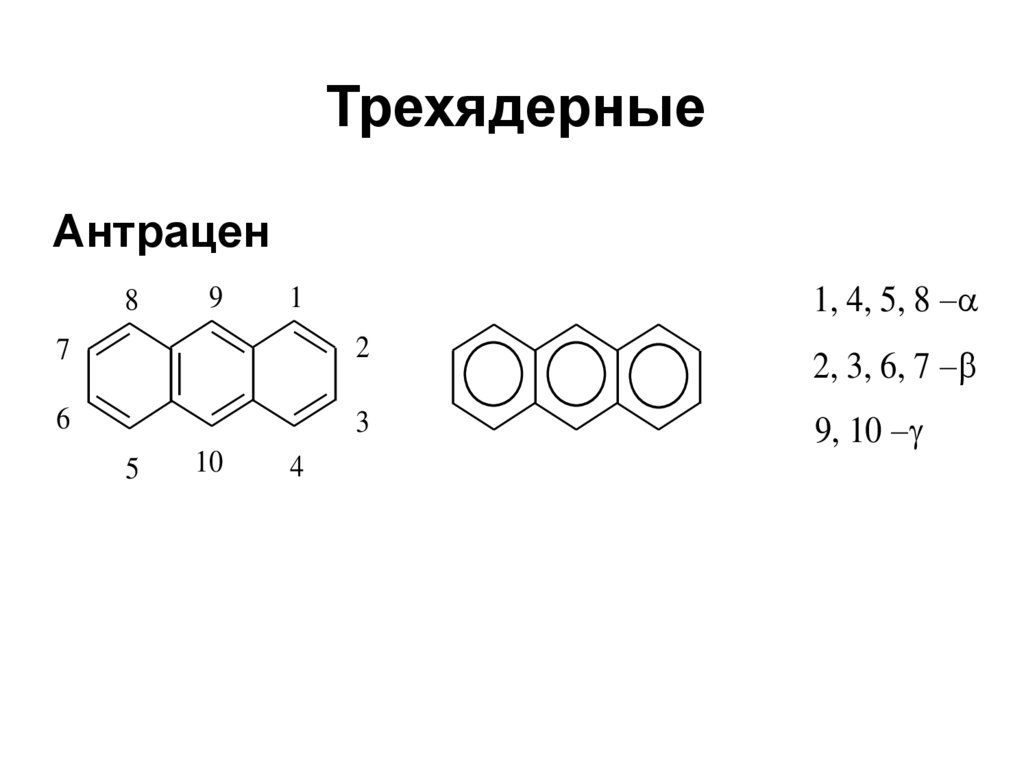
дифенилметан55. Трехядерные
Антрацен8
9
1, 4, 5, 8
1
7
2
2, 3, 6, 7
6
3
9, 10
5
10
4
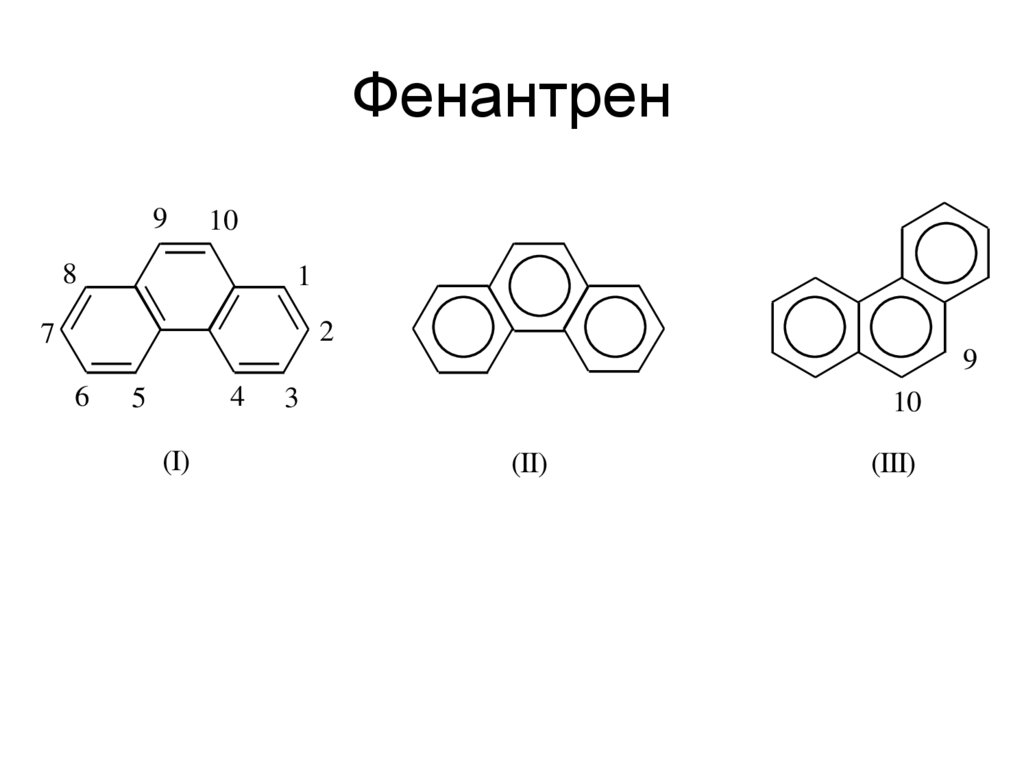
56. Фенантрен
910
8
1
2
7
9
6
4
5
(I)
3
10
(II)
(III)
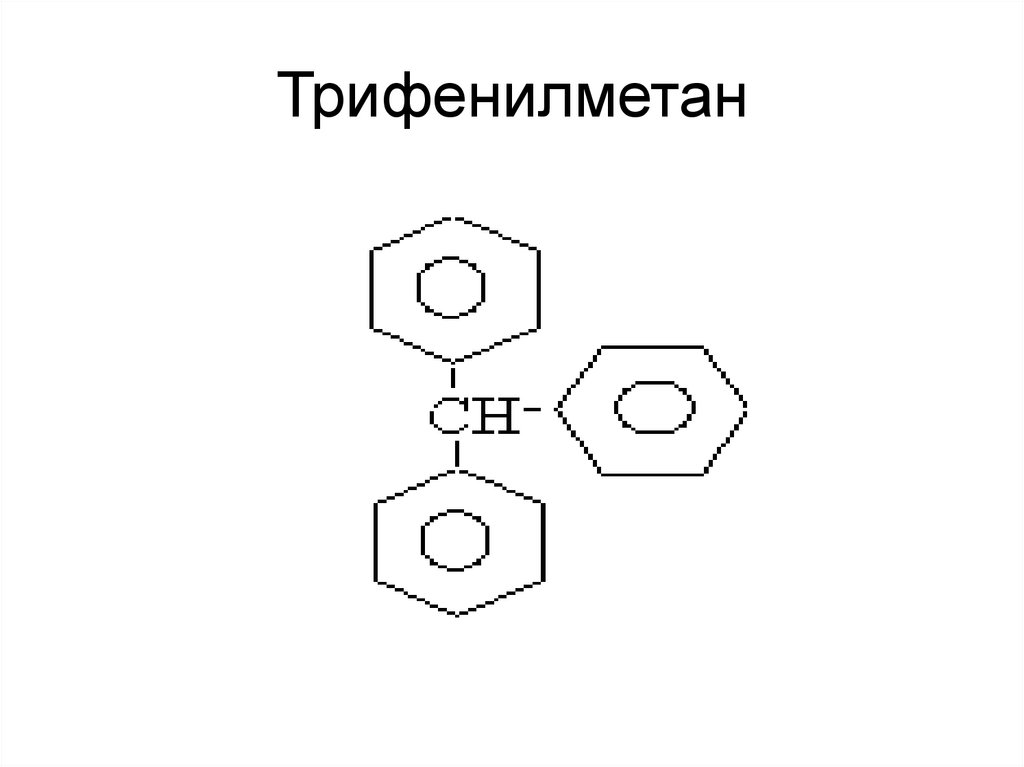
57. Трифенилметан
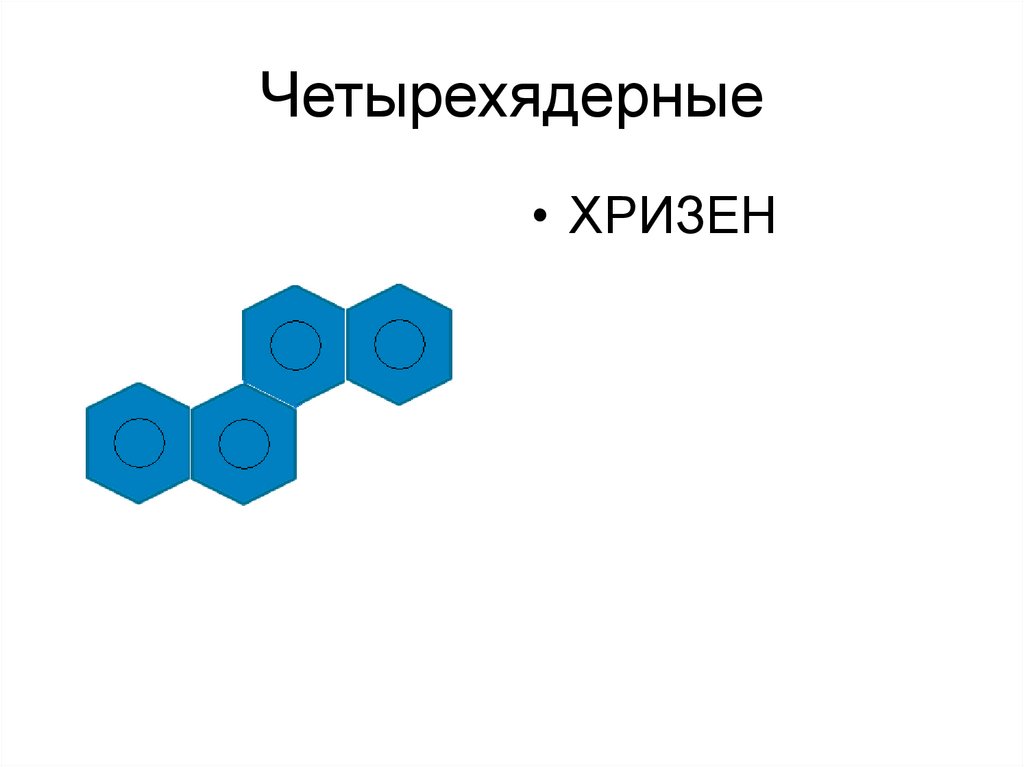
58. Четырехядерные
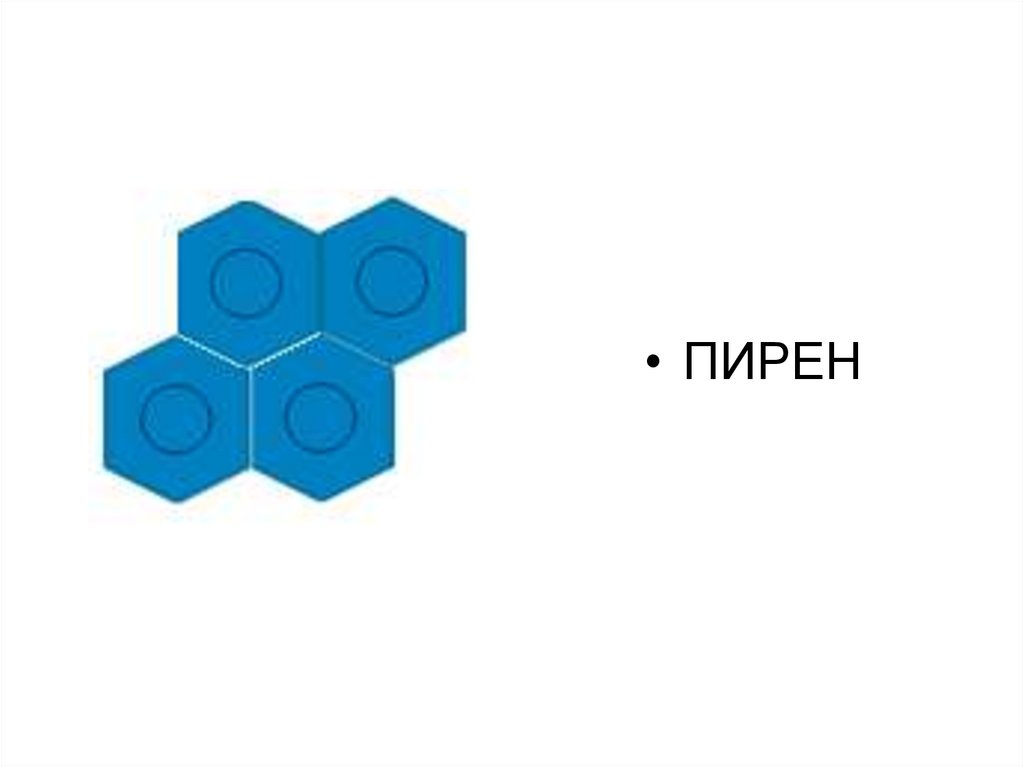
• ХРИЗЕН59.
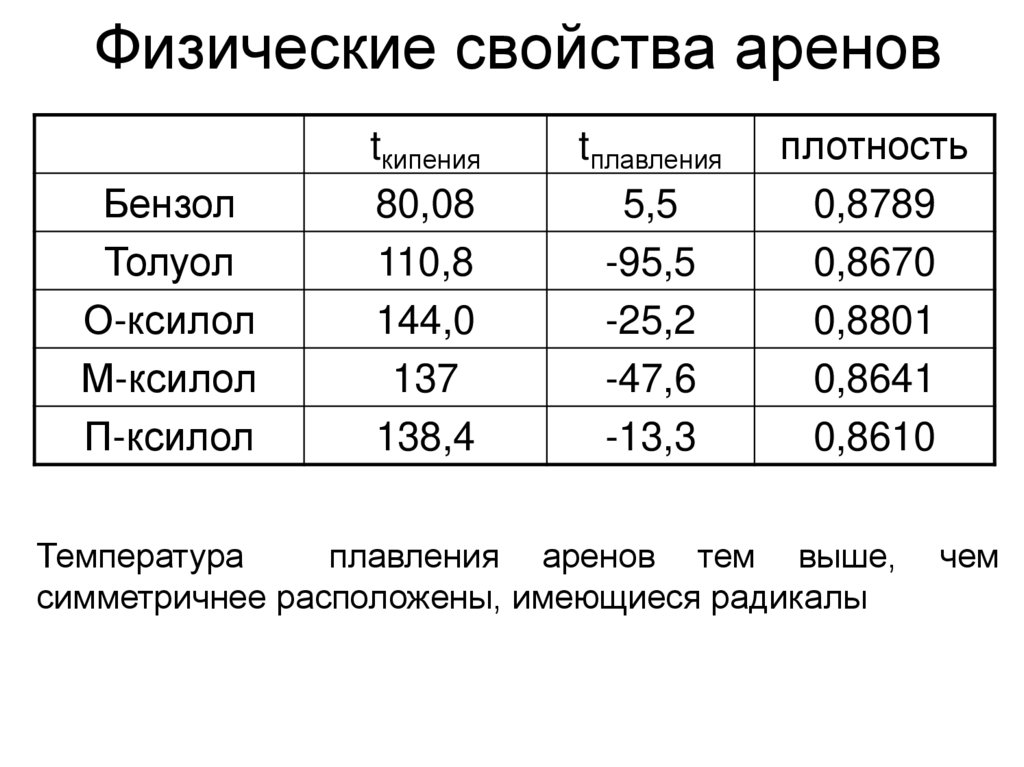
• ПИРЕН60. Физические свойства аренов
БензолТолуол
О-ксилол
М-ксилол
П-ксилол
tкипения
80,08
110,8
144,0
137
138,4
tплавления
5,5
-95,5
-25,2
-47,6
-13,3
плотность
0,8789
0,8670
0,8801
0,8641
0,8610
Температура
плавления аренов тем выше,
симметричнее расположены, имеющиеся радикалы
чем
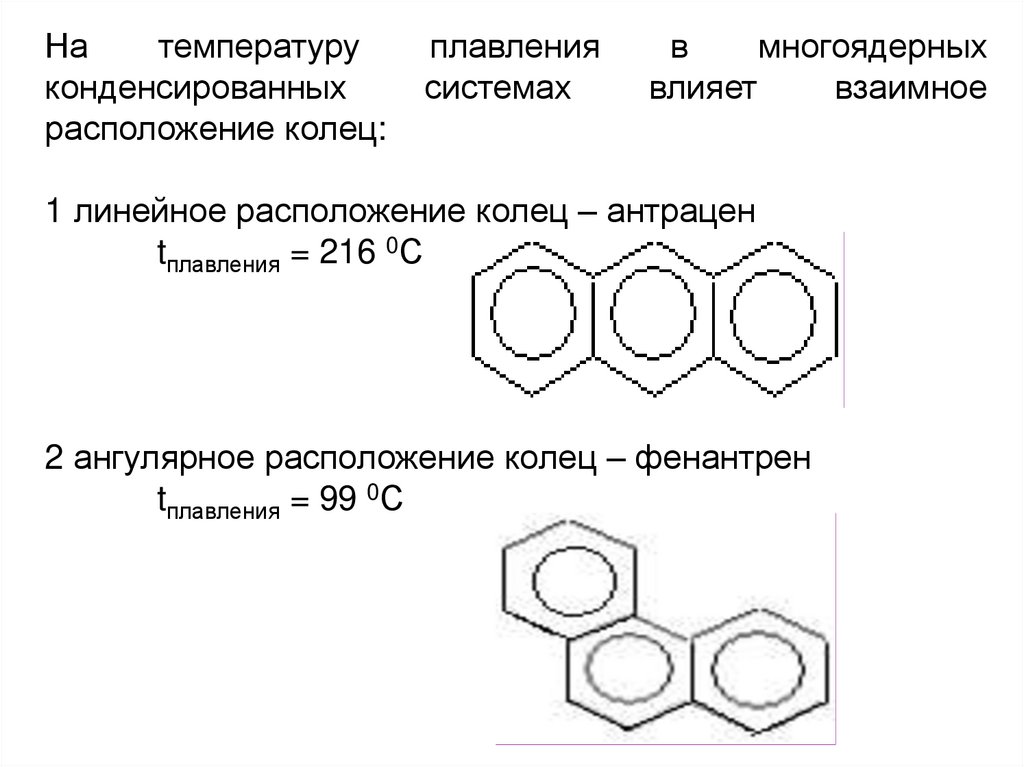
61.
Натемпературу
конденсированных
расположение колец:
плавления
системах
в
многоядерных
влияет
взаимное
1 линейное расположение колец – антрацен
tплавления = 216 0С
2 ангулярное расположение колец – фенантрен
tплавления = 99 0С
62. Распределение ароматических углеводородов по количеству циклов
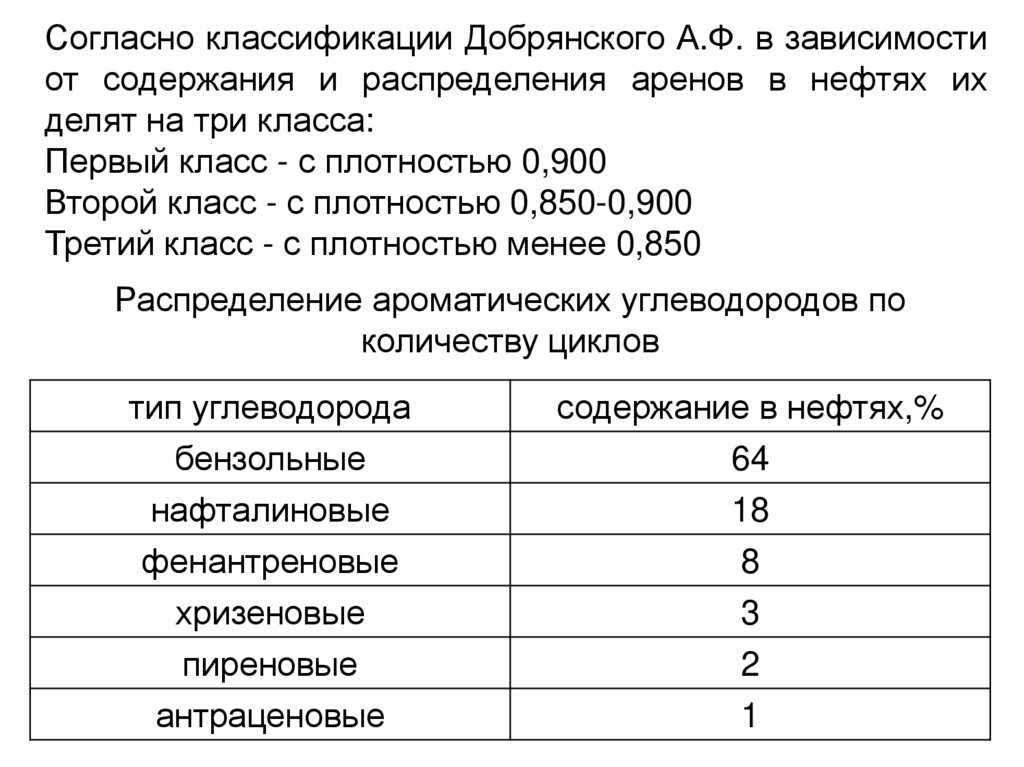
Согласно классификации Добрянского А.Ф. в зависимостиот содержания и распределения аренов в нефтях их
делят на три класса:
Первый класс - с плотностью 0,900
Второй класс - с плотностью 0,850-0,900
Третий класс - с плотностью менее 0,850
Распределение ароматических углеводородов по
количеству циклов
тип углеводорода
бензольные
нафталиновые
содержание в нефтях,%
64
18
фенантреновые
хризеновые
пиреновые
8
3
2
антраценовые
1






























 Химия
Химия








