Похожие презентации:
Этапы лабораторного процесса – нормативно-техническое обеспечение
1. Этапы лабораторного процесса – нормативно-техническое обеспечение
Этапы лабораторногопроцесса – нормативнотехническое обеспечение
Татаринова
Лидия Евгеньевна
Главный внештатный специалист ДЗ
ТО по клинической лабораторной
диагностике
Зав. Центром по лабораторному делу и
контролю качества Томской области
Томск 25.09.2020
2. Этапы процесса лабораторного исследования
Преаналитический этап 57,5 %3. Этапы процесса лабораторного исследования
Преаналитический этап 57,5 %Аналитический этап 25 %
4. Этапы процесса лабораторного исследования
Преаналитический этап 57,5 %Аналитический этап 25 %
Постаналитический этап
17,5%
5. НТД, регламентирующие деятельность КДЛ
Приказы, правила, инструкции, методические указания МЗ РФ итерриториальных органов управления здравоохранения
Национальные стандарты РФ. Лабораторная медицина и
медицинские изделия для диагностики in vitro
Методические указания и инструкции по применению
лабораторных методов исследования
Инструкции по применению наборов реагентов
Паспорта, технические описания и инструкции по эксплуатации
приборов
6. Нормативные документы (все этапы лабораторного процесса)
ГОСТ Р ИСО 15189-2015 «Лаборатории медицинские.Частные требования к качеству и компетентности»
Принят в 2006 году, 2010 год - обновленная редакция, в июне 2016 г –
новая редакция
Сформулированы основные требования к системе менеджмента
качества клинико-диагностической лаборатории ее компонентам
Представлены основные технические требования к персоналу,
условиям
среды в лаборатории, процедурам всех этапов
лабораторного процесса
7.
НТД преаналитическогоэтапа
8. Нормативные документы (преаналитический этап)
ГОСТ Р ИСО 53079.4-2008 «Технологии лабораторныеклинические. Обеспечение качества клинических
лабораторных исследований». Часть 3.
Правила взаимодействия персонала клинических
подразделений и КДЛ медицинских организаций при
выполнении клинических лабораторных исследований.
Устанавливает единые правила на всех этапах лабораторного исследования
взаимодействия персонала клинических подразделений и клиникодиагностических лабораторий медицинских организаций всех форм
собственности при проведении клинических лабораторных исследований и
обеспечении их качества, соответствующего потребностям эффективной
медицинской помощи пациентам. Настоящий стандарт предназначен для
применения всеми организациями и учреждениями, деятельность которых
связана с оказанием медицинской помощи.
9. Нормативные документы (преаналитический этап)
ГОСТ Р ИСО 53079.4-2008 «Технологии лабораторные клинические.Обеспечение качества клинических лабораторных исследований».
Часть 4.
Правила ведения преаналитического этапа.
Устанавливает
требования
к
условиям
и
процедурам
ведения
преаналитического этапа клинических лабораторных исследований с целью
исключения или ограничения влияния эндогенных, экзогенных, ятрогенных и
иных факторов, мешающих правильному отражению состояния внутренней
среды обследуемых пациентов в результатах клинических лабораторных
исследований.
Кроме того включает правила оформления запросов на исследования,
подготовку пациентов, взятие образцов, транспортировку, хранение, обработку
клинических проб.
10. Нормативные документы (преаналитический этап)
ГОСТ Р ИСО 56395-2015 «Лаборатории медицинские.Снижение ошибок посредством менеджмента риска и
постоянного улучшения»
Устанавливает потенциальные риски на каждом этапе каждого процесса.
Описывает предупреждающие и корректирующие действия, лабораторные
несоответствия. Описана ответственность руководства за предупреждающие и
корректирующие действия.
11. Нормативные документы (преаналитический этап)
ГОСТ Р ИСО 52905-2007 (ИСО 15190: 2003)«Лаборатории медицинские. Требования безопастности»
Устанавливает требования по обеспечению безопасной работы в
медицинской
лаборатории.
Содержит
общие
требования
к
проектированию помещений медицинской лаборатории (требования к
помещениям), физическим факторам влияющим на работу,
ответственность персонала, идентификацию опастностей и пути их
устранения, так же требования к СИЗ-ам. Описан порядок безопасной
работы со всеми материалами биологического происхождения.
12. Нормативные документы (преаналитический этап)
ГОСТ Р ИСО 52239-2004 «Перчатки медицинские диагностическиеодноразовые»
Часть 1. Спецификация на перчатки из каучукового латекса или
раствора
Устанавливает эксплуатационные характеристики упакованных стерильных и
неупакованных нестерильных перчаток из каучукового латекса или раствора,
предназначенных для одноразового использования с целью защиты пациента и
специалиста от взаимного заражения, а также перчаток из каучукового латекса,
предназначенных для использования при работе с зараженными медицинскими
материалами.
Надежность и правильное применение диагностических перчаток, способы
стерилизации с последующим транспортированием и хранением не входят в
область распространения данной части стандарта.
13. Нормативные документы
Актуальные версии ГОСТ-ов на сайте:www.protect.gost.ru
14. Нормативные документы (преаналитический этап)
Приказ МЗ СССР от 04.10.1980 № 1030«Об утверждении форм первичной документации учреждений
здравоохранения»
Приказом МЗ СССР от 05.10.1988 № 750* «О признании утратившими силу
нормативных актов Минздрава СССР» настоящий приказ признан
утратившим силу, однако, поскольку впоследствии МЗ РФ в него
неоднократно были внесены изменения, настоящий приказ фактически
продолжает свое действие (последнее изменение – январь 2003 г).
* - текст приказа официально опубликован не был
15. Учетно – отчетная документация медицинской лаборатории
Журнал регистрации анализов и их результатов (форма 250/у)Рабочий журнал лабораторных исследований (форма 251/у)
Журнал контроля работы стерилизаторов (форма 257/у)
Рабочий журнал исследований на стерильность (форма 258/у)
Листок ежедневного учета работы сотрудников (форма 261/у)
Журнал учета количества выполненных анализов (форма 262/у)
Бланки анализов:
- указание референтной величины каждого исследуемого параметра,
- заключение по комплексу результатов лабораторных исследований
Журнал учета спирта
Журнал сильнодействующих и ядовитых веществ
16. Прочая документация
Режим работы КДЛ, утвержденный руководителем медицинскогоучреждения
Журнал регистрации температурного режима холодильников и
термостатов
Журнал регистрации биологических аварий с вложенными
подготовленными чистыми бланками актов
Журнал проведения генеральных уборок
17.
НТД аналитического этапа18. Нормативные документы (аналитический этап)
Приказ МЗ РФ № 45 от 07.02.2000 г.«О системе мер по повышению качества клинических
лабораторных исследований в учреждениях
здравоохранения Российской Федерации»
1.4.4. Разработка и осуществление мер обеспечения качества
клинических лабораторных исследований на уровне клинико диагностической лаборатории и их отражение в "Руководстве по
качеству клинических лабораторных исследований" данной
лаборатории является обязанностью заведующего лабораторией.
19. Нормативные документы (ВКК)
Приказ МЗ РФ № 220 от 26.05.2003 г«Об утверждении отраслевого стандарта
«Правила проведения внутрилабораторного контроля качества
количественных методов клинических лабораторных
исследований с использованием контрольных материалов»
Устанавливает единый порядок ВКК количественных исследований, выполняемых
в КДЛ.
Приложение 1
Предельные допускаемые значения смещения (В) и коэффициента вариации (СV)
определения лабораторных показателей в контрольном материале
20. Нормативные документы (ВКК)
Приказ МЗ РФ № 220 от 26.05.2003 г«Об утверждении отраслевого стандарта
«Правила проведения внутрилабораторного контроля качества
количественных методов клинических лабораторных
исследований с использованием контрольных материалов»
Приложение 2
Регистрационная форма «Оценка сходимости результатов измерения»
Приложение 3
Регистрационная форма «Результаты установочных серий измерений показателя в
контрольных материалах»
Приложение 4
Журнал «Регистрация отбракованных результатов внутрилаборатор-ного
контроля качества»
21. Нормативные документы
ОС 91500.13.000.2003 приложение к приказу МЗ РФ № 220 «Правилапроведения внутрилабораторного контроля качества количественных
методов клинических лабораторных исследований с использованием
контрольных материалов»
…6.1.3. При использовании реактивов и калибраторов одного
производителя рекомендуется применять аттестованные
контрольные материалы другого производителя
К сожалению, в ГОСТ этой рекомендации нет
22. Нормативные документы (аналитический этап)
ГОСТ Р 53022-2008«Технологии лабораторные медицинскиеклинические.
Требования к качеству клинических лабораторных
исследований»
Часть 2. Оценка аналитической надежности методов
исследования (точность, чувствительность, специфичность)
Устанавливает
единые требования при оценке правильности,
прецизионности,
чувствительности,
специфичности
клинических
лабораторных исследований, выполняемых в клинико-диагностических
лабораториях медицинских организаций. Соблюдение этих требований
обеспечивает уровень аналитической надежности результатов лабораторных
исследований, необходимый для уверенного использования этих результатов
при принятии клинических решений.
23. Нормативные документы (аналитический этап)
• Методические указания и инструкции по применению лабораторныхметодов исследования
• Инструкции по применению наборов реагентов
• Инструкции по эксплуатации приборов
24.
НТД постаналитическогоэтапа
25. Нормативное обеспечение
ГОСТ Р ИСО 15189-2015 «Лаборатории медицинские. Частныетребования к качеству и компетентности»
ГОСТ Р 53079.2-2008 «Обеспечение качества клинических
лабораторных исследований. Часть 3. Правила взаимодействия
персонала клинических подразделений и клинико-диагностических
лабораторий
медицинских
организаций
при
выполнении
клинических лабораторных исследований»
Приказ МЗ СССР от 04.10.1980 г. N 1030 "Об утверждении форм
первичной документации учреждений здравоохранения"
26. Нормативное обеспечение
ГОСТ Р 53022.3-2008«Технологии лабораторные клинические.
Требования к качеству клинических лабораторных исследований»
Часть 3. Правила оценки клинической информативности
лабораторных тестов
Устанавливает единые правила оценки клинической информативности
лабораторных исследований, выполняемых в клинико-диагностических
лабораториях медицинских организаций в целях оценки состояния здоровья,
клинической диагностики и слежения за эффективностью лечения пациентов.
Освещает физиологические и биохимические факторы, влияющие на
результат лабораторного теста; вариации лабораторных результатов;
референтные интервалы содержания аналитов и правила их установления.
27. Нормативное обеспечение
ГОСТ Р 53022.4-2008«Технологии лабораторные клинические.
Требования к качеству клинических лабораторных исследований»
Часть 4. Правила разработки требований к своевременности
предоставления лабораторной информации
Устанавливает единые правила разработки требований к срокам
выполнения клинических лабораторных исследований в клиникодиагностических лабораториях и порядок их применения при
организации лабораторного обеспечения деятельности медицинских
организаций. Обозначены факторы, влияющие на сроки получения
результатов; рекомендуемые сроки выполнения исследований,
результать которых имеют жизненно важное значение для пациентов в
критических ситуациях.
28. Нормативные документы
ФГБУ «Центр мониторинга и клинико – экономической экспертизы»Росздравнадзора
Предложения (практические рекомендации)
по внутреннему контролю качества и безопасности деятельности
медицинской лаборатории, 2018 г
1.
2.
3.
4.
5.
6.
7.
8.
Управление персоналом
Обеспечение ресурсами
Идентификация и прослеживаемость
Производственная среда и безопасность
Управление информацией и информационная безопасность
Управление преаналитическими процедурами
Управление аналитическими процедурами
Управление постаналитическими процедурами
29. Нормативные документы
Инструменты оценки показателей30. Нормативные документы
31.
Взятие крови32. Взятие крови в вакуумную пробирку
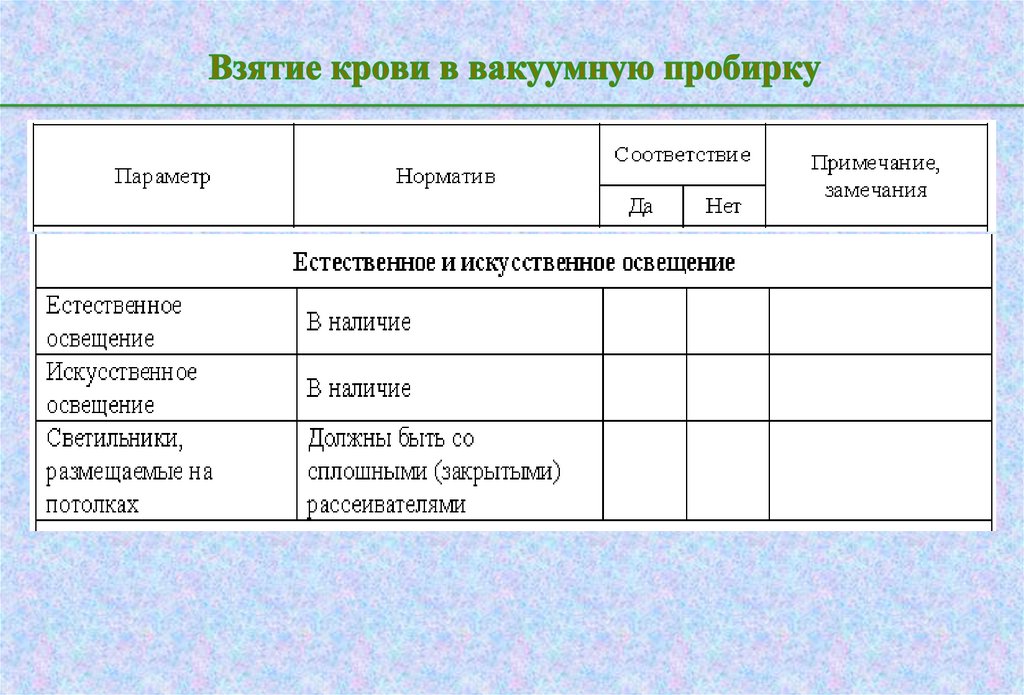
33. Взятие крови в вакуумную пробирку
Check – лист инспекционного контроля (аудита) КДЛ(процедурного кабинета)
Соответствие требованиям согласно:
СанПиН 2.1.3.2630-10
«Санитарно – эпидемиологические требования к
организациям, осуществляющим
медицинскую деятельность»
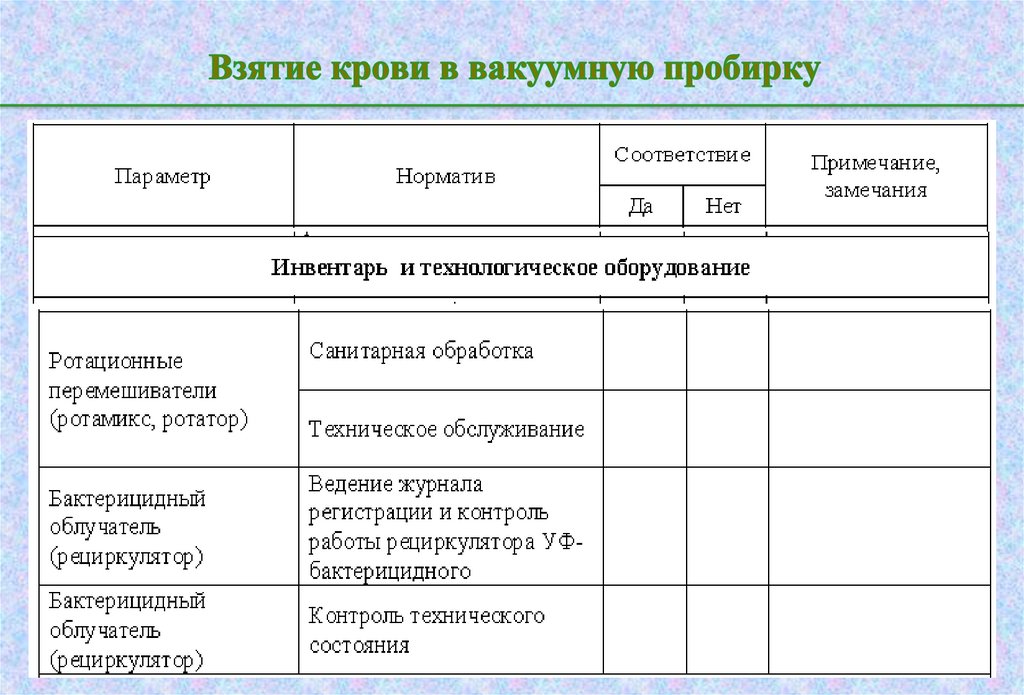
34. Взятие крови в вакуумную пробирку
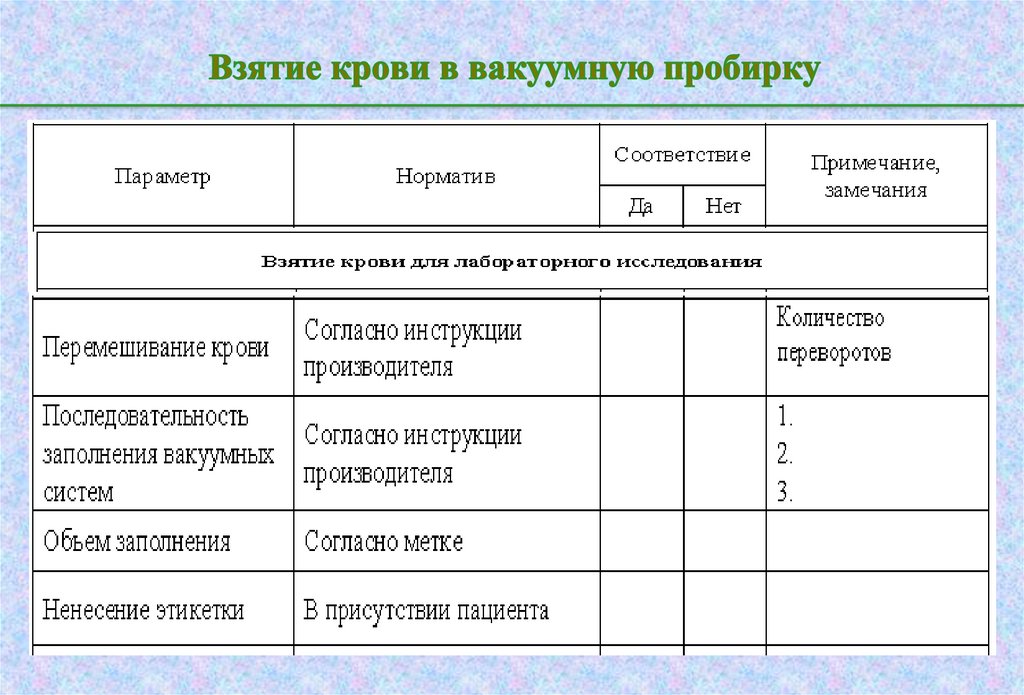
35. Взятие крови в вакуумную пробирку
36. Взятие крови в вакуумную пробирку
37. Взятие крови в вакуумную пробирку
38. Взятие крови в вакуумную пробирку
39. Взятие крови в вакуумную пробирку
40. Взятие крови в вакуумную пробирку
41. Взятие крови в вакуумную пробирку
42. Взятие крови в вакуумную пробирку
43. Взятие крови в вакуумную пробирку
44. Предотвращение ошибок
Самый эффективный путь предотвращения ошибок на любом этапеисследования – это разработка стандартов (СОП-ов) для каждой
его процедуры, разработка критериев оценки качества каждой
процедуры и квалифицированный персонал.
45. БЛАГОДАРЮ ЗА ВНИМАНИЕ
+7 (3822) 915-076tatarinovalida@mail.ru









































 Медицина
Медицина








