Похожие презентации:
Электролитическая диссоциация
1.
2. Кислоты – электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка
HClHNO3
H2SO4
+
-
H + Cl
H+ + NO3−
2H+ + SO42−
Слабые многоосновные кислоты диссоциируют ступенчато:
H2SO3
H+ + HSO3−
HSO3−
H+ + SO32−
Общие характерные свойства кислот обусловлены
присутствием катионов водорода
3.
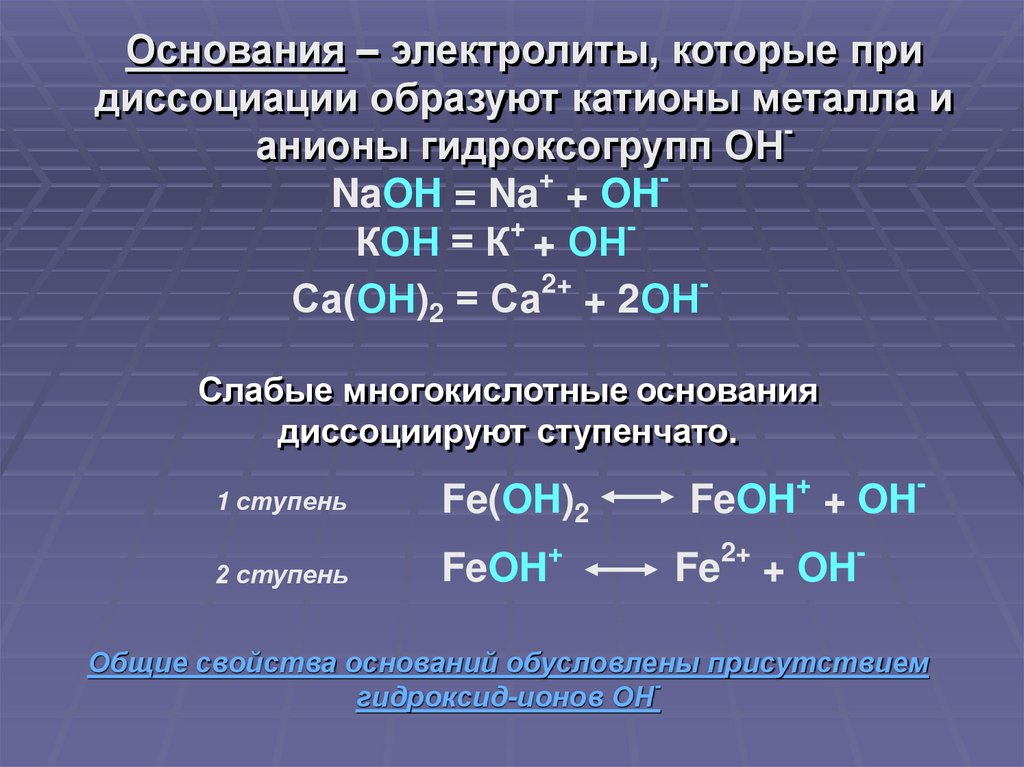
Основания – электролиты, которые придиссоциации образуют катионы металла и
анионы гидроксогрупп ОН
+
NaOH = Na + OH
+
КОН = К + ОН
2+
Са(ОН)2 = Са + 2ОН
Слабые многокислотные основания
диссоциируют ступенчато.
1 ступень
2 ступень
Fe(OH)2
+
FeOH
+
-
FeOH + OH
Fe
2+
-
+ OH
Общие свойства оснований обусловлены присутствием
гидроксид-ионов ОН-
4.
Средние соли – сильные электролиты, которые придиссоциации образуют катионы металла (или аммония
NH4+) и анионы кислотных остатков
К3РО4
3К+ + РО43NH4Cl
NH4+ + Cl−
Кислые соли – электролиты, диссоциирующие на катион
металла и сложный анион, в состав которого входят
атомы водорода и кислотный остаток
NaHCO3
Na+ + HCO3−
α1 >> α2
HCO3−
H+ + CO32−
Основные соли – электролиты, которые при
диссоциации образуют анионы кислотного
остатка и сложные катионы, состоящие из атомов
металла и гидроксогрупп ОН−
(FeOH)2SO4
2FeOH+ + SO42−
FeOH+
Fe2+ + OH−
α1 >> α2
5.
Запишите понятия, соответствующие этим определениямВещества, растворы которых проводят электрический ток.
Процесс распада электролита на ионы.
Положительно заряженные ионы.
Отрицательно заряженные ионы
Электролиты, которые при диссоциации образуют катионы
водорода и анионы кислотного остатка.
6. Электролиты, которые при диссоциации образуют катионы
металла и анионы гидроксогрупп ОН−.
7. Электролиты, которые при диссоциации образуют катионы
металла и анионы кислотных остатков.
8. Количественная характеристика электролитической
диссоциации
9. Молекулы, имеющие два электрических заряда, равных по
величине, но противоположных по знаку, и расположенных на
некотором расстоянии друг от друга
10. Автор теории электролитической диссоциации.
1.
2.
3.
4.
5.




 Химия
Химия