Похожие презентации:
Основы биотехнологии. Лекция № 2 (1)
1.
Национальный исследовательский университетРоссийский государственный университет нефти и газа (НИУ)
имени И. М. Губкина
Основы биотехнологии
Лекция № 2 (1)
Для групп ХТ-19-1-7
Иванова Людмила Вячеславовна
профессор
кафедры органической химии и химии нефти
e-mail: ivanova.l@gubkin.ru
Москва, 2021
2.
Белки-сложные полимерные
вещества,
построенные из остатков
аминокислот
Аминокислоты -полифункциональные
соединения, содержащие
одновременно амино- и
карбоксильную группы
3.
2α1
NH2-CH2-COOH 2-аминоэтановая кислота
α-аминоуксусная кислота
глицин
β
3
α
2
1
СН3-СН-СООН
NH2
β
3
α
2
2-аминопропановая кислота
α-аминопропионовая кислота
аланин
1
NH2-CH2CH2-COOH 3-аминопропановая кислота
β-аминопропионовая кислота
4.
HR
C
NH2
COOH
5.
Важнейшие аминокислотыНазвание
Сокращенное
обозначение
Глицин
Гли
Формула
Gly
H CH
COOH
Название
Сокращенное
обозначение
Треонин
Тре
Формула
CH3 CH CH COOH
Thr
OH NH2
NH2
Аланин
Ала
H3C
Ala
CH
Цистеин
COOH
NH2
Валин
Вал
CH3
Val
CH3
CH CH
Метионин
COOH
цисSH
Cys
Мет
Met
HS CH2 CH
NH2
CH3 S CH2 CH2 CH
NH2
Лейцин
Лей
Leu
CH3
CH3
Изолейцин
Илей
Ile
COOH
COOH
NH2
Фенилаланин
CH CH2 CH COOH
Фен
Phe
CH2 CH
NH2
COOH
NH2
CH3 CH2 CH CH COOH
Тирозин
Тир
Орнитин
Орн
Пролин
Про
Оксипролин
ПроОН
Tyr
CH2 CH
HO
CH3 NH
COOH
2
Аспаргиновая
кислота
Асп
Asp
HOOC CH2 CH
COOH
NH2
Глутаминова
я кислота
Глу
Гистидин
Гис
Glu
NH2
HOOC CH2 CH2 CH
COOH
HN
Pro
His
N
Лиз
Lys
NH
COOH
HN
Три
H2N CH2 CH2 CH2 CH2 CH
Trp
CH2 CH
COOH
Серин
Сер
HO CH2 CH
Ser
COOH
Аргинин
Арг
Arg
Gln
O
H2N
H2N
HN
N
H
Глн
COOH
NH2
NH2
Глутамин
COOH
HO
NH2
NH2
Триптофан
COOH
NH2
CH2 CH
Лизин
NH2
H2N CH2 CH2 CH2 CH COOH
NH CH2 CH2 CH2 CH
NH2
C CH2 CH2 CH
NH2
COOH
Аспарагин
Асн
Asn
O
H2N
C CH2 CH
NH2
COOH
COOH
6.
Способы получения α-аминокислот1. Действие аммиака на α-галогенкислоты
2NH3 + Cl-CH2-COOH
NH2-CH2-COOH + NH4Cl
7.
2. Циангидринный методOH
O
CH3-C
+ H-CN
CH3 C
CN
H
α-оксинитрил
H
OH
NH2
CH3 C
CN
+ NH3
-H2O
CH3 C
H
H аминонитрил
NH2
CH3 C
H
CN
NH2
H+
CN + 2H2O
CH3 C
COOH + NH3
H α-аминокислота
8.
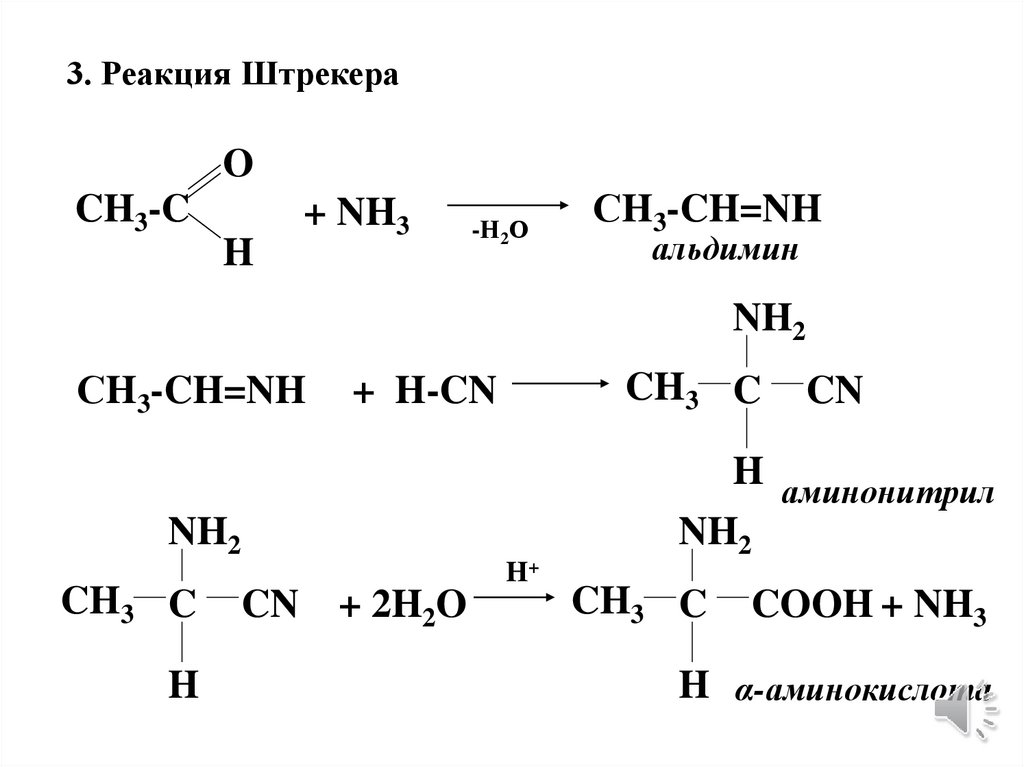
3. Реакция ШтрекераO
CH3-C
H
+ NH3
-Н2О
СH3-CH=NH
альдимин
NH2
СH3-CH=NH
CH3 C
+ H-CN
CN
H аминонитрил
NH2
CH3 C
H
NH2
H+
CN + 2H2O
CH3 C
COOH + NH3
H α-аминокислота
9.
4. Восстановление α-нитрокислот, оксимов α-оксокислотСН3
СН3
СН-СН-СООН + Н2
[Ni, Pd, Pt]
СН3
-2H2O
СН3
NO2
α-нитроизовалерьяновая
кислота
СН3
СН3
СН-С-СООН
СН-СН-СООН
NH2
валин
2 Н2
NOН
оксим α-оксоизовалерьяновой
кислоты
СН3
СН3
СН-СН-СООН
NH2
валин
10.
5. Метод В.В.ФеофилактоваO
O
СН3-С-СН-С
OC2H5
R
производное
ацетоуксусного эфира
O N=N-C6OH5
СН3-С--С--С
O-C2H5
R
изомеризация
N-NH-C6H5
R-C-COOH
+
+ C6H5N≡NCl
ОН-
соль фенилдиазония
N=N-C6H5
НОН
-СН3СООН
-СН3СН2ОН
[H]
Zn+HCl
фенилгидразон α-кетокислоты
HC-COOH
R
NH2
R-CH-COOH
α-аминокислота
+ C6H5NH2
11.
6. Микробиологический синтез-основан на гидролизе белков и последующем
разделением смеси.
12.
Физические свойства α-аминокислот- бесцветные кристаллические вещества;
- легко растворимы в воде;
- многие обладают сладким вкусом;
- имеют высокую температуру плавления;
- водные растворы одноосновных аминокислот
проявляют практически нейтральную среду:
рН=6,8;
-в растворах существуют в виде внутренней соли
– биполярного иона:
13.
Биполярный ионNH2-CH2-COOH
_
+
NH3-CH2-COO
Н+
ОН-
_
+
NH2-CH2-COO
NH3-CH2-COOH
сопряженное основание
глицина
сопряженная кислота
глицина
(щелочная среда)
(кислая среда)
14.
Все α-аминокислоты (кроме глицина) имеютхиральный центр и существуют в виде двух
энантиомеров: L и D
COOH
COOH
HO
*
H
NH2
*
CH3
CH3
L-молочная кислота
L-аланин
H
15.
COOHNH2
H
НООC
H
R
NH2
H
НООC
*
R
NH2
пространственное строение L-аминокислот
R
16.
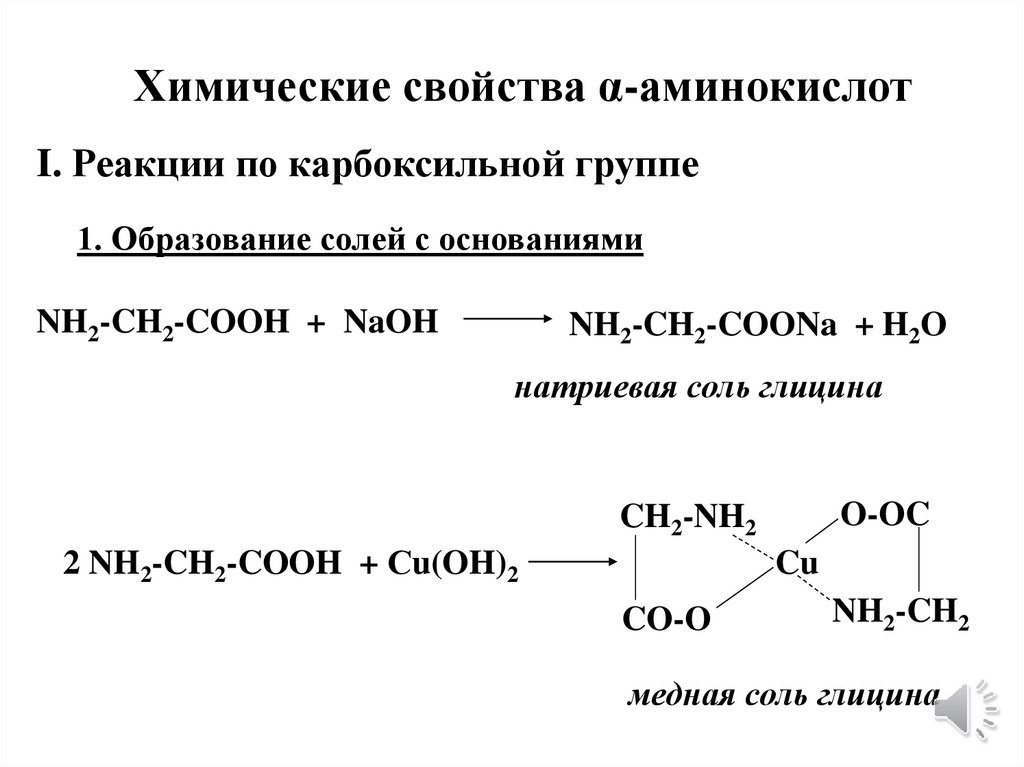
Химические свойства α-аминокислотI. Реакции по карбоксильной группе
1. Образование солей с основаниями
NH2-CH2-COOH + NaOH
NH2-CH2-COONa + H2O
натриевая соль глицина
O-OC
CH2-NH2
2 NH2-CH2-COOH + Сu(OH)2
Cu
CO-O
NH2-CH2
медная соль глицина
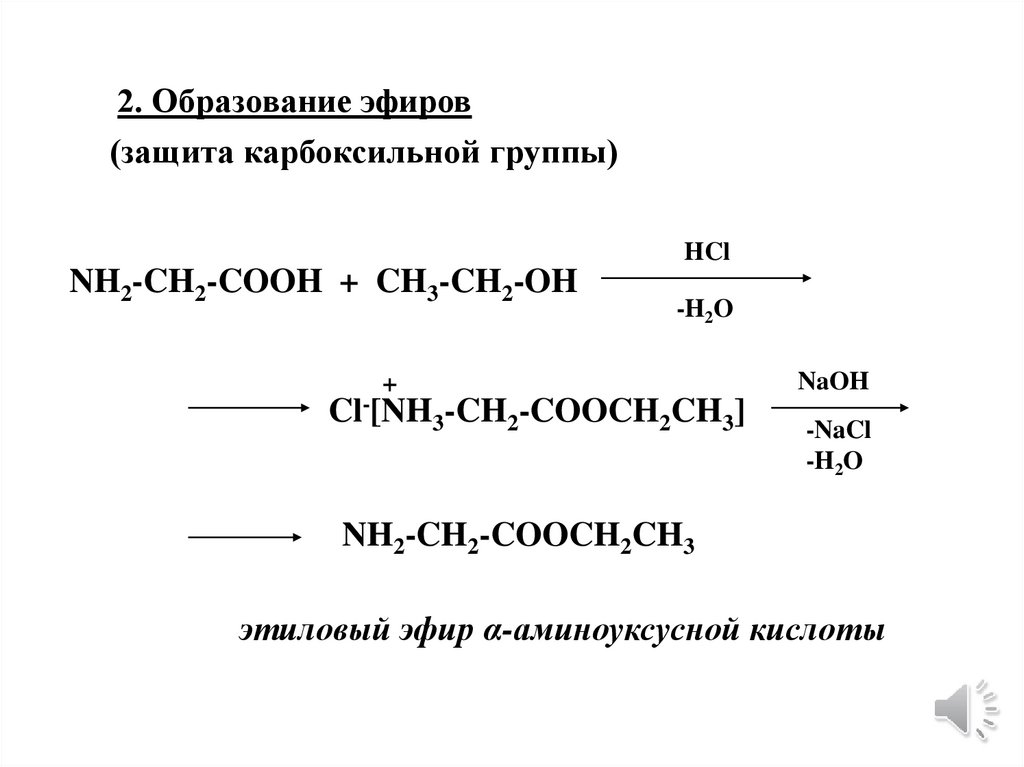
17.
2. Образование эфиров(защита карбоксильной группы)
HCl
NH2-CH2-COOH + CH3-CH2-OH
-H2O
+
Cl-[NH3-CH2-COOCH2CH3]
NaOH
-NaCl
-H2O
NH2-CH2-COOCH2CH3
этиловый эфир α-аминоуксусной кислоты
18.
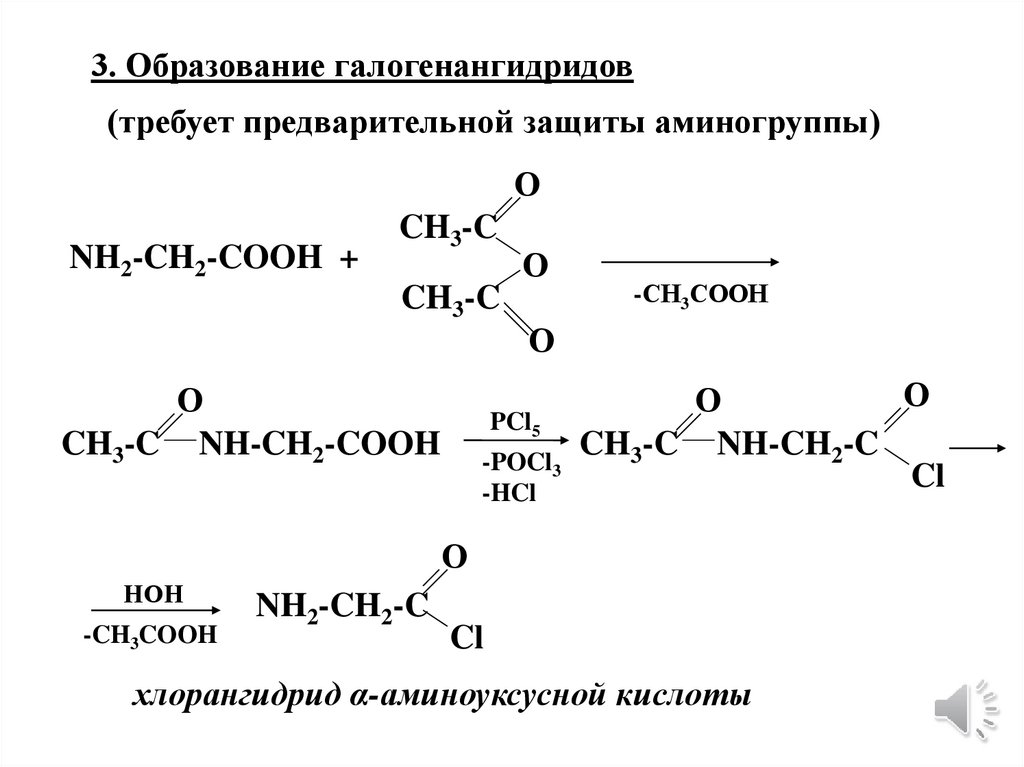
3. Образование галогенангидридов(требует предварительной защиты аминогруппы)
О
NH2-CH2-COOH +
CH3-C
CH3-C
О
-СН3СООН
О
О
О
PCl5
CH3-C NH-CH2-C
-POCl3
Cl
-HCl
О
CH3-C NH-CH2-COOH
О
НОН
-CH3COOH
NH2-CH2-C
Cl
хлорангидрид α-аминоуксусной кислоты
19.
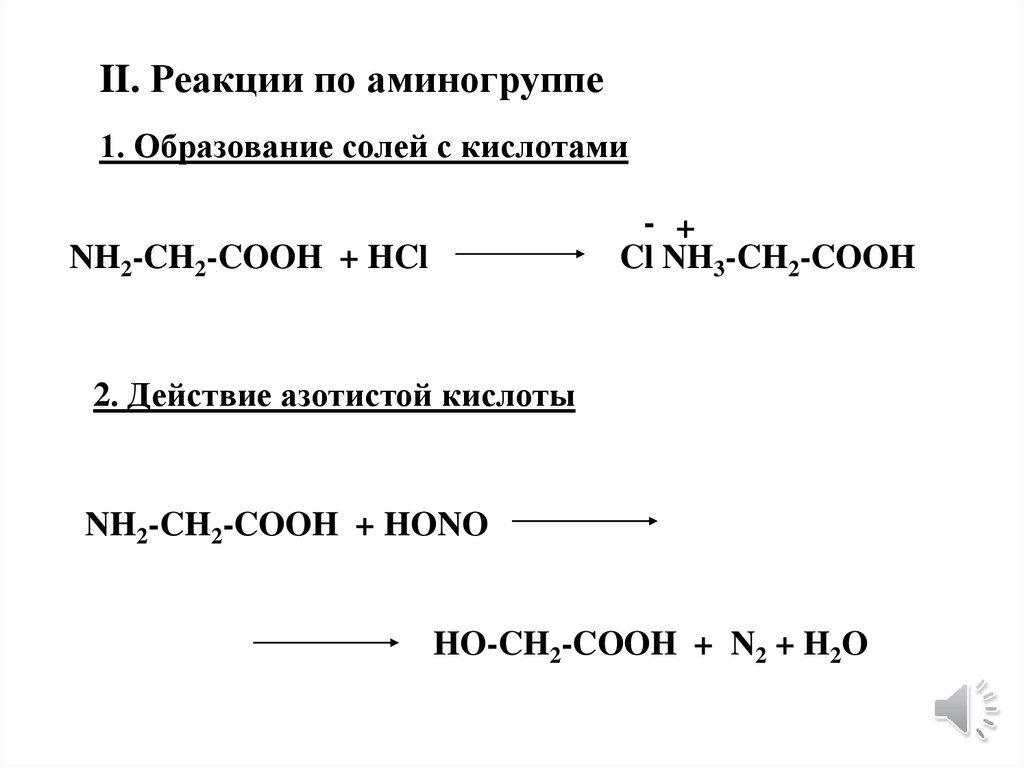
II. Реакции по аминогруппе1. Образование солей с кислотами
- +
Cl NH3-CH2-COOH
NH2-CH2-COOH + HCl
2. Действие азотистой кислоты
NH2-CH2-COOH + HONO
HO-CH2-COOH + N2 + H2O
20.
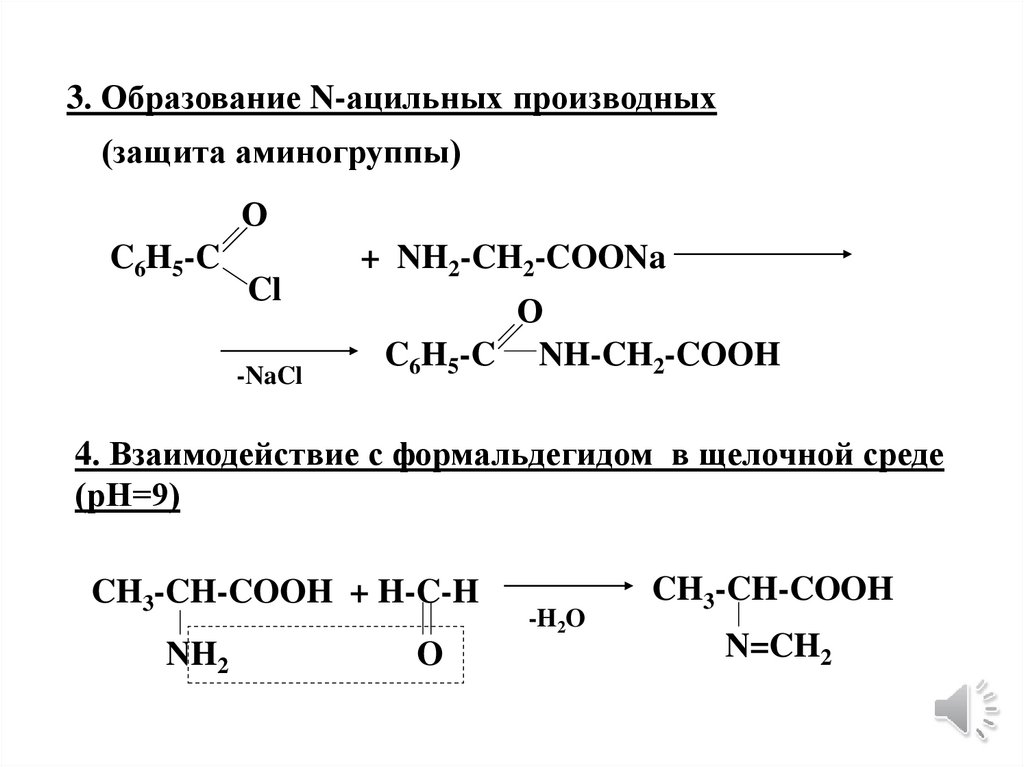
3. Образование N-ацильных производных(защита аминогруппы)
О
C6H5-C
Cl
-NaCl
+ NH2-CH2-COONa
О
C6H5-C NH-CH2-COOH
4. Взаимодействие с формальдегидом в щелочной среде
(рН=9)
CH3-CH-COOH + H-C-H
NH2
O
-H2O
CH3-CH-COOH
N=CH2
21.
III. Реакции, характерные для α-аминокислот1. Декарбоксилирование
декарбоксилаза
R-CH-COOH
R-CH2-NH2 + CO2
амин
NH2
2. Дезаминирование
R-CH-COOH
O
[O]
-NH3
NH2
3. Переаминирование
R-C-COOH
α-оксокислота
O
R-CH-COOH + R’-C-COOH
NH2
O
R-C
H
+CO2
O
ферменты
R-C-COOH
+
R’-CH-COOH
NH2
22.
4. Реакция с нингидриномО
О
Н
ОН
ОН
NH2
О
нингидрин
О
О
О
N
О
О
О
О
+ NH3 +
H
О
+ NH3
гидриндантин
+CO2
Н
ОН
ОН
ОН
+
+ R-C
О
R-CH-COOH +
O
ОН
+ 3H2O
сине-фиолетовое
окрашивание
23.
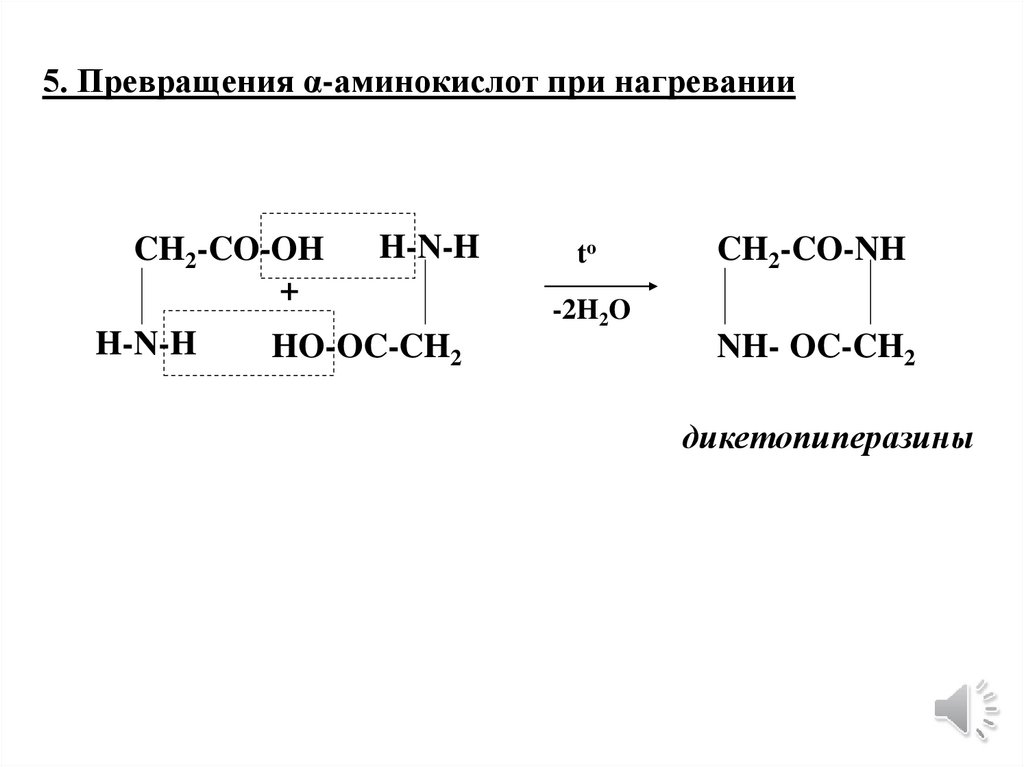
5. Превращения α-аминокислот при нагреванииCH2-CO-OH
+
H-N-H
H-N-H
HO-OC-CH2
to
CH2-CO-NH
-2H2O
NH- OC-CH2
дикетопиперазины
24.
6. Образование пептидной связиO
O
CH3-CH-C-OH + H-N-CH2-C-OH
NH2
аланин
H
-Н2О
глицин
O
-O
C- N-CH
CH3-CH-CN- 2-C-OH
NH2 H
пептидная связь
ди пептид
* А.Я.Данилевский (1891 г.)
25.
Полипептид – пептид, содержащий более10 аминокислотных звеньев
Белок – пептид, содержащий более
50 аминокислотных остатков
O
O
CH3-CH-C- N-CH2-C-OH
NH2 H
аланил
аланин
глицин
Ala-Gly
26.
трипептидС-концевая
аминокислота
N-концевая
аминокислота
O
O
H2N-CH-C-NH-CH-C-NH-CH-COOH
CH2
CH3
CH2
OH
серил аланил фенилаланин
Ser- Ala- Phe
27.
Национальный исследовательский университетРоссийский государственный университет нефти и газа (НИУ)
имени И. М. Губкина
Спасибо за внимание
Иванова Людмила Вячеславовна
профессор
кафедры органической химии и химии нефти
e-mail: ivanova.l@gubkin.ru
Москва, 2020




















 Химия
Химия