Похожие презентации:
Химические формулы. 8 класс
1. Химические формулы 8 класс
2.
3.
В химии при письме вместоназваний используют формулы
веществ.
Как вы думаете, почему?
4.
Формулы веществ записыватьбыстрее,
они занимают мало место
и несут много информации.
Наша задача сегодня – узнать,
что такое химические формулы
и научиться видеть ту
информацию, которую они
содержат
5.
Химическаяформула - это
условная запись состава вещества с
помощью
химических знаков
и индексов
6.
химическиезнаки
индекс
О
Н
Н
показывает
количество
атомов в
молекуле
7.
Информация, которую содержатхимические формулы:
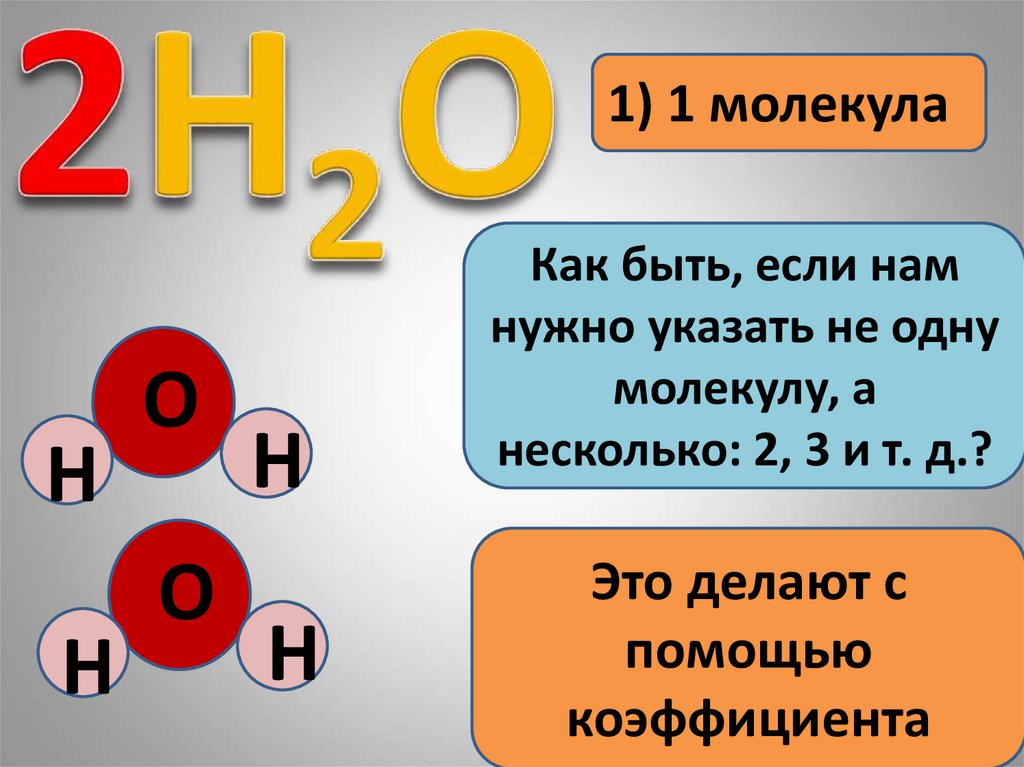
1) 1 молекула
8.
1) 1 молекулаН
Н
О
О
Н
Н
Как быть, если нам
нужно указать не одну
молекулу, а
несколько: 2, 3 и т. д.?
Это делают с
помощью
коэффициента
9.
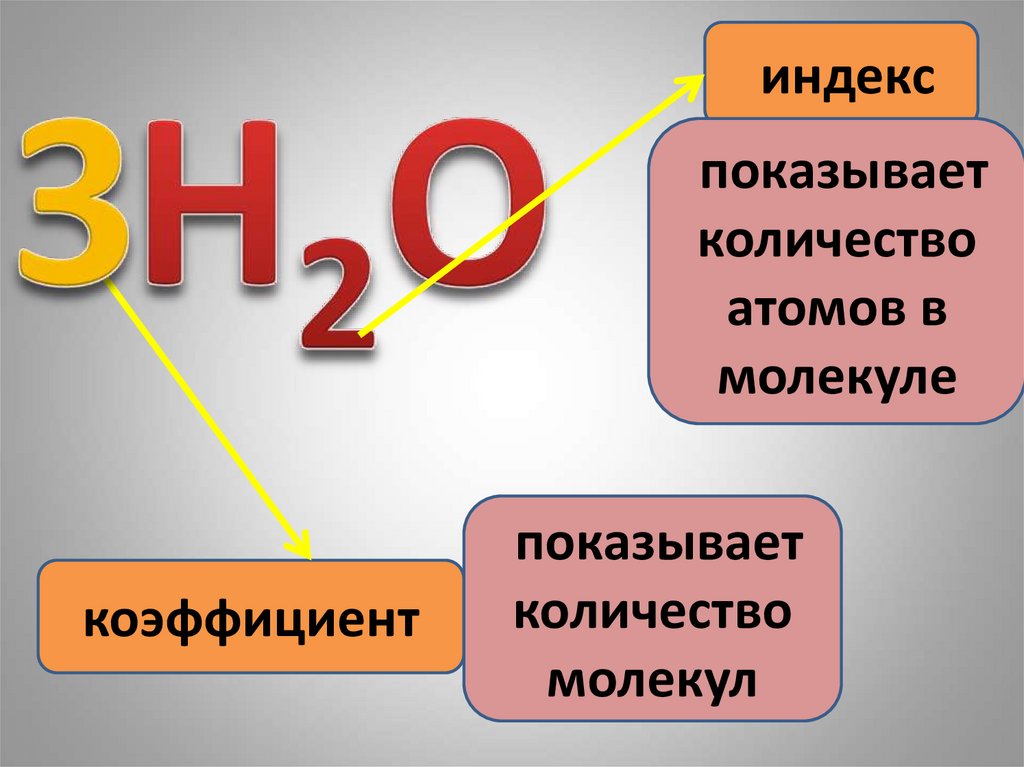
индекспоказывает
количество
атомов в
молекуле
коэффициент
показывает
количество
молекул
10.
25/10/22II. Чтение химических формул.
Примеры:
1. NH3 – молекула эн аш три
состоит из одного атома азота и трех атомов водорода.
2. Al(OH)3 – молекула алюминий о аш трижды
состоит из одного атома алюминия,
кислорода и трех атомов водорода.
трех атомов
3. K3BO3 – молекула калий три бор о три
трех атомов калия,
атомов кислорода.
C
(NH
P
Fe
BaCO
Na
O
SO
)
PO
KHCO
PbSiO
AlCl
CH
ZnMnO
Ca(OH)
AgNO
COOH
82H
232O
18
4
5
3
3
3
3 3442 4
одного атома
состоит из
бора и трех
11.
1. В записи 5SO3 коэффициент равен:б) 15;
а) 5;
в) 3;
г) коэффициент отсутствует.
2. В записи 5SO3 индекс равен:
а) 5;
б) 15;
в) 3;
г) индекс отсутствует.
12.
3. В записи СO2коэффициент равен:б) 3;
а) 1;
в) 2;
г) коэффициент отсутствует.
3. В записи MgO индекс равен:
б) 0;
а) 1;
в) 2;
г) индекс отсутствует.
13.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
14.
2) Название вещества3) Качественный состав
вода
Состоит из
водорода и
кислорода
15.
2) Название вещества3) Качественный состав
углекислый газ
состоит из
углерода и
кислорода
16.
2) Название веществакислород
3) Качественный
состав
состоит из
кислорода
17.
2) Название вещества3) Качественный состав
это вещество
состоит из
алюминия и
кислорода
18.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
4) Количественный состав
19.
1) 1 молекула2) Название вещества
воды
4) Количественный
состав
Состоит из двух
атомов водорода и
одного атома
кислорода
20.
1) 1 молекула2) Название вещества
углекислого газа
4) Количественный
состав
состоит из одного
атома углерода и двух
атомов кислорода
21.
1) 1 молекула2) Название вещества
кислорода
4) Количественный
состав
состоит из двух
атомов кислорода
22.
1) 1 молекула2) Название вещества
этого вещества
4) Количественный
состав
состоит из двух атомов
алюминия и трех
атомов кислорода
23.
1.Сколько молекул серной кислоты записано?2.Сколько атомов водорода записано?
3.Сколько атомов серы записано?
4.Сколько атомов кислорода записано?
5.Сколько всего атомов?
24.
Когда мы знакомились с элементами, тоузнали, что для измерения масс атомов
ввели новую физическую величину. Какую?
Буква Физическая величина Единица измер.
А
Относительная
r атомная масса
-
Как мы узнаем значение относительных
атомных масс элементов?
Из таблицы Менделеева
25.
Зная массы атомов, по химической формулеможно найти массу молекулы, которую
назвали
Буква
Физическая величина
Единица
измерения
Относительная
r молекулярная масса
-
М
То есть с помощью химической формулы
мы можем получить 5-ый вид информации
Относительную молекулярную массу
26.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
4) Количественный состав
5) Относительная молекулярная масса
27.
Чтобы найти относительную молекулярнуюмассу вещества, надо сложить
относительные атомные массы элементов
Аr(О)= 16
Аr(Н)= 1
Мr(Н2О)= 2*1 + 16 =18
28. Относительная молекулярная масса -Мr
Относительная молекулярная масса -Мr
Mr (CO2)=
Ar (C)+Ar (O)×2 =12+16×2=12 +32 = 44
29.
Найдите относительнуюмолекулярную массу углекислого
газа
Мr(СО2)=12 + 2*16= 44
30.
Найдите относительные молекулярные массы следующих веществ:1) кислорода О2 Мr(О2)=2*16= 32
2) аммиака NH3 Мr(NH3)=14+3*1=17
Мr(Аl2О3)=2*27+3*16=102
3) Оксида алюминия
Аl2О3
Мr(H2SO4)=2*1+32+4*16=98
4) серной кислоты
H2SO4
Мr(HСl)=1+35,5=36,5
5) соляной кислоты
HСl
6) Поваренной М
соли
NaСl
r(NaСl)=23+35,5=58,5
31. Рассчитайте
• Мr (H2) =• Mr (СаСl2) =
• Mr (CaCO3) =
• Мr (Ca(OH)2)=
• Mr (СН3СООН)=
• Мr (Ca3(PO4)2)=
1× 2 =2
40+35,5×2=111
40+12+16×3=100
40+16×2+1×2 =74
12×2+1×4+16×2=60
40×3+31×2+16×8 =
=120+62+128=310
32.
САМОСТОЯТЕЛЬНАЯ РАБОТАMr (Н2SO4)
98
Mr (Н3РO4)
Mr (SO3)
80
Mr (MgO)
5 Mr (CH4)
80
2 Mr (NaOH)
17
Mr (PH3)
Mr (NH3)
98
40
80
34































 Химия
Химия








