Похожие презентации:
Химические формулы
1.
Химические формулы2.
В химии при письме вместоназваний используют формулы
веществ.
Как вы думаете, почему?
3.
Формулы веществ записыватьбыстрее,
они занимают мало место
и несут много информации.
Наша задача сегодня – узнать,
что такое химические формулы
и научиться видеть ту
информацию, которую они
содержат
4.
Химическаяформула - это
условная запись состава вещества с
помощью
химических знаков
и индексов
5.
химическиезнаки
индекс
Н
О
Н
показывает
количество
атомов в
молекуле
6.
Информация, которую содержатхимические формулы:
1) 1 молекула
7.
1) 1 молекулаН
Н
О
О
Н
Н
Как быть, если нам
нужно указать не одну
молекулу, а несколько:
2, 3 и т. д.?
Это делают с
помощью
коэффициента
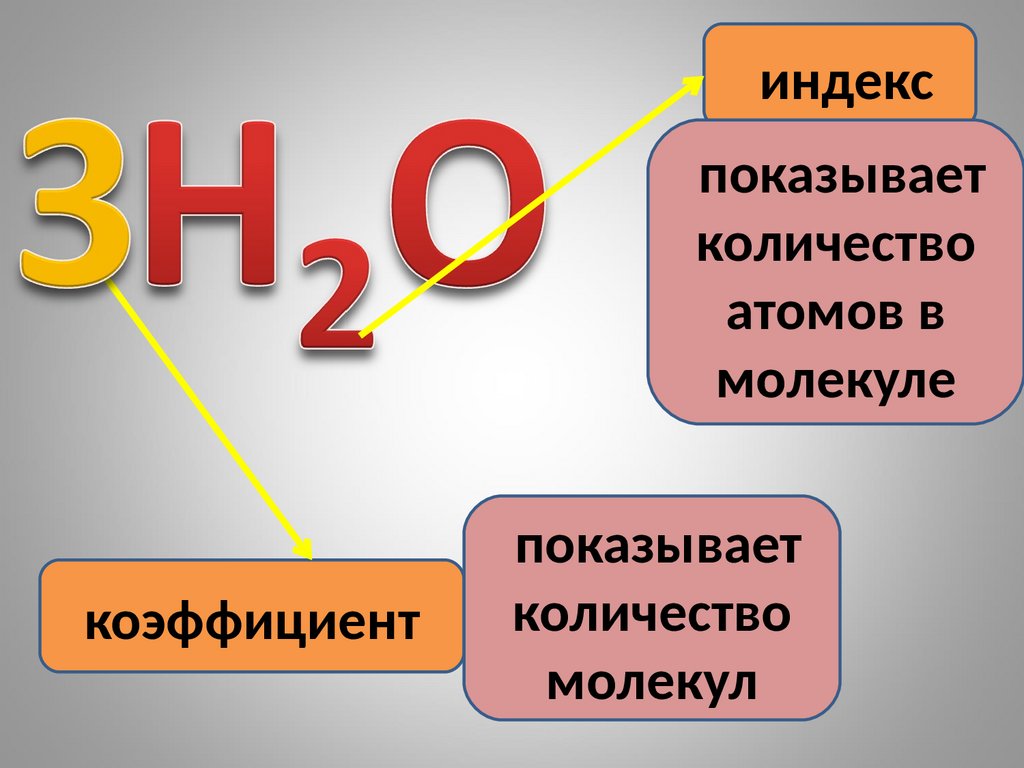
8.
индекспоказывает
количество
атомов в
молекуле
коэффициент
показывает
количество
молекул
9.
1. В записи 5SO3 коэффициент равен:а) 5;
б) 15;
в) 3;
г) коэффициент отсутствует.
2. В записи 5SO3 индекс равен:
а) 5;
б) 15;
в) 3;
г) индекс отсутствует.
10.
3. В записи СO2коэффициент равен:а) 1;
б) 3;
в) 2;
г) коэффициент отсутствует.
3. В записи MgO индекс равен:
б) 0;
а) 1;
в) 2;
г) индекс отсутствует.
11.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
12.
2) Название вещества3) Качественный состав
вода
Состоит из
водорода и
кислорода
13.
2) Название вещества3) Качественный состав
Оксид алюминия
состоит из
алюминия и
кислорода
14.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
4) Количественный состав
15.
1) 1 молекула2) Название вещества
воды
4) Количественный
состав
Состоит из двух
атомов водорода и
одного атома
кислорода
16.
1) 1 молекула2) Название вещества
4) Количественный
состав
Оксид алюминия
состоит из двух атомов
алюминия и трех атомов
кислорода
17.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
4) Количественный состав
5) Относительная молекулярная масса
18.
Чтобы найти относительную молекулярнуюмассу вещества, надо сложить
относительные атомные массы элементов
Аr(О)= 16
Аr(Н)= 1
Мr(Н2О)= 2*1 + 16 =18
19.
Найдите относительнуюмолекулярную массу углекислого
газа
Мr(СО2)=12 + 2*16= 44
20.
Найдите относительные молекулярные массы следующих веществ:1) кислорода О2 Мr(О2)=2*16= 32
2) аммиака NH3 Мr(NH3)=14+3*1=17
Мr(Аl2О3)=2*27+3*16=102
3) Оксида алюминия
Аl2О3
Мr(H2SO4)=2*1+32+4*16=98
4) серной кислоты
H2SO4
Мr(HСl)=1+35,5=36,5
5) соляной кислоты
HСl
6) Поваренной М
соли
NaСl
(NaСl)=23+35,5=58,5
r
21.
Рассчитайте• Мr (H2) =
• Mr (СаСl2) =
• Mr (CaCO3) =
• Мr (Ca(OH)2)=
• Mr (СН3СООН)=
• Мr (Ca3(PO4)2)=
1× 2 =2
40+35,5×2=111
40+12+16×3=100
40+16×2+1×2 =74
12×2+1×4+16×2=60
40×3+31×2+16×8 =
=120+62+128=310
22.
23.
Мы знаем, что вещества состоят измолекул , а молекулы из атомов.
Чтобы атомы оставались вместе,
образуя молекулу, их должна
удерживать сила. Эту силу назвали
химической связью.
которая
Химическая
связь
- это сила,
А способность
элемента
образовывать
удерживает
атомы
в молекуле.
лллллллллллллллллллллллллллллллллл
определенное
количество
связей назвали
лллллллллллллллллллллллллллллллл
валентностью.
24.
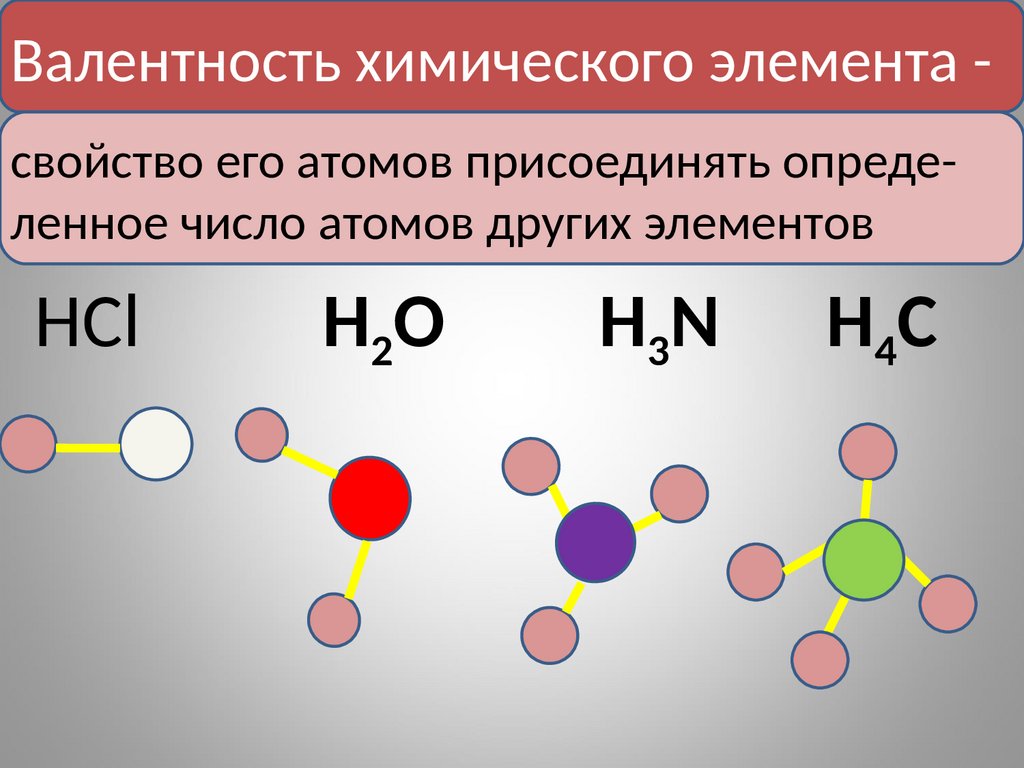
Валентность химического элемента свойство его атомов присоединять определенное число атомов других элементовHCl
H2O
H3N
H4C
25.
Определитевалентность
натрия, бора,
Как же можно
узнать валентность
элемента?
углерода, кислорода, хлора, кальция,
алюминия,
серы,
магния и азота
Очень просто!
Из фосфора,
таблицы Менделеева!
Валентность элемента совпадает с номером группы
26.
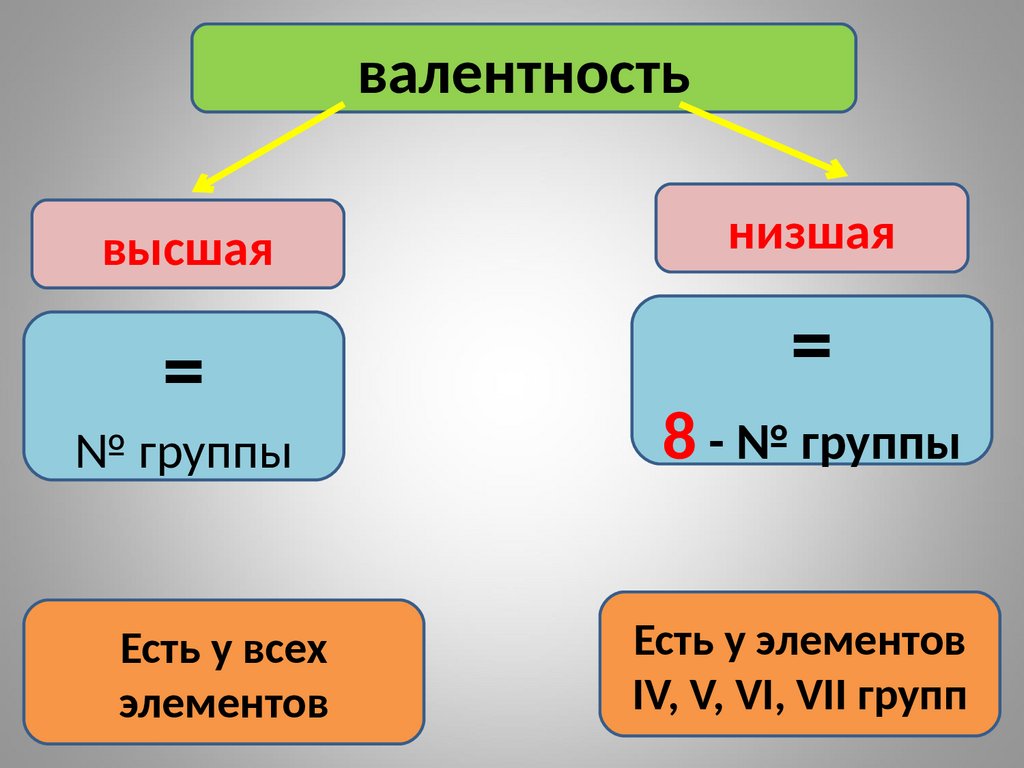
валентностьвысшая
=
№ группы
Есть у всех
элементов
низшая
=
8 - № группы
Есть у элементов
IV, V, VI, VII групп
27.
Как узнать, когда элемент обладаетвысшей валентностью, а когда
низшей?
Для этого вводят еще одно свойство
атомов – электроотрицательность.
Значения электроотрицательности
атомов элементов мы будем брать из
таблицы
28.
Договорились, что при составленииформул элемент с большей электроотрицательностью надо записывать
справа, а с меньшей - слева
Т.е справа записывают элемент,
который имеет низшую валентность, а
слева - высшую
29.
1.1.Рядом записываем знаки химическихэлементов.
2.2.Определяем валентность элементов:
У элемента,
который
записан
слева – она
высшая и
=№ группы
4.Считаем индексы:
У элемента,
который
записан справа
– она низшая и
=8 - №
группы
30.
слеваменее
электроотрицательный
3III
справа
более
электроотрицательный
II 2
Аl низшая
=
= O
№ группы
8 - № группы
высшая



























 Химия
Химия








