Похожие презентации:
Химические формулы. 8 класс
1. Химические формулы 8 класс
Кривошапкина В. В.Учитель химии, биологии
МОУ «СОШ № 1»
Г.Котлас
2.
14/09/21Проверка знаний:
Знаки химических элементов.
I
FeZn
P
Cu
Br
Ba
b
Hg
Al
C
B
Na
O
Ag
Ca
FH
K
Sl N
Si Au
- название
- произношение
3.
4.
В химии при письме вместоназваний используют формулы
веществ.
Как вы думаете, почему?
5.
Формулы веществ записыватьбыстрее,
они занимают мало место
и несут много информации.
Наша задача сегодня – узнать,
что такое химические формулы
и научиться видеть ту
информацию, которую они
содержат
6.
Химическаяформула - это
условная запись состава вещества с
помощью
химических знаков
и индексов
7.
химическиезнаки
индекс
О
Н
Н
показывает
количество
атомов в
молекуле
8.
Информация, которую содержатхимические формулы:
1) 1 молекула
9.
1) 1 молекулаН
Н
О
О
Н
Н
Как быть, если нам
нужно указать не одну
молекулу, а
несколько: 2, 3 и т. д.?
Это делают с
помощью
коэффициента
10.
индекспоказывает
количество
атомов в
молекуле
коэффициент
показывает
количество
молекул
11.
Соотнеситепонятия:
индекс
коэффициент
показывает
количество
молекул
показывает
количество
атомов в
молекуле
12.
14/09/21II. Чтение
химических формул.
Примеры:
1. NH3 – молекула эн аш три
состоит из одного атома азота и трех атомов водорода.
2.
Al(OH)3 – молекула алюминий о аш трижды
состоит из одного атома алюминия,
трех атомов
кислорода и трех атомов водорода.
3.
K3BO3 – молекула калий три бор о три состоит из
трех атомов калия, одного атома бора и трех
атомов кислорода.
C
(NH
P
Fe
BaCO
Na
O
SO
)
PO
KHCO
PbSiO
AlCl
CH
ZnMnO
Ca(OH)
AgNO
COOH
82H
232O
18
4
5
3
3
3
3 3442 4
13.
1. В записи 5SO3 коэффициент равен:б) 15;
а) 5;
в) 3;
г) коэффициент отсутствует.
2. В записи 5SO3 индекс равен:
а) 5;
б) 15;
в) 3;
г) индекс отсутствует.
14.
3. В записи СO2коэффициент равен:б) 3;
а) 1;
в) 2;
г) коэффициент отсутствует.
3. В записи MgO индекс равен:
б) 0;
а) 1;
в) 2;
г) индекс отсутствует.
15.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
16.
2) Название вещества3) Качественный состав
вода
Состоит из
водорода и
кислорода
17.
2) Название вещества3) Качественный состав
углекислый газ
состоит из
углерода и
кислорода
18.
2) Название веществакислород
3) Качественный
состав
состоит из
кислорода
19.
2) Название вещества3) Качественный состав
это вещество
состоит из
алюминия и
кислорода
20.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
4) Количественный состав
21.
1) 1 молекула2) Название вещества
4) Количественный
состав
воды
Состоит из двух
атомов водорода и
одного атома
кислорода
22.
1) 1 молекула2) Название вещества
4) Количественный
состав
углекислого газа
состоит из одного
атома углерода и двух
атомов кислорода
23.
1) 1 молекула2) Название вещества
4) Количественный
состав
кислорода
состоит из двух
атомов кислорода
24.
1) 1 молекула2) Название вещества
4) Количественный
состав
этого вещества
состоит из двух атомов
алюминия и трех
атомов кислорода
25.
1.Сколько молекул серной кислоты записано?2.Сколько атомов водорода записано?
3.Сколько атомов серы записано?
4.Сколько атомов кислорода записано?
5.Сколько всего атомов?
26.
Когда мы знакомились с элементами, тоузнали, что для измерения масс атомов
ввели новую физическую величину. Какую?
Буква Физическая величина Единица измер.
А
Относительная
r атомная масса
-
Как мы узнаем значение относительных
атомных масс элементов?
Из таблицы Менделеева
27.
Зная массы атомов, по химической формулеможно найти массу молекулы, которую
назвали
Буква
Физическая величина
Единица
измерения
Мr
Относительная
молекулярная масса
-
То есть с помощью химической формулы
мы можем получить 5-ый вид информации
Относительную молекулярную массу
28.
Информация, которую содержатхимические формулы:
1) 1 молекула
2) Название вещества
3) Качественный состав
4) Количественный состав
5) Относительная молекулярная масса
29.
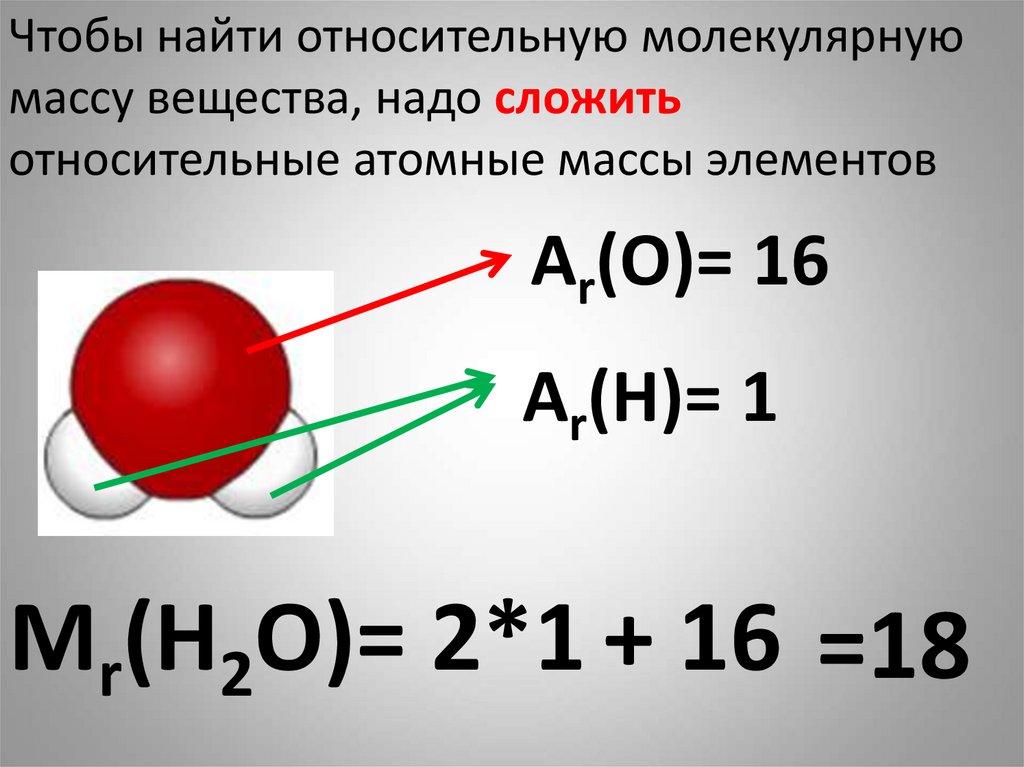
Чтобы найти относительную молекулярнуюмассу вещества, надо сложить
относительные атомные массы элементов
Аr(О)= 16
Аr(Н)= 1
Мr(Н2О)= 2*1 + 16 =18
30. Относительная молекулярная масса -Мr
Относительная молекулярная масса -Мr
Mr (CO2)=
Ar (C)+Ar (O)×2 =12+16×2=12 +32 = 44
31.
Найдите относительнуюмолекулярную массу углекислого
газа
Мr(СО2)=12 + 2*16= 44
32.
Найдите относительные молекулярные массы следующих веществ:1) кислорода О2 Мr(О2)=2*16= 32
2) аммиака NH3 Мr(NH3)=14+3*1=17
Мr(Аl2О3)=2*27+3*16=102
3) Оксида алюминия
Аl2О3
Мr(H2SO4)=2*1+32+4*16=98
4) серной кислоты
H2SO4
Мr(HСl)=1+35,5=36,5
5) соляной кислоты
HСl
6) Поваренной М
соли
NaСl
r(NaСl)=23+35,5=58,5
33. Рассчитайте
Мr (H2) =
Mr (СаСl2) =
Mr (CaCO3) =
Мr (Ca(OH)2)=
Mr (СН3СООН)=
Мr (Ca3(PO4)2)=
1× 2 =2
40+35,5×2=111
40+12+16×3=100
40+16×2+1×2 =74
12×2+1×4+16×2=60
40×3+31×2+16×8 =
=120+62+128=310
34.
САМОСТОЯТЕЛЬНАЯ РАБОТАMr (Н2SO4)
98
Mr (Н3РO4)
Mr (SO3)
80
Mr (MgO)
5 Mr (CH4)
80
2 Mr (NaOH)
17
Mr (PH3)
Mr (NH3)
98
40
80
34

































 Химия
Химия








