Похожие презентации:
Алканы. Химические свойства
1.
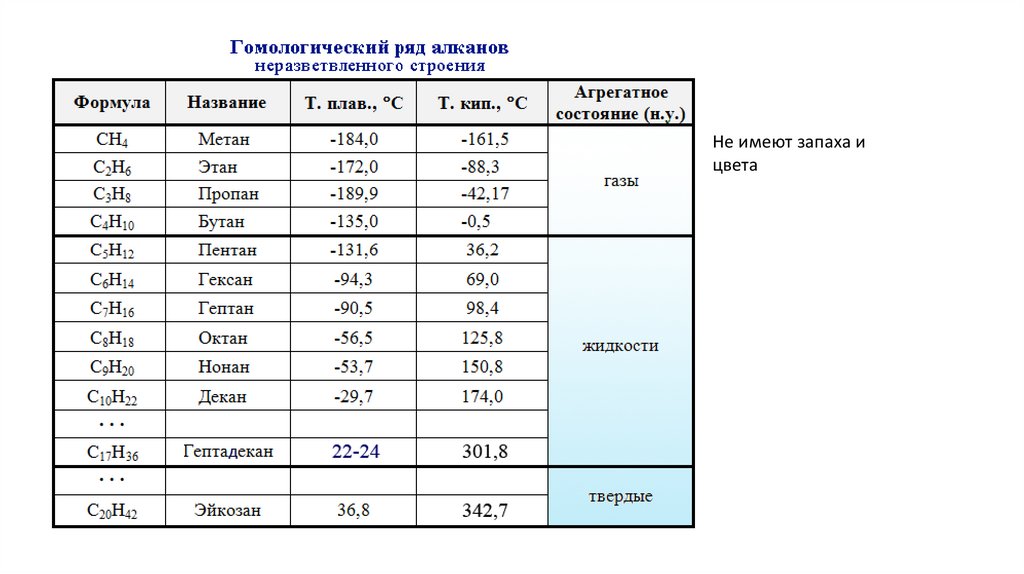
Алканы- Ацеклические углеводороды, с общей формулой : CnH2n+2
2.
Не имеют запаха ицвета
3.
Изомерия• Углеродного скелета
4.
Получение• 1. Основной источник: природные и газы и нефть. В
промышленности углеводороды получают перегонкой
нефтепродуктоы.
• 2. Прямой синтез:
5.
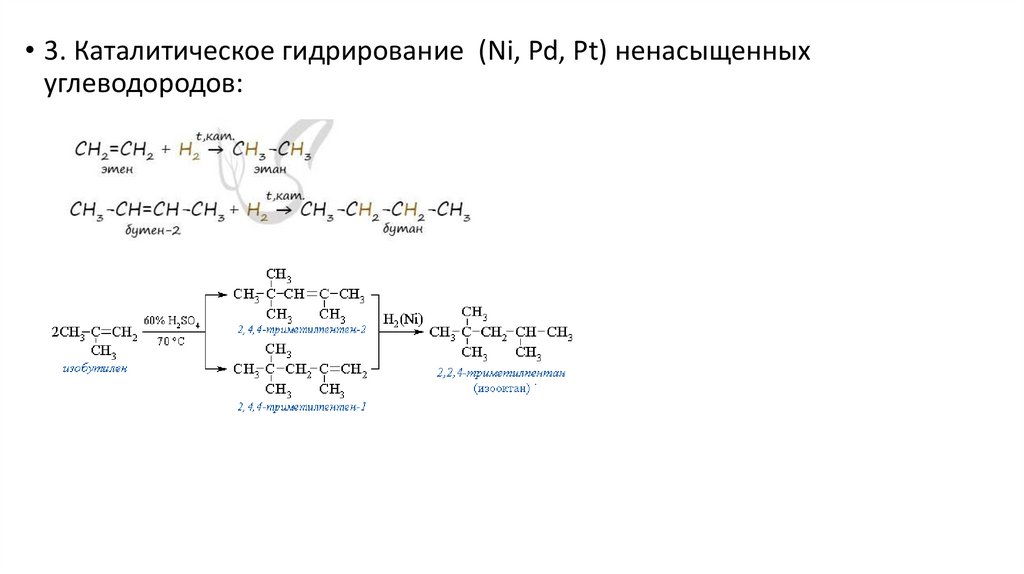
• 3. Каталитическое гидрирование (Ni, Pd, Pt) ненасыщенныхуглеводородов:
6.
• 4. Реакция Вюрца ( увеличение углеводородной цепи)7.
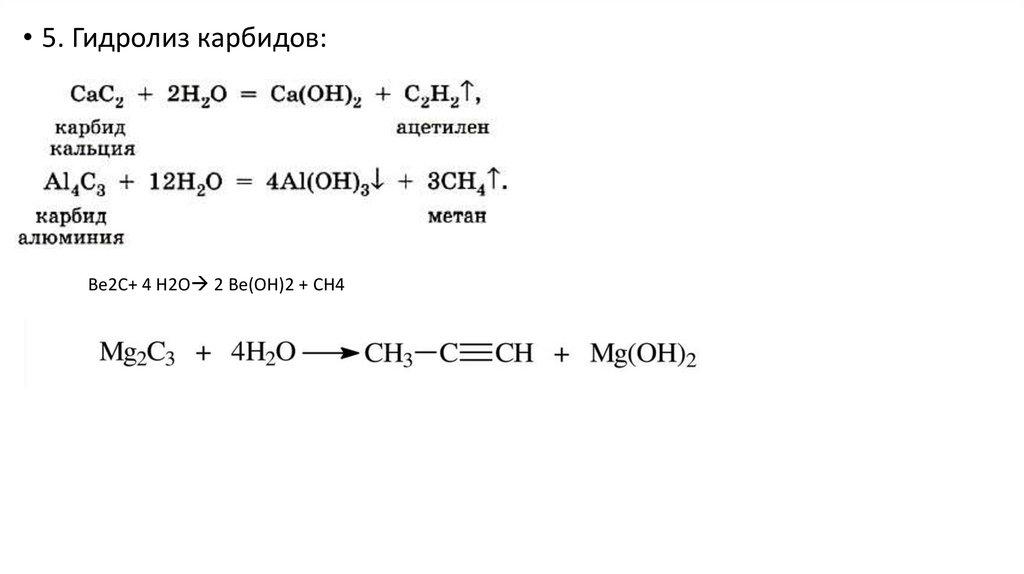
• 5. Гидролиз карбидов:Be2C+ 4 H2O 2 Be(OH)2 + CH4
8.
• 6. Пиролиз натриевых солей к.к ( или, реакция Дюма)9.
• 7. Синтез Кольбе ( Электролиз солей к.к)10.
Химические свойства• В молекулах алкана соедржатся только малополярные и
неполярные прочные Ϭ- связи, поэтому этот класс углеводородов
очень малоактивен и может вступать в химические реакции либо
с очень активными реагентами, либо в очень жестких условиях.
11.
• 1.Галогенирование ( р-я радикального замещения, протекающаяпо цепному механизму)
12.
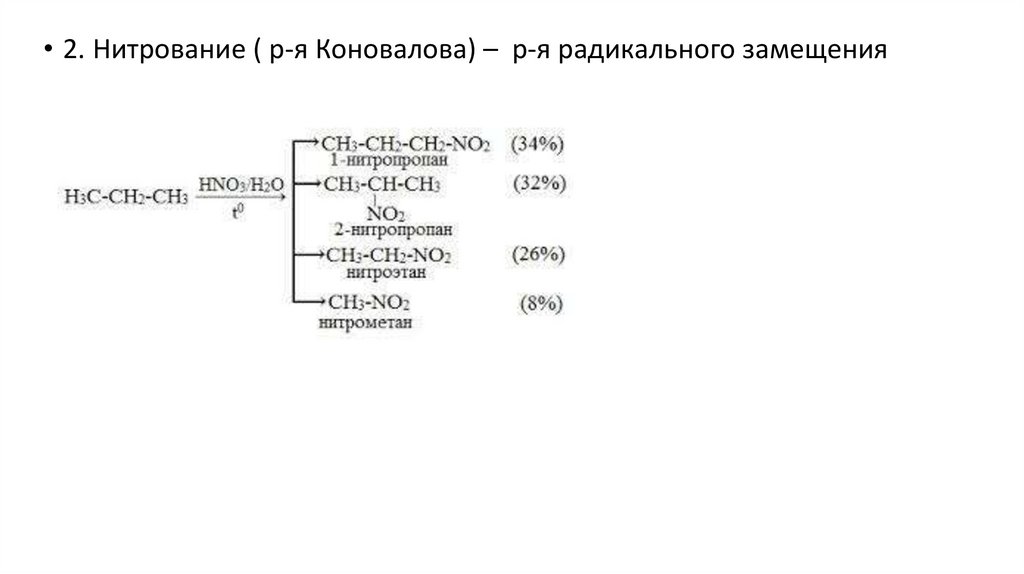
• 2. Нитрование ( р-я Коновалова) – р-я радикального замещения13.
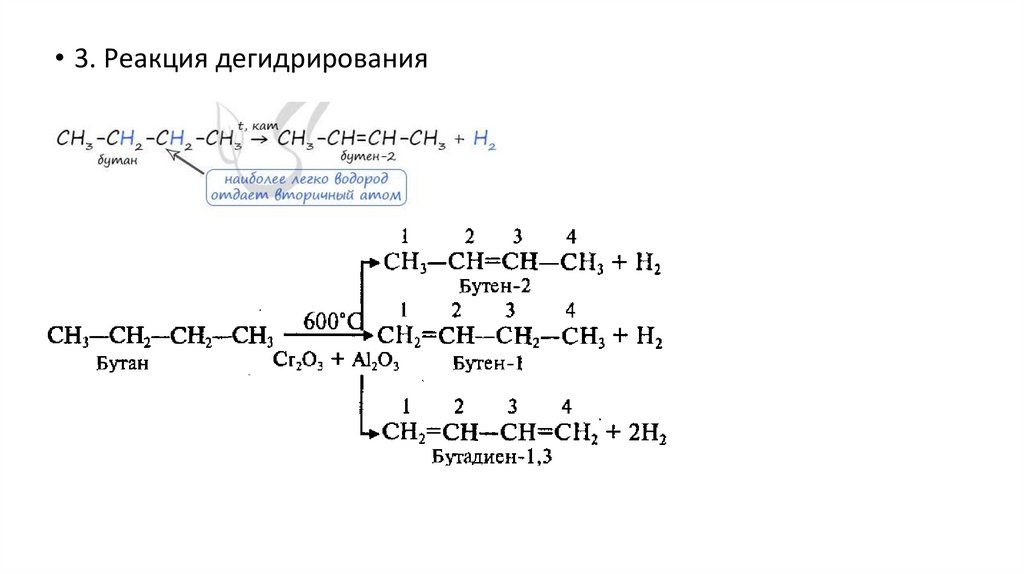
• 3. Реакция дегидрирования14.
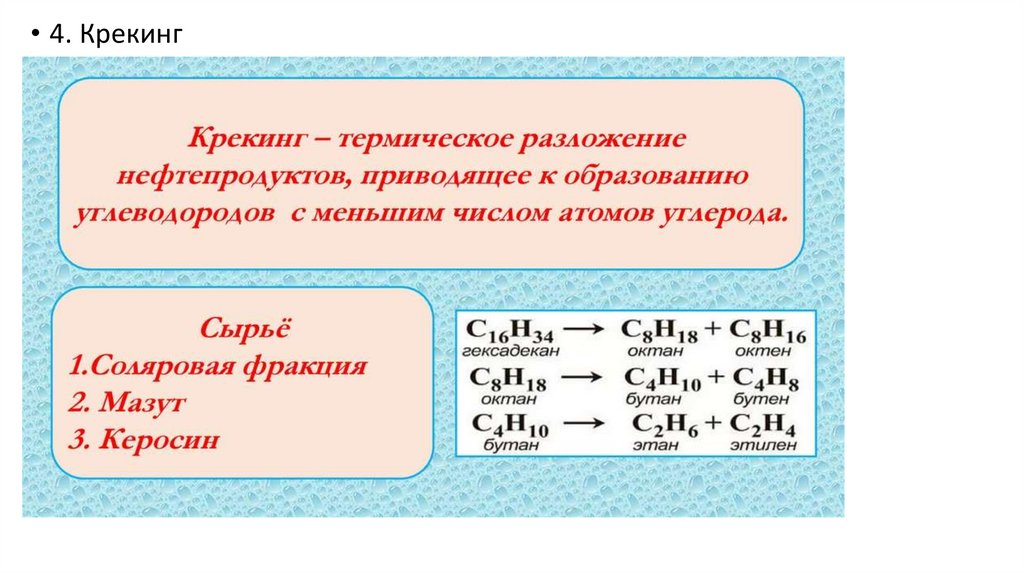
• 4. Крекинг15.
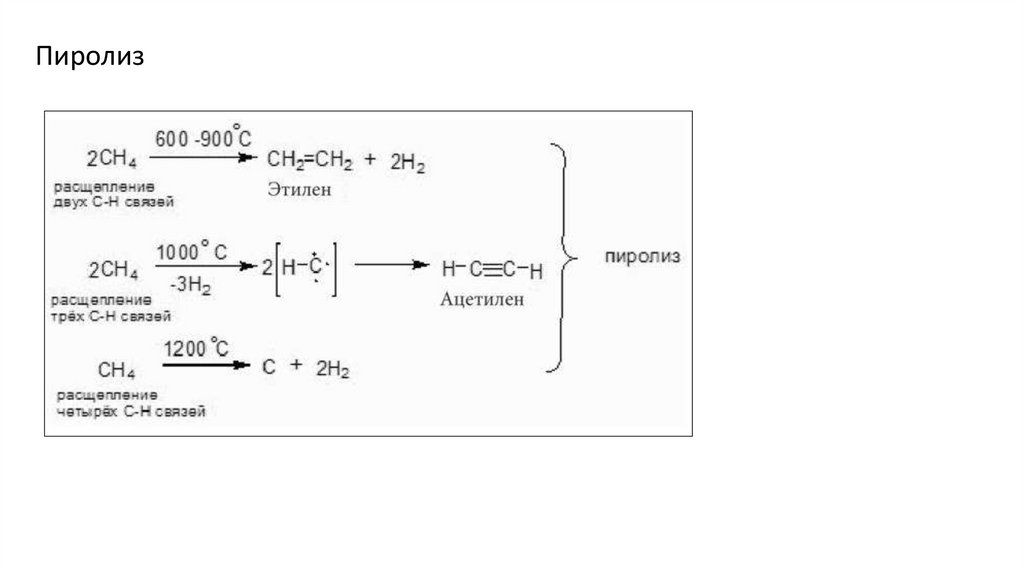
Пиролиз16.
• 5. Реакция каталитического окисления• Окисление бутана в присутствии кат при t используется в пром
для пол уксусной к-ты
• Оx метана в зависимости от ( kat, t, P, oкислителя) может
приводить к образованию различных продуктов.
• Реакция окисления метана водой или CO2 называются
конверсией метана:
Смесь полученная
называется – синтез –
газ
17.
• Высокотемпературное или каталитическое оксление метана приочень высоких P и большом избытке метана позволяет получить
метанол:
При небольшое Р и большом кол-ве
кислорода + кат оксид металла
При использовании в качестве
катализатора Pd, Pt и еще
большем кол-ве O2
18.
• 6. Реакция горения19.
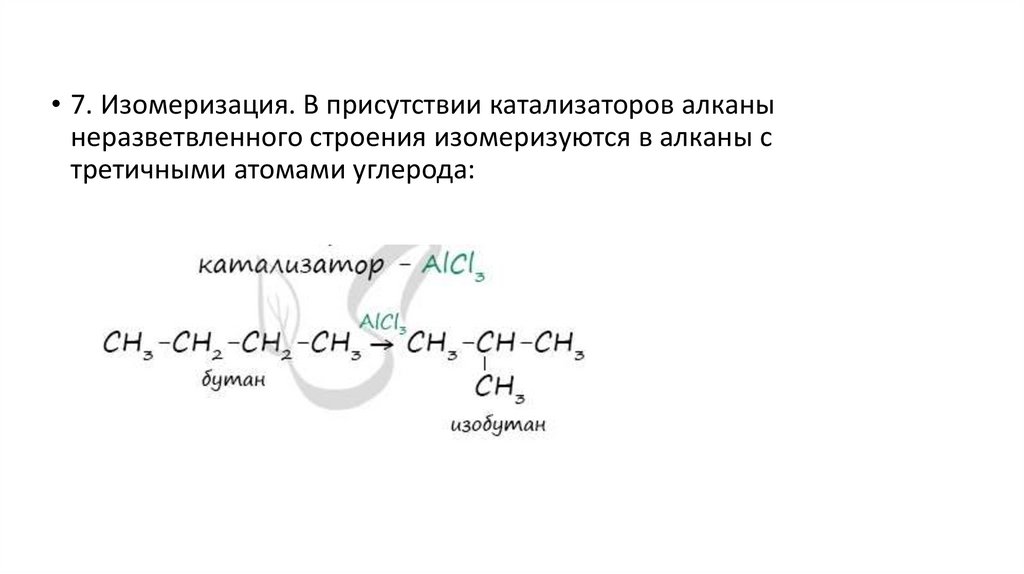
• 7. Изомеризация. В присутствии катализаторов алканынеразветвленного строения изомеризуются в алканы с
третичными атомами углерода:










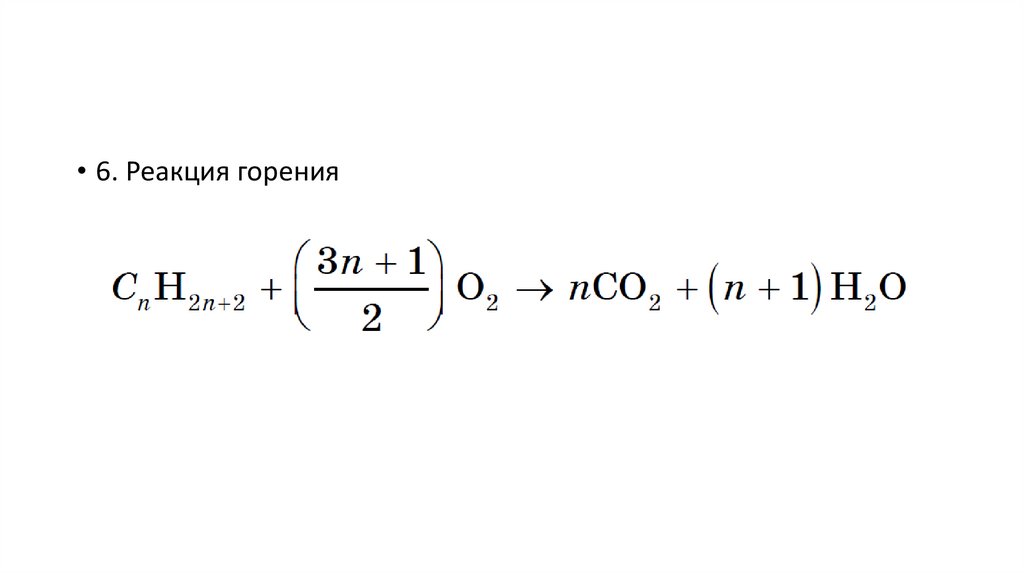
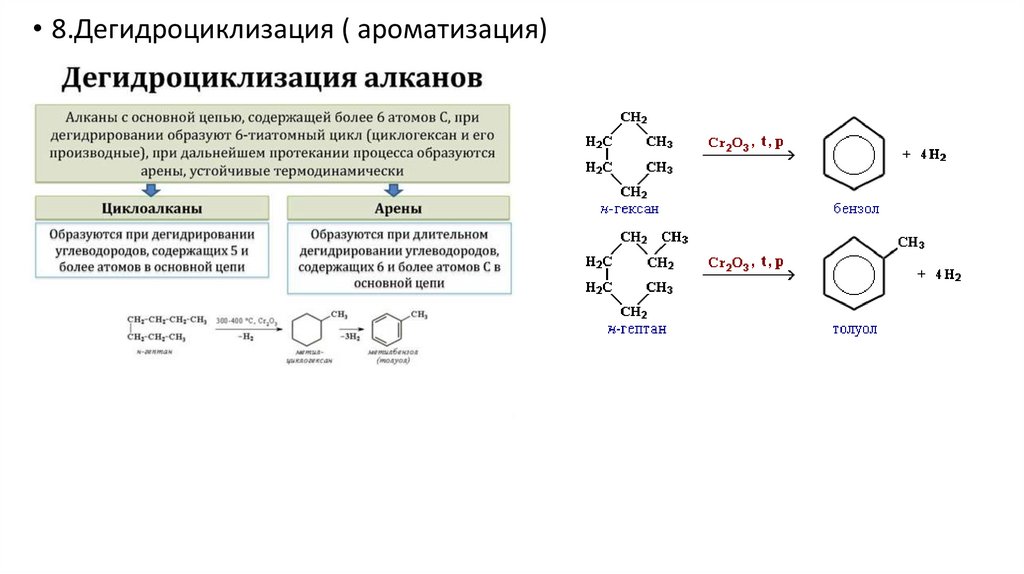

 Химия
Химия








