Похожие презентации:
Toxikologia
1. Toxikológia
• Doc. Ing. Elena Piecková, MPH,PhD.
Slovenská zdravotnícka univerzita
Limbová 14
Bratislava-Kramáre
Tel.: 02/59370 376, 788
elena.pieckova@szu.sk
Konzultácie: Ut vždy po prednáške
1 hod
2. Učebnica
Liptáková, D., Prachar, V., ValíkĽ.:
Vybrané kapitoly zo
všeobecnej, potravinárskej a
nutričnej toxikológie.
STU Bratislava, 2015.
3. Najstaršie záznamy o jedoch: v podobe pracovných postupov na ich prípravu, Ebersov papyrus (1500 pred n. l.). Starí Egypťania
TOXIKOLÓGIANajstaršie záznamy o jedoch: v podobe pracovných
postupov na ich prípravu, Ebersov papyrus (1500 pred n.
l.). Starí Egypťania poznali: bolehlav, digitalín, opiáty,
zlúčeniny
olova,
medi
a
iné.
V období začiatkov rozvoja gréckej kultúry (400 r. pred n. l.)
lekár Hippokrates rozšíril poznatky o jedoch a začal sa
zaoberať dávkovaním a používaním jedov a liečiv.
Kráľ Mithridates používal pri hľadaní antidót proti
jedovatým látkam odsúdencov - MITRIDATIZMUS
Pôvod toxikológie → používanie jedov na vraždy,
samovraždy. Katarína Medicejská testovala jedy na
chudobných a chorých a pozorovala klinické príznaky.
Medzi známe travičky patrila aj Lucrezia Borgia (1480 –
1519, dcéra pápeža Alexandra VI.), ktorá využívala jedy na
odstránenie
nepohodlných
ľudí
v
politike.
4. Historický vývoj toxikológie - pokračovanie
Historický vývojtoxikológie pokračovanie
• Rozvoj poznatkov o jedoch súvisel s rozvojom
medicíny. Okrem Avicenu sa do histórie významne
zapísal aj Paracelsus (1492 – 1541): nemecký chemik,
lekár a prírodovedec, pôsobil ako profesor v Bazileji.
• Alma mater: University of Ferrara
• Otec toxikológie → Sola dosis facit venenum
• V rokoch 1521, 1526, 1527 a 1537 navštívil územie
Slovenska - skúmanie drahých kovov.
• Ďalšou významnou postavou v toxikológii: španielsky
lekár Orfila (1787 – 1853): lekár na dvore kráľa
Ľudovíta XVIII. Ako prvý prišiel s pojmom toxikológia,
ktorej podstatou bolo štúdium jedov. Toxikológiu
vyčlenil ako samostatnú vedu → sledovanie toxických
a terapeutických účinkov chemických zlúčenín.
• Padova, dr. Ramazzini: Choroby robotníkov
(1700)
5. Novodobá história toxikológie
Ďalší rozvoj toxikológie: Louis Lewin, nemecký
farmakológ, ktorý sa zaoberal štúdiom vyšších
alkaloidov, opiátov, halucinogénov a pod..Zostavil
systém psychoaktívnych drog a rastlín na základe ich
farmakologického účinku.
• V priebehu 20. st. sa v laboratóriu pripravil jeden
z prvých antidót proti organickým zlúčeninám arzénu
(Voegtlin, rok 1924). Objavenie penicilínu Flemingom
(škótsky biológ, farmakológ a botanik) v roku 1928
zahájilo proces izolácie antibiotík. V r. 1945 získal spolu
s H. Floreyom a E. B. Chainom Nobelovu cenu za
fyziológiu a medicínu
• DDT (dichlórdifenyltrichlóretán) – následne hodnotenie
celkovéo chemického rizika látok
• V súčasnosti sa venuje pozornosť účinkom vzájomných
vzťahov medzi jednotlivými látkami v organizme
a reakciám vo vnútornom prostredí. Viaceré chemické
katastrofy, ako napr. v r. 1976 v Sevese únik dioxínov,
v minulosti predznamenali významné medzníky
v rozvoji toxikológie.
6. Toxikológia
Multidisciplinárna veda, zaoberajúca sa:
Účinkom jedov a škodlivých látok
Diagnostikou otráv a ich liečením
Analytickým stanovením príčin otravy
• Základné rozdelenie:
• EXPERIMENTÁLNA TOXIKOLÓGIA študuje účinok jedov
predovšetkým na experimentálnych zvieratách,
objasňuje mechanizmus účinku jedov a ich
metabolizmus v organizme a hľadá protijedy.
• KLINICKÁ TOXIKOLÓGIA sleduje klinické prejavy otráv
na ľudský organizmus, jeho jednotlivé orgány a hľadá
vhodnú terapiu otráv.
7. Rozdelenie toxikológie (odvetvové):
Lekárska, toxikológia liečiv
Priemyselná (havárie) (patrí aj potravinárska)
Súdna
Veterinárna (krmivá)
Rastlinná, toxikológia agrochemikálií (vplyv
pesticídov, herbicídov)
• Sociálna (užívanie, alkoholu, tabaku, drog a pod.)
• Toxikológia životného prostredia, vrátane
Ekotoxikológie (dynamika populácie)
Cieľ potravinárskej toxikológie: Zhromaždiť
informácie o látkach prítomných v potravinách
(prirodzene/ zámerne pridávané/kontaminanty z
prostredia), ktoré by mohli poškodiť zdravie
konzumenta
8. Otrava
-celkové ochorenie organizmu – DS, GIT, koža asliznice -––- poškodenie CNS
-vyznačuje sa:
• Pôvodcom, inkubačnou dobou, následkami,
anatomicko-patologickým nálezom
Delenie otráv:
• Akútne
• Subakútne
• Subchronické
• Chronické
• Štatisticky najvyššie percentuálne zastúpenia
predstavujú: otravy liekmi (50 %), obchodnými
prípravkami (30 %), požitie rastlín (8 %), chemických
látok (5 %), húb (2 %), drog (1 %), otravy živočíšnymi
jedmi (1 %) a ostatné (1 %).
9. Jed (noxa) vs. škodlivina
--
látka, ktorá po vniknutí do organizmu v malom
množstve vyvolá po svojom vstrebaní chorobné zmeny
→ môže nastať smrť
Pôsobenie jedov na organizmus: miestne,
dráždivé, dusivé, alergény, narkotiká, orgánová
toxicita, génová toxicita
Rozdelenie jedov podľa pôvodu:
• Prírodné (rastlinné a živočíšne; strychnín = LD50 p.o.
pre ľudí 2 mg/kg, opiáty, hadí jed, saxitoxín (mušle) =
LD50 p.o. pre ľudí 5,7 g/kg, a ďalšie)
• Syntetické (organické, anorganické: dioxíny, DDT = LD50
p.o. pre ľudí 100 mg/kg ťažké kovy, PCB---Spolana
Neratovice ČR, Chemko Strážske SR a iné)
• Jedna z najstarších definícií jedu (podľa Paracelsa):
všetky látky sú jedmi a závisí len na dávke, kedy látka
prestáva byť jedom. Jedom, toxickou látkou môžu byť
aj chemikálie a lieky, ktoré sú v nízkej koncentrácii
nejedovaté alebo dokonca liečivé. Naopak aj bežné
a pre život potrebné zlúčeniny ako NaCl alebo glukóza,
môžu mať vo vysokých koncentráciách a bez lekárskej
pomoci za následok smrť (LD50 NaCl je 3000 mg/kg
10. Spôsoby prenikania jedov do organizmu:
Ústami (perorálne; rýchle ; využitie v medicíne:
nitroglycerín u kardiakov)
Kožou (subkutánne, najhlavnejšou prekážkou je
najvrchnejšia membrána = stratum corneum). Ošetrenie
kože metanolom, etanolom, acetónom a pod. zvyšuje
permeabilitu/priepustnosť kože pre iné tox. látky.
Sliznicami
Vnútrožilovo (intravenózne ; rýchle)
Vnútrosvalovo (intramuskulárne)
Respiračne (plyny, aerosóly a prachové častice);
pôsobenie dráždivé, dusivé alebo po vstrebaní do
cirkulácie systémová toxicita
Rýchlosť prenikania jedu do organizmu je ovplyvnená:
• Fyzikálno-chemickými vlastnosťami jedu (lipo-,
hydrofilita)
• Koncentráciou, dobou expozície, spôsobom prenikania do
organizmu, hodnotou pH v prostredí (v žalúdku)
• rezistenciou organizmu (vek, pohlavie, zdravotný stav,
rýchlosť metabolizmu a pod.)
Distribúcia jedov a škodlivín v organizme – krv
(albumín)
11. Metabolizmus toxínov
• Eliminácia (biologický polčas)vs. kumulácia –– kumulatívna otrava
• Biotransformácia – detoxikácia:
1. fáza (cyt P-450): - hydrolýza
- oxidácia
- redukcia
2. fáza: - konjugácia
12. Toxicita
- schopnosť látky vyvolať intoxikáciu, charakterizovanáletálnou dávkou
Kategórie toxicity:
• Extrémne toxický
• Vysoko toxický
• Stredne toxický
• Slabo toxický
• Prakticky toxický
• Relatívne neškodný
<1 mg/kg ľudskej váhy
1-50 mg/kg
50-500 mg/kg
05-5 g/kg
5-15 g/kg
> 15 g/kg
• Prejavy toxicity buď na konkrétnom orgáne (pľúca,
pečeň, obličky...) alebo na viacerých miestach→
systémová toxicita
• Nebezpečnosť – schopnosť látky pôsobiť toxicky
13. Skúmanie toxicity: z hľadiska akútneho, subakútneho, chronického a kombinovaného účinku -
Skúmanie toxicity: z hľadiskaakútneho, subakútneho,
chronického
a kombinovaného účinku LABORATÓRNE ZVIERATÁ vs.
ORGÁNOVÉ/BUNKOVÉ KULTÚRY
Pre akútny toxický účinok sa uvádzajú 2 parametre:
• Horný parameter jedovatosti (smrteľné koncentrácie)
• Dolný parameter jedovatosti (minimálne účinné
koncentrácie)
- Čím je rozdiel medzi parametrami menší → tým je
látka nebezpečnejšia
- Prejavy napr. zmena krvného tlaku, arytmie, kŕče,
dráždenie dýchacích ciest, ale aj smrť
- Napr. otrava etanolom alebo arzénom
Posúdenie jedovatosti:
- absolútna smrteľná koncentrácia
- LD50
- minimálna smrteľná koncentrácia
- maximálna znesiteľná dávka
14.
-Subakútny účinok – 10 % očakávanej dĺžky života
(kumulatívny účinok)
-
Subchronický účinok- cieľ hodnotenia je získať
podklady pre zistenie biologického účinku látok- zistiť
kumulatívny účinok a patologické zmeny
(koncentrácie, pri ktorých zmeny nastanú)
15. Chronický a kombinovaný účinok:
• Chronický účinok: spojený s celoživotnou expozícioutoxickej látke (napr. DDT, arzén, olovo, ortuť).
Hodnotíme kumulatívne vlastnosti látok a schopnosť
sumácie účinkov. Štúdium karcinogénov.
• Podstata sumácie účinkov: látka po vstupe do
organizmu sa buď odbúra alebo vylúči → účinok látky
však pretrváva → zmeny na biolog. molekulách (DNA)
-
Komb. účinok: sledujú sa zmeny na organizmoch po
interakcii viacerých látok
a) Aditívny účinok (po kombinácii 2 látok sa nemení
intenzita účinku, napr. lieky a alkohol)
b) Potenciovanie (účinok kombinácie je silnejší ako
aditívny, napr. warfarín a lieky s väzbou na albumín)
c) Antagonizmus (účinok sa zoslabí /vymizne, napr. jedy a
antidóta , napr. EDTA pre kovy)
d) Synergizmus (napr. etanol a chlorid uhličitý)
16. Teratogénny účinok (nie dedičný):
Teratogén: štrukturálne, funkčné a biochemické zmenyv organizme.
Veda skúmajúca poruchy organizmu počas vývoja =
teratológia
Príklady teratogénov:
1. chem. látky, napr. zlúčeniny ortuti, PCB, dioxíny
2. vírusy, napr. vírus rubeoly---šedý zákal; vírus Zikka--mikrocefália; herpetické vírusy, coxsackie B --- potrat,
mŕtvornaodené deti, mikrocefália, mentálna
retardácia
3. infekčné agens, napr. toxoplazmy ---poškodenie
mozgu (TORCH syndrome)
4. liečivá, napr. antibiotiká, anestetiká, warfarín,
talidomid, antidepresíva
5. ochorenia matky, napr. listerióza---potrat ; syfilis,
astma, diabetes ; fenylketonúria---mentálna
retardácia; Mumps, kiahne, hepatitída B---potrat,
mŕtvornaodené deti, poškodenie pečene, končatín a
prstov, zraku a mozgu
17.
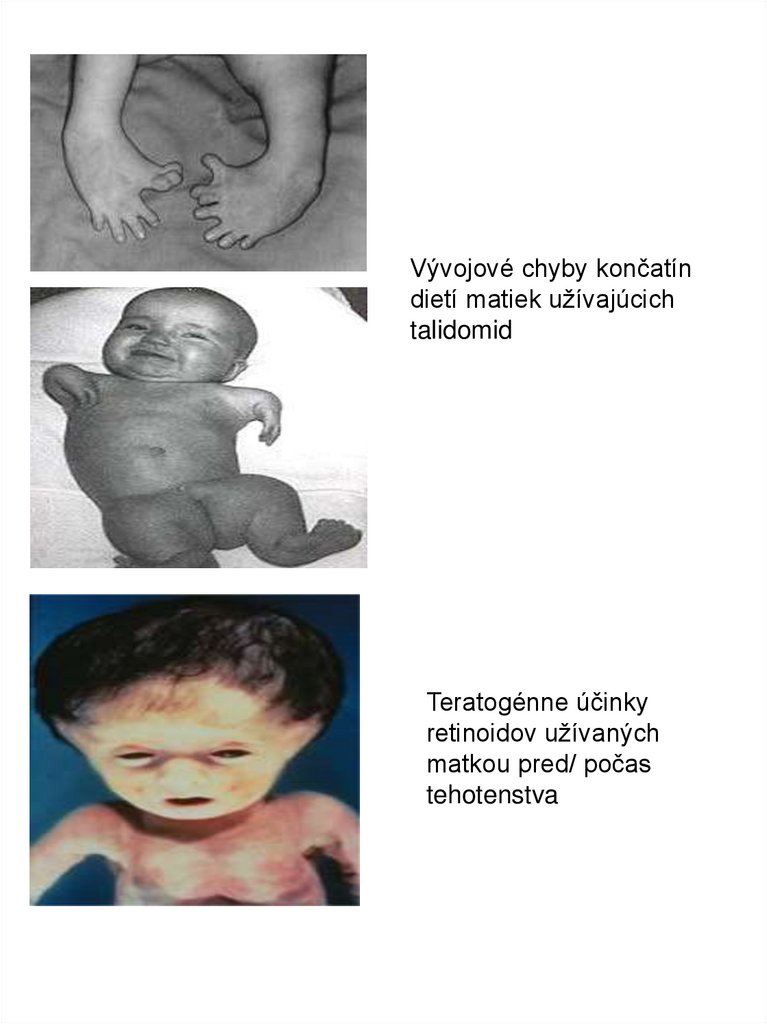
Vývojové chyby končatíndietí matiek užívajúcich
talidomid
Teratogénne účinky
retinoidov užívaných
matkou pred/ počas
tehotenstva
18.
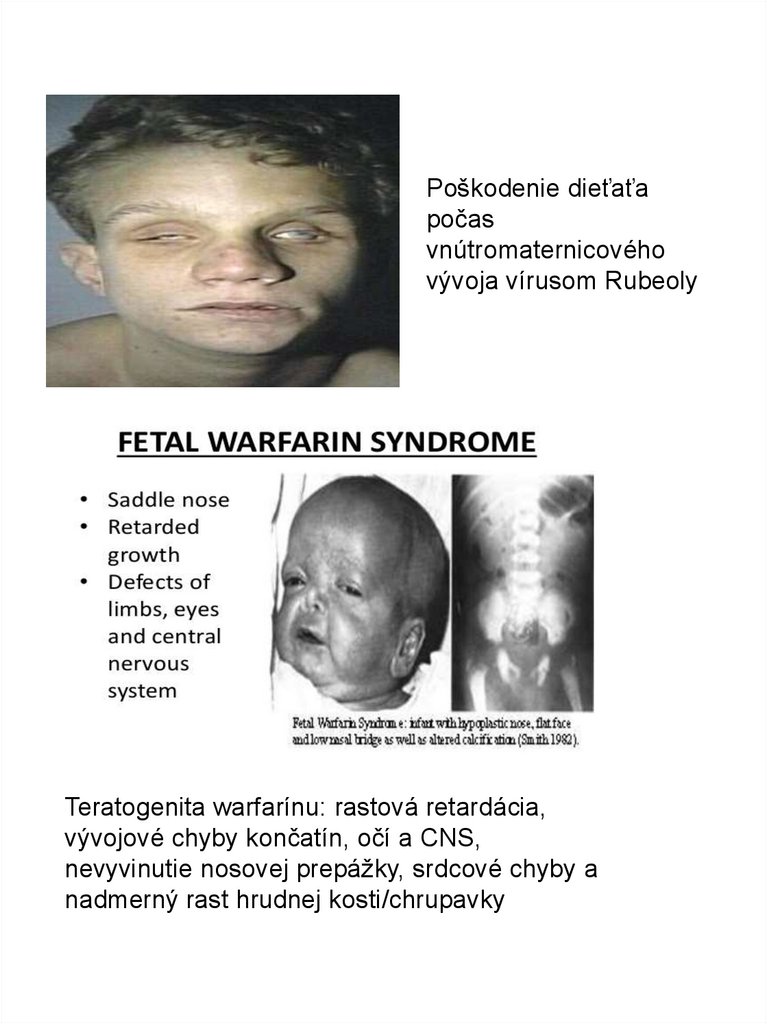
Poškodenie dieťaťapočas
vnútromaternicového
vývoja vírusom Rubeoly
Teratogenita warfarínu: rastová retardácia,
vývojové chyby končatín, očí a CNS,
nevyvinutie nosovej prepážky, srdcové chyby a
nadmerný rast hrudnej kosti/chrupavky
19. Vývojová toxicita
-Toxicita pôsobiaca od embrya po pohlavnú dospelosť.
K expozícii došlo: pred počatím, počas tehotenstva, po
narodení až do dospelosti.
Prejavy nepriaznivých účinkov na organizmus:
1. Úmrtie pred/ po narodení
2. Výskyt abnormalít
3. Zmeny rastu, funkčné deficity
Štádiá vývoja:
Gametogenéza a oplodnenie (Embryoletalita)
Preimplantácia (zahniezdenie) dtto
Embryonálne obdobie (Embryotoxicita), teratogenita
Fetálne obdobie (plod) (Teratogenita)
Postnatálne obdobie
20. Štádiá vývoja:
• Embryonálne obdobie: prudký rast a diferenciáciabuniek, tvorba orgánov a orgánových systémov,
najkritickejšie obdobie 17. – 90.- ty deň od
oplodnenia. Expozícia nevhodným podmienkam vedie
k potratu, k ťažkým vývojovým chybám (napr. rázštep
podnebia a neurálnej trubice)
• Fetálne obdobie: rast a diferenciácia orgánových
systémov. Expozícia plodu nevhodným faktorom
prostredia môže vyvolať rastovú retardáciu, spustenie
karcinogenézy, vývojové chyby a pod.
• Postnatálne obdobie: expozícia nevhodnými faktormi v
prostredí inhalačne, orálne, cez kožu alebo materské
mlieko. Negatíva expozície napr. zožltnutie zubov
(dioxíny, tetracyklín), rastová retardácia,
karcinogenéza (ťažké kovy) a pod.
21. Sledované konečné toxické pôsobenie na matku: mortalita, neplodnosť, zmeny hmotnosti tela (aj zmeny hmotnosti orgánov v prípade
priberania), klinické zmeny,príjem potravy a vody, pitevné a histologické nálezy
Sledované konečné dôsledky
vývojovej toxicity:
Potrat, štrukturálne abnormality, hmotnosť plodu, pomer
pohlaví, mŕtve narodené deti, poruchy funkcií, pitevné
a histologické nálezy.
22. Mutagénny účinok: GENOTOXIKOLÓIA
Mutagénny účinok: Kvalitatívna a kvantitatívna zmena vgenetických informáciách organizmu
Mutagénny účinok majú:
- Chemické látky (polycyklické uhľovodíky, organické
rozpúšťadlá, DDT), ionizačné žiarenie (aj RTG),
infekčné agensy (onkogénne vírusy ako napr. herpes
vírusy, vírus Epsteina-Barrovej a i.), lieky
(antikoncepcia, cytostatiká), psychotropné látky
(alkohol, drogy)
-
Rozdelenie mutagénov: širokospektrálne,
úzkospektrálne
-
Mutácie: chromozómové, génové (bodové mutácie) a
genómové (trizómie – Downov syndróm a i.)
Prekryv medzi karcinogénom a mutagénom je 80-85 %
→ každá mutagénna látka sa považuje za
karcinogénnu, kým sa nezistí opak
TESTY: Amesov test – génové mutácie
cytogenetické testy
-
-
23.
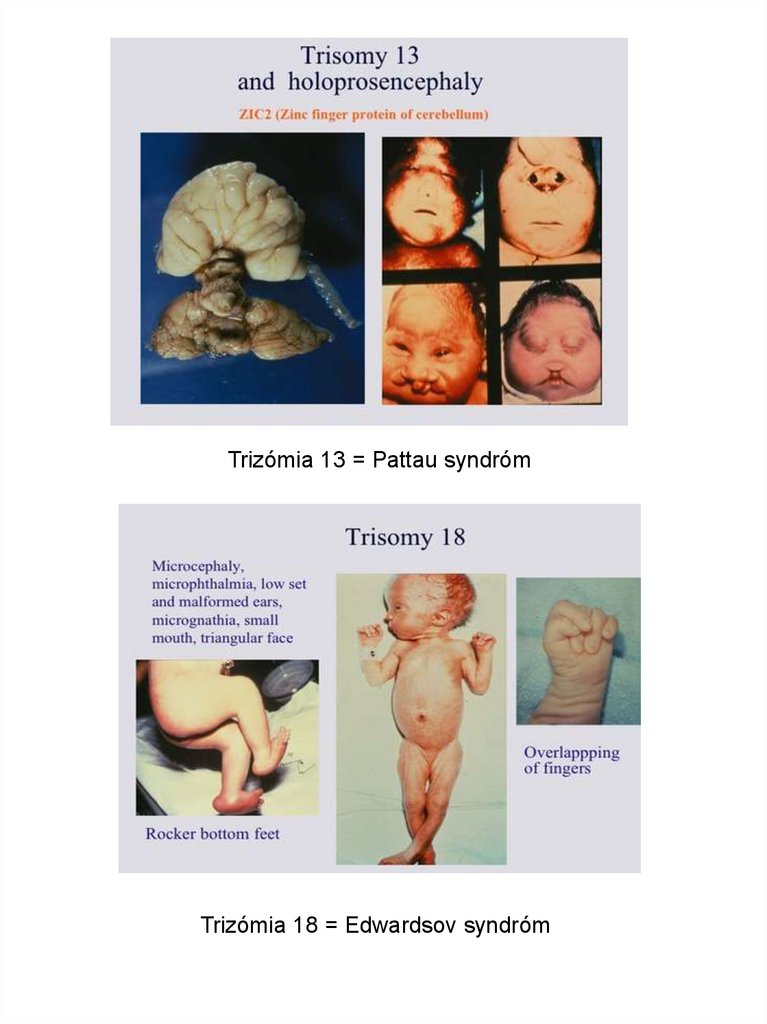
Trizómia 13 = Pattau syndrómTrizómia 18 = Edwardsov syndróm
24. Karcinogénny účinok
• Karcinogenita = mnohostupňový procesabnormálneho rastu a diferenciácie buniek, ktorý
môže viesť k rakovine. Má 3 štádiá: iniciácia, promócia
a progresia
• Karcinogenéza = tvorba nádorov
• Nádory: benígne a malígne
• Tvorba metastáz:
• 1. uvoľnenie z primárneho nádoru
• 2. vstup do krvného riečišťa a lymfatického systému
• 3. proliferácia/množenie na sekundárnom mieste
• Karcinogény podľa IARC = Medzinárodná agentúra pre
výskum rakoviny rozdelené do 4 kategórií:
• 1. dokázané karcinogény (arzén, aflatoxíny, ionizujúce
žiarenie)
• 2. potenciálne karcinogény (olovo, PCB)
• 3. látky podozrivé z karcinogenézy (DDT,
chloramfenikol)
• 4. pravdepodobne nekarcinogénne pre ľudí
25.
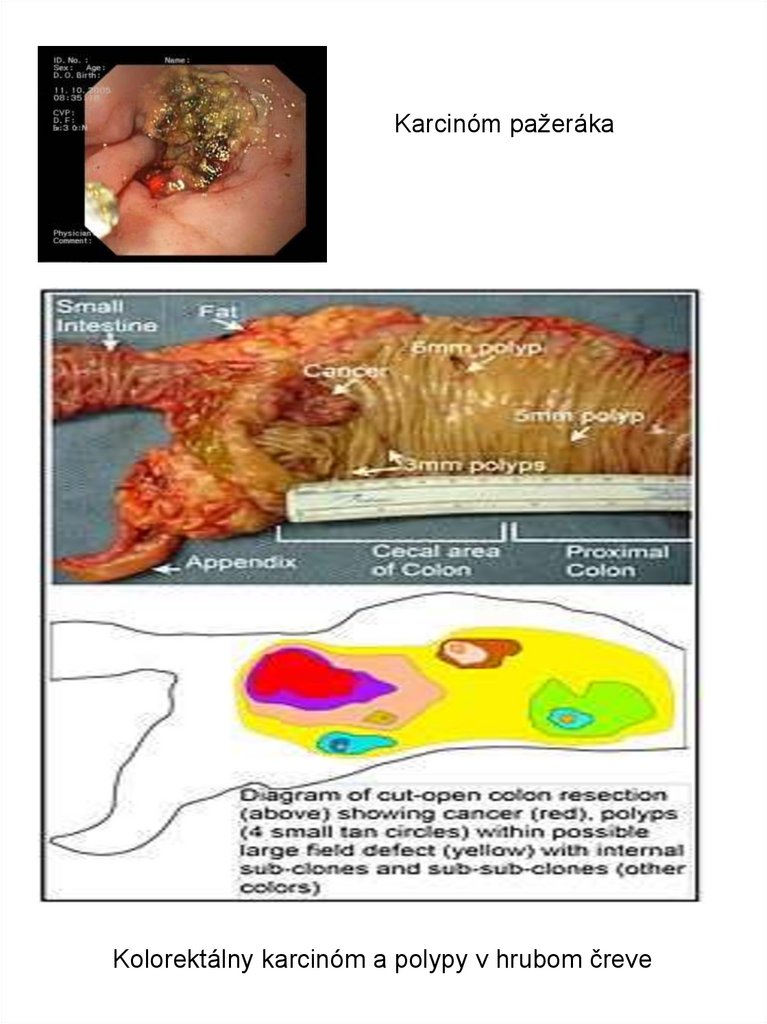
Karcinóm pažerákaKolorektálny karcinóm a polypy v hrubom čreve
26.
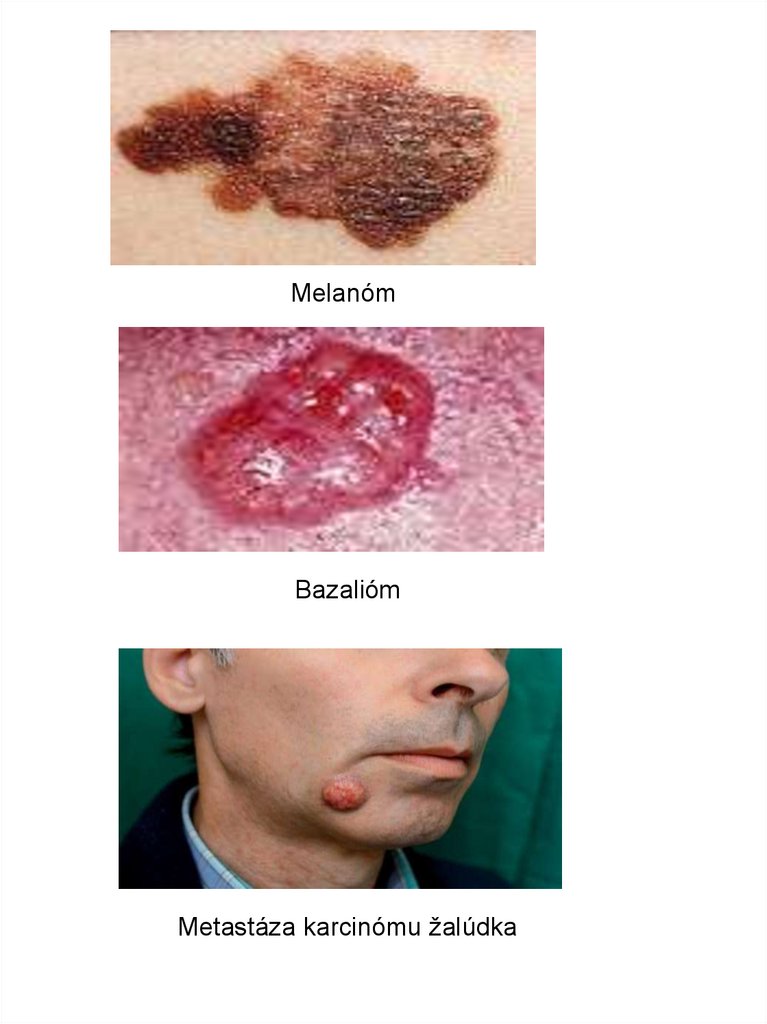
MelanómBazalióm
Metastáza karcinómu žalúdka
27.
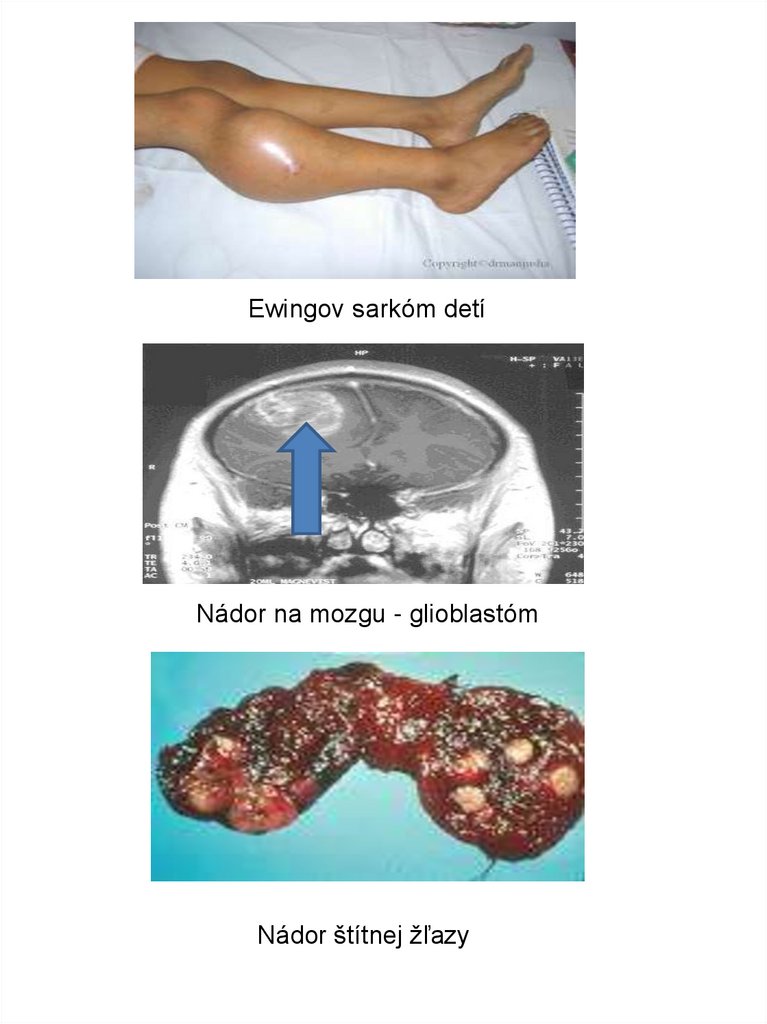
Ewingov sarkóm detíNádor na mozgu - glioblastóm
Nádor štítnej žľazy





















 Медицина
Медицина





