Похожие презентации:
Амины. Аминокислоты. Белки
1.
Преподаватель ГПОУ КИТСолуянова Инна Валерьевна
2.
Цели урокасоздание условий для:
- формирования у учащихся знаний о разновидностях
органических веществ, их строении на примере аминов,
аминокислот и белков; о значении органических веществ в
жизнедеятельности человеческого организма
- формирование навыков применять правила систематической
международной номенклатуры как средства различения и
идентификации веществ по их составу и строению
- формирование личностных результатов – готовности и
способности к образованию и самообразованию в течение
всей жизни
- формирование метапредметных результатов – умение
самостоятельно формулировать цели деятельности,
продуктивно общаться и взаимодействовать, готовность к
самостоятельной информационно-познавательной
деятельности, умение излагать свои мысли.
3.
Производные аммиака, в молекуле которогоодин или несколько атомов водорода
замещены на углеводородные радикалы
4.
У первичных аминов азот связан только с однимуглеводородным радикалом
У вторичных аминов азот связан с двумя
радикалами
У третичных аминов азот связан с тремя
радикалами
5.
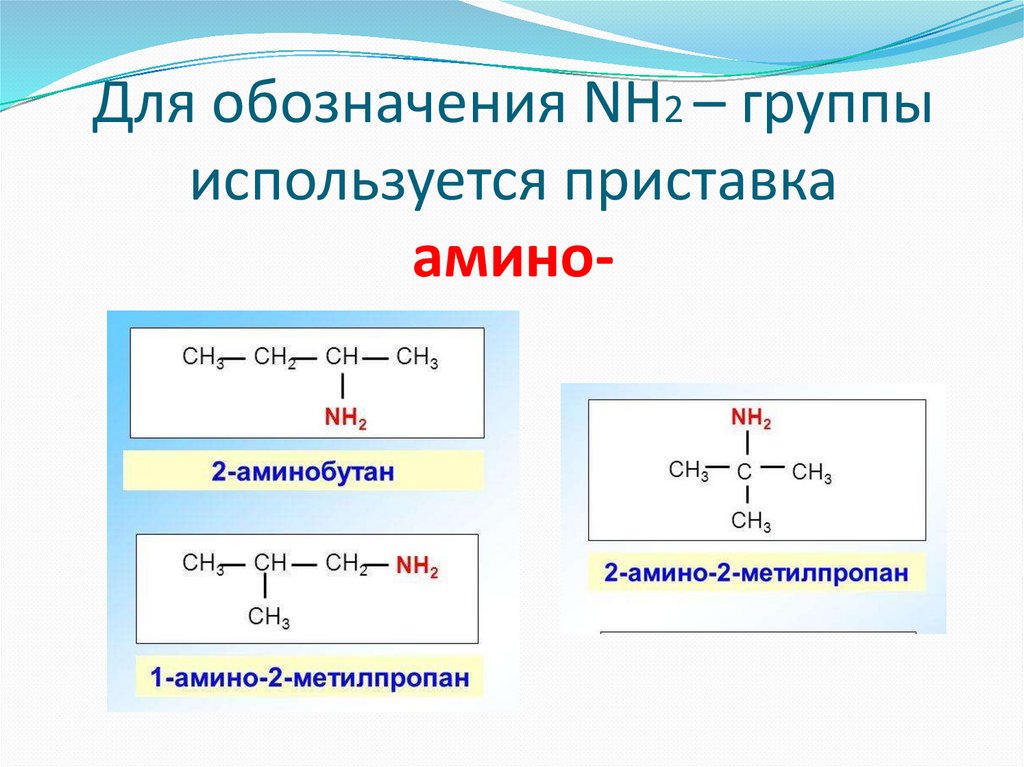
Для обозначения NH2 – группыиспользуется приставка
амино-
6.
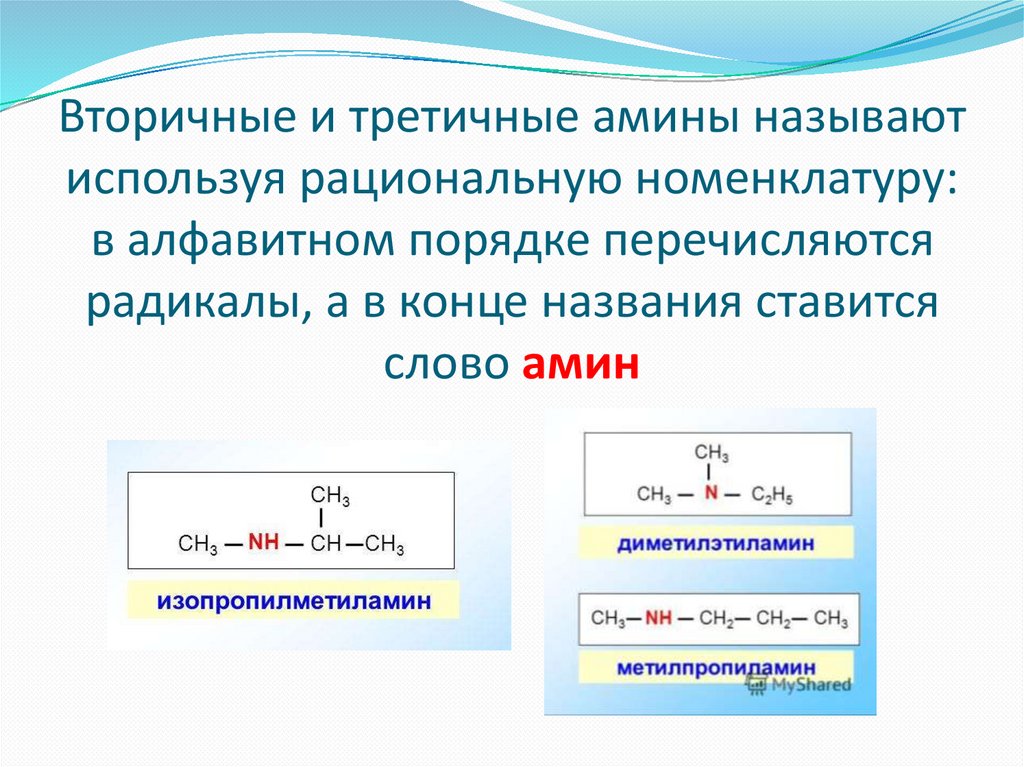
Вторичные и третичные амины называютиспользуя рациональную номенклатуру:
в алфавитном порядке перечисляются
радикалы, а в конце названия ставится
слово амин
7.
Физические свойстваПервые амины – газы с характерным запахом,
хорошо растворимы в воде.
Первичные и вторичные амины менее летучие, чем
третичные, и лучше растворимы.
8.
9.
Основные свойства(подобно аммиаку)
Реагируют с кислотами:
Первые представители аминов при
растворении в воде дают щелочную среду
10.
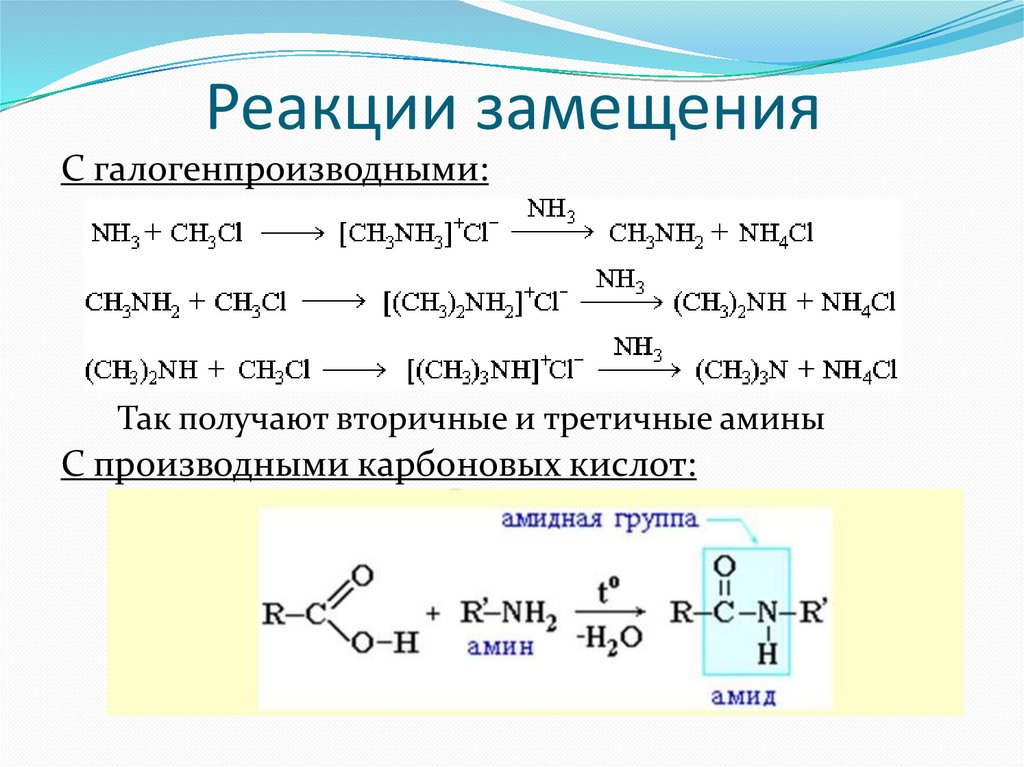
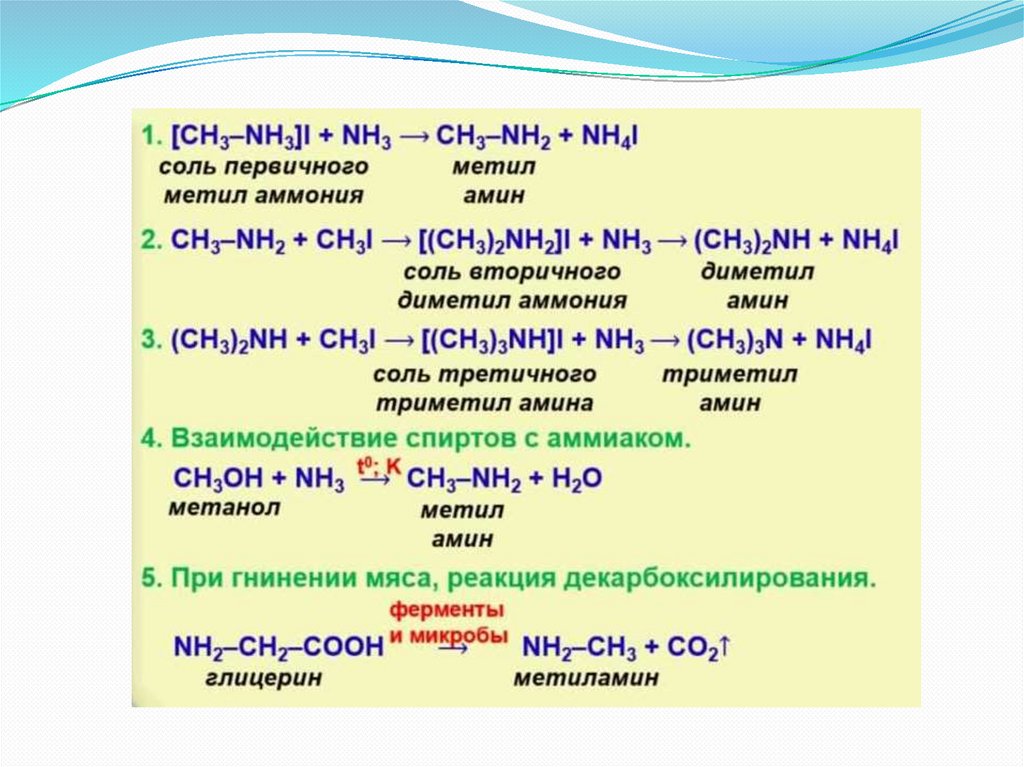
Реакции замещенияС галогенпроизводными:
Так получают вторичные и третичные амины
С производными карбоновых кислот:
11.
Качественная реакция на аминыРазрушение азотистой кислотой первичных аминов:
12.
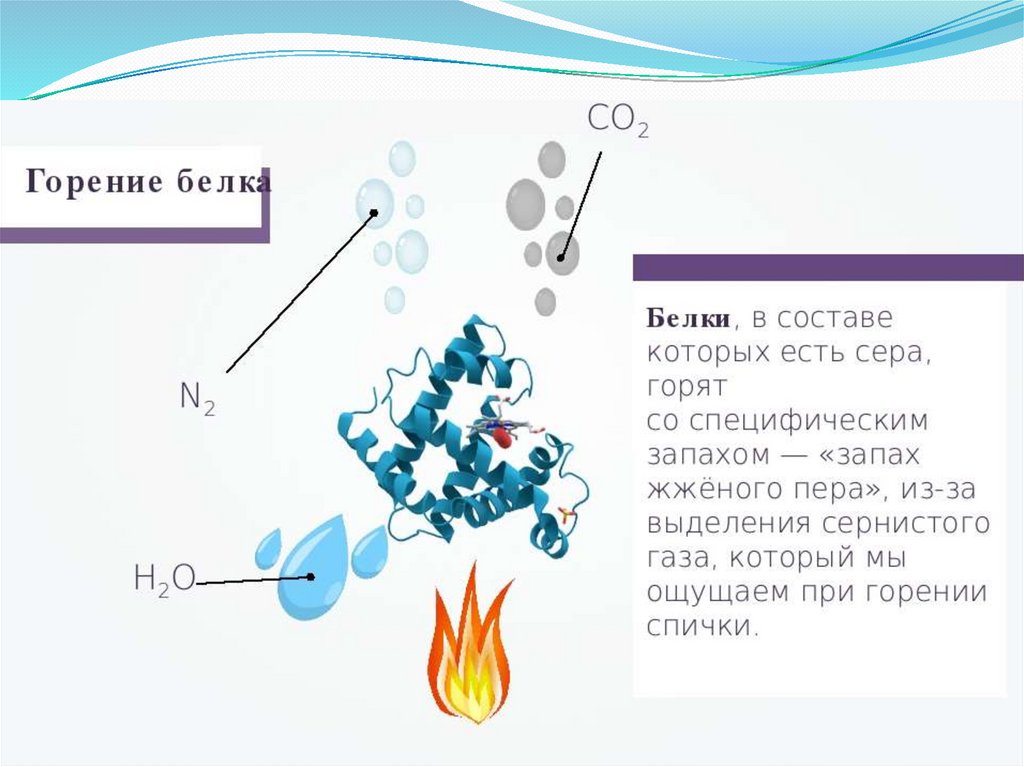
Окисление и горение13.
14.
15.
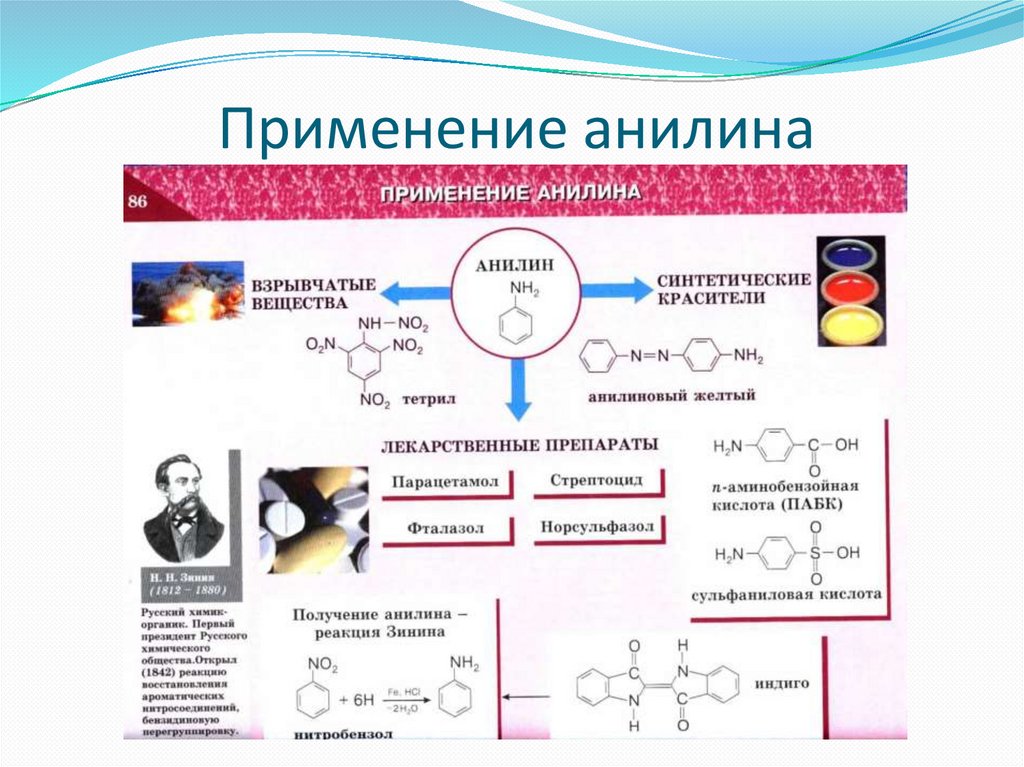
Анилин16.
Применение анилина17.
Производные карбоновых кислот,содержащие в своем составе одну или
несколько аминогрупп
18.
Природные аминокислотысодержат аминогруппу во 2-м
положении
19.
В названии аминокислотуказывается положение и
название аминогруппы, а затем
карбоновая кислота
20.
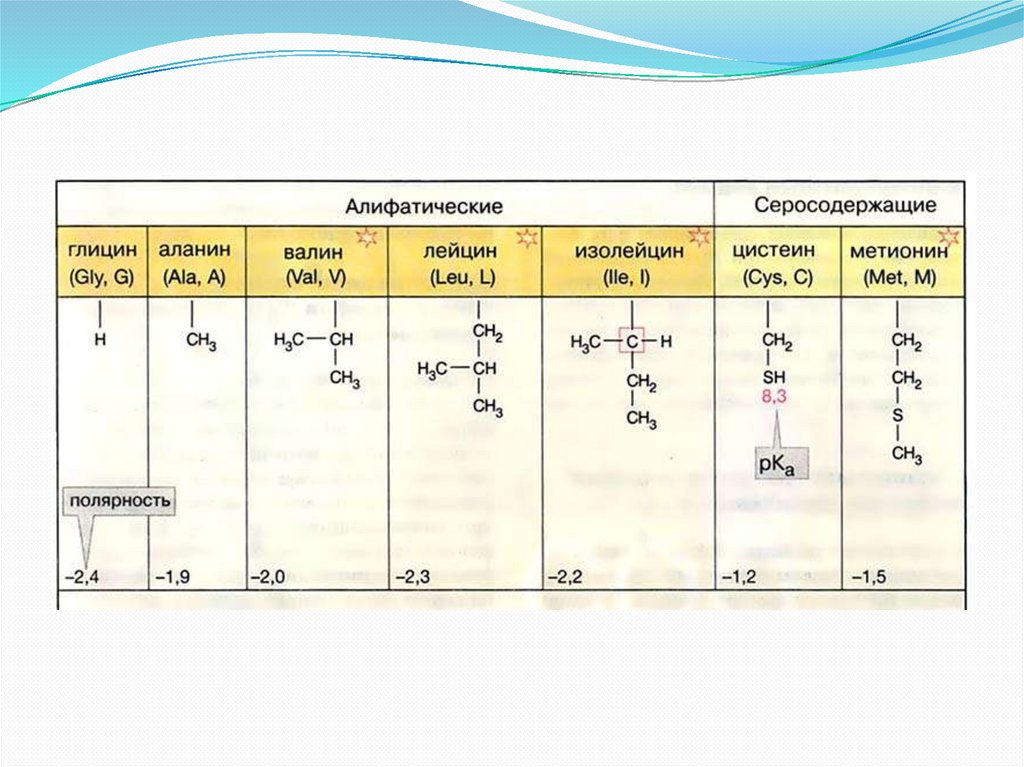
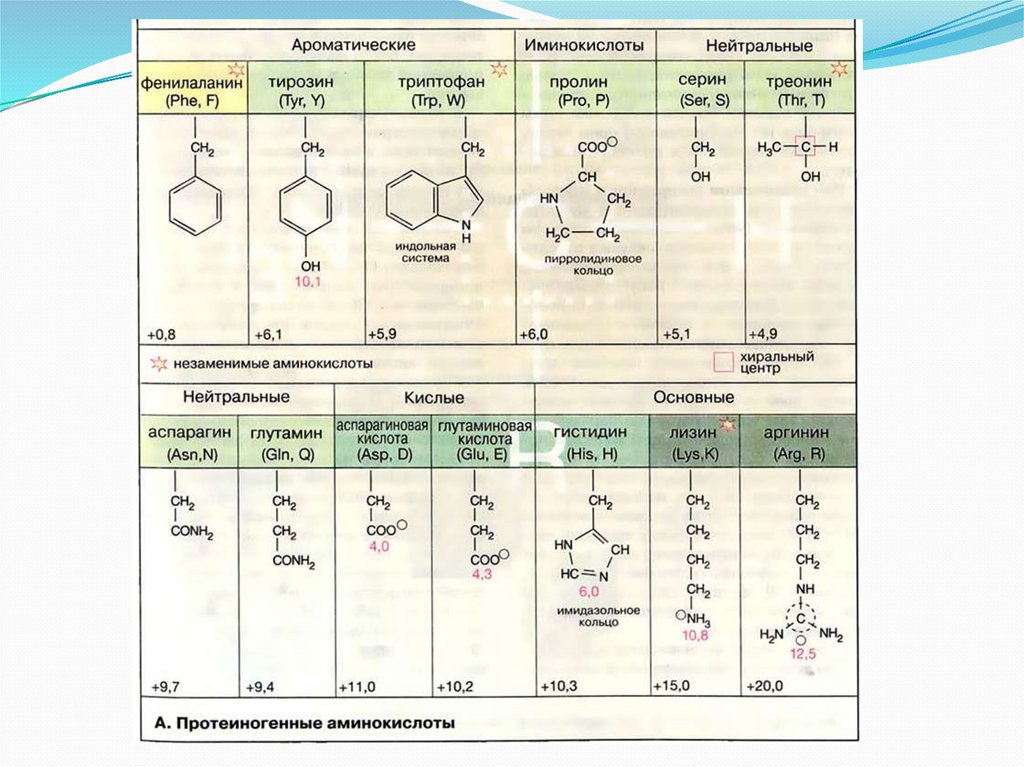
Из белков выделено 20аминокислот:
21.
22.
23.
Аминокислоты – амфотерныевещества
24.
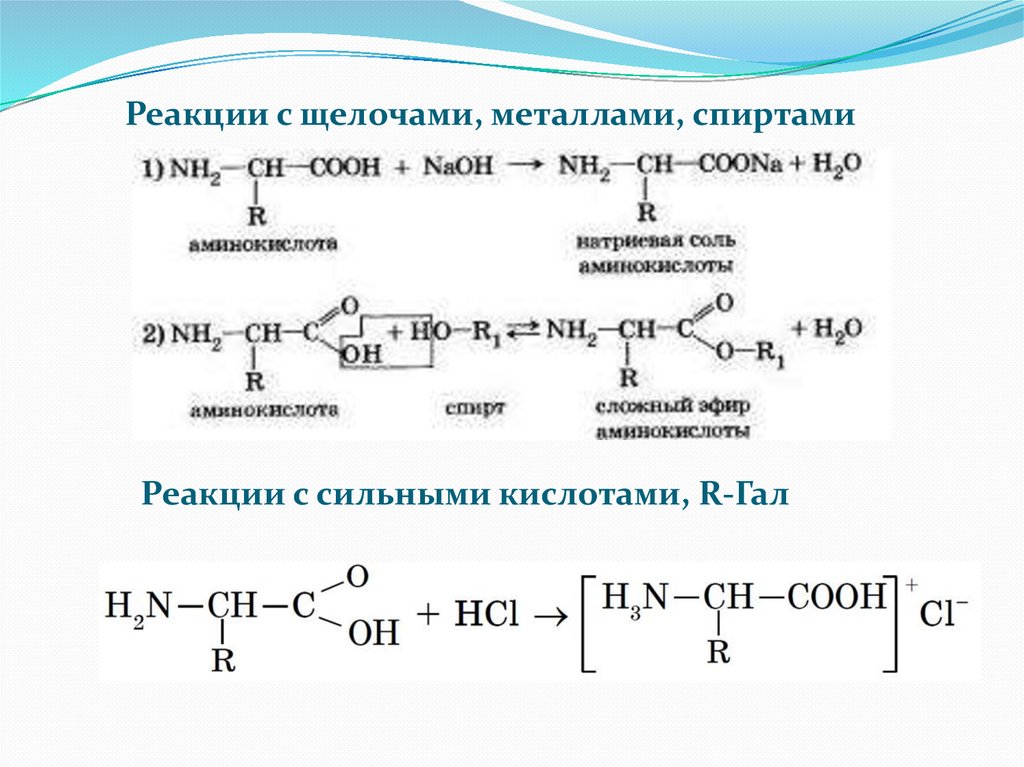
Реакции с щелочами, металлами, спиртамиРеакции с сильными кислотами, R-Гал
25.
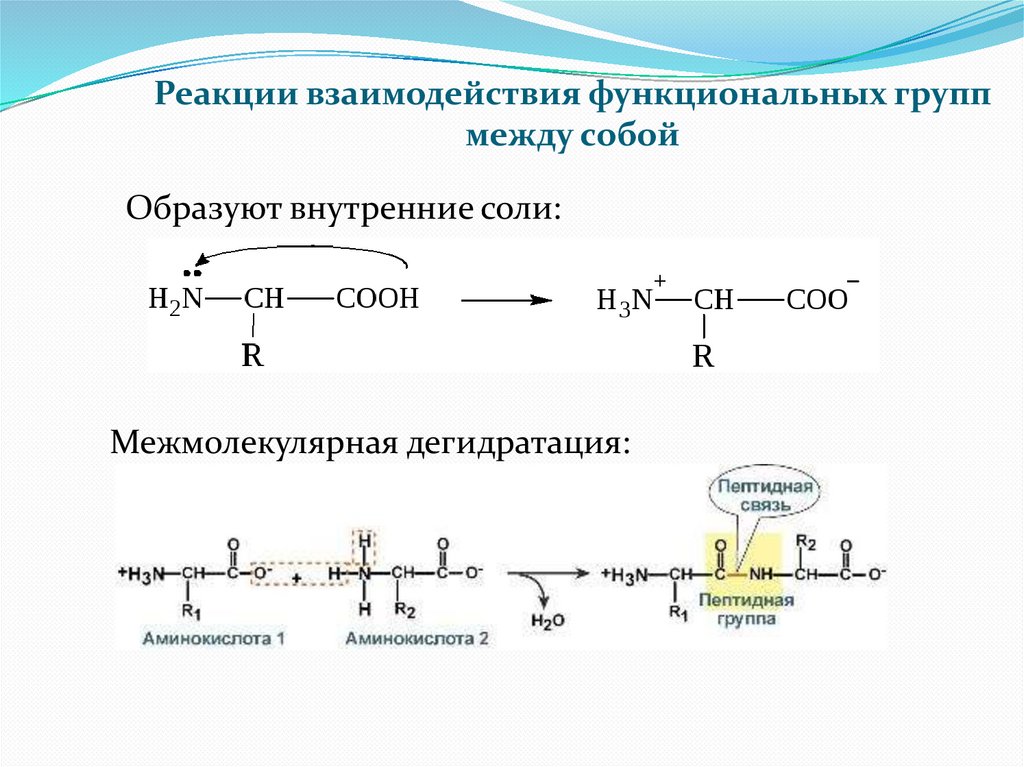
Реакции взаимодействия функциональных группмежду собой
Образуют внутренние соли:
Межмолекулярная дегидратация:
26.
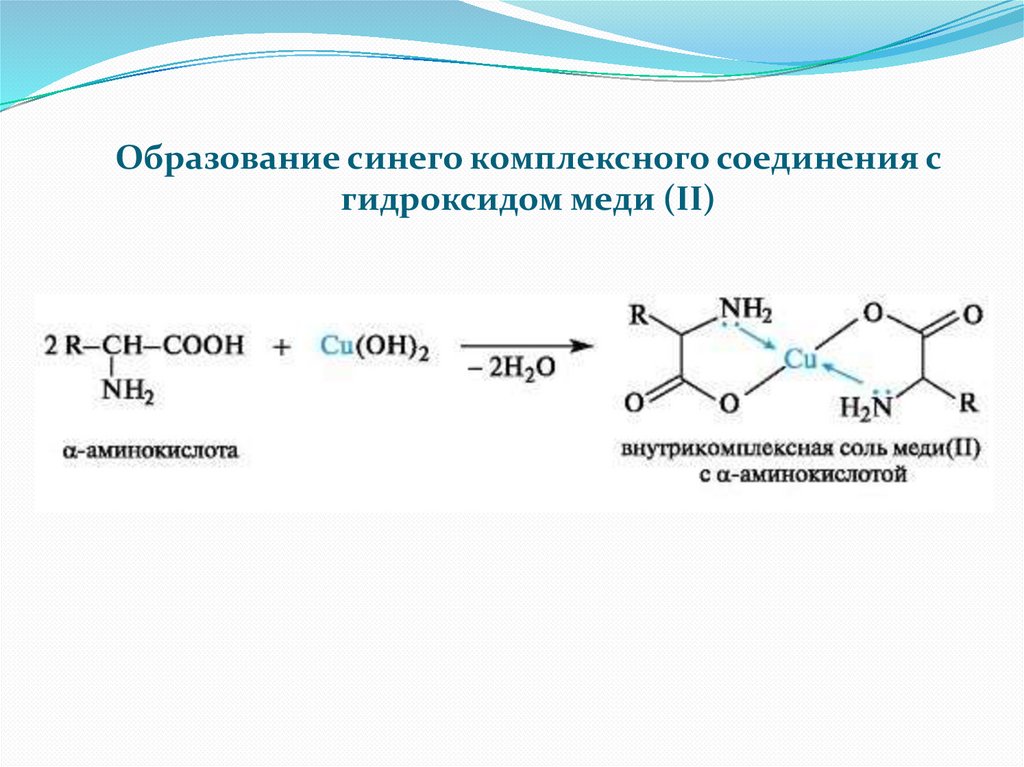
Образование синего комплексного соединения сгидроксидом меди (II)
27.
Биологические полимеры,состоящие из остатков аминокислот
28.
29.
Протеины30.
Протеиды31.
32.
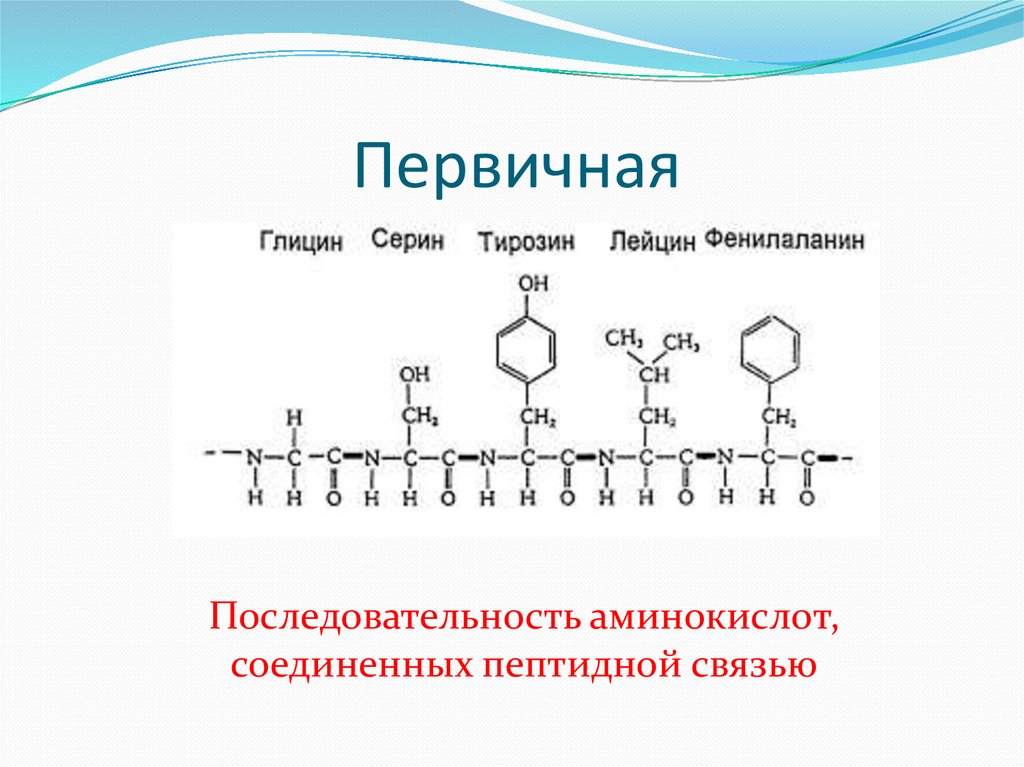
ПервичнаяПоследовательность аминокислот,
соединенных пептидной связью
33.
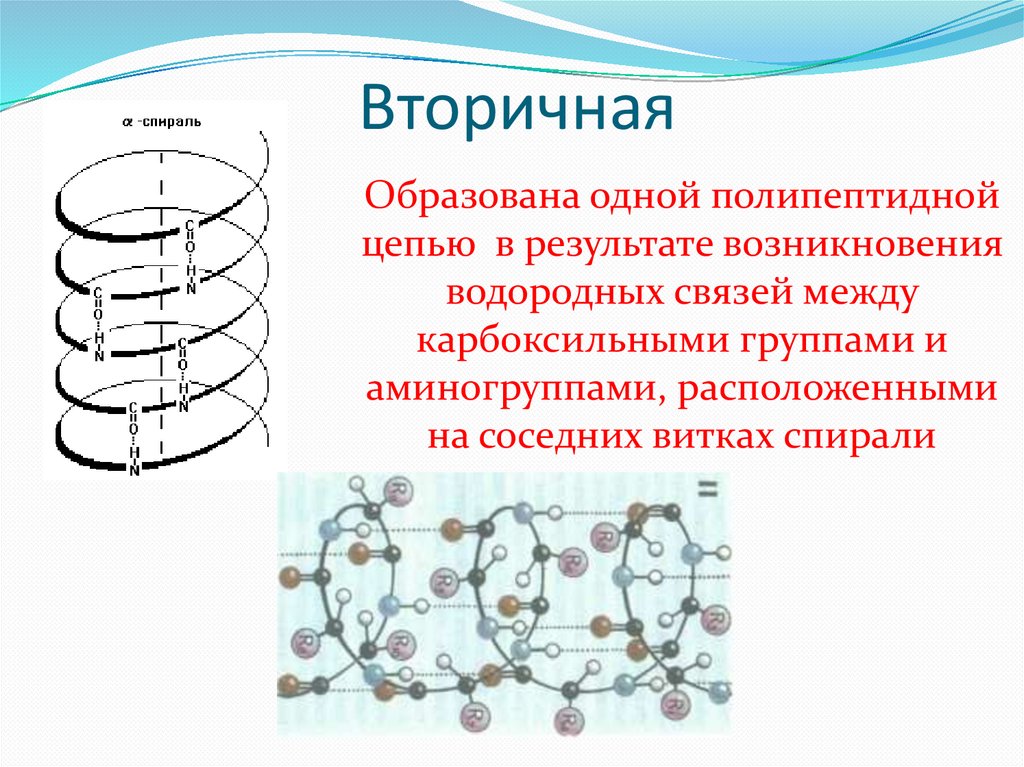
ВторичнаяОбразована одной полипептидной
цепью в результате возникновения
водородных связей между
карбоксильными группами и
аминогруппами, расположенными
на соседних витках спирали
34.
ТретичнаяОбразована полипептидными цепочками, поразному расположенными в пространстве за счет
водородных связей, ионного и гидрофобного
взаимодействия
35.
Четвертичная36.
37.
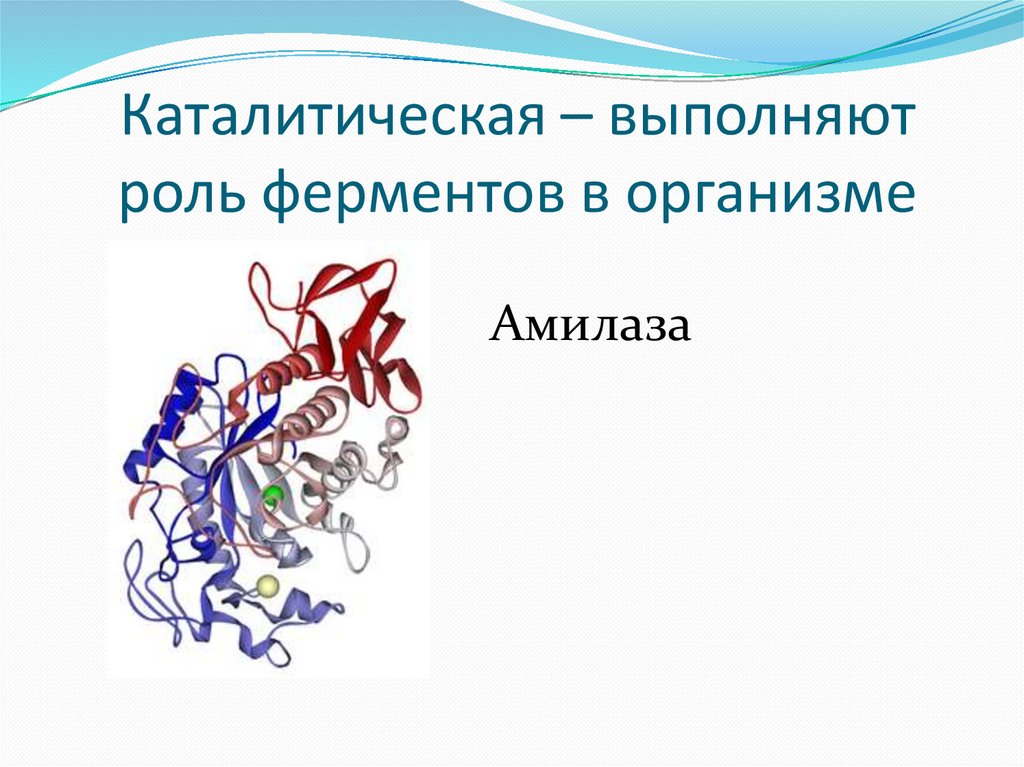
Каталитическая – выполняютроль ферментов в организме
Амилаза
38.
Защитная – выполняют рольантител в организме
39.
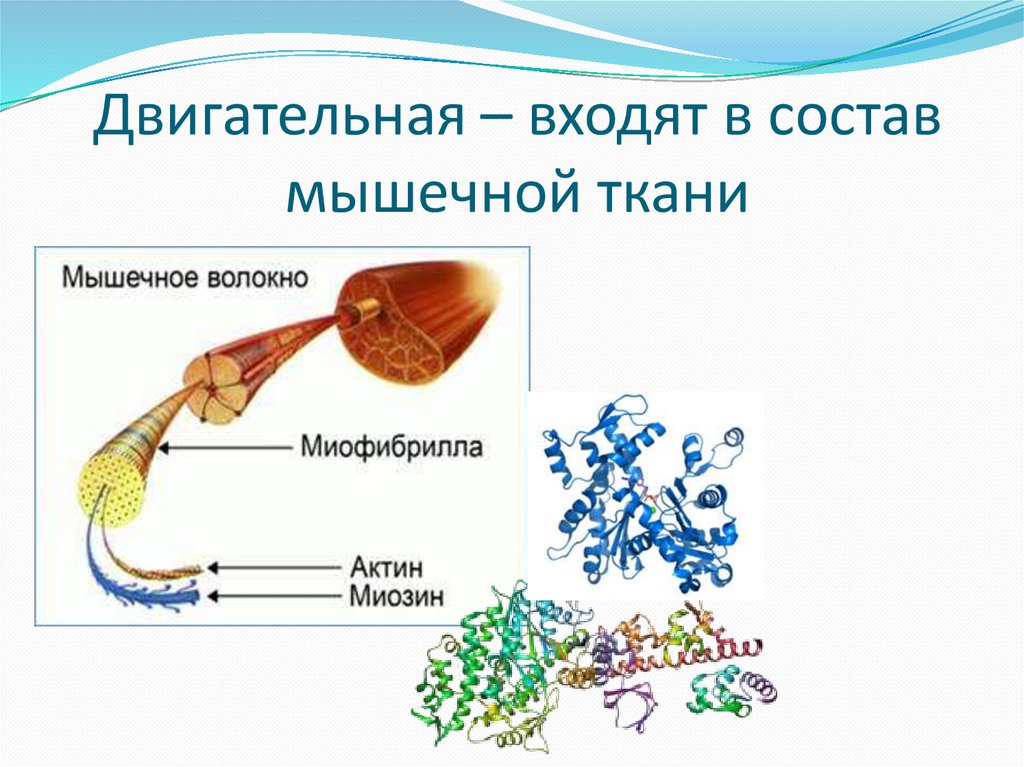
Двигательная – входят в составмышечной ткани
40.
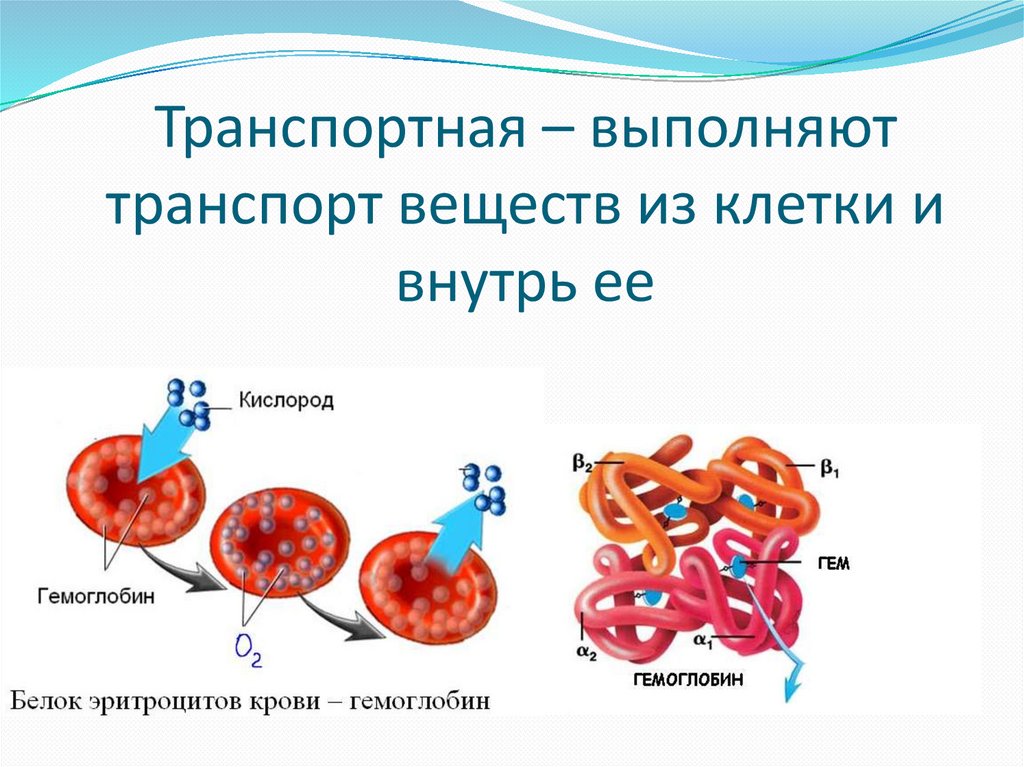
Транспортная – выполняюттранспорт веществ из клетки и
внутрь ее
41.
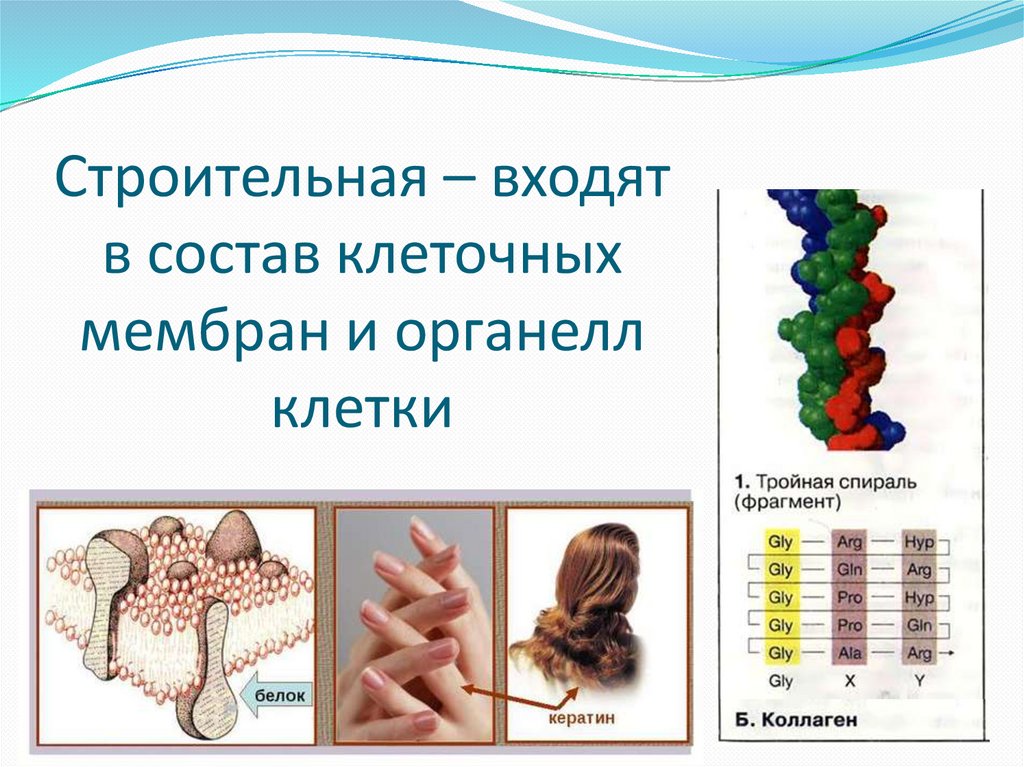
Строительная – входятв состав клеточных
мембран и органелл
клетки
42.
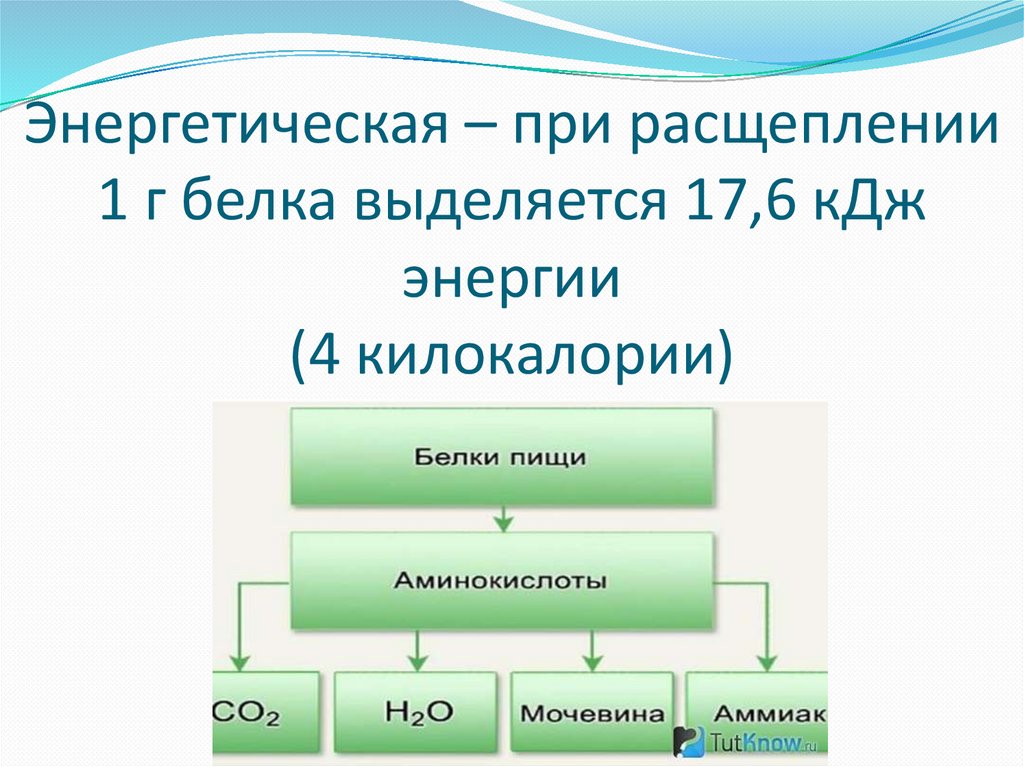
Энергетическая – при расщеплении1 г белка выделяется 17,6 кДж
энергии
(4 килокалории)
43.
44.
45.
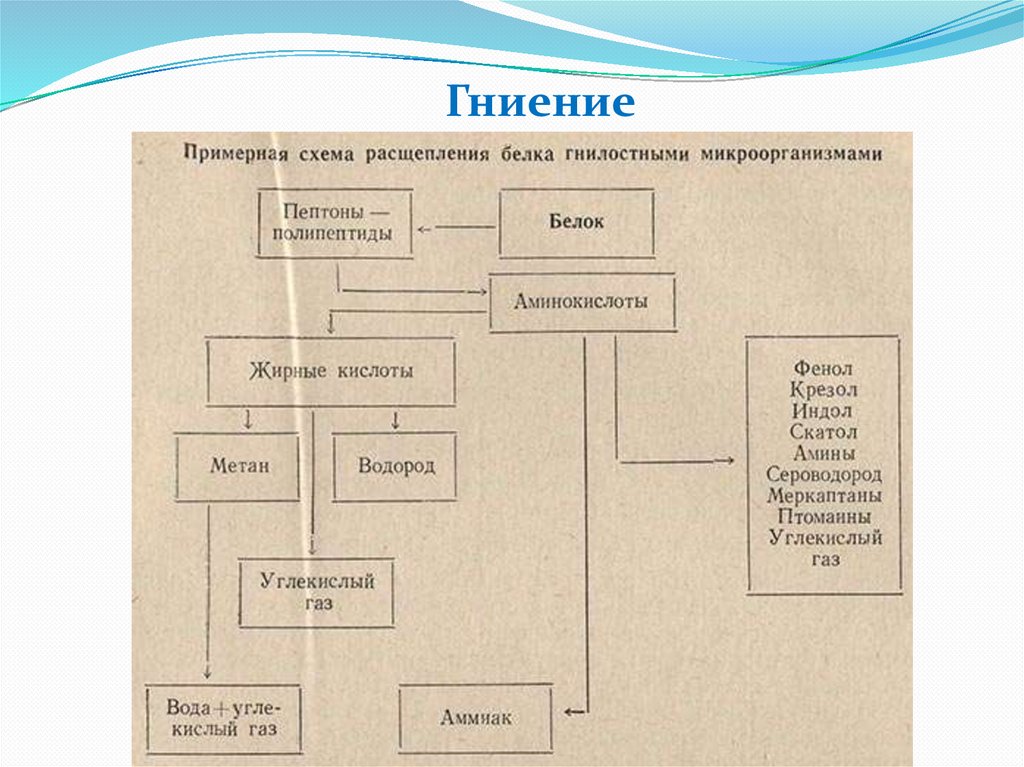
Гниение46.
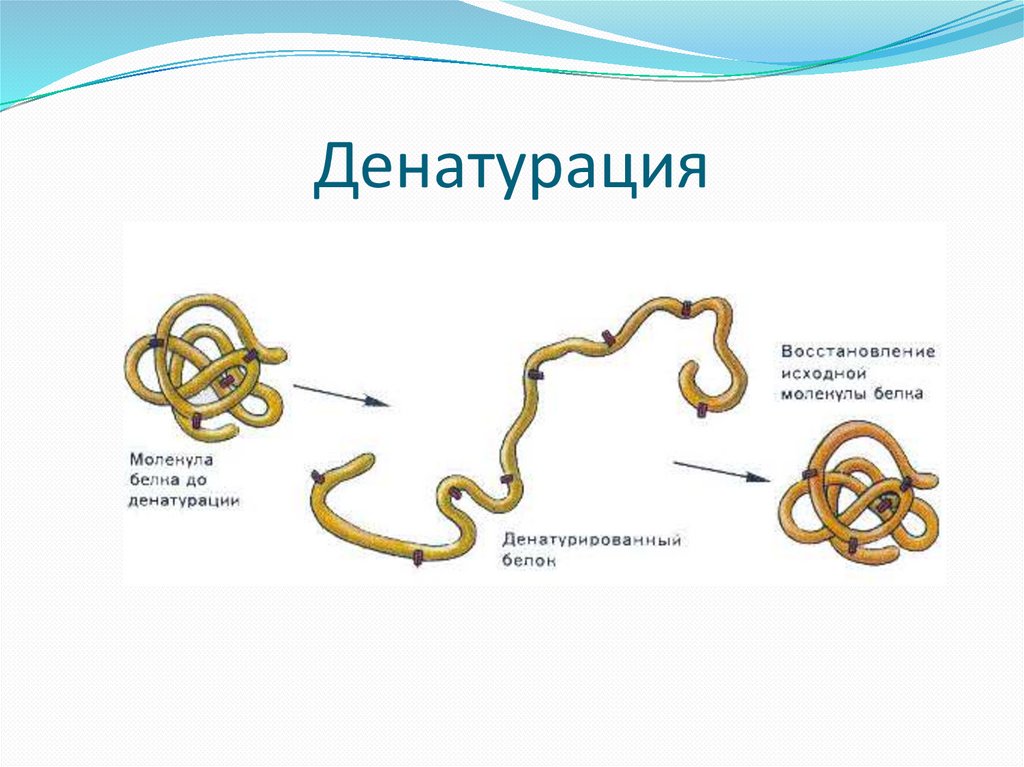
Денатурация47.
Гидролиз48.
49.
Биуретовая реакцияКачественная реакция на пептидные связи
Белок
Гидроксид Внутрикомплексное
меди (II)
соединение
50.
Ксантопротеиновая реакцияКачественная реакция на ароматические циклы
Белок
Азотная
кислота
конц.
Комплексное
соединение
51.
Реакция на серу (Фоля)Белок
Нитрат
свинца
Плюмбат серы
52.
Домашнее заданиеРазработка тестов по темам:
Использование гидролиза белков в
промышленности.
Аминокапроновая кислота.
Капрон как представитель полиамидных волокон.
































 Химия
Химия








