Похожие презентации:
Химическое уравнение. Количество реакции вещества
1.
2Na + 2H2O = 2NaOH + H2↑Химическое уравнение
m V
Количество реакции
вещества
2.
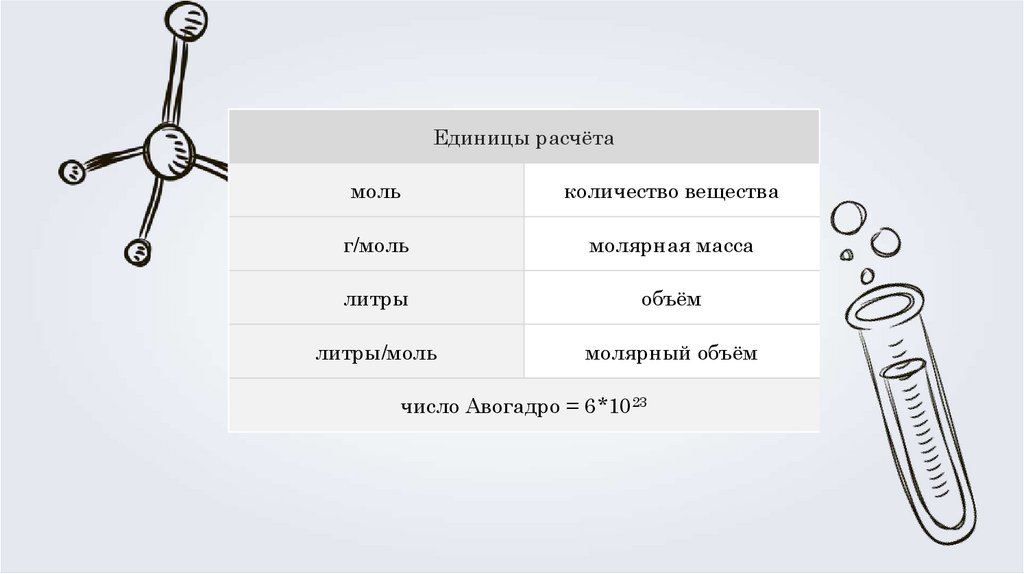
Единицы расчётамоль
количество вещества
г/моль
молярная масса
литры
объём
литры/моль
молярный объём
число Авогадро = 6*1023
3.
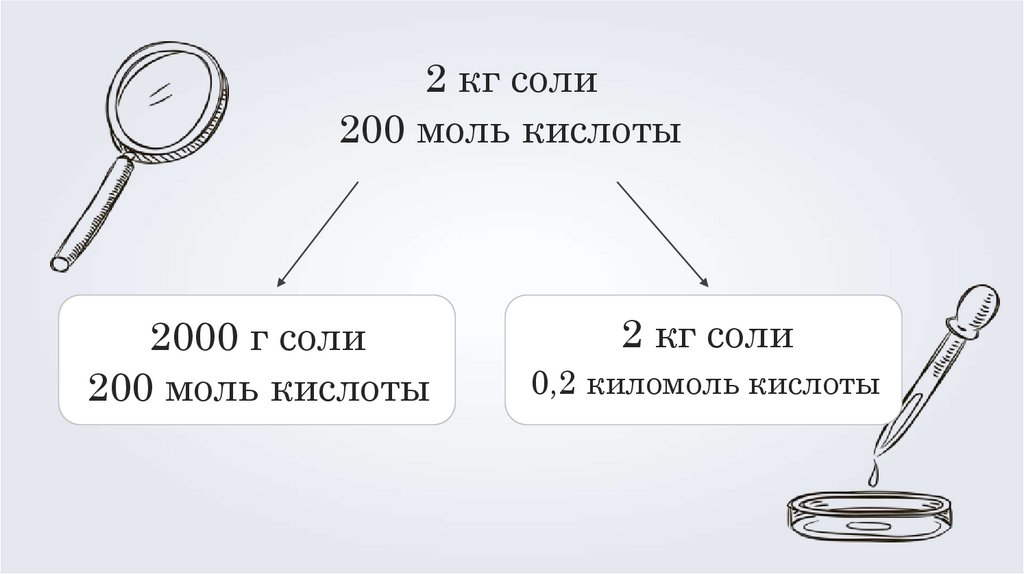
2 кг соли200 моль кислоты
2000 г соли
200 моль кислоты
2 кг соли
0,2 киломоль кислоты
4.
Алгоритм решения расчетных задач поуравнению реакции:
1. Составление уравнения реакции.
2. Привидение данных задачи (массы,
объёма) в соответствие с количеством
вещества в уравнении реакции.
3. Обозначение найденных данных и то, что
необходимо найти над формулами
соответствующих веществ через х икс и у
игрек.
4. Нахождение количества исходных
веществ.
5. Ответ.
5.
Задача 1Решение:
Дано:
2Na + 2H2O = 2NaOH + H2↑
m (Na) = 2,3 г
m (NaOH) — ?
2,3 г
x
2Na + 2H2O = 2NaOH + H2↑
M (Na) = 2,3 г/моль
m (Na) = M (Na) ⋅ n (Na)
m (Na) = 2 моль ⋅ 23 г/моль = 46 г.
M (NaОН) = 23 + 16 +1 = 40 г/моль
m (NaОH) = 2 моль ⋅ 40 г/моль = 80 г.
46 г — 80 г
2,3 г — x
Ответ: m (NaOH) =4 г.
6.
Задача 2Решение:
Дано:
СаСО3 = СаО + СО2↑
m (СaO) = 223 т
m (СaCO 3) — ?
t
x
t
223 т
СаСО3 = СаО + СО2↑
M (CaCo3) = 40 + 12 + 16 ⋅ 3 = 100 т/кмоль
M (CaO) = 40 + 16 = 56 т/моль
m=M⋅n
m (CaCО3) = 1 кмоль ⋅ 100 т/кмоль = 100 т
m (CaО) = 1 кмоль ⋅ 56 т/кмоль = 56 т
100 т — 56 т
x т — 224 т
Ответ: m (СaCO 3) = 400 т.
7.
Задача 3Решение:
Дано:
2ZnS + 3O2 = 2ZnO + 2SO2
m (ZnS) = 300 г
V m = 22,4 л
300 г
V—?
n—?
2ZnS + 3O2 = 2ZnO + 2SO2
M (ZnS) = 65 + 32 = 97 г/моль
V (O 2) — ?
n (ZnO) — ?
ZnS
O2
2 моль — 2 моль
3 моль — х моль
ZnS
ZnO
2 моль — 2 моль
3 моль — х моль
Ответ: V(O2) = 100,8 л ; n (ZnO) = 3 моль.





 Химия
Химия








