Похожие презентации:
Классификация химических реакций в неорганической химии
1. Классификация химических реакций в неорганической химии
КЛАССИФИКАЦИЯХИМИЧЕСКИХ РЕАКЦИЙ В
НЕОРГАНИЧЕСКОЙ ХИМИИ
2. Химические реакции
ХИМИЧЕСКИЕ РЕАКЦИИЭто химические процессы, в результате
которых из одних веществ образуются
другие, отличающиеся от них по составу и
(или) строению.
При химических реакциях обязательно
происходит изменение веществ, при котором
рвутся старые и образуются новые связи между
атомами
Реагенты
Продукты
3. Закон сохранения массы
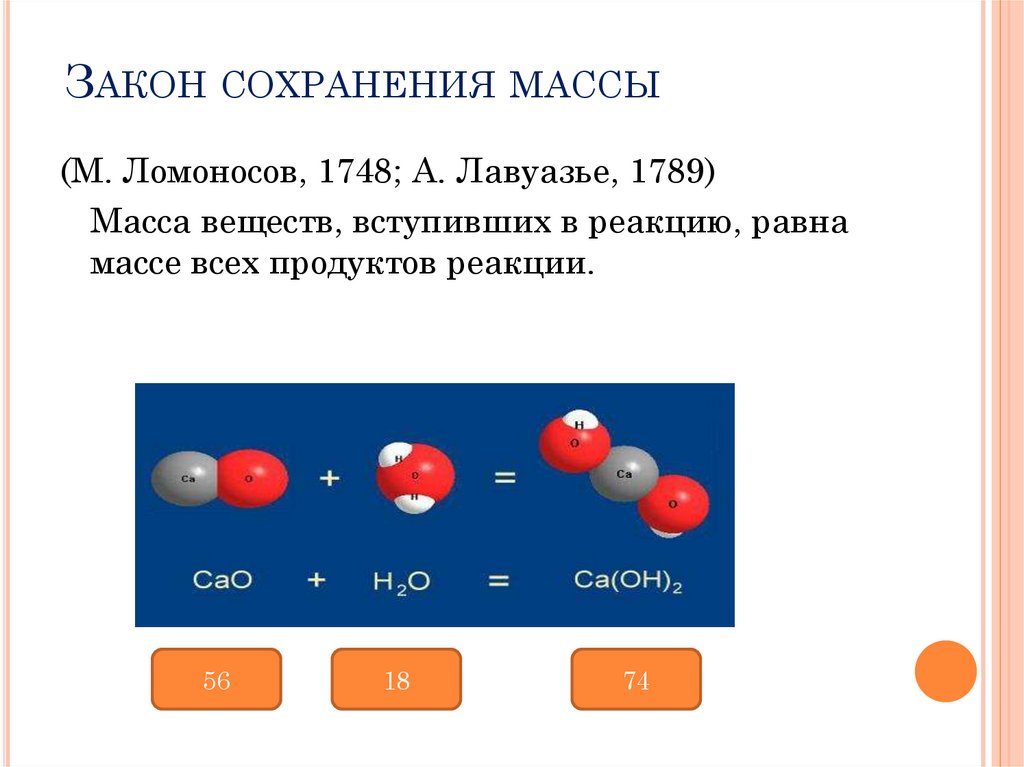
ЗАКОН СОХРАНЕНИЯ МАССЫ(М. Ломоносов, 1748; А. Лавуазье, 1789)
Масса веществ, вступивших в реакцию, равна
массе всех продуктов реакции.
56
18
74
4. Условия проведения химических реакций
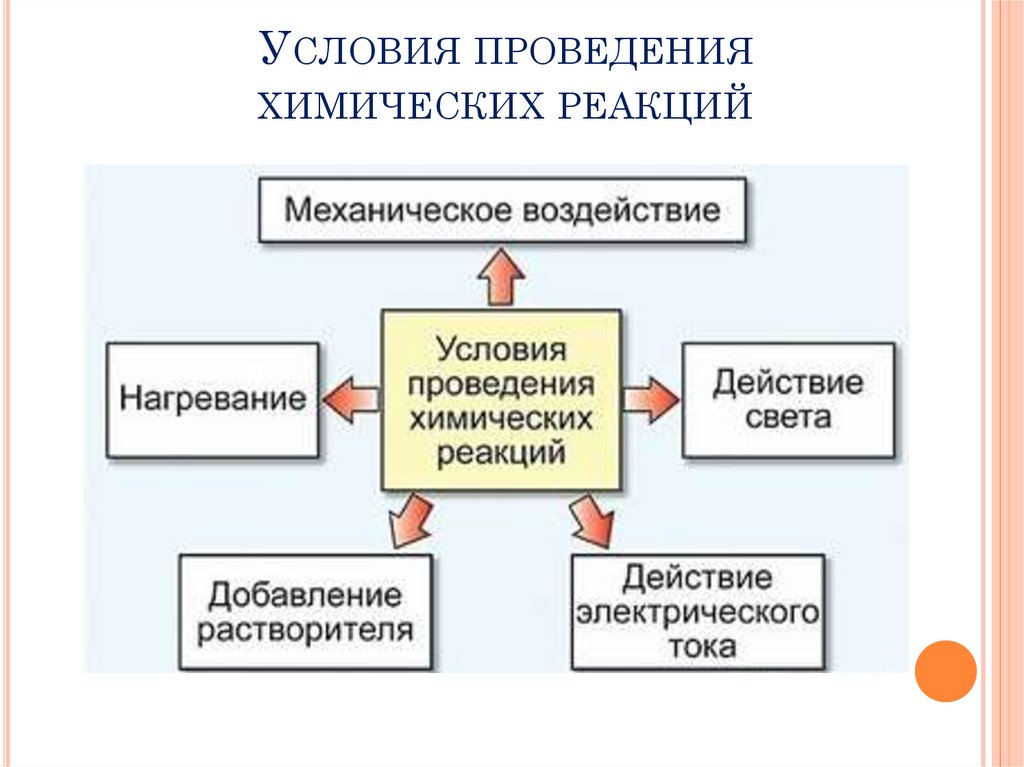
УСЛОВИЯ ПРОВЕДЕНИЯХИМИЧЕСКИХ РЕАКЦИЙ
5. Признаки химических реакций
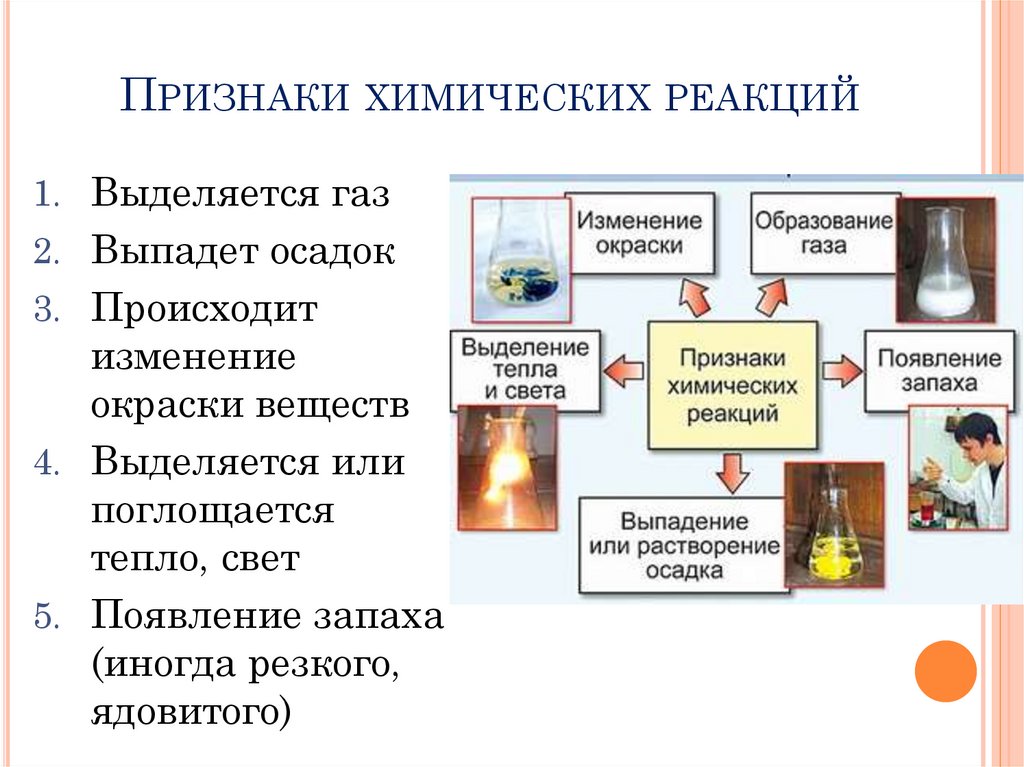
ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ1. Выделяется газ
2. Выпадет осадок
3. Происходит
изменение
окраски веществ
4. Выделяется или
поглощается
тепло, свет
5. Появление запаха
(иногда резкого,
ядовитого)
6. Типы химических реакций
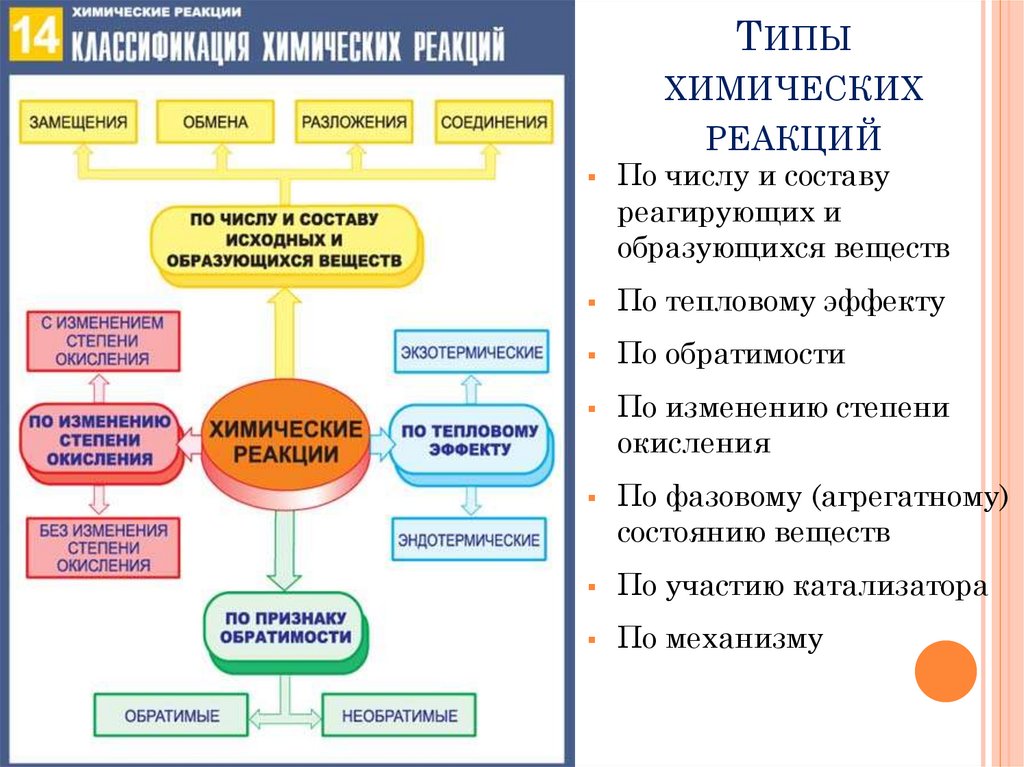
ТИПЫХИМИЧЕСКИХ
РЕАКЦИЙ
По числу и составу
реагирующих и
образующихся веществ
По тепловому эффекту
По обратимости
По изменению степени
окисления
По фазовому (агрегатному)
состоянию веществ
По участию катализатора
По механизму
7. 1. По составу реагирующих веществ:
1. ПО СОСТАВУ РЕАГИРУЮЩИХ ВЕЩЕСТВ:Реакции, идущие без изменения состава
веществ
В неорганической химии к таким реакциям можно
отнести процессы получения аллотропных модификаций
одного химического элемента, например:
С (графит) <=> С (алмаз)
3О2 (кислород) <=> 2О3 (озон)
Sn (белое олово) <=> Sn (серое олово)
S (ромбическая) <=> S (пластическая)
Р (красный) <=> Р (белый)
В органической химии это реакции изомеризации:
СН3 СН 2 СН 2 СН3
AlCl3 ;100 C
CН 3 СН СН3
|
СН 3
Реакции, идущие с изменением состава вещества
Реакции разложения
Реакции соединения
Реакции замещения
Реакции обмена
8. 2. По числу вступивших в реакцию веществ
2. ПО ЧИСЛУ ВСТУПИВШИХ В РЕАКЦИЮВЕЩЕСТВ
Реакции
соединения
Реакции
разложения
Реакции
замещения
Реакции
обмена
Из нескольких
веществ образуется
одно новое вещество
Из одного вещества
образуется несколько
новых веществ
Атомы простого
вещества замещают
атомы одного из
элементов в сложном
веществе
Два сложных
вещества
обмениваются своими
составными частями
Zn + 2HCl =
NaOH + HCl =
= NaCl + H2O
где NaOH – гидроксид
натрия,
NaCl – хлорид натрия
S + O2 = SO2
где SO2 - оксид серы (IV)
t
CaCO3 CaO CO2
где CaCO3 - карбонат
кальция
= ZnCl2 + H2↑
где HCl – соляная
кислота,
ZnCl2 - хлорид цинка
9. Реакции соединения -
РЕАКЦИИ СОЕДИНЕНИЯ это реакции, в результате которых из двух илинескольких простых или сложных веществ
образуется одно более сложное.
- С + О2 →CO2
- 2Сu + O2 →2CuO
- Na2O + CO2 → Na2CO3
-
10. Реакции разложения -
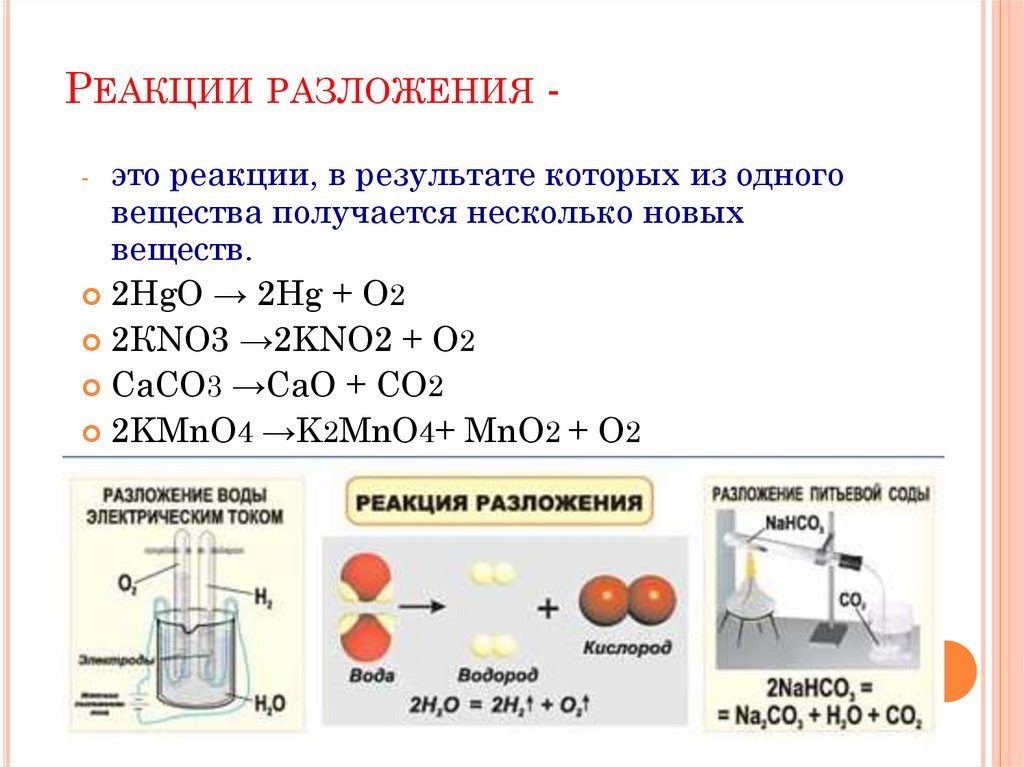
РЕАКЦИИ РАЗЛОЖЕНИЯ это реакции, в результате которых из одноговещества получается несколько новых
веществ.
2HgO → 2Hg + O2
2КNO3 →2KNO2 + O2
CaCO3 →CaO + CO2
2KMnO4 →K2MnO4+ MnO2 + O2
-
11. Реакции замещения -
РЕАКЦИИ ЗАМЕЩЕНИЯ -это реакции между простым и сложным
веществом, в результате которых атомы
простого вещества замещают атомы одного из
химических элементов в сложном веществе.
Zn +2HCl → ZnCl2 +H2
- CuSO4 + Fe →Cu + FeSO4
- 2Na + 2H2O →2NaOH + H2
-
12. Реакции обмена -
РЕАКЦИИ ОБМЕНА -это реакции, между двумя сложными
веществами, при протекании которых их
молекулы обмениваются своими составными
частями.
CuSO4 + 2NaOH→Сu(OH)2↓+ Na2SO4
- 2HNO3 + Ba(OH)2→ Ba(NO3)2 + 2Н2О
- NH4Cl + KOH → KCl + NH3↑+ H2O
-
13. 3. По тепловому эффекту
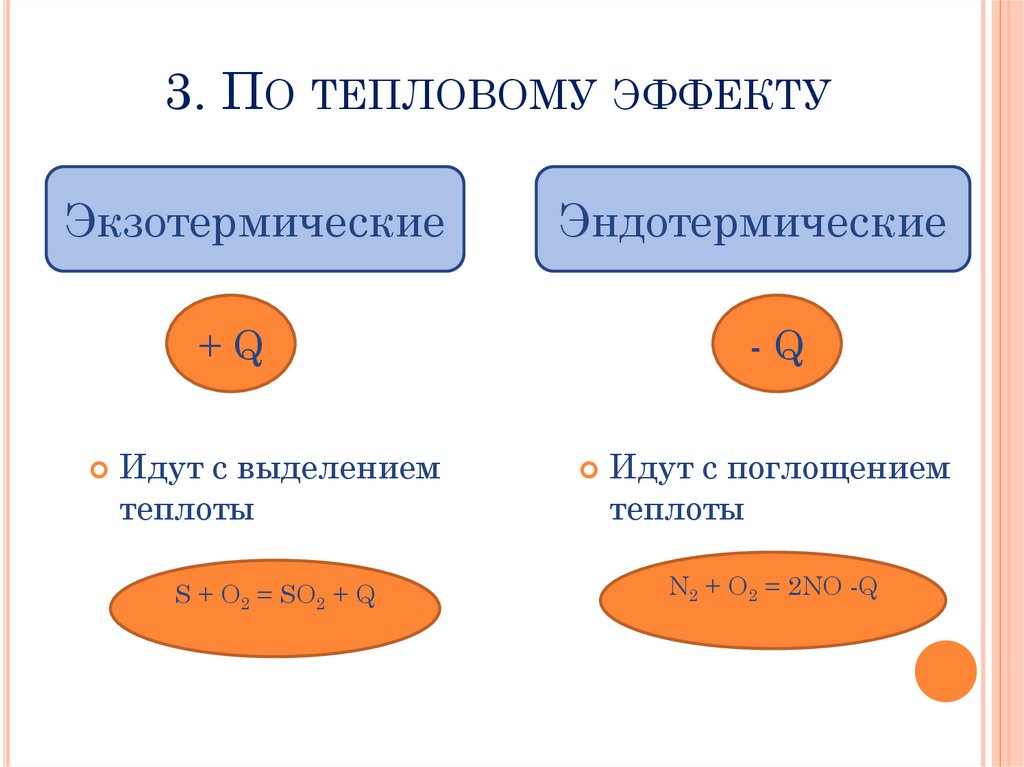
3. ПО ТЕПЛОВОМУ ЭФФЕКТУЭкзотермические
Эндотермические
+Q
-Q
Идут с выделением
теплоты
S + O2 = SO2 + Q
Идут с поглощением
теплоты
N2 + O2 = 2NO -Q
14. По тепловому эффекту
ПО ТЕПЛОВОМУ ЭФФЕКТУЭкзотермические реакции
Экзотермические реакции – реакции, протекающие с
выделением энергии во внешнюю среду. К ним относятся почти все
реакции соединения. Экзотермические реакции, которые протекают
с выделением света, относят к реакциям горения, например:
4Р + 5О2 = 2Р2О5 + Q
Эндотермические реакции
Эндотермические реакции – реакции, протекающие с
поглощением энергии. К ним относятся почти все реакции
разложения, например:
t
Обжиг известняка:
СаСО3 CaO + CO2 - Q
Уравнение химической реакции с указанием теплового
эффекта называют термохимическим уравнением, например:
H2(г)+ Cl2(г) = 2HCl(г) + 92.3 кДж
N2(г) + O2(г) = 2NO – 90.4 кДж
15. 4. По обратимости
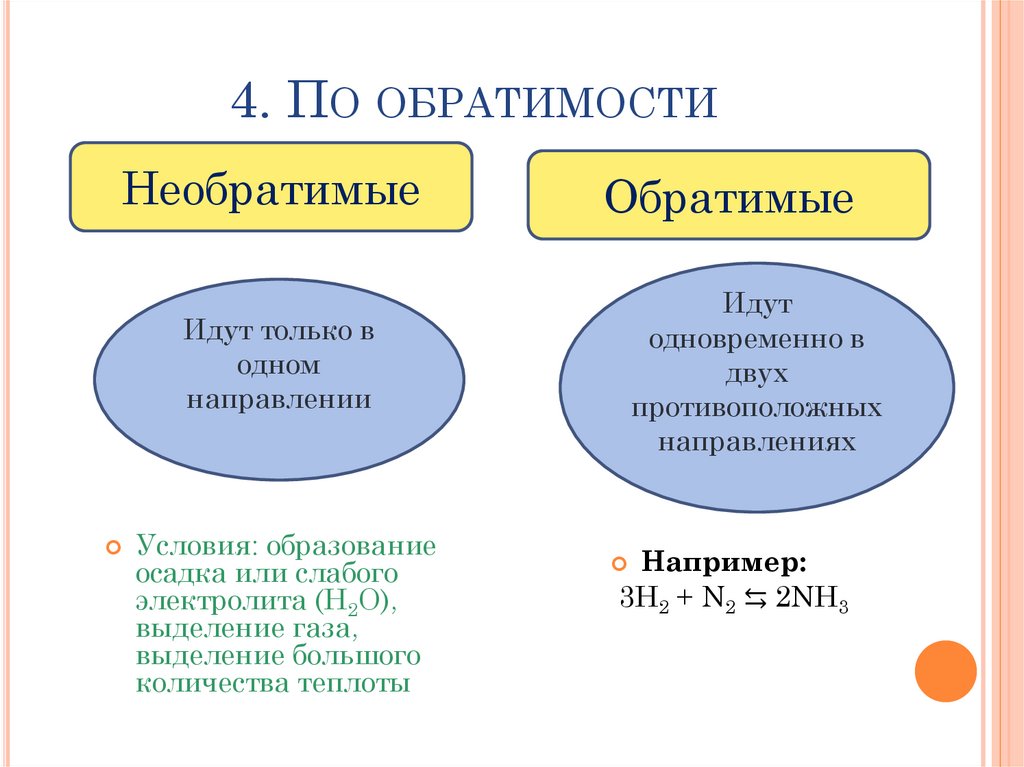
4. ПО ОБРАТИМОСТИНеобратимые
Идут только в
одном
направлении
Условия: образование
осадка или слабого
электролита (Н2О),
выделение газа,
выделение большого
количества теплоты
Обратимые
Идут
одновременно в
двух
противоположных
направлениях
Например:
3H2 + N2 ⇆ 2NH3
16.
Необратимые реакции:Необратимые реакции протекают в данных условиях только
в одном направлении. К таким реакциям можно отнести все
реакции обмена, сопровождающиеся образованием осадка, газа или
малодиссоциирующего вещества (воды) и все реакции горения.
H 2 SO4 BaCl 2 BaSO4 2 HCl
Обратимые реакции
Обратимые реакции в данных условиях протекают
одновременно в двух противоположных направлениях. Таких
реакций подавляющее большинство. Например:
2SO2 + O2 <=> 2SO3
N2 +3H2 <=> 2NH3
В органической химии: гидрирование-дегидрирование,
гидратация-дегидратация, полимеризация-деполимеризация,
этерификация-гидролиз и т.д.
17. 5. По изменению степени окисления
5. ПО ИЗМЕНЕНИЮ СТЕПЕНИОКИСЛЕНИЯ
Окислительно –
восстановительные
реакции
Без изменения
степени окисления
элементов
Идут с изменением
CaCO3 = CaO + CO2
степени окисления
2Na + Cl2 = 2NaCl
18.
Окислительно-восстановительные реакцииОВР–
реакции,
идущие
с
изменением
степеней
окисления элементов.
К ним относится множество реакций, в том числе все
реакции замещения, а также те реакции соединения и
разложения, в которых участвует хотя бы одно простое
вещество:
0
+1
+2
0
0
а) Mg + H2SO4 = MgSO4 + H2
0
+2
+1
0
Mg – 2e¯ Mg – окисление
2Н + 2e¯ H2 – восстановление
0
+2 -2
б) 2Мg + O2 = 2MgO
0
+2
Mg – 2e¯ Mg
окисление
0
-2
O2 + 4e¯ 2O
восстановление
2
1
19. Не окислительно-восстановительные реакции
НЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИНе
окислительно-восстановительные
реакции
–
реакции, идущие без изменения степеней окисления
элементов.
К ним относятся все реакции ионного обмена, например:
Na2CO3 + 2HCl = 2NaCl + Н2СО3
многие реакции соединения :
Li2O + H2O = 2LiOH
а также многие реакции разложения:
t
2Fe(OH)3 Fe 2O3 + 3H2O
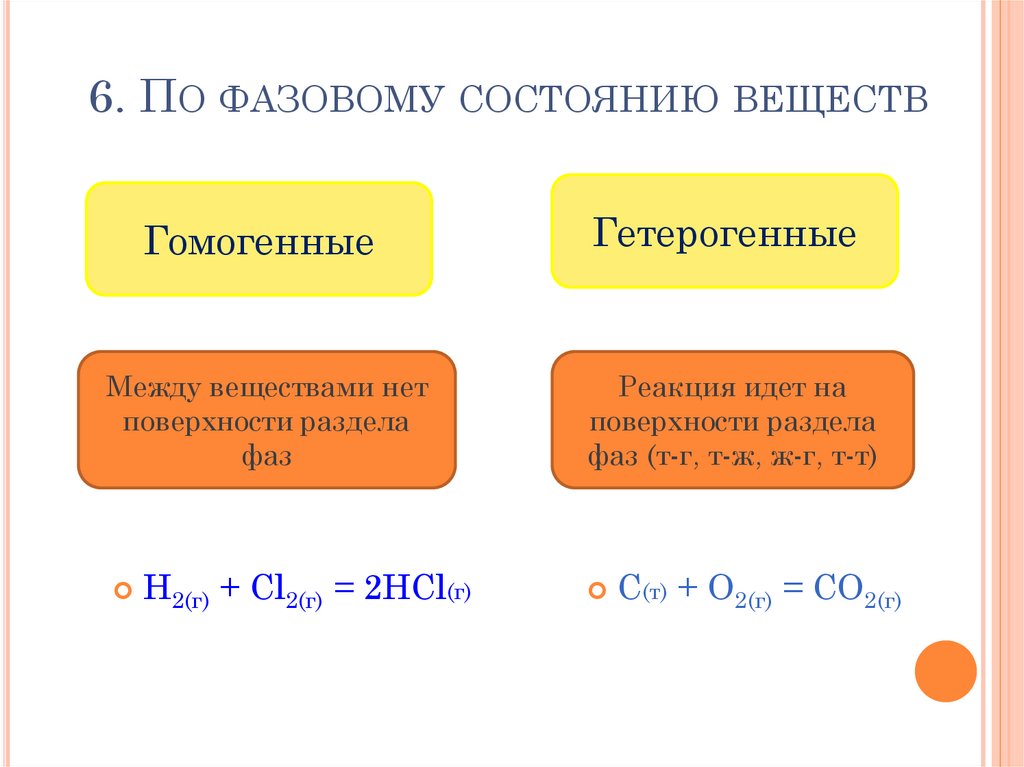
20. 6. По фазовому состоянию веществ
6. ПО ФАЗОВОМУ СОСТОЯНИЮ ВЕЩЕСТВГомогенные
Гетерогенные
Между веществами нет
поверхности раздела
фаз
Реакция идет на
поверхности раздела
фаз (т-г, т-ж, ж-г, т-т)
H2(г) + Cl2(г) = 2HCl(г)
С(т) + О2(г) = СО2(г)
21. По фазовому состоянию реагирующих веществ
ПО ФАЗОВОМУ СОСТОЯНИЮРЕАГИРУЮЩИХ ВЕЩЕСТВ
Гетерогенные реакции:
Гетерогенные реакции – реакции, в которых реагирующие
вещества и продукты реакции находятся в разных агрегатных состояниях
(в разных фазах):
FeO(т) + СО(г) Fe(т) + СО2(г) + Q
2Al(т) + 3СuСl2 (р-р) = 3Сu(т) + 2AlCl3(р-р)
CaC2(т) + 2H2O(ж) = C2H2 + Ca(OH)2(р-р)
Гомогенные реакции:
Гомогенные реакции – реакции, в которых реагирующие
вещества и продукты реакции находятся в одном агрегатном
состоянии (в одной фазе):
2С2Н6(г) + 7О2(г) 4СО2(г) + 6Н2О(г)
2 SO2(г) + O2(г) = 2SO3(г) +Q
H2(г) + F2(г) = 2HF(г)
22. 7. По участию катализатора:
7. ПО УЧАСТИЮ КАТАЛИЗАТОРА:Катализаторы – это вещества, участвующие в химической
реакции изменяющие ее скорость или направление, но по
окончании реакции остающиеся неизменными качественно и
количественно.
Некаталитические реакции:
Некаталитические реакции - реакции, идущие без участия
катализатора:
t
2HgO 2Hg + O2
t
2Al + 6HCl 2AlCl3 + 3H2
Каталитические реакции:
Каталитические реакции – реакции, идущие с участием
катализатора:
H2O
2Al + 3I2 2AlI3
t,MnO2
2KClO3 2KCl + 3O2
P,t
CO + NaOH H-CO-ONa
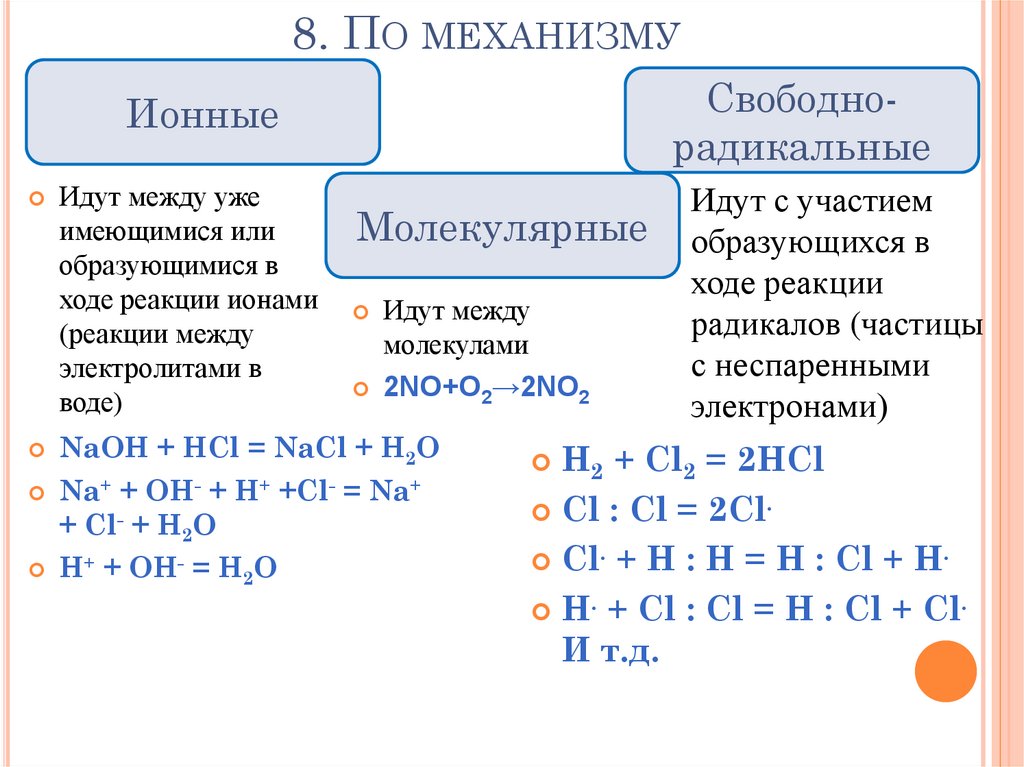
23. 8. По механизму
8. ПО МЕХАНИЗМУСвободнорадикальные
Ионные
Идут между уже
имеющимися или
образующимися в
ходе реакции ионами
(реакции между
электролитами в
воде)
Молекулярные
Идут между
молекулами
2NO+O2→2NO2
NaOH + HCl = NaCl + H2O
Na+ + OH- + H+ +Cl- = Na+
+ Cl- + H2O
H+ + OH- = H2O
Идут с участием
образующихся в
ходе реакции
радикалов (частицы
с неспаренными
электронами)
H2 + Cl2 = 2HCl
Cl : Cl = 2Cl.
Cl. + H : H = H : Cl + H.
H. + Cl : Cl = H : Cl + Cl.
И т.д.
24. Закрепление.
ЗАКРЕПЛЕНИЕ.1. Расставьте коэффициенты в следующих
уравнениях реакций. Определите типы реакций:
1.
СаСО3 → СаО + CO2
2.
Na2SO4 + ВаСl2 → NaСl + ВаSO4
3.
SO3 + H2O → H2SO4
4.
Cu +HNO3(конц) →Cu(NO3)2 + NO2↑+ H2O
5.
Fe(OH)3 → Fe2O3 + H2O
6.
Аl2(SO4)3 + NaOH → Na2SO4 + Аl(OH)3↓
25. Закрепление.
ЗАКРЕПЛЕНИЕ.2. Напишите уравнения реакций по названиям
исходных веществ и продуктов реакций.
Определите типы реакций.
Сульфат магния + гидроксид натрия →
гидроксид магния + сульфат натрия.
Хлорид калия + нитрат серебра →
нитрат калия + хлорид серебра.
Железо + соляная кислота →
хлорид железа (II) + водород.
Оксид меди + оксид азота (V) → нитрат меди.
Железо + сера → сульфид железа (II).















 Химия
Химия








