Похожие презентации:
Кислородсодержащие органические вещества. Спирты
1.
2.
Это органические соединения, в молекулах которыхуглеводородный радикал связан с функциональной
гидроксильной группой (гидроксо-группой)
Общая формула
C n H 2n + 1 OH или R – OH,
где R- углеводородный радикал
СН3ОН метанол (метиловый спирт)
СН3СН2ОН этанол (этиловый спирт)
3.
Название спирта образуется от названиясоответствующего алкана с добавлением
суффикса –ол
СН4 - метан => СН3ОН – метанол
С2Н6 – этан => С2Н5ОН – этанол
4.
5.
6.
7.
Углеродногоскелета
Межклассовая
(простые
эфиры
R – О - R)
Положения
функциональной группы
Виды
изомерии
8.
СН3 - СН2 - СН2 - ОНПропанол -1
СН3 - СН2 - СН3
Пропанол -2
Изомерия положения функциональной группы
9.
--
10.
11.
Составить формулы изомеров С4Н9ОНСН3 - СН2 - СН2 - СН2 - ОН СН3 - СН2 - СН – СН3
ОН
Бутанол – 1
Бутанол - 2
СН3 - СН - СН2 - ОН
СН3
2-метилпропанол – 1
СН3
СН3 - С – СН3
ОН
2-метилпропанол - 2
СН3СН2 ― О ― СН2СН3 диэтиловый эфир
12.
…О - Н …О - Н …О - Н …О - Н …О - Н …О – Н …R
R
R
R
R
R
Первые члены гомологического ряда спиртов по сравнению с
соответствующими алканами являются жидкостями.
Это объясняется наличием водородных связей между
молекулами спиртов
Связь между атомом водорода одной молекулы и атомом сильно
электроотрицательных элементов ( кислород) другой молекулы
называют водородной
13.
…О - Н …О - Н …О - Н …О - Н …О - Н …О – Н …Н
R
Н
R
Н
R
Первые представители гомологического ряда предельных
одноатомных спиртов (метанол и этанол) очень хорошо
растворяются в воде, так как образуют водородные связи с
молекулами воды
14.
Получение спиртов1) Из галогенопроизводных алканов
а) СН3–СН2–Cl + NaOH→СН3–СН2–OH + NaCl + H2O
б) СН2–СН2 +2NaOH → СН2–СН2+2NaCl +2H2O
|
|
|
|
Cl
Cl
ОН
ОН
15.
Получение спиртов2) Двухатомные спирты (гликоли)
получают окислением алкенов:
СН2=СН2 + [O] + H2O → СН2–СН2
|
|
ОН ОН
этиленгликоль
16.
Получение спиртов3) Одноатомные спирты (алканолы)
получают гидратацией алкенов:
СН2=СН2 + H2O t,H SO
2
4
СН3–СН2
|
ОН
этанол
17.
Правило МарковниковаВодород присоединяется к наиболее
гидрогенизованному атому углерода:
СН2=СН–СН3 + Н-ОН t,H SO
СН3–СН–СН3
2
4
|
ОН
пропанол-2
18.
Химические свойстваCH3 – CH2 - O H
+
Na
H2 ↑
Этилат натрия
2CH3 – CH2 – OH + 2Na → 2CH3 – CH2 – ONa + H2 ↑
19.
Специфические способыполучения спиртов
• Метанол получают из угля в результате
следующих реакций:
С + Н2О t СО + Н2
СО + 2Н2 t, Р, Каt СН3–ОН
• Этанол получают при брожении
глюкозы:
С6Н12О6 дрожжи 2С2Н5–ОН + 2СО2
20.
Химические свойстваспиртов
1. Взаимодействие спирта с
щелочными металлами (замещение):
2СН3–СН2–ОН +2Na →2CH3–CH2–O–Na+H2
21.
Химические свойстваВнутримолекулярная
Н3 - СН2 - ОН
СН
H2SO4, t
+ СН2 = СН2
Межмолекулярная
С2Н5 -ОН
НО- С2Н5
ОН + Н
H2SO4, t
+ С2Н5 -О-С2Н5
22.
Правило ЗайцеваВодород отщепляется от наименее
гидрогенизованного атома углерода:
СН3–СН–СН2–СН3 t,H SO
2
4
|
ОН
→ СН3–СН=СН–СН3 + Н2О
23.
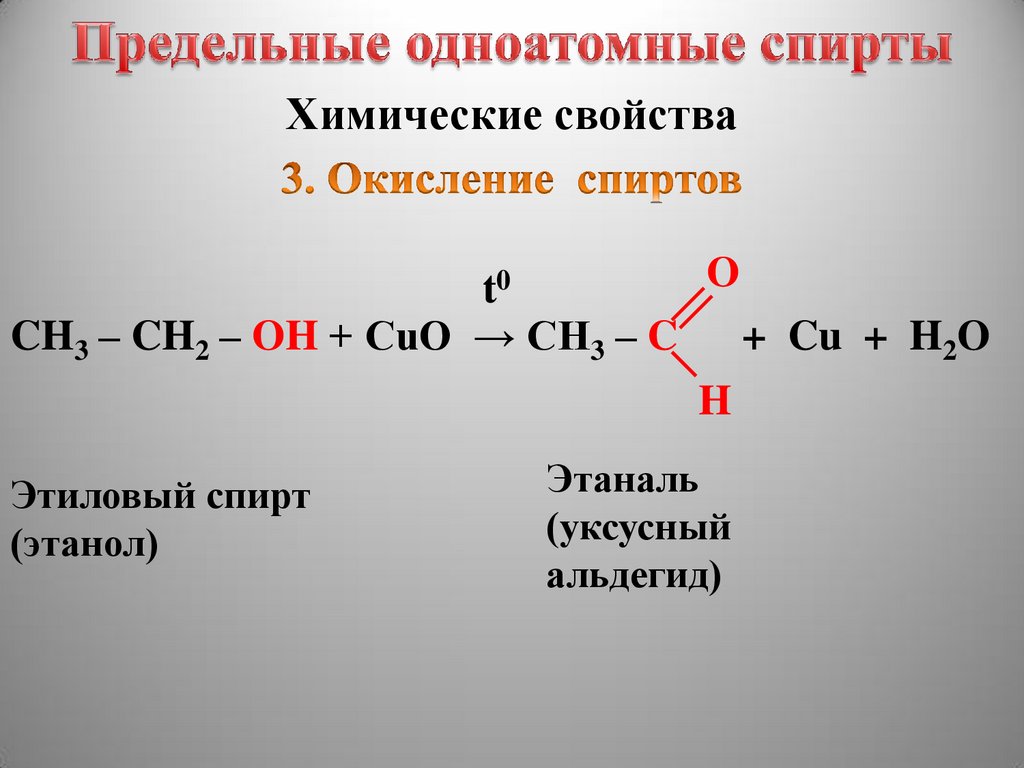
Химические свойстваO
t0
CH3 – CH2 – OH + CuO → CH3 – C
+ Cu + H2O
H
Этиловый спирт
(этанол)
Этаналь
(уксусный
альдегид)
24.
Химические свойстваO
R–C +
H2SO4 ,t0
HO
H -R
O
+ R–C
OH
ОH
Кислота
О-R
Спирт
Сложный эфир
CH3 – CОOH + HОC2H5 ↔ CH3 – СООC2H5 + H2О
уксусная
кислота
этиловый
спирт
этиловый эфир
уксусной кислоты
25.
26.
27.
28.
29.
СН2 - СН2СН2 – СН - СН2
ОН
ОН
ОН
этиленгликоль
ОН
ОН
глицерин
Качественная реакция на многоатомность спиртов
–
взаимодействие со свежеприготовленным голубым осадком
гидроксида меди (+2) при обычных условиях с образованием
ярко-синего раствора
Cu(OH)2
глицерин




























 Химия
Химия








