Похожие презентации:
Природные кислоты и щелочи. Индикаторы. Лабораторный опыт №7 «Изучение кислотности и щелочности среды растворов»
1. Тема урока: Природные кислоты и щелочи. Индикаторы Лабораторный опыт №7 «Изучение кислотности и щелочности среды растворов»
2. Цель обучения:
7.3.4.1 знать, что «кислые» и «мылкие» вещества могут бытьприродными кислотами и щелочами;
7.3.4.2 определять кислоты и щелочи при помощи
универсального индикатора
Критерии оценивания
Определяет кислоту и щелочь по изменению цвета
индикатора
Исследует реакцию кислот и щелочей с помощью
индикаторов
3.
4.
Растворы кислот имеют кислый вкус.Во многих плодах содержатся кислоты,
которые придают им кислый вкус.
В цитрусовых плодахапельсинах,грейпфруктах, лимонахсодержатся- лимонная и аскорбиновая
кислоты, в помидорах-салициловая кислота, в
молоке- молочная кислота.
Отсюда названия кислот- лимонная,
яблочная, молочная, щавелевая и т.д .
5.
Не все кислоты можно пробовать на вкус,среди них встречаются не только
растительного происхождения но и ядовитые
(минеральные кислоты).
Соляная кислота- HCl
Азотная кислота- HNO3
Серная кислота- H2SO4
Фосфорная кислота-H3PO4
Угольная кислота-H2CO3
Все кислоты содержат атомы водорода,
которые участвуют в реакциях с различными
6. Правила техники безопасности
При работе кислотами и щелочами следует соблюдатьособую осторожность, так как они вызывают ожоги и
отравления:
1. В кабинете химии запрещается пробовать вещества на
вкус
2. Кислоты и щелочи при попадании на кожу вызывают
ожоги. При разбавлении кислоты: сначала надо налить в
сосуд воду, затем кислоту, а не наоборот
3. Пораженный кислотой или щелочью участок кожи следует
промыть струей воды
4. Забор кислоты или щелочи производите отдельными
пипетками.
5. Работайте аккуратно над столом.
7.
В составе желудочного сока содержитсясоляная кислота.
Избыток ее (повышенная кислотность)
вызывает изжогу в организме.
Если соляной кислоты ниже нормы, то у
человека пониженная кислотность.
Соляная кислота- необходима для быстрого
переваривания пищи, для уничтожения
вредных бактерий, которые попадают вместе
с пищей.
Больным с повышенной кислотностью
выписывают антацидные препараты- оксид
магния, карбонат магния, гидроксид
алюминий.
8.
Антацидные средства (греч. anti - против + лат.acidum- кислота) – лекарственные средства,
снижающие кислотность желудочного
содержимого путем нейтрализации соляной
кислоты желудочного сока.
Азотная, серная, фосфорная кислоты применяют в
получении минеральных удобрений, красителей,
взрывчатых веществ, а раствор угольной кислоты входит в
состав различных напитков
9.
Щелочи- едкие вещества, которые разъедаютмногие органические вещества, при работе с
ними необходимо соблюдать особую
осторожность.
Гидроксид натрия- NaOH
Гидроксид калия-KOH
Гидроксид кальция-Ca(OH)2
Растворы щелочей мылкие на ощупь.
10.
Открытие индикаторовВпервые применение индикаторов
описал английский ученый Роберт
Бойль (1627–1691). Он заметил, что
отвары цветов некоторых растений в
растворах кислот и щелочей
приобретают неодинаковую окраску.
А произошло это так: В лабораторию
зашёл садовник. Он принес корзину с
фиалками. Бойль очень любил цветы, но
предстояло начать опыт. Он взял
несколько цветков, понюхал и положил
их на стол. Опыт начался, открыли колбу,
из нее повалил едкий пар. Когда же опыт
кончился, Бойль случайно взглянул на
цветы, они дымились. Чтобы спасти
цветы, он опустил их в стакан с водой. И
– что за чудеса- фиалки, их темнофиолетовые лепестки, стали красными.
Случайный опыт? Случайная находка?
11.
Индикаторы – это вещества, которые изменяют свой цвет взависимости от реакции среды.
Лакмус
Метиловый оранжевый
Фенолфталеин
«Реактив-хамелеон:
В щелочах синеет он,
В кислоте опасной
Он окрашен в
красный..
«От щелочи я желтею,
как в лихорадке, Краснею
от кислот, как от стыда. И
я бросаюсь в воду без
оглядки, Здесь я
оранжевый практически
всегда»
«Попасть в кислоту для
других неудача, Но он
перетерпит без вздохов, без
плача, Зато в щелочах у
фенолфталеина
Не жизнь, а малина,
сплошная малина!»
С помощью индикаторов можно не только распознать кислоту
или щелочь, но и определить кислотность среды- pH
12.
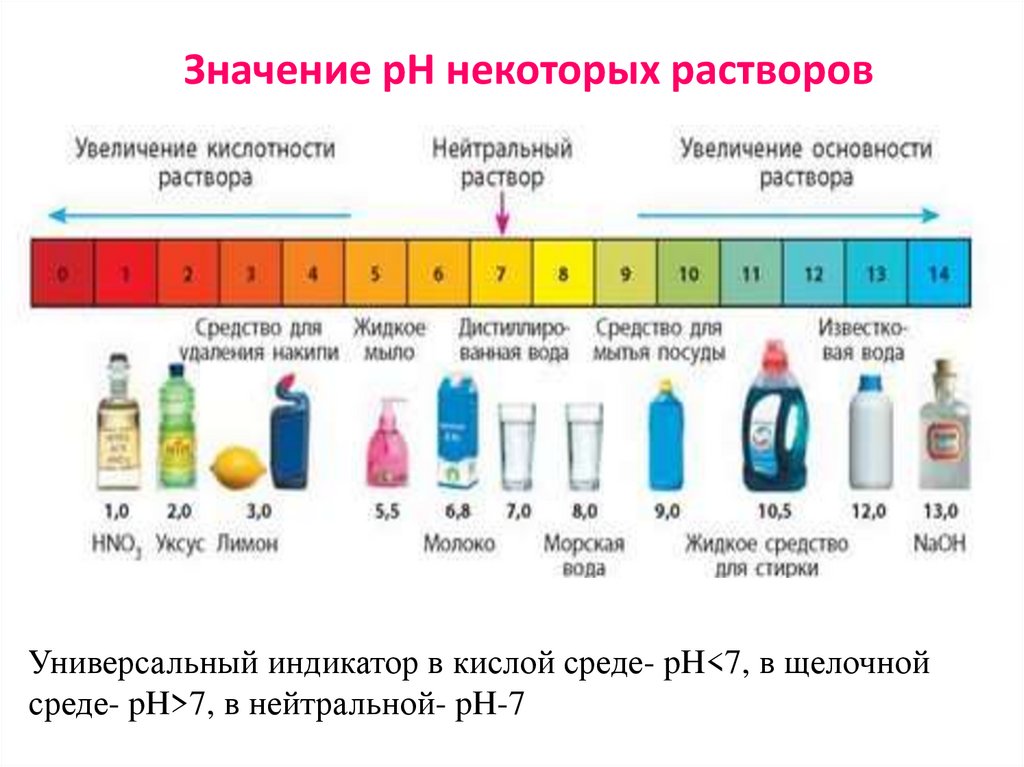
Значение рН некоторых растворовУниверсальный индикатор в кислой среде- pH<7, в щелочной
среде- pH>7, в нейтральной- pH-7
13.
Природные индикаторыЯгоды малины
Кора крушины
Краснокочанная капуста













 Химия
Химия








