Похожие презентации:
Водород. Жан-Франсуа Пилатр де Розье
1.
2. Отгадайте о чём идёт речь
Я, газ, легчайший и бесцветный,Неядовитый и безвредный,
Соединяясь с кислородом,
Я для питья даю вам воду!
3. Водород
4.
«гидрогениум»5. Осторожно: ВОДОРОД!
Обычно легок и летуч,Он вдруг становится могуч:
Его нагрев, неосторожно
Взорвать в округе все возможно.
Осторожно: ВОДОРОД!
• Смесь водорода с одним объемом
кислорода – гремучий газ
• Смесь водорода и воздуха –
взрывоопасна!
6.
• Франц.химик Жан Франсуа Пилатр деРозье Как-то решил проверить, что будет,
если вдохнуть водород. До него никто
такого эксперимента не проводил. Не
заметив никакого эффекта, ученый решил
убедиться, проник ли водород в легкие?
Он ещё раз глубоко вдохнул этот газ, а
затем выдохнул его на огонь свечи,
ожидая увидеть вспышку пламени.
Однако водород в легких
экспериментатора смешался с воздухом и
произошел сильный взрыв. “Я думал, что
у меня вылетели все зубы вместе с
корнями”, - так Розье характеризовал
испытанные ощущения. Эксперимент чуть
не стоил ему жизни.
7.
Пилатр де Розье был первым официальнопризнанным человеком, взлетевшим на
воздушном шаре и первой жертвой
катастрофы этого ненадежного
летательного аппарата.
8. Жан-Франсуа Пилатр де Розье
9.
• Розье задумал преодолеть по воздуху ЛаМанш, для чего построил комбинированныйаэростат. Его оболочка была поделена на две
части, одна из которых была наполнена
водородом, а вторая подогретым воздухом.
Такая конструкция облегчала процесс
управления полетом. И вот в июне 1785 года
Розье со своим помощником отправились в
свой рекордный полет. Увы, он закончился
трагически, аэростат загорелся в воздухе и
оба пилота, вместе с горящими остатками
шара утонули в море (хотя по другим данным,
катастрофа произошла еще до того, как они
достигли пролива). Эта трагедия стала первой,
но далеко не последней в истории
воздухоплавания.
10. 1937 г катастрофа дирижабля «Гинденбург»
11. Историческая справка
Водород был известен ещё в XVI векеТеофрасту Парацельсу (1493-1541)
1766 г. – водород открыл Г. Кавендиш
1784 г. – А. Лавуазье назвал водород
hydrogene (др.-греч. hydro genes порождающий воду)
12.
• Катастрофа дирижабля «Гинденбург» произошла 6 мая 1937года в Нью-Джерси, США.На его борту находилось 97 человек. В
результате катастрофы погибло 35 человек.
• Катастрофа потрясла мир и промышленность в области
воздухоплавания и авиации.
• По официальной версии, причиной стала утечка водорода с
последующим его возгоранием, вызванная разрывом
водородного баллона во время приземления дирижабля.
• Катастрофа «Гинденбурга» стала началом конца эры дирижаблей
и заставила страны отказаться от использования водорода в
дирижаблях.
13. 1.Общая характеристика
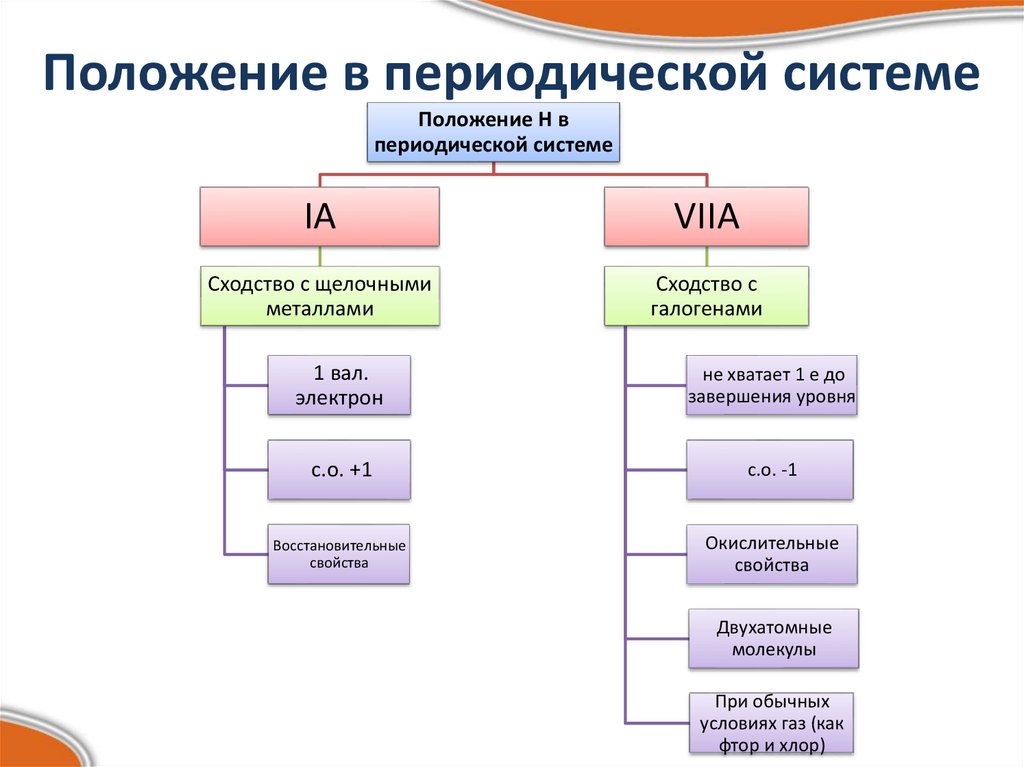
14. Положение в периодической системе
Положение Н впериодической системе
IА
VIIА
Сходство с щелочными
металлами
Сходство с
галогенами
1 вал.
электрон
не хватает 1 е до
завершения уровня
с.о. +1
с.о. -1
Восстановительные
свойства
Окислительные
свойства
Двухатомные
молекулы
При обычных
условиях газ (как
фтор и хлор)
15. 2. Нахождение в природе
Водородная туманность «Сердце»16. 3.Физические свойства
1. Газ без цвета, вкуса изапаха.
2. Легче воздуха в 14,5 раз.
3. Плохо растворим в воде.
17. 4.Получение
Электролизом воды:эл.ток
H2O =
18.
2) Действием разбавленных кислотна металлы:
Zn + HCl =
Zn + H2SO4 =
19.
3) Взаимодействием активныхметаллов с водой:
Na + H2O =
Ca + H2O =
20.
4) Разложением органических веществ :СH4=
С2Н6 =
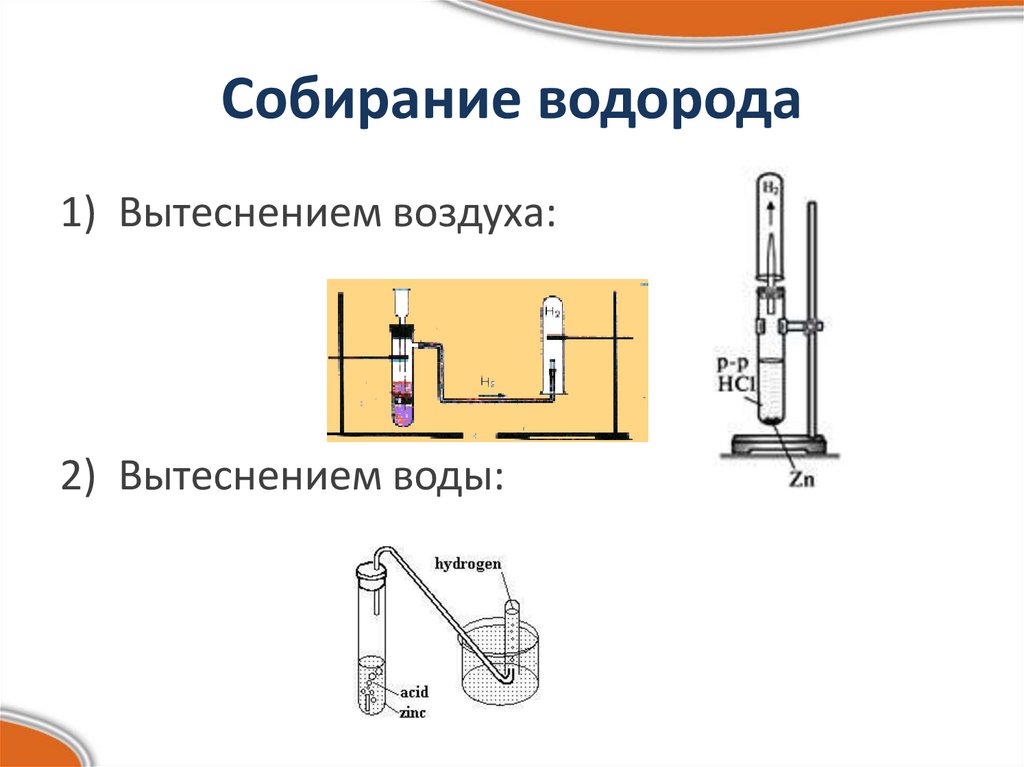
21. Собирание водорода
1) Вытеснением воздуха:2) Вытеснением воды:
22. 4.Химические свойства
23. Взаимодействие с простыми веществами
1.Взаимодействие с неметаллами1. H2 + O2 =
2.H2 + S =
3.N2 + H2 =
4. H2 + F2 =
24.
2.Водород взаимодействует с активнымиметаллами, образуя гидриды:
Na + H2 =
Ca + H2 =
25. Взаимодействие со сложными веществами
• 3.Взаимодействует с оксидамиметаллов
• CuO + H2 =
• Fe2O3 + H2 =
• WO3 + H2 =
26. Применение
1) Химическая промышленность: получениеаммиака, метанола, мыла, пластмасс и др.
27. Применение
2) Пищевая промышленность:а) производство маргарина
б) пищевая добавка Е949 (упаковочный газ)
28. Применение
3) Топливо (ракетное, машинное)29. Применение
4) Военная промышленность (производствоводородных бомб)
30. Применение
5) Резка и сварка металловПламенем водородной горелки
можно резать и сваривать металлы
31. Задание
1. Напишите возможные уравненияреакций:
1) Ba + H2O =
2) Mg + HCl=
3) Cu + H2O =
4) S + NaOH=
5) Li + HCl=
6) K + H2O =
32.
ДОМАШНЕЕ ЗАДАНИЕНапишите возможные уравнения
реакций:
1) Cu + H2 =
2) WO3+ H2=
3) H2 + CI2 =
4) K + H2O =
5) Ag + H2O =
6) Ba + H2 =





























 Химия
Химия История
История








