Похожие презентации:
Многоатомные спирты. 10 класс
1. Многоатомные спирты
10 класс. ХимияУчитель: Грабко Вероника
Николаевна
МБОУ СОШ № 4 г. Балтийск
2.
Феодосий Печерский:«Бесноватый страдает по
неволе и может удостоиться
жизни вечной, а пьяный
страдает по собственной воле
и предан на вечную муку».
К. Ушинский: «Пьяному на
светлой улице темно».
И. Ефимов: «Нет крепких
вин, есть слабые головы».
Н. Семашко: «Можно
сказать, что сколько мужья
выпили водки, столько их
жены и дети пролили слез».
3. Цель урока:
Познакомитьсясо строением, физическими и
химическими свойствами многоатомных спиртов,
значением и применением их в промышленности и в
повседневной жизни;
развить умение составлять структурные формулы
спиртов, записывать уравнения реакций, уметь
составлять генетическую связь с другими классами
органических веществ;
воспитать экологическое сознание, техники
безопасности при работе со спиртами.
4. Устный опрос:
1. Какие вещества называются спиртами?2. По каким признакам их классифицируют?
3. Какое строение имеют одноатомные спирты?
5. Написать формулу:
2,3 - диметилбутанол - 1.3,3 - диметилбутанол - 1.
гексанол - 3.
6. План урока:
Строение и физические свойствамногоатомных спиртов;
Химические свойства многоатомных
спиртов;
Применение спиртов.
7. Определение
Многоатомные спирты –органические соединения, в
молекулах которых
содержится несколько
гидроксильных групп (-ОН),
соединённых с
углеводородным радикалом
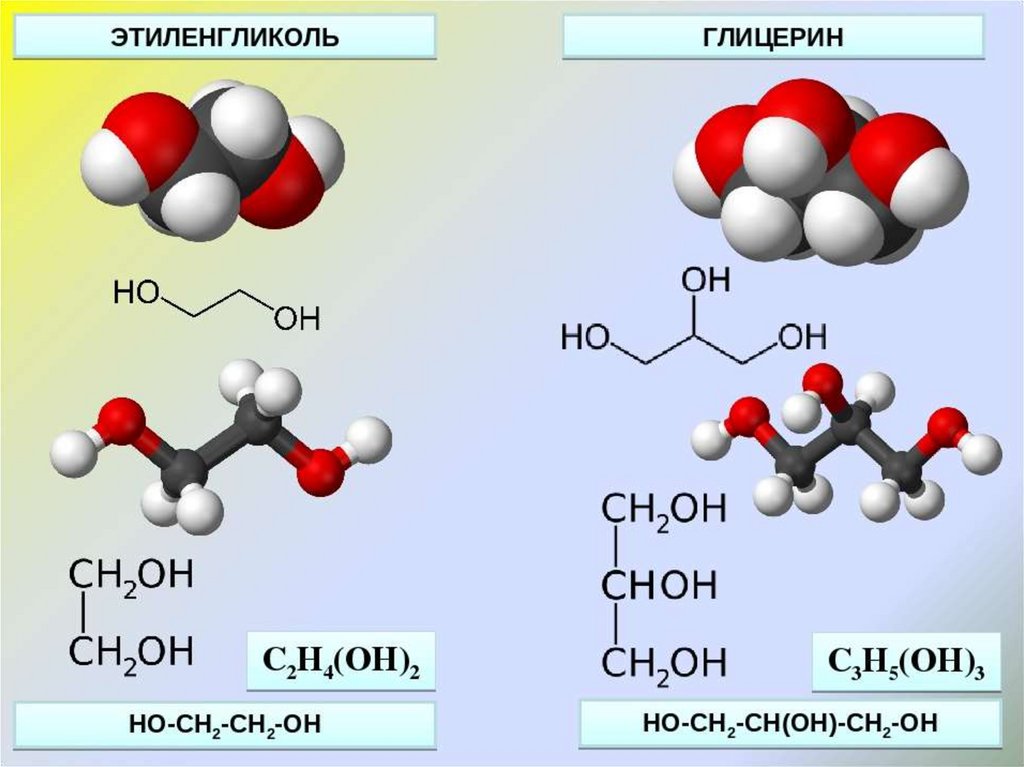
8.
9. Интересный факт
Этиленгликоль - является одним из суррогатовалкоголя. Первые случаи отравления
этиленгликолем в нашей стране отмечены в период
Великой Отечественной войны в 1943-1944 годах,
когда этот препарат в качестве антифриза и
тормозной жидкости стал применяться для
технического обслуживания боевой техники и
танковых войсках. Тогда же антифриз получил
среди бойцов название "бешеное шампанское", что
указывает на крепость и сильное действие
этиленгликоля, а также на наличие в антифризе
пузырьков. Тормозную жидкость тогда же окрестили
"шасси-коньяком" или "ликером Шасси". Названия
сохранились до наших дней. Как и в случае с
другими суррогатами алкоголя, отравления
этиленгликолем обычно носят групповой или
массовый характер.
10.
Физические свойстваСиропообразная, вязкая бесцветная жидкость,
имеет спиртовой запах, хорошо смешивается с
водой, сильно понижает температуру
замерзания воды
(60%-ый раствор
замерзает при -49 ˚С) –это используется в
системах охлаждения двигателей – антифризы.
Этиленгликоль токсичен – сильный Яд!
Угнетает ЦНС и поражает почки.
11. Физические свойства
ТриолыБесцветная, вязкая сиропообразная жидкость,
сладкая на вкус. Не ядовит. Без запаха. Хорошо
смешивается с водой.
Распространён в живой природе. Играет важную
роль в обменных процессах, так как входит в состав
жиров (липидов) животных и растительных
тканей.
12. Номенклатура
В названиях многоатомных спиртов(полиолов) положение и число
гидроксильных групп указывают
соответствующими цифрами и
суффиксами -диол (две ОН-группы), триол (три ОН-группы) и т.д.
13. Например:
14. Получение многоатомных спиртов
I. Получение двухатомных спиртовВ промышленности
1. Каталитическая гидратация оксида этилена
(получение этиленгликоля):
2. Взаимодействие дигалогенпроизводных
алканов с водными растворами щелочей:
15. 3. Из синтез-газа:
3. Из синтез-газа:2CO +3H2 250°,200МПа,kat → CH2(OH)CH2(OH)
В лаборатории
Окисление алкенов:
16. II. Получение трёхатомных спиртов (глицерина)
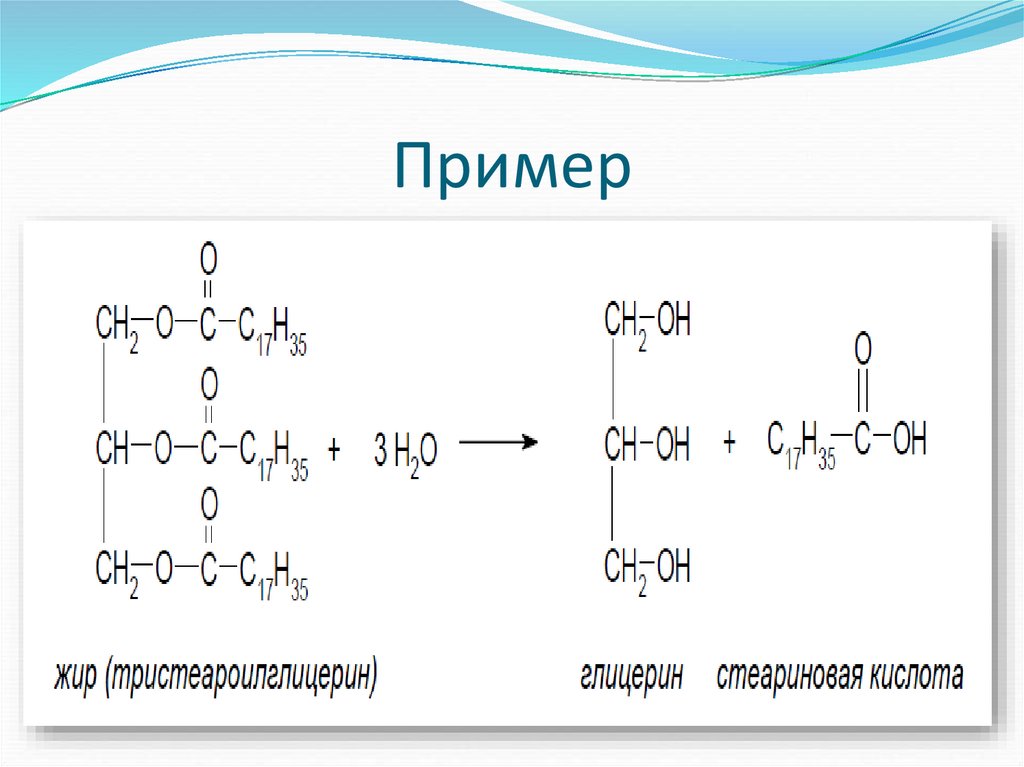
В промышленностиОмыление жиров (триглицеридов):
17. Пример
18. Химические свойства многоатомных спиртов
Химические свойствамногоатомных спиртов
1. С активными металлами:
HO-CH2-CH2-OH + 2Na →
H2↑+ NaO-CH2-CH2-ONa
(гликолят натрия)
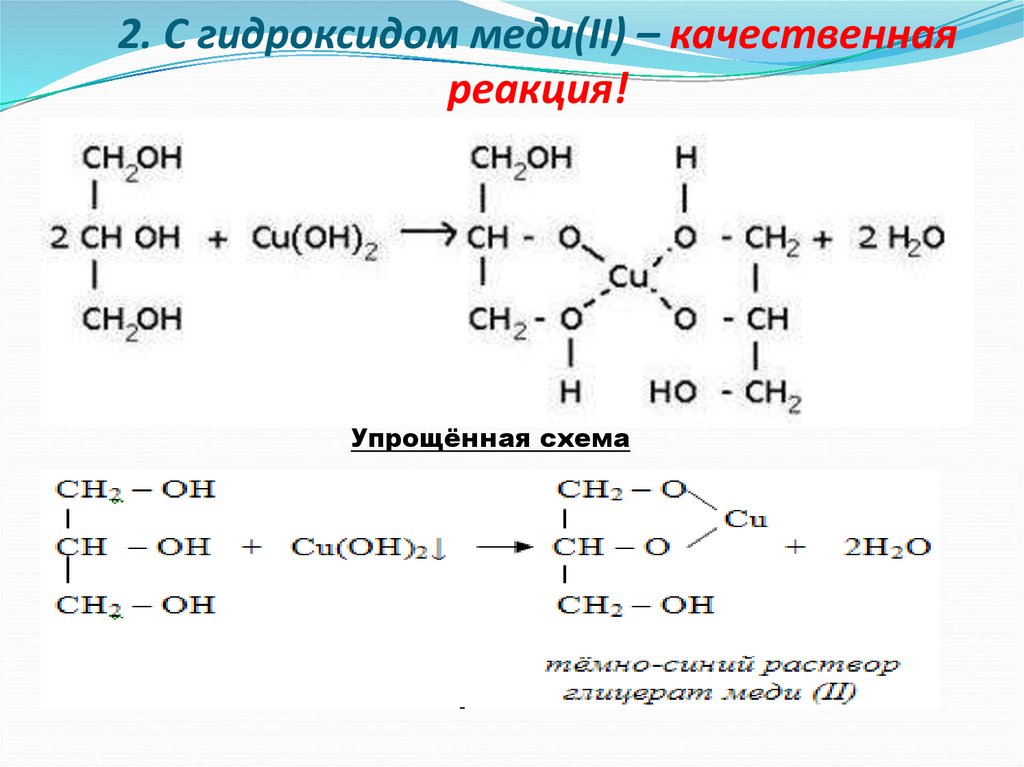
19. 2. С гидроксидом меди(II) – качественная реакция!
Упрощённая схема20.
Глицерат меди (2)Лабораторный опыт.
Распознавание многоатомных спиртов
21.
Качественная реакция многоатомныхспиртов , позволяющая отличить
соединения этого класса, –
взаимодействие со
свежеприготовленным гидроксидом
меди(II). В щелочной среде при
достаточной концентрации глицерина
голубой осадок Cu(OH) 2 растворяется
с образованием раствора ярко-синего
цвета – гликолята меди(II):
22.
Специфические свойстваГлицерин взаимодействует с азотной кислотой с образованием
сложных эфиров. В зависимости от условий реакции (мольного
соотношения реагентов, концентрации катализатора – серной
кислоты и температуры) получаются моно-, ди- и
тринитроглицериды:
23.
24.
25.
Тест по теме «Спирты»1. Функциональная группа в молекулах спиртов:
1) -OH
2) -COOH
3) -COH
2. Реакция этерификации это реакция взаимодействия между:
1) спиртом и кислотой
2) альдегидом и кислородом
3) металлом и неметаллом
3. Установите соответствие между названием органического вещества и его формулой:
А
H
H
│
│
H― C― C―OH
│ │
H H
Б
H
│
H― C―OH
│
H
В
H H
H
│
│
│
H― C ― C ― C ― H
│
│
│
OH OH OH
1. пропантриол - 1. 2, 3 или глицерин
2. метанол или метиловый спирт
3. этанол или этиловый спирт
Ответ запишите в виде последовательности цифр (например 132)
_______________
26. Тесты
1. При окислении пропанола-1 образуется1) пропилена
2) пропанон
3) пропаналь
4) пропан
27. 2. В схеме реакции
NaOH + X → C2H5OH + NaClвеществом «Х» является
1) хлорэтан
2) 1,2-дибромэтан
3) ацетилен
4) этаналь
28. Тесты
3. В результате дегидратации пропанола-1образуется
1) пропанол-2 2) пропан 3) пропен 4) пропин
4. В схеме превращений пропанол1→ X → пропанол-2
веществом «X» является
1) 2-хлорпропан
2) пропановая кислота
3) пропин
4) пропен
29.
Ответы: 1-3, 2-1, 3-3, 4-430. Тест:
Какое из перечисленных веществ может принадлежать к классу многоатомныхспиртов:
а) С 7 Н 15ОН
б)С 7 Н 14
в)С 7 Н 12 О2
г)С 7Н 12(ОН)2
2. С какими веществами реагирует многоатомные спирты:
а)НСI
б)Br
в)О 2
г) СsNO 3
3.Установите соответствие между формулой и названием вещества:
Формула вещества
Название вещества
1.С 2 Н 5 ОН
А. бутантриол-1,2,3
2. СН 2-ОН –СН –ОН-СН2—ОН
Б. глицерин
3. СН 2ОН –СН2—СН2 ОН
В.Этанол
4. СН3—СН 2 ОН --СН2 ОН---СН2ОН
Г. Пропандиол-1,3
1.
4 .Установите соответствие между названием и классом органического вещества:
Название вещества
Класс соединения
1.Бутилен
А. Спирт
2. Бензол
Б. Алкан
3. Пентантриол -1,3,5
В. Диен
4. 2-метилпропан
Г. Арен
31. Ответы.
1.2.
3.
4.
Г
А, В
В, Б, Г, А
В, Г, А, Б
32. Домашнее задание
1. Выписать главное.Написать реакции:
- глицерина с натрием;
- этиленгликоля с азотной кислотой;
33. Домашнее задание
Как изменится скорость реакции этанола сбромоводородом при увеличении температуры с 20
до 40 ºС, если температурный коэффициент ВантГоффа равен 3.
При полном сгорании смеси метилового и этилового
спиртов массой 3,48 г израсходовано 4032 мл
кислорода (н. у.). Массовая доля метанола в исходной
смеси составляла:
73,6% , 62,2%, 34,8%, 24,6%






























 Химия
Химия








