Похожие презентации:
Сложные эфиры
1.
СЛОЖНЫЕ ЭФИРЫ.2. Общая формула:
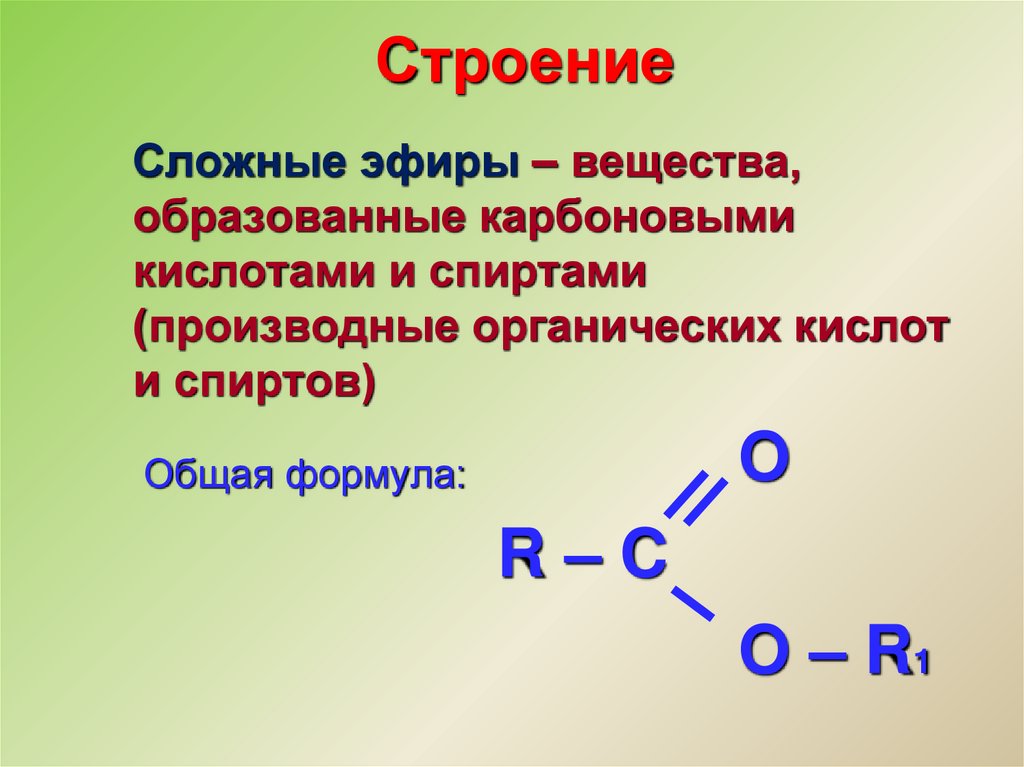
СтроениеСложные эфиры – вещества,
образованные карбоновыми
кислотами и спиртами
(производные органических кислот
и спиртов)
O
Общая формула:
R–C
O – R1
3. Общая формула:
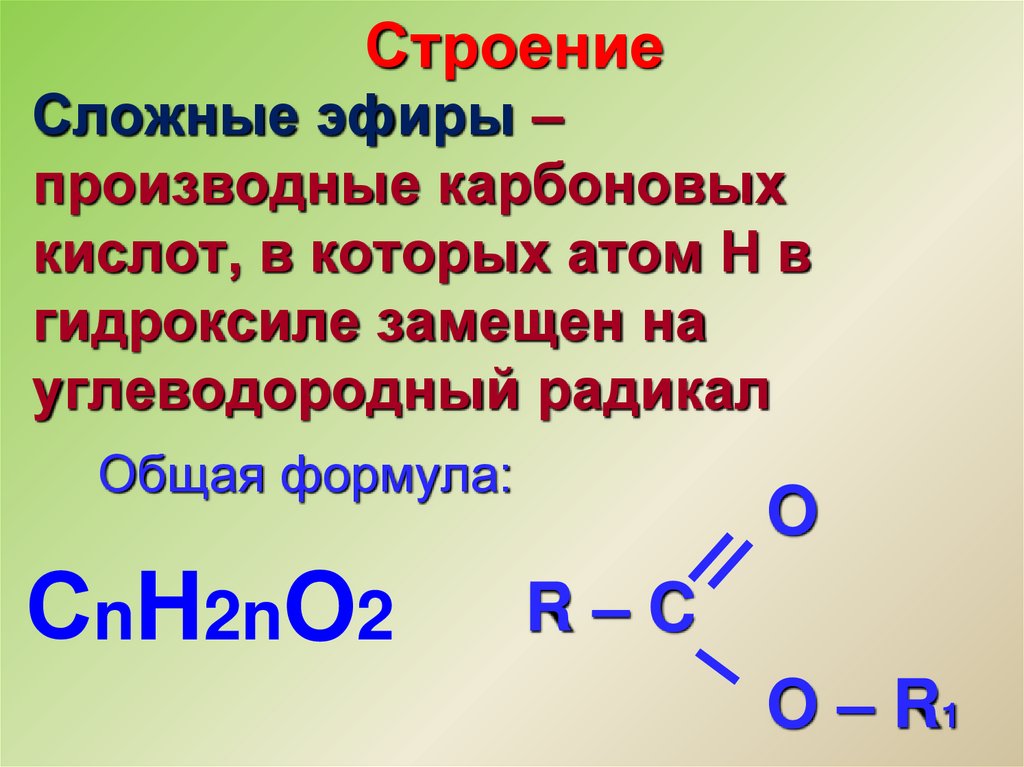
СтроениеСложные эфиры –
производные карбоновых
кислот, в которых атом Н в
гидроксиле замещен на
углеводородный радикал
Общая формула:
СnH2nO2
O
R–C
O – R1
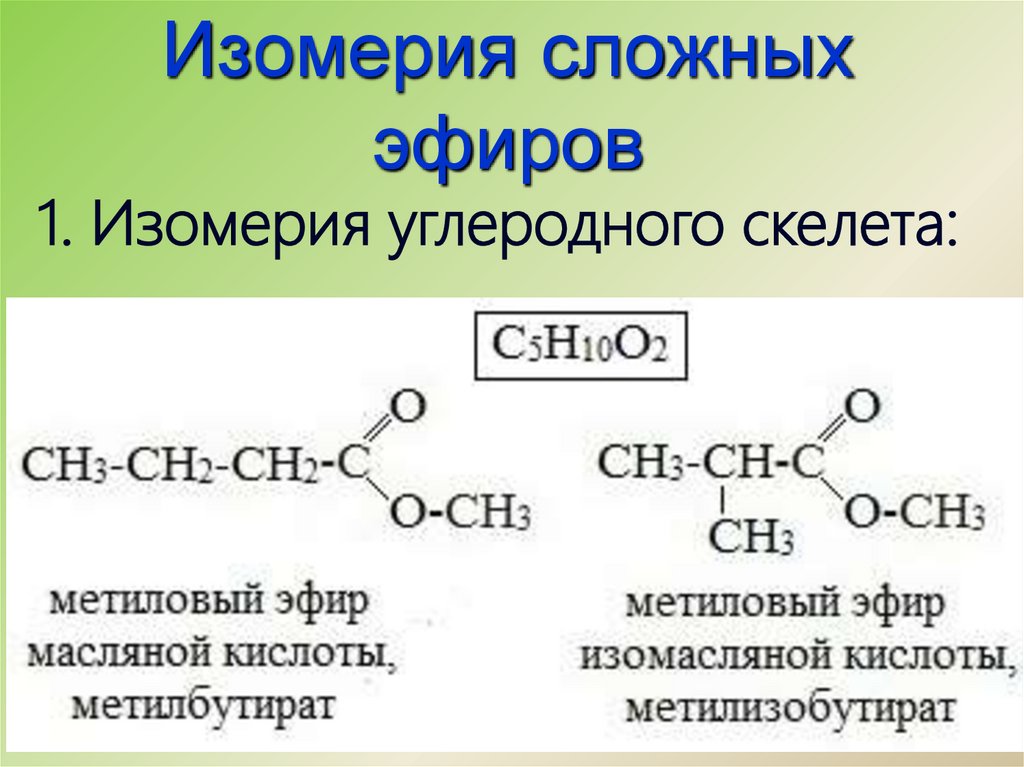
4. Изомерия сложных эфиров
1. Изомерия углеродного скелета:5. Изомерия сложных эфиров
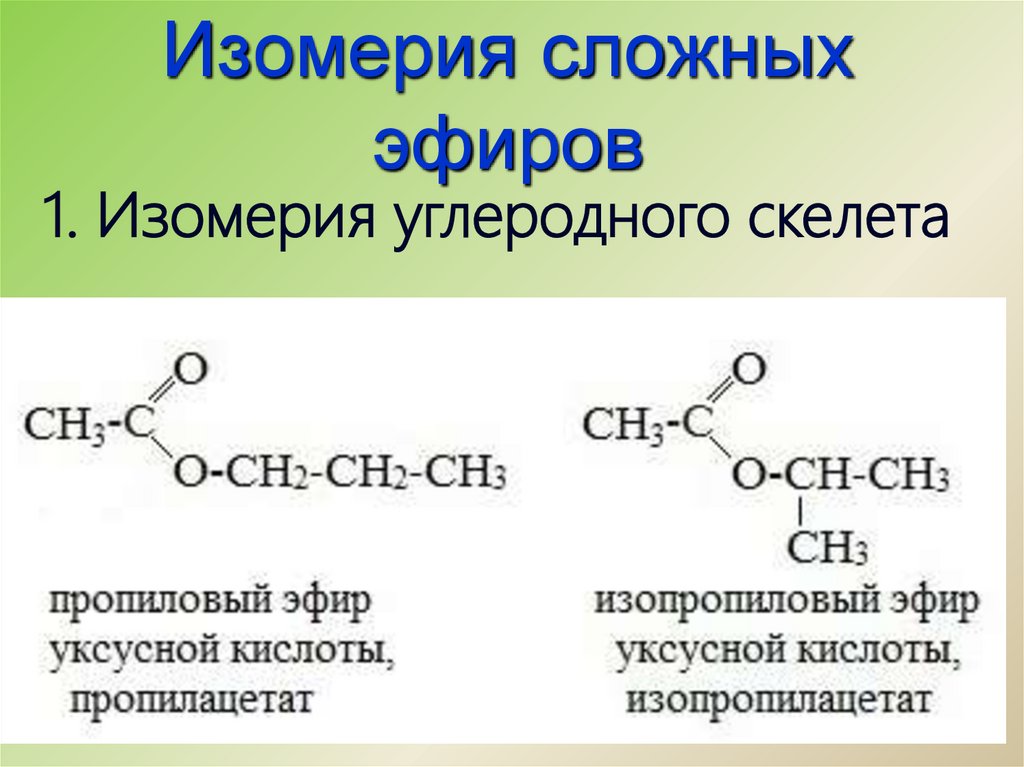
1. Изомерия углеродного скелета6. Изомерия сложных эфиров
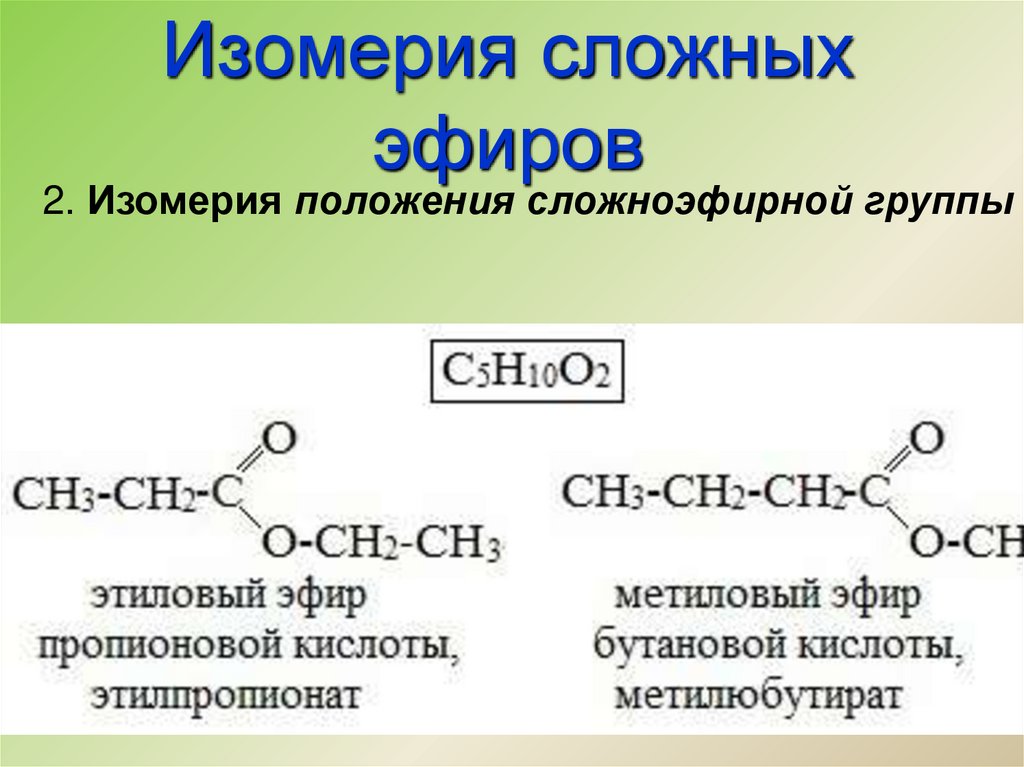
2. Изомерия положения сложноэфирной группы7. Изомерия сложных эфиров
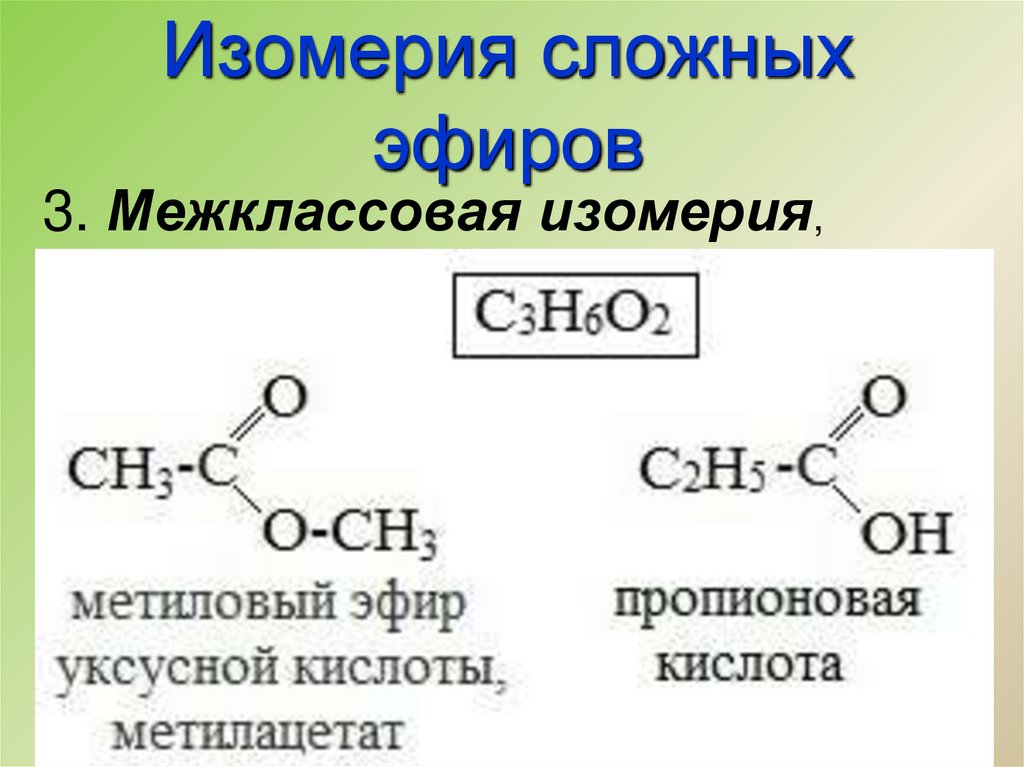
3. Межклассовая изомерия,8.
НоменклатураВ основе номенклатуры лежат два способа названия
сложных эфиров:
1) по названию радикала спирта и
кислотного остатка кислоты (как
соли). Например: этилацетат
2) полное название эфира по радикалу
спирта и названию кислоты.
Например: этиловый эфир
уксусной кислоты.
9.
Название сложного эфираТривиальное название Формула эфира
Метилметаноа
Метилформиат HCOOCH3
т
Этилметаноат Этилформиат
HCOOC2H5
Метилэтаноат
Метилацетат
CH3COOCH3
Этилэтаноат
Этилацетат
CH3COOC2H5
Пропилэтаноа
Пропилацетат
т
CH3COOCH2C
H2CH3
10.
Сложные эфиры простейшихкислот и спиртов :
• Бесцветные летучие жидкости;
• Нерастворимые в воде;
• Имеют запахи фруктов и
цветов;
• Имеют невысокие температуры
кипения
11.
12.
Сложные эфиры высшихкислот и высших спиртов -
воски:
• Пчелиный воск
С15Н31СООС31Н63
13. Нахождение в природе
Пчелиный воск –эфир
пальмитиновой
кислоты и
мирицилового
спирта
С15Н31СООС31Н63
14. Применение сложных эфиров
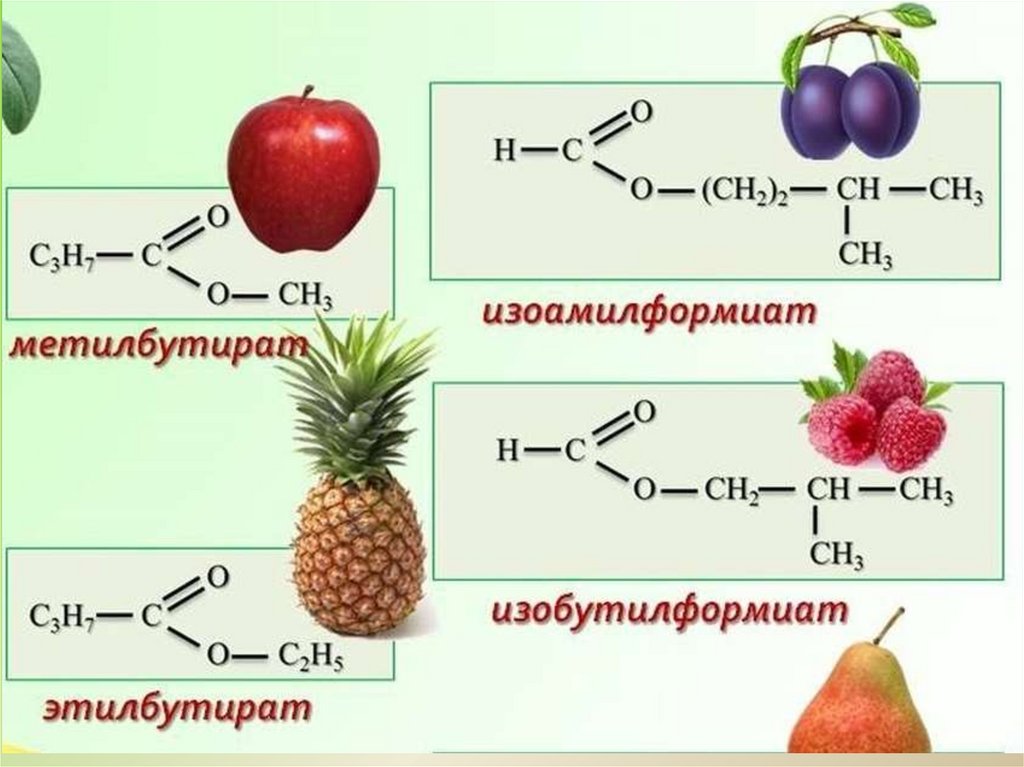
Ароматизаторы применяемые в пищевой промышленностисладости
йогурты
газированные напитки
15. Применение сложных эфиров
В бытовой химии:парфюмерия
растворители, лаки, краски и
др.
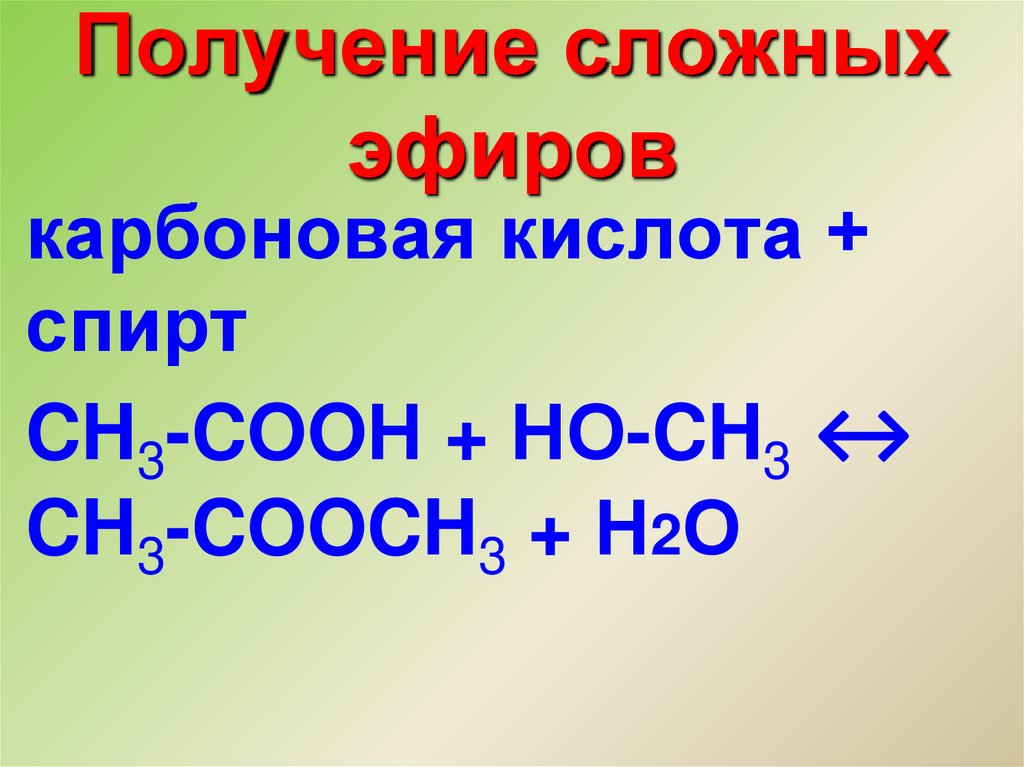
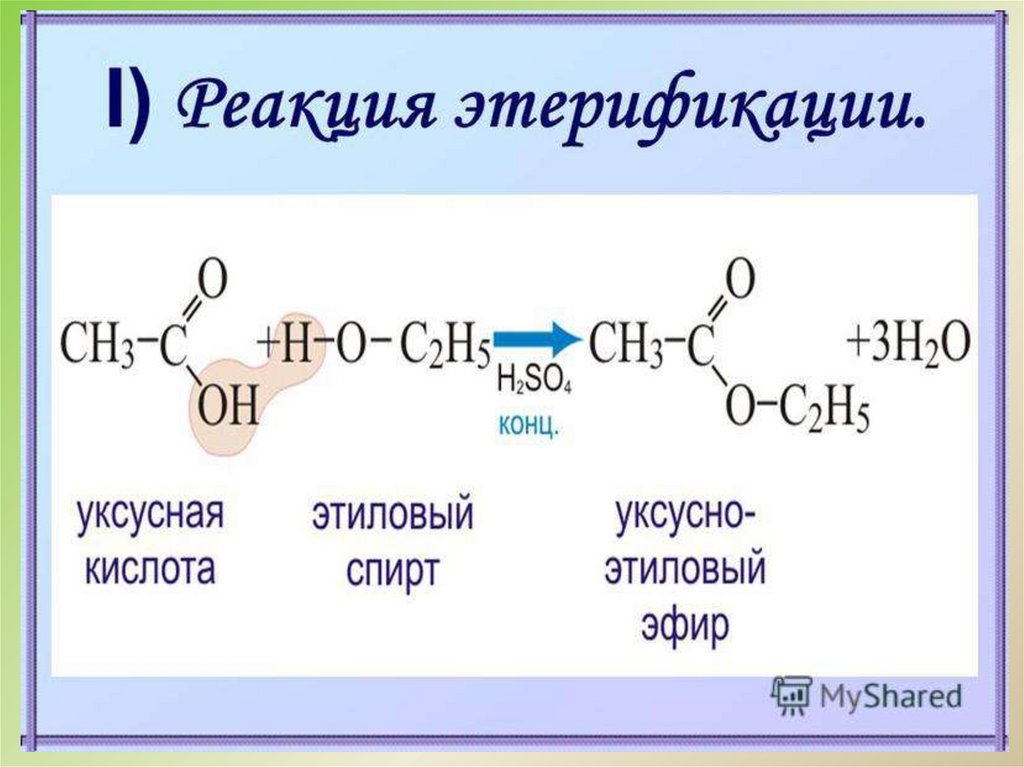
16. Получение сложных эфиров
карбоновая кислота +спирт
CH3-COOН + НО-CH3 ↔
CH3-COOCH3 + Н2О
17.
H-COONa + C2H5-Cl = H-COOC2H5 +NaCl
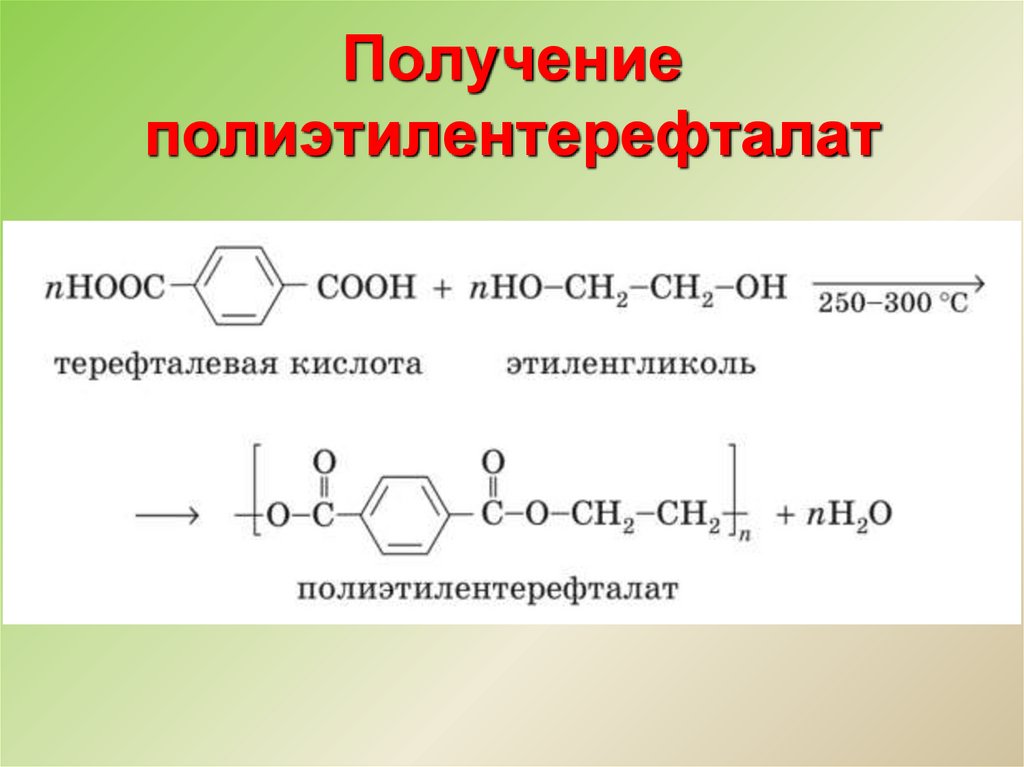
18. Получение полиэтилентерефталат
19. Получение полиэтилентерефталат
20. Получение сложных эфиров
Соли карбоновых кислот+ галогеналкан
CH3-COONa + CH3-Cl →
CH3-COOCH3 + NaCl
21. Получение сложных эфиров
Соли карбоновых кислот+ галогеналкан
H-COONa + C2H5-Cl →
H-COOC2H5 + NaCl
22.
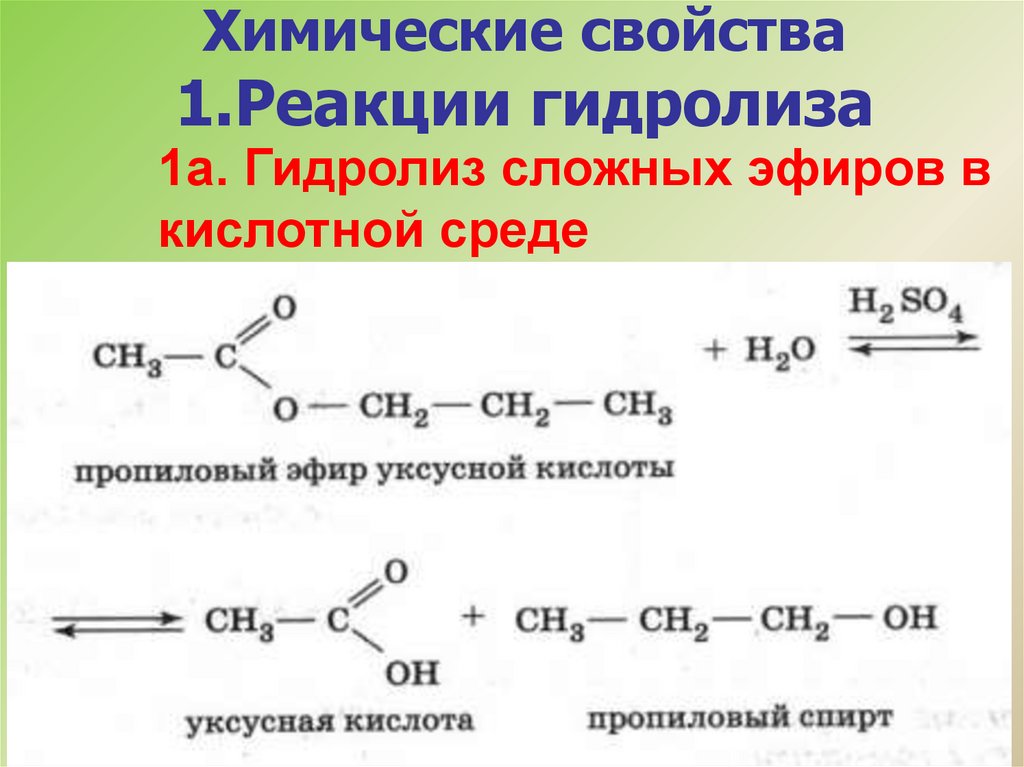
Химические свойства1.Реакции гидролиза
1а. Гидролиз сложных эфиров в
кислотной среде
23.
Химические свойства1. Реакции гидролиза
1б. Гидролиз сложных эфиров в
щелочной среде
24.
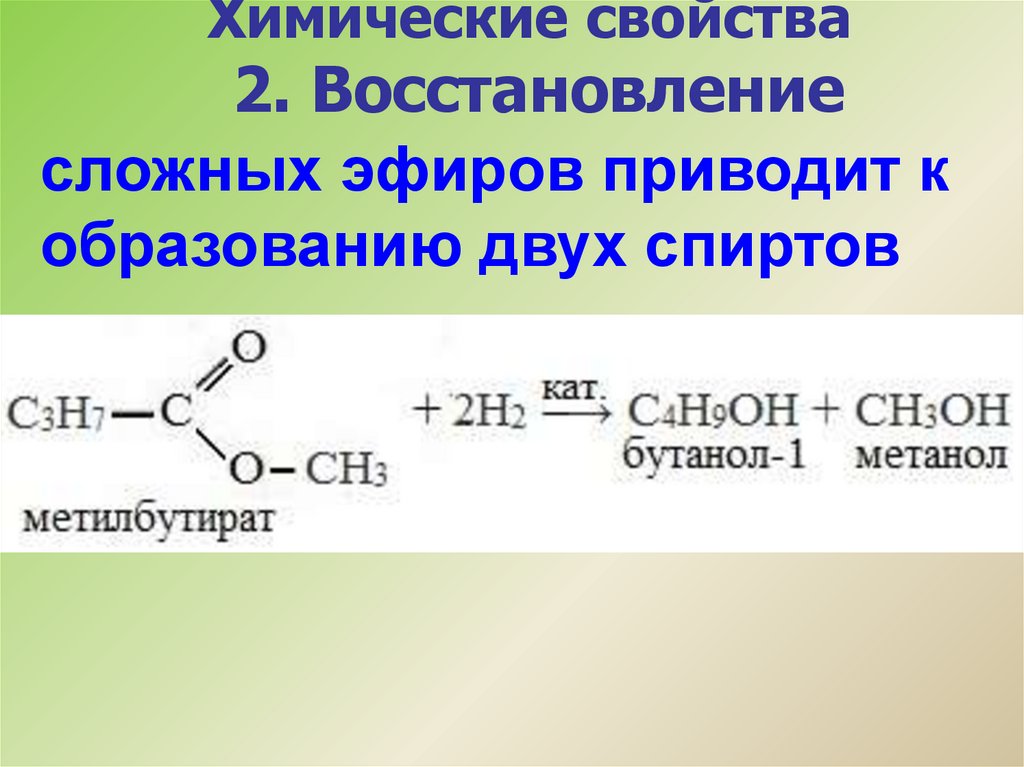
Химические свойства2. Восстановление
сложных эфиров приводит к
образованию двух спиртов
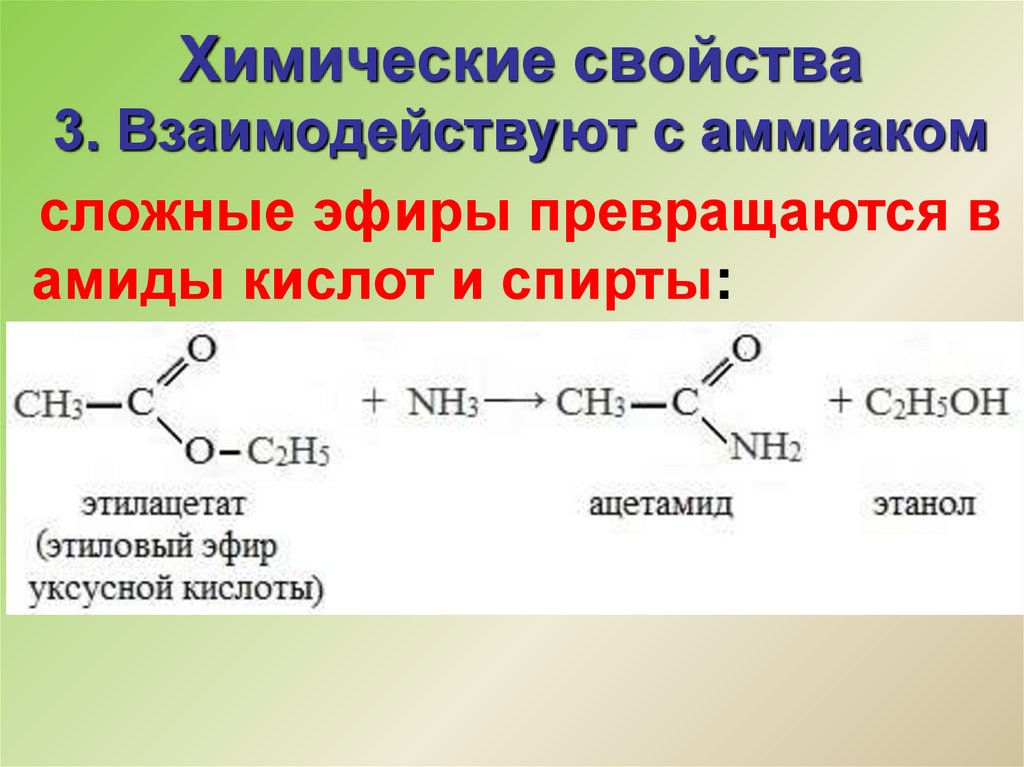
25. Химические свойства 3. Взаимодействуют с аммиаком
сложные эфиры превращаются вамиды кислот и спирты:
26. Сложные эфиры имеют большое практическое значение
1. Их применяют в промышленности вкачестве растворителей и
промежуточных продуктов при
синтезе различных органических
соединений.
2. Сложные эфиры с приятным
запахом используют в парфюмерии
и пищевой промышленности.
3. Сложные эфиры часто служат
исходными веществами в
производстве многих
фармацевтических препаратов.
27. Домашнее задание
Составьте уравнения реакцийА) этерификации уксусной
кислоты 3-метилбутанолом -1
Б) этерификации муравьиной
кислоты пропанолом-2
В) гидролиза пропилового эфира
бензойной кислоты
28. Решите задачу
Какую массуэтилацетата можно
получить из 120 г
уксусной кислоты
и 138 г этанола?
29. Решите задачу
Какую массу этилацетатаможно получить из 120 г
уксусной кислоты и 138 г
этанола, если выход
сложного эфира составляет
90% от теоретически
возможного?
30. Изомеры
Одно из двух веществ составаC3H6O2 вытесняет оксид углерода
(IV) из карбоната кальция, другое не
реагирует с этим карбонатом ,но
при нагревании с гидроксидом
натрия образует спирт и соль.
Напишите структурные формулы
этих веществ. Напишите уравнения
соответствующих реакций.
31.
Два органических соединения имеютодин и тот же элементный состав:
54,55 % углерода, 9.09 % водорода и
кислород. Плотность паров одного
из них по воздуху равна 1,517,
плотность второго по азоту равна
3,143. Первое вещество легко окисляется,
второе устойчиво к действию окислителей.
Первое не изменяет окраски индикаторов,
второе окрашивает лакмус в красный цвет.
Назовите эти вещества,
32. Решите цепочки превращений
карбидкальция → ацетилен →
ацетальдегид → уксусная кислота
→ метилацетат
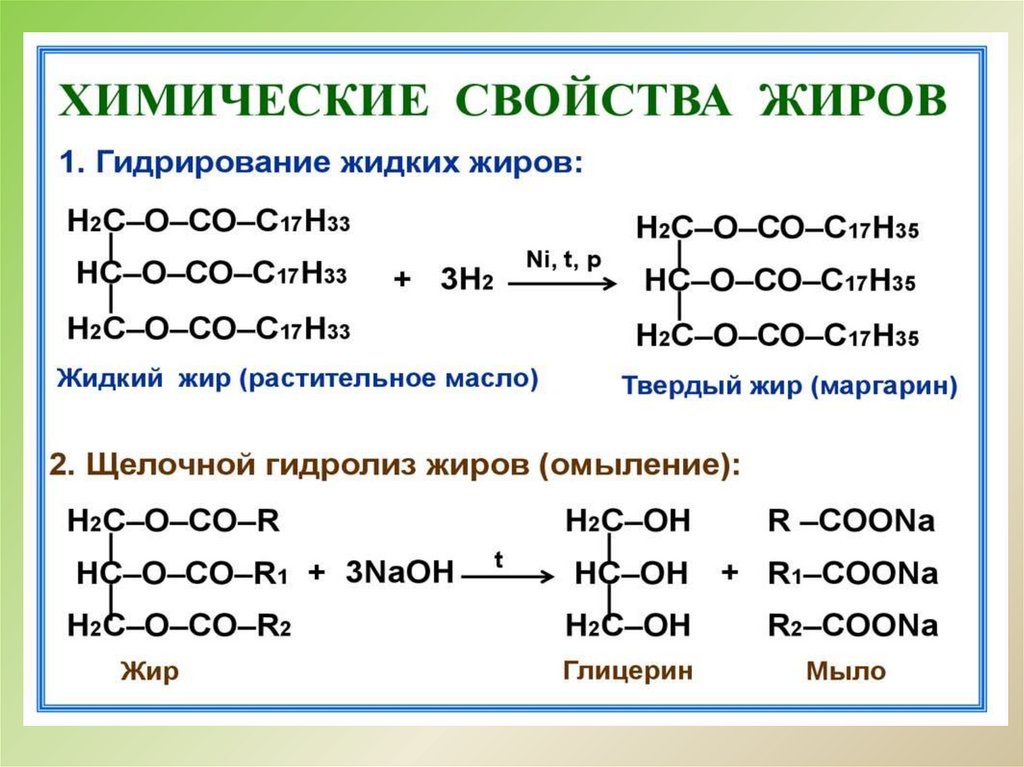
трипальмитин → глицерин
→ триолеин → тристеарин →
стеарат калия



















 Химия
Химия








