Похожие презентации:
Оксиды. Формулы оксидов ( 8 класс)
1.
Тема урокаОксиды
2.
1. Сформировать понятия об оксидах;2. Закрепить на оксидах значение химической
номенклатуры для бинарных соединений;
3. Показать значение важнейших
представителей оксидов в природе и жизни
человека
3.
-дайте названия следующим соединениям:КСl, КН, Р2О5, СО2.
-
какие соединения называют бинарными?
- Что общего у двух последних соединений
(Р2О5, СО2)?
4.
5.
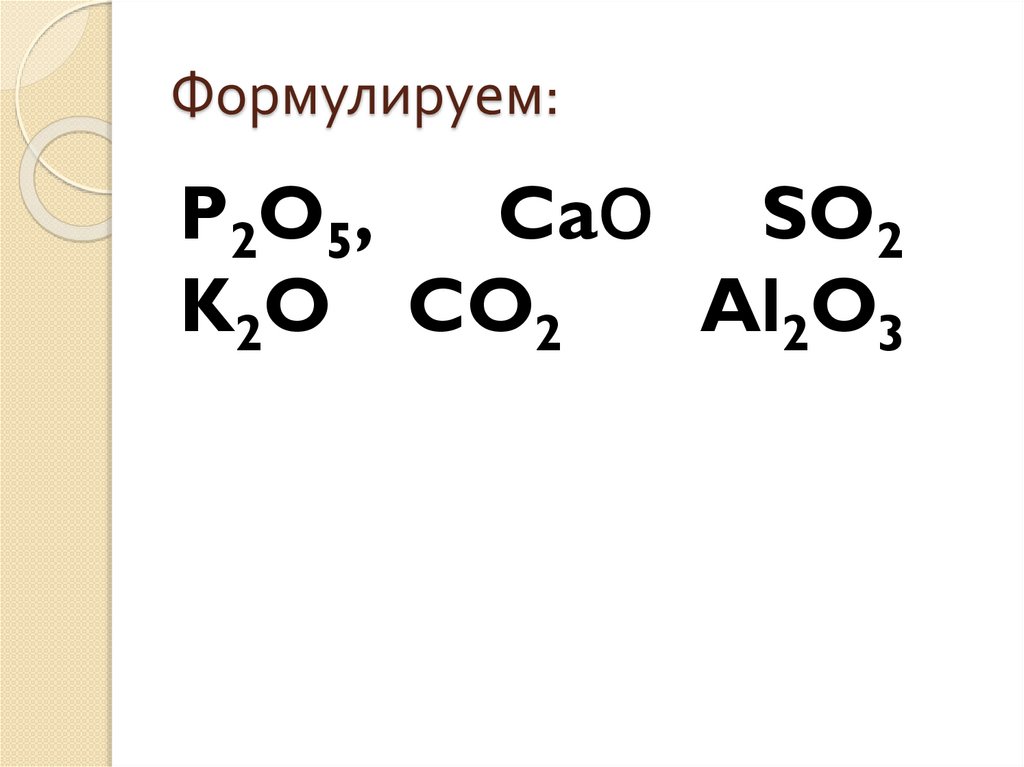
Формулируем:P2O5,
CaО SO2
K2O CO2
Al2O3
6.
Оксиды - сложные вещества,состоящие из двух элементов, один
из которых кислород.
Общая формула - ЭхОу
7.
Составить таблицуОксиды
Основания
Кислоты
Соли
8.
А) по международной номенклатуре:Название = «Оксид» + название элемента в
родительном падеже + (с.о. римскими цифрами)
Б) тривиальные названия: NO – окись азота, N2O –
закись азота.
9.
Дать названия следующимвеществам:
I вариант
II вариант
PO3
K2O
CuO
CaO
Al2O3
ZnO
SiO2
SO3
FeO
Na2О.
df
10.
I вариантPO3 оксид фосфора
CuO оксид меди
Al2O3 оксид алюминия
SiO2 оксид кремния
FeO оксид железа
II вариант
K2O оксид калия
CaO оксид кальция
ZnO оксид цинка
SO3 оксид серы
Na2О оксид натрия
df
11.
Напишите формулы оксидовI вариант
Оксид меди (II)
Оксид железа (III)
Оксид железа (II)
Оксид серы (VI)
Оксид цинка (II)
II вариант
Оксид меди (I)
Оксид железа (II)
Оксид серы (IV)
Оксид фосфора (III)
Оксид магния (II)
12.
I вариантII вариант
Оксид меди (II) CuO Оксид меди (I) Cu2O
Оксид железа (III)Fe2O3 Оксид железа (II) FeO
Оксид железа (II) FeO Оксид серы (IV) SO2
Оксид серы (VI) SO3 Оксид фосфора (III)P2O3
Оксид цинка (II) ZnO Оксид магния (II) MgO
13.
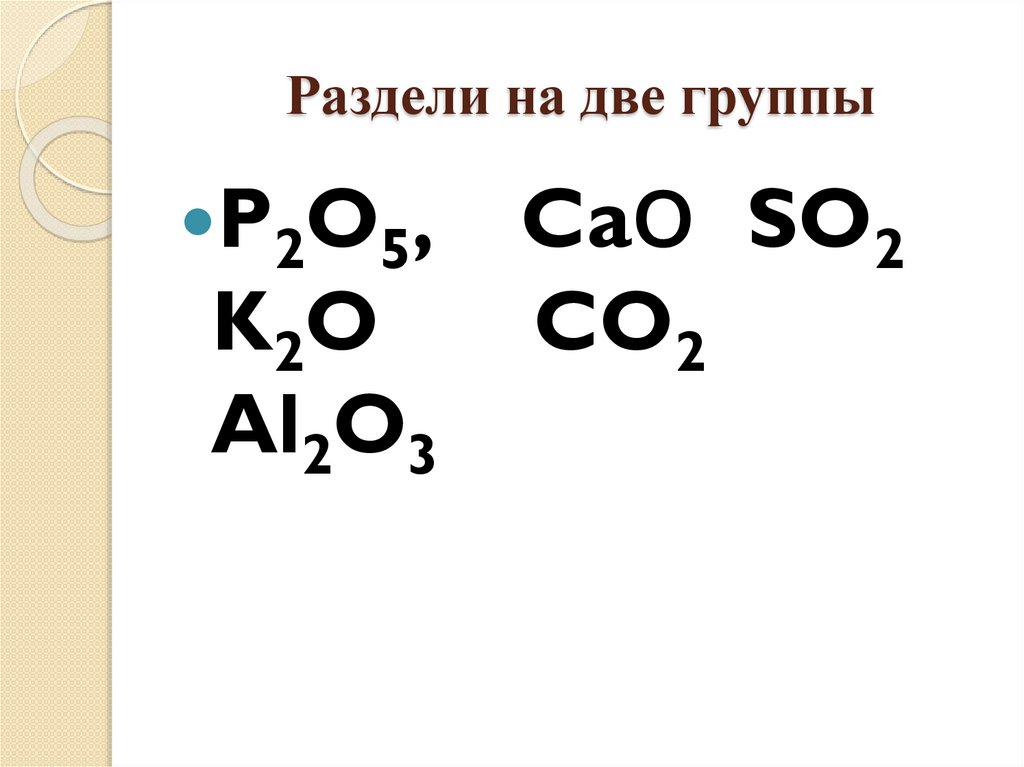
Раздели на две группыP2O5,
K 2O
Al2O3
CaО SO2
CO2
14.
ОксидыМеталлов
Неметаллов
CaО,
K2O,
Al2O3
P2O5,
SO2,
CO2
15.
Важнейшие оксидыВода( оксид водорода) Углекислый газ(оксид углерода(IV) Негашенная известь(оксид кальция) –
Песок( оксид кремния (IV) –
Составьте их
химические формулы
16.
Важнейшие оксидыВода( оксид водорода) - H2O
Углекислый газ(оксид углерода(IV) - CO2
Негашенная известь(оксид кальция) – CaO
Песок( оксид кремния (IV) – SiO2
17.
Вода18.
Углекислый газ(оксид углерода(IV))19.
Негашеннаяизвесть(оксид кальция)
-
20.
Песок( оксид кремния (IV))21.
Изумруд - 2Al2O3 *P2O5 *5H2O22.
Рубин - Al2O323.
Сапфир - Al2O324.
Аметист - SiO2 (кремнезём)25.
Агат - SiO2 (кремнезём)26.
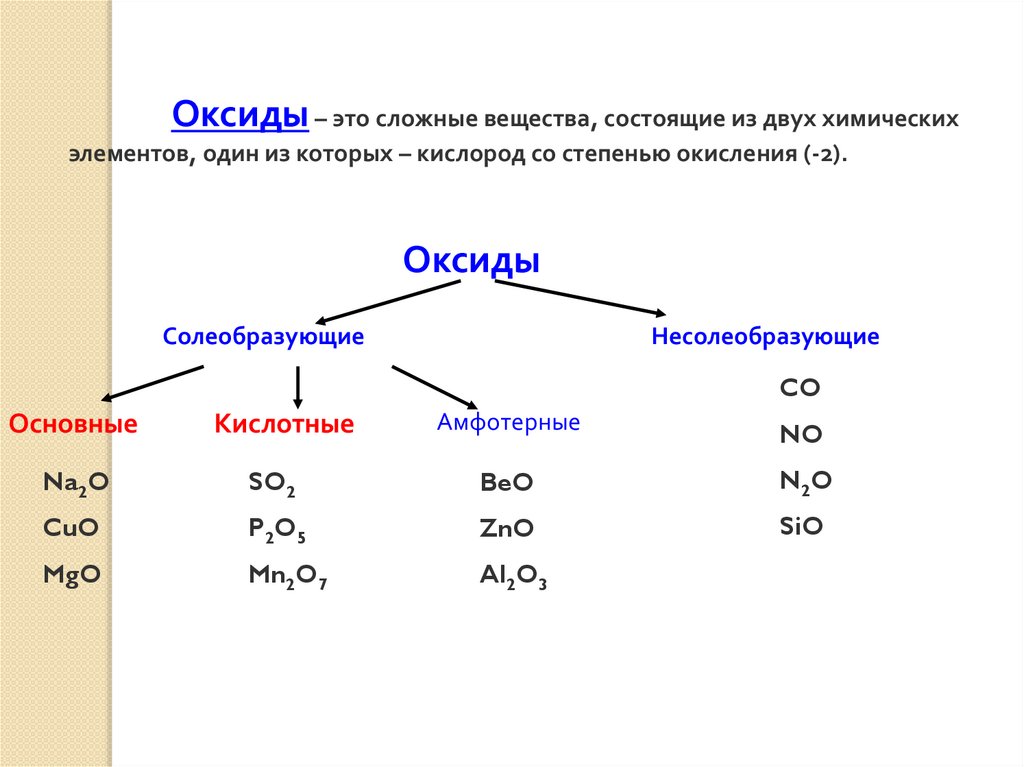
Оксиды – это сложные вещества, состоящие из двух химическихэлементов, один из которых – кислород со степенью окисления (-2).
Оксиды
Солеобразующие
Несолеобразующие
CO
Основные
Кислотные
Амфотерные
NO
Na2O
SO2
BeO
N2O
CuO
P2O5
ZnO
SiO
MgO
Mn2O7
Al2O3
27.
ОксидыОсновные
Кислотные
стр.102
стр.103
28.
ОксидыОсновные
Оксиды металлов
Кислотные
Им соответствуют
Оксиды неметаллов
Им соответствуют
основания
кислоты
K2O
CO2
KOH
(записать в таблицу)
H2CO3
29.
Выписать оксиды, дать им названияОксиды
Основные
K2O - оксид калия
Кислотные
CO2 - оксид углерода
30.
Выпишите оксиды,1 вариант
CaO, NaOH,
CO2, H2SO3,
FeCl3, N2O5,
Zn(OH)2, N2O,
Li2O, Fe2O3,
W(OH)2,SO2
Na2SO4, ZnO,
дайте им названия:
2 вариант
CaCO3, NaCl
N2O5, MgO,
Ca(OH)2, N2O3,
FeO, SO3, Na2SO4,
Na2O, CuO, KOH,
CO, Fe(OH)3
KMnO4
31.
Химические свойства оксидовОсновные оксиды
1) С кислотами
2) С водой
3) С кислотными оксидами
Кислотные оксиды
1) С растворимыми основаниями (щелочами)
2) С водой
3) С основными оксидами
Приведем примеры и рассмотрим в свете ЭД и ОВР
32.
Химические свойства основных оксидов1) Взаимодействуют с кислотами
выписать пример из учебника
2) с водой
выписать пример из учебника
3) с кислотными оксидами
CaO + CO2 = CaCO3
33.
Химические свойства кислотных оксидов1) с растворимы основаниями
(щелочами)
выписать пример из учебника
2) с водой
выписать пример из учебника
3) менее летучие кислотные оксиды
вытесняют более летучие из солей
CaCO3 +SiO2 = CaSiO3 + CO2↑
34.
Домашнее заданиеПараграфы 14, 23
35.
Выпишите оксиды, дайте имназвания
CaO, NaOH, CO2, H2SO3, CaCl2, FeCl3,
Zn(OH)2, N2O5, Al2O3, Ca(OH)2, N2O,
FeO, SO3, Na2SO4, ZnO, CaCO3, Mn2O7,
CuO, KOH, CO, Fe(OH)3
36.
Химические свойства основных оксидов1) Взаимодействуют с кислотами
CuO + H2SO4 = CuSO4 +H2O
2) с водой
Na2O + H2O = 2NaOH
3) с кислотными оксидами
CaO + CO2 = CaCO3
37.
Химические свойства кислотных оксидов1) с растворимы основаниями
(щелочами)
CO2 + 2NaOH = Na2CO3 + H2O
2) с водой
Р2O5 + 3H2O = 2H3PO4
3) менее летучие кислотные оксиды
вытесняют более летучие из солей
CaCO3 +SiO2 = CaSiO3 + CO2↑






























 Химия
Химия








