Похожие презентации:
Химическая связь, её природа и типы
1.
ХИМИЧЕСКАЯСВЯЗЬ, ЕЕ ПРИРОДА
И ТИПЫ.
2.
Максимально можетнаходиться на первом слое 2
электрона, а на втором и далее
слоях 8 электронов. И если «не
хватает» электронов, то слой
называется незавершенным;
если хватает – завершенный.
3.
Химическая связь – взаимодействие,которое связывает отдельные атомы в
более сложные системы.
Электростатическая природа – когда
частицы имеют разные заряды.
4.
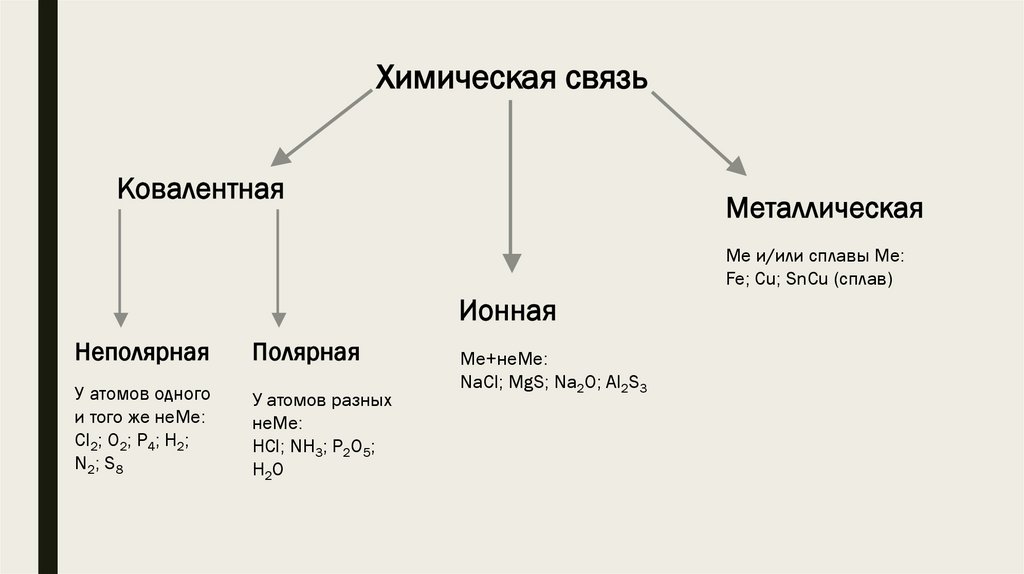
Химическая связьКовалентная
Металлическая
Ме и/или сплавы Ме:
Fe; Cu; SnCu (сплав)
Ионная
Неполярная
Полярная
У атомов одного
и того же неМе:
Cl2; O2; P4; H2;
N2; S8
У атомов разных
неМе:
HCl; NH3; P2O5;
H2O
Ме+неМе:
NaCl; MgS; Na2O; Al2S3
5.
Ковалентная связь – химическаясвязь, возникающая в результате
образования общих электронных
пар между двумя атомами.
6.
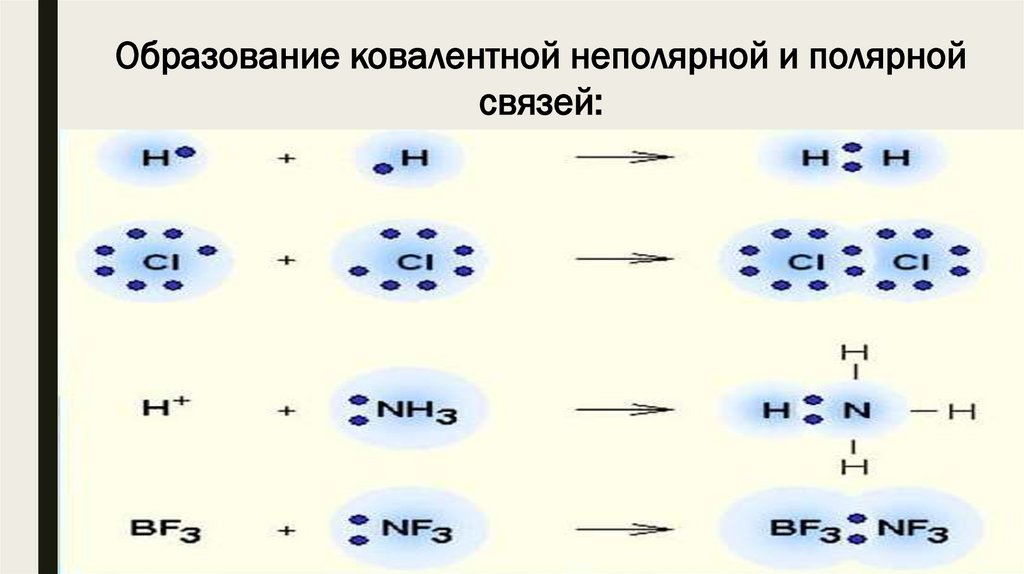
Образование ковалентной неполярной и полярнойсвязей:
7.
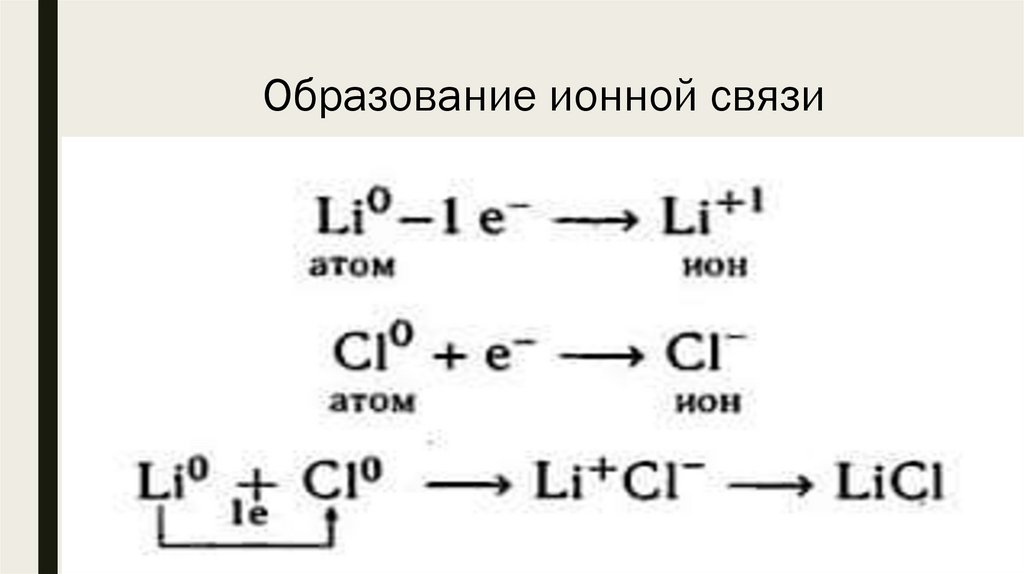
Образование ионной связи8.
Образование металлической связи:Men+=Me0+n e
Где n – число внешних
участвующих в связи.
+
Na =Na+1e
2+
Mg = Mg+ 2e
Al3+= Al+3e
электронов,
9.
Межмолекулярное взаимодействие– взаимодействие, в котором
молекулы могут притягиваться друг
к другу за счет электростатических
сил.
Межмолекулярное взаимодействие
имеет электростатическую природу.
10.
11.
Распределить вещества по типу химической связи.Показать образование связи в веществах
MgCl2, H2, CO2, NaI, HF, Al, ZnO, Fe, Br2, Ca3N2, O2, SO3,
HBr, Al2S3, CuSn (сплав), Na2O, H2O, BaO, CI2, KCI, Mg,
CO2, P4, C, AIBr3, SiO2
Ионная связь
Ковалентная
полярная
Ковалентная
неполярная
Металлическ
ая
12.
Домашнее задание: параграф3 №7 (определить у каждого
вещества тип связи и показать
образование такой связи).









 Химия
Химия








