Похожие презентации:
Электролитическая диссоциация кислот, оснований и солей
1.
ЭЛЕКТРОЛИТИЧЕСКАЯДИССОЦИАЦИЯ
КИСЛОТ, ОСНОВАНИЙ И
СОЛЕЙ.
2.
Кислоты – это электролиты, при диссоциации которых вводных растворах в качестве катионов образуются
только ионы водорода.
Кислоты диссоциируют на катион водорода и анион
кислотного остатка.
Растворы, которые содержат ионы водорода,
называют кислыми, и имеют кислотный характер.
3.
Основания – это электролиты, при диссоциациикоторых в водных растворах в качестве анионов
образуются только гидроксид-ионы.
Основания диссоциируют на катион металла и анион
ОН-.
4.
Соли – это электролиты, которые в водных растворахдиссоциируют на катионы металлов и анионы кислотных
остатков.
Раствор, в котором находятся одинаковые количества
ионов водорода и гидроксид-ион, как в чистой воде,
называют нейтральным.
Если в растворе содержится больше ионов водорода,
такой раствор называют кислым; а раствор, в котором
больше гидроксид-ионов, – щелочным.
5.
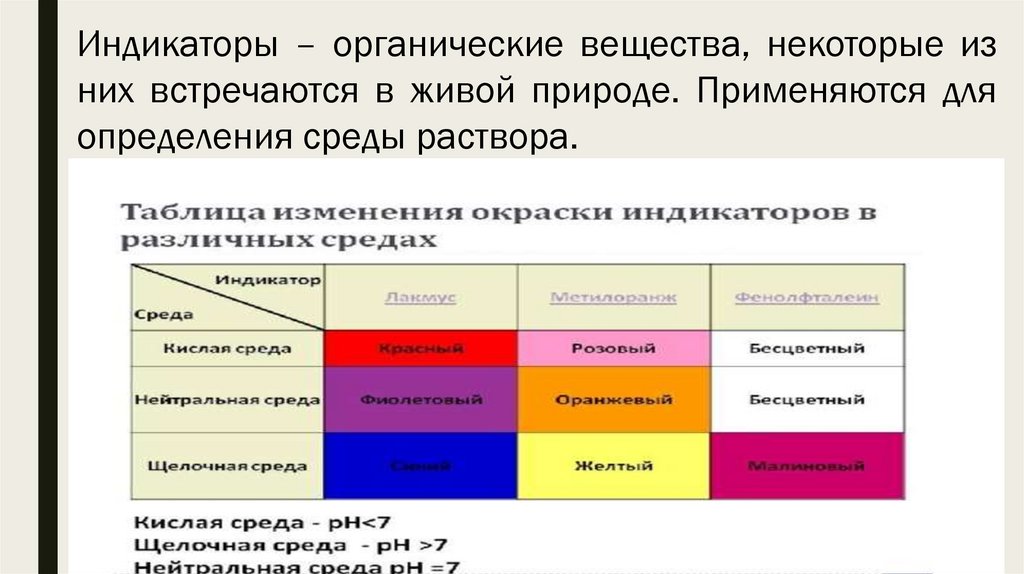
Индикаторы – органические вещества, некоторые изних встречаются в живой природе. Применяются для
определения среды раствора.
6.
Домашнее задание:параграф 11 № 4, № 5,
№ 6.





 Химия
Химия








