Похожие презентации:
Области применения хроматографических методов
1.
1Области применения хроматографических методов.
• Химическая промышленность
• Производственный анализ
• Нефтехимия
• Газовая и нефтяная промышленность
• Экологический мониторинг
• Медицина
• Судебно-медицинская экспертиза
• Фармацевтическая промышленность
• Биохимическая промышленность
• Пищевая промышленность
2.
История создания• 1903 год 21 марта
Михаил Семенович Цвет
«О новой категории адсорбционных
явлений и о применении их к
биохимическому анализу»
• 1947
Приор Фитц
Газо-адсорбционная хроматография
• 1950
Арчер Джон Портер Мартин
Газо-жидкостная хроматография
3.
3Хроматография – это процесс, основанный на
многократном повторении актов сорбции и
десорбции вещества при перемещении его в
потоке подвижной фазы вдоль неподвижного
сорбента.
Газовая хроматография - это вид хроматографии, в
которой подвижной фазой служит газ (пар).
В зависимости от агрегатного состояния неподвижной
фазы различают газоадсорбционную
хроматографию (неподвижная фаза -твердое тело)
и газо-жидкостную хроматографию (неподвижная
фаза - жидкость, нанесенная тонким слоем на
твердый носитель).
4.
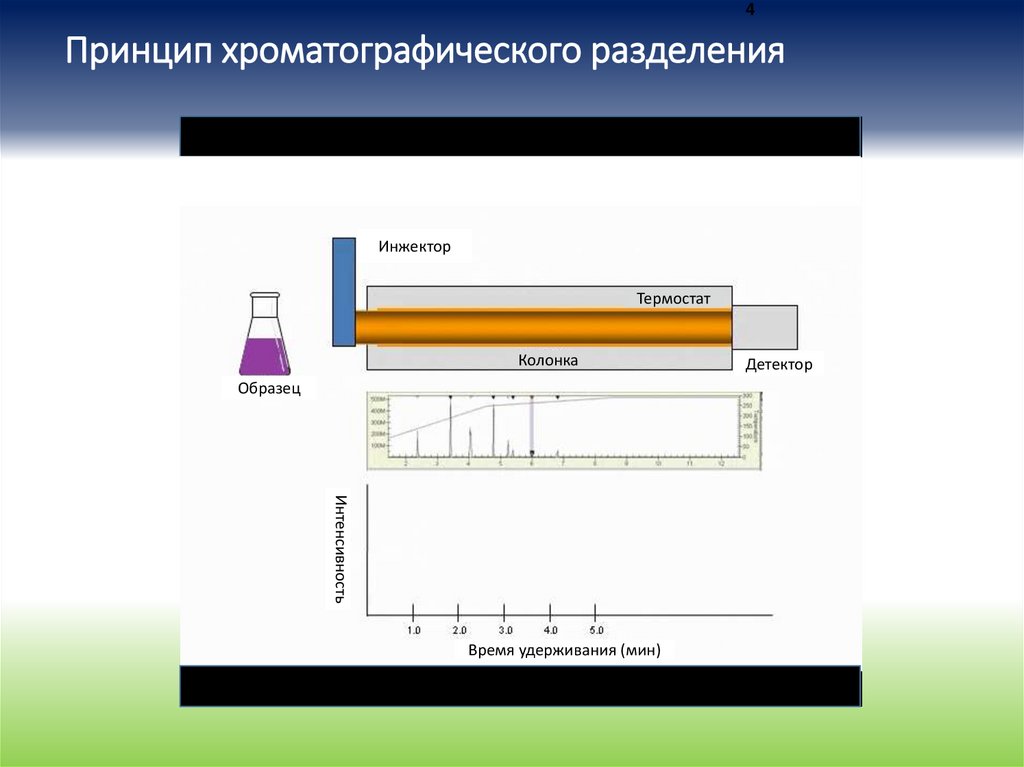
4Принцип хроматографического разделения
Инжектор
Термостат
Колонка
Образец
Интенсивность
Время удерживания (мин)
Детектор
5.
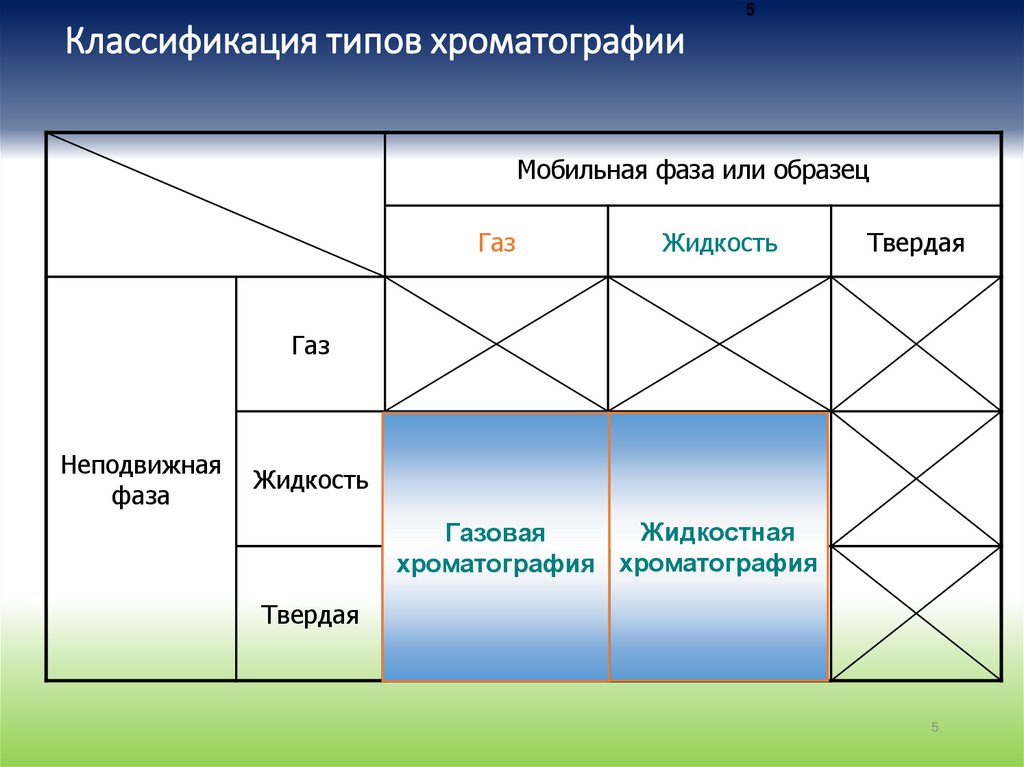
5Классификация типов хроматографии
Мобильная фаза или образец
Газ
Жидкость
Твердая
Газ
Неподвижная
фаза
Жидкость
Твердая
Газожидкостная
хроматография
Жидкостная
Газовая
хроматография хроматография
Газоадсорбционная
хроматография
5
6.
6Достоинства газовой хроматографии
•Избирательность
возможность идентификации и количественного
определения индивидуальных компонентов
сложных смесей
• Производительность
высокая чёткость разделения и быстрота процесса
• Небольшой объем пробы
0.1 – 10 мкл
• Широкий спектр проб
возможность анализа широкого круга объектов – от
простых газов до сложных органических соединений
• Автоматизация процесса
7.
7Основные задачи хроматографического анализа
• Разделение всех компонентов анализируемой смеси
• Идентификация необходимых компонентов смеси
• Количественная оценка идентифицированных компонентов
Задача аналитика: подобрать оптимальные условия для проведения
качественного и количественного анализа.
Два крайних случая:
1. Компоненты смеси разделяются достаточно, но их отклики на
детекторе малы - количественный анализ затруднен.
2. Отклики компонентов на детекторе хорошие, но не все компоненты
разделены. Это затрудняет качественный и количественный анализ.
8.
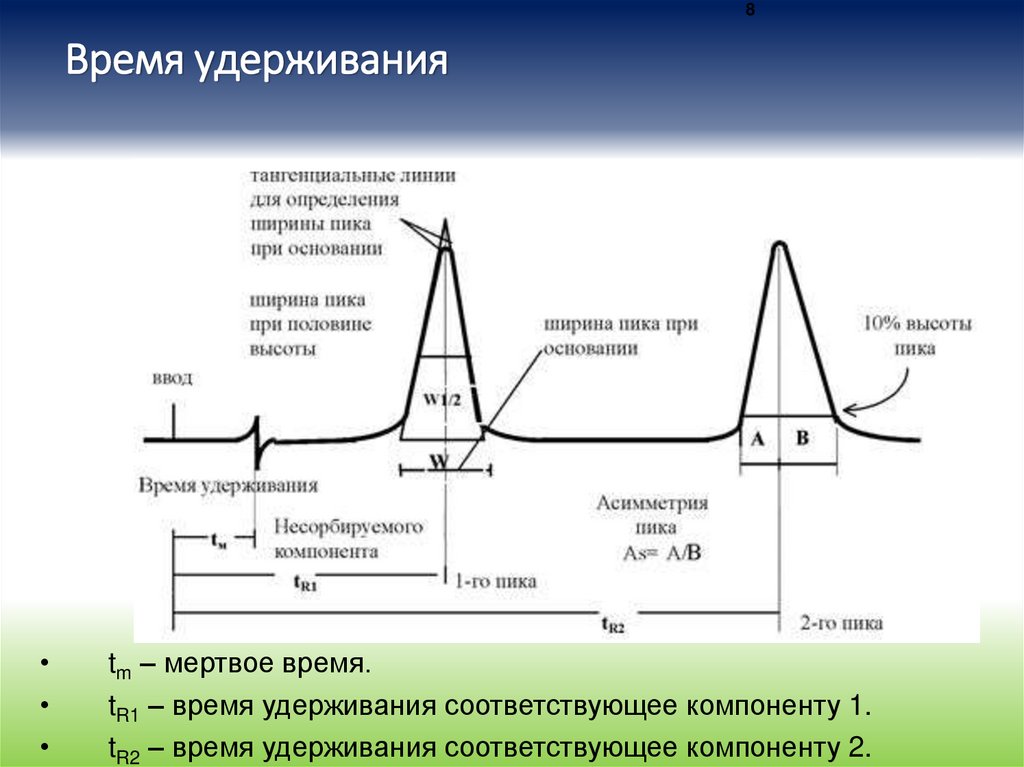
8Время удерживания
tm – мертвое время.
tR1 – время удерживания соответствующее компоненту 1.
tR2 – время удерживания соответствующее компоненту 2.
9.
9Характеристики пика
Время ( tR )
Ширина основания пика - W
Высота пика – h
Площадь пика – Si = h*Wh
Wh – ширина пика на половине высоты
10.
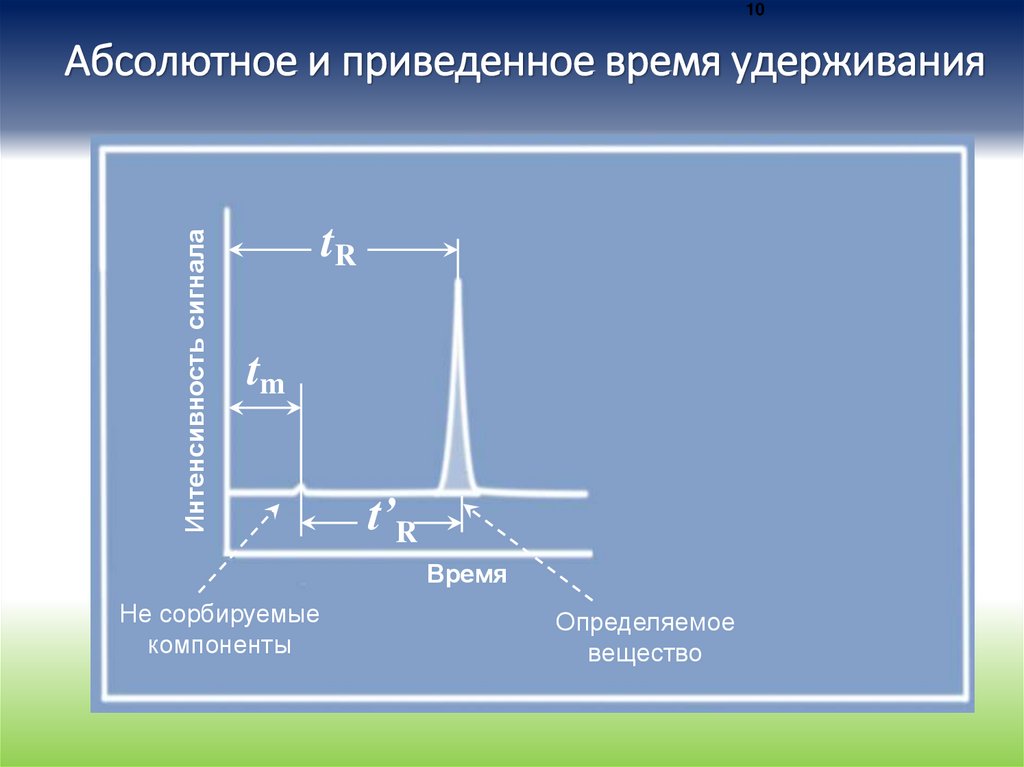
10Интенсивность сигнала
Абсолютное и приведенное время удерживания
tR
tm
t’R
Время
Не сорбируемые
компоненты
Определяемое
вещество
11.
11Различия между абсолютным и приведенным
временами удерживания
t’R = tR - tm
• tR - абсолютное время удерживания
• tm - «мертвое время»
• t`R исправленное временя удерживания
• K = t’R/tm фактор удерживания, (фактор емкости). Не
зависит от габаритов колонки и скорости подвижной
фазы
12.
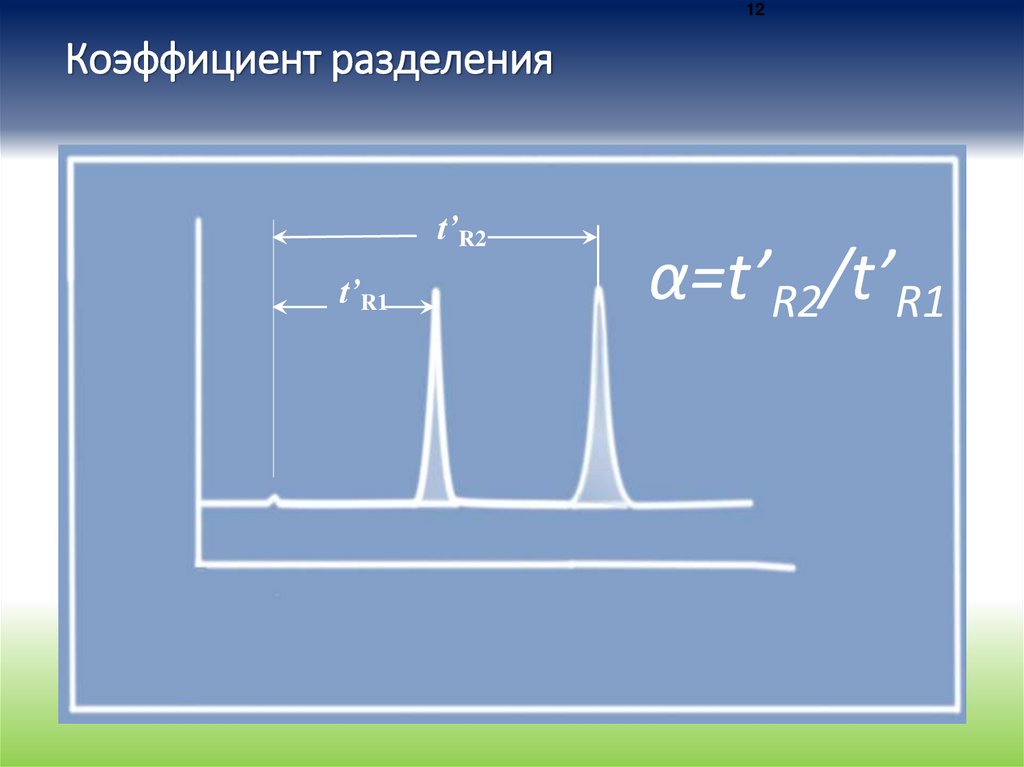
12Коэффициент разделения
t’R2
t’R1
α=t’R2/t’R1
• где tR - времена удерживания соединений i и j
• Wb - ширина их пиков у основания
13.
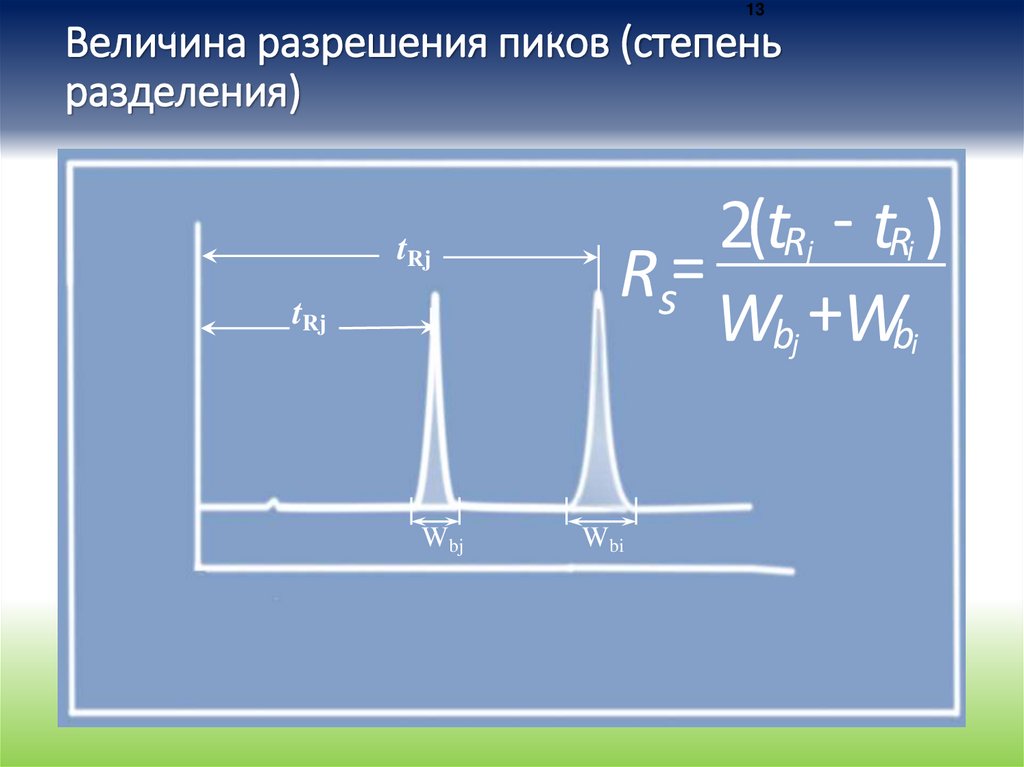
13Величина разрешения пиков (степень
разделения)
tRj
tRj
Wbj
2(tRj - tRi )
Rs=
Wbj +Wbi
Wbi
• где tR - времена удерживания соединений i и j
• Wb - ширина их пиков у основания
14.
14Степень разделения R
15.
15Селективность и эффективность
Эффективность колонки– мера уширения хроматографической
зоны вещества при прохождении через колонку.
Характеризуется числом теоретических тарелок.
Чем выше эффективность, тем более узкие пики при том же
времени удерживания.
Селективность колонки – величина, отражающая селективные
физико-химические взаимодействия между анализируемыми
веществами и хроматографической системой.
a= t’R2/t’R1
Чем выше селективность, тем лучше разделяются пики между
собой.
16.
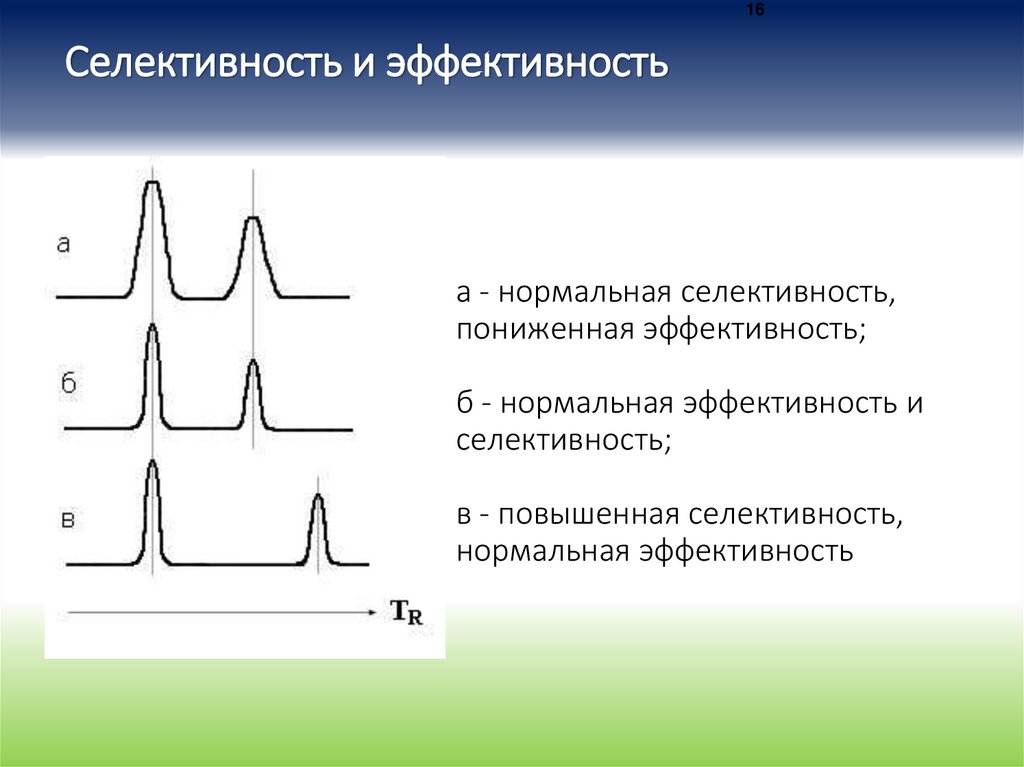
16Селективность и эффективность
а - нормальная селективность,
пониженная эффективность;
б - нормальная эффективность и
селективность;
в - повышенная селективность,
нормальная эффективность
17.
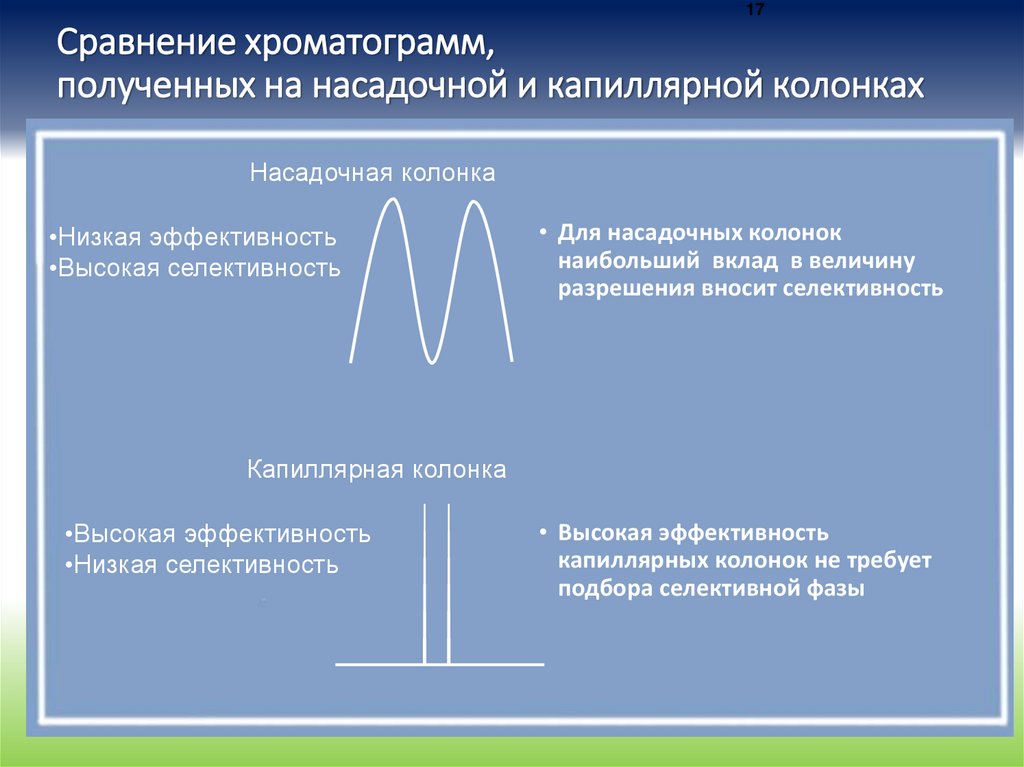
17Сравнение хроматограмм,
полученных на насадочной и капиллярной колонках
Насадочная колонка
•Низкая эффективность
•Высокая селективность
• Для насадочных колонок
наибольший вклад в величину
разрешения вносит селективность
Капиллярная колонка
•Высокая эффективность
•Низкая селективность
• Высокая эффективность
капиллярных колонок не требует
подбора селективной фазы
18.
18Теория тарелок
• Теоретическая тарелка – участок колонки, в пределах
которого устанавливается равновесное распределение
вещества между подвижной и неподвижной фазами.
• Высота Н, эквивалентная теоретической тарелке (ВЭТТ) высота слоя сорбента, при прохождении которого акт
сорбции-десорбции совершается в среднем один раз.
N= L/H
N – число теоретических тарелок
L – длина колонки, мм
H – ВЭТТ, мм
19.
19Расчет числа теоретических тарелок
N = 5,545(ti / W0.5)2
N = 16(ti / Wi)2
N - число теоретических тарелок
ti - время удерживания
W 0.5 – ширина пика на половине высоты
W I – ширина пика у основания
20.
20Факторы, влияющие на размывание
хроматографической полосы
• Турбулентная диффузия
• Молекулярная диффузия
• Сопротивление колонки массообмену
21.
21Турбулентная диффузия
• Присутствует в насадочных колонках
• Причины – неравномерность заполнения.
• Следствие – различные траектории молекул при
прохождении через колонку.
• Способ подавления – использование однорoдного материала
для набивки колонки, равномерное заполнение колонки.
• Невозможность полного исключения в насадочных колонках
22.
22Молекулярная диффузия
• Причина – броуновское движение. Молекулы двигаются не
только к выходу колонки, но и в других направлениях
• В насадочных колонках влияние молекулярной диффузии
сильнее, чем в капиллярных
• Способ подавления – увеличение плотности газовой среды
23.
23Сопротивление колонки массообмену
• Причина – конечность скорости установления равновесия
распределения вещества между фазами.
• Способы подавления:
Насадочные колонки – носители с невысокой удельной
поверхностью, однородные пленки жидкой фазы
24.
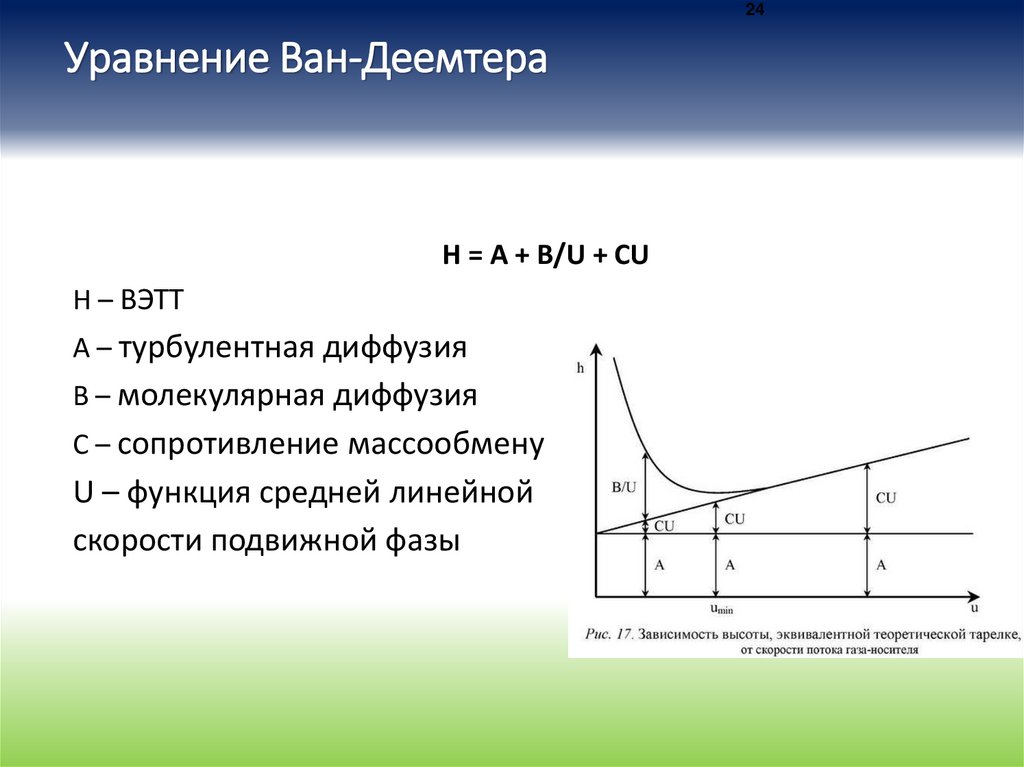
24Уравнение Ван-Деемтера
H = A + B/U + CU
H – ВЭТТ
А – турбулентная диффузия
В – молекулярная диффузия
С – сопротивление массообмену
U – функция средней линейной
скорости подвижной фазы
25.
25Уравнение Голея
H = A + B/U + CU
Уравнение Ван-Деемтера
В открытых капиллярных колонках отсутствует влияние насадки
А – турбулентная диффузия
=0
H = B/U + CU
H – ВЭТТ
В – молекулярная диффузия
С – сопротивление массообмену
U – функция средней линейной
скорости подвижной фазы
26.
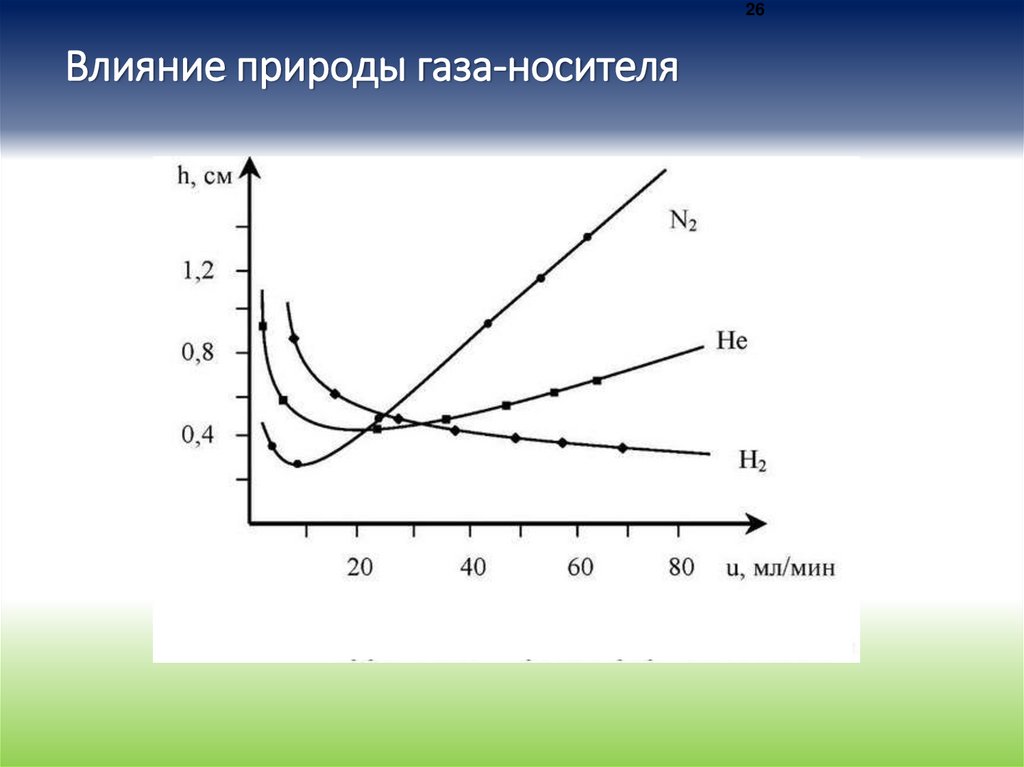
26Влияние природы газа-носителя
27.
27Зависимость степени разделения от
параметров, связанных с колонкой
1.
2.
3.
4.
Сорбент. Природа сорбента определяет тип и силу взаимодействия
между сорбентом и сорбатом и, следовательно, селективность
разделения. Селективность зависит также от доли неподвижной фазы
в единице объема колонки. Чем больше доля неподвижной фазы – тем
селективнее колонка.
Длина колонки. Степень разделения R пропорциональна квадратному
корню из длины колонки.
Диаметр колонки. Разделительная способность колонки обратно
пропорциональна диаметру колонки. Ширина пика прямо
пропорциональна сечению колонки.
Форма колонки. Наибольшая эффективность на прямых и U образных.
28.
28Зависимость степени разделения от
параметров, связанных с колонкой
5. Размер зерен сорбента. Размывание за счет вихревой диффузии
уменьшается с уменьшением диаметра частиц и с увеличением
однородности. Сферические частицы 0.1 – 0.3 мм.
6. Толщина пленки жидкой фазы. Чем толще, тем больше селективность,
но падает эффективность.
7. Температура. Влияет на время удерживания, селективность,
эффективность разделения. В большинстве случаев с ростом
температуры время удерживания уменьшается.
29.
29Зависимость результатов хроматографического
анализа от параметров опыта
1.
2.
3.
4.
Колонка – природа сорбента, температура, геометрия (длина, сечение,
форма), зернение (размер, форма зерен), толщина жидкой пленки или
пористость сорбента (удельная поверхность, средний диаметр пор),
качество набивки.
Газ-носитель – природа, скорость, вязкость, давление.
Параметры, относящиеся к работе дозатора – размер пробы, способ
дозирования.
Параметры детектирующих систем – предел детектирования
(чувствительность), инерционность, линейный диапазон, стабильность
детектора (шум, дрейф)
30.
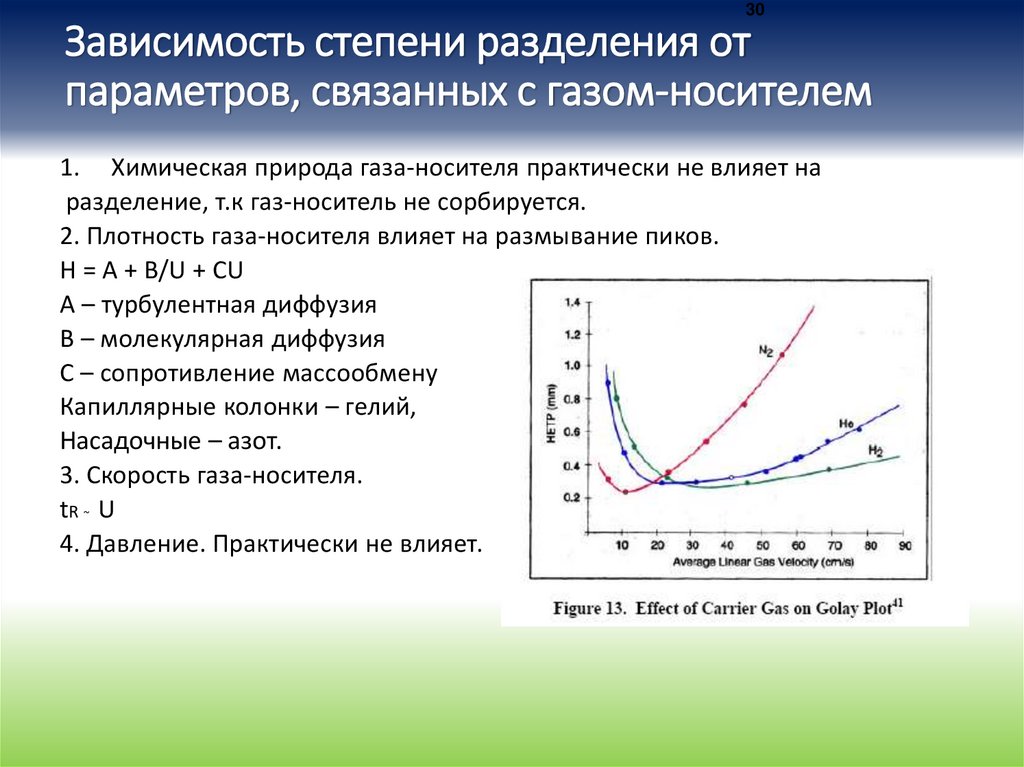
30Зависимость степени разделения от
параметров, связанных с газом-носителем
1. Химическая природа газа-носителя практически не влияет на
разделение, т.к газ-носитель не сорбируется.
2. Плотность газа-носителя влияет на размывание пиков.
H = A + B/U + CU
А – турбулентная диффузия
В – молекулярная диффузия
С – сопротивление массообмену
Капиллярные колонки – гелий,
Насадочные – азот.
3. Скорость газа-носителя.
tR ~ U
4. Давление. Практически не влияет.
31.
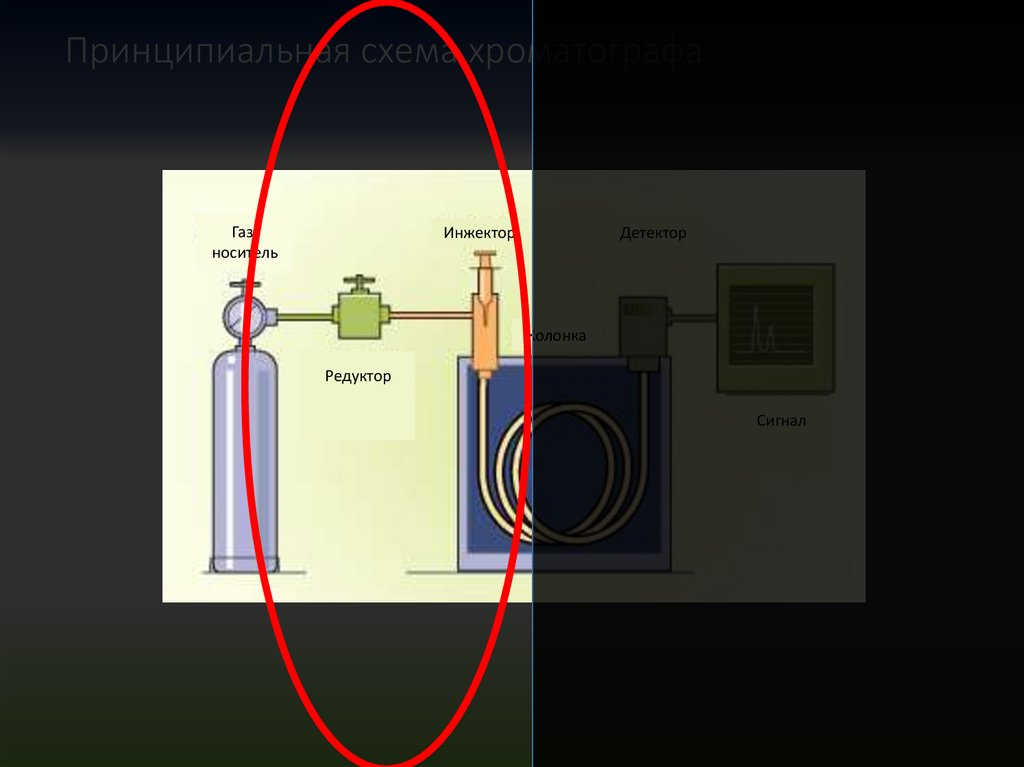
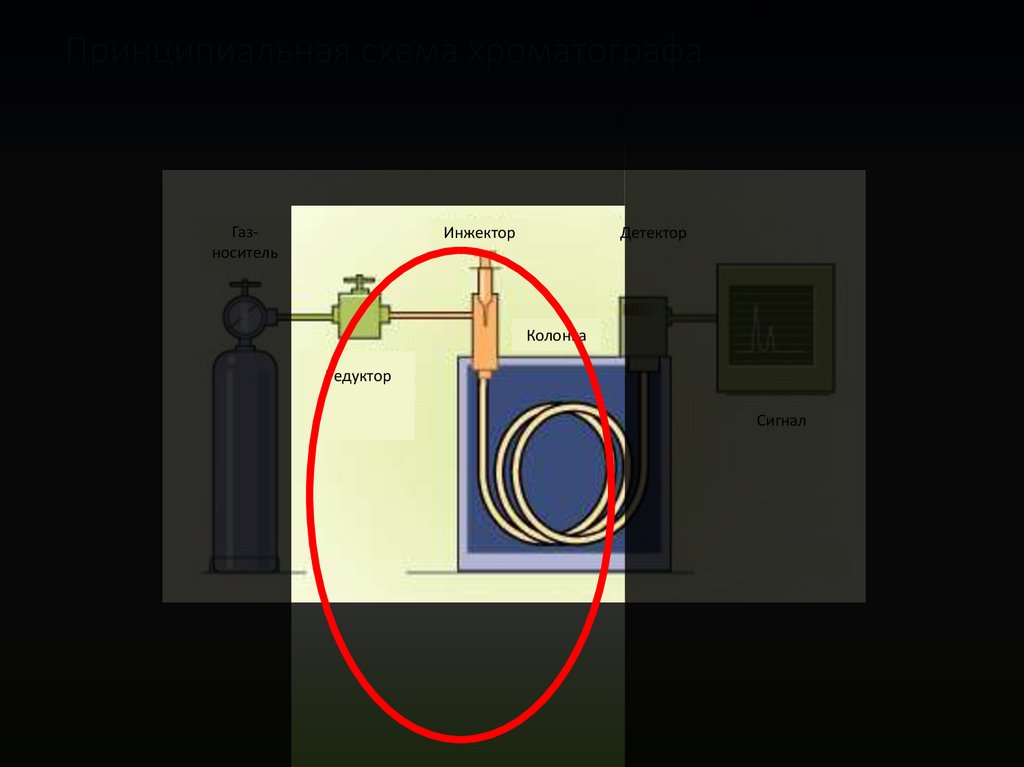
31Принципиальная схема хроматографа
Газноситель
Инжектор
Детектор
Колонка
Редуктор
Сигнал
32.
32Газ-носитель
• Является подвижной фазой в газовой
хроматографии
• Обеспечивает перенос десорбированных молекул
по колонке
• Регулирует константы равновесия, а, следовательно,
и удерживание в результате взаимодействия с
неподвижной фазой
33.
33Требования к газу-носителю
• газ-носитель должен способствовать обеспечению
оптимального разделения компонентов смеси;
• газ-носитель должен обеспечить максимально высокую
чувствительность детектора;
• газ-носитель должен характеризоваться химической
инертностью по отношению к компонентам
разделяемой смеси, наполнителю хроматографической
колонки, материалу, из которого изготовлена колонка и
газовые магистрали (например, при использовании
водорода возможно гидрирование ненасыщенных
соединений);
• газ-носитель должен иметь достаточно высокую степень
чистоты (99,9 - 99,99 % основного компонента);
34.
34Требования к газу-носителю
• газ-носитель должен значительно слабее удерживаться
неподвижной фазой по сравнению с любым из
разделяемых компонентов, поскольку только в этом
случае выполняются условия элюентного анализа;
• газ-носитель должен иметь небольшую вязкость для
поддержания минимального перепада давления в
колонке, минимального значения разности давлений
газа-носителя на входе в колонку и на выходе из нее;
• газ-носитель должен обеспечивать оптимальное
значение коэффициентов диффузии разделяемых
компонентов, способствующее минимальному
размыванию полос;
35.
35Требования к газу-носителю
• газ-носитель должен быть взрывобезопасен;
• газ-носитель должен иметь низкую стоимость.
• В практике газовой хроматографии в качестве газаносителя чаще всего используются индивидуальные
газы и смеси газообразных соединений: азот,
водород, гелий, аргон, углекислый газ, воздух.
36.
36Основные характеристики газов-носителей
Газ-носитель
азот
Преимущества
доступность;
простота очистки;
низкая стоимость;
безопасность в работе.
высокая теплопроводность
(обеспечивает высокую
чувствительность детектора по
водород
теплопроводности);
легко получается в чистом виде
электролизом.
теплопроводность близкая к
водороду;
гелий
безопасность в работе.
доступность,
аргон
низкая стоимость.
доступность,
углекислый газ
низкая стоимость.
Недостатки
низкая теплопроводность,
близкая к легким
углеводородам,
обуславливающая низкую
чувствительность детектора
по теплопроводности.
взрывоопасность при
утечке.
высокая стоимость,
обусловленная трудностями
получения и очистки.
низкая теплопроводность.
низкая теплопроводность.
37.
37Фильтры для газов-носителей
38.
38Функции фильтры для газов-носителей
• Очистка газов-носителей от сопутствующих примесей,
которые могут повлиять негативно на чувствительность
детектора, способствовать деградации
хроматографической колонки и собционной активации
узлов хроматографической системы
• Снижение пульсации потока газа-носителя
39.
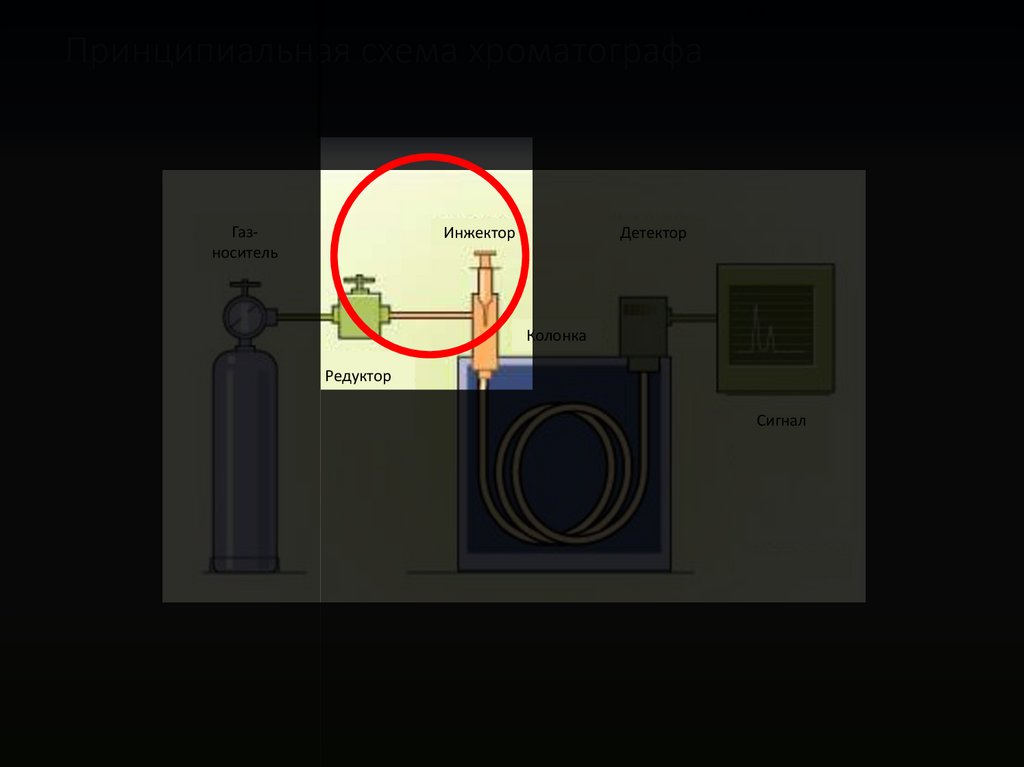
39Принципиальная схема хроматографа
Газноситель
Инжектор
Детектор
Колонка
Редуктор
Сигнал
40.
40Требования к газовым редукторам
Редуктор газовый должен:
• Обеспечивать точную регулировку давления газа на выходе
• Обладать инертностью к редуцируемым газам
• Минимизировать пульсирование потока газа при
редуцировании
• Обеспечивать герметичность всей газовой системы
41.
41Устройства ввода пробы
Способы ввода проб:
Газ : Кран-дозатор или газоплотный шприц.
Жидкость : Микрошприц
Твердое : Растворение и дозирование микрошприцом,
либо прямое дозирование твердого образца с помощью
специального устройства.
42.
42Устройства ввода пробы
Шприцы для ввода пробы
43.
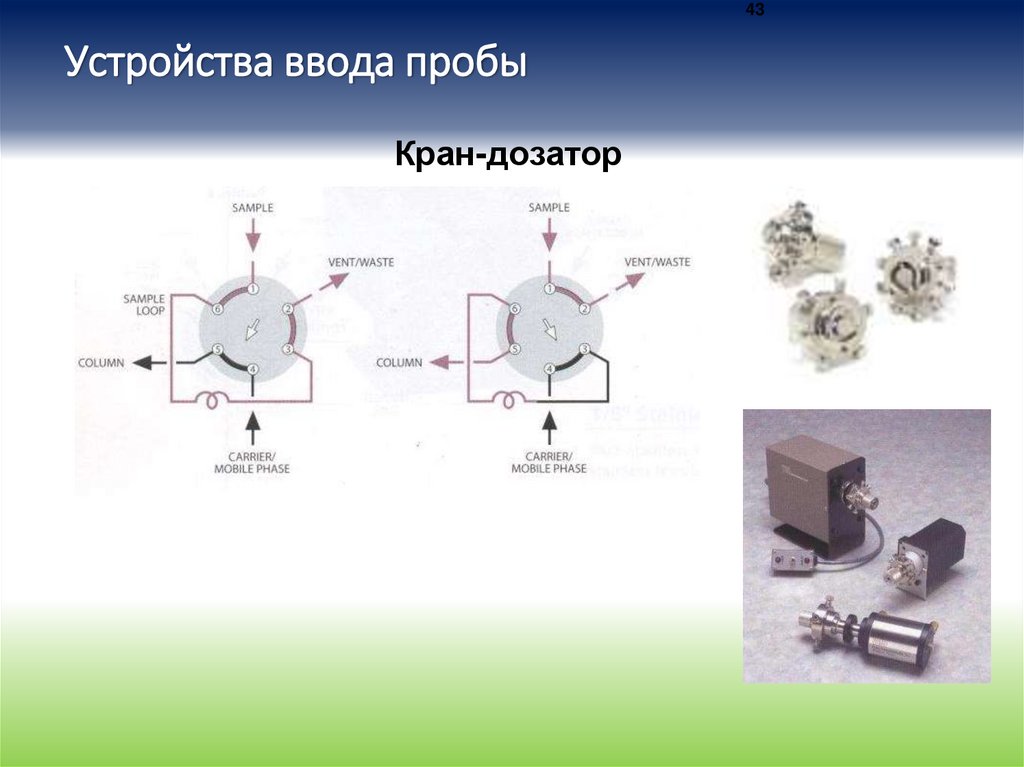
43Устройства ввода пробы
Кран-дозатор
44.
44Устройства ввода пробы
• Микрошприцы МШ-1, МШ-10, Газохром, Hamilton, SGE
• Газовые шприцы
• Автоматические дозаторы
• Шприцы SPME
• Кран-дозаторы
• Термодесорберы
• Пиролизеры
45.
45Параметры, относящиеся к работе дозатора
• Скорость дозирования: быстрое дозирование – узкая полоса,
медленное – широкая, возможность деградации пробы
• Размер пробы не должен вызывать перегрузку колонки.
Большие объемы пробы могут привести к изменению
времен удерживания
46.
46Дозируемые объемы
1. Насадочные колонки
Газ
: 0.5-5 мл
Жидкость : 0.1-10мкл
2. Капиллярные колонки
Газ
: 0.1-1 мл
Жидкость : 0.01-2.0мкл
47.
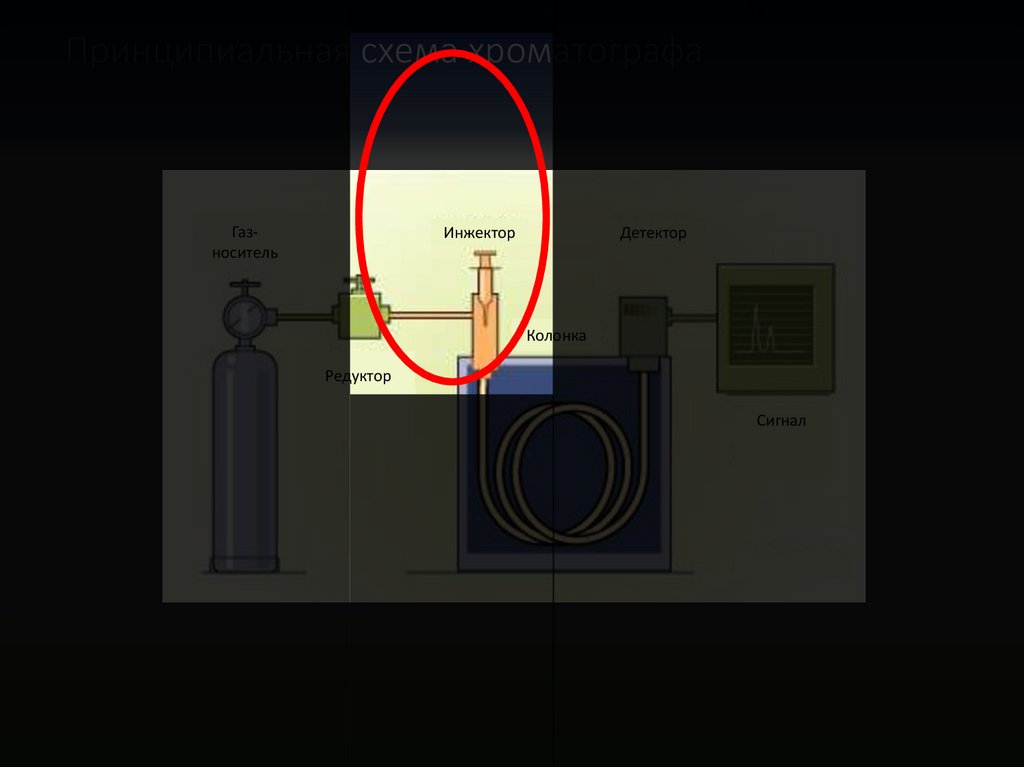
47Принципиальная схема хроматографа
Газноситель
Инжектор
Детектор
Колонка
Редуктор
Сигнал
48.
48Типы инжекторов
1. Инжектор для насадочных колонок
2. Инжектор для капиллярных колонок
- Split инжектор
- Splitless инжектор
- PTV(Температурно-программируемый инжектор)
- Cool on-column инжектор
- Wide-bore инжектор для широких капиллярных колонок.
49.
49Способы ввода пробы в капиллярную систему
1. Split – инжекция с делением потока
-Split / Splitless injector
-PTV injector
2. Splitless – инжекция без деления потока
-Split и Splitless injector
3. Прямая инжекция в колонку
- on-column injector
-Wide bore инжектор для широких капиллярных
колонок
50.
50Схема инжектора для насадочных колонок
Шприц
Игла шприца
септа
Верхняя крышка прибора
Блок нагрева инжектора
Газ-носитель
Колонка
муфта
Колонка
51.
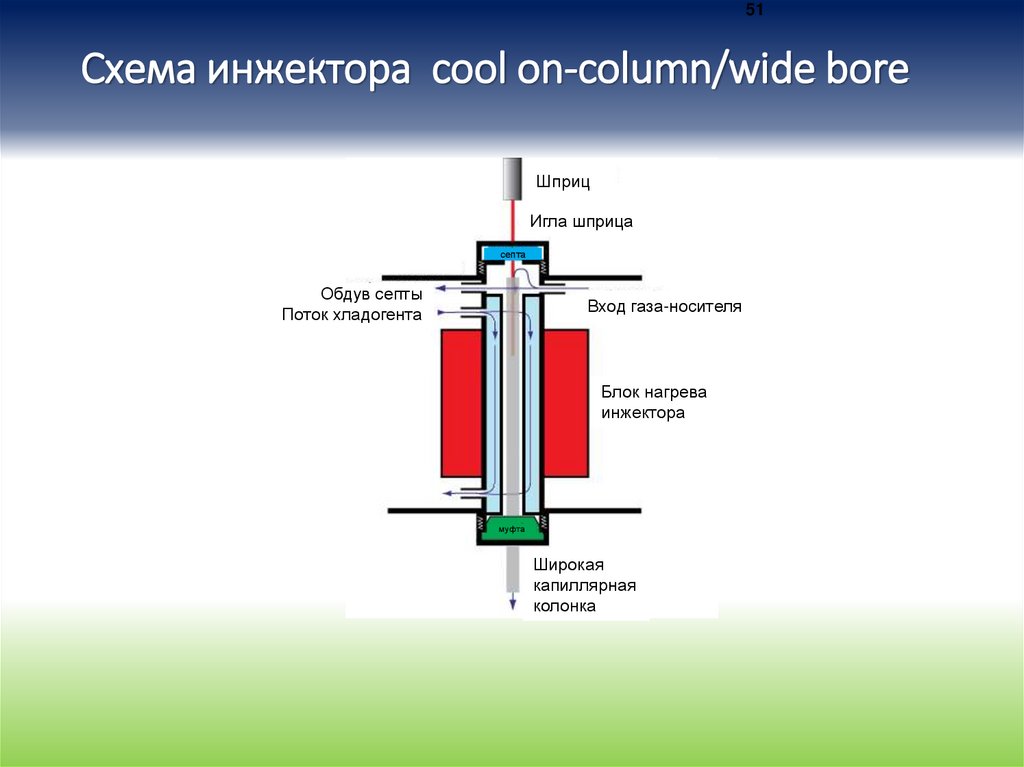
51Схема инжектора cool on-column/wide bore
Шприц
Игла шприца
Верхняя крышка прибора
септа
Обдув септы
Поток хладогента
Вход газа-носителя
Стеклянный лайнер
Блок нагрева
инжектора
Верхняя крышка прибора
муфта
Широкая
капиллярная
колонка
52.
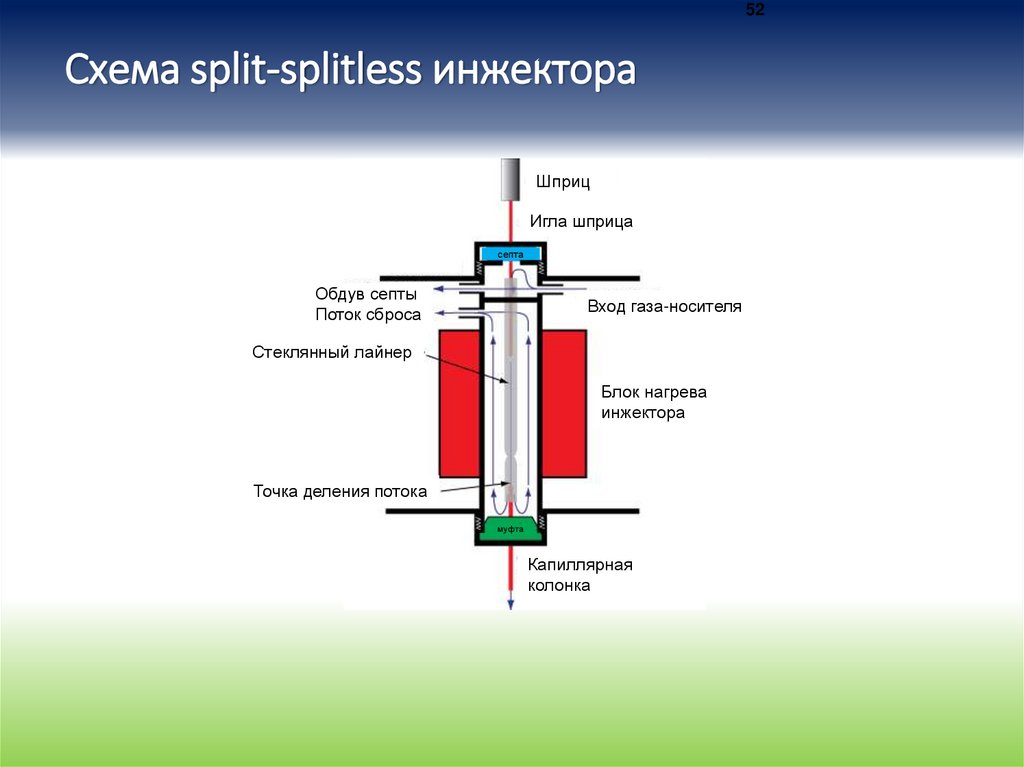
52Схема split-splitless инжектора
Шприц
Игла шприца
Верхняя крышка прибора
септа
Обдув септы
Поток сброса
Вход газа-носителя
Стеклянный лайнер
Блок нагрева
инжектора
Точка деления потока
Верхняя крышка прибора
муфта
Капиллярная
колонка
53.
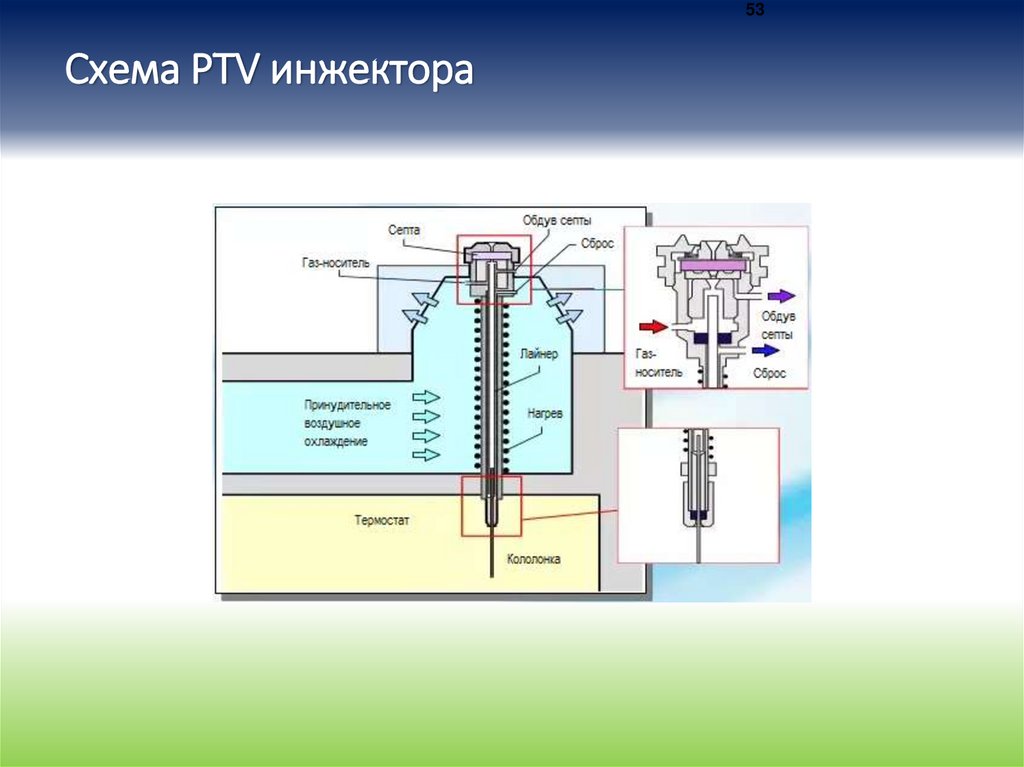
53Схема PTV инжектора
Верхняя крышка прибора
54.
54Лайнер для инжектора
• Лайнер – вставка в инжектор из тугоплавкого стекла
• Функции лайнера:
• Испарение жидкой пробы
• Равномерное перемешивание пробы с газом-носителем
• Быстрый перенос испаренных компонентов в колонку
• Удерживание трудно-летучих и нелетучих компонентов пробы
• Обеспечение стабильного и воспроизводимого ввода пробы
55.
55Лайнер для режима работы Split
• Режим работы Split используется в случае высоких
концентраций аналитов в пробе или отсутствия
необходимости достигать низких пределов обнаружения
Деактивированная стекловата
Циклонная вставка
56.
56Лайнер для режима работы Splitless
• Режим работы Splitless используется в случае
необходимости определения низких концентраций
аналитов в пробе
Деактивированная стекловата
Циклонная вставка
57.
57Лайнер для режима работы Direct
• Режим работы Direct используется в случае
необходимости определения следовых количеств
аналитов в пробе
58.
58Лайнер для ввода газовой пробы или SPME
Лайнеры для ввода газовых проб
Лайнер для SPME
59.
59Лайнер для PTV инжектора
• Принцип работы PTV инжектора следующий: проба
вводится в холодный инжектор с последующим его
разогревом.
60.
60Основные производители лайнеров
на сайте представлен обширный выбор
лайнеров для приборов различных производителей
компания предлагает использовать
программу облегчающую выбор лайнера под
конкретную задачу (бесплатно скачать на сайте)
является одним из основных
поставщиков комплектующих для приборов различных
производителей
Фирмы производители приборов (agilent, shimadzu,
thermo …)
61.
61Принципиальная схема хроматографа
Газноситель
Инжектор
Детектор
Колонка
Редуктор
Сигнал
62.
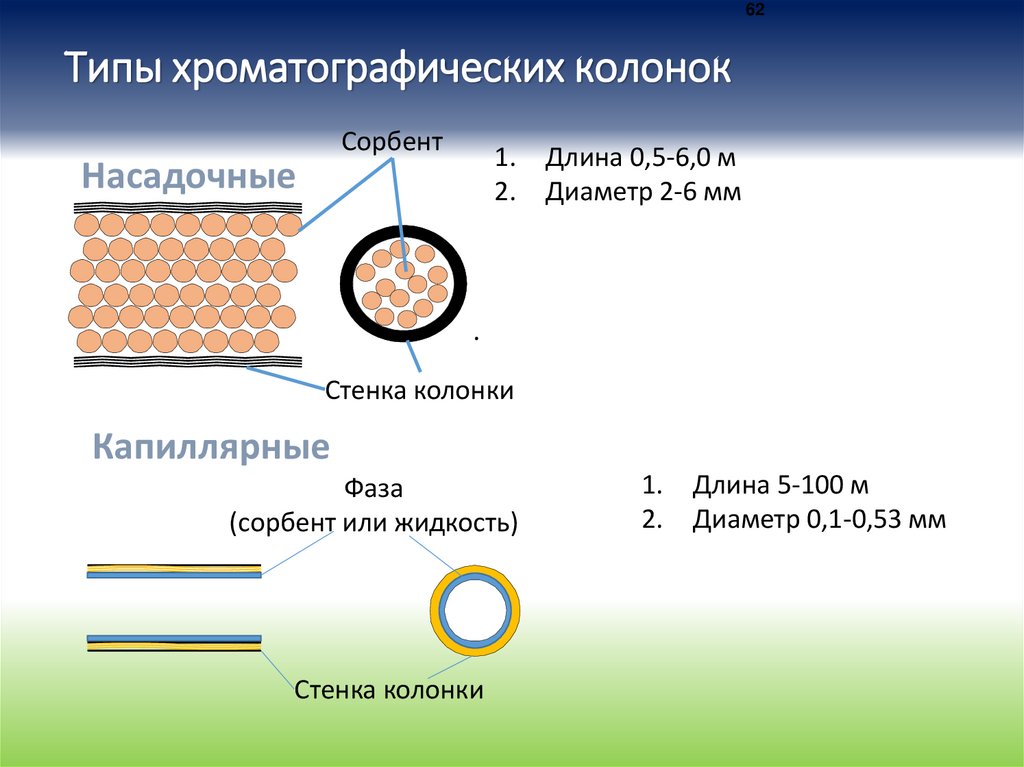
62Типы хроматографических колонок
Сорбент
1.
2.
Насадочные
Длина 0,5-6,0 м
Диаметр 2-6 мм
.
Стенка колонки
Капиллярные
Фаза
(сорбент или жидкость)
Стенка колонки
1.
2.
Длина 5-100 м
Диаметр 0,1-0,53 мм
63.
63Хроматографические колонки
Капиллярные колонки
Насадочные колонки
64.
64Насадочные колонки
• Обладают большей емкостью по сравнению с
капиллярными
• Сорбент подбирается под конкретную задачу
• Материал колонки может варьироваться в зависимости
от задачи
• Обладают большей селективностью по сравнению с
капиллярными
• Могут быть изготовлены в лаборатории
65.
65Адсорбенты
S уд = 10 – 103 м2/г ( оптимальное 60 -400 м2/г)
Углеродные сорбенты (Carbopack, Carboxen и др)
Силикагель (Силохром, Сhromosil , силипор)
Оксид алюминия
Молекулярные сита (цеолиты)(4А – NaA, 5А – СаА , 10Х – СаХ,
13Х – NaX)
Пористые полимеры (Полисорб, Порапак, Hayesep, Тенакс)
66.
66Носители для жидкой фазы
•Задача носителя – локализация жидкой фазы
и обеспечение максимального массообмена
между подвижной и неподвижной фазами
•Требования: механическая прочность,
термостабильность, развитая поверхность,
инертность к разделяемым компонентам.
•Sуд.≈ 1 – 10 м2/г
67.
67Типы носителей
Диатомитовые
SiO2...Al2O3 ...K2O ...CaO...NaO
Хроматон, инертон, динохром,
Хромосорб, хезасорб, сферохром
Хромосорб Р розовый
Хромосорб W белый
Хромосорб W АW промытый кислотой
Хромосорб W АW DMCS силанизированный
Недиатомитовые
Стеклянные шарики,
тефлон,
неорганические
соли
68.
68Неподвижные жидкие фазы
Требования:
дифференцированное разделение анализируемых веществ,
термическая устойчивость (t кип. н.ф. > t кол. на 100 – 200о),
химическая стабильность,
инертность по отношению к разделяемым соединениям
Не смешиваемость с подвижной фазой
Нижний и верхний температурный предел
69.
69Наиболее распространенные неподвижные
фазы
• Силоксановые смазки (каучуки) на основе полиметилсилоксанов:
метилсиликоновые (SE-30, OV-1, HP-1, DB-1), фенилметилсиликоновые (
SE-54, OV-17, HP-5), цианопропилсиликоновые (OV-275, OV-225, SPB-225)
• Полигликоли (карбоваксы) ПЭГ, ПЭГА (HP INNOWAX, Supelcowax)
• Апиезоны L и М.
• Сквалан (С30Н62 гексаметилтетракозан)
70.
70Полярность неподвижной фазы
• Взаимодействие анализируемого вещества и неподвижной
фазы обусловливают: дисперсионные взаимодействия,
специфические взаимодействия (дипольные, водородные
связи)
• Полярность обусловливает взаимодействие НФ с полярными
группами анализируемого вещества
• Шкала полярности 0 – сквалан; 100 – оксидипропионитрил
• Колонки на основе ионных жидкостей по шкале полярности
расположены выше отметки 100
71.
71Выбор насадочной колонки
• При выборе насадочной колонки нужно
ориентироваться:
• Справочные данные по данному типу анализа
• Учитывать возможность сорбции компонентов пробы на выбранном
сорбенте
• Учитывать инертность материала колонки по отношению к
компонентам пробы
• Свойства сорбента и нанесенной жидкой фазы
«Насадочные колонки в газовой хроматографии»
автор Супина Вальтер
72.
72Капиллярные колонки
• Обладают большей эффективностью по сравнению с
насадочными
• На одной колонке возможно эффективно решать
несколько аналитических задач
• Материал колонки может варьироваться в зависимости
от задачи
• Не могут быть изготовлены в лаборатории
73.
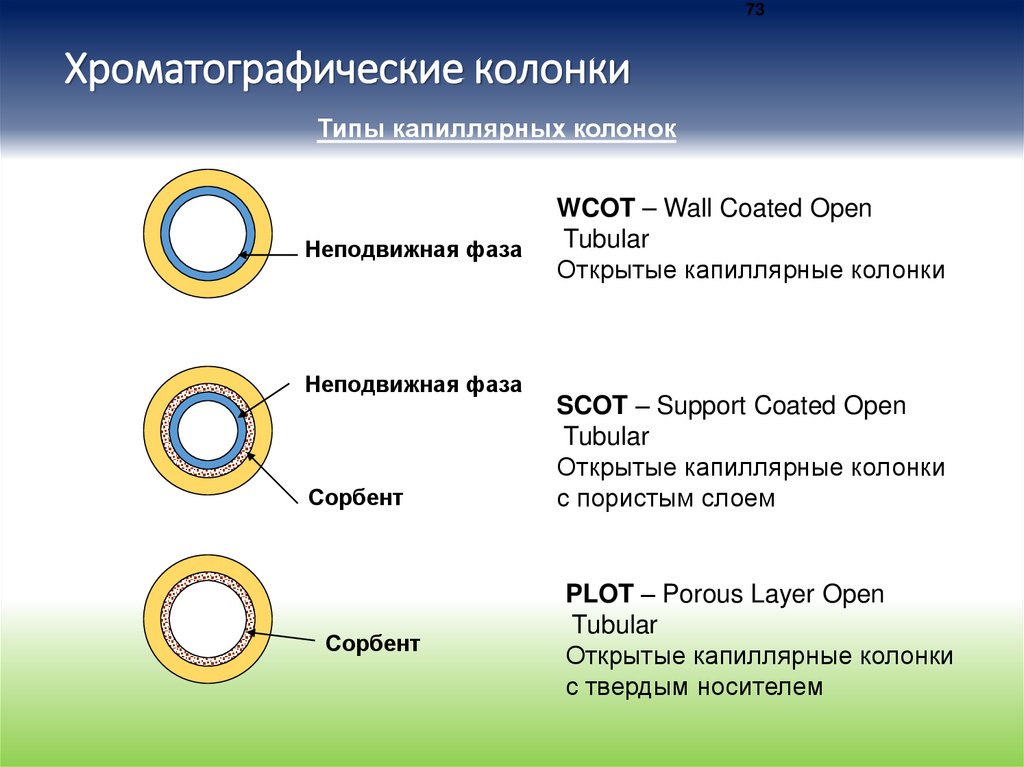
73Хроматографические колонки
Типы капиллярных колонок
Неподвижная фаза
Неподвижная фаза
Сорбент
Сорбент
WCOT – Wall Coated Open
Tubular
Открытые капиллярные колонки
SCOT – Support Coated Open
Tubular
Открытые капиллярные колонки
с пористым слоем
PLOT – Porous Layer Open
Tubular
Открытые капиллярные колонки
с твердым носителем
74.
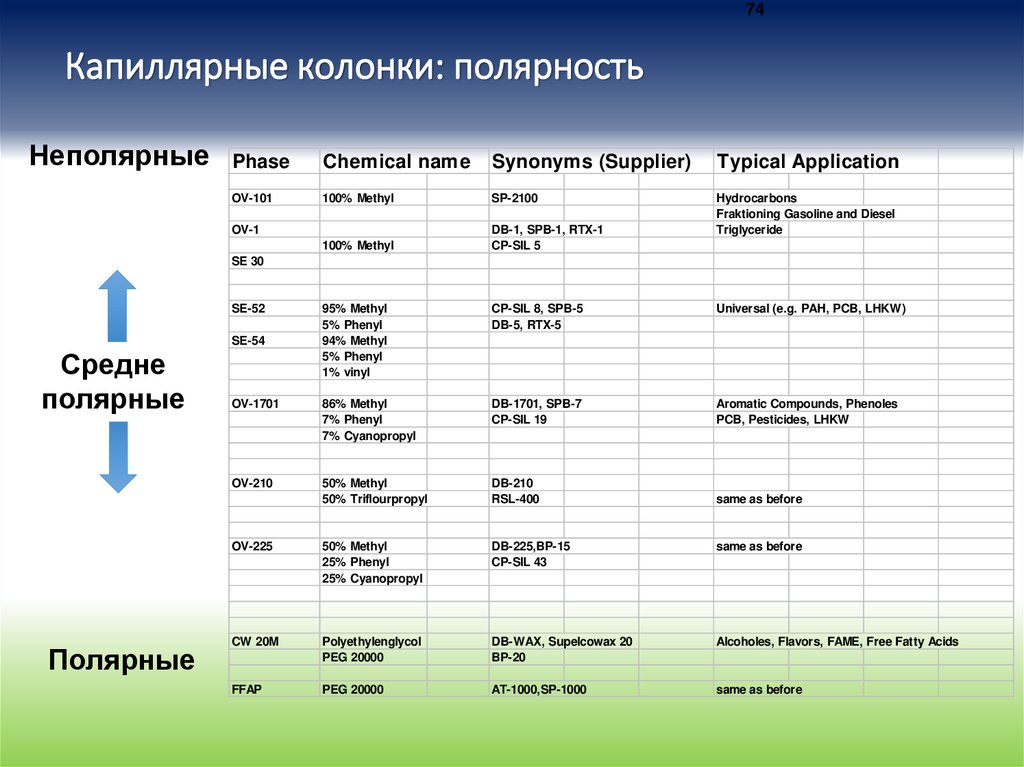
74Капиллярные колонки: полярность
Неполярные
Phase
Chemical name
Synonyms (Supplier)
Typical Application
OV-101
100% Methyl
SP-2100
100% Methyl
DB-1, SPB-1, RTX-1
CP-SIL 5
Hydrocarbons
Fraktioning Gasoline and Diesel
Triglyceride
OV-1
SE 30
SE-52
95% Methyl
5% Phenyl
94% Methyl
5% Phenyl
1% vinyl
CP-SIL 8, SPB-5
DB-5, RTX-5
Universal (e.g. PAH, PCB, LHKW)
OV-1701
86% Methyl
7% Phenyl
7% Cyanopropyl
DB-1701, SPB-7
CP-SIL 19
Aromatic Compounds, Phenoles
PCB, Pesticides, LHKW
OV-210
50% Methyl
50% Triflourpropyl
DB-210
RSL-400
same as before
OV-225
50% Methyl
25% Phenyl
25% Cyanopropyl
DB-225,BP-15
CP-SIL 43
same as before
CW 20M
Polyethylenglycol
PEG 20000
DB-WAX, Supelcowax 20
BP-20
Alcoholes, Flavors, FAME, Free Fatty Acids
FFAP
PEG 20000
AT-1000,SP-1000
same as before
SE-54
Средне
полярные
Полярные
75.
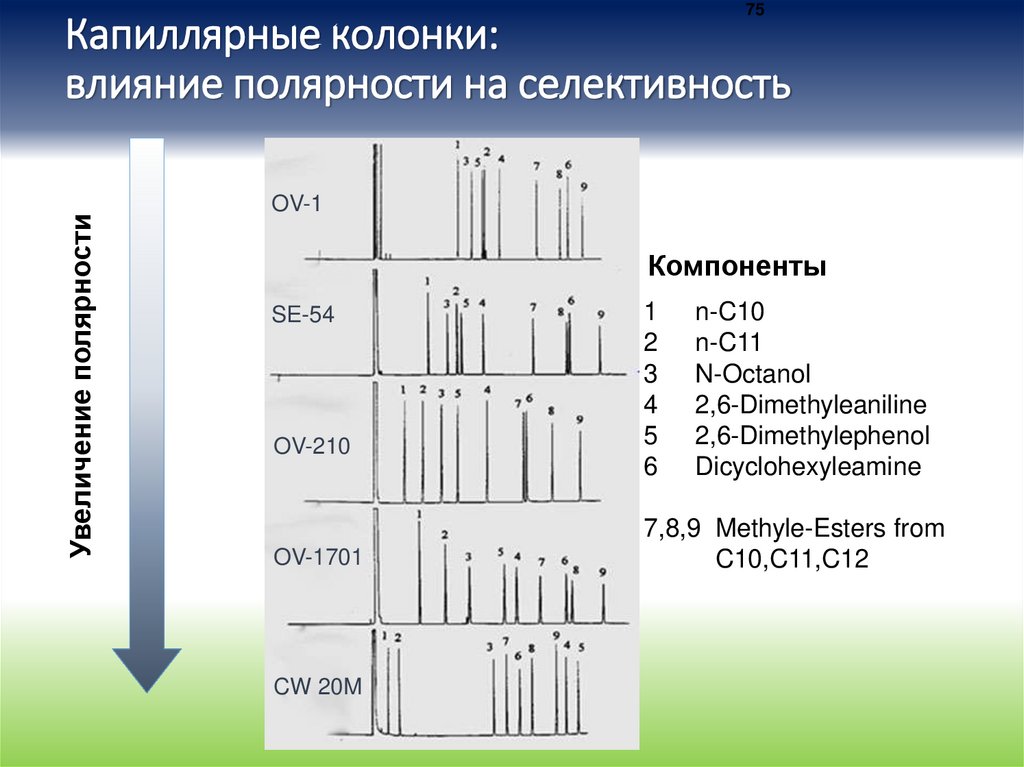
75Увеличение полярности
Капиллярные колонки:
влияние полярности на селективность
OV-1
Компоненты
SE-54
OV-210
OV-1701
CW 20M
1
2
3
4
5
6
n-C10
n-C11
N-Octanol
2,6-Dimethyleaniline
2,6-Dimethylephenol
Dicyclohexyleamine
7,8,9 Methyle-Esters from
C10,C11,C12
76.
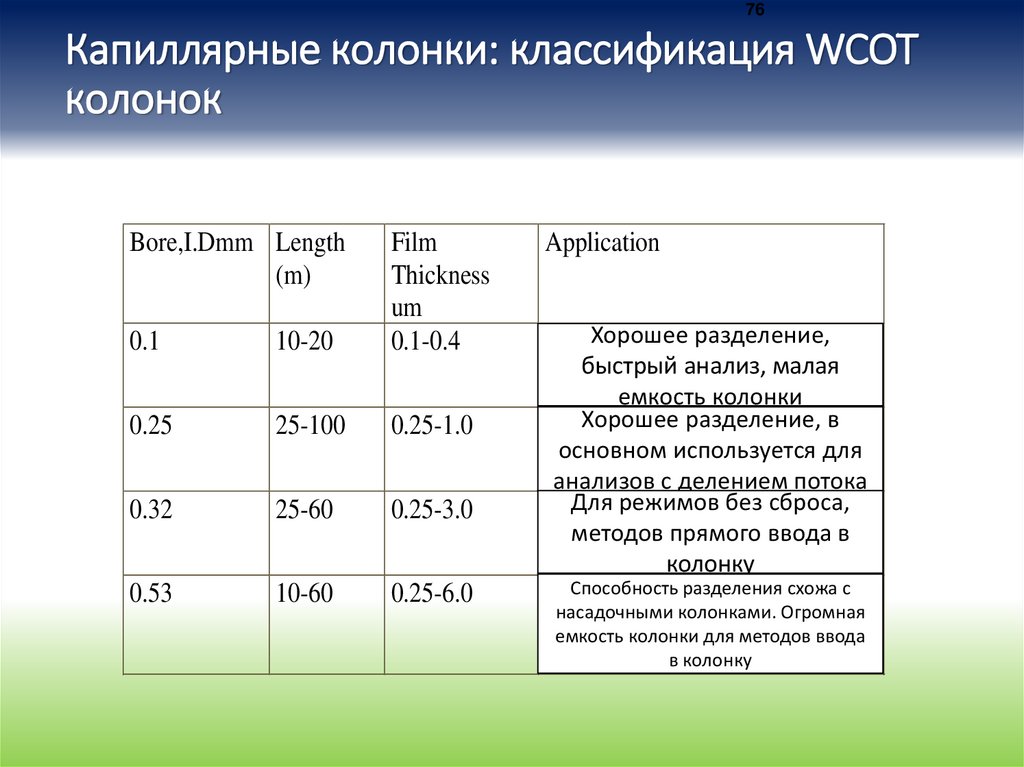
76Капиллярные колонки: классификация WCOT
колонок
Bore,I.Dmm Length
(m)
0.1
10-20
Film
Thickness
um
0.1-0.4
0.25
25-100
0.25-1.0
0.32
25-60
0.25-3.0
0.53
10-60
0.25-6.0
Application
разделение,
HighХорошее
Separation,
Fast analysis,
анализ,
veryбыстрый
small column
loadмалая
емкость колонки
разделение,
в
HighХорошее
separation,
generally used
используется для
inосновном
split type analysis
анализов с делением потока
Дляinрежимов
без сброса,
Used
splitless, on-column
методов
прямого ввода в
injection
method
колонку
Способность
разделения
схожа
Separation
ability
equal to
thatсof
насадочными колонками. Огромная
packed
Large
column
емкостьcolumn.
колонки для
методов
ввода
в колонку
load, on-column
injection method
77.
Уменьшается диаметр – уменьшается ВЭТТ77
ВЭТТ и диаметр колонки
78.
78Выбор капиллярной колонки
• При выборе капиллярной колонки нужно
ориентироваться:
• Справочные данные по данному типу анализа
• Справочные данные по конкретной колонке
• Учитывать инертность пробы к капиллярной колонке
• Свойства сорбента или нанесенной жидкой фазы
У каждого производителя есть приложения по капиллярным
колонкам, таблицы сравнения аналогов.
79.
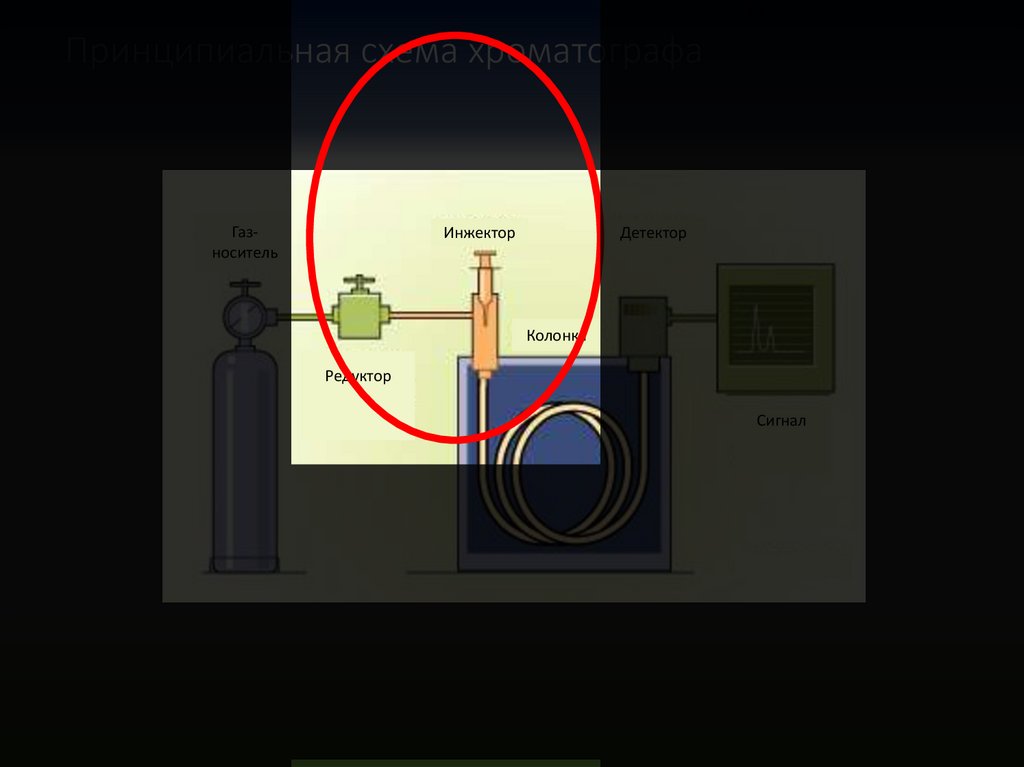
79Принципиальная схема хроматографа
Газноситель
Инжектор
Детектор
Колонка
Редуктор
Сигнал
80.
80Детекторы в газовой хроматографии
Хроматографический детектор представляет собой
прибор, предназначенный для обнаружения и
количественного определения выходящих из колонки в
потоке газа-носителя компонентов анализируемой смеси.
Регистрация сигнала осуществляется за счет
преобразования изменения химических, физических или
физико-химических свойств газового потока в
электрические.
81.
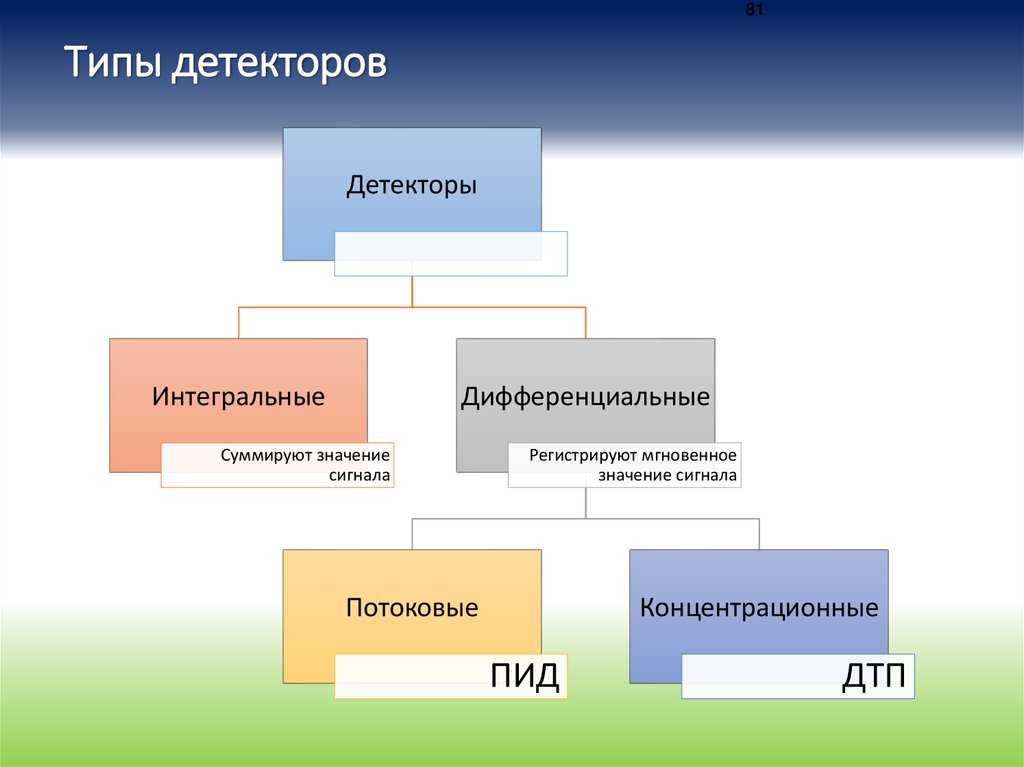
81Типы детекторов
Детекторы
Интегральные
Дифференциальные
Суммируют значение
сигнала
Регистрируют мгновенное
значение сигнала
Потоковые
Концентрационные
ПИД
ДТП
82.
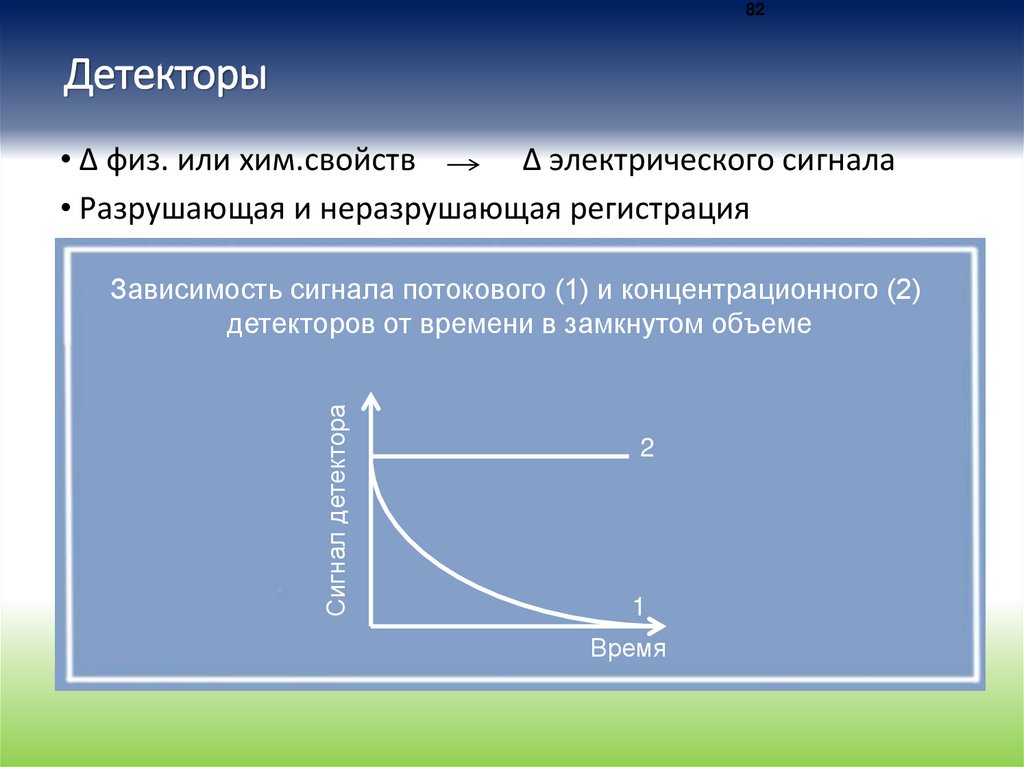
82Детекторы
• Δ физ. или хим.свойств
Δ электрического сигнала
• Разрушающая и неразрушающая регистрация
Сигнал детектора
Зависимость сигнала потокового (1) и концентрационного (2)
детекторов от времени в замкнутом объеме
2
1
Время
83.
83Типы детекторов
Наименование
детектора
Аббревиатура
Принцип работы
ДТП
Регистрируется различие в
теплопроводности
анализируемого вещества и газаносителя
ДПИ
Универсальный для
Образование и регистрация ионов соединений,
при сгорании анализируемых
содержащих С и Н,
веществ в пламени
деструктивный,
ионизационный
МС
Образование
Универсальный,
молекулярных и фрагментарных
деструктивный,
ионов при электронном ударе или
ионизационный
химической ионизации
ДЭЗ
Захват анализируемым веществом
тепловых электронов,
Селективный,
образованных при облучении βнедеструктивный,
частицами или
ионизационный
высокоэнергетическими
электронами газа-носителя
По теплопроводности
Пламенноионизационный
Масс-спектрометр
Электронозахватный
Классификация
Универсальный,
недеструктивный,
неионизационный
84.
84Типы детекторов
Наименование
детектора
Пламеннофотометрический
Термоионный, щелочиопламенноионизационной
Фотоионизациониый
Гелиевый
ионизационный
Аббревиатура
Принцип работы
Классификация
ДПФ
Возбуждение анализируемого
вещества в пламени и излучение
света в зависимости от типа
присутствующего в веществе
элемента
ДТИ
Образование и регистрация ионов
Селективный к N и Р,
в водородном пламени в
деструктивный,
присутствии ионов щелочного
ионизационный
металла (Na, Cs, K, Rb)
ДФИ
Селективен в
Фотохимическое образование и
зависимости от
регистрация ионов под действием
потенциалов ионизации,
жесткого УФ-излучения на
недеструктивный,
анализируемое вещество
ионизационный
ДГИ
Получение метастабильного гелия
различными способами,
Универсальный,
ионизация молекул веществ
деструктивный,
посредством столкновения с
ионизационный
метастабильным гелием
Селективный,
деструктивный,
Спектральный
85.
85Типы детекторов
Наименование
детектора
Термохимический
Хемилюминисцентный
По плотности
Аббревиатура
Принцип работы
Классификация
ДТХ
Каталитическое разложение
анализируемого вещества и
регистрация теплового эффекта
Селективный,
деструктивный,
Спектральный
ДХЛ
Разложение серосодержащих и
азотсодержащих соединений,
которые при реакции с озоном
дают хемилюминисценцию
Селективный к N и S,
деструктивный,
спектральный
ДП
Селективен в
Регистрируется различие
зависимости от
плотностей смеси анализируемого
потенциалов ионизации,
вещества с газом-носителем и
недеструктивный,
чистого газа-носителя
ионизационный
86.
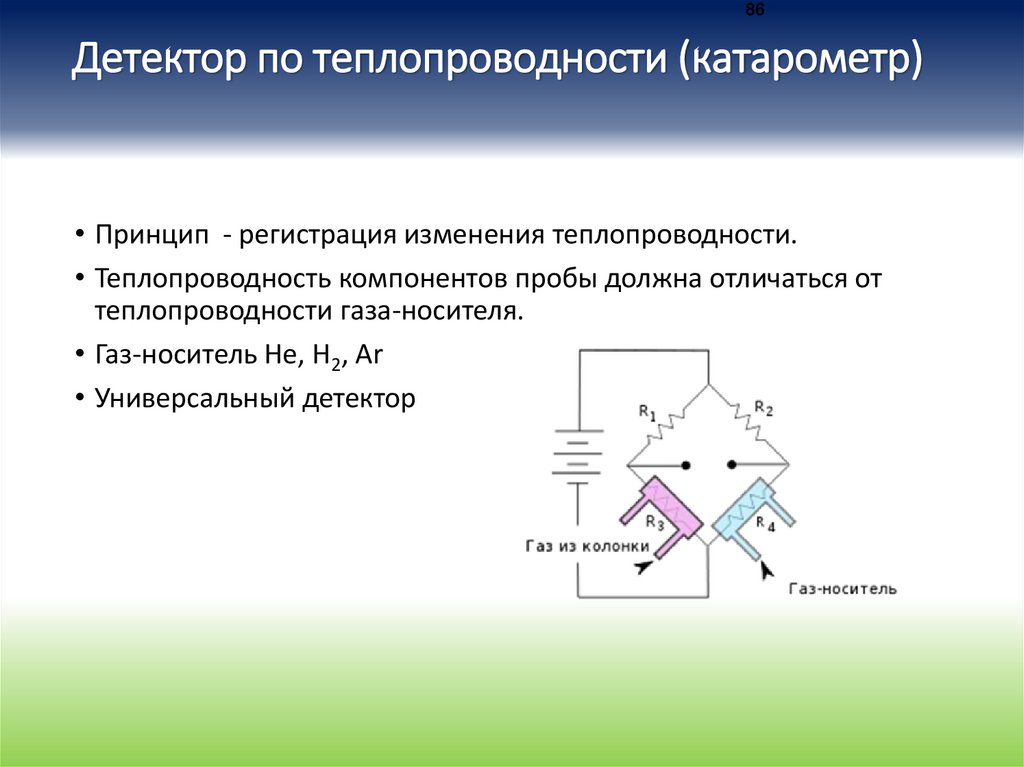
86Детектор по теплопроводности (катарометр)
• Принцип - регистрация изменения теплопроводности.
• Теплопроводность компонентов пробы должна отличаться от
теплопроводности газа-носителя.
• Газ-носитель Не, Н2, Аr
• Универсальный детектор
87.
87Катарометр
При работе с детектором по теплопроводности хроматографист задает и
контролирует следующие параметры режима работы детектора:
- природу газа-носителя;
- расход газа-носителя (концентрационный детектор, площадь обратно
пропорциональна скорости г-н);
- температуру детектора;
- ток моста детектора;
Для увеличения чувствительности следует: увеличивать силу тока моста,
уменьшать температуру блока детектора, выбирать газ носитель с
наивысшей теплопроводностью
88.
88Пламенно-ионизационный детектор (ПИД)
• Сигнал детектора – увеличение силы тока вследствие ионизации.
Рекомбинация отсутствует.
• Ионизация г-н практически отсутствует, фоновый ток мал.
• Источник ионизации – водородное пламя.
• СН + О = СНО+
СНО+ + Н2О = Н3О+ + СО
• Широкий линейный диапазон
• Мин. детектируемые концентрации ~ 5х10-6%
• Зависимость чувствительности от расходов газов
89.
89ПИД
При работе с детектором пламенно-ионизационным хроматографист
задает и контролирует следующие параметры режима работы детектора:
- природу газа-носителя;
- расход поддувочных газов обеспечивающих работу детектора;
- температуру детектора;
90.
90Детектор электронного захвата
• Сигнал детектора – уменьшение силы тока вследствие уменьшения
количества заряженных частиц.
• Газ-носитель:N2, Ar, He и др. электронодонорные газы
• Схема детектирования
N2 = N2+ + eM + e- = MM- + N2+ = M + N2
• Малый диапазон зависимости от концентрации.
Селективность к электронодефицитным соединениям
91.
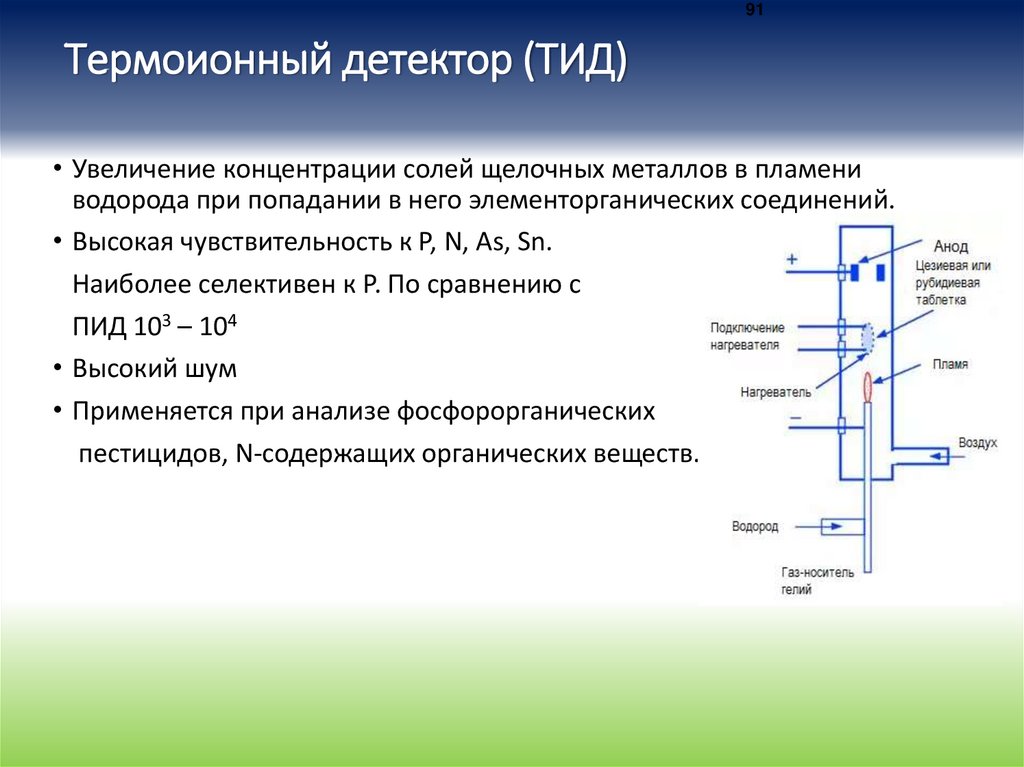
91Термоионный детектор (ТИД)
• Увеличение концентрации солей щелочных металлов в пламени
водорода при попадании в него элементорганических соединений.
• Высокая чувствительность к Р, N, As, Sn.
Наиболее селективен к Р. По сравнению с
ПИД 103 – 104
• Высокий шум
• Применяется при анализе фосфорорганических
пестицидов, N-содержащих органических веществ.
92.
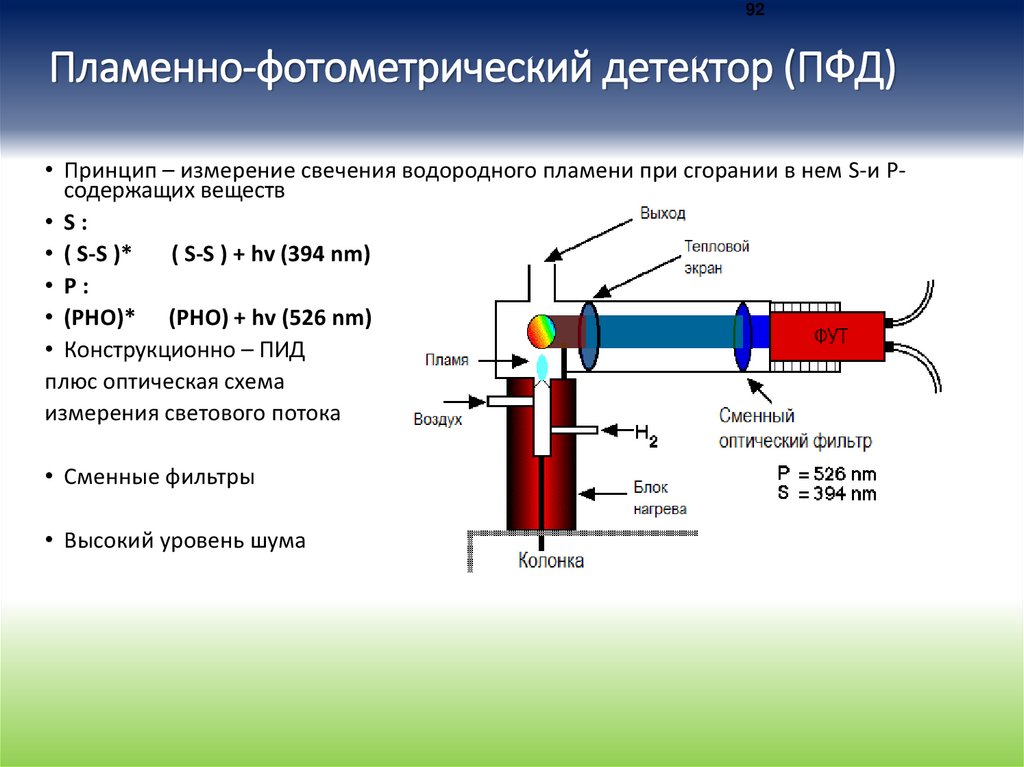
92Пламенно-фотометрический детектор (ПФД)
• Принцип – измерение свечения водородного пламени при сгорании в нем S-и Рсодержащих веществ
• S:
• ( S-S )*
( S-S ) + hv (394 nm)
• P:
• (PHO)* (PHO) + hv (526 nm)
• Конструкционно – ПИД
плюс оптическая схема
измерения светового потока
• Сменные фильтры
• Высокий уровень шума
93.
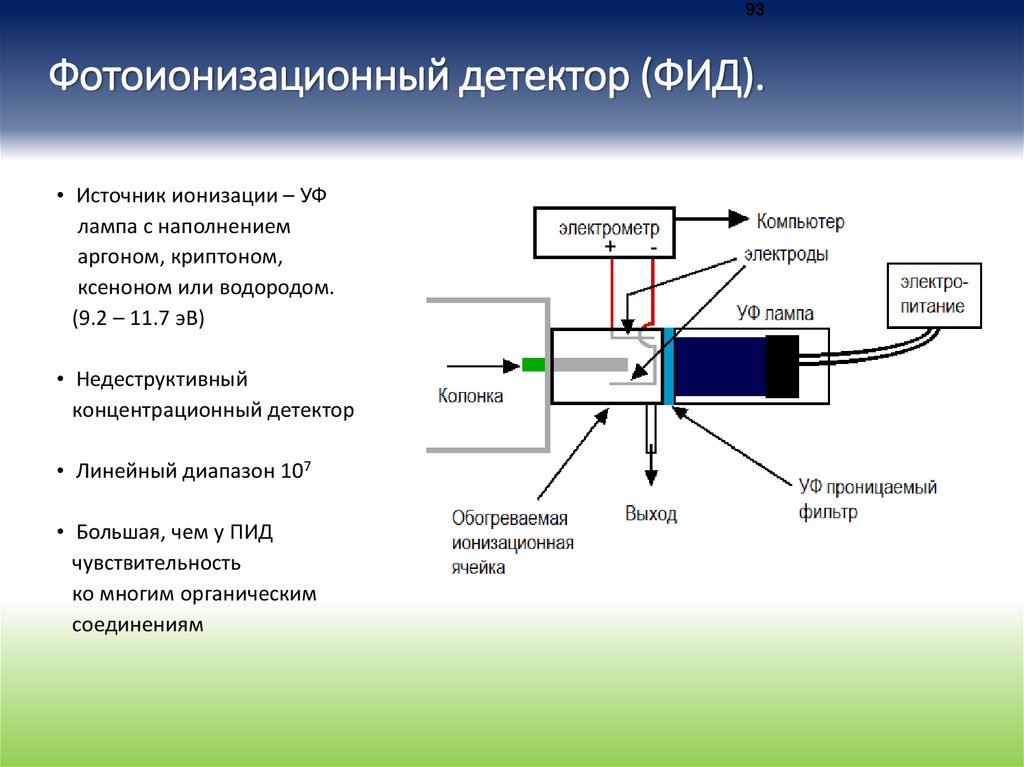
93Фотоионизационный детектор (ФИД).
• Источник ионизации – УФ
лампа с наполнением
аргоном, криптоном,
ксеноном или водородом.
(9.2 – 11.7 эВ)
• Недеструктивный
концентрационный детектор
• Линейный диапазон 107
• Большая, чем у ПИД
чувствительность
ко многим органическим
соединениям
94.
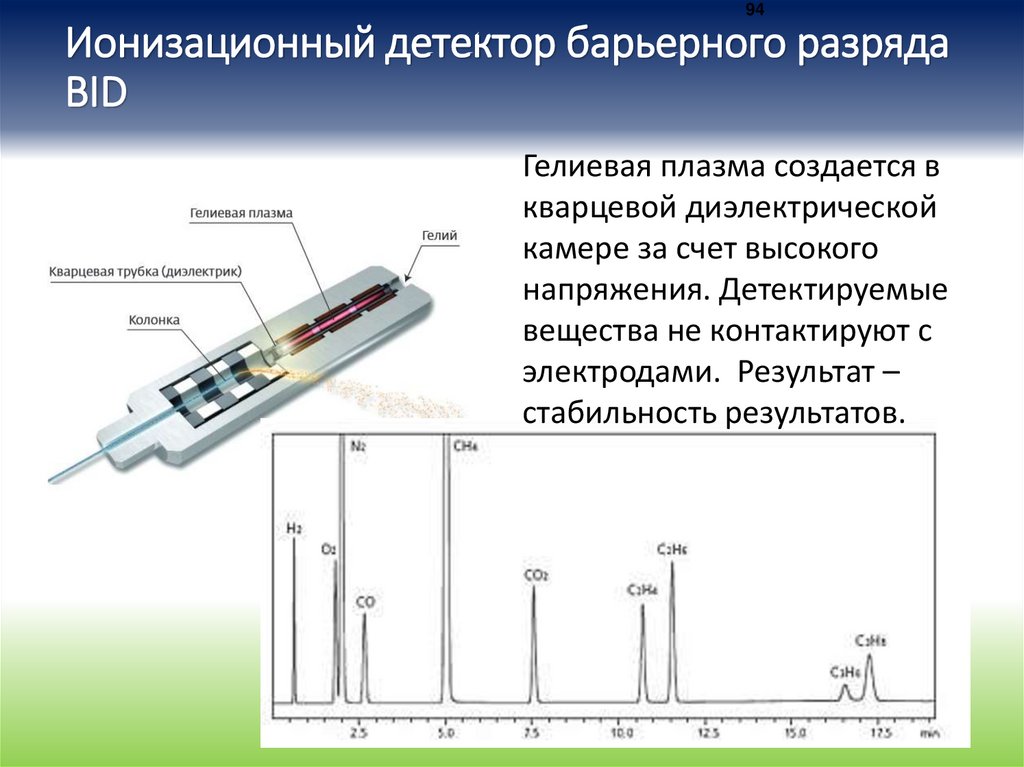
94Ионизационный детектор барьерного разряда
BID
Гелиевая плазма создается в
кварцевой диэлектрической
камере за счет высокого
напряжения. Детектируемые
вещества не контактируют с
электродами. Результат –
стабильность результатов.
95.
95Гелиевый детектор
• Вторичная ионизация
А →А+ + е
А + е → А* (метастабильное состояние)
Потенциал ионизации М < Энергия А*
А* + М → А + М+ + е
Увеличение числа зарядов, увеличение тока
Газы-носители с высоким П.и.
Аргоновый и гелиевый детектор
Высокая чистота газов, узкий линейный диапазон
96.
96Параметры, связанные с детектированием
• Детектор не должен быть инерционным и не должен
искажать форму пика. Малые постоянные времени
• Необходимость работы в линейной области
• Минимизация шумов и дрейфа базовой линии
97.
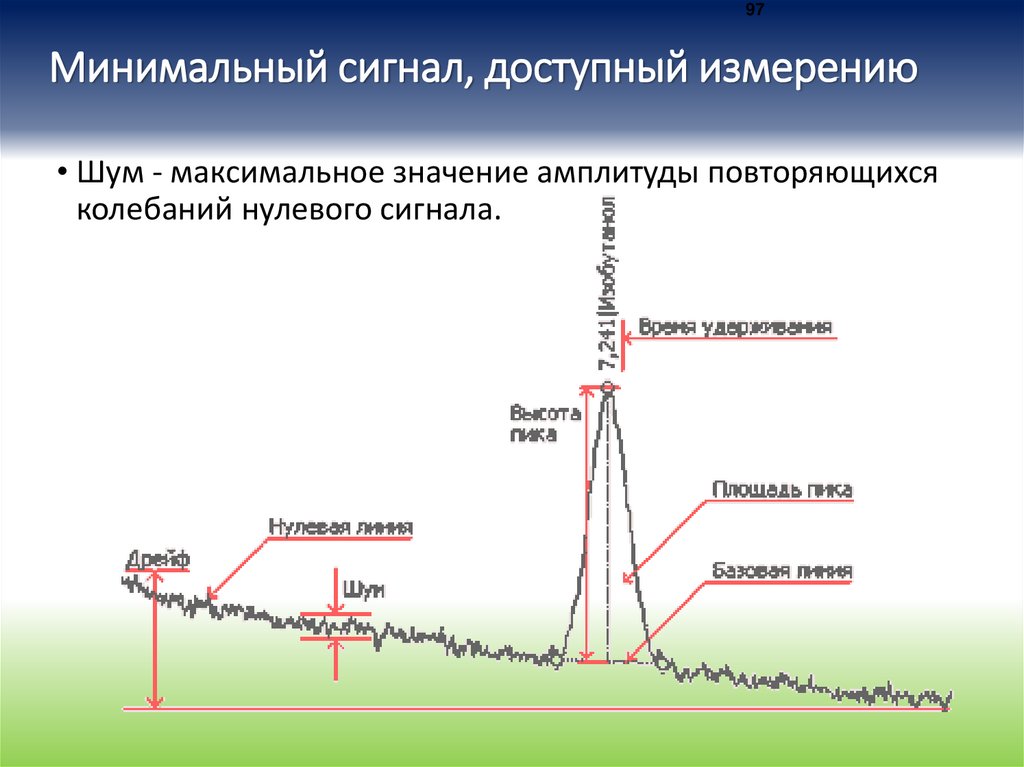
97Минимальный сигнал, доступный измерению
• Шум - максимальное значение амплитуды повторяющихся
колебаний нулевого сигнала.
98.
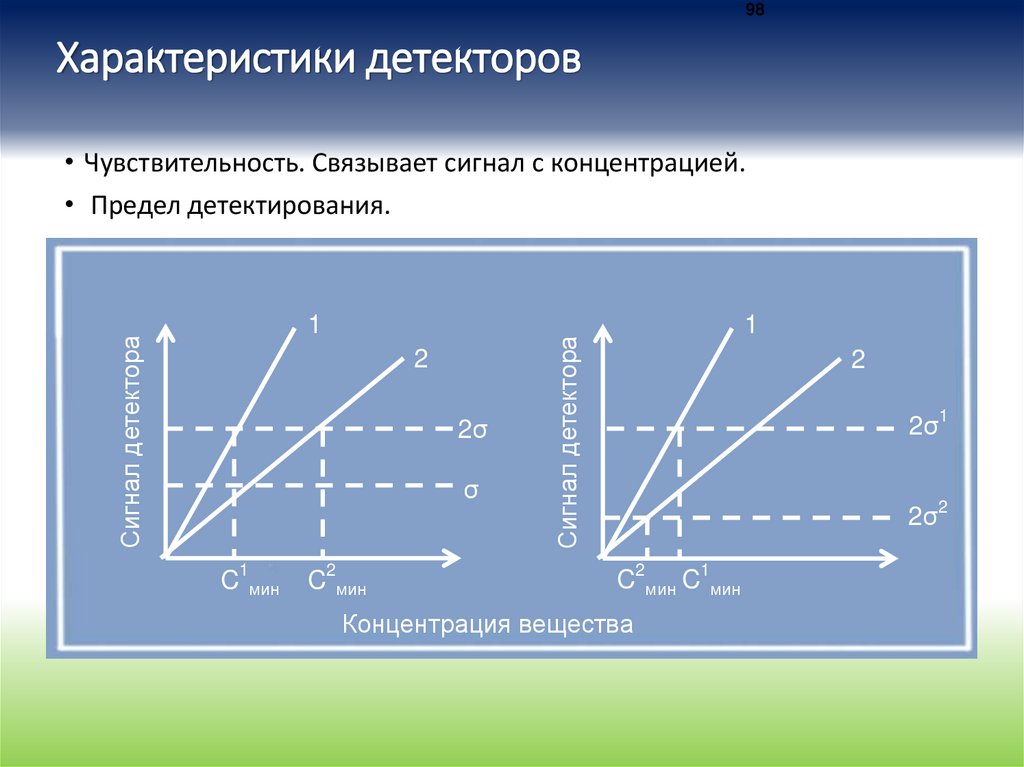
98Характеристики детекторов
• Чувствительность. Связывает сигнал с концентрацией.
• Предел детектирования.
2
2σ
σ
C1мин
C2мин
1
Сигнал детектора
Сигнал детектора
1
2
2σ1
2σ2
C2мин C1мин
Концентрация вещества
99.
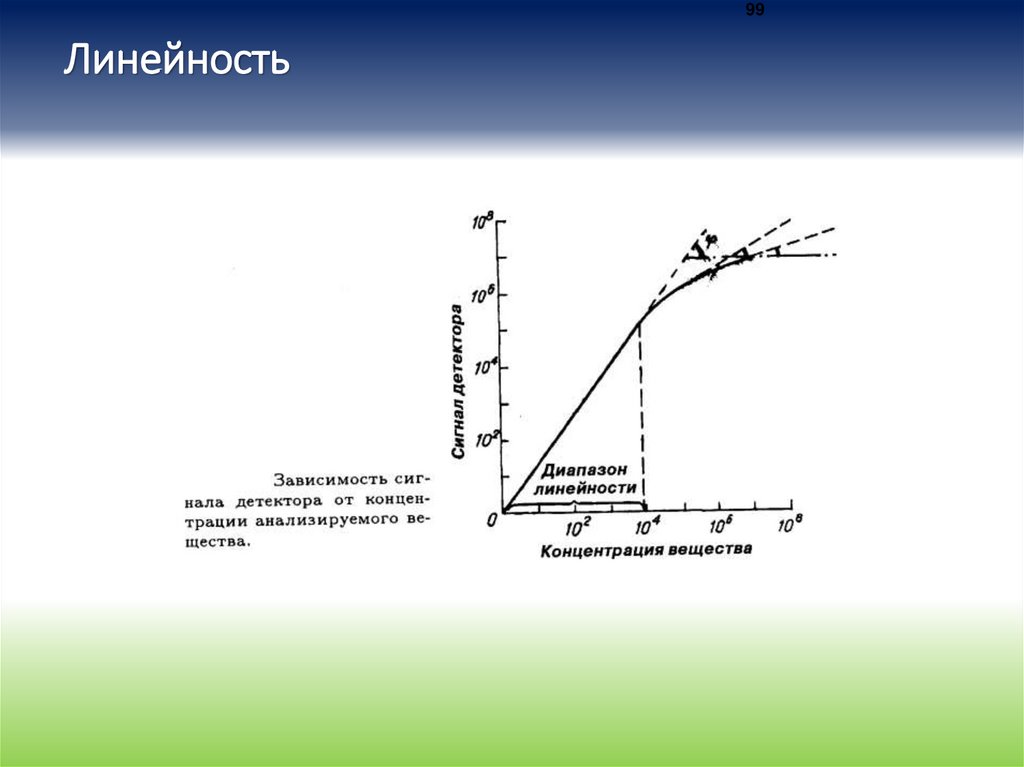
99Линейность
100.
Термостаты колонок10
0
• Поддержание оптимального температурного режима
• Возможность программирования температуры
• Возможность охлаждения до отрицательных температур
101.
101
Термостат колонок
Температура
Температура
• Изотермический анализ
• Анализ с программированием температуры
Изотермический: 150°C
Программируемый T: 50°C- 250°C at 8°C/min
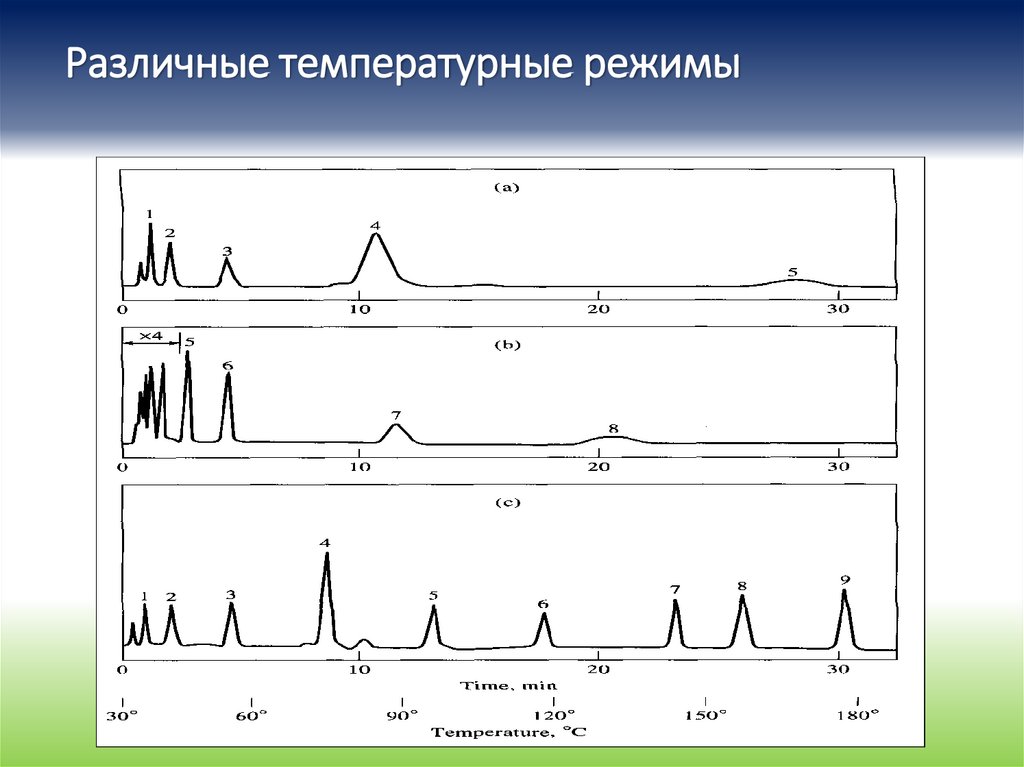
102.
Различные температурные режимы103.
103
Системы регистрации сигнала детектора
• Самописцы
• Интеграторы
• Программное обеспечение
104.
Что необходимо для быстройхроматографии?
10
4
• ГХ должна обеспечивать воспроизводимый контроль
высоких скоростей потока и высоких давлений с
возможностью программирования температуры..
• Узкие капиллярные колонки требуют малых времен
инжекции, т.о. автодозатор должен обеспечивать
быструю инжекцию.
• Система обработки данных должна обеспечивать
быструю обработку сигнала детектора в условиях
регистрации узких пиков и быстрого разделения..
• МС должен иметь высокую скорость сканирования и
высокую чувствительность.
105.
105
Проблемы, возникающие при использовании
узких капиллярных колонок.
• Ограничения количества вводимого образца из-за малой
емкости колонок.
• Увеличение давления в колонке при уменьшении радиуса.
(0.32 mm V= 30 cm/c
P= 7.7 psi
0.10 mm
P= 79.2 psi)
• Необходимость регистрировать узкие пики.
106.
Высокоскоростная хроматографияВысокое давление
Скорость газа-носителя
Быстрый нагрев
Быстрое охлаждение
Быстрый отклик детектора
970 KРa
1200 мл/мин
70°C/мин
от 450 до 50°C за 3.4 мин
4 мсек, 250Гц
107.
Типы задач качественного анализа1. Отнесение пиков на хроматограмме смеси, состав которой
известен.
2. Групповая классификация веществ в смеси. (использование
детекторов различных принципов действия, привлечение
приемов реакционной хроматографии)
3. Идентификация пиков неизвестных смесей с
использованием гибридных методов. (ИК, ХМС)
108.
Методы идентификации• сравнение экспериментально установленных
значений параметров удерживания разделяемых
соединений с приведенными в литературе
значениями этих параметров для известных
веществ;
• получение для гомологических групп веществ
корреляционных зависимостей типа параметр
удерживания – физико-химические характеристики
вещества;
• идентификация по эталонным веществам;
• использование селективных детекторов;
• реакционная хроматография.
109.
Основные методы количественного анализа• Метод абсолютной градуировки
• Метод внутренней нормализации
• Метод внутреннего стандарта.
110.
Метод абсолютной градуировки• Устанавливается зависимость между концентрацией (массой) и
площадью (высотой) пика
• На линейном участке hi = fi(ci)
fi – градуировочный множитель
• Необходимость точность и воспроизводимость дозирования пробы
(краны-дозаторы, микрошприцы, автоматические дозаторы)
111.
Метод внутренней нормализации• Отнесение измеренного количественного параметра пика к суммарному
сигналу детектора на все компонеты
• Сi (%) = (Pi/ ΣPj ) 100
• fi = (Ci/Pi)/(Cst/Pst)
• Нет необходимости точного дозирования пробы, соблюдения условий
хроматографирования.
• Необходимо регистрировать все пики. Для определения fi надо знать
качественный состав
112.
Метод внутреннего стандарта• Прибавление к известному количеству образца известного количества не
содержащегося в нем эталона, хроматографирование полученной смеси
• Сi = (Pifiqst /Pstqсм) 100 Pi площадь интересующего
в-ва
Pst – площадь стандарта
fi – фактор отклика i-го в-ва
относит. стандарта
qst q см –количества в-ва и стандарта
113.
Требования к стандартуСтандарт должен быть полностью растворен в
анализируемой смеси
Близость физико-химических свойств вещества и
стандарта
Содержание вещества и стандарта по массам
должны быть примерно одинаково и площади пиков
должны быть близки
Время элюирования должно быть как можно ближе
времени элюирования вещества
Стандарт должен заведомо отсутствовать в пробе
114.
Преимущества и недостатки методавнутреннего стандарта
• Преимущества – нет необходимости дозирования строго заданных
количеств пробы и соблюдения постоянства всех параметров
хроматографирования
• Недостатки – процедуры взятия навесок, перемешивания явл.
источником погрешностей, трудности при выборе стандарта,
наличие «окна» на хроматограмме
115.
Метод внутреннего стандарта. Когдацелесообразно применять?
• Многокомпонентные смеси. В случае метода внешнего стандарта
надо всегда иметь набор многих стандартов. Удобнее один раз
точно определить факторы отклика в дальнейшем иметь только
один стандарт.
• Случаи сложной пробоподготовки. Возможность контроля потерь.
• Разновидность метода - метод стандартной добавки
116.
Источники погрешностей в количественноманализе
• Отбор пробы, проба должна быть максимально представительной
• Устранение потерь при дозировании. Качество шприца, опыт
оператора, деструкция пробы
• Выход за границы линейного диапазона
• Ошибки при обработке хроматограмм
• Полнота разделения пиков
117.
Отбор пробыАнализ загрязнителей в объектах окружающей среды.
Доставка аналитического оборудования к месту
анализа
Отбор проб в контейнеры и доставка в лабораторию
Концентрирование при отборе проб
118.
Пробоподготовка• Жидкость-жидкостная экстракция (ЖЖЭ)
• Жидкостная экстракция твердых матриц
• Статическая и динамическая парофазная экстракция
• Паровая дистилляция
• Твердофазная микроэкстракция, ТФМЭ
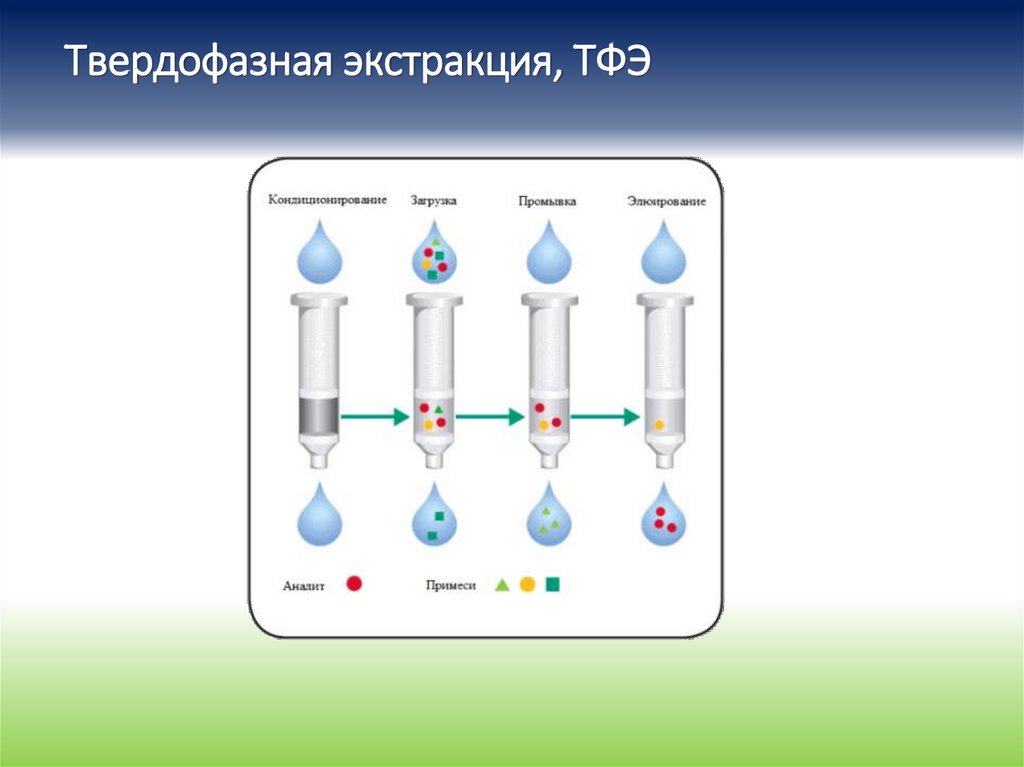
• Твердофазная экстракция (ТФЭ)
119.
Жидко-жидкостная экстракцияПреимущества ЖЖЭ:
• Простота метода
• Универсальность метода:
• Для больших объемов образца высокая скорость проведения
экстракции
Недостатки ЖЖЭ:
• Возможно достаточно трудоемкой, а иногда и достаточно
длительной и ресурсоемкой процедурой
• Образованием эмульсии на границе между слоями
• Не позволяет добиться полного извлечения целевых
соединений
120.
Жидкостная экстракция твердых матриц• Экстракция в аппарате Сокслета
• Ультразвуковая экстракция
• Микроволновая экстракция
• Жидкостная экстракция под давлением
121.
Статическая и динамическая парофазнаяэкстракция
• Статическая парофазная экстракция (Headspace)
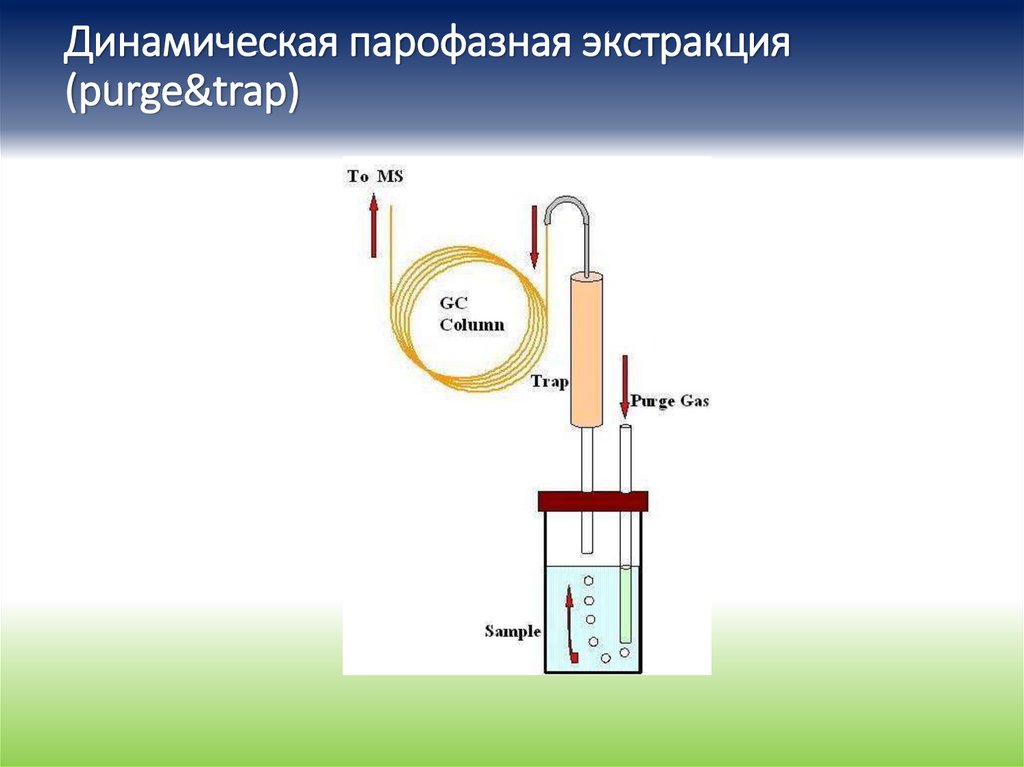
• Динамическая парофазная экстракция (purge&trap)
122.
Статическая парофазная экстракция(Headspace)
Статический ПФА
После уравновешивания
Герметизация
GC
Загрузка образца
Нагрев
123.
Динамическая парофазная экстракция(purge&trap)
124.
Твердофазная микроэкстракция, ТФМЭ125.
Различные жидкие фазы на волокнах ТФМЭ• Карбоксен/полидиметилсилоксан – газы с малой молекулярной
массой
• Полидиметилсилоксан – легколетучие соединения
• Полидиметилсилоксан/дивинилбензол – амины,
нитроароматика
• Полиакрилат – полярные соединения
• Карбовакс – спирты, эфиры
126.
Твердофазная экстракция, ТФЭ127.
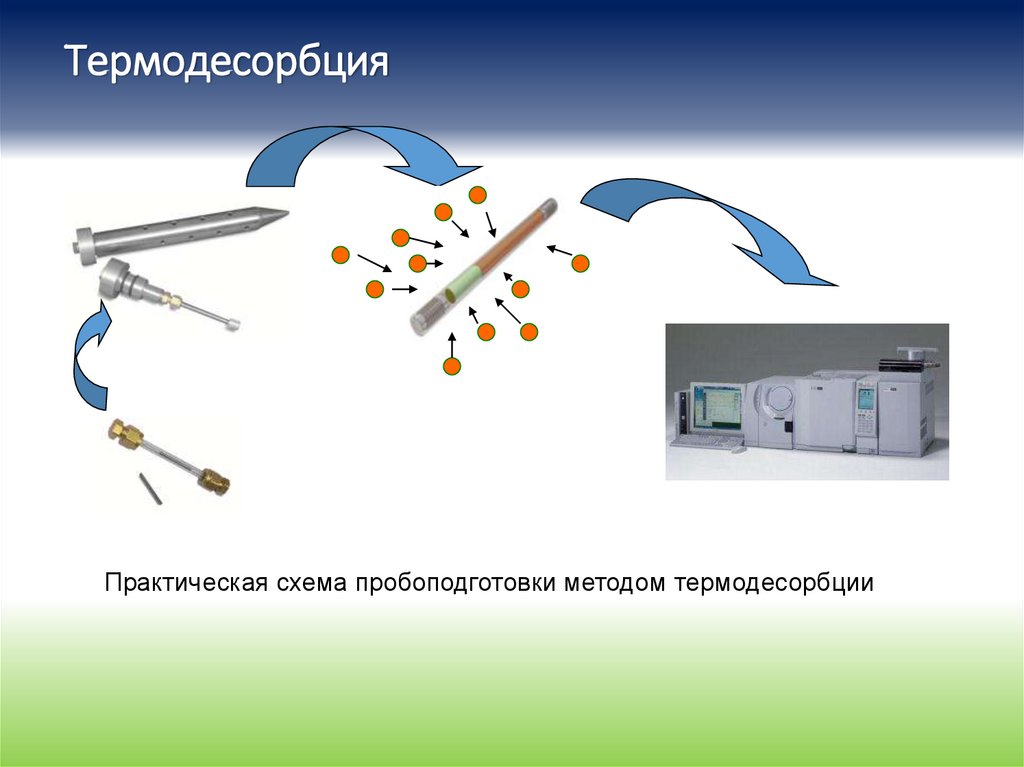
ТермодесорбцияПрактическая схема пробоподготовки методом термодесорбции
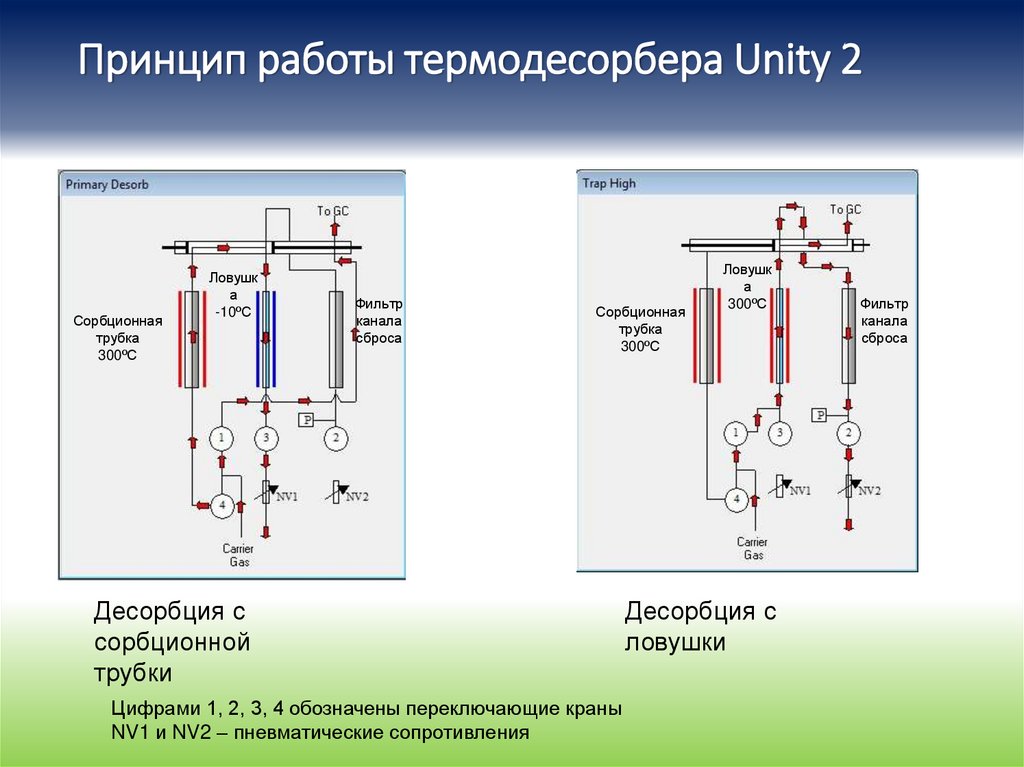
128.
Принцип работы термодесорбера Unity 2Сорбционная
трубка
300ºС
Ловушк
а
-10ºС
Фильтр
канала
сброса
Сорбционная
трубка
300ºС
Десорбция с
сорбционной
трубки
Цифрами 1, 2, 3, 4 обозначены переключающие краны
NV1 и NV2 – пневматические сопротивления
Ловушк
а
300ºС
Десорбция с
ловушки
Фильтр
канала
сброса
129.
Десорбция и экстракция: преимущества инедостатки
Термодесорбция:
• + легкость автоматизации, возможность многократного использования
трубок-концентраторов, минимальное дополнительное разбавление
образца
• - возможность термического разложения, необходимость использования
сложного оборудования, возможность потерь летучих соединений
Экстракция растворителем:
• + простота инструментального исполнения, применимость для
извлечения ВМС, удобно для термолабильных соединений
• - разбавление растворителем и поэтому потеря чувствительности,
необходимость отделения растворителя от веществ на хроматограмме,
проблема чистых растворителей
130.
Сорбционное концентрирование• Требования к сорбенту: улавливание из большого объема без
проскока.
• Гидрофобность
• Инертность по отношению к сорбату в процессе отбора пробы,
хранения и десорбции.
Термодесорбция, смыв растворителем.
Силикагели, углеродные сорбенты, полимерные
сорбенты(Порапаки, Хромосорбы серии 100, Тенакс, Hayesep)
Комбинирование сорбентов
Углеродный сорбент (легкие соединения) → полимерный сорбент


























































































 Физика
Физика