Похожие презентации:
Хроматографические методы анализа
1.
Хроматографические методы анализа• Хроматография
–
метод разделения и
определения смесей веществ, основанный на
различном
распределении
(различной
сорбируемости) веществ, проходящих с током
подвижной фазы через неподвижную. И
многократном перераспределении между двумя
контактирующими фазами.
2.
Хроматографические методы анализа3.
Хроматографические методы анализа4.
Хроматографические методы анализа• Хроматограмма – графическое или иное
представление сигнала детектора от
времени или объема подвижной фазы
5.
6.
7.
Хроматографические методыанализа
Дифференциальная
хроматограмма:
1 — нулевая линия; 2 —
пик несорбирующегося
компонента; 3» 4 — пики
определяемых компонентов
tR (VR)– время удерживания (
объем ) –время от момента ввода
пробы вещества в поток
подвижной фазы до момента
выхода из колонки зоны вещества
с максимальной концентрацией
VR = tR·ύ
ύ – объемная скорость подвижной
Базовая линия – сигнал от подвижной фазы
Пик – часть хроматограммы, регистрирующая отклик детектора
фазы
Основание пика – продолжение базовой линии, соединяющее начало и коне пика
Площадь пика – площадь хроматограммы, заключенная между кривой, описывающей пик, и
его основанием
Высота пика – расстояние от максимума пика до его основания, измеренное параллельно
оси отклика детектора
Время удерживания – время, необходимое для элюирования вещества. Соответствует
времени появления максимума пика на хроматограмме.
8.
Хроматографические методы анализаВремя (объем)
удерживания tR (VR)
хроматографируемого
вещества складывается
из времени (объема)
пребывания вещества в
подвижной фазе tо (Vо)
и времени(объема)
пребывания вещества в
неподвижной фазе t R (V R),
tR =tо + t R,
VR =Vо + V R
Время t R( объем ) V R называют приведенным временем
( объемом ) удерживания
9.
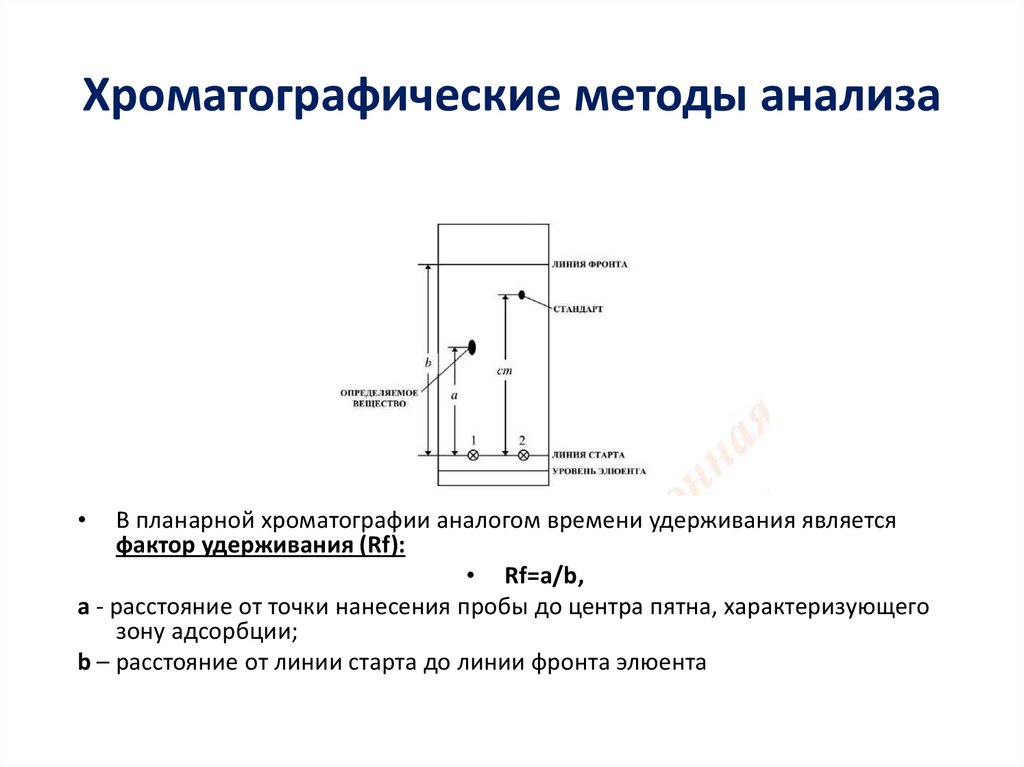
Хроматографические методы анализаВ планарной хроматографии аналогом времени удерживания является
фактор удерживания (Rf):
• Rf=a/b,
a - расстояние от точки нанесения пробы до центра пятна, характеризующего
зону адсорбции;
b – расстояние от линии старта до линии фронта элюента
10.
11.
12.
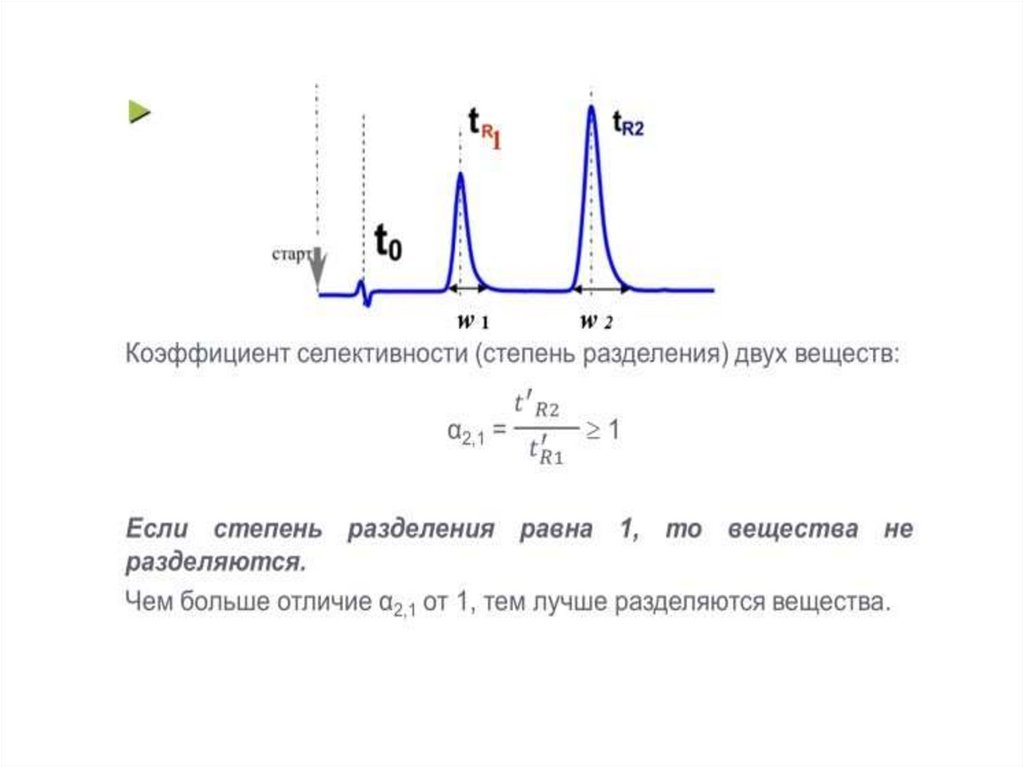
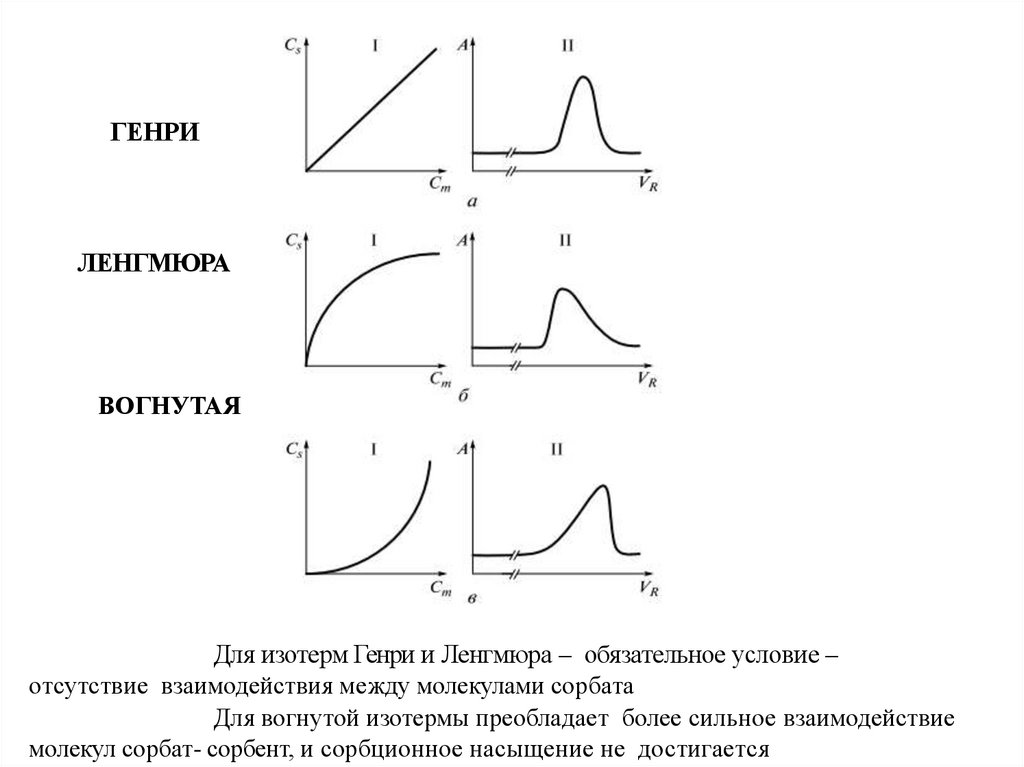
ГЕНРИЛЕНГМЮРА
ВОГНУТАЯ
Для изотерм Генри и Ленгмюра – обязательное условие –
отсутствие взаимодействия между молекулами сорбата
Для вогнутой изотермы преобладает более сильное взаимодействие
молекул сорбат- сорбент, и сорбционное насыщение не достигается
13.
14.
15.
Допущения и недостатки16.
17.
Пути улучшения эффективностьразделения
1.Уменьшение диаметра частиц неподвижной
фазы d;
2.Улучшение набивки колонки;
3.Увеличение длины колонки;
4.Повысить температуру ( снижается вязкость)
5.Изменить диаметр колонки. С увеличением
диаметра усиливается размывание
18.
Расчет содержания определяемыхвеществ
• 1.
Метод
нормирования
(метод
внутренней нормализации). Основан на
предположении, что на хроматограмме
зарегистрированы все вещества, входящие
в состав анализируемой смеси, и что доля
площади каждого пика от суммы площадей
всех пиков соответствует содержанию
вещества в массовых процентах.
19.
Методы определениясодержания веществ
20.
Расчет содержания определяемыхвеществ
• 2.
Метод
внешнего
стандарта.
Концентрацию
испытуемого
вещества
определяют путем сравнения сигнала
(пика), полученного на хроматограммах
испытуемого
раствора,
сигнала,
полученного на хроматограммах раствора
стандартного образца.
21.
Расчет содержания определяемыхвеществ
3. Метод внутреннего стандарта. Основан на введении в анализируемую
смесь определенного количества стандартного вещества (внутренний
стандарт). В испытуемый и стандартные растворы вводят известные
количества внутреннего стандарта, хроматографируют растворы и
определяют отношения площадей пиков определяемого вещества к
площади пика внутреннего стандарта в испытуемом и стандартном
растворах.
22.
Расчет содержания определяемыхвеществ
• 4. Метод стандартных добавок. Основан на введении в
анализируемую
смесь
известного
количества
определяемого вещества и сравнении сигналов,
полученных для испытуемого раствора со стандартной
добавкой и без добавки определяемого вещества.
23.
Любой сорбционный процесс характеризуется константойраспределения, которая представляет собой отношение равновесной
концентрации вещества в одной определенной форме в неподвижной
фазе (c1) и концентрации вещества в той же форме в подвижной фазе
(с2):
Краспр. = c1/ с2
В хроматографии определяемое вещество может присутство вать не
только в одной форме. В этом случае применяют коэф фициент
распределения КD, отражающий равновесное распределение
вещества А:
КD = cАнеп./сАпод.,
cАнеп , сАпод - общая аналитическая концентрация (или количество)
всех форм вещества А соответственно в неподвижной и
подвижной фазах.
24.
Газовая хроматография25.
Газо-жидкостная хроматография (ГЖХ)https://spectroscopy-lab.ru/catalog/gazovayakhromatografiya/gazovyy-khromatograf-agilent-7890b/
Это хроматография, в которой подвижная фаза
находится в состоянии газа или пара, называясь газноситель. Неподвижной фазой (НЖФ) является в
основном высокомолекулярная жидкость,
закрепленная на пористый носитель или на стенки
длинной капиллярной трубки.
Применение
летучие, термостабильные соединения либо летучие
производные веществ.
Углеводороды, амины, серусодержащие соединения, пестициды,
полихлорированные бензолы, эфирные масла, жирные кислоты, сложные
эфиры, алкалоиды, лекарственные препараты, галогенсодержащие
соединения, стероиды, ароматические соединения
26.
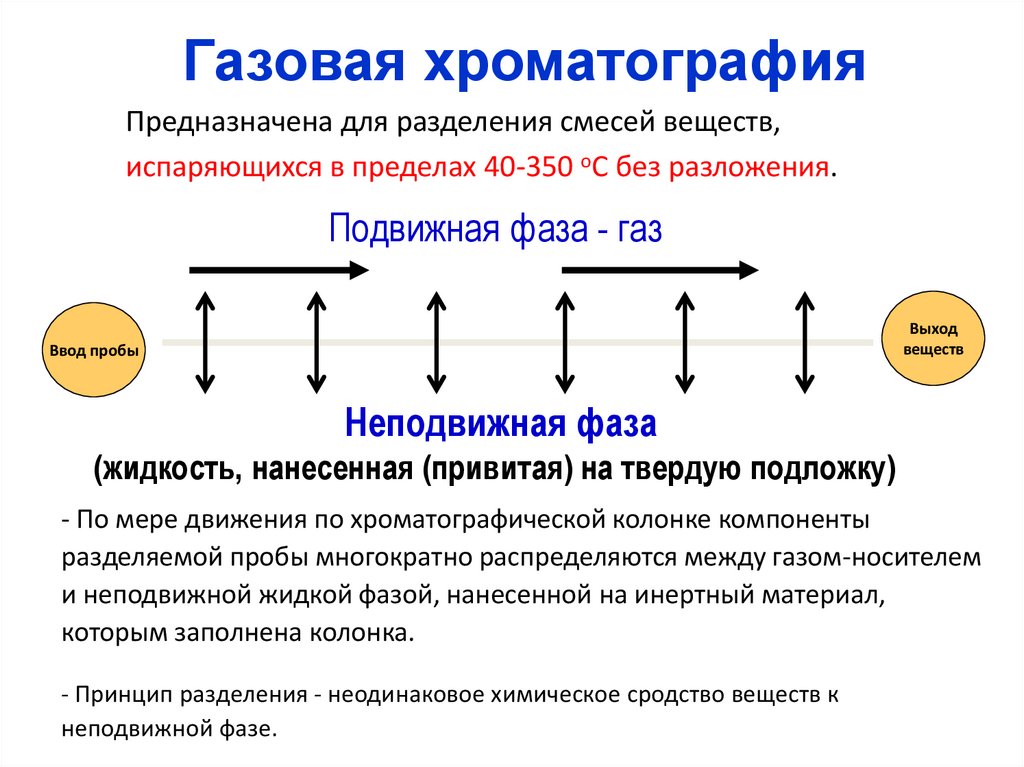
Газовая хроматографияПредназначена для разделения смесей веществ,
испаряющихся в пределах 40-350 оС без разложения.
Подвижная фаза - газ
Выход
веществ
Ввод пробы
Неподвижная фаза
(жидкость, нанесенная (привитая) на твердую подложку)
- По мере движения по хроматографической колонке компоненты
разделяемой пробы многократно распределяются между газом-носителем
и неподвижной жидкой фазой, нанесенной на инертный материал,
которым заполнена колонка.
- Принцип разделения - неодинаковое химическое сродство веществ к
неподвижной фазе.
27.
Достоинства газовой хроматографии1) возможность идентификации и количественного определения
индивидуальных компонентов сложных смесей, например нефтей;
2) высокая четкость и быстрота разделения, обусловленные низкой
вязкостью подвижной фазы - газа;
3) микропробы и автоматическая запись результатов, благодаря
высокой чувствительности и малой инерционности приборов;
4) возможность анализа широкого круга объектов — от легких газов до
высокомолекулярных органических соединений и некоторых металлов;
5) возможность изучения различных свойств веществ и физикохимических взаимодействий в газах, жидкостях и на поверхности
твердых тел.
28.
Недостатки газовой хроматографии1) Ограничение лишь парообразными пробами;
2) Вещества должны иметь точку кипения ниже 350 оС; не быть
термолабильными;
3) Нередко необходима интенсивная пробоподготовка;
4) Для идентификации пиков часто необходимы сложные методы –
масс спектрометрия;
Но!
Газовая хроматография сейчас – одна из самых
распространенных аналитических техник;
более 50 тыс. действующих в мире приборов.
29.
Фирмы, выпускающие газовые хроматографы:~ 130 производителей в мире:
Thermo Fisher Scientific, Agilent, Perkin-Elmer, Shimadzu,
Brucker, Chromtech, Dionex
5 значимых производителей в России: Хроматэк, Хромос, МетаХром,
Аналитприбор, ЦветАналитик
30.
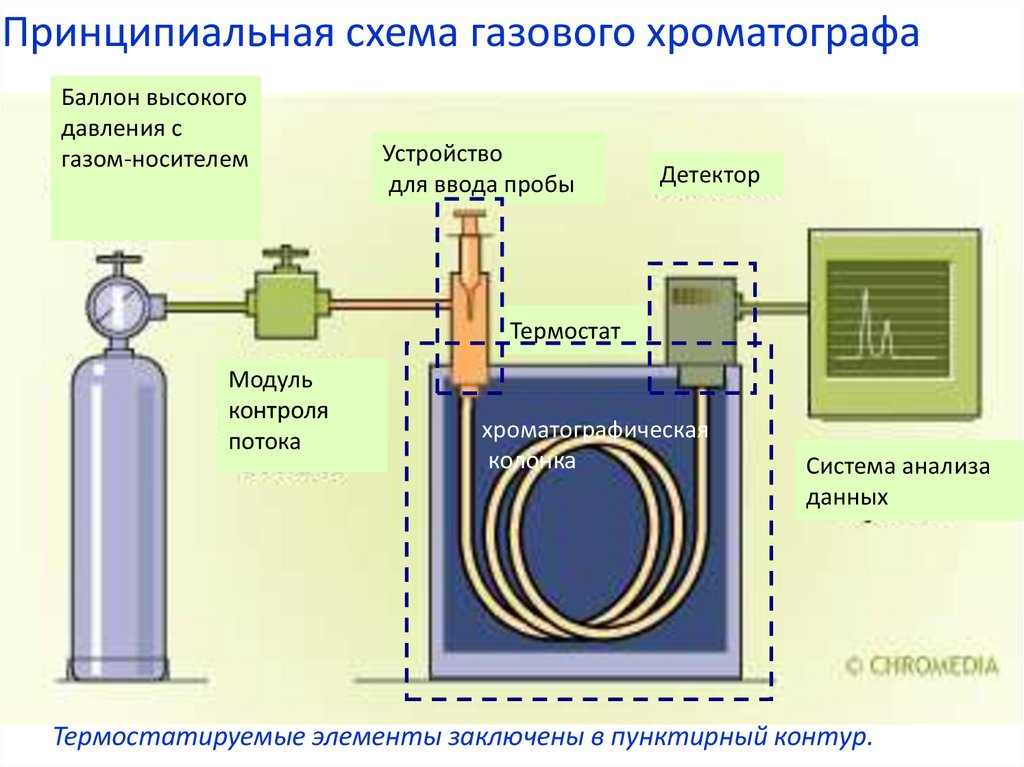
Принципиальная схема газового хроматографаБаллон высокого
давления с
газом-носителем
Устройство
для ввода пробы
Детектор
Термостат
Модуль
контроля
потока
хроматографическая
колонка
Система анализа
данных
Термостатируемые элементы заключены в пунктирный контур.
31.
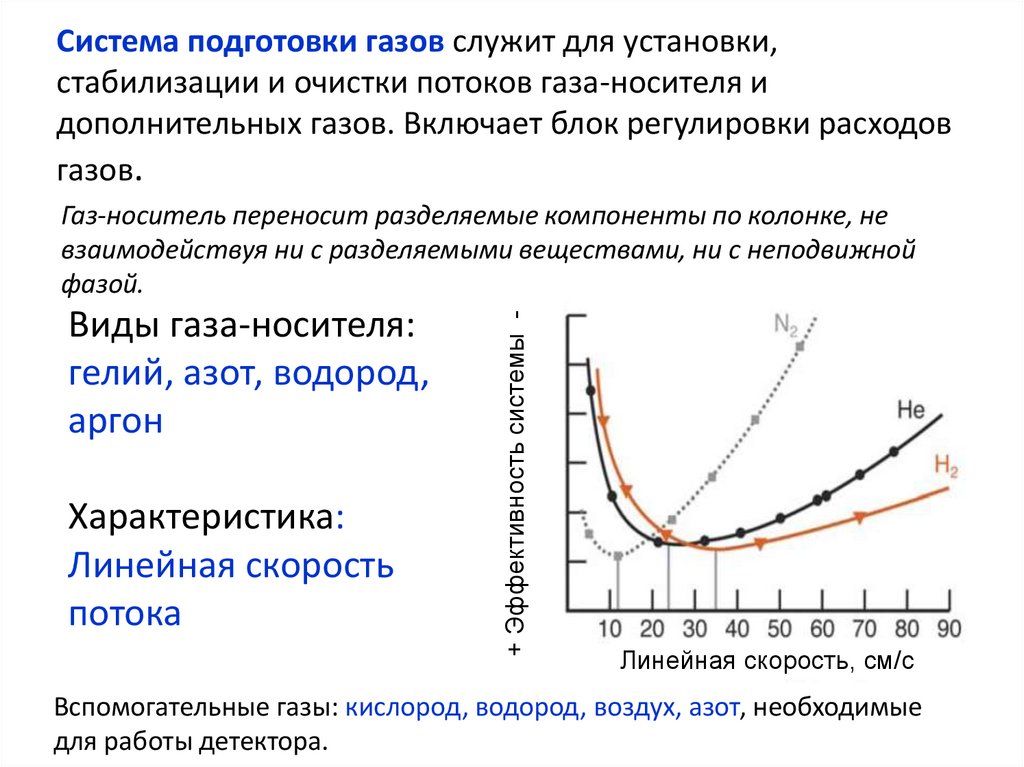
Система подготовки газов служит для установки,стабилизации и очистки потоков газа-носителя и
дополнительных газов. Включает блок регулировки расходов
газов.
Виды газа-носителя:
гелий, азот, водород,
аргон
Характеристика:
Линейная скорость
потока
+ Эффективность системы -
Газ-носитель переносит разделяемые компоненты по колонке, не
взаимодействуя ни с разделяемыми веществами, ни с неподвижной
фазой.
Линейная скорость, см/с
Вспомогательные газы: кислород, водород, воздух, азот, необходимые
для работы детектора.
32.
В России принята цветовая маркировка баллонов, содержащих различные газы.АЗОТ
Водород
ГЕЛИЙ
АРГОН
Кислород
Газовый реду́ктор — устройство для
понижения давления газа на выходе из какойлибо ёмкости (баллона или газопровода) до
рабочего.
Пропан
33.
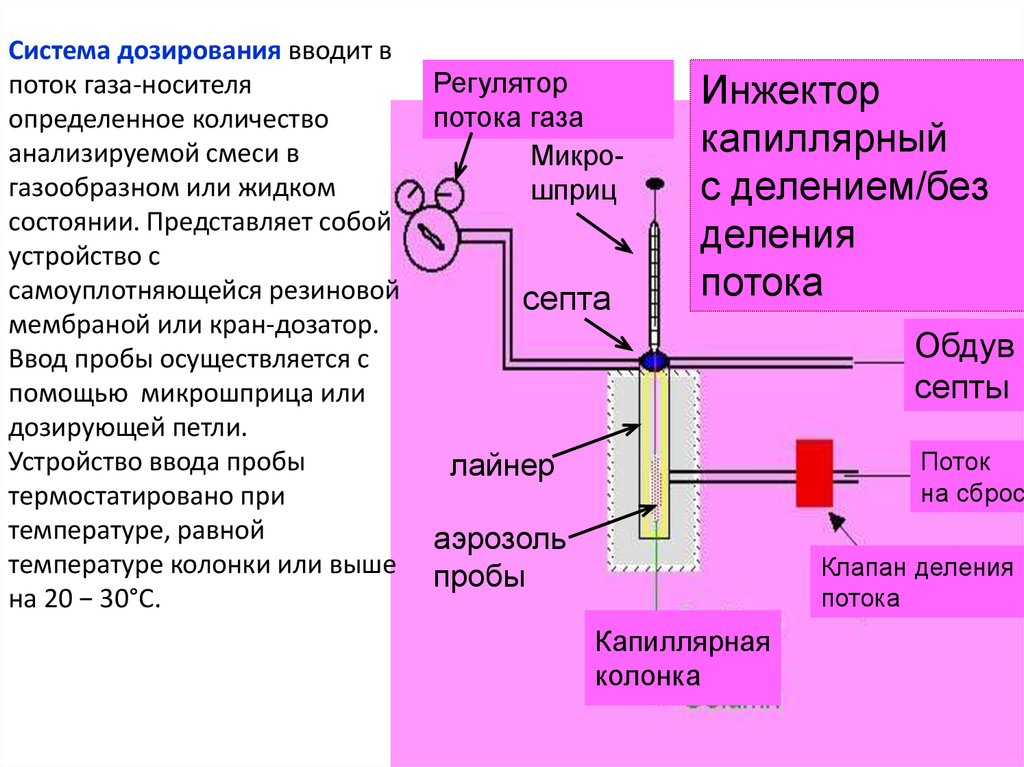
Система дозирования вводит впоток газа-носителя
определенное количество
анализируемой смеси в
газообразном или жидком
состоянии. Представляет собой
устройство с
самоуплотняющейся резиновой
мембраной или кран-дозатор.
Ввод пробы осуществляется с
помощью микрошприца или
дозирующей петли.
Устройство ввода пробы
термостатировано при
температуре, равной
температуре колонки или выше
на 20 − 30°С.
Регулятор
потока газа
Микрошприц
септа
Инжектор
капиллярный
с делением/без
деления
потока
Обдув
септы
Поток
на сброс
лайнер
аэрозоль
пробы
Клапан деления
потока
Капиллярная
колонка
34.
С потоком газа-носителя проба из инжектора переносится вколонку, которая помещена в термостат.
Параметр
Набивные
(насадочные)
Капиллярные
Длина колонки, м
1-6
10-100
Внутренний диаметр, мм
2-4
0,25-0,55
Среднее число
теоретических тарелок
5 000
150 000
Толщина пленки, мкм
1-10
0,005-0,5
Материалом для изготовления колонок служат стекло, нержавеющая сталь, медь,
иногда фторопласт. Наиболее распространены капиллярные колонки, изготовленные
из кварца с полиамидными пленками.
35.
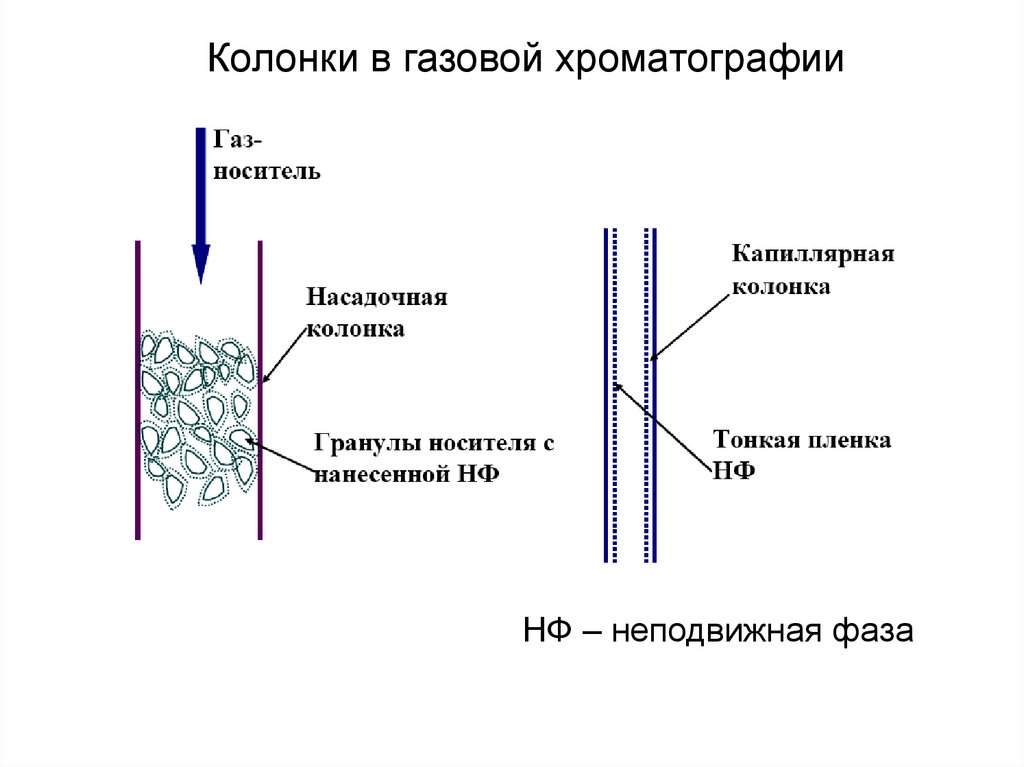
Колонки в газовой хроматографииНФ – неподвижная фаза
36.
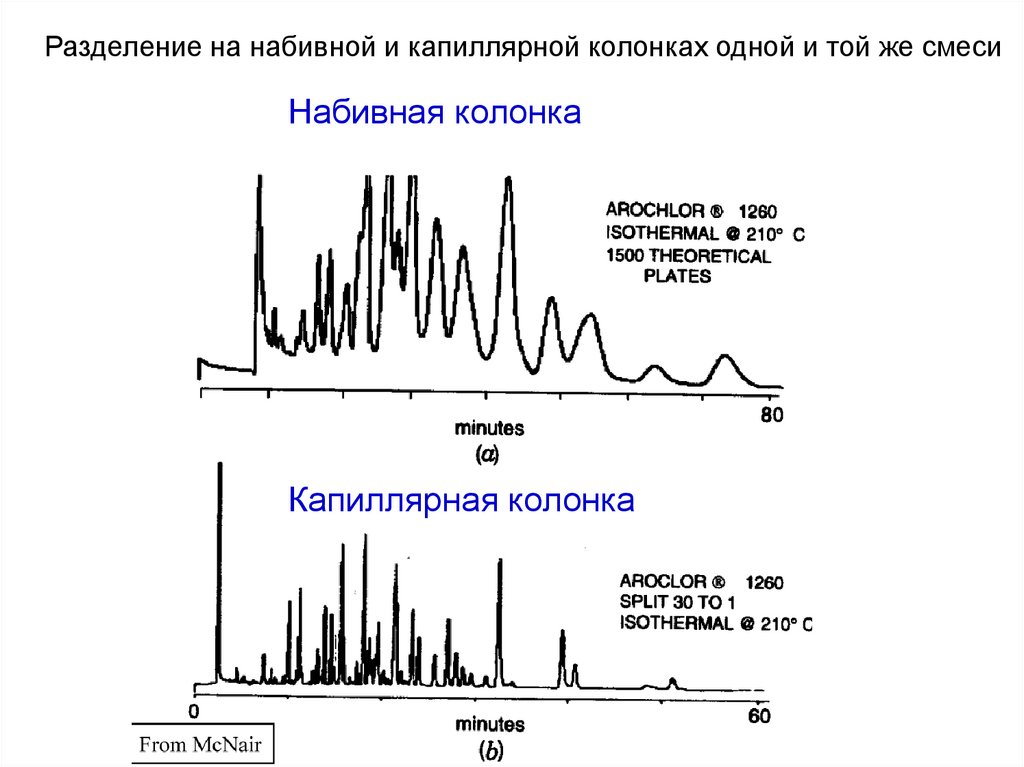
Разделение на набивной и капиллярной колонках одной и той же смесиНабивная колонка
Капиллярная колонка
37.
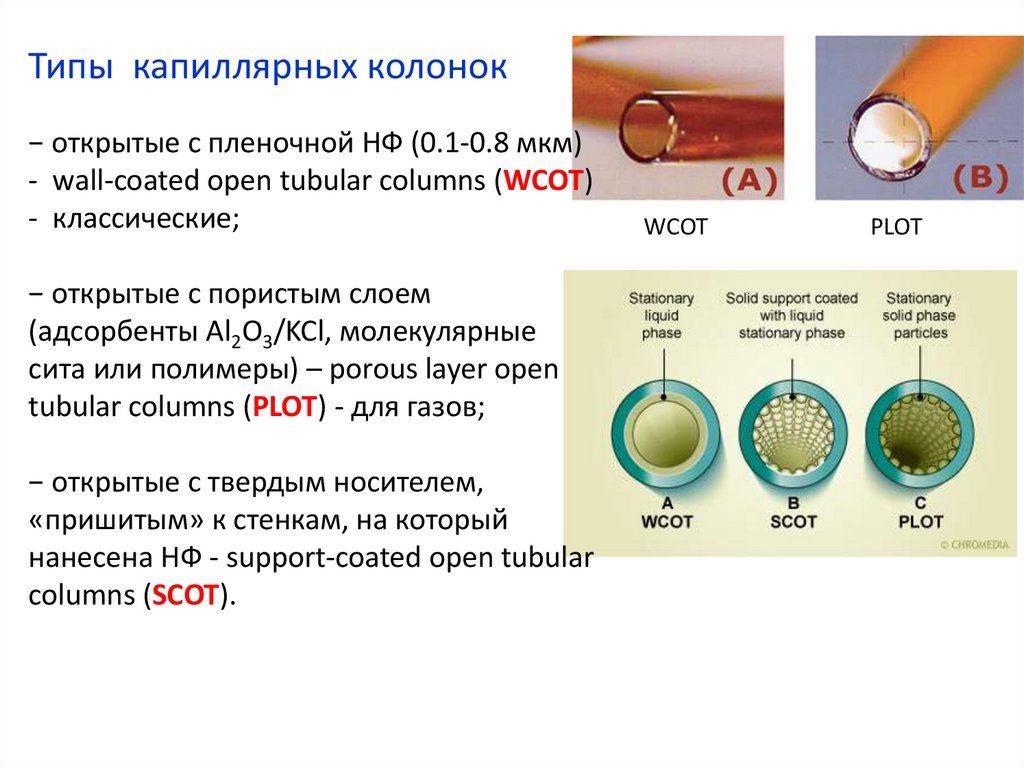
Типы капиллярных колонок− открытые с пленочной НФ (0.1-0.8 мкм)
- wall-coated open tubular columns (WCOT)
- классические;
− открытые с пористым слоем
(адсорбенты Al2O3/KCl, молекулярные
сита или полимеры) – porous layer open
tubular columns (PLOT) - для газов;
− открытые с твердым носителем,
«пришитым» к стенкам, на который
нанесена НФ - support-coated open tubular
columns (SCOT).
WCOT
PLOT
38.
Классификация неподвижных фаз по максимальнодопустимой рабочей температуре:
− органическая до 240°С
− кремнийорганическая до 360°С
Верхний предел температуры работы НФ в колонке
определяется величиной испарения;
Любая НФ при работе подвергается медленному уносу с
потоком газа-носителя.
39.
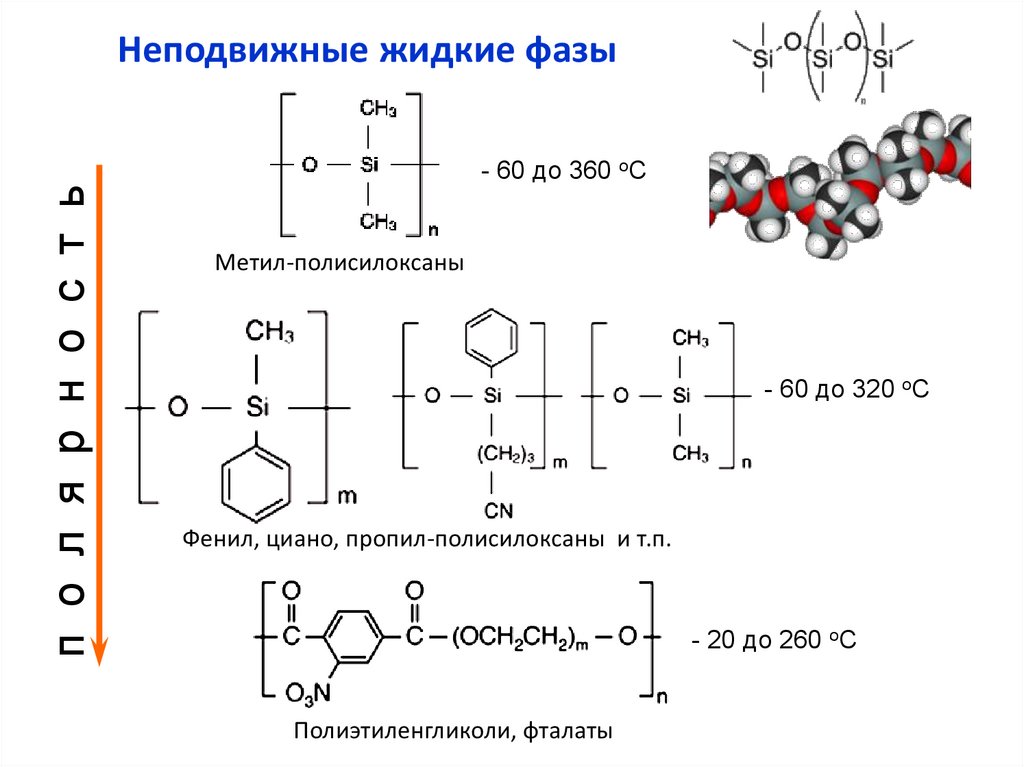
Неподвижные жидкие фазып о л я р н о с т ь
- 60 до 360 оС
Метил-полисилоксаны
- 60 до 320 оС
Фенил, циано, пропил-полисилоксаны и т.п.
- 20 до 260 оС
Полиэтиленгликоли, фталаты
40.
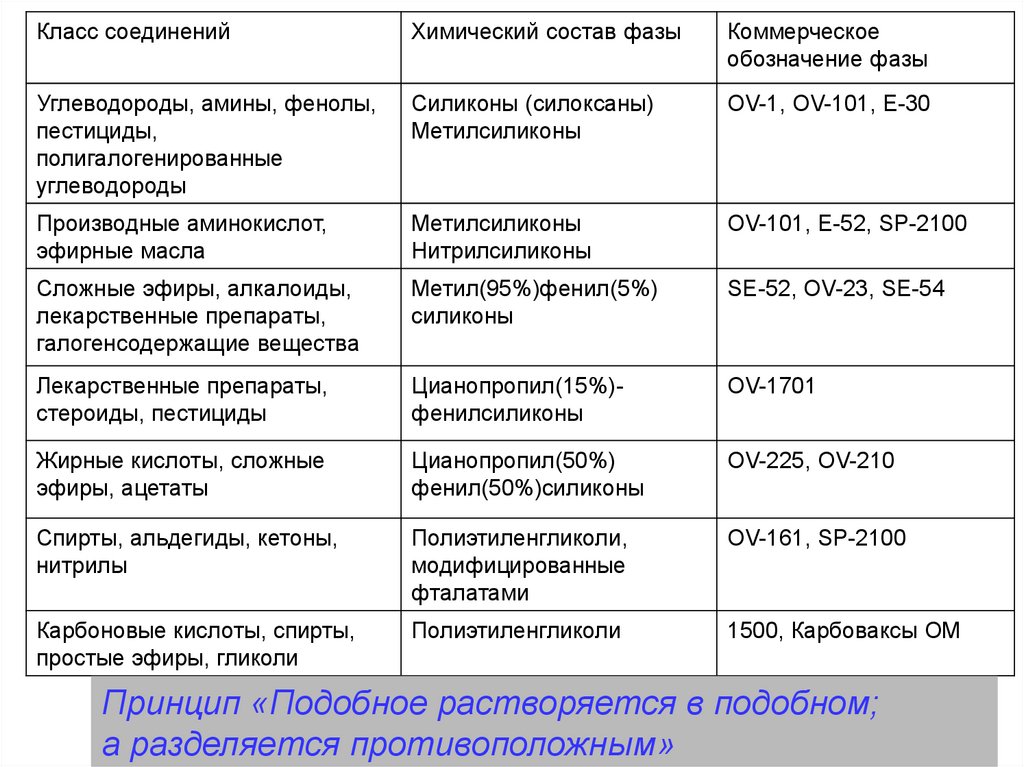
Класс соединенийХимический состав фазы
Коммерческое
обозначение фазы
Углеводороды, амины, фенолы,
пестициды,
полигалогенированные
углеводороды
Силиконы (силоксаны)
Метилсиликоны
OV-1, OV-101, Е-30
Производные аминокислот,
эфирные масла
Метилсиликоны
Нитрилсиликоны
OV-101, Е-52, SP-2100
Сложные эфиры, алкалоиды,
лекарственные препараты,
галогенсодержащие вещества
Метил(95%)фенил(5%)
силиконы
SE-52, OV-23, SE-54
Лекарственные препараты,
стероиды, пестициды
Цианопропил(15%)фенилсиликоны
OV-1701
Жирные кислоты, сложные
эфиры, ацетаты
Цианопропил(50%)
фенил(50%)силиконы
OV-225, OV-210
Спирты, альдегиды, кетоны,
нитрилы
Полиэтиленгликоли,
модифицированные
фталатами
OV-161, SP-2100
Карбоновые кислоты, спирты,
простые эфиры, гликоли
Полиэтиленгликоли
1500, Карбоваксы ОМ
Принцип «Подобное растворяется в подобном;
а разделяется противоположным»
41.
Факторы, влияющие на эффективность разделенияДиаметр колонки
малые внутренние диаметры, например 0,25 мм,
предпочтительнее
Длина колонки
длину следует увеличивать в 4 раза, чтобы получить в 2 раза
большую степень разделения
Газ-носитель
Легкие водород, гелий лучше применять для колонок с малым содержанием НЖФ,
которые работают с высокими скоростями потока для быстрых аналитических
разделений.
Тяжелые газы-носители (азот, аргон) наиболее пригодны для колонок с высоким
содержанием НЖФ, в полупрепаративном режиме.
Скорость газа-носителя
На практике линейная скорость составляет 1 - 24 см3/сек.
42.
Факторы, влияющие на эффективность разделенияТемпература
Оптимальная температура - компромисс между разделением,
которое ухудшается, и скоростью анализа, которая увеличивается
с возрастанием температуры.
t, min
смесь налканов
t, min
t, min
43.
Факторы, влияющие на эффективность разделенияРежим работы хроматографа
Программирование температуры: вещества проходят по колонке при
температуре, оптимальной для их разделения, если
соответствующим образом выбраны начальная температура и
скорость нагрева. В результате продолжительность анализа
значительно снижается, достигается хорошее разрешение, а высота
последних пиков возрастает.
44.
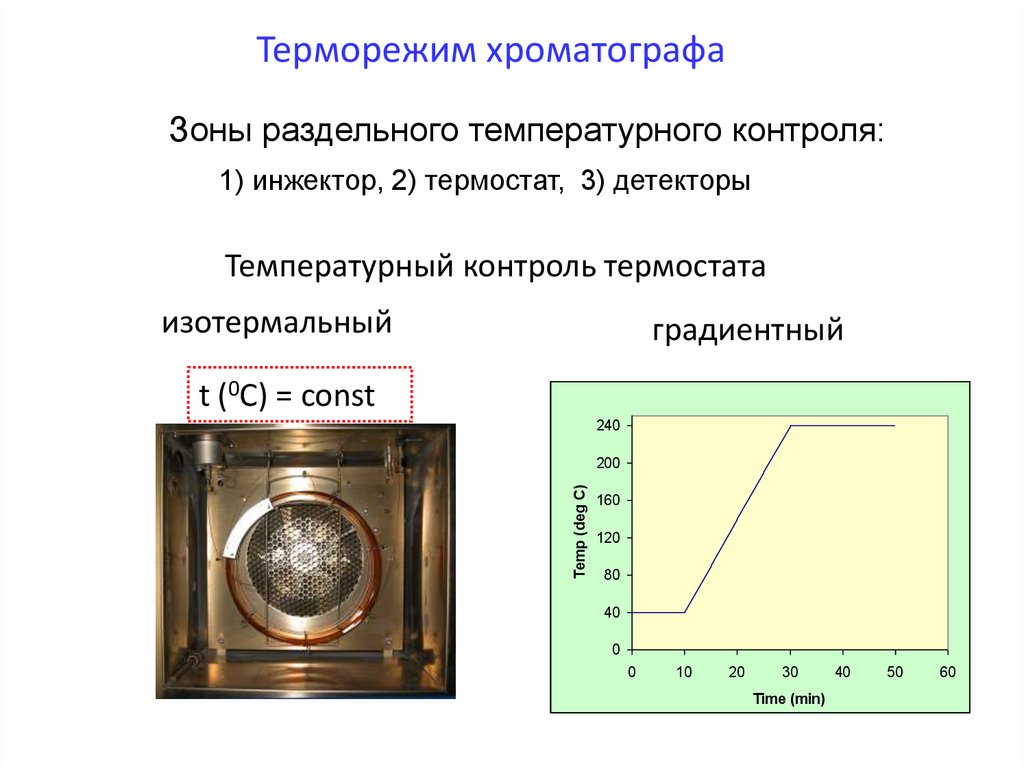
Терморежим хроматографаЗоны раздельного температурного контроля:
1) инжектор, 2) термостат, 3) детекторы
Температурный контроль термостата
изотермальный
градиентный
t (0C) = const
240
Temp (deg C)
200
160
120
80
40
0
0
10
20
30
Time (min)
40
50
60
45.
Система детектирования измеряет изменения физикохимических свойств выходящей из колонки смеси (газ-носитель+ вещество) и преобразует в электрический сигнал. Величина
сигнала зависит как от природы вещества, так и от содержания
его в анализируемой смеси.
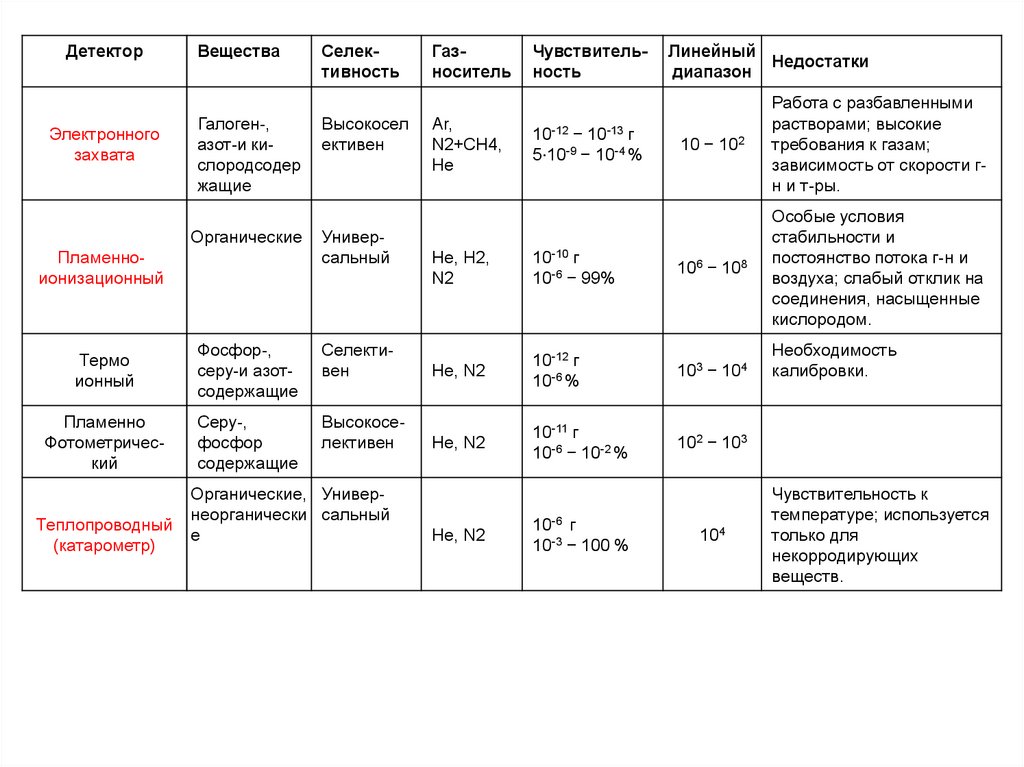
Критерии оценки детекторов:
− чувствительность, минимально детектируемая
концентрация;
− уровень шума, дрейфа нулевой линии;
− диапазон линейности;
− эффективный объем и время отклика
(быстродействие);
− селективность.
46.
ДетекторЭлектронного
захвата
Вещества
Селективность
Газноситель
Галоген-,
азот-и кислородсодер
жащие
Высокосел
ективен
Ar,
N2+CH4,
He
Органические
Универсальный
Пламенноионизационный
Чувствительность
10-12 − 10-13 г
5⋅10-9 − 10-4 %
Особые условия
стабильности и
постоянство потока г-н и
воздуха; слабый отклик на
соединения, насыщенные
кислородом.
10-10 г
10-6 − 99%
106 − 108
103 − 104
102 − 103
Фосфор-,
серу-и азотсодержащие
Селективен
Не, N2
10-12 г
10-6 %
Пламенно
Фотометрический
Серу-,
фосфор
содержащие
Высокоселективен
Не, N2
10-11 г
10-6 − 10-2 %
Теплопроводный
(катарометр)
10 − 102
Работа с разбавленными
растворами; высокие
требования к газам;
зависимость от скорости гн и т-ры.
Не, Н2,
N2
Термо
ионный
Органические, Универнеорганически сальный
е
Линейный
Недостатки
диапазон
Не, N2
10-6 г
10-3 − 100 %
104
Необходимость
калибровки.
Чувствительность к
температуре; используется
только для
некорродирующих
веществ.
47.
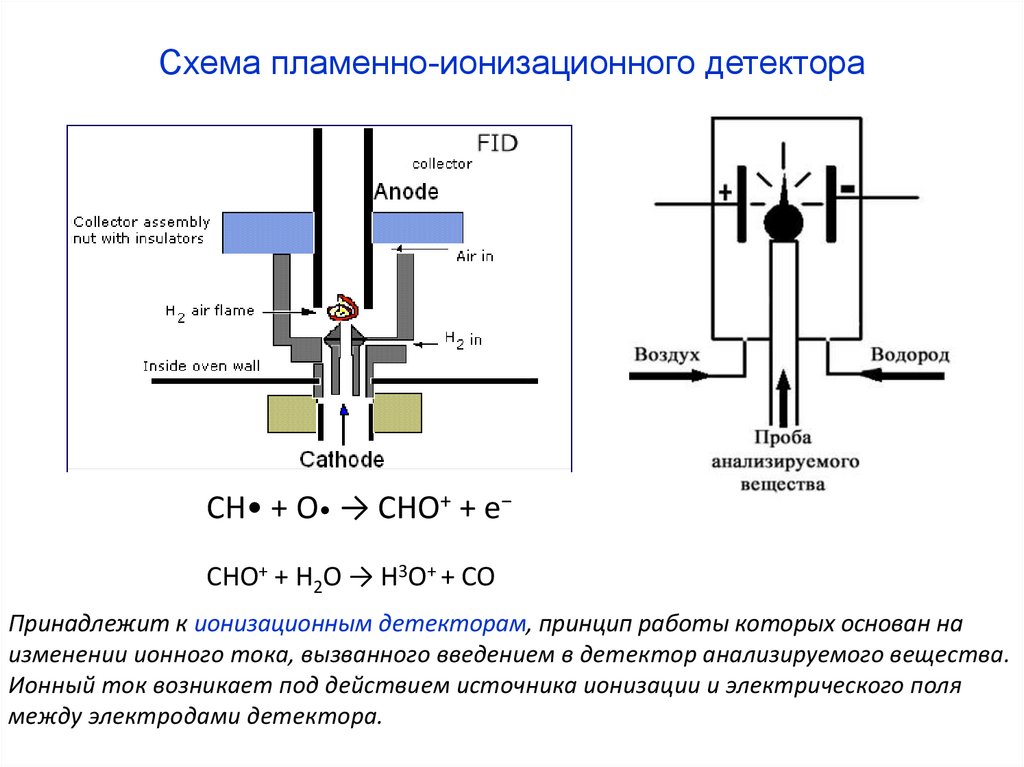
Схема пламенно-ионизационного детектораCH• + O• → CHO+ + e−
CHO+ + H2O → H3O+ + CO
Принадлежит к ионизационным детекторам, принцип работы которых основан на
изменении ионного тока, вызванного введением в детектор анализируемого вещества.
Ионный ток возникает под действием источника ионизации и электрического поля
между электродами детектора.
48.
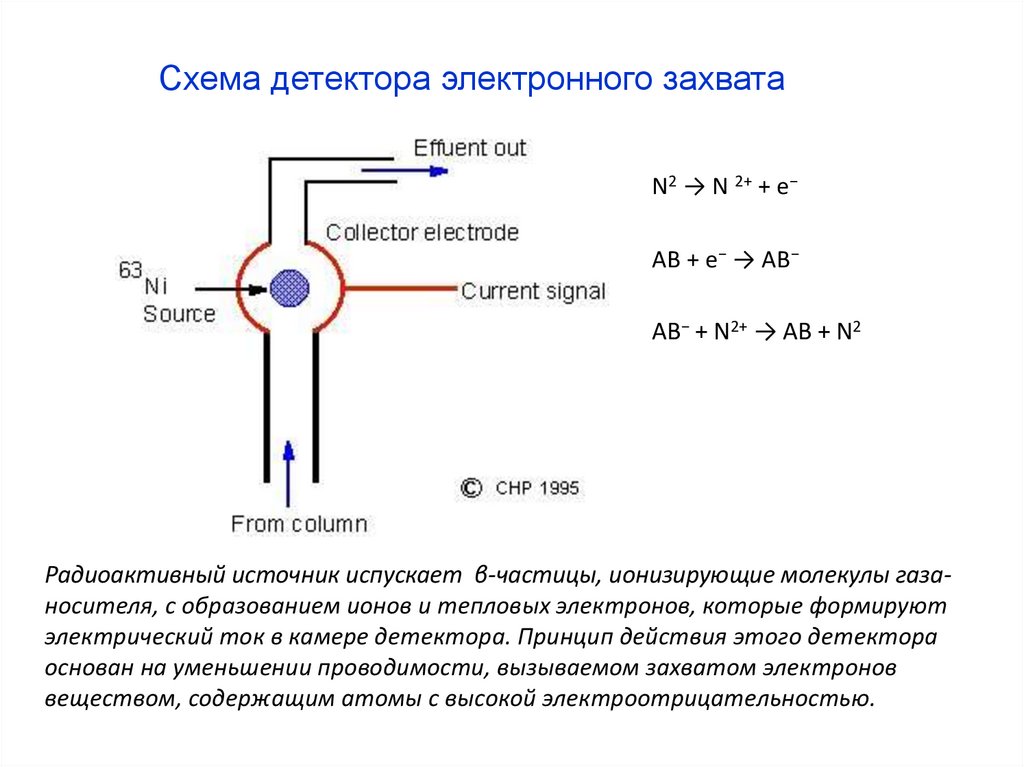
Схема детектора электронного захватаN2 → N 2+ + e−
АВ + e− → АВ−
АВ− + N2+ → АВ + N2
Радиоактивный источник испускает β-частицы, ионизирующие молекулы газаносителя, с образованием ионов и тепловых электронов, которые формируют
электрический ток в камере детектора. Принцип действия этого детектора
основан на уменьшении проводимости, вызываемом захватом электронов
веществом, содержащим атомы с высокой электроотрицательностью.
49.
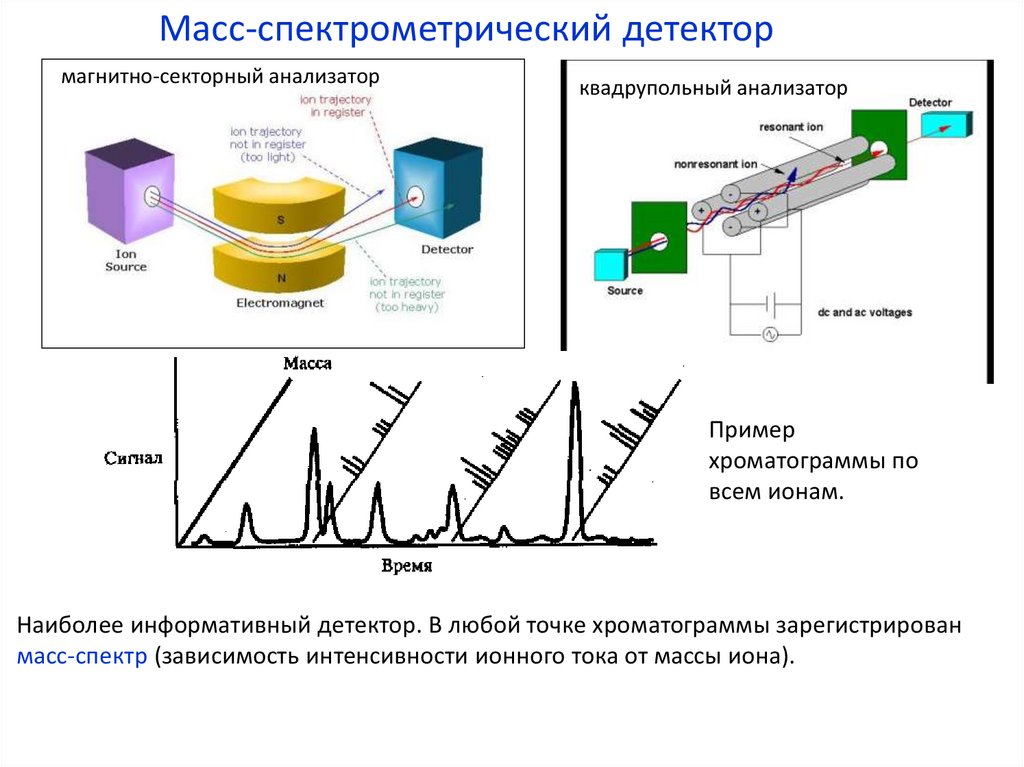
Масс-спектрометрический детектормагнитно-секторный анализатор
квадрупольный анализатор
Пример
хроматограммы по
всем ионам.
Наиболее информативный детектор. В любой точке хроматограммы зарегистрирован
масс-спектр (зависимость интенсивности ионного тока от массы иона).
50.
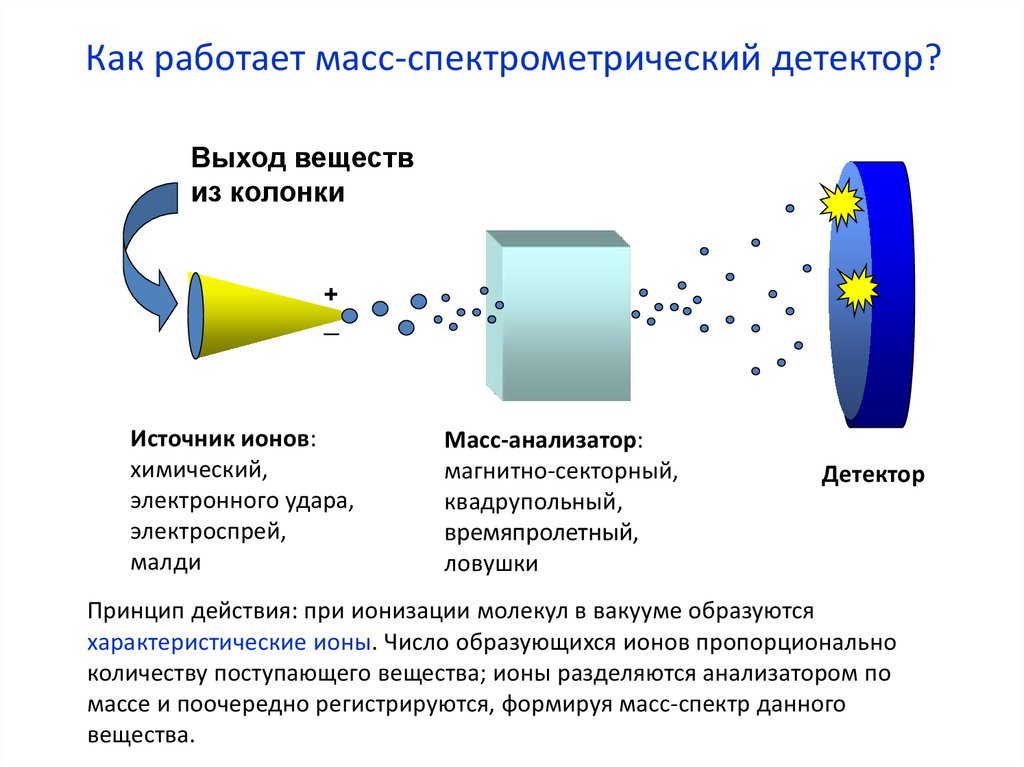
Как работает масс-спектрометрический детектор?Выход веществ
из колонки
+
_
Источник ионов:
химический,
электронного удара,
электроспрей,
малди
Масс-анализатор:
магнитно-секторный,
квадрупольный,
времяпролетный,
ловушки
Детектор
Принцип действия: при ионизации молекул в вакууме образуются
характеристические ионы. Число образующихся ионов пропорционально
количеству поступающего вещества; ионы разделяются анализатором по
массе и поочередно регистрируются, формируя масс-спектр данного
вещества.
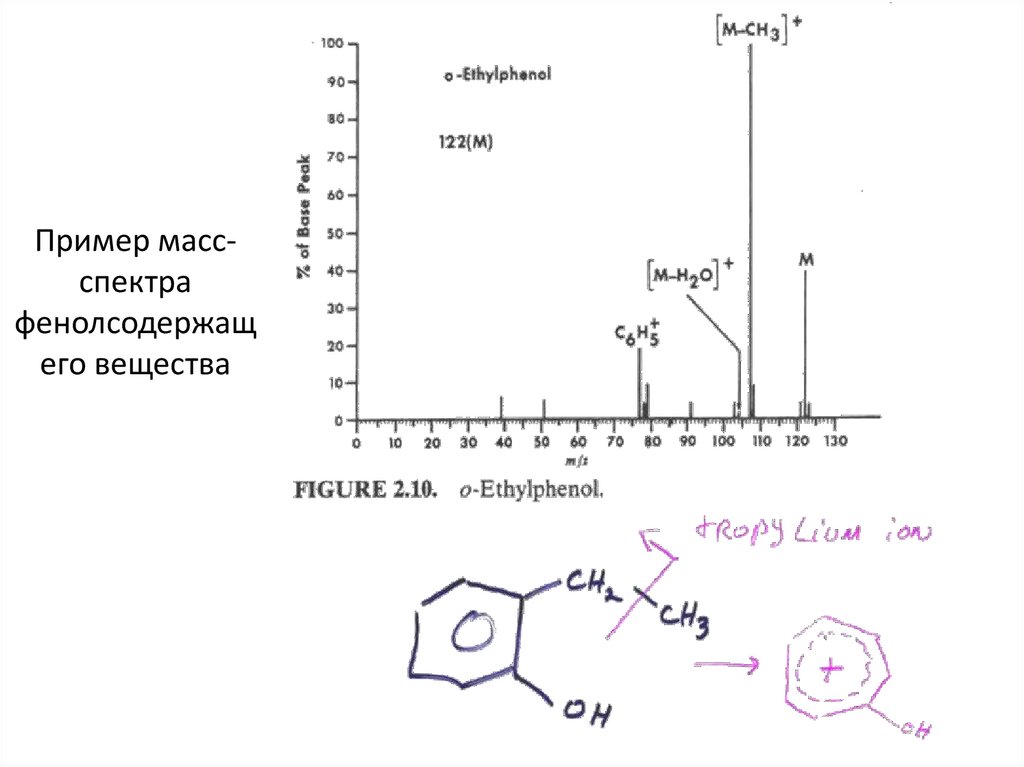
51.
Пример массспектрафенолсодержащ
его вещества
52.
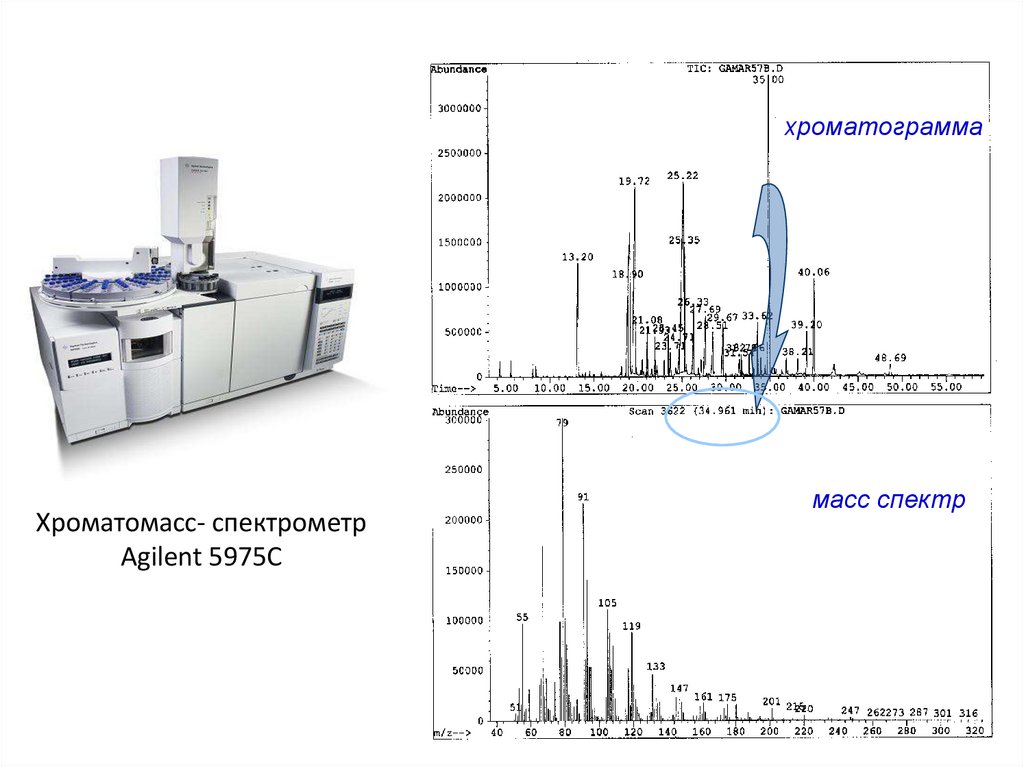
хроматограммаХроматомасс- спектрометр
Agilent 5975С
масс спектр
53.
Подготовка биологических образцов дляхроматографических анализов
Биологические пробы часто не подходят для
прямого анализа газовой хроматографией !
• Низкие концентрации определяемых веществ;
• Многокомпонентная матрица, мешающая разделению;
• Матрица вредна или несовместима с хроматографической
колонкой;
• Интересующие вещества нелетучи либо разрушаются
при высоких температурах.
54.
Методические приемы подготовкибиологических образцов
Гомогенизация (измельчение)
Добавление реагентов
Установка рН
Смешивание (встряхивание)
Нагревание (охлаждение)
Осаждение
Жидкофазная и твердофазная экстракция
Фильтрование
Центрифугирование
Выпаривание
Дериватизация
Очистка на колонках или в тонком слое
55.
ВЭЖХВЭЖХ – метод колоночной хроматографии, в котором подвижной фазой служит
жидкость, движущаяся через хроматографическую колонку, заполненную
неподвижной фазой (сорбентом).
56.
Демонстрационный материал по:ВЭЖХ
Вопросы:
1) Строение прибора
2) Применение (примеры из фармакопеи)
3) Зачем насос?
4) Плюсы ВЭЖХ
https://www.youtube.com/watch?v=eWBEDdJ
kTBw
57.
Высокоэффективная жидкостнаяхроматография (ВЭЖХ)
По сути -это изначально созданная колоночная
жидкостная хроматография, в которой применение
современного оборудования позволило достичь
высоких скоростей и высокой эффективности разделения.
70-е гг. XX в. - гигантский прогресс в инструментальной
базе явился основой для современной
высокоэффективной жидкостной хроматографии.
58.
ВЭЖХ. Область применения1. Углеводороды с различными заместители:
Алканы и алкены, бензолы, многоядерные
ароматические, гетероциклы
2. Биоорганические соединения:
Углеводы, сложные липиды, гормоны,
органические кислоты, пептиды, витамины,
пигменты, ПАВ
3. Биоорганические соединения: Белки, ДНК, РНК
4. Полимеры, их моно- и олигомеры
5. Ионы: неорганические и органические
«Подлинность»
«Посторонние примеси»
«Растворение»
«Однородность дозирования»
«Количественное определение»
59.
Модели аналитическиххроматографов для ВЭЖХ
Agilent 1200, США
Alliance, Waters, США
МИЛИХРОМ А-02, Россия
60.
Условия ВЭЖХ:- «мягкий» температурный диапазон
- применение неразрушающих детекторов
- простота сбора вытекающей подвижной фазы
- развитие препаративных разделений в
лабораториях для сбора очищенных веществ
- развитие промышленных систем для
выделения и очистки веществ, используемых в
практических целях
61.
Препаративные хроматографы сколлекторами фракций
коллектор фракций
62.
Принцип «Подобное растворяется в подобном,а разделяется противоположным»
работает и в ВЭЖХ
Элюция – процесс прохождения веществ через колонку с потоком
подвижной фазы
Элюат – выходящий из колонки поток подвижной фазы с
компонентами разделяемой смеси
Элюент – растворитель (или смесь), использующийся в качестве
подвижной фазы
Элюирующая сила – способность подвижной фазы (смеси растворителей)
десорбировать и вымывать компоненты пробы с сорбента данного типа
Элюотропный ряд – ряд, в котором растворители расположены в порядке
возрастания элюирующей силы
63.
время удерживания ~ объем удерживанияV=T·S
V - oбъем прошедшей подвижной фазы, мл
S - скоростъ потока, const, мл/мин
T - время, мин
64.
Классификация жидкостной хроматографииПо характеристикам и взаимодействиям неподвижной фазы:
• Варианты:
Адсорбционная – разделение веществ за счет различной способности
адсорбироваться и десорбироваться с поверхности сорбента.
Распределительная - разделение веществ за счет различия коэффициентов
распределения между неподвижной и подвижной фазами.
Нормально-фазовая – неподвижная фаза – полярная, подвижная –
неполярная
Обращенно-фазовая – неподвижная фаза – неполярная, подвижная фаза –
полярная.
Ионообменная – разделение смеси веществ, диссоциированных в растворе
на ионы, за счет различной силы взаимодействия определяемых ионов с
ионными группами сорбента
Эксклюзионная (ситовая, гель-проникающая, гель-фильтрационная) –
молекулы веществ разделяются по размеру за счет их разной способности
проникать в поры неподвижной фазы.
Хиральная – разделение оптически активных соединений.
65.
Виды ЖХНеподвижная фаза
Подвижная фаза
Применение
Хиральная
Сорбенты с модифицированной
поверхностью, содержащие хитозаны,
циклодекстрины, полисахариды и тд. С
различными модификаторами
(хиральные комплексы металлов,
нейтральные жирные лиганды, ион
парные реагенты
Например: метанола в гексанизопропанол
Для разделения и анализа
энантиомеров
Обращенно
фазовая (ОФ)
Неполярная. Чаще всего сорбент с
химически пришитыми непол
группами. Н:октодецил (С18),
гексодецил (С16), бутил, метил
Полярная Н: смеси с водой,
спиртами, ацетонитрилом и тд.
Применяется в 80% лабораторий,
где используется ВЭЖХ .
Н: для разделения
полиароматических ув(ПАУВ)
Нормально
фазовая (нф)
Сорбент на основе силикогеля с полярн
модифик-ми
Неполярная. Н: гексан, пентан,
изооктан, гептан
Смеси сахаров, белков и
пептидов, органические изомеры
Эксклюзионная
Акриловые и полиуглеводородные
полимеры
Любой растворитель( в котором
растворяется и обеспец-т
отсутствие сорбции посторон-х
комп-в) . Н: ацетон
Макромолекулы биологич.
Происхожд-я и для очистки
полимеров
Гидрофильная
Полярн. стационарная фаза
Полярн: вода, ацетон, спирт
Полярные орг-е соединения
Н: изомеры спиртов, витамины
Ионообменная
Ионообменные смолы, или на основе
силикогеля, модифицированнные
функц-ми группами
Растворы солей или буф-х систем
на их основе
Для неорганических ионов и
ионогенных орг. вещ-в.
Н: катионы и анионы в воде
66.
Нормально-фазовая жидкостная хроматография:неподвижная фаза – полярная,
подвижная фаза – неполярная.
Неподвижные фазы:
силикагель и его модификации, оксид алюминия
силоксановые
связи
Элюенты:
углеводороды,
эфиры,
спирты и пр.
гидроксильные
группы
Поверхность пористой частицы
силикагеля
67.
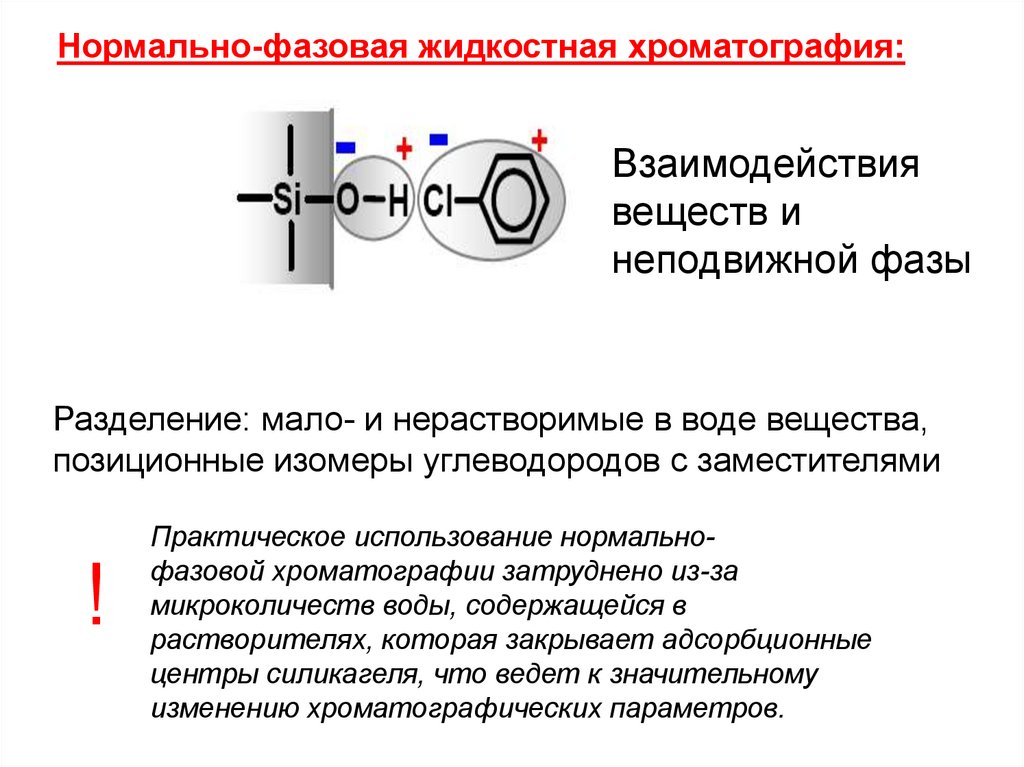
Нормально-фазовая жидкостная хроматография:Взаимодействия
веществ и
неподвижной фазы
Разделение: мало- и нерастворимые в воде вещества,
позиционные изомеры углеводородов с заместителями
!
Практическое использование нормальнофазовой хроматографии затруднено из-за
микроколичеств воды, содержащейся в
растворителях, которая закрывает адсорбционные
центры силикагеля, что ведет к значительному
изменению хроматографических параметров.
68.
Обращенно-фазовая жидкостная хроматография:неподвижная фаза – неполярная,
подвижная фаза – полярная.
Неподвижные фазы: модификации силикагеля
R = -CH3, -C4H9, -C8H17, -C18H37, -C6H5
Элюенты: спирты, нитрилы, вода и пр., добавки солей
69.
Обращенно-фазовая жидкостная хроматографияВзаимодействия
веществ и
неподвижной фазы
Разделение: нейтральные органические вещества,
слабые кислоты, слабые основания и пр.
75 % от всех разделений ВЭЖХ – это
обращенно-фазовый тип
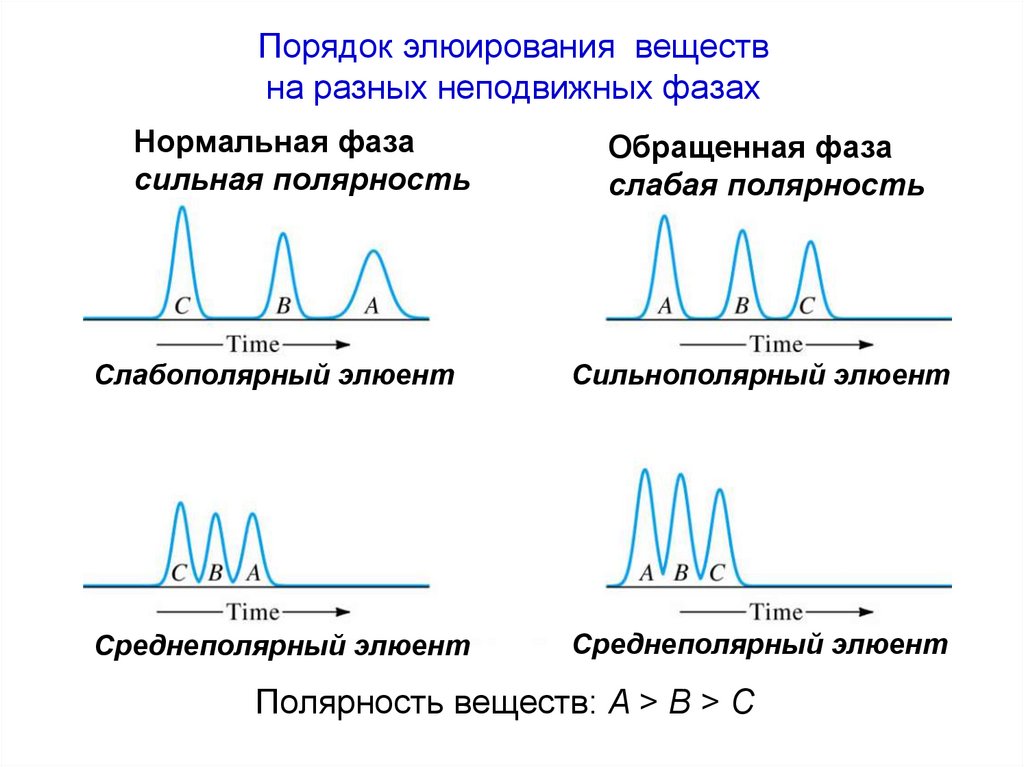
70.
Порядок элюирования веществна разных неподвижных фазах
Нормальная фаза
сильная полярность
Обращенная фаза
слабая полярность
Слабополярный элюент
Сильнополярный элюент
Среднеполярный элюент
Среднеполярный элюент
Полярность веществ: A > B > C
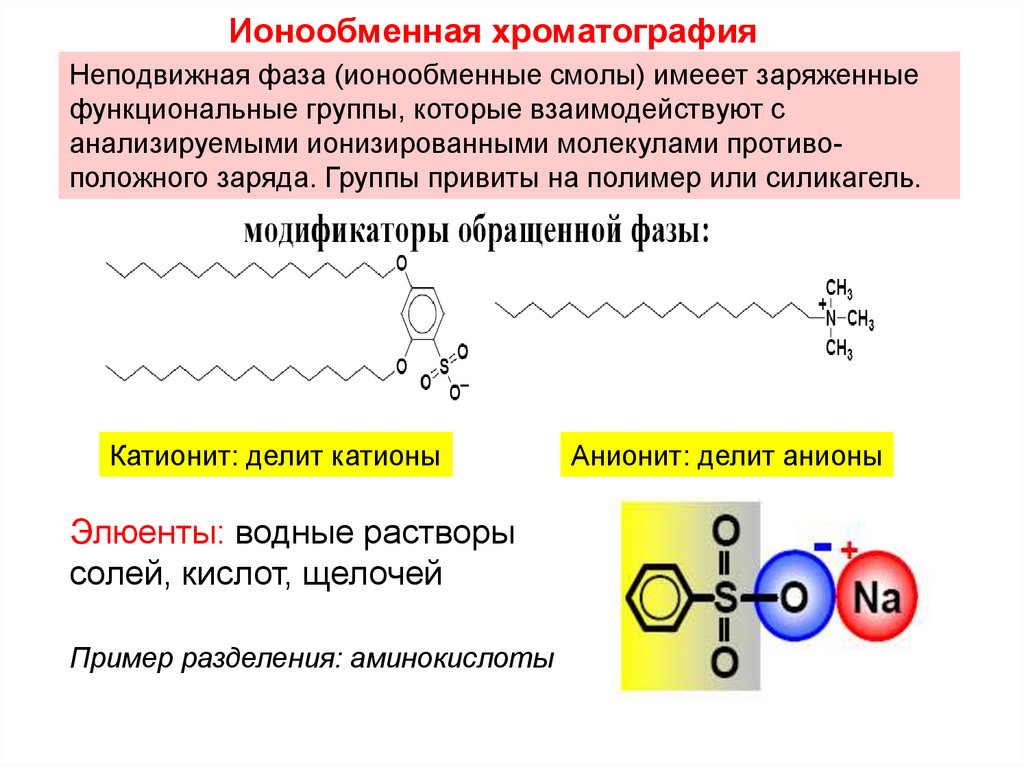
71.
Ионообменная хроматографияНеподвижная фаза (ионообменные смолы) имееет заряженные
функциональные группы, которые взаимодействуют с
анализируемыми ионизированными молекулами противоположного заряда. Группы привиты на полимер или силикагель.
Катионит: делит катионы
Элюенты: водные растворы
солей, кислот, щелочей
Пример разделения: аминокислоты
Анионит: делит анионы
72.
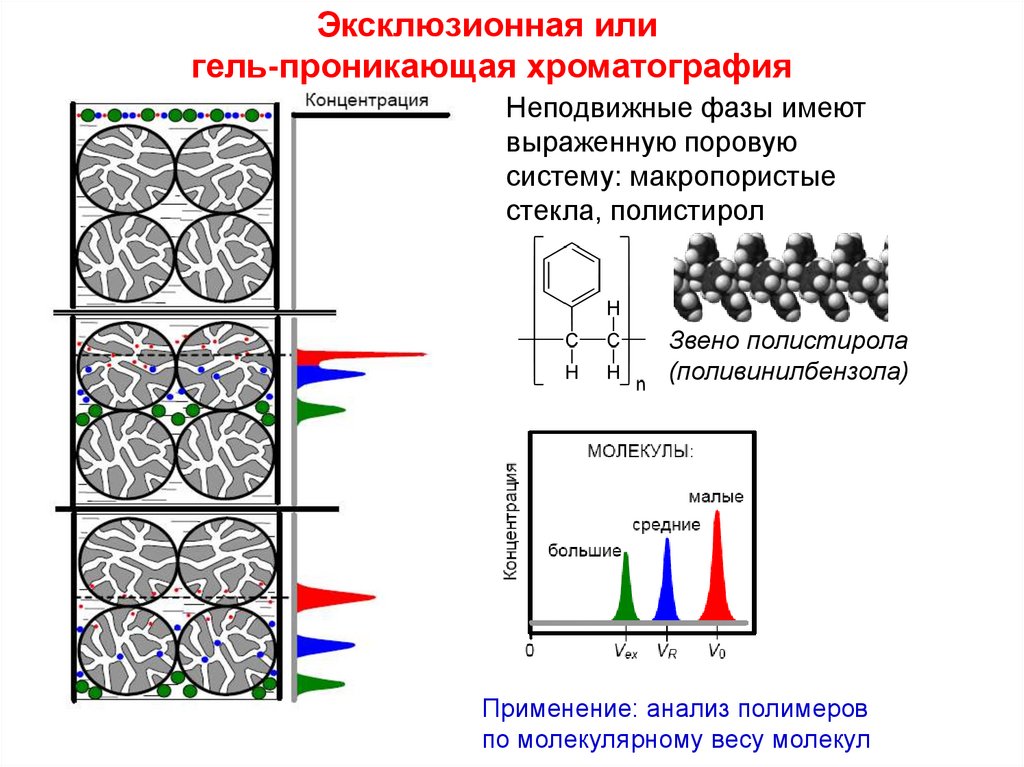
Эксклюзионная илигель-проникающая хроматография
Неподвижные фазы имеют
выраженную поровую
систему: макропористые
стекла, полистирол
Звено полистирола
(поливинилбензола)
Применение: анализ полимеров
по молекулярному весу молекул
73.
Масс-спектрометрическийдетектор в ВЭЖХ
Времяпролетный
масс-спектрометр
74.
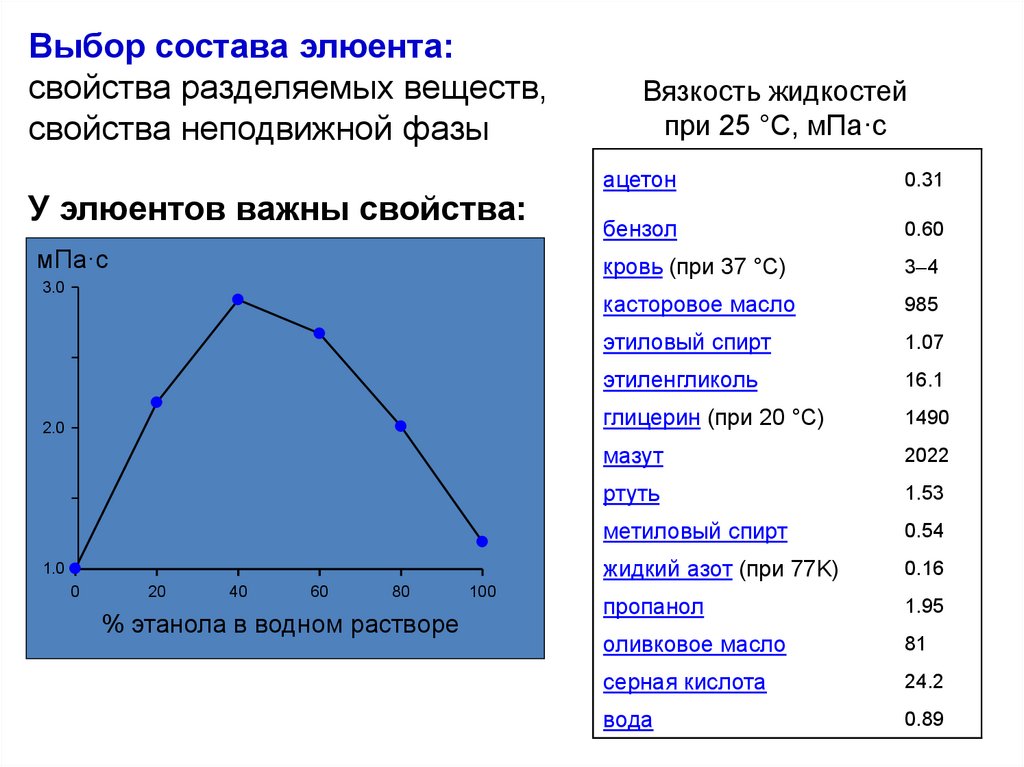
Выбор состава элюента:свойства разделяемых веществ,
свойства неподвижной фазы
Вязкость жидкостей
при 25 °C, мПа·с
ацетон
0.31
бензол
0.60
мПа·с
кровь (при 37 °C)
3–4
Вязкость
касторовое масло
985
этиловый спирт
1.07
этиленгликоль
16.1
глицерин (при 20 °C)
1490
мазут
2022
ртуть
1.53
метиловый спирт
0.54
жидкий азот (при 77K)
0.16
пропанол
1.95
оливковое масло
81
серная кислота
24.2
вода
0.89
У элюентов важны свойства:
3.0
Прозрачность в УФ-диапазоне
Индекс
рефракции
2.0
Элюирующая сила
Тип взаимодействия
1.0Чистота
0
20
40
60
80
% этанола в водном растворе
Смешиваемость
100
75.
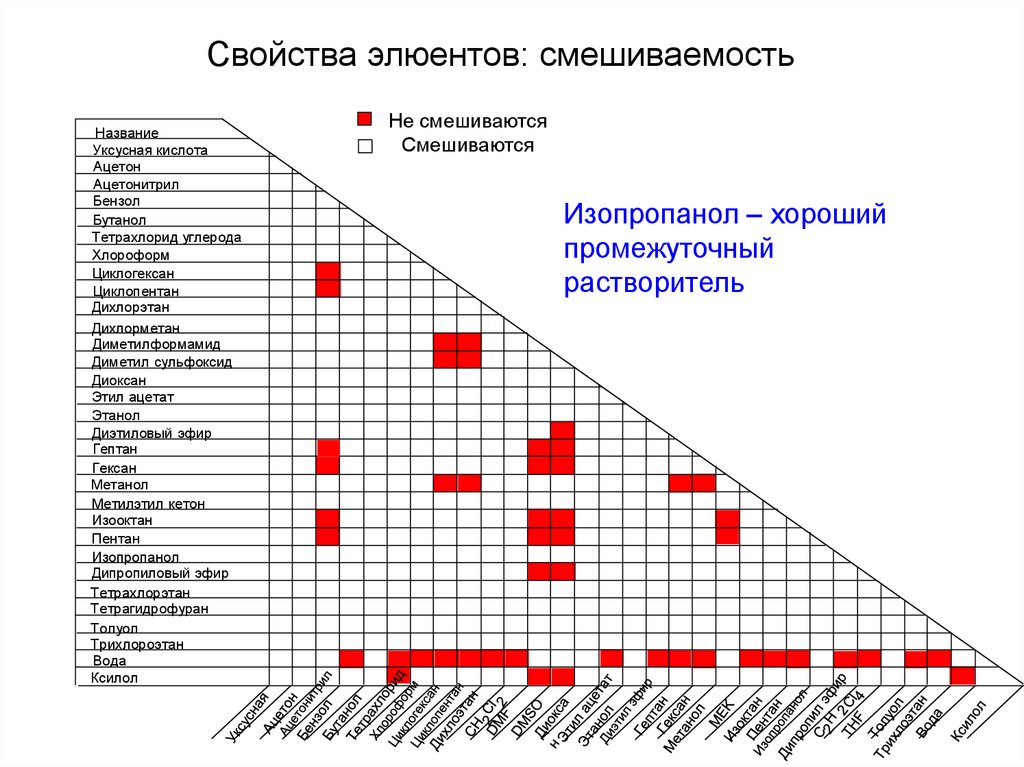
Свойства элюентов: смешиваемостьНазвание
Уксусная кислота
Ацетон
Ацетонитрил
Бензол
Бутанол
Тетрахлорид углерода
Хлороформ
Циклогексан
Циклопентан
Дихлорэтан
Дихлорметан
Диметилформамид
Диметил сульфоксид
Диоксан
Этил ацетат
Этанол
Диэтиловый эфир
Гептан
Гексан
Метанол
Метилэтил кетон
Изооктан
Пентан
Изопропанол
Дипропиловый эфир
Тетрахлорэтан
Тетрагидрофуран
Толуол
Трихлороэтан
Вода
Ксилол
Не смешиваются
Смешиваются
Изопропанол – хороший
промежуточный
растворитель
76.
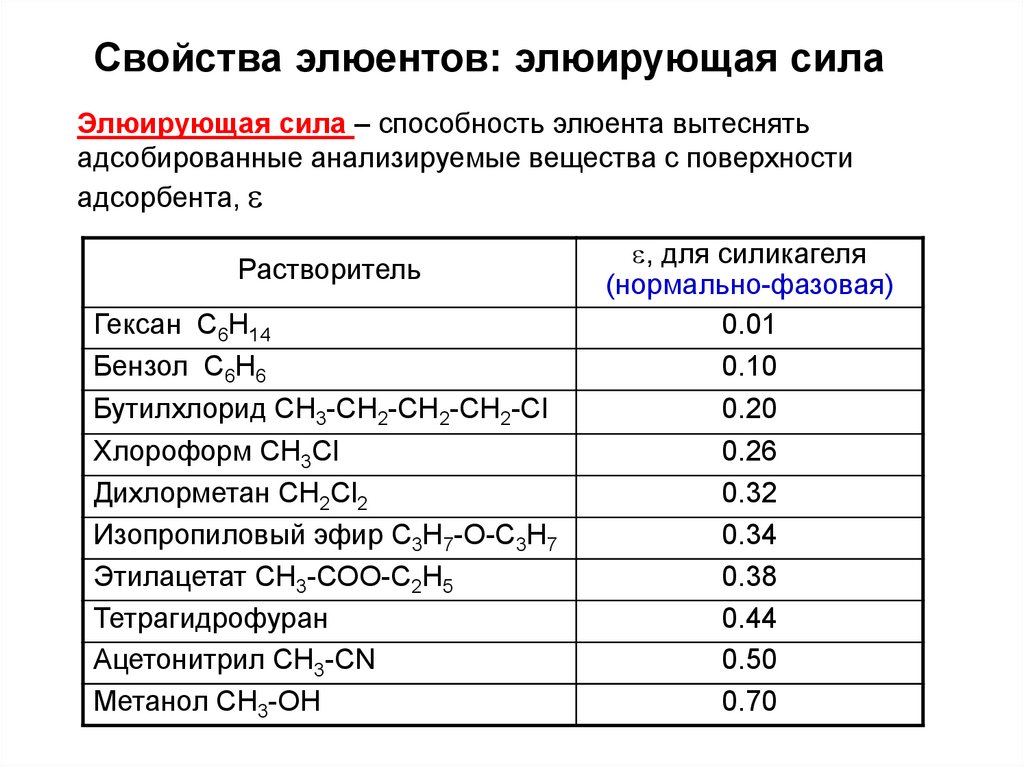
Свойства элюентов: элюирующая силаЭлюирующая сила – способность элюента вытеснять
адсобированные анализируемые вещества с поверхности
адсорбента,
Растворитель
Гексан C6H14
Бензол C6H6
Бутилхлорид CH3-CH2-CH2-CH2-Cl
Хлороформ CH3Cl
Дихлорметан CH2Cl2
Изопропиловый эфир C3H7-O-C3H7
Этилацетат CH3-СОO-C2H5
Тетрагидрофуран
Ацетонитрил CH3-CN
Метанол CH3-ОН
, для силикагеля
(нормально-фазовая)
0.01
0.10
0.20
0.26
0.32
0.34
0.38
0.44
0.50
0.70
77.
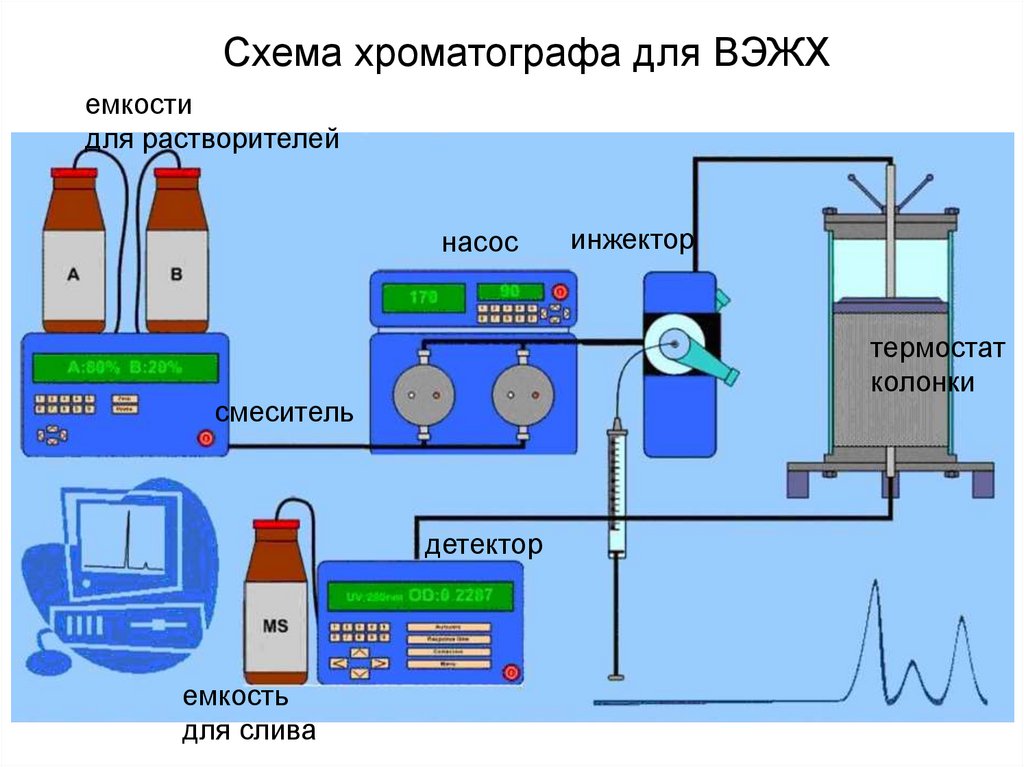
Схема хроматографа для ВЭЖХемкости
для растворителей
насос
термостат
колонки
смеситель
детектор
емкость
для слива
инжектор
78.
Компоненты ВЭЖХ прибора: Система подачи элюентовФильтрация
Дегазация
Смешивание
Контроль
давления (50-200 атм)
79.
80.
Низкие скорости потока1-10 мл/мин
81.
82.
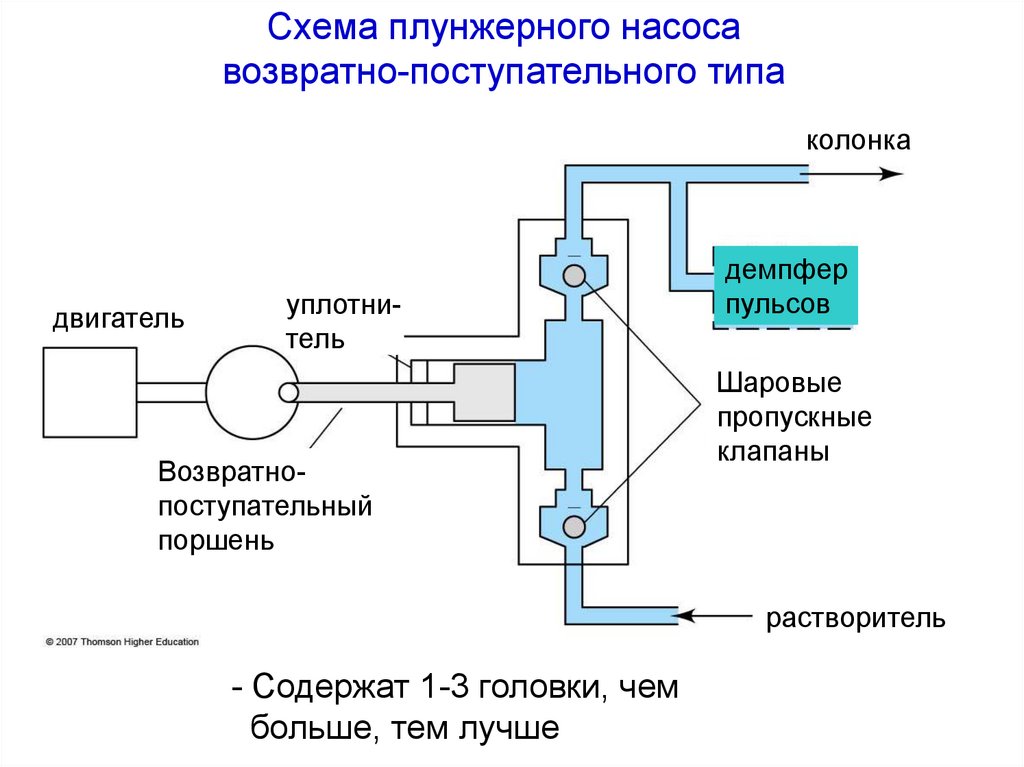
Схема плунжерного насосавозвратно-поступательного типа
колонка
двигатель
уплотнитель
Возвратнопоступательный
поршень
демпфер
пульсов
Шаровые
пропускные
клапаны
растворитель
- Содержат 1-3 головки, чем
больше, тем лучше
83.
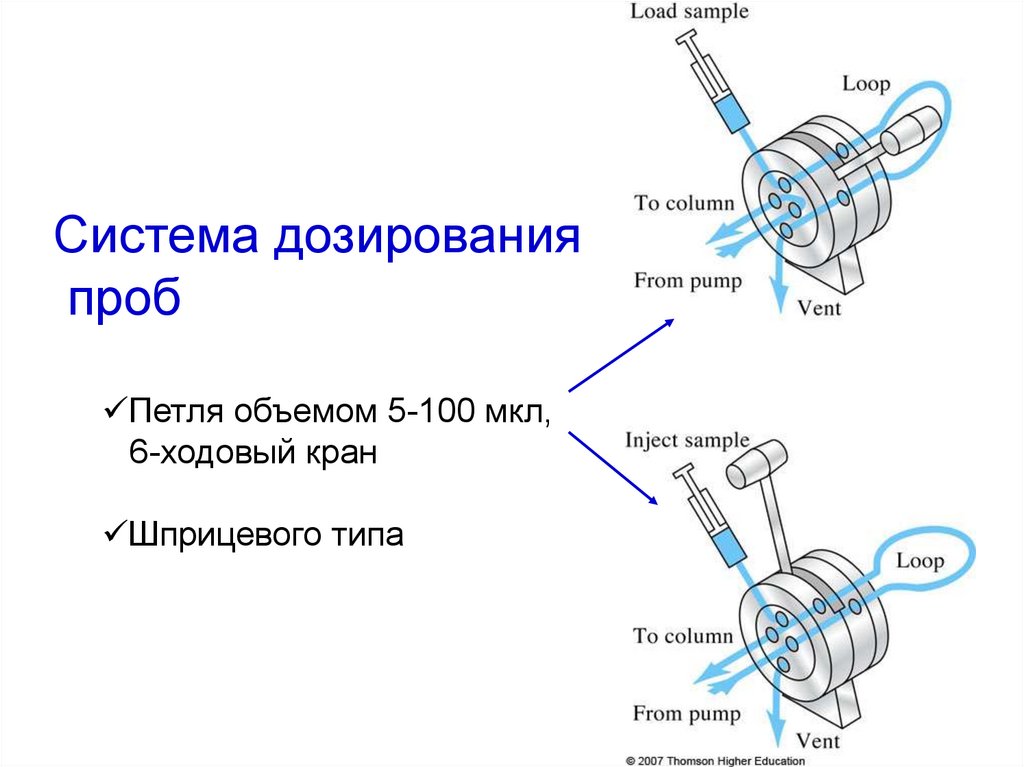
Система дозированияпроб
Петля объемом 5-100 мкл,
6-ходовый кран
Шприцевого типа
84.
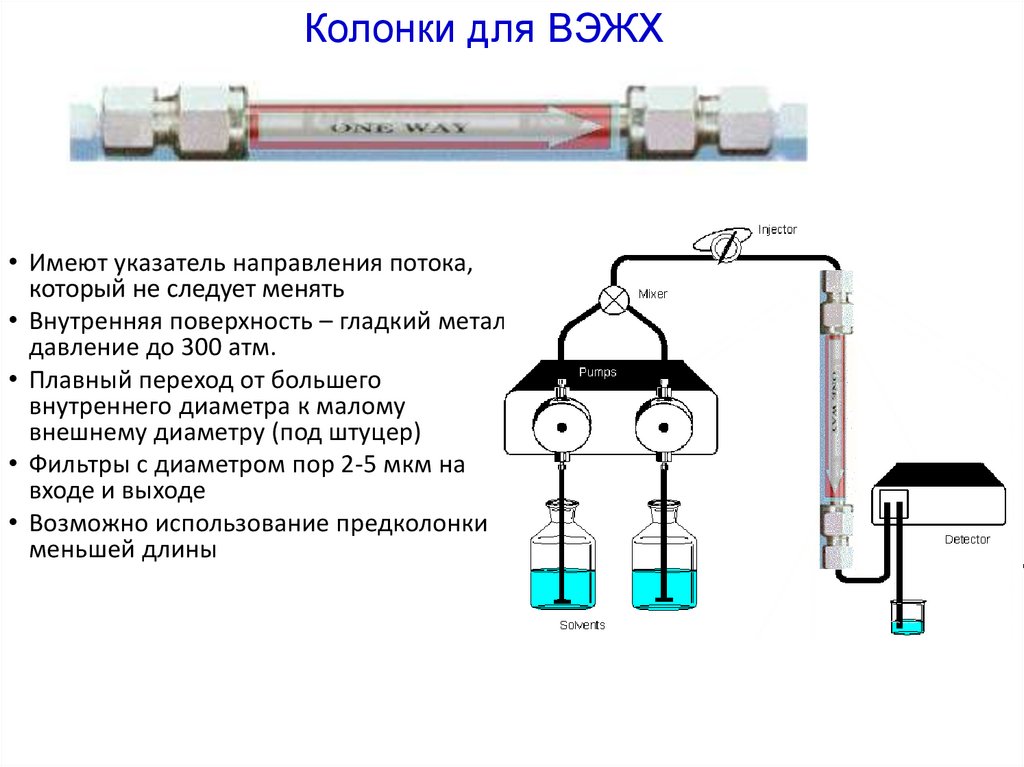
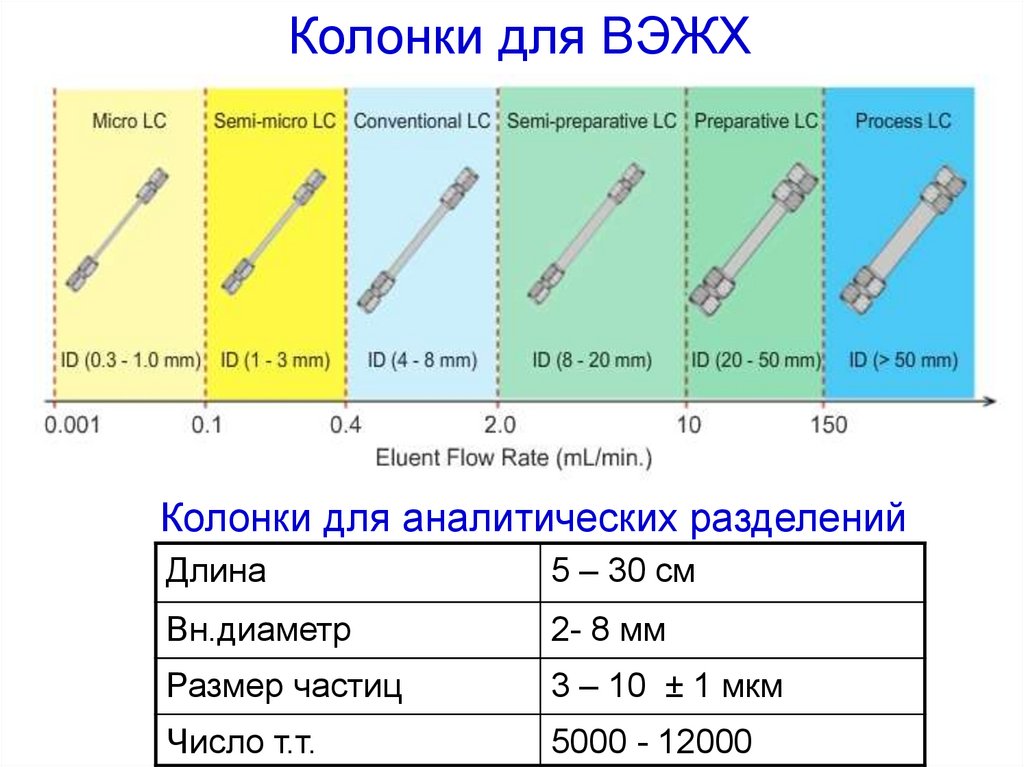
Колонки для ВЭЖХ• Имеют указатель направления потока,
который не следует менять
• Внутренняя поверхность – гладкий металл,
давление до 300 атм.
• Плавный переход от большего
внутреннего диаметра к малому
внешнему диаметру (под штуцер)
• Фильтры с диаметром пор 2-5 мкм на
входе и выходе
• Возможно использование предколонки
меньшей длины
85.
Колонки для ВЭЖХКолонки для аналитических разделений
Длина
5 – 30 см
Вн.диаметр
2- 8 мм
Размер частиц
3 – 10 ± 1 мкм
Число т.т.
5000 - 12000
86.
КОЛОНКА – «СЕРДЦЕ» ХРОМАТОГРАФАУспех разделения в ВЭЖХ во многом зависит от типа
частиц и качества их упаковки им колонки.
«Идеальная» частица
адсорбента с порами
Реальные частицы адсорбента,
заполняющие колонку
87.
ДЕТЕКТОР – «ГЛАЗА» ХРОМАТОГРАФАВ ВЭЖХ - это преобразователь концентрации анализируемого
вещества, растворенного в подвижной фазе, в электрический
сигнал, по изменению физических свойств жидкости
Детектор
Измеряемое физическое
свойство
Чувствительность, г
Селективность
Спектрофотометрический
Оптическая плотность на
определенной длине волны
(фильтр или монохроматор)
10-9
Высокая
Рефрактометрический
Разность показателя
преломления
10-6
Низкая
Флуорометрический
Излучение света на
определенной длине волны
10-11
Очень высокая
Амперометрический
Ток окисления или
восстановления
10-9 - 10-11
Очень высокая
Кондуктометрический
Электропроводность
элюента
10-10
Низкая
Масс-спектрометрический
Ионный поток, возникающий
при различных
энергетических
воздействиях
10-9
Средняя
88.
Рефрактометрический детекторДостоинства:
Универсальность
Простота
Дешевизна
Применимость для неокрашенных веществ
89.
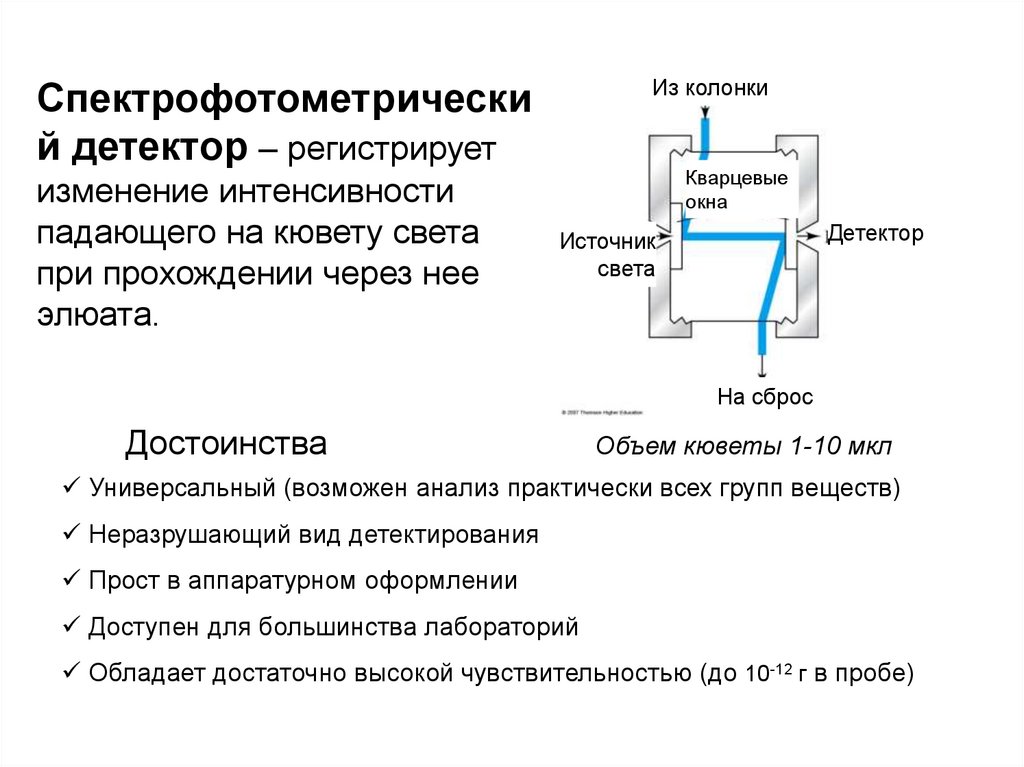
Из колонкиСпектрофотометрически
й детектор – регистрирует
изменение интенсивности
падающего на кювету света
при прохождении через нее
элюата.
Кварцевые
окна
Детектор
Источник
света
На сброс
Достоинства
Объем кюветы 1-10 мкл
Универсальный (возможен анализ практически всех групп веществ)
Неразрушающий вид детектирования
Прост в аппаратурном оформлении
Доступен для большинства лабораторий
Обладает достаточно высокой чувствительностью (до 10-12 г в пробе)
90.
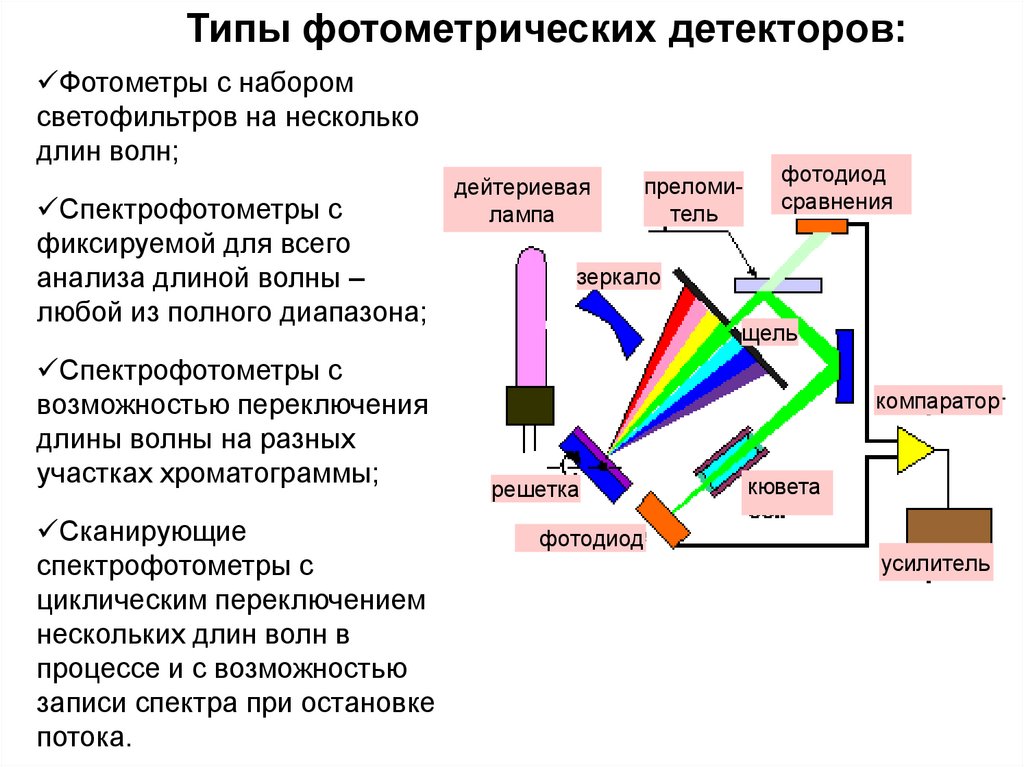
Типы фотометрических детекторов:Фотометры с набором
светофильтров на несколько
длин волн;
Спектрофотометры с
фиксируемой для всего
анализа длиной волны –
любой из полного диапазона;
Спектрофотометры с
возможностью переключения
длины волны на разных
участках хроматограммы;
Сканирующие
спектрофотометры с
циклическим переключением
нескольких длин волн в
процессе и с возможностью
записи спектра при остановке
потока.
дейтериевая
лампа
преломитель
фотодиод
сравнения
зеркало
щель
компаратор
решетка
фотодиод
кювета
усилитель
91.
СПЕКТРОФОТОМЕТРИЯ В ВЭЖХСРАВНЕНИЕ СПЕКТРОВ ПОГЛОЩЕНИЯ





















































 Физика
Физика