Похожие презентации:
Ферменты-1
1. КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ
Лекция по теме:«ФЕРМЕНТЫ - 1»
КРАСНОДАР
2009
2.
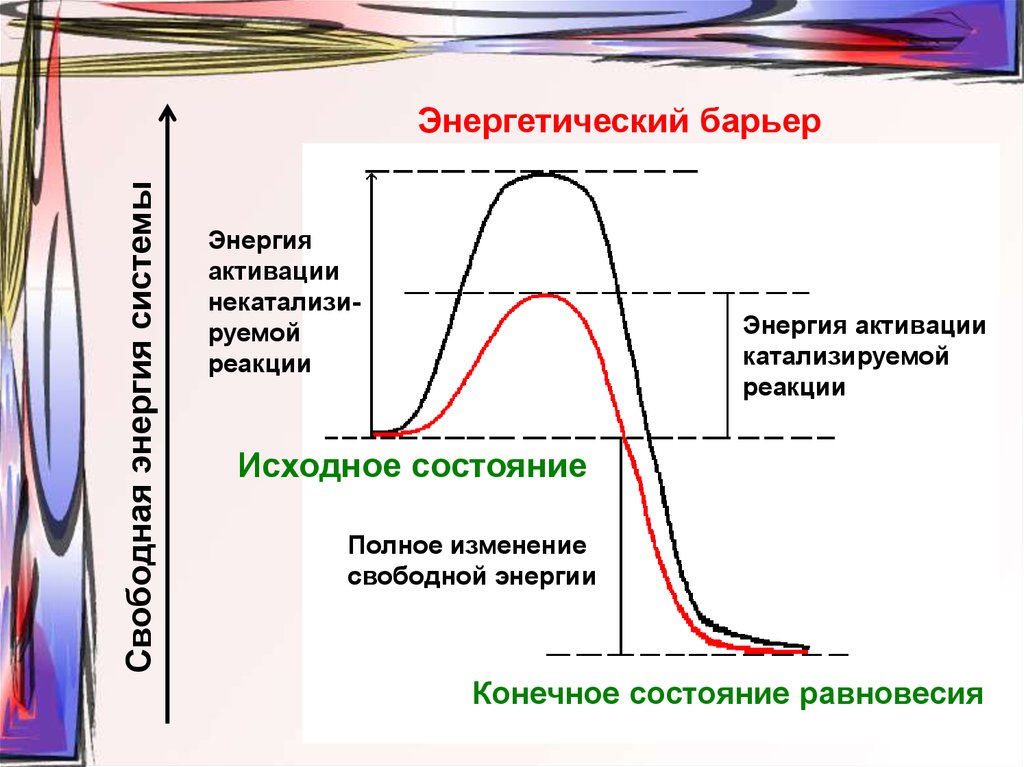
Свободная энергия системыЭнергетический барьер
Энергия
активации
некатализируемой
реакции
Энергия активации
катализируемой
реакции
Исходное состояние
Полное изменение
свободной энергии
Конечное состояние равновесия
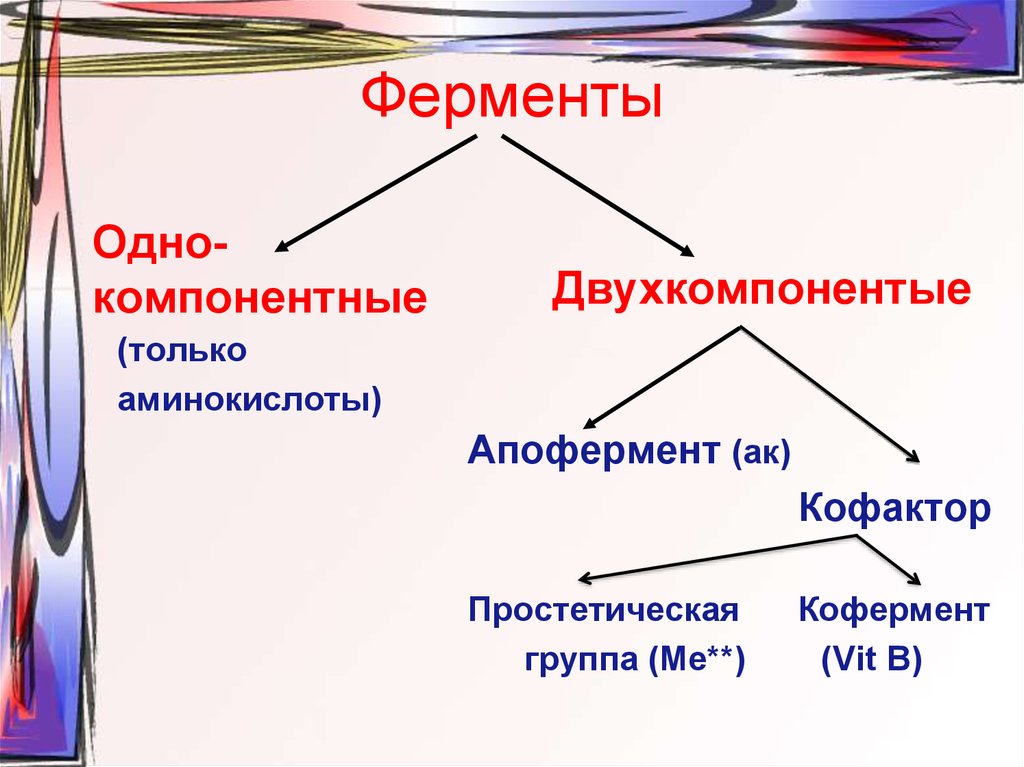
3. Ферменты
ОднокомпонентныеДвухкомпонентые
(только
аминокислоты)
Апофермент (ак)
Кофактор
Простетическая
группа (Ме**)
Кофермент
(Vit В)
4. Собственные свойства ферментов
• Высокая биологическая активность• Ферментная специфичность
• действия
• субстратная
• Иная зависимость от факторов,
влияющих на скорость реакции
• Наличие механизмов регуляции
активности
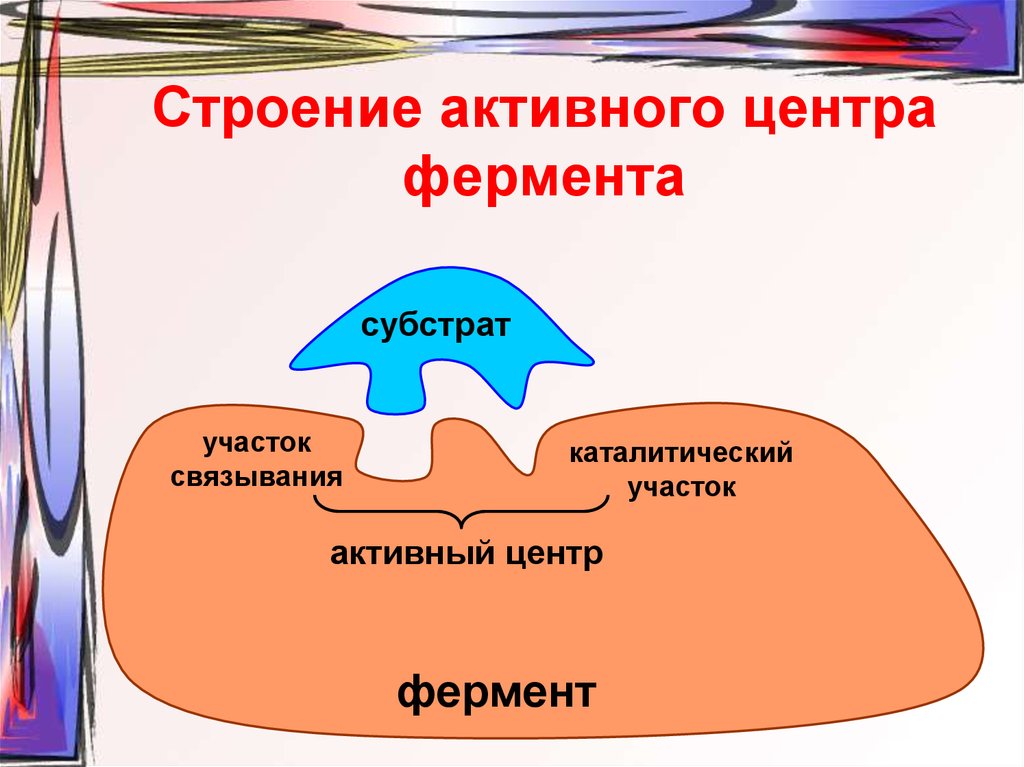
5. Строение активного центра фермента
субстратучасток
связывания
каталитический
участок
активный центр
фермент
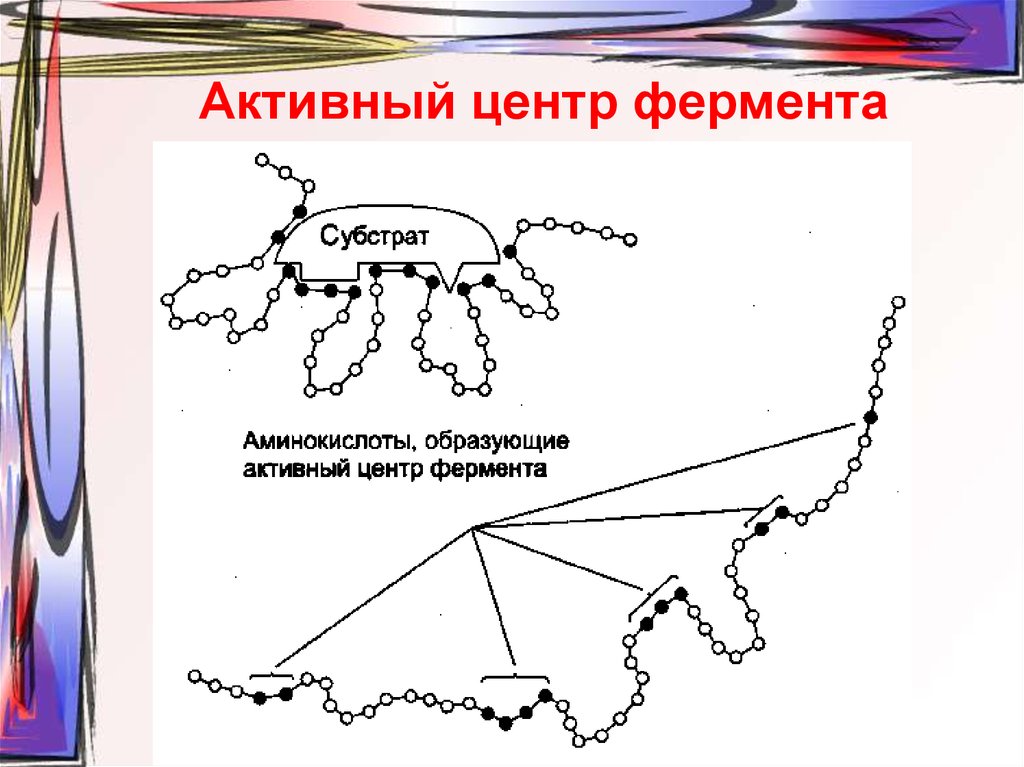
6. Активный центр фермента
7. Металлы, содержащиеся в ферментах
Алкогольдегидрогеназа,карбоангидраза
Аргиназа, аминопептидаза
Дипептидаза
Mn
Co
Фосфатаза, фосфокиназа
Mg
Тирозиназа
Cu
Сукцинатдегидрогеназа
Fe
Ксантиноксидаза
Mo
Zn
8. Каталитические центры ферментов
Ко-А, глутатион, липоевая кислотапиридоксальфосфат
тетрагидрофолиевая кислота
флавины
биотин
тиаминпирофосфат
НАД+ и НАДФ+
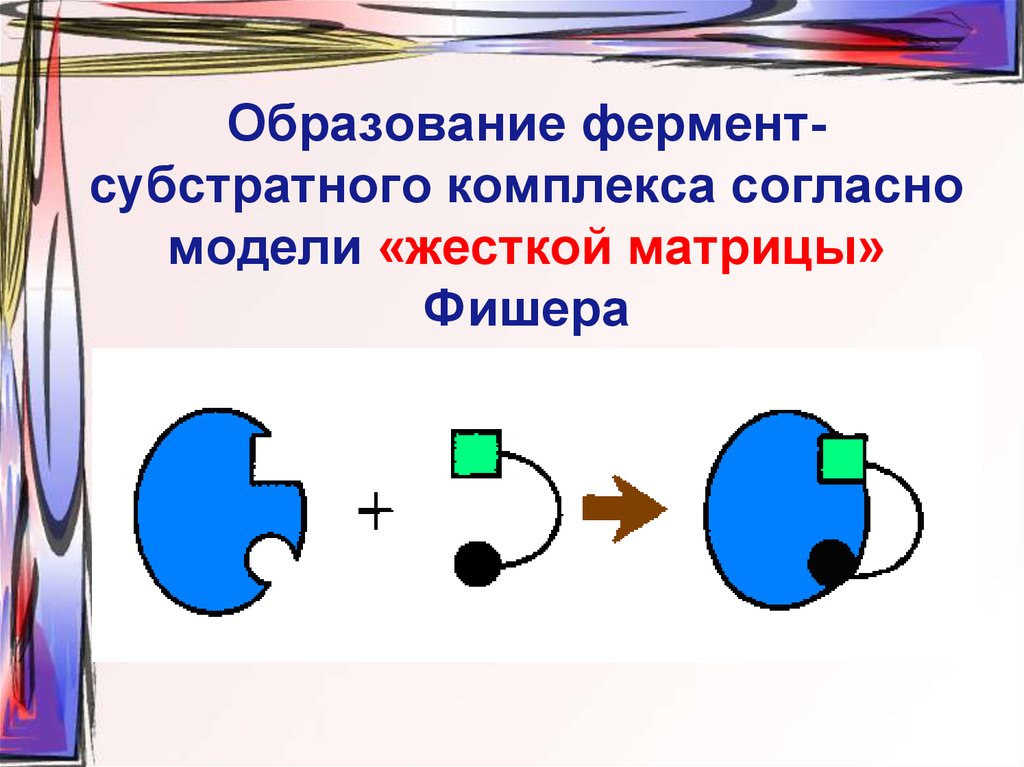
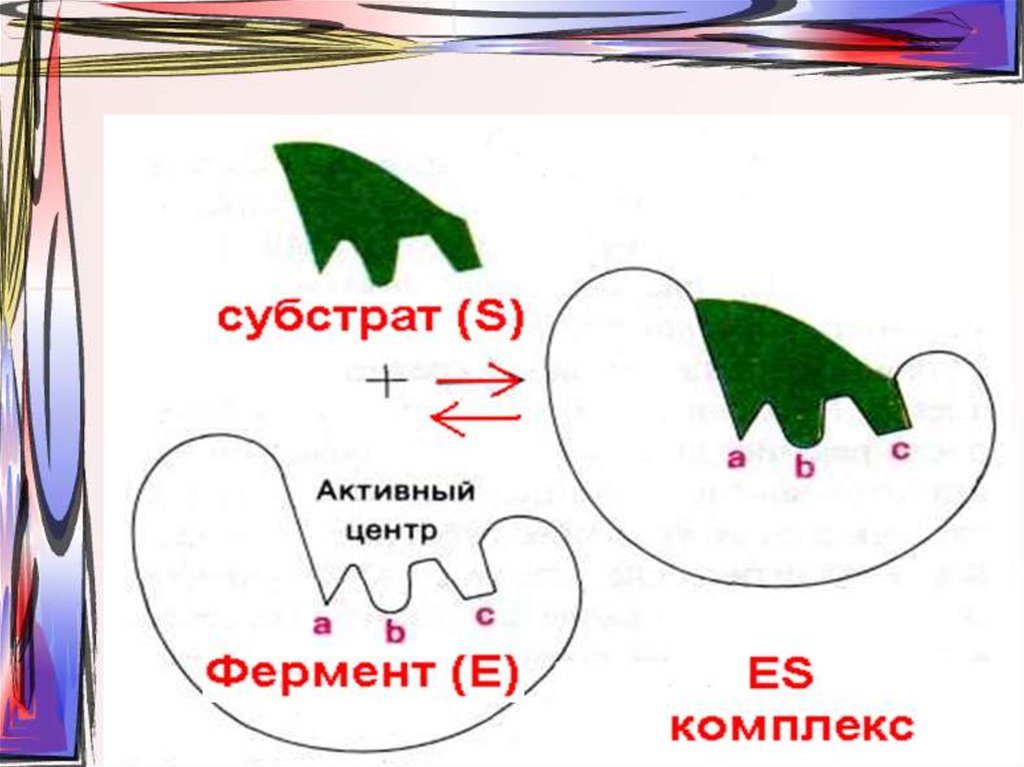
9. Образование фермент-субстратного комплекса согласно модели «жесткой матрицы» Фишера
Образование ферментсубстратного комплекса согласномодели «жесткой матрицы»
Фишера
10.
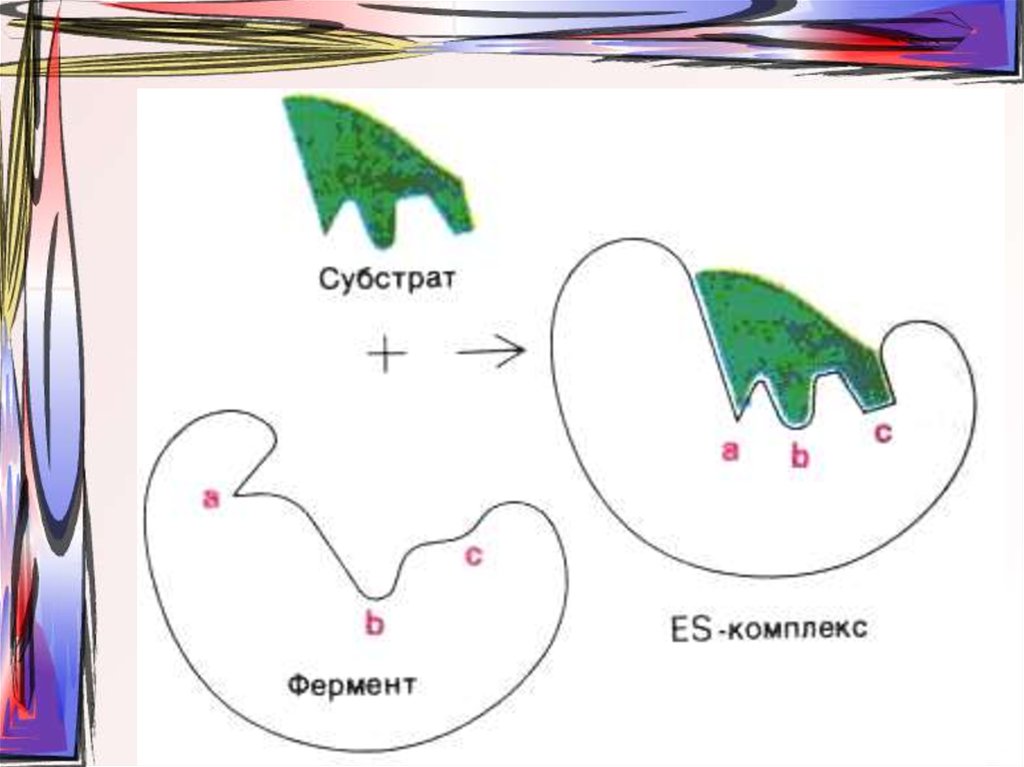
11. Схематическое представление конформационных изменений в молекуле фермента при связывании субстрата согласно модели «индуцированного со
Схематическое представлениеконформационных изменений в
молекуле фермента при связывании
субстрата согласно модели
«индуцированного соответствия»
Кошланда
12.
13. Общее уравнение ферментативной реакции:
E+Sk1
k2
ES
k3
EP
E+P
14. Стадии ферментативного катализа
III
III
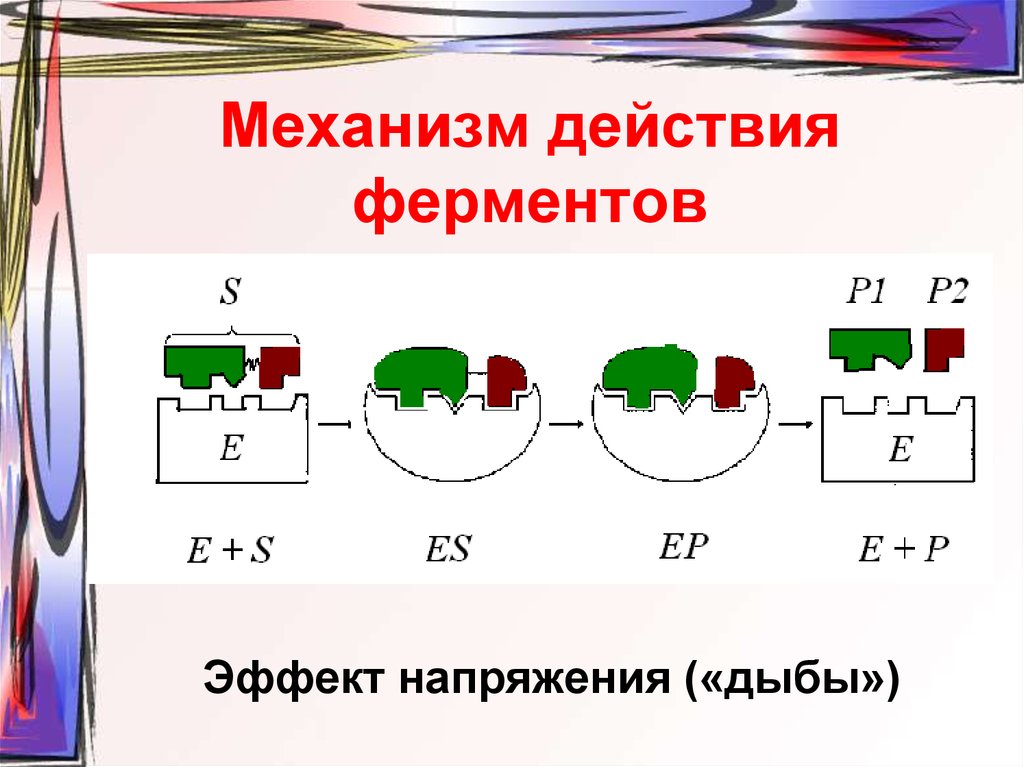
15. Механизм действия ферментов
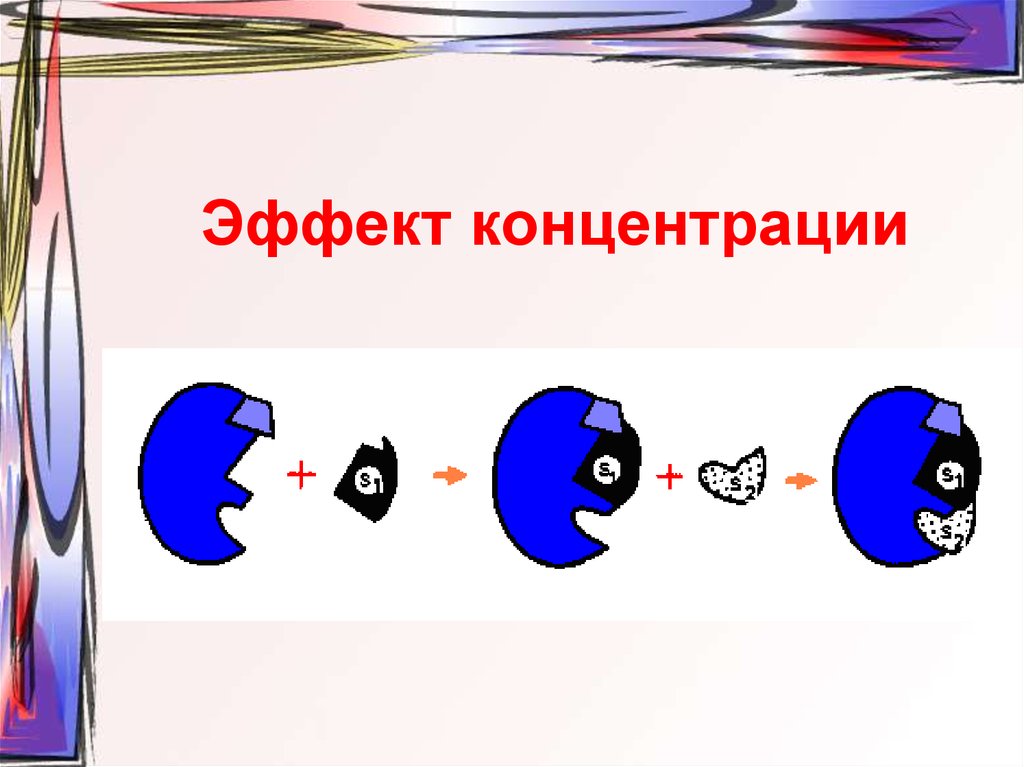
Эффект напряжения («дыбы»)16. Эффект концентрации
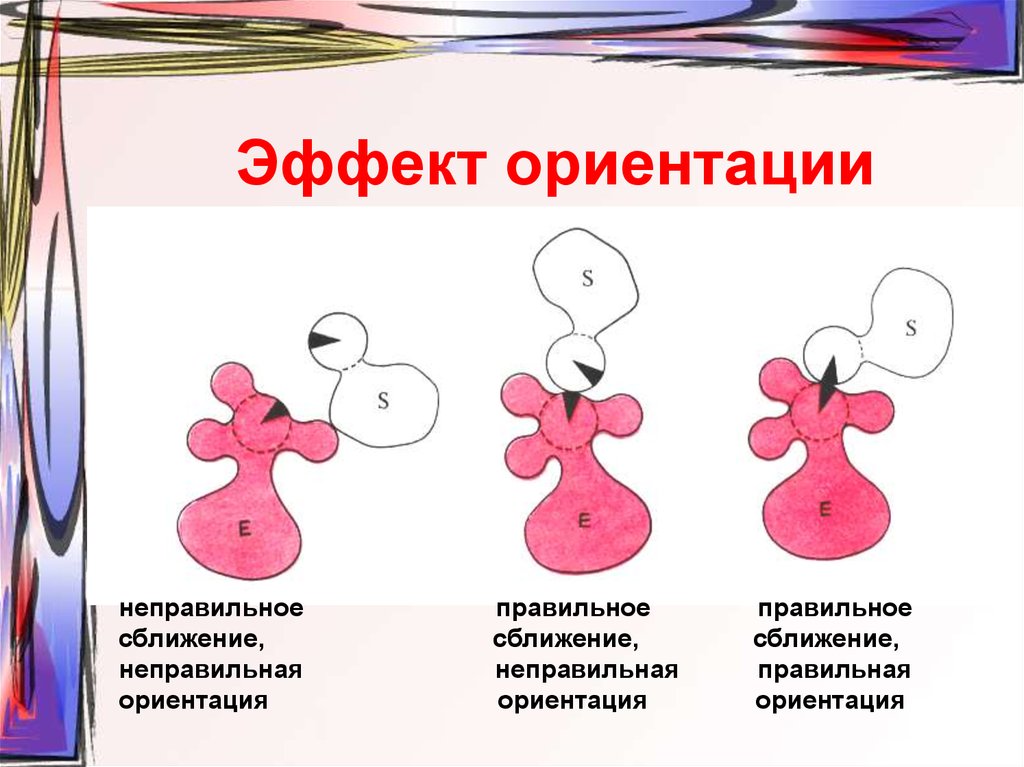
17. Эффект ориентации
неправильноесближение,
неправильная
ориентация
правильное
сближение,
неправильная
ориентация
правильное
сближение,
правильная
ориентация
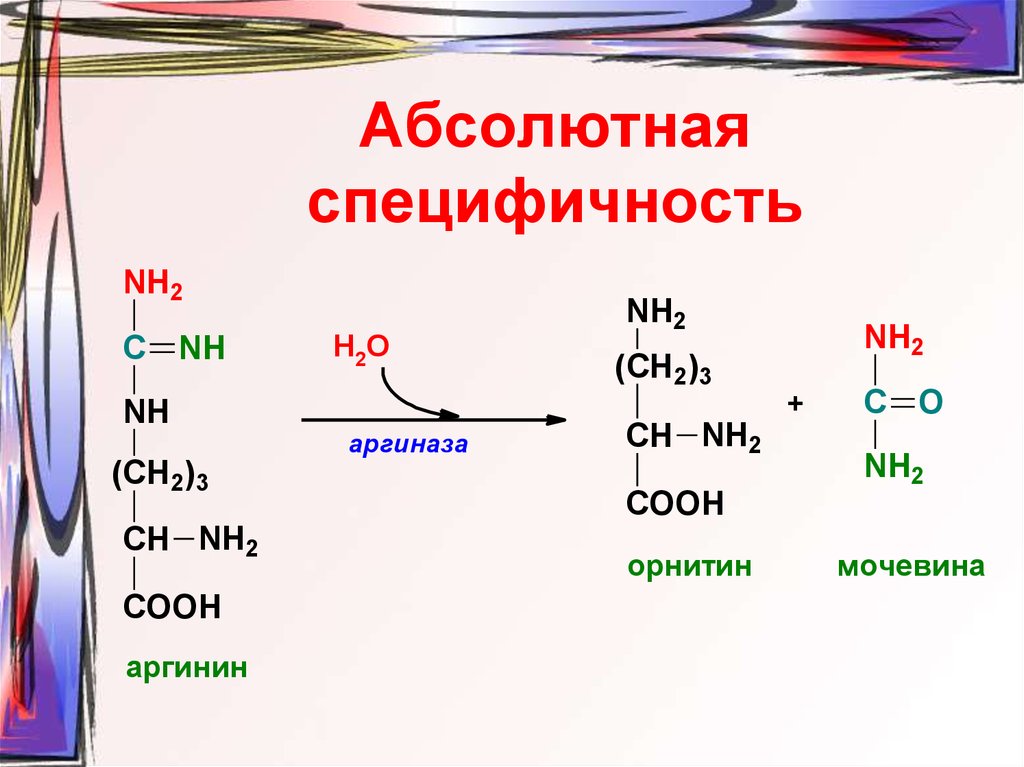
18. Абсолютная специфичность
NH2С NH
NH
(СН2)3
СН NH2
COOH
аргинин
Н2О
аргиназа
NH2
NH2
(СН2)3
СН NH2
+
С O
NH2
COOH
орнитин
мочевина
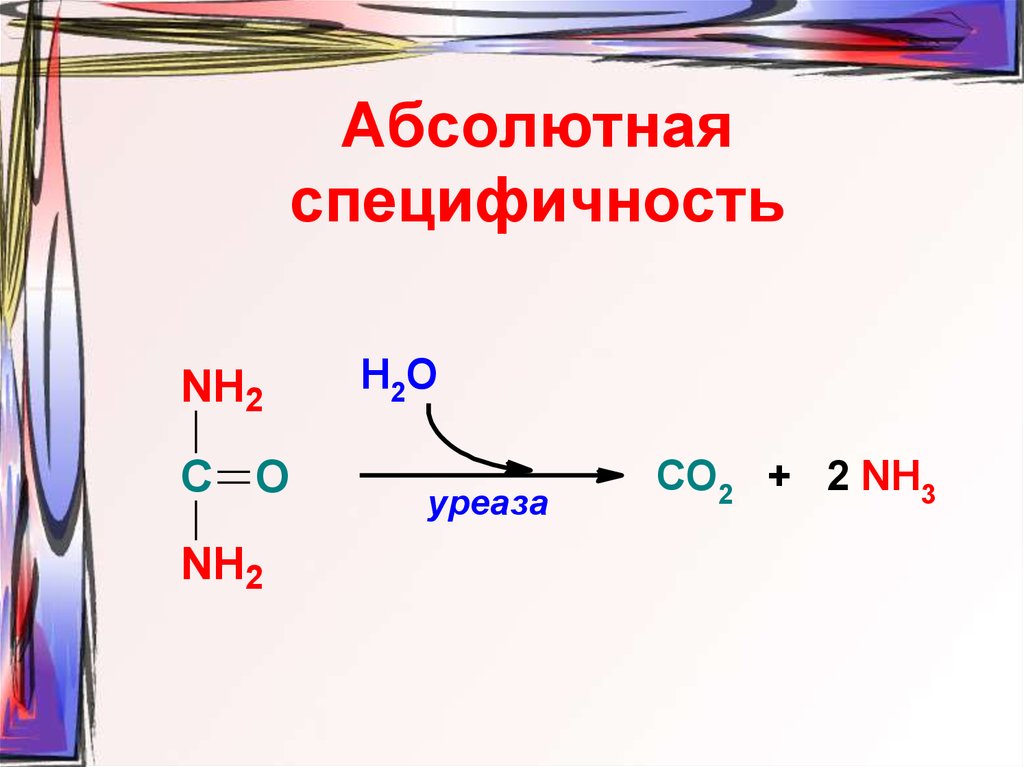
19. Абсолютная специфичность
NH2С O
NH2
Н2О
уреаза
СО2 + 2 NH3
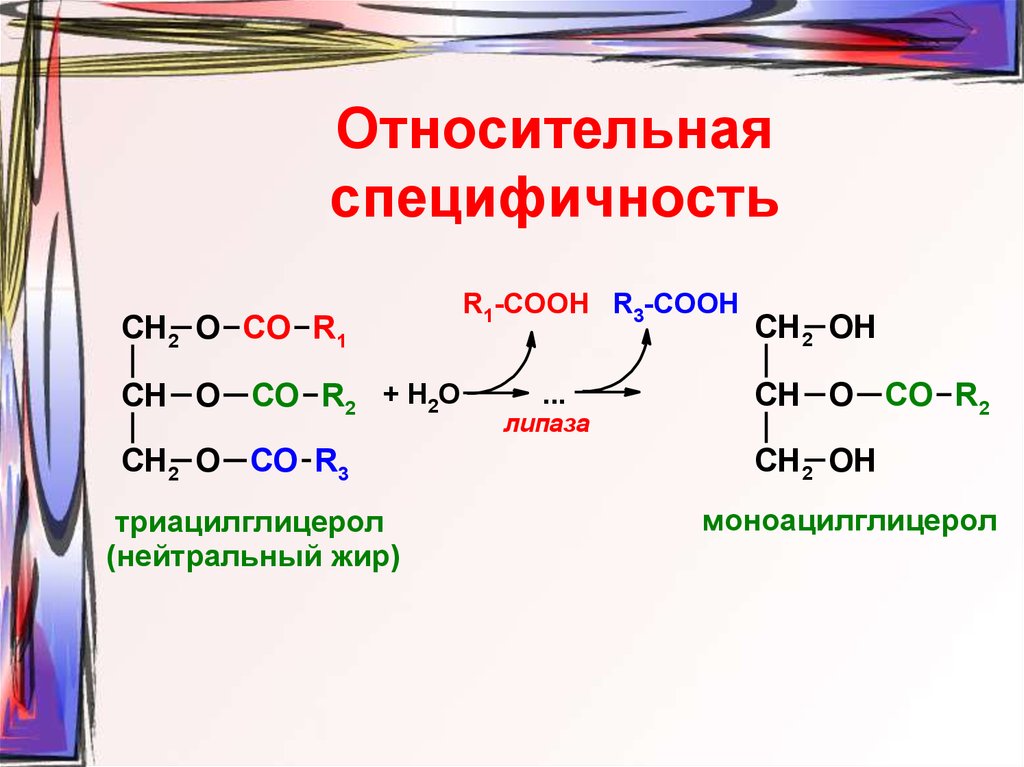
20. Относительная специфичность
СН2 O CО R1СН O CО R2 + Н2О
СН2 O СО R3
триацилглицерол
(нейтральный жир)
R1-COOH R3-COOH
...
липаза
СН2 OH
СН O CО R2
СН2 OH
моноацилглицерол
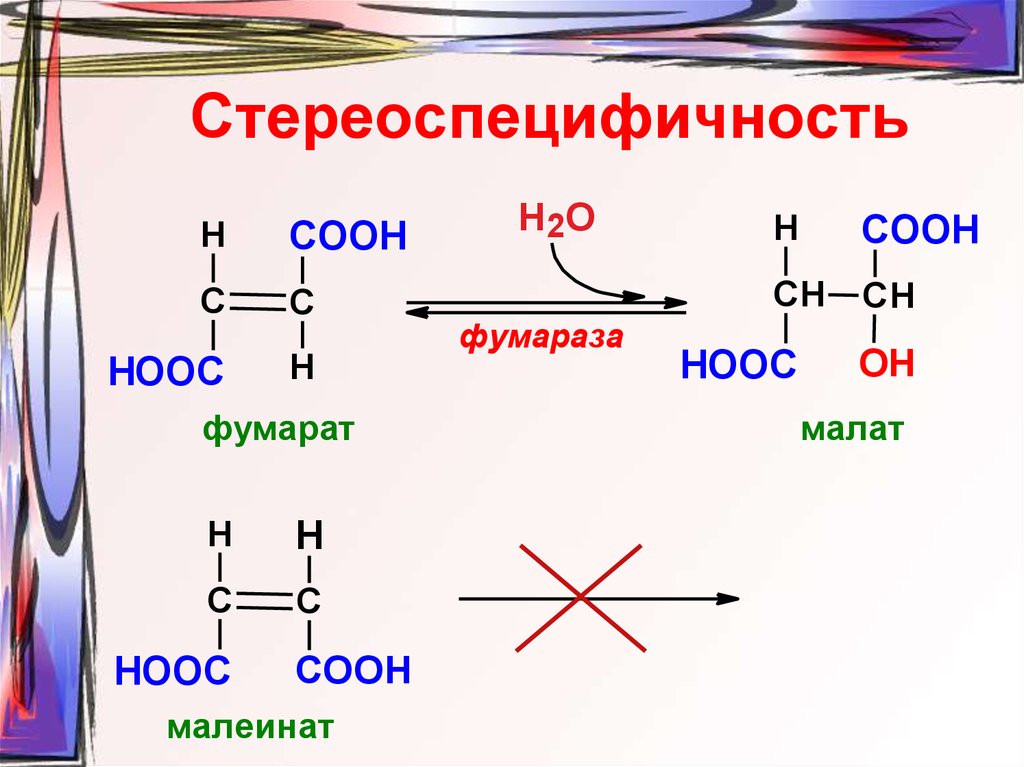
21. Стереоспецифичность
HCOOH
С
С
HOOC
H
фумарат
H
H
С
С
HOOC
COOH
малеинат
Н 2О
фумараза
H
COOH
СН
СН
HOOC
OH
малат
22. Общее уравнение ферментативной реакции:
E+Sk1
k2
ES
k3
EP
E+P
23. Константа Михаэлиса
24. Зависимость скорости ферментативной реакции от концентрации субстрата
25.
[S] >> Km; V = Vmax[S] << Km; V = Vmax [S] /Km
[S] = Km; V = ½ Vmax
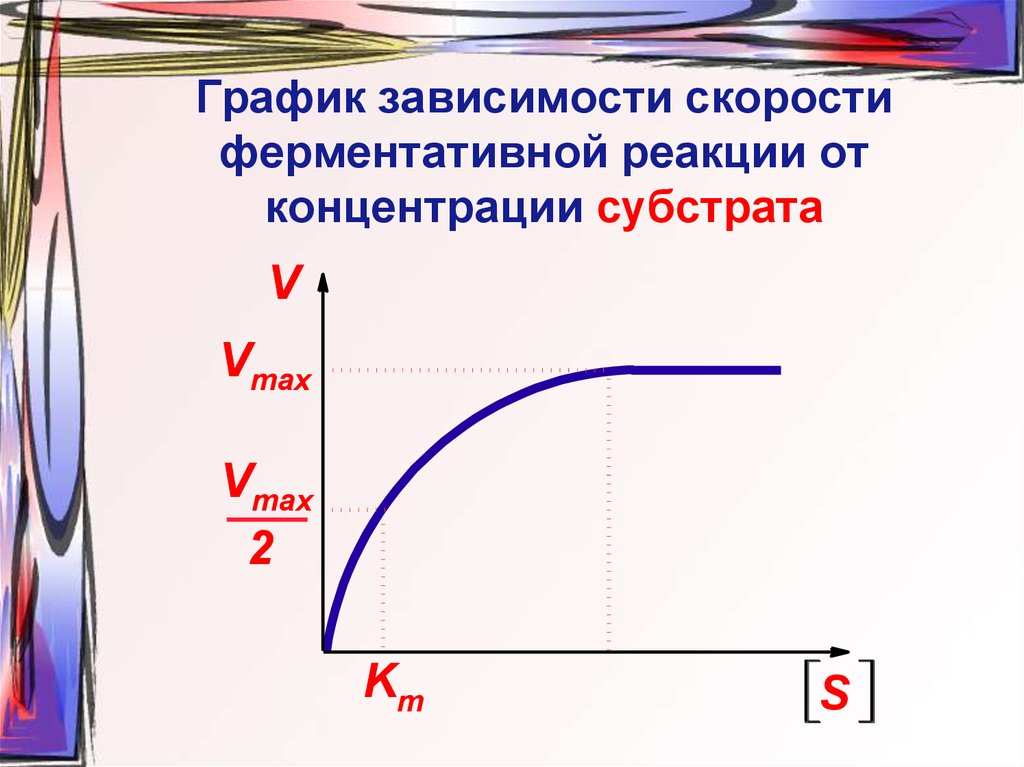
26. График зависимости скорости ферментативной реакции от концентрации субстрата
VVmax
Vmax
2
Km
S
27. Зависимости скорости ферментативной реакции от концентрации фермента
VE
28. Зависимость скорости ферментативной реакции от температуры
opt to≈ 40oC
29. Зависимость скорости ферментативной реакции от рН среды
Vплатообразная
зависимость
pH opt
pH
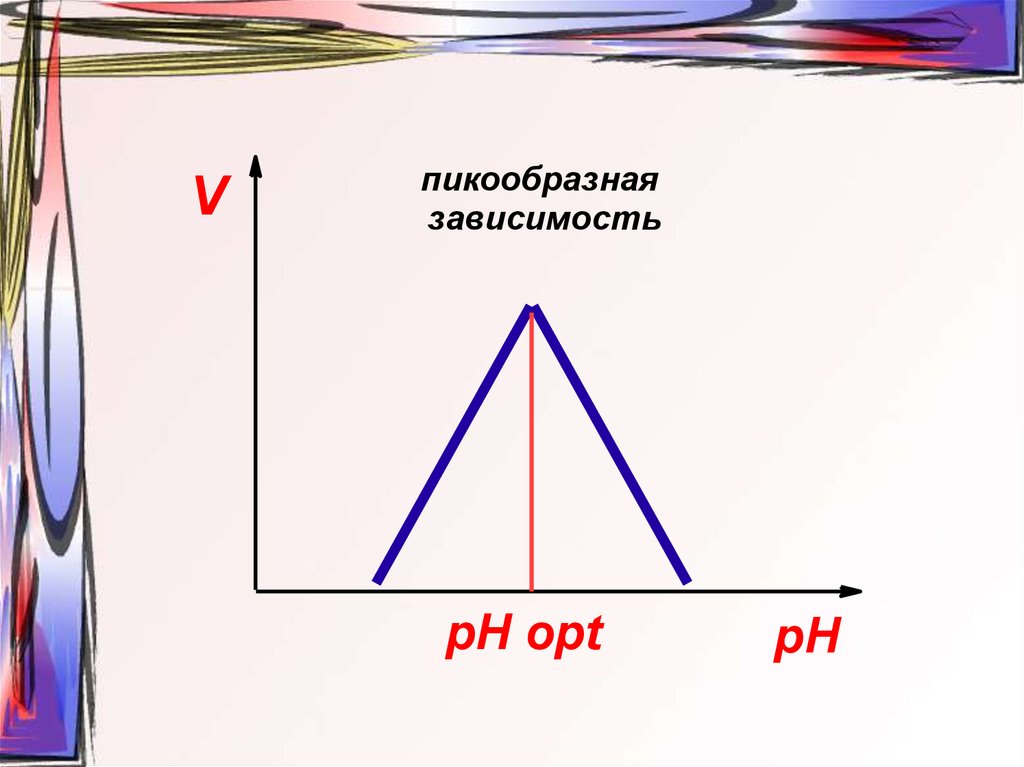
30.
Vпикообразная
зависимость
pH opt
pH
31.
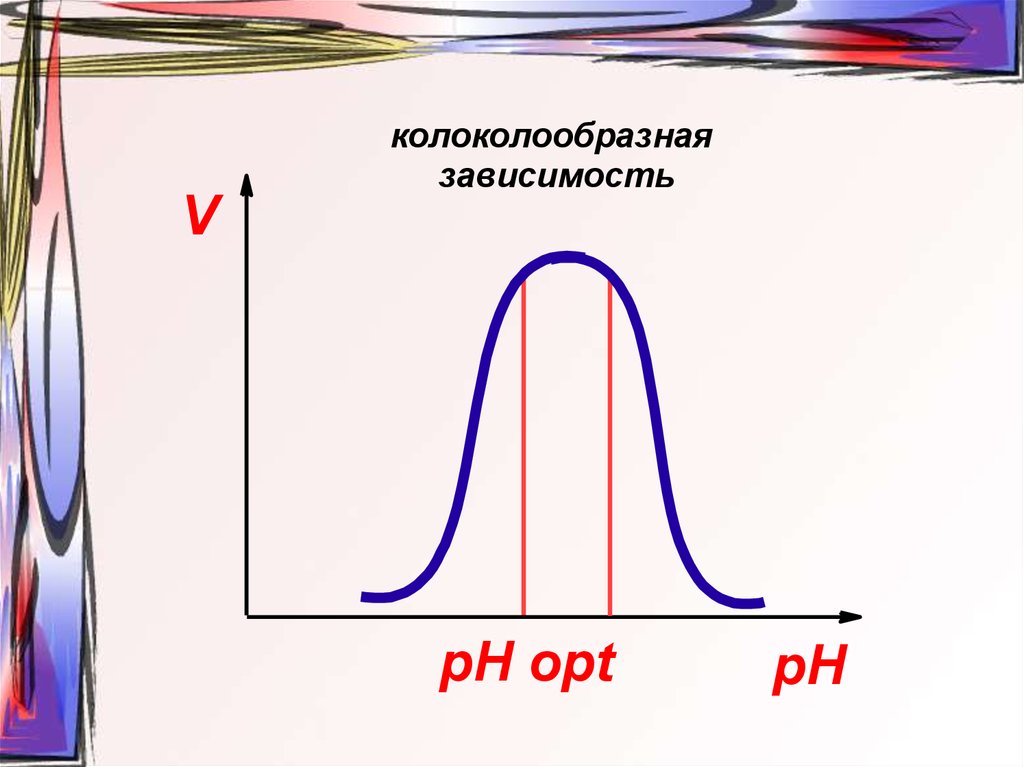
колоколообразнаязависимость
V
pH opt
pH
32. Оптимальное значение рН
Пепсин1,5-2,5
Трипсин
8,0-9,0
Сахараза
6,2
Мальтаза
6,1
Амилаза
≈ 7,0
Липаза
7,0-8,5
Фосфатаза
6,0-9,0
Аргиназа
9,8
Карбоксилаза
4,8















 Биология
Биология








