Похожие презентации:
Механизм развития атеросклеротической бляшки
1. Механизм развития атеросклеротической бляшки
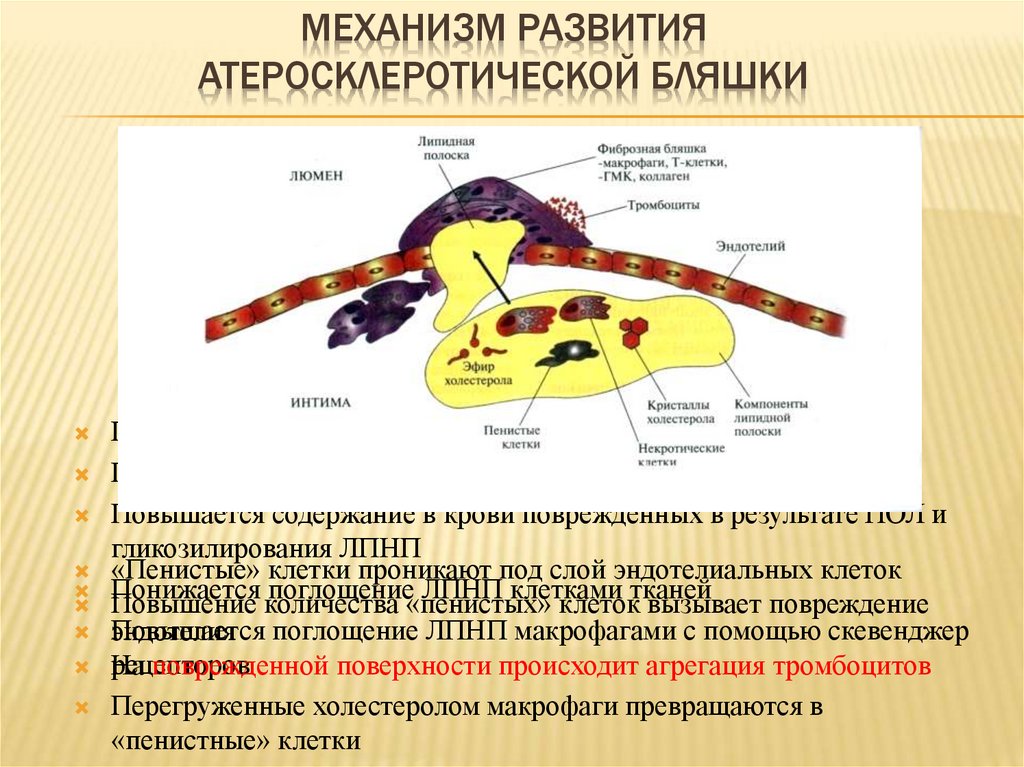
МЕХАНИЗМ РАЗВИТИЯАТЕРОСКЛЕРОТИЧЕСКОЙ БЛЯШКИ
Повышается содержание ЛПНП в крови
Повышается время жизни ЛПНП
Повышается содержание в крови поврежденных в результате ПОЛ и
гликозилирования ЛПНП
«Пенистые» клетки проникают под слой эндотелиальных клеток
Понижается поглощение ЛПНП клетками тканей
Повышение количества «пенистых» клеток вызывает повреждение
Повышается поглощение ЛПНП макрофагами с помощью скевенджер
эндотелия
рецепторов
На
поврежденной поверхности происходит агрегация тромбоцитов
Перегруженные холестеролом макрофаги превращаются в
«пенистные» клетки
2. Биохимические принципы профилактики и лечения атеросклероза
БИОХИМИЧЕСКИЕ ПРИНЦИПЫПРОФИЛАКТИКИ И ЛЕЧЕНИЯ АТЕРОСКЛЕРОЗА
Первичная
профилактика
начинается
с
момента
возникновения высокой вероятности развития осложнений
атеросклероза:
1. Коэффициент атерогенности Хобщ. - Хлпвп Хлпнп
Х лпвп
Хлпвп
2. Содерожание Хобщ. - не более 5,2 ммоль/л
Максимальное снижение факторов риска !
- не более 3,5
3. Биохимические принципы профилактики и лечения атеросклероза
БИОХИМИЧЕСКИЕ ПРИНЦИПЫПРОФИЛАКТИКИ И ЛЕЧЕНИЯ АТЕРОСКЛЕРОЗА
Вторичная профилактика начинается после осложнений атеросклероза
(инсульт, инфаркт миокарда и т.д.), по существу это лечебные мероприятия:
Изменение питания
Изменение
образа жизни
- снижение потребления
холестерина
Медикаментозное
лечение
- отказ
от курения
(никотин
ПОЛ,
в т.ч. ЛПНП)
снижение
калорийности
заповышает
счет жиров
и углеводов
- увеличение
полимеры, физической
адсорбирующие
желчные
кислоты
(холестид,
холестероламин
Эфферентные
методы лечения
нагрузки
(повышает
синтез
ЛПВП)
потребления
витаминов
с антиоксидантным
действием
(С, Е, Р, А) и
-др.)
гемосорбция,
плазмосорбция
снижение стрессорных
нагрузок
- ниацин и производные (снижают образование ЛПОНП)
- фибраты (клофебрат и др.) -повышают содержание ЛПВП
-препараты, содержащие полиненасыщенные жирные кислоты (омакора и др.)
(снижают риск тромбообразования)
- ингибиторы ГМГ-СоА-редуктазы – статины (мевакор, закор и др.)
4.
«Медицина есть прибавление и отнятие.Отнятие всего того, что изменено,
прибавление же недостающего.
И кто это лучше делает,
тот и наилучший врач»
ГИППОКРАТ
5. ОБМЕН ФОСФОЛИПИДОВ, кетоновых тел. Особенности обмена липидов в органах и тканях
ОБМЕН ФОСФОЛИПИДОВ, КЕТОНОВЫХ ТЕЛ.ОСОБЕННОСТИ ОБМЕНА ЛИПИДОВ
В ОРГАНАХ И ТКАНЯХ
6. Обмен кетоновых тел
ОБМЕН КЕТОНОВЫХ ТЕЛ7.
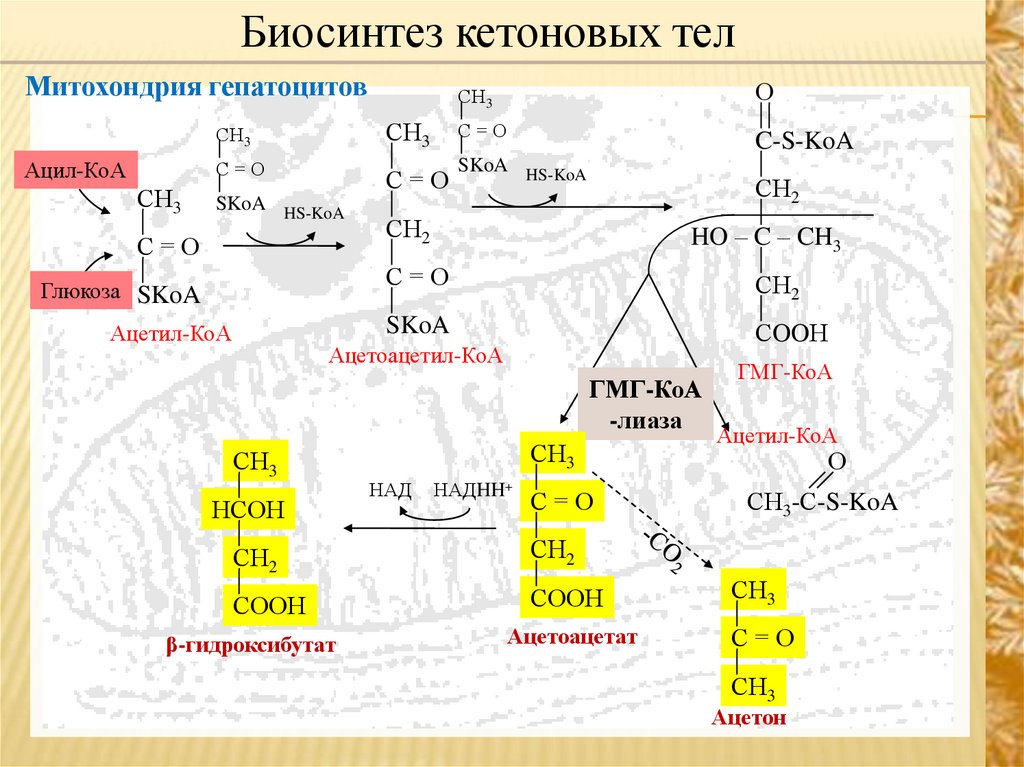
Биосинтез кетоновых телМитохондрия гепатоцитов
Ацил-КоА
СН3
О
СН3
СН3
СН3
С=О
С=О
С=О
SKoA HS-KoA
SKoA HS-KoA
С=О
Глюкоза SKoA
Ацетил-КоА
C-S-KoA
СН2
СН2
HO – C – CH3
С=О
СН2
SKoA
СOOН
Ацетоацетил-КоА
ГМГ-КоА
-лиаза
СН3
НСОН
СН3
НАД
НАДHH+
С=О
ГМГ-КоА
Ацетил-КоА
О
СН3-С-S-KoA
СН2
СН2
СООН
СООН
СН3
Ацетоацетат
С=О
β-гидроксибутат
СН3
Ацетон
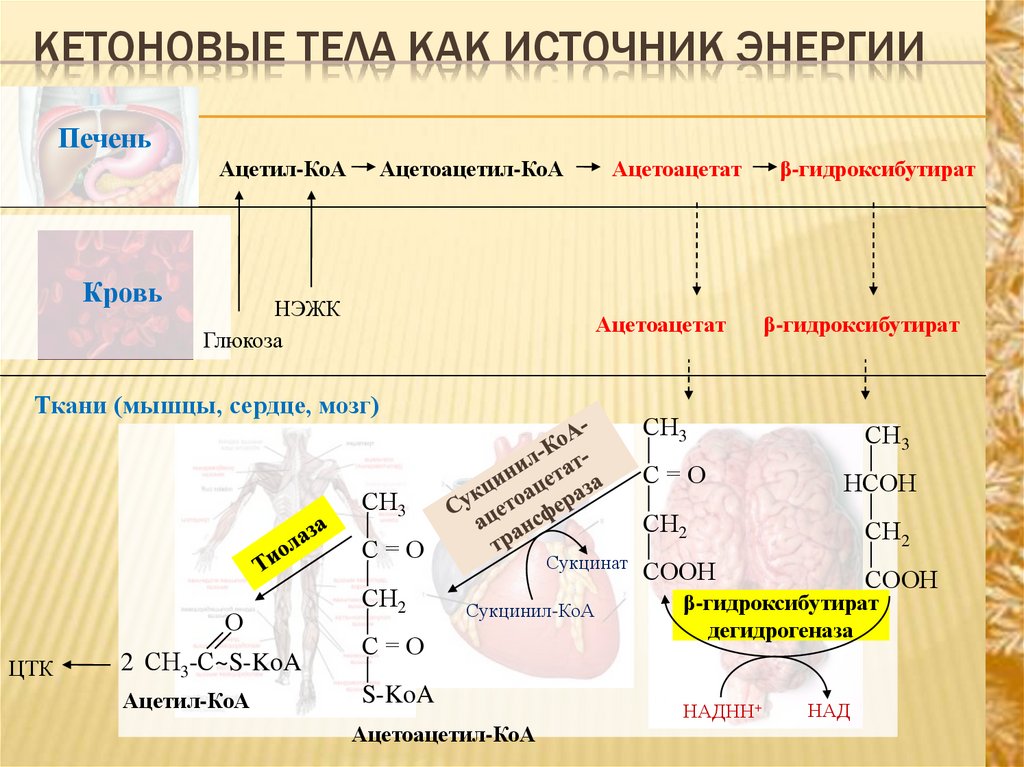
8. Кетоновые тела как источник энергии
КЕТОНОВЫЕ ТЕЛА КАК ИСТОЧНИК ЭНЕРГИИПечень
Ацетил-КоА
Кровь
Ацетоацетил-КоА
НЭЖК
Глюкоза
Ацетоацетат
Ацетоацетат
Ткани (мышцы, сердце, мозг)
СН3
С=О
О
ЦТК
2 СН3-С~S-KoA
Ацетил-КоА
СН2
Сукцинат
Сукцинил-КоА
С=О
S-KoA
Ацетоацетил-КоА
β-гидроксибутират
β-гидроксибутират
СН3
СН3
С=О
НСОН
СН2
СН2
СООН
СООН
β-гидроксибутират
дегидрогеназа
НАДНН+
НАД
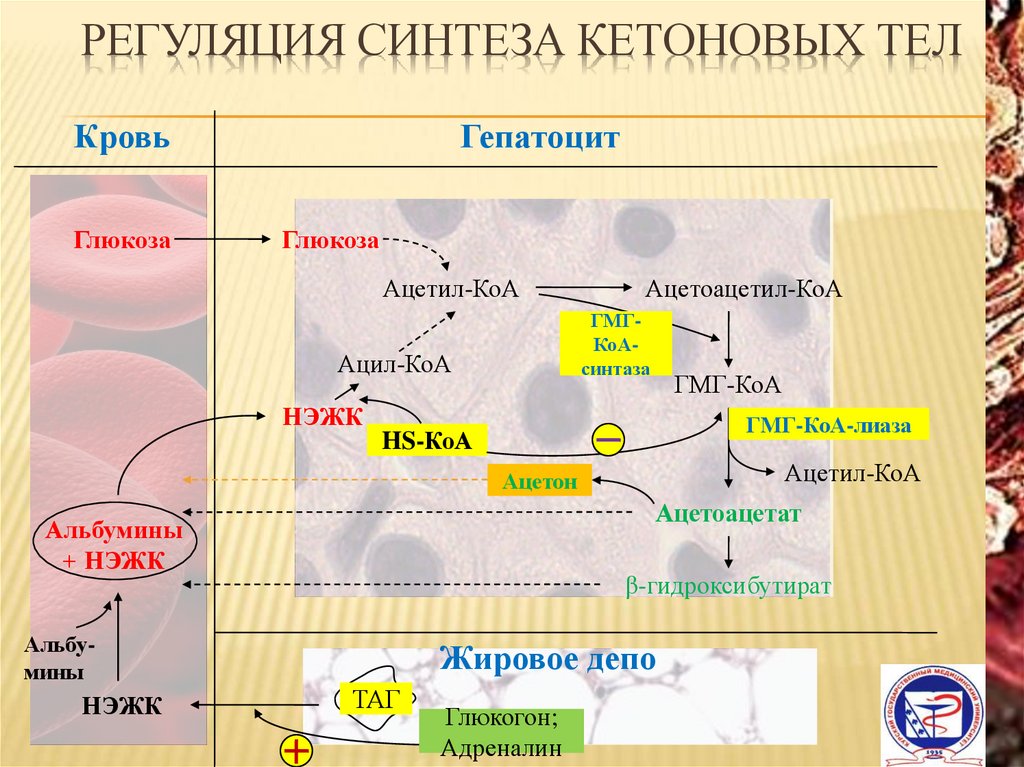
9. Регуляция синтеза кетоновых тел
РЕГУЛЯЦИЯ СИНТЕЗА КЕТОНОВЫХ ТЕЛКровь
Глюкоза
Гепатоцит
Глюкоза
Ацетил-КоА
Ацетоацетил-КоА
ГМГКоАсинтаза
Ацил-КоА
ГМГ-КоА
НЭЖК
ГМГ-КоА-лиаза
HS-КоА
Ацетил-КоА
Ацетон
Ацетоацетат
Альбумины
+ НЭЖК
β-гидроксибутират
Альбумины
НЭЖК
Жировое депо
ТАГ
Глюкогон;
Адреналин
10. Метаболизм фосфолипидов
МЕТАБОЛИЗМ ФОСФОЛИПИДОВ11.
Значение фосфолипидов (ГФЛ, СФЛ, ГЛ)В отличии от ТГ и ЖК, ФЛ не являются существенным
энергетическим материалом . ФЛ играют важную роль:
1. структура и функции клеточных мембран;
2. формирование липопротеидных комплексов;
3. активация мембранных и лизосомальных ферментов;
4. проведение нервных импульсов;
5. свертывание крови;
6. процессы клеточной пролиферации и регенерации
тканей;
12. Переваривание, всасывание и транспорт ГлицероФОСФОлипидов
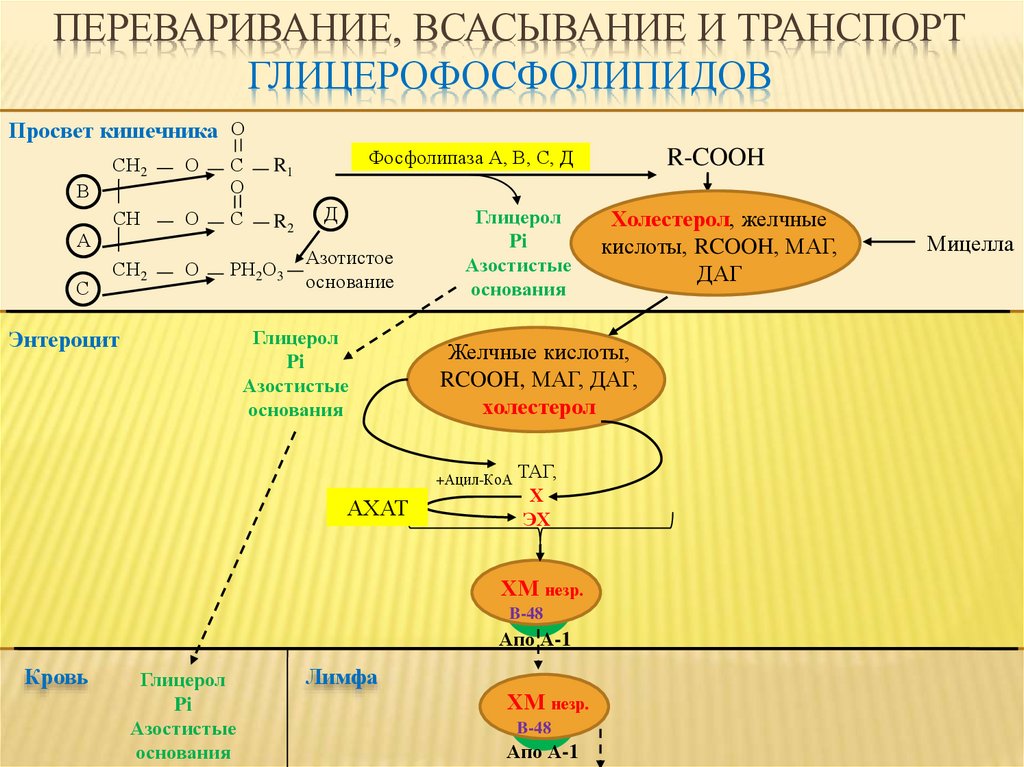
ПЕРЕВАРИВАНИЕ, ВСАСЫВАНИЕ И ТРАНСПОРТГЛИЦЕРОФОСФОЛИПИДОВ
Просвет кишечника О
СН2
О
С
О
R1
СН
О
С
R2
В
А
С
СН2
О
РН2О3
Фосфолипаза А, В, С, Д
Д
Азотистое
основание
Глицерол
Pi
Азостистые
основания
Энтероцит
Глицерол
Pi
Азостистые
основания
Х
ЭХ
ХМ незр.
B-48
Апо А-1
Кровь
Глицерол
Pi
Азостистые
основания
Холестерол, желчные
кислоты, RCOOH, МАГ,
ДАГ
Желчные кислоты,
RCOOH, МАГ, ДАГ,
холестерол
+Ацил-КоА ТАГ,
АХАТ
R-COOH
Лимфа
ХМ незр.
B-48
Апо А-1
Мицелла
13.
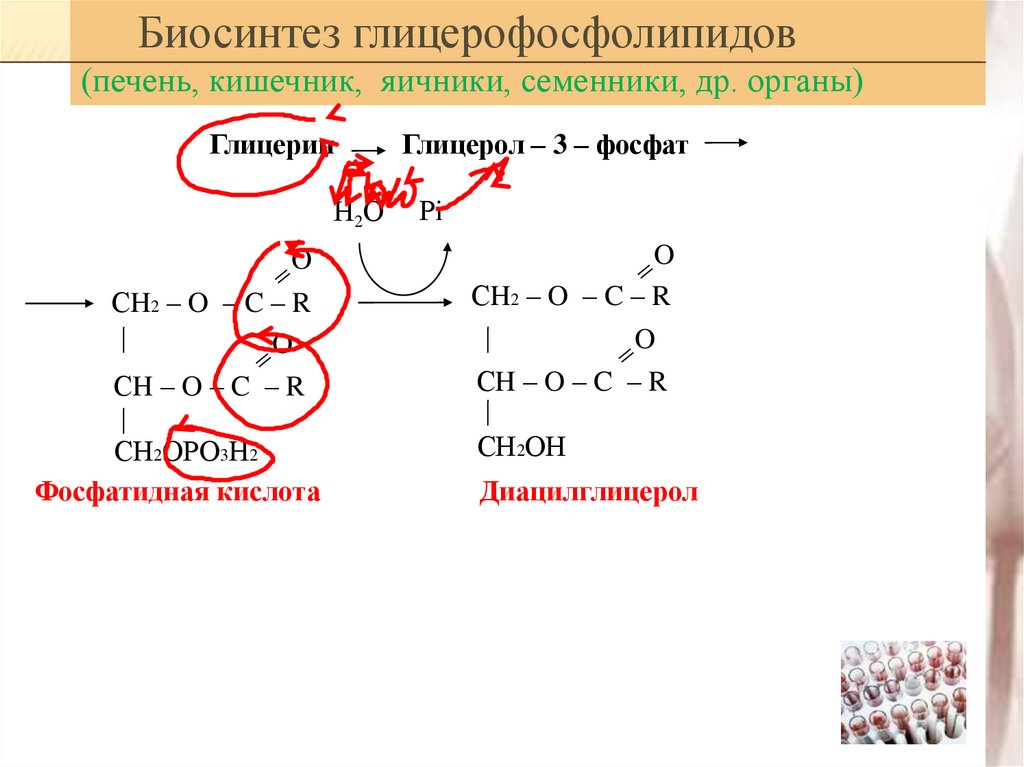
Биосинтез глицерофосфолипидов(печень, кишечник, яичники, семенники, др. органы)
Глицерин
Н2О
O
СH2 – O – C – R
O
СH – O – C – R
СН2ОРО3Н2
Фосфатидная кислота
Глицерол – 3 – фосфат
Рi
O
СH2 – O – C – R
O
СH – O – C – R
СН2ОН
Диацилглицерол
14.
OСH2 – O – C – R
O
СH – O – C – R
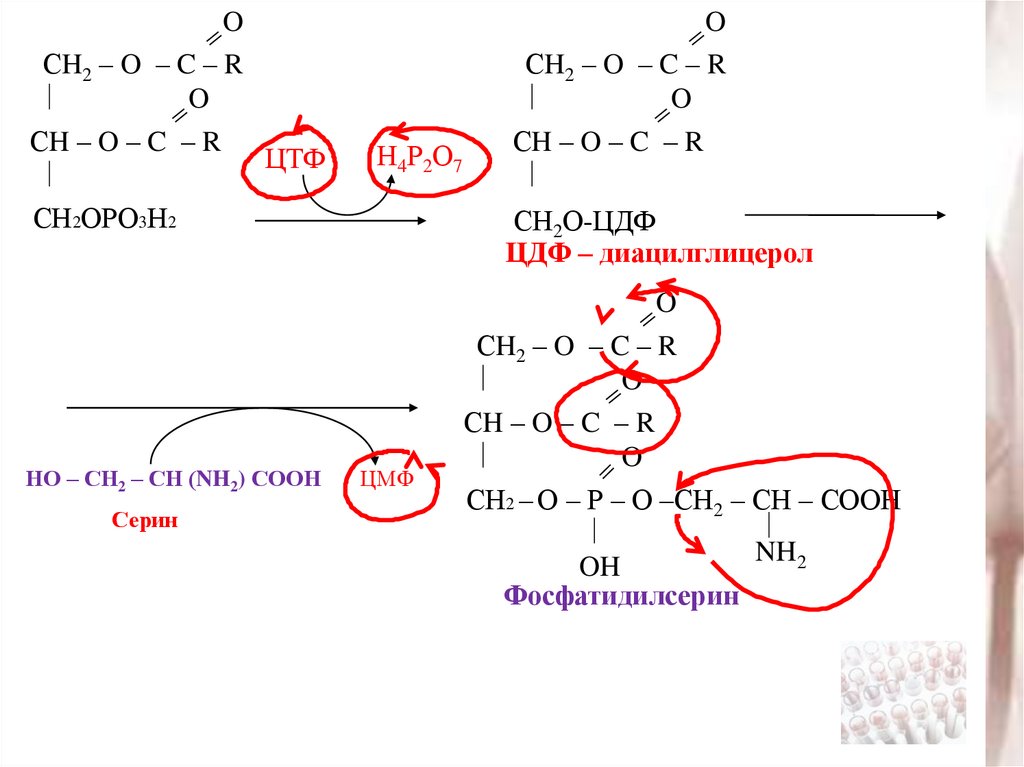
ЦТФ
Н 4 Р2 О 7
СН2ОРО3Н2
НО – СН2 – СН (NH2) СООН
Серин
O
СH2 – O – C – R
O
СH – O – C – R
СН2О-ЦДФ
ЦДФ – диацилглицерол
ЦМФ
O
СH2 – O – C – R
O
СH – O – C – R
O
СН2 – О – Р – О –СН2 – СН – СООН
OH
Фосфатидилсерин
NH2
15.
OR O P O
OH
CH2 CH COOH
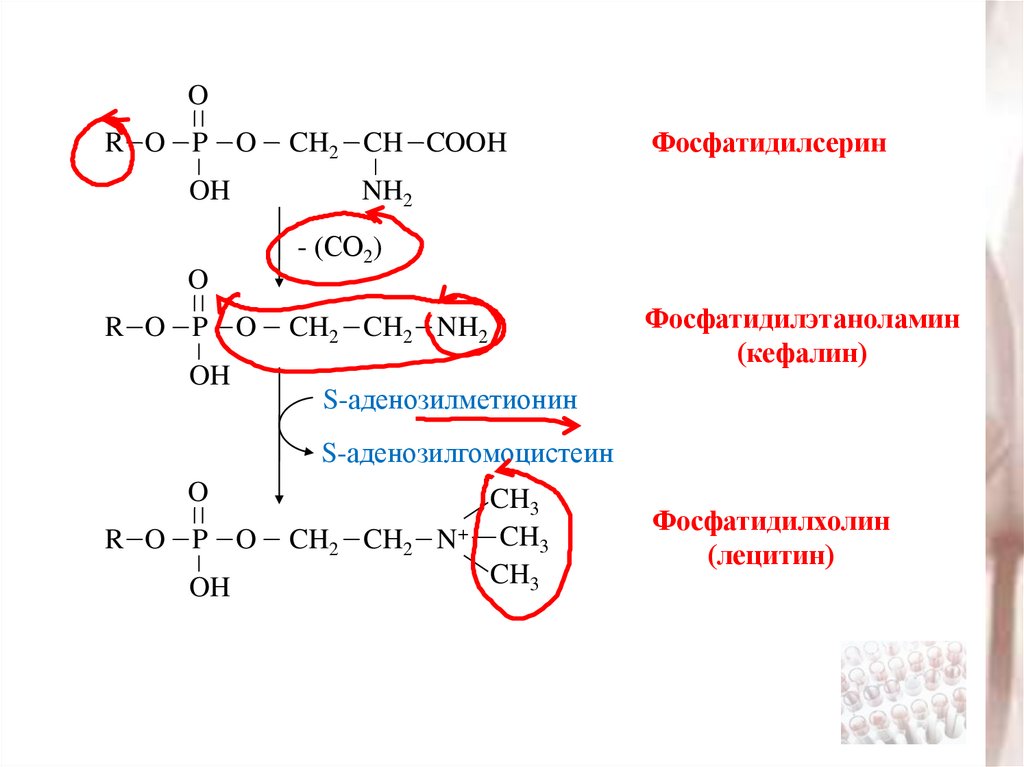
Фосфатидилсерин
NH2
- (СО2)
O
R O P O
OH
Фосфатидилэтаноламин
(кефалин)
CH2 CH2 NH2
S-аденозилметионин
S-аденозилгомоцистеин
O
R O P O
OH
CH2 CH2 N+
CH3
CH3
CH3
Фосфатидилхолин
(лецитин)
16.
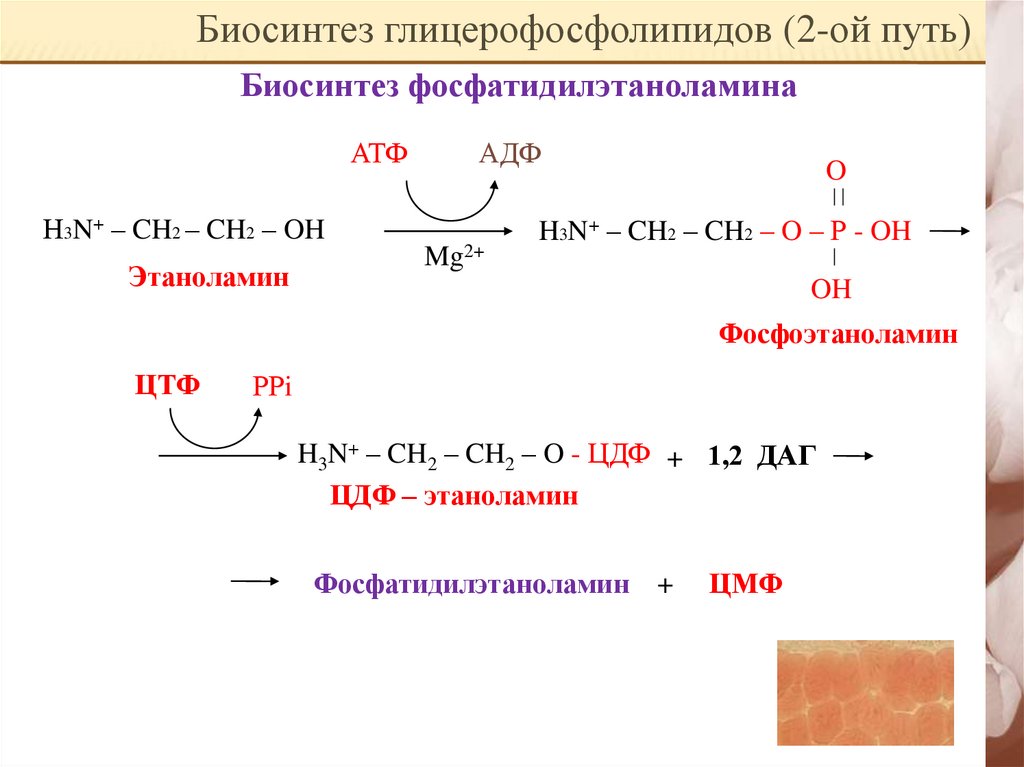
Биосинтез глицерофосфолипидов (2-ой путь)Биосинтез фосфатидилэтаноламина
АТФ
Н3N+ – CH2 – CH2 – OH
Этаноламин
АДФ
Mg2+
O
H3N+ – CH2 – CH2 – O – Р - OH
OH
Фосфоэтаноламин
ЦТФ
РРi
H3N+ – CH2 – CH2 – O - ЦДФ + 1,2 ДАГ
ЦДФ – этаноламин
Фосфатидилэтаноламин +
ЦМФ
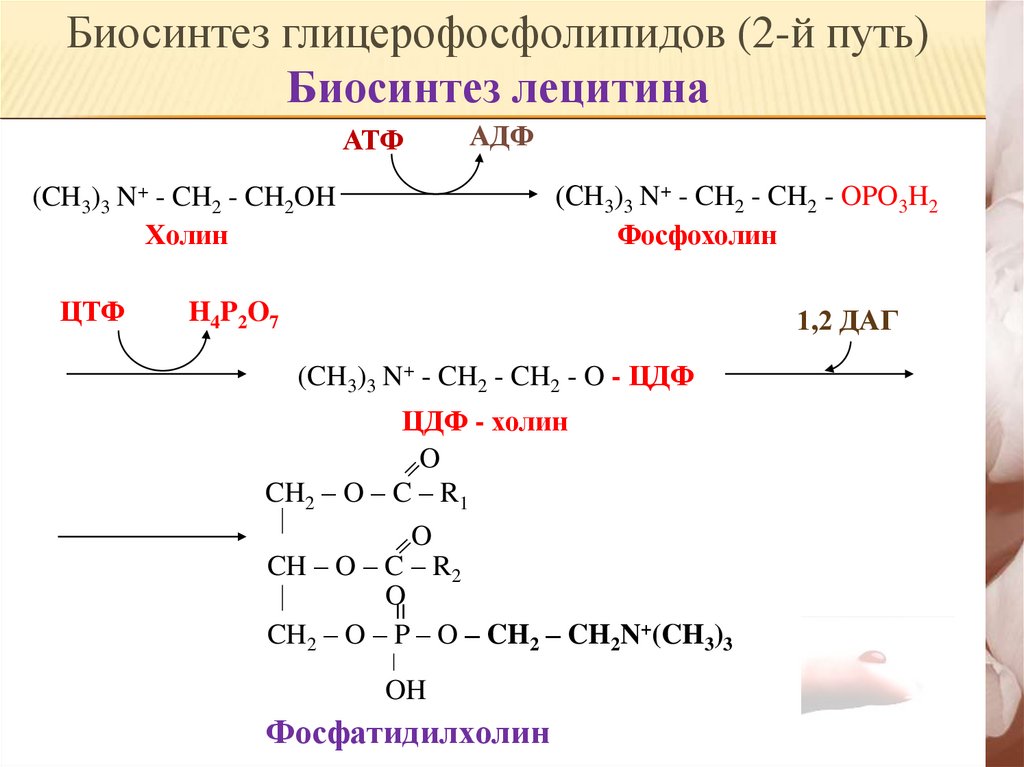
17.
Биосинтез глицерофосфолипидов (2-й путь)Биосинтез лецитина
АТФ
АДФ
(СH3)3 N+ - CH2 - CH2 - OPO3H2
Фосфохолин
(CH3)3 N+ - CH2 - CH2OH
Холин
H4P2O7
1,2 ДАГ
(CH3)3 N+ - CH2 - CH2 - O - ЦДФ
ЦДФ - холин
O
CH2 – O – C – R1
O
CH – O – C – R2
O
CH2 – O – P – O – CH2 – CH2N+(CH3)3
=
ЦТФ
OH
Фосфатидилхолин
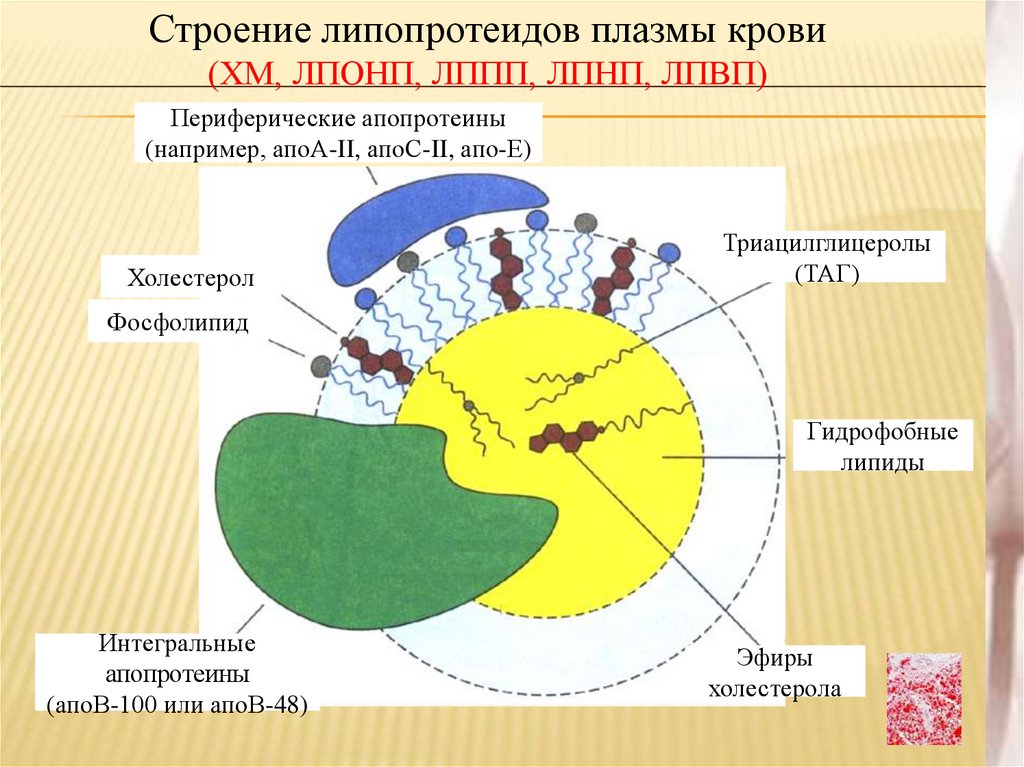
18.
Строение липопротеидов плазмы крови(ХМ, ЛПОНП, ЛППП, ЛПНП, ЛПВП)
Периферические апопротеины
(например, апоА-II, апоС-II, апо-Е)
Холестерол
Триацилглицеролы
(ТАГ)
Фосфолипид
Гидрофобные
липиды
Интегральные
апопротеины
(апоВ-100 или апоВ-48)
Эфиры
холестерола
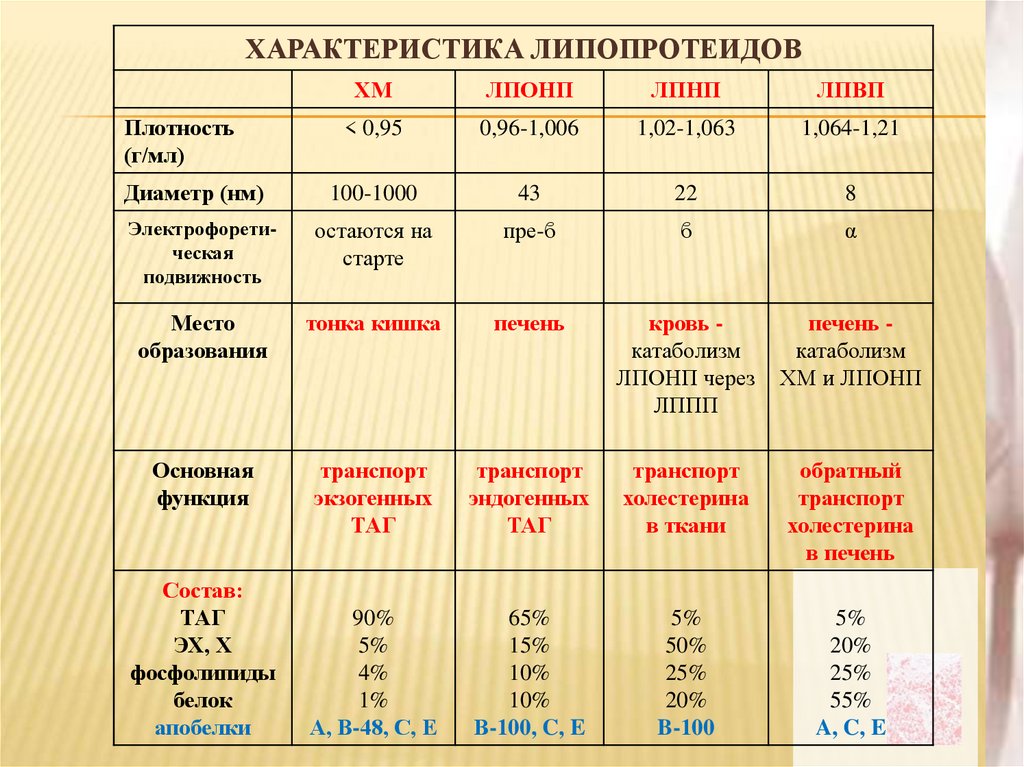
19.
ХАРАКТЕРИСТИКА ЛИПОПРОТЕИДОВХМ
ЛПОНП
ЛПНП
ЛПВП
Плотность
(г/мл)
< 0,95
0,96-1,006
1,02-1,063
1,064-1,21
Диаметр (нм)
100-1000
43
22
8
Электрофоретическая
подвижность
остаются на
старте
пре-ϐ
ϐ
α
Место
образования
тонка кишка
печень
кровь катаболизм
ЛПОНП через
ЛППП
печень катаболизм
ХМ и ЛПОНП
Основная
функция
транспорт
экзогенных
ТАГ
транспорт
эндогенных
ТАГ
транспорт
холестерина
в ткани
обратный
транспорт
холестерина
в печень
90%
5%
4%
1%
А, В-48, С, Е
65%
15%
10%
10%
В-100, C, E
5%
50%
25%
20%
B-100
5%
20%
25%
55%
A, C, E
Состав:
ТАГ
ЭХ, Х
фосфолипиды
белок
апобелки
20.
ОСОБЕННОСТИ ОБМЕНАЛИПИДОВ В ОРГАНАХ И ТКАНЯХ
21. Особенности обмена липидов в органах и тканях
Печень1. Обмен холестерола
- синтез эндогенного холестерола;
- катаболизм холестерола из тканей и органов;
- образование холестеридов
2. Биосинтез ЛПОНП и ЛПВП
3. Образование глицерофосфолипидов
(серинфосфолипиды, этаноламинофосфосфолипиды–
кефалины, холинфосфолипиды – лецитины)
4. Обмен желчных кислот (биосинтез, выведение, обратное всасывание)
5. Утилизация ХМост. и ЛПВПз
6. Обмен НЭЖК (биосинтез на экспорт, катаболизм неиспользованных
жирных кислот (с короткой углеродной цепью, полиненысыщенных, с
нечетным числом углеродных атомов)
7. Биосинтез ТАГ на экспорт
8. Синтез кетоновых тел
22.
Жировая ткань(сальник, брыжейка, подкожная клетчатка, костный мозг).
До 90% массы жировой ткани – ТАГ.
Более 50% в ТАГ - олеиновая и линолевая жирные кислоты
1. Синтез жирных кислот в период изобилия
2. Источник энергии (в период покоя и работы средней
продолжительной интенсивности)
3. Изолирование внутренних органов от переохлаждения и
перегревания
4. Механическая функция (предохранение от ушибов,
повреждений)
5. Сглаживание острых углов скелета («эстетические
функции»)
6. Синтез ТАГ (из собственных и НЭЖК транспортных
липопротеидов (ХМзр., ЛПНП – ТАГ, НЭЖК+альбумины)
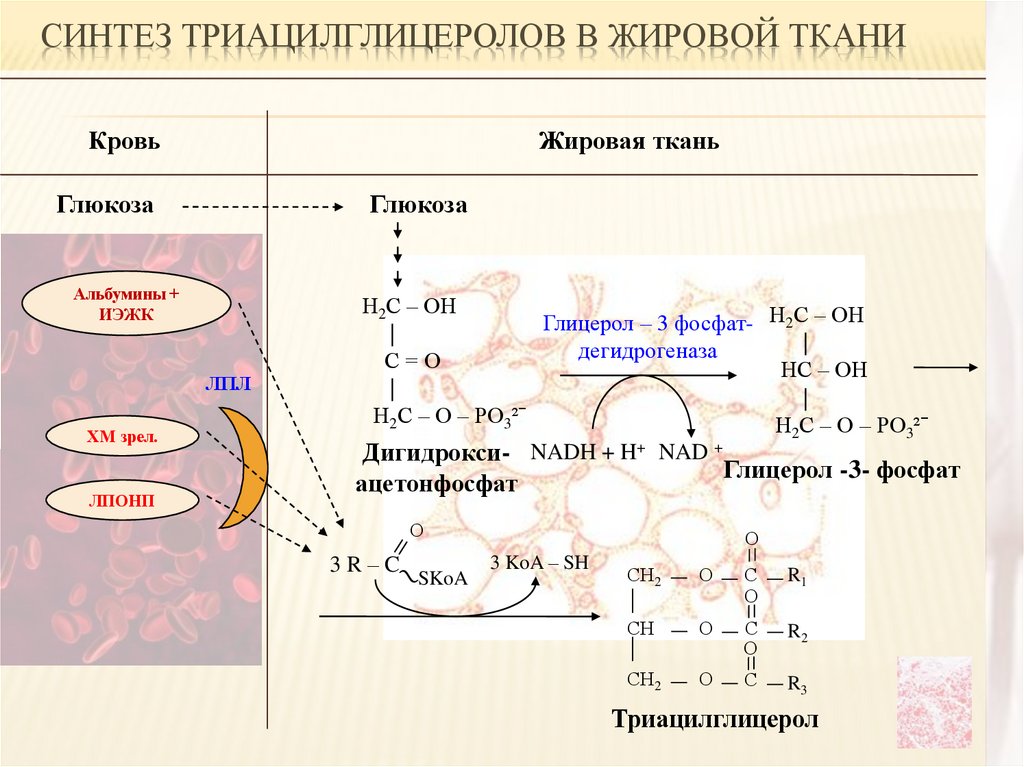
23.
СИНТЕЗ ТРИАЦИЛГЛИЦЕРОЛОВ В ЖИРОВОЙ ТКАНИКровь
Жировая ткань
Глюкоза
Глюкоза
Альбумины +
ИЭЖК
ЛПЛ
ХМ зрел.
ЛПОНП
Н2С – ОН
Глицерол – 3 фосфат- Н2С – ОН
|
|
дегидрогеназа
С=О
НС – ОН
|
|
Н2С – О – РО3²ˉ
Н С – О – РО ²ˉ
Дигидроксиацетонфосфат
2
NADH + H+
NAD +
О
3R–C
SKoA
Глицерол -3- фосфат
О
3 KoA – SH
3
СН2
О
С
О
R1
СН
О
С
О
R2
СН2
О
С
R3
Триацилглицерол
24.
Мышцы1. Окисление жирных кислот для обеспечения энергии в
период покоя и в условиях длительной работы средней
интенсивности (вместе с углеводами), причем чем
длительнее работа, тем больше используются жирные
кислоты.
2. Сердечная мышца и гладкие мышечные волокна
сосудистой стенки используют как энергетический
материал НЭЖК в большей степени чем глюкозу.
3. Окисление кетоновых тел как энергетического
материала.
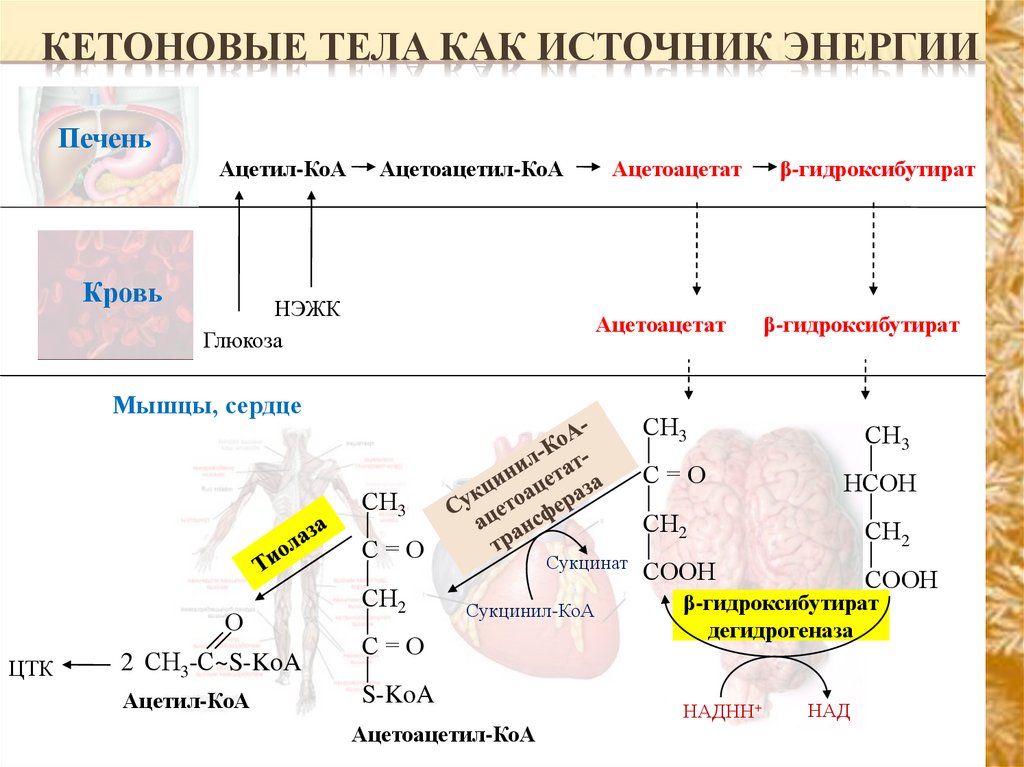
25. Синтез триацилглицеролов в жировой ткани
КЕТОНОВЫЕ ТЕЛА КАК ИСТОЧНИК ЭНЕРГИИПечень
Ацетил-КоА
Кровь
Ацетоацетил-КоА
НЭЖК
Глюкоза
Ацетоацетат
Ацетоацетат
Мышцы, сердце
СН3
С=О
О
ЦТК
2 СН3-С~S-KoA
Ацетил-КоА
СН2
Сукцинат
Сукцинил-КоА
С=О
S-KoA
Ацетоацетил-КоА
β-гидроксибутират
β-гидроксибутират
СН3
СН3
С=О
НСОН
СН2
СН2
СООН
СООН
β-гидроксибутират
дегидрогеназа
НАДНН+
НАД
26.
Нервная ткань1. Энергетические
потребности
нервной
ткани
обеспечиваются на 95-97% за счет окисления глюкозы и
3-5% за счет окисления кетоновых тел (в период покоя, при
голодании резко увеличивается).
2. Липиды составляют до 50% от массы нервной ткани
- липиды серого вещества входят в состав мембран
нейронов (особенно их состав не отличается от состава
клеточных мембран других органов и тканей)
- липиды белого вещества (миелиновый футляр) состоят
из холестерола, фофолипидов (глицерофосфолипиды и
сфингофосфолипиды) и гликолипиды.
3. Все сложные липиды нервной ткани синтезируются из
глюкозы, НЭЖК и других низкомолекулярных продуктов.
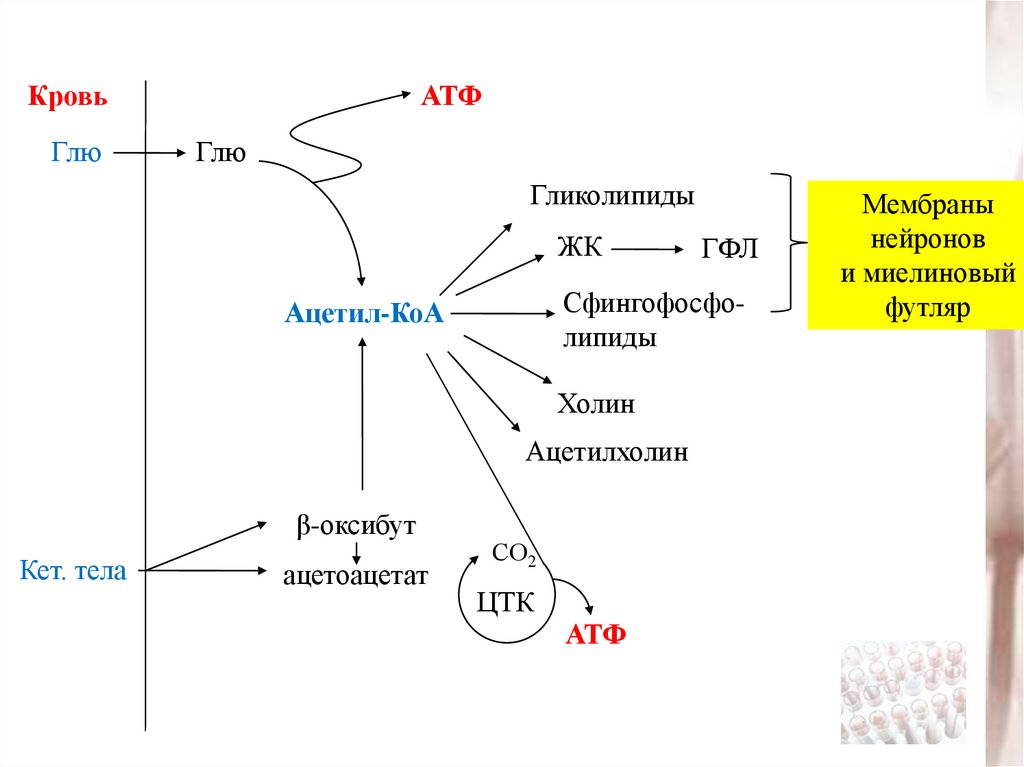
27. Кетоновые тела как источник энергии
КровьГлю
АТФ
Глю
Гликолипиды
ЖК
Сфингофосфолипиды
Ацетил-КоА
Холин
Ацетилхолин
β-оксибут
Кет. тела
ацетоацетат
ГФЛ
СО2
ЦТК
АТФ
Мембраны
нейронов
и миелиновый
футляр












 Медицина
Медицина








