Похожие презентации:
Аминокислоты
1.
2.
Аминокислоты – бифункциональныесоединения, которые обязательно содержат
две функциональные группы: аминогруппу
– NH2 и карбоксильную группу – COOH,
связанные с углеводородным радикалом
Аминокислоты – производные кислот,
которые можно рассматривать как
продукты замещения одного или более
атомов водорода в их радикалах на одну или
более аминогрупп
3.
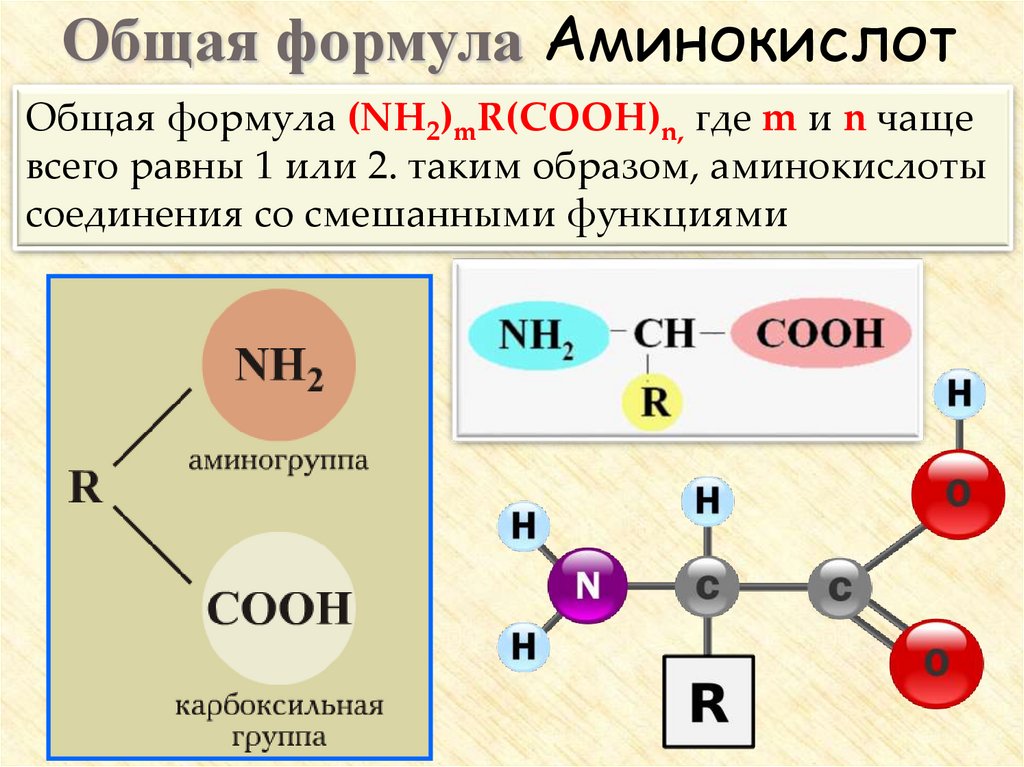
Общая формула АминокислотОбщая формула (NH2)mR(COOH)n, где m и n чаще
всего равны 1 или 2. таким образом, аминокислоты
соединения со смешанными функциями
4.
5.
моноаминомонокарбоновые кислоты;диаминомонокарбоновые кислоты
моноаминодикарбоновые кислоты
6.
α –аминокислоты, β – аминокислоты, γаминокислоты, δ – аминокислоты, ε – аминокислотыи т.д.
7.
ПредельныеНепредельные
Циклические
Ароматические
8.
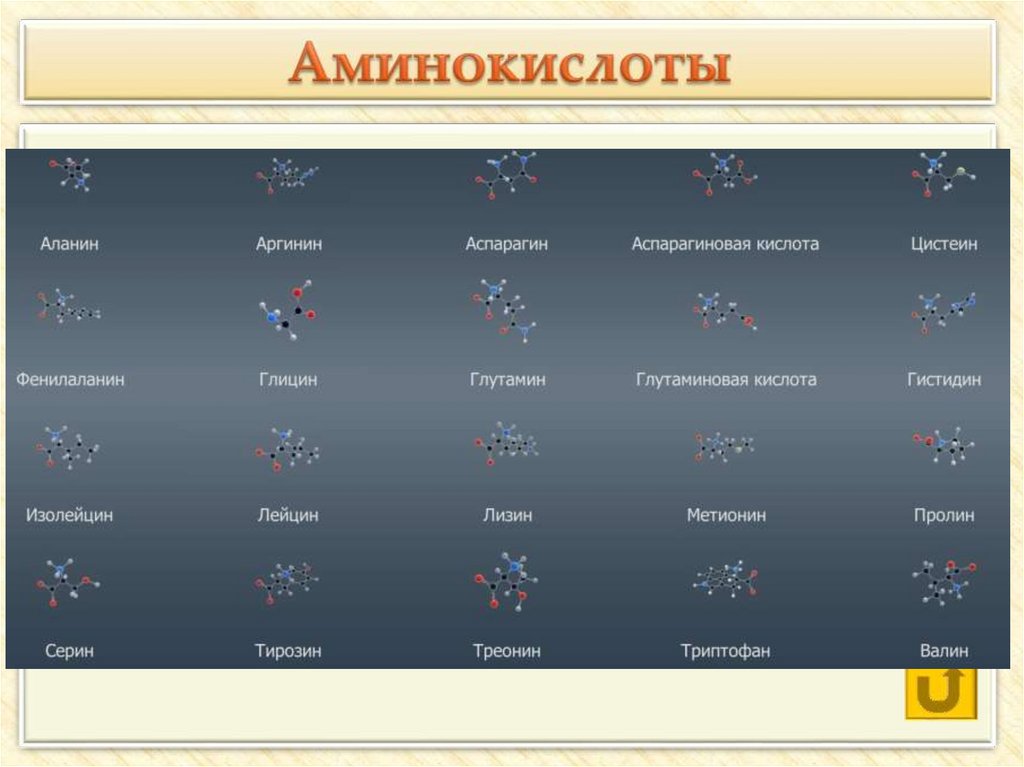
• ПриродныеИх около 150, они
были обнаружены в
живых организмах,
около 20 из них входят
в состав белков.
Половина этих
аминокислот –
незаменимые (не
синтезируются в
организме человека),
они поступают с
пищей.
• Синтетические
Получают кислотным
гидролизом белков,
либо из карбоновых
кислот, воздействуя
на них галогенном и,
далее, аммиаком.
9.
α-аминокислоты10.
СистематическаяРациональная
Тривиальное
11.
1. выбрать самую длинную цепь содержащуюкарбоксильную группу и аминогруппу;
2. пронумеровать начиная с углерода
карбоксильной группы;
3. Место (NH2) – сколько – амино – место R –
сколько –какая – овая кислота
Например: 2-аминопропановая кислота
12.
По рациональной номенклатуре положениеаминогруппы указывается буквами греческого
алфавита, начиная со второго атома углерода
от - СООН: α, β, γ, δ, ε и т.д. Например:
α – аминопропионовая кислота
13.
Многие аминокислоты имеют тривиальныеназвания, например:
Аланин
14.
Историческисложившиеся названия аминокислот.
δ
γ
CH2
CH
β
2 CH2
α
CH
COOH
NH2
α- аминовалериановая кислота
15.
16.
17.
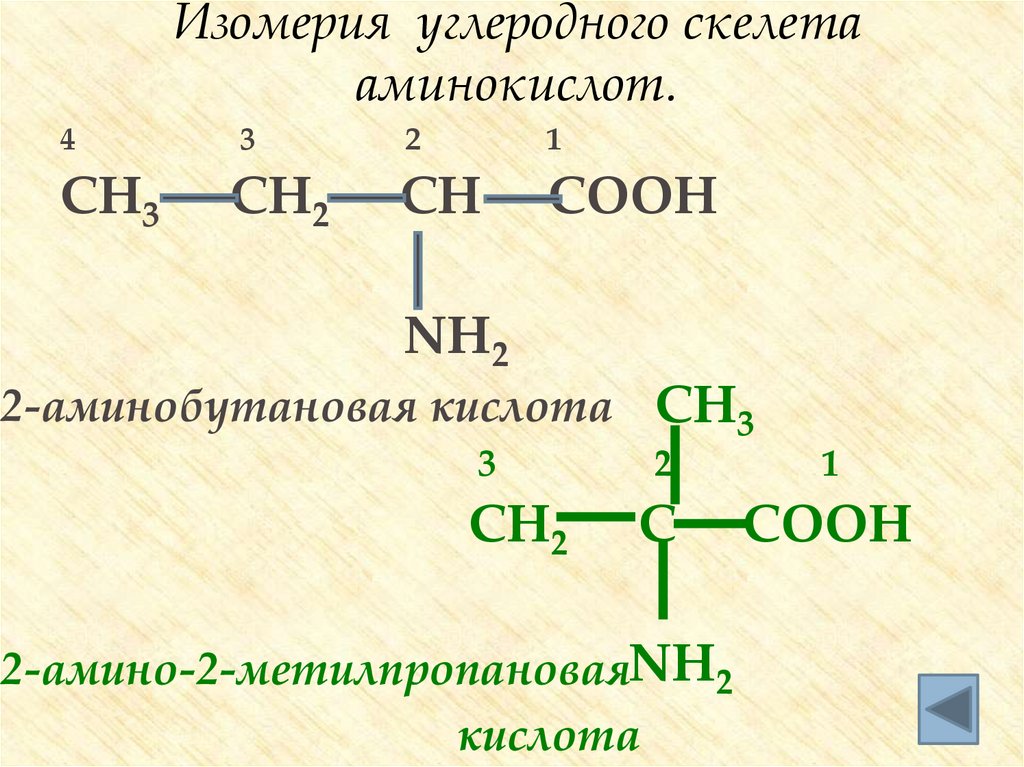
Изомерия углеродного скелетааминокислот.
4
3
2
1
CH3
CH2
CH
COOH
NH2
2-аминобутановая кислота CH3
3
2
1
CH2
C
COOH
2-амино-2-метилпропановаяNH2
кислота
18.
(С≥4), например; С4H9NO2β- аминомаслянная кислота
(3-аминобутановая)
α - амино - αметилпропионовая кислота
(2-амино-2метилпропановая
кислота)
19.
(С≥3), например; С3H7NO2β-аминопропионовая
кислота
(3-аминопропановая
кислота)
α-аминопропионовая
кислота
(2-аминопропановая
кислота)
20.
Изомерия положения аминогруппы.4
3
2
1
CH3
CH2
CH2
COOH
NH2
2-аминобутановая кислота.
4
3
CH3
CH2
NH2
1
2
CH2
COOH
3-аминобутановая кислота.
21.
(С≥2), например; С3H7NO21-нитропропан
2-аминопропановая
кислота
22.
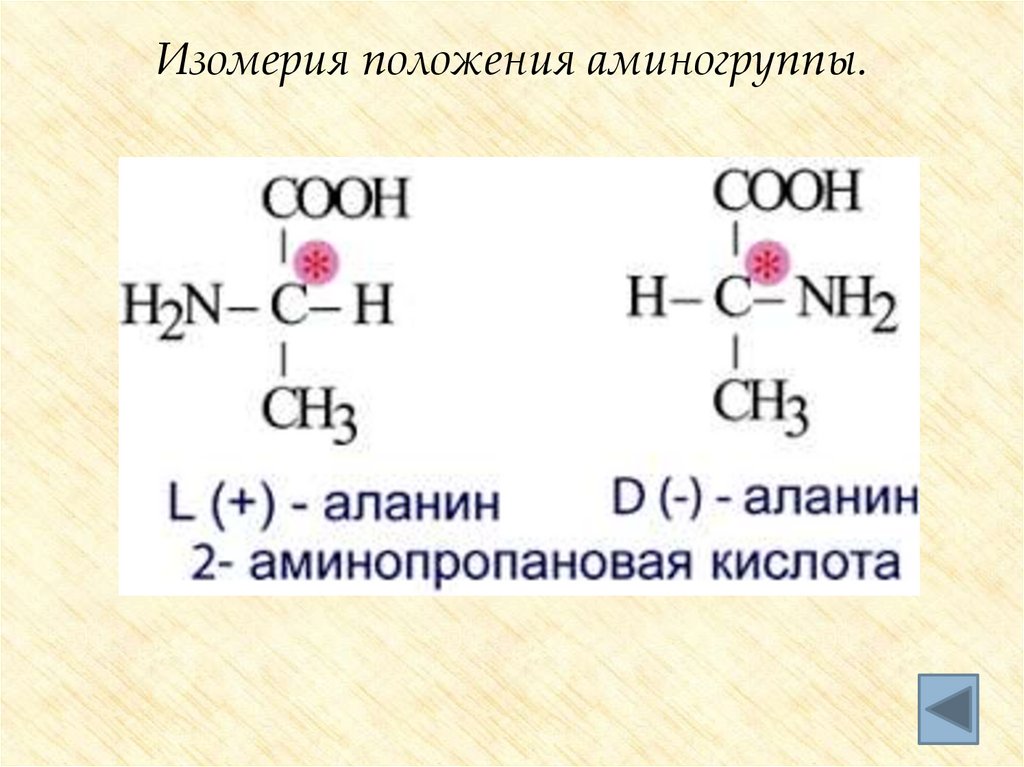
Стереоизомерияα - Аминокислоты - хиральные соединения.
Исключение составляет глицин
Относительная конфигурация - аминокислот
определяется по положению –NН2 группы.
Расположение аминогруппы слева соответствует L конфигурации, справа - D - конфигурации.
Почти все природные - аминокислоты
принадлежат к L - ряду.
23.
Изомерия положения аминогруппы.24.
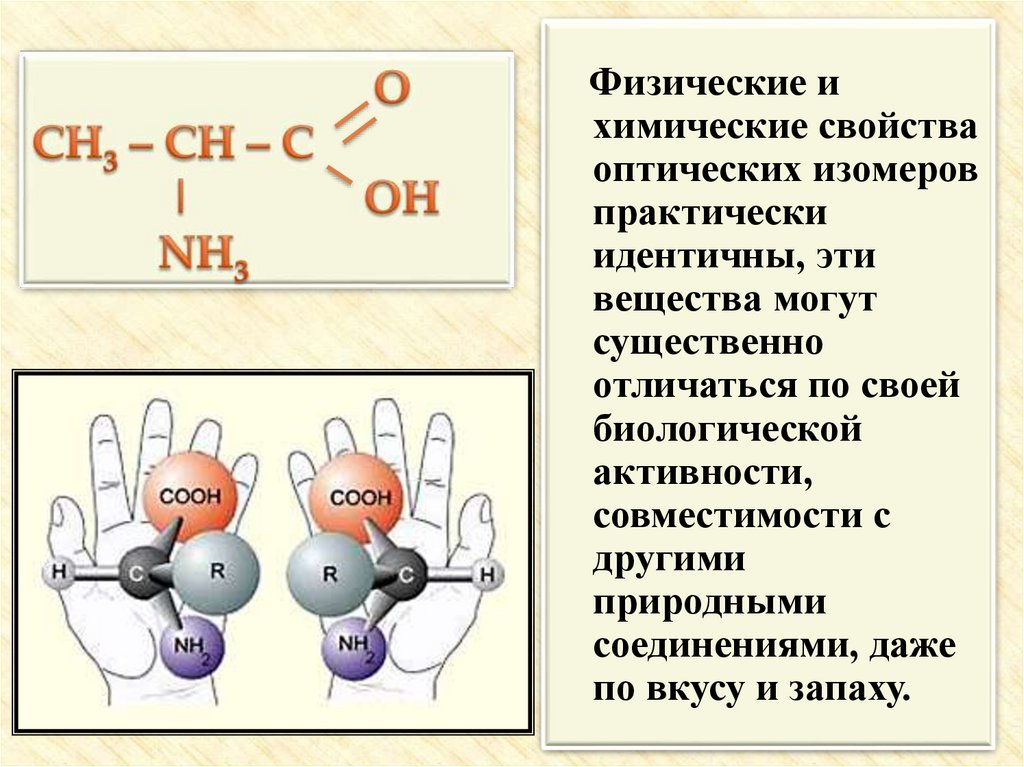
25.
Физические ихимические свойства
оптических изомеров
практически
идентичны, эти
вещества могут
существенно
отличаться по своей
биологической
активности,
совместимости с
другими
природными
соединениями, даже
по вкусу и запаху.
26.
Аминокислоты – бесцветные кристаллическиевещества с высокими температурами
плавления. Плавятся с разложением,
нелетучие. Хорошо растворимы в воде и плохо
растворимы во многих органических
растворителях, водные растворы
электропроводны
В большинстве аминокислоты D-ряда сладкие
на вкус, L-ряда горькие или безвкусные.
27.
28.
С активными металламиОксидами металлов
Гидроксидами металлов
С солями слабых летучих кислот
Со спиртами
29.
1. Mg + 2NH2 – CH2 – COOH → (NH2 – CH2 – COO)2Mg + H2Глицинат магния
2. MgO + 2NH2 – CH2 – COOH → (NH2 – CH2 – COO)2Mg +
H2O
3. 2Na + 2NH2 – CH2 – COOH → 2NH2 – CH2 – COONa + H2 ↑
Глицинат натрия
4. Na2CO3 + 2NH2 – CH2 – COOH → 2NH2 – CH2 – COONa +
H2O + CO2↑
H2SO4 (к)
5. NH2 – CH2 – COOH + HOC2H5 ↔ NH2 – CH2 – CO - OC2H5
этиловый эфир аминоуксусной кислоты
+ H2O
30.
6. Взаимодействие аминокислот со щелочами.H2N–CH2–COOH + HCl → [H3N+–CH2–COOH] Cl-
31.
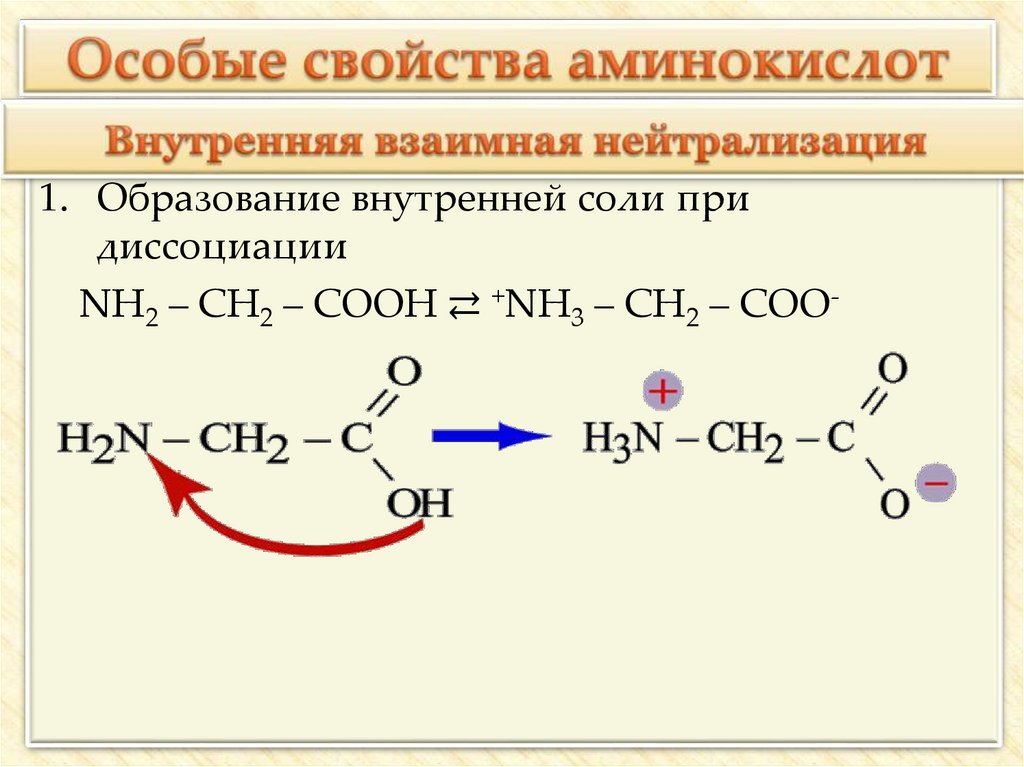
1. Образование внутренней соли придиссоциации
NH2 – CH2 – COOH ⇄ +NH3 – CH2 – COO-
32.
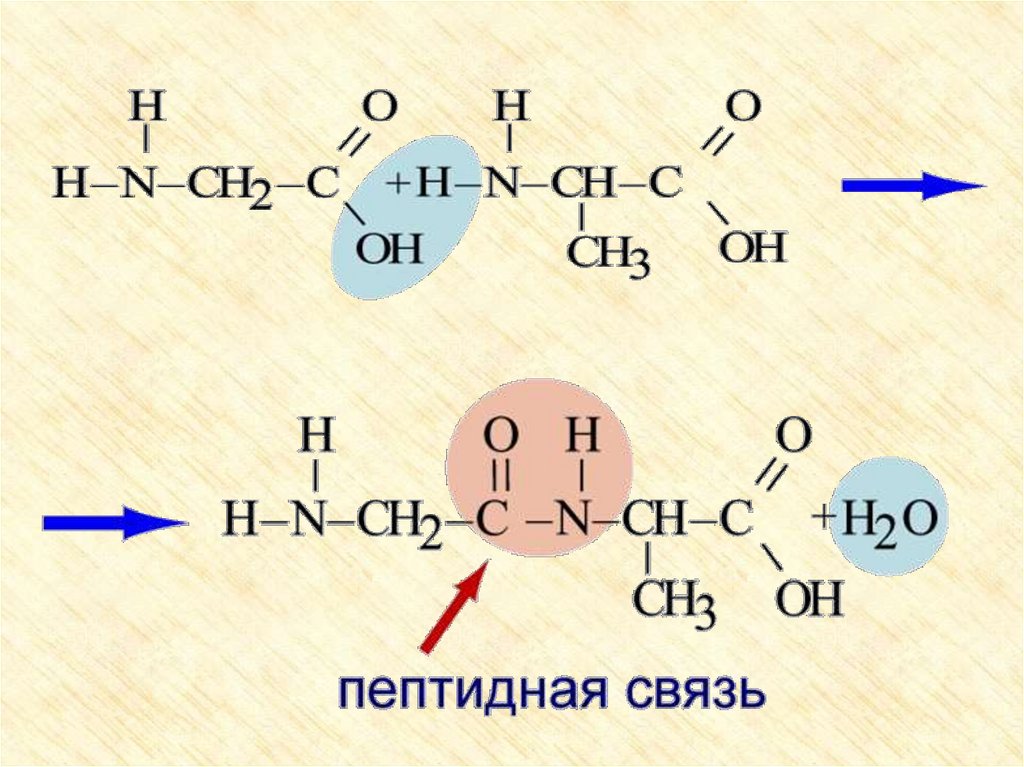
2. Образование пептидов (реакцияполиконденсации):
3.Горение аминокислот.
4NH2CH2COOH + 13O2 → 8CO2 + 10H2O + 2N2
33.
34.
3. Декарбоксилирование :NH2 – CH2 – CH2 – COOH → NH2 – CH2 – CH3 + CO2
4. Образование циклических амидов.
5. Образование комплексных солей
35.
I.Гидролиз белков под влиянием ферментов, кислот
или щелочей.
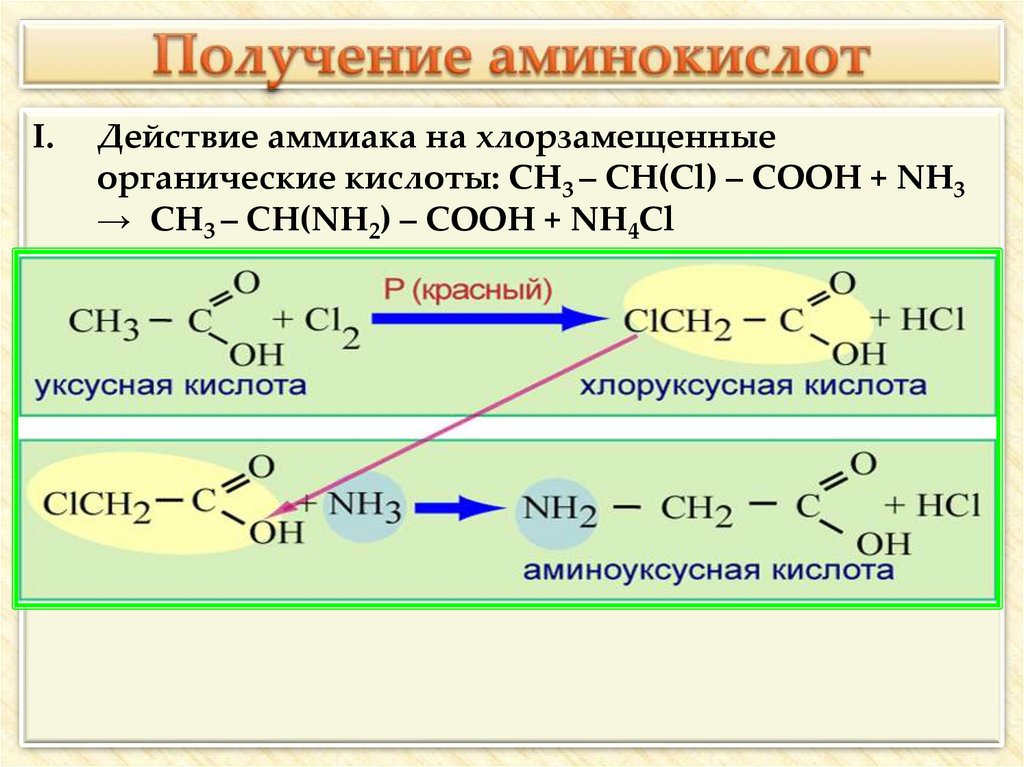
II. Действие аммиака на хлорзамещенные
органические кислоты: CH3 – CH(Cl) – COOH + NH3
→ CH3 – CH(NH2) – COOH + NH4Cl
III. Действие цианистого аммония на оксосоединения
(реакция Н.Д.Зелинского)
IV. Присоединение аммиака к непредельным
кислотам
CH2 = CH – COOH + 2NH3 → H2N –CH2 – CH2 – COONH4
V. Микробиологический синтез
36.
I.Действие аммиака на хлорзамещенные
органические кислоты: CH3 – CH(Cl) – COOH + NH3
→ CH3 – CH(NH2) – COOH + NH4Cl
37.
Аминокислоты, входящие в составбелков проявляют особые свойства
Все относятся к α-аминокислотам
Являются L-стереоизомерами
Относятся к амфотерным
соединениям
38.
Все α-аминокислоты, за исключениемглицина, имеют асимметрический атом
углерода и существуют в виде
энантиомеров, относящихся к D- и Lрядам. В белках животных организмов
представлены L-аминокислоты, в белках
микроорганизмов встречаются и
аминокислоты D-ряда. D-аминокислоты
животным организмом не усваиваются
39.
ЛекарстваГлутаминовая кислота, анестезин,
новокаин, п-аминосалициловая
кислота
Аминокислоты
Пищевая
промышленность
Глутамат натрия
Синтетические волокна
Капрон
40.
1.Лизин — противовирусная и повышающая иммунитетаминокислота;
2.Метионин, который регулирует выработку гормона роста;
3.Треонин, отвечающий за поддержание надлежащего увлажнения
кожи и правильное функционирование нервной системы;
4.Лейцин, основная функция которого — регулировать уровень
секреции кортизола, уровень сахара и поддерживать заживление
ран;
5.Изолейцин — аминокислота, участвующая в механизмах
метаболизма в мышечных тканях;
6.Валин, который поддерживает регенерацию мышц и способствует
сбрасыванию лишнего жира;
7.Триптофан — прекурсор серотонина, который, как считается,
улучшает качество сна и повышает настроение, а также регулирует
аппетит;
8.Фенилаланин, который является прекурсором многочисленных
важных для организма гормонов, включая тирозин, дофамин,
адреналин и норадреналин.
































 Химия
Химия