Похожие презентации:
Синтез и исследование свойств бифункционального Zr-содержащего катализатора
1.
Тема: «СИНТЕЗ И ИССЛЕДОВАНИЕ СВОЙСТВБИФУНКЦИОНАЛЬНОГО Zr-СОДЕРЖАЩЕГО КАТАЛИЗАТОРА НА
ОСНОВЕ SBA-15 В РЕАКЦИИ КАТАЛИТИЧЕСКОГО ОКИСЛЕНИЯ
ГЕМИЦЕЛЛЮЛОЗЫ ДРЕВЕСИНЫ ОСИНЫ»
Выпускник
Я.Р. Шаер
Руководитель профессор, д-р хим. наук
С.Д. Кирик
Консультант
канд. хим. наук, науч. сотр. С.А. Новикова
2.
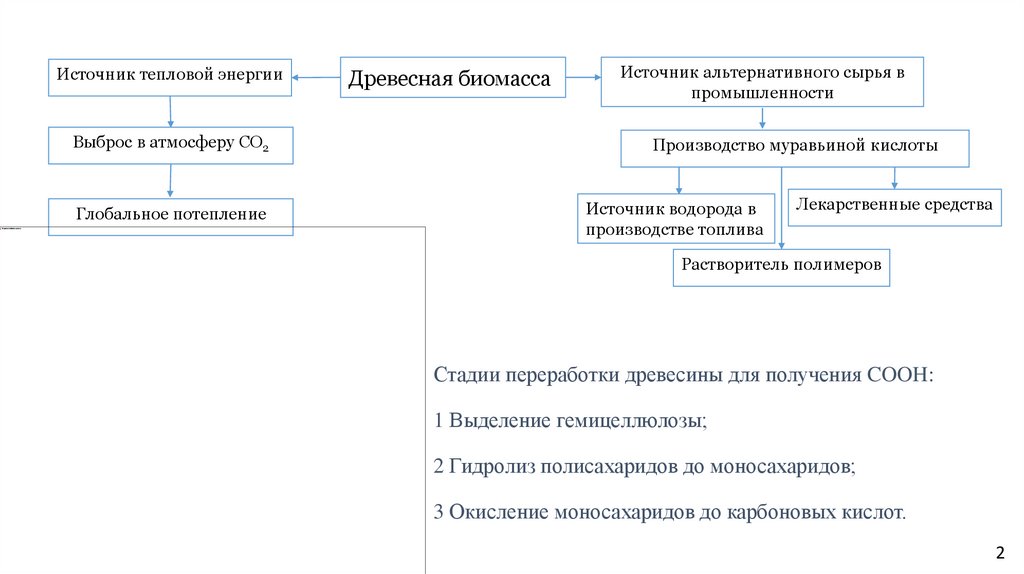
Источник тепловой энергииВыброс в атмосферу СО2
Глобальное потепление
Древесная биомасса
Источник альтернативного сырья в
промышленности
Производство муравьиной кислоты
Источник водорода в
производстве топлива
Лекарственные средства
Растворитель полимеров
Стадии переработки древесины для получения COOH:
1 Выделение гемицеллюлозы;
2 Гидролиз полисахаридов до моносахаридов;
3 Окисление моносахаридов до карбоновых кислот.
2
3.
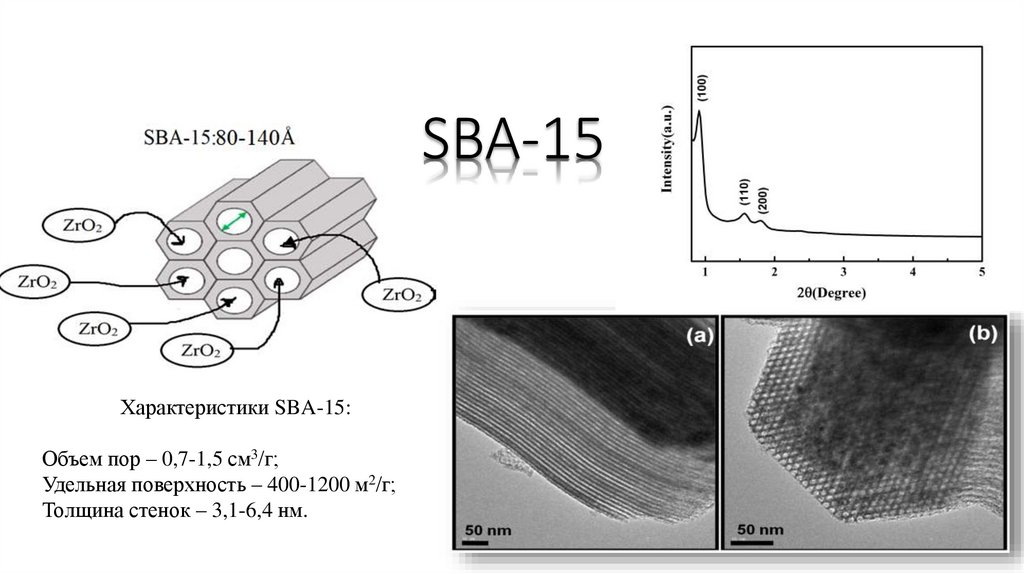
SBA-15Характеристики SBA-15:
Объем пор – 0,7-1,5 см3/г;
Удельная поверхность – 400-1200 м2/г;
Толщина стенок – 3,1-6,4 нм.
4.
Цель работы:Синтез бифункционального гетерогенного катализатора ZrO2-SBA-15 и
применение его в процессе окисления гемицеллюлозы древесины осины
кислородом воздуха.
Задачи:
1.
Изучить характеристики композита ZrO2-SBA-15 методами рентгеновской дифракции,
газовой адсорбции азота, электронной микроскопии (ПЭМ,СЭМ);
2.
Синтезировать материал SBA-15 и сравнить характеристики с ZrO2-SBA-15;
3.
Определить общую кислотность материалов;
4.
Подобрать оптимальные условия для работы катализатора в процессе окисления
гемицеллюлозы до муравьиной кислоты.
3
5.
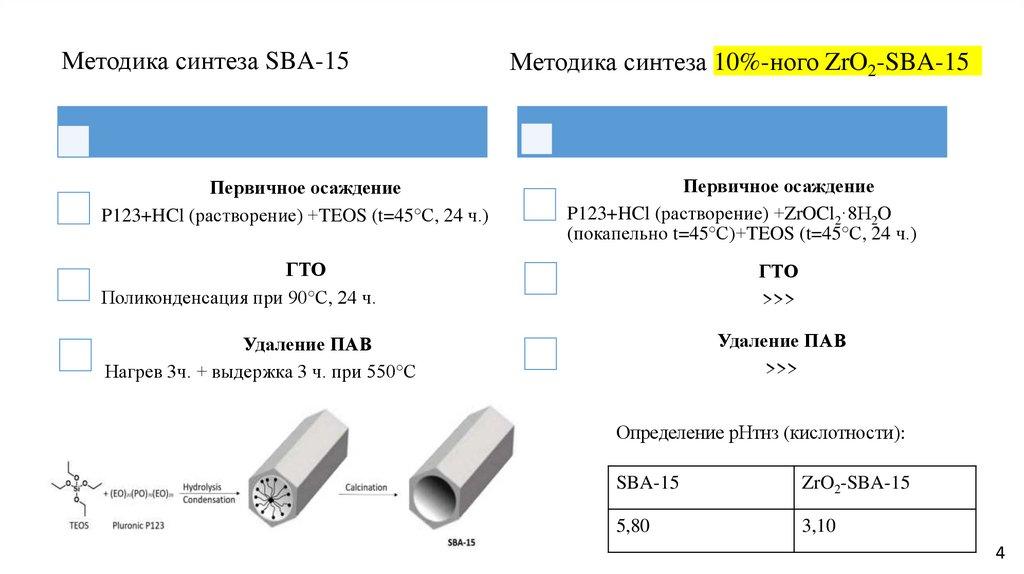
Методика синтеза SBA-15Первичное осаждение
P123+HCl (растворение) +TEOS (t=45°С, 24 ч.)
Методика синтеза 10%-ного ZrO2-SBA-15
Первичное осаждение
P123+HCl (растворение) +ZrOCl2·8H2O
(покапельно t=45°С)+TEOS (t=45°С, 24 ч.)
ГТО
Поликонденсация при 90°С, 24 ч.
ГТО
>>>
Удаление ПАВ
>>>
Удаление ПАВ
Нагрев 3ч. + выдержка 3 ч. при 550°С
Определение рНтнз (кислотности):
SBA-15
ZrO2-SBA-15
5,80
3,10
4
6.
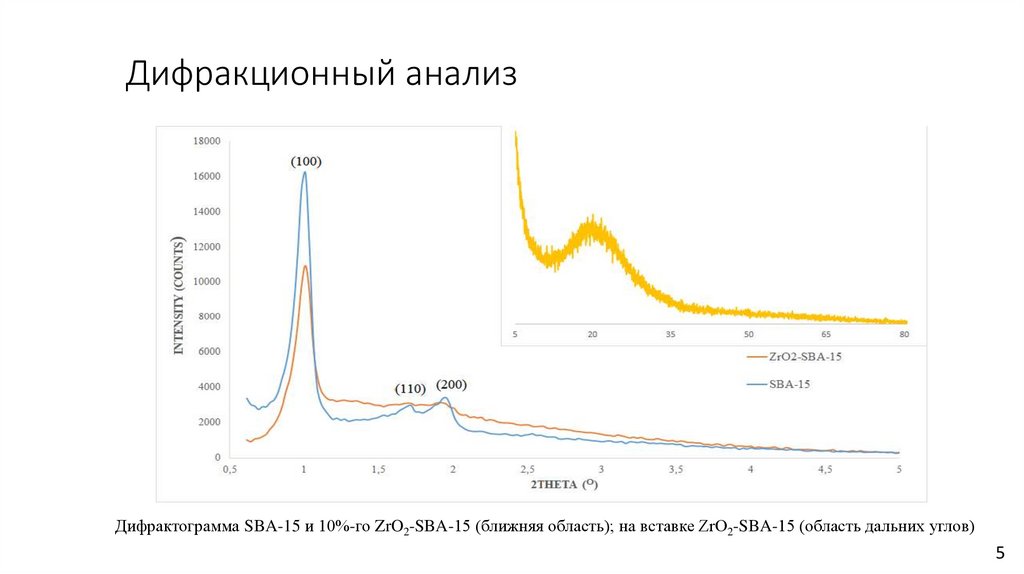
Дифракционный анализДифрактограмма SBA-15 и 10%-го ZrO2-SBA-15 (ближняя область); на вставке ZrO2-SBA-15 (область дальних углов)
5
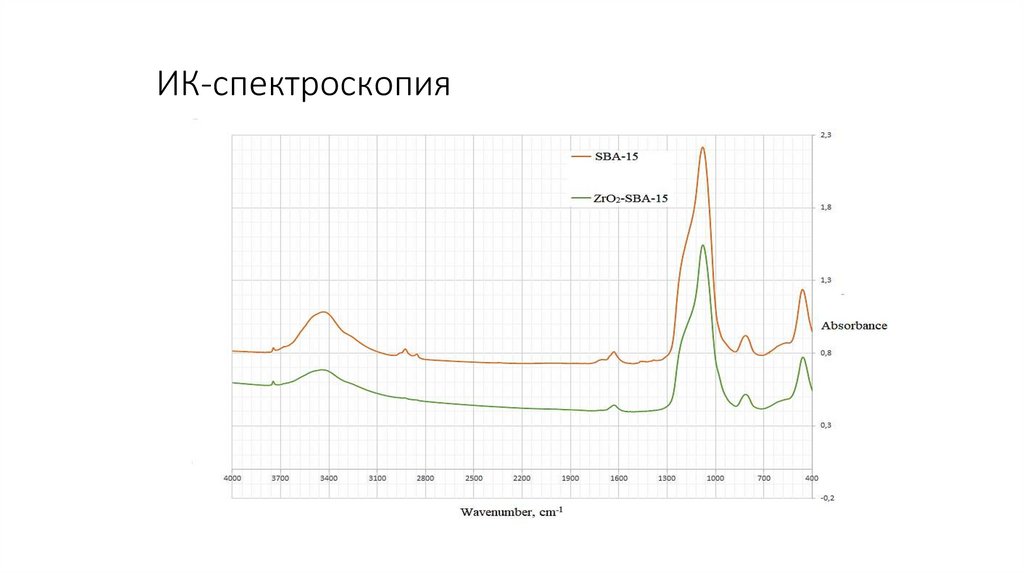
7.
ИК-спектроскопия8.
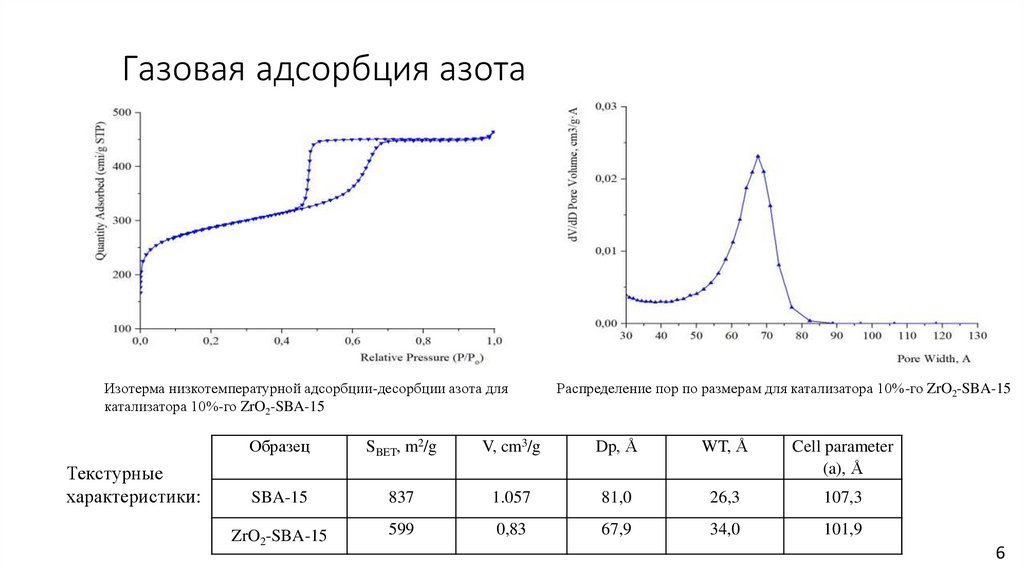
Газовая адсорбция азотаИзотерма низкотемпературной адсорбции-десорбции азота для
катализатора 10%-го ZrO2-SBA-15
Текстурные
характеристики:
Распределение пор по размерам для катализатора 10%-го ZrO2-SBA-15
Образец
SBET, m2/g
V, cm3/g
Dp, Å
WT, Å
Cell parameter
(a), Å
SBA-15
837
1.057
81,0
26,3
107,3
ZrO2-SBA-15
599
0,83
67,9
34,0
101,9
6
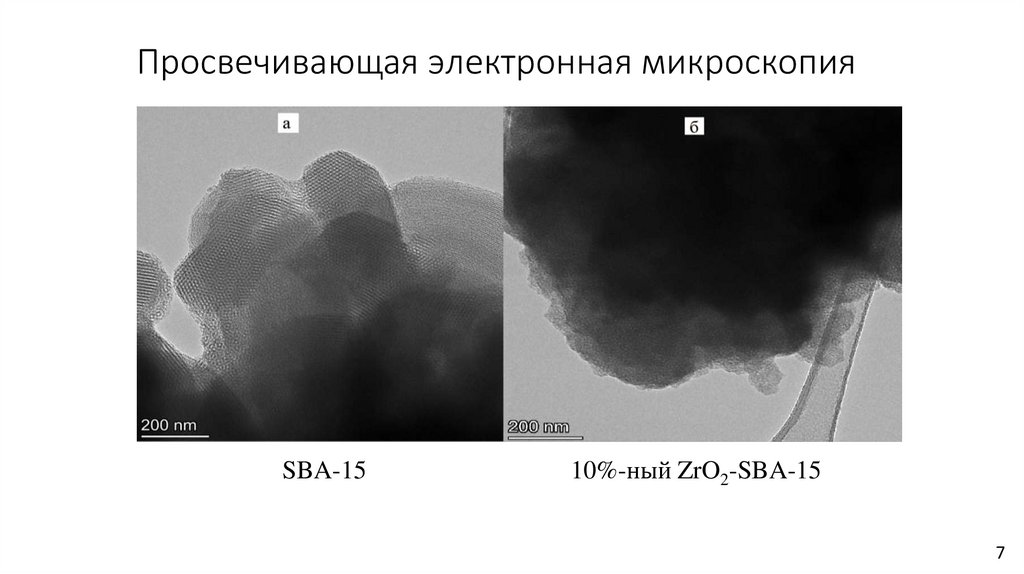
9.
Просвечивающая электронная микроскопияSBA-15
10%-ный ZrO2-SBA-15
7
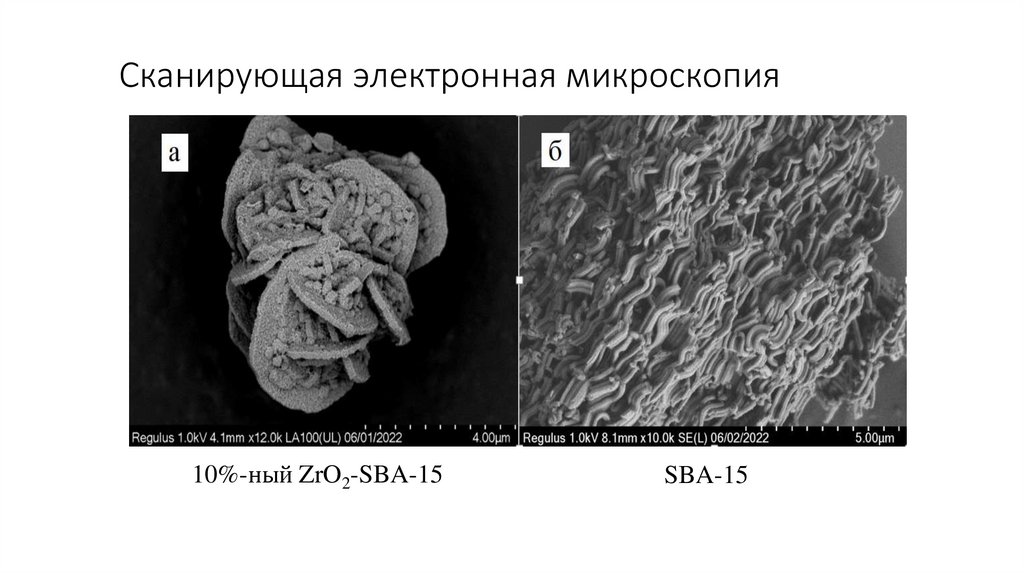
10.
Сканирующая электронная микроскопия10%-ный ZrO2-SBA-15
SBA-15
11.
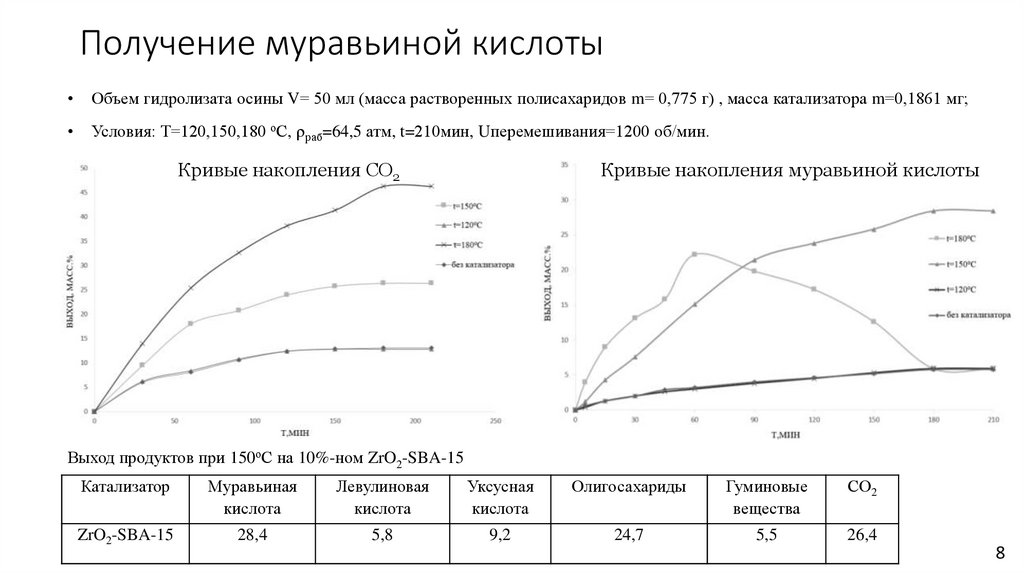
Получение муравьиной кислотыОбъем гидролизата осины V= 50 мл (масса растворенных полисахаридов m= 0,775 г) , масса катализатора m=0,1861 мг;
Условия: Т=120,150,180 оС, раб=64,5 атм, t=210мин, Uперемешивания=1200 об/мин.
Кривые накопления CO2
Кривые накопления муравьиной кислоты
Выход продуктов при 150оС на 10%-ном ZrO2-SBA-15
Катализатор
Муравьиная
кислота
Левулиновая
кислота
Уксусная
кислота
Олигосахариды
Гуминовые
вещества
СО2
ZrO2-SBA-15
28,4
5,8
9,2
24,7
5,5
26,4
8
12.
Выводы1.
Синтезированы композитные материалы SBA-15 и ZrO2-SBA-15.
2.
Методом потенциометрии доказали, что с введением в матрицу SBA-15 диоксида циркония, увеличивается
общая кислотность материала (с 5,80 до 3,10).
3.
По данным анализа рентгеновской дифракции материалы имеют упорядоченную мезопористую структуру.
4.
Методом газовой адсорбции азота были получены текстурные характеристики материалов. Изучено, что с
введением ZrO2 уменьшается общая площадь поверхности и объем пор. Из данных BET и рентгеновской
дифракции у ZrO2-SBA-15 увеличилась толщина стенки на порядок.
5.
По данным ПЭМ и СЭМ изображений SBA-15 представляет собой параллельные каналы с порами в виде
пчелиных сот. Также доказали, что ZrO2-SBA-15 представляет собой искаженную пластинчатую структуру.
6.
Практическое применение катализатора ZrO2-SBA-15 было рассмотрено в реакции окисления кислородом
воздуха гемицеллюлозы древесины осины. Данный катализатор способствует ускорению образования
муравьиной кислоты и в меньшей степени инициирует образование побочных продуктов (гуминов).
Катализатор хорошо работает в окислительных процессах из-за высокой активности кислотных центров.
7.
Оптимальной температурой для активации катализатора является 150оС, при более высоких температурах
выделение МК будет высоким в начале процесса, затем скорость распада будет превышать скорость
образования. Также оптимальным временем процесса является 3 часа.
9



 Химия
Химия








