Похожие презентации:
Классификация химических реакций. 8 класс
1. Классификация химических реакций 8 класс
учитель: Амирджанян Светлана Суреновна2.
Все что нас окружает состоит из веществ.Кажется, что они живут своей жизнью, таинственной
и непостижимой. Взаимодействуя, они изменяют
свои свойства и состав. Без химических реакций
невозможна жизнь и все многообразие веществ. И
задача человека, изучив этот мир, постараться
использовать полученные знания во благо.
Сегодня мы продолжим знакомство с этим
удивительным и волшебным миром.
3. Отгадай загадку и узнай о чем пойдет речь на сегодняшнем уроке
Онаидет,
она
прошла!
Никто
не скажет,
что пришла!
Она - ********** ******* !
4. Что такое химическая реакция?
Химические реакции или химическиеявления – это процессы, в
результате которых из одних
веществ образуются другие;
5. По каким признакам можно определить химические реакции?
• Выделение газа;• Образование осадка;
• Выделение (поглощение)
тепла и света;
• Появление или
изменение запаха или
вкуса;
• Изменение цвета;
6. Каковы условия возникновения реакций:
• Смешивание веществ;• Нагревание;
• Измельчение;
• Соприкосновение ;
• Растворение;
1) Образование
хлорида аммония
3) Взаимодействие алюминия с
иодом
2) Горение магния
7.
Химическиереакции.
Как
классифицировать ?
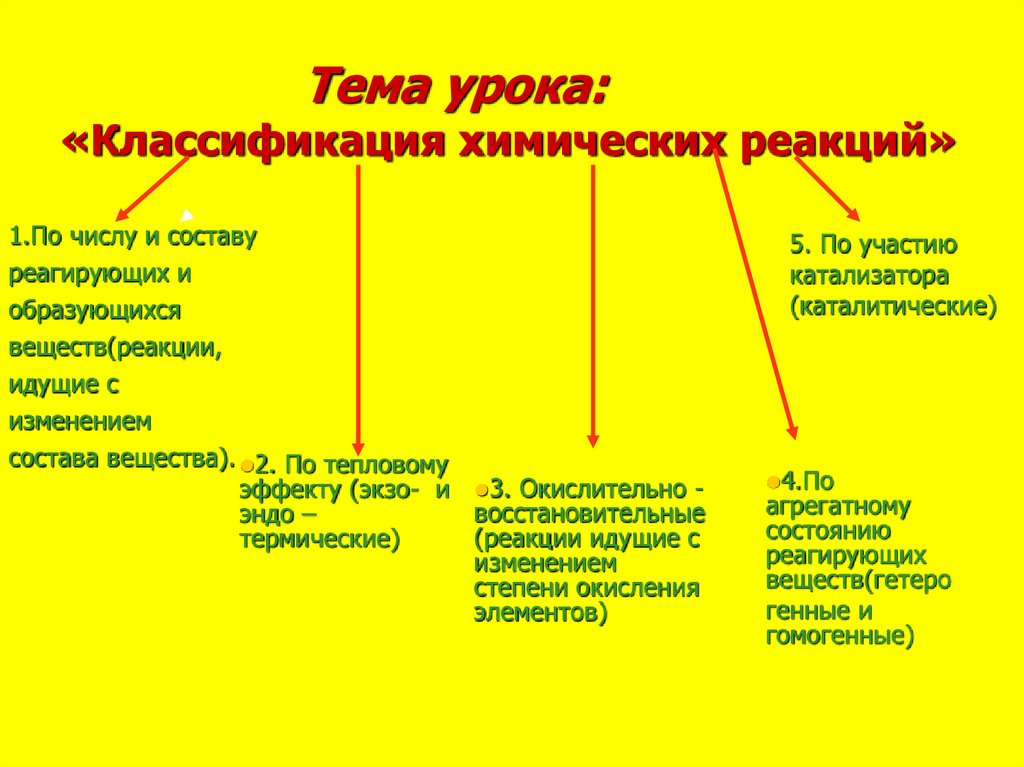
8. Тема урока: «Классификация химических реакций»
1.По числу и составуреагирующих и
образующихся
веществ(реакции,
идущие с
изменением
состава вещества). 2. По тепловому
эффекту (экзо- и 3. Окислительно восстановительные
эндо –
(реакции идущие с
термические)
изменением
степени окисления
элементов)
5. По участию
катализатора
(каталитические)
4.По
агрегатному
состоянию
реагирующих
веществ(гетеро
генные и
гомогенные)
9.
Можно ли выделить признак,по которому возможно разделить
эти реакции на группы?
2H2 + O2 → 2H2O
CaO + H2O → Ca(OH)2
Cu(OH)2 → CuO + H2O;
Различаются ли между
собой реакции одной группы?
2HgO → 2Hg + O2
10.
Реакциисоединения
…Al +… O2 → …Al2O3
…P + …O2 → …P2O5
Na2O + SO3 → Na2SO4
Li2O + H2O →… LiOH
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать
процесс, который протекает?
11.
Реакцииразложения
…Fe(OH)3 → Fe2O3 +… H2O
…HgO → …Hg + O2
CaCO3 → CaO + CO2
…NO → N2 + O2
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать
процесс, который протекает?
12.
Реакциизамещения
CuCl2 + Fe → Cu + FeCl2
Cr2O3 + …Al → …Cr + Al2O3
Mg + …HCl → MgCl2 + H2
Что объединяет все эти реакции?
Как одним словом мы можем назвать
процесс, который протекает?
13.
Реакцииобмена
CuO + …HCl → CuCl2 + H2О
BaCl2 + K2SO4 → BaSO4 + …KCl
Что объединяет все эти реакции?
Как одним словом мы можем назвать
процесс, который протекает?
14.
Химическиереакции
Соединения
Разложения
Замещения
Обмена
A + B → AB
AB → A + B
AB + C→ A + CB
AB + CD→ AD + CB
AB + CB → AB2C
AB2C → AB + BC
15. Задания группам:
Внимательно прочитайте инструктивнуюкарточку по проведению опыта.
Соблюдая технику безопасности проведите
химическую реакцию.
Определите тип реакции, запишите
уравнение реакции в тетрадь, укажите
признаки прохождения реакции.
Подготовьте отчет своей группы.
16. Уравнения к лабораторным опытам.
• 1. Zn +2HCl = ZnCl2 + H2 --- реакция замещения,выделяется газ водород.
• 2. CuSO4 +2KOH = Cu(OH)2 + K2SO4 ---
реакция обмена, выпадение голубого осадка (гидроксида меди(II) )
17.
Химическиереакции
Соединения
Mg+O2=
Разложения
Cu(OH)2 =
Замещения
Обмена
Zn + H2SO4 =
AgNO3 + HCl =
18. Проверим свои знания !
На листке с тестом запишите своюфамилию. Для заданий части А, правильные
ответы выделите кружком. В часть Б
внесите соответствующие записи.
Каждый вопрос оценивается баллами,
максимальное количество баллов за тест 22
балла.
На выполнение теста
отводится 10 минут
Желаю удачи!
19. Домашнее задание: Классификация химических реакций( схема в тетради),упражнение№5 на стр.214
Спасибо за урок!До новых встреч!


















 Химия
Химия








