Похожие презентации:
Соединения алюминия
1.
2.
I ВАРИАНТII ВАРИАНТ
ИТЧОРП
ОМЬСИП
Критерии оценки:
Всё верно – «5»
1-2 ошибки – «4»
3 ошибки – «3»
4 и более – учи ешё
3.
4. Взаимодействие с кислотами
Al+
HCl → AlCl3 + H ↑
Al2O3
+
HCl → AlCl3 + H O
Al(OH)3 +
2
2
HCl → AlCl3+ H O
2
5. Взаимодействие со щелочами
Al+ NaOH → Na[Al(OH)4] + H2↑
раствор
Al2O3 + NaOH → Na[Al(OH)4] + H2O
раствор
Al(OH)3+ NaOH → Na[Al(OH)4]+H2O
раствор
AlCl3+ NaOH → Na[Al(OH)4] + NaCl
раствор, избыток
6.
Оксид алюминия в видекорунда используется как
абразивный материал для
обработки металлических
изделий.
Корунд
(кристаллический
глинозём)
Al2O3
7.
РубинПрозрачные кристаллы
корунда, окрашенные
примесями в синий цвет,
называют сапфиром, в
красный – рубином.
Оксид алюминия
в виде рубина
широко
используется в
лазерной технике.
Сапфир
8.
Гель изгидроксида
алюминия входит в
состав лекарств
для лечения
болезней желудка.
9.
А10
20
30
40
50
20
30
40
50
Б
?
В
10
20
30
40
50
Г
10
20
30
40
50
10.
назад11.
назад12. В растворе какого вещества образуется избыток гидроксид-анионов?
назадКислота
Соль
Щелочь
Вода
13. Число нейтронов в ядре атома 27AL равно
назад27
14
13
40
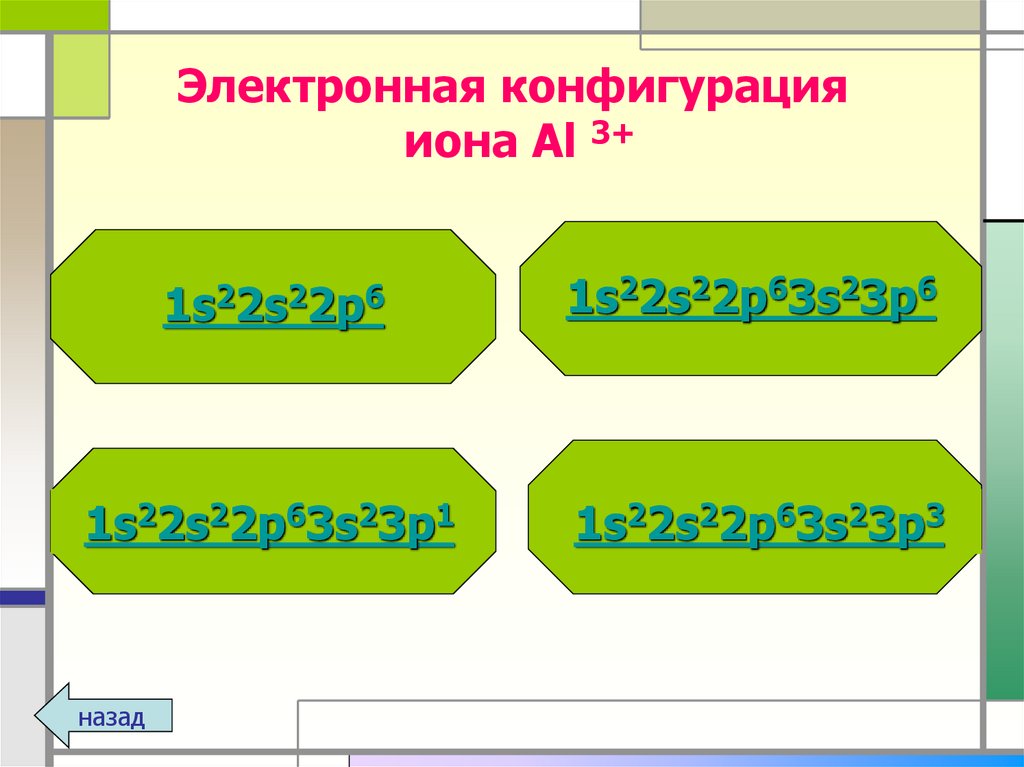
14. Электронная конфигурация иона Al 3+
1s22s22p61s22s22p63s23p6
1s22s22p63s23p1
1s22s22p63s23p3
назад
15. С оксидом алюминия не реагирует
Гидроксиднатрия
Соляная
кислота
назад
Сульфат
кальция
Оксид
кальция
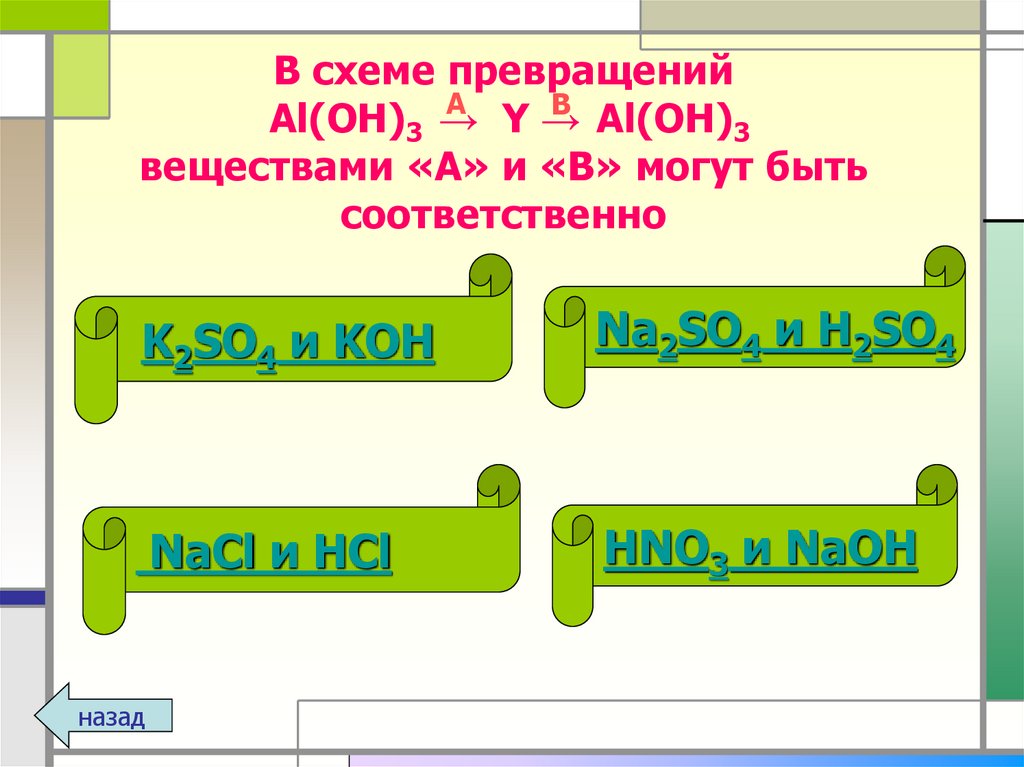
16. В схеме превращений Al(OH)3 → Y → Al(OH)3 веществами «А» и «В» могут быть соответственно
В схеме превращенийА
В
Al(OH)3 →
Y→
Al(OH)3
веществами «А» и «В» могут быть
соответственно
K2SO4 и KOH
Na2SO4 и H2SO4
NaCl и HCl
HNO3 и NaOH
назад
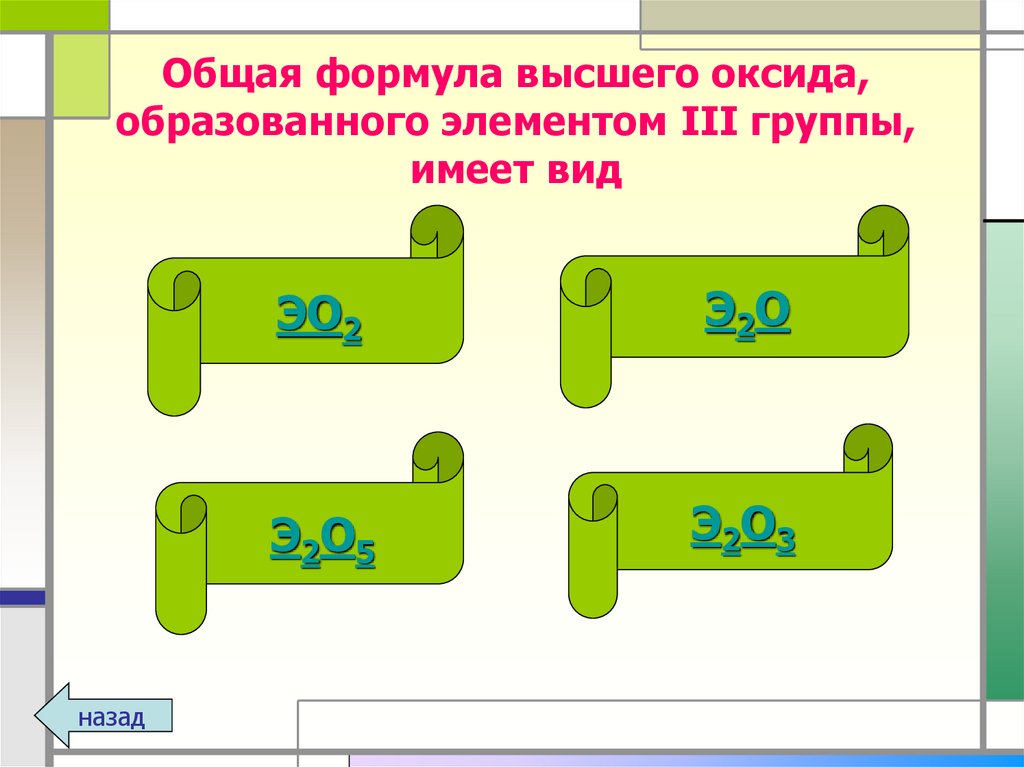
17. Общая формула высшего оксида, образованного элементом III группы, имеет вид
назадЭО2
Э2О
Э2О5
Э2О3
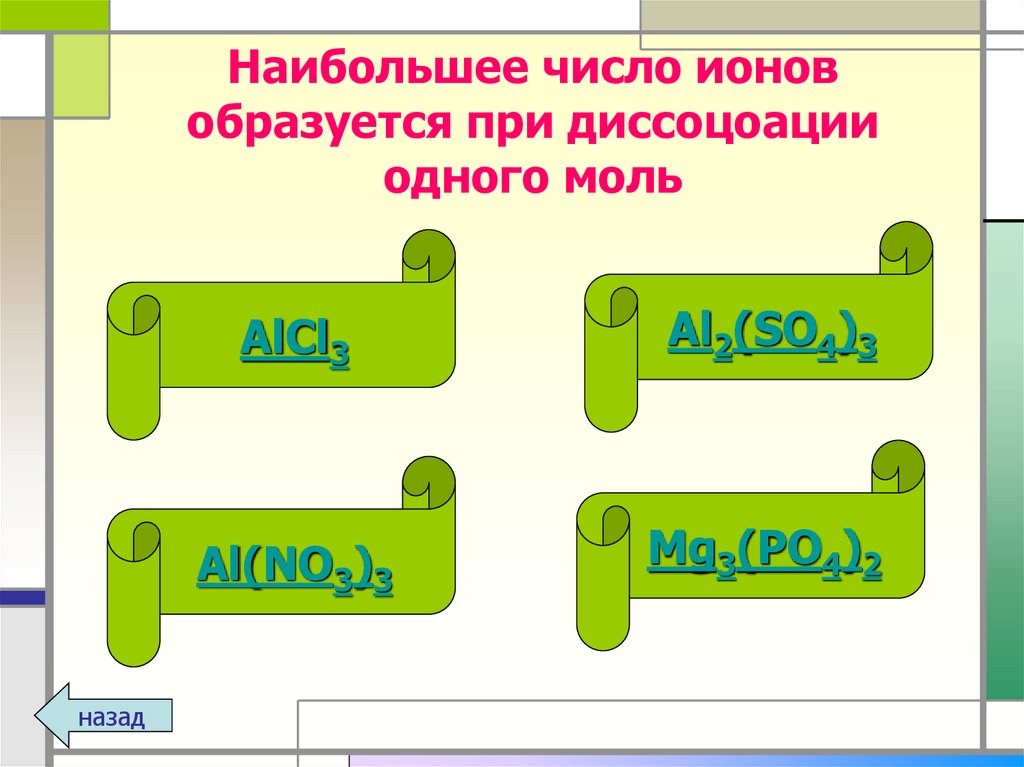
18. Наибольшее число ионов образуется при диссоцоации одного моль
назадAlCl3
Al2(SO4)3
Al(NO3)3
Mg3(PO4)2
19. Формулы амфотерных оксидов записаны в ряду
N2O,CuO,CaOMgO, K2O, Li2O
назад
BeO, Al2O3,ZnO
Na2O, CO2, Al2O3
20. В ряду MgO - Al2O3 – SiO2 – P2O5 свойства оксидов изменяются от
Основных камфотерным
Амфотерных
к кислотным
Основных к
кислотным
Кислотных
к основным
назад
21. Продукты реакции Al2O3 + NaOH → сплавление
NaAlO2 + H2ONaOH + Al(OH)3
назад
Na[Al(OH)4]+H2O
Na2O + Al(OH)3
22.
При взаимодействии алюминия сразбавленной соляной кислотой
образуются вещества
AlCl3 и H2
AlCl3 и H2O
AlH3 и Cl2
Al(OH)3 и Cl2
назад
23. В каком ряду химические элементы расположены в порядке усиления металлических свойств
Na – Mg – AlAl – Mg – Na
K – Na – Li
Ca – Mg – Be
назад
24. Гидроксид калия реагирует с
назадводой
кислотой
щёлочью
кислотой и
щёлочью
25. При действии избытка раствора гидроксида калия на раствор сульфата алюминия образуется
Al2O3KAlO2
назад
Al(OH)3
K[Al(OH)4]
26. Оксид алюминия реагирует с каждым из веществ
назадNaCl и H2O
H2SO4 и Ba(OH)2
H2SO4 и H2O
BaSO4 и Br2
27. Можно квасить капусту в алюминиевой посуде?
нет, капустапотемнеет
нет,
капуста станет
очень кислой
нет,
разрушается
посуда
да, можно
назад
28. Д.И. Менделееву за его заслуги в области химии вручили
золотуюмедаль
алюминиевую
кружку
назад
Нобелевскую
премию
серебряную
ложку
29. Что добывают во Франции и в Мурманской области?
бокситыполиметаллы
назад
уголь
нефть
30. Гидроксид натрия не реагирует с
назадAl(OH)3
H2SO4
ZnO
Ba(OH)2
31. Гидроксид калия не реагирует с
Cl2 и HNO3Na2SO4 и MgO
назад
H2SO4 и CO2
ZnSO4 и FeCl2
32. Домашнее задание
□ § 13 (повт.)□ РТ: стр. 84, упр. 3 (а, б),
□
стр. 86, задача №4
□
* стр. 86, задача №5



















 Химия
Химия








