Похожие презентации:
Знакомство с кислотами. Общие свойства кислот. 8 класс
1. Урок-путешествие «Знакомство с кислотами. Общие свойства кислот» 8 класс
Автор: Лозинская Л.Ф.,учитель химии МОУ ТСШ № 17
г. Тирасполь
2. Путешествие
3. Цель и задачи путешествия
4. Формулы кислот
Серная кислотаСоляная кислота
Азотная кислота
Фосфорная кислота
Сероводородная кислота
Плавиковая кислота
Угольная кислота
Кремниевая кислота
H2SO4
HCI
HNO3
H3PO4
H 2S
HF
H2CO3
H2SiO3
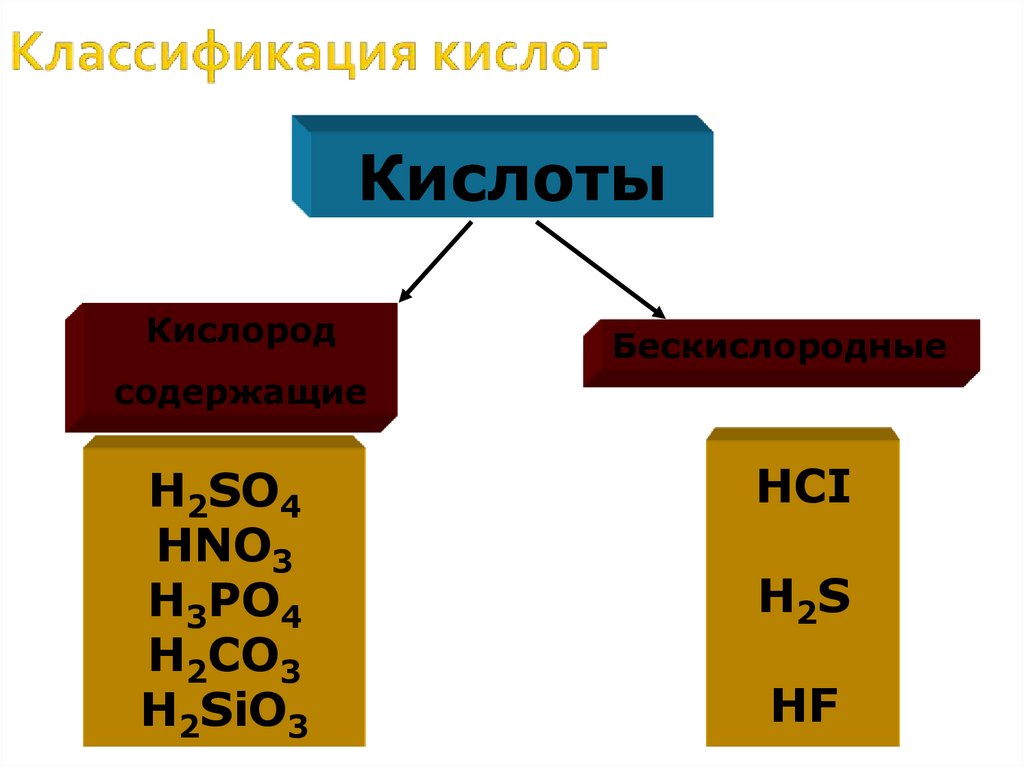
5. Классификация кислот
КислотыКислород
Бескислородные
содержащие
H2SO4
HNO3
H3PO4
H2CO3
H2SiO3
HCI
H2S
HF
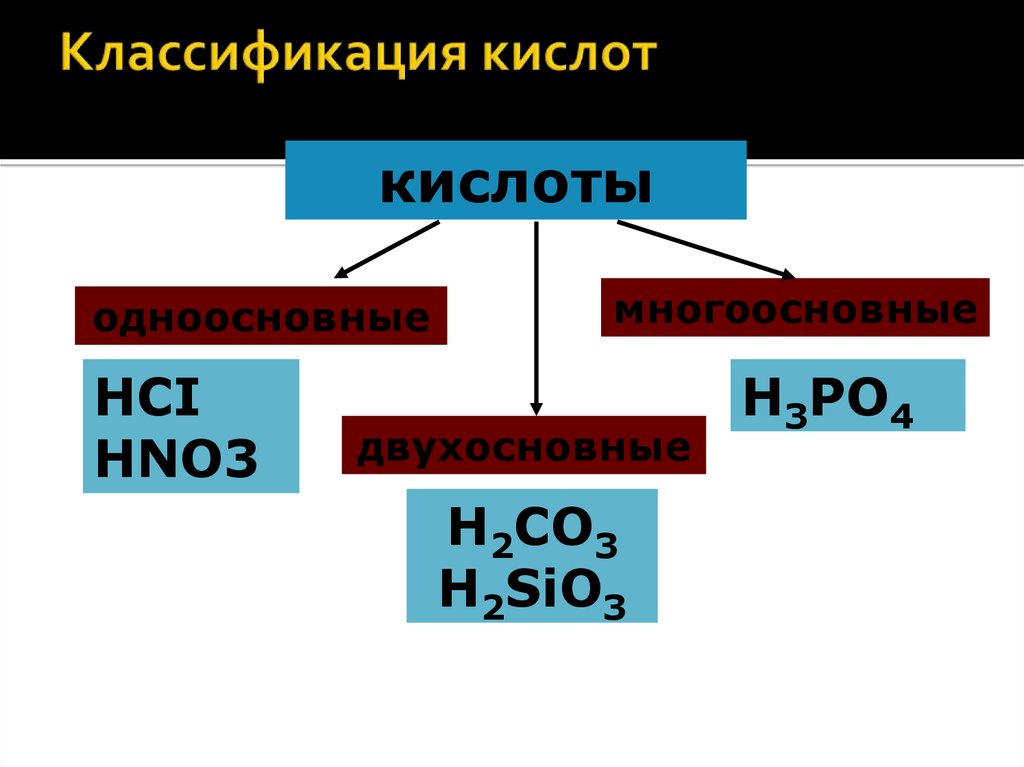
6. Классификация кислот
кислотыодноосновные
HCI
HNO3
многоосновные
двухосновные
H2CO3
H2SiO3
H3PO4
7. Характеристика кислот
H2SO4HCI
8. Остановка «Информационная»
Первая известнаячеловечеству кислота –
уксусная CH3COOH. Люди
выращивали виноград,
готовили вино, при
прокисании вина получался
уксус.
Слово «кислота» произошло
от латинского названия
уксуса.
9. Природные кислоты
Углекислый газвоздуха, растворяясь
в дождевой воде
превращается в
угольную кислоту.
Н2О+СО2=Н2СО3
10. Природные кислоты
Во время грозы образуютсяоксиды азота, растворяясь в
дождевой воде они дают
азотную кислоту.
При извержении вулканов и
работе химических заводов
выделяются оксиды серы,
участвующие в образовании
серной кислоты.
11. Кислотные дожди
Разрушают почвыУгнетают развитие
растений
Разрушают здания,
скульптуры.
Необходимо на химических
производствах принимать
меры по очистке
выбрасываемых газов.
12. Пищевые кислоты
ЯблочнаяЩавелевая
Молочная
Лимонная
Аскорбиновая
Ацетилсалициловая
Олеиновая
13. Кислоты в организме человека
В желудочном соке –соляная кислота.
В обмене веществ
участвуют янтарная,
уксусная, молочная
кислоты и т.д.
14. Синильная кислота
15. Угольная кислота
16. Муравьиная кислота
17. ПТБ – правила техники безопасности
Растворение серной кислоты в водеДействие серной кислоты на дерево и
бумагу
Вывод: работать с кислотами надо очень
осторожно, в специальной одежде и
защитных очках.
18. Первая помощь
При попадании кислотына кожу: промыть
большим количеством
воды и 5% раствором
соды.
Хранение: в недоступном
для маленьких детей
месте, лучше в
пластиковой посуде. Не
хранить в пищевой
посуде
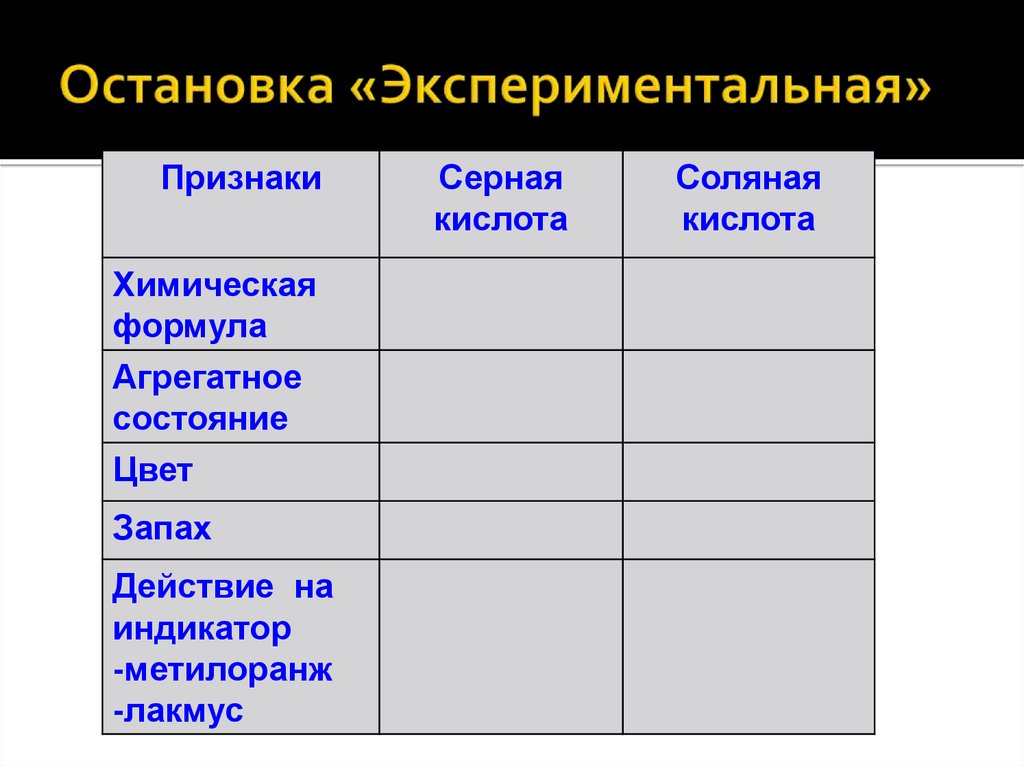
19. Остановка «Экспериментальная»
ПризнакиХимическая
формула
Агрегатное
состояние
Цвет
Запах
Действие на
индикатор
-метилоранж
-лакмус
Серная
кислота
Соляная
кислота
20. Остановка «Индикаторная»
Индикатор указательВ пробирку налить 1 мл
раствора индикатора,
добавить 2-3 капли
кислоты, отметить
наблюдения в таблице,
повторить с другой
кислотой и другим
индикатором.
21. Вывод
Индикаторы меняют свойцвет в растворах кислот - это
общее свойство кислот,
обусловленное
особенностями их строения.
22. Домашнее задание
§Выучить формулы кислот


















 Химия
Химия








