Похожие презентации:
Реакции замещения. Понятие о сущности реакций замещения
1. Реакции замещения
МОУ «Средняя общеобразовательная школа №76» г. СаратоваРЕАКЦИИ
ЗАМЕЩЕНИЯ
Класс: 8
Учитель: Царева Татьяна Викторовна
2. ЦелИ урока:
ЦЕЛИ УРОКА:I. Дать понятие о сущности реакций замещения.
II. Познакомить с:
1) электрохимическим рядом напряжений металлов;
2) условиями взаимодействия металлов с растворами
кислот и солей.
III. Продолжить формирование умений составлять
уравнения реакций и расставлять коэффициенты.
3.
Проверка домашнего задания1. Какие типы реакций по признаку «числу и составу
исходных веществ и продуктов реакции» вы знаете?
2. Какие реакции выделяют по условиям проведения?
3. Дайте определение реакций соединения, условия их
проведения.
4. Дайте определение реакций разложения, условия их
проведения.
5. Что такое уравнения химических реакций? Для чего
в них расставляют коэффициенты?
4. Составить уравнения и расставить коэффициенты:
СОСТАВИТЬ УРАВНЕНИЯ И РАССТАВИТЬКОЭФФИЦИЕНТЫ:
1. Оксид азота(V) + вода = азотная кислота
В1.
2. Оксид натрия + вода = гидроксид натрия
3. Гидроксид железа (III) = оксид железа (III) + вода
1. Оксид углерода(IV) + вода = угольная кислота
В2.
2. Оксид лития + вода = гидроксид лития
3. Гидроксид меди (II) = оксид меди (II) + вода
5.
Реакция замещенияА + ВС = АС + В
Уравнение реакции в общем виде
6.
Реакции замещения7. Взаимодействие кислот с металлами
Zn + 2HCl = ZnCl2 + H28.
Лабораторный опыт«Взаимодействие кислот с металлами»
Правила работы с реактивами и оборудованием
Аккуратно, не спешите!
Реактивы брать в минимальных
количествах!
Пробирки должны находиться в штативе!
Строго выполняйте указания учителя
9.
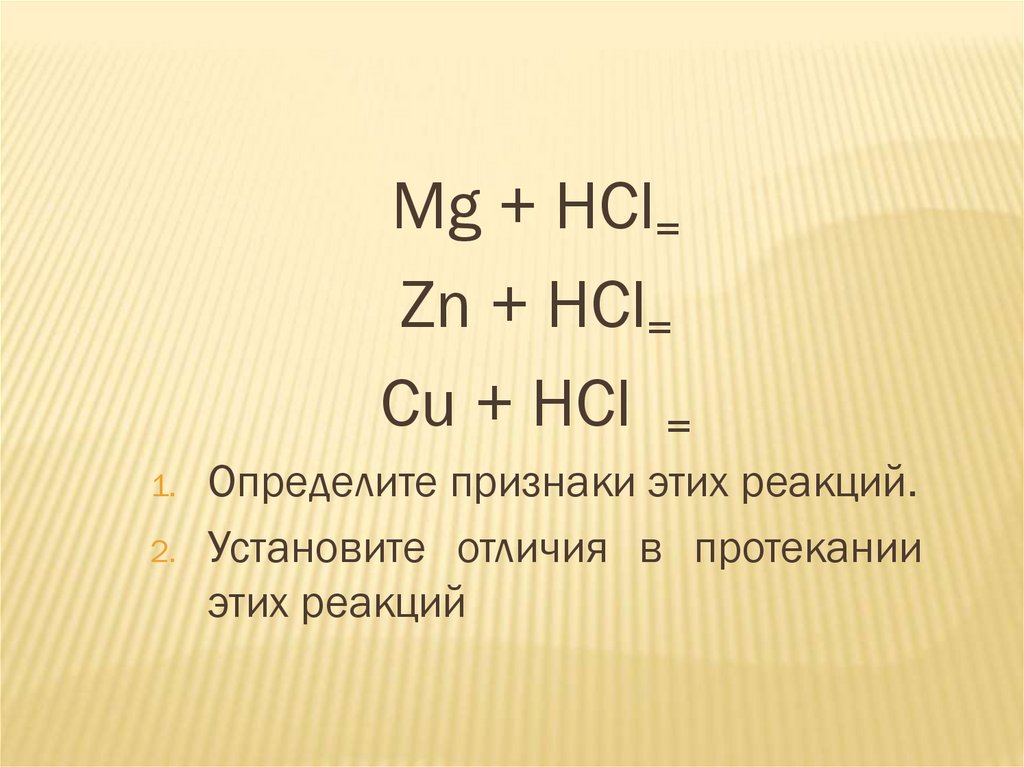
Мg + HCl=Zn + HCl=
Cu + HCl =
1.
2.
Определите признаки этих реакций.
Установите отличия в протекании
этих реакций
10. Электрохимический ряд напряжений
ЭЛЕКТРОХИМИЧЕСКИЙ РЯД НАПРЯЖЕНИЙПравило 1:
Каждый из металлов, расположенных в ряду напряжений до
водорода вытесняет водород из водных растворов кислот.
Образованная соль должна быть растворима.
Li, K, Ca, Na, Mg, Al, Mn, Zn, Fe, Pb, H2, Cu, Ag, Au
Концентрированная H2SO4 пассивирует Fe и Al
Азотная кислота при любой концентрации реагирует с металлами поособому.
Металлы расположенные до Al в водных растворах кислот вытесняют
водород из воды.
11. Проверка написания уравнений реакций
ПРОВЕРКА НАПИСАНИЯ УРАВНЕНИЙРЕАКЦИЙ
Мg
+ 2HCl= МgCl 2 + H2 ↑
Zn + 2HCl=ZnCl 2 + H2 ↑
Cu + HCl = не идет
12. Вытеснение металлов из солей.
ВЫТЕСНЕНИЕ МЕТАЛЛОВ ИЗ СОЛЕЙ.Правило 2: В реакциях между металлами и солями:
Каждый металл вытесняет из солей (в водных растворах) все те
металлы, которые стоят правее его в электрохимическом ряду.
Новая соль должна быть растворима.
Закончить уравнения практически осуществимых реакций:
Fe + CuCl2 = FeCl2 + Cu↓
Fe + AlCl3 =
Fe + HgCl2 =
Al + PbCl2 =
Li, Ca, Na, Mg, Al, Mn, Zn, Fe, Pb, H2, Cu, Hg, Ag.
13. Проверка написания уравнений реакций
ПРОВЕРКА НАПИСАНИЯ УРАВНЕНИЙРЕАКЦИЙ
Fe
+ CuCl2 = FeCl2 + Cu↓
Fe + AlCl3 =не идет
Fe + HgCl2 =FeCl2 + Hg↓
2Al + 3PbCl2 = 2AlCl3 + 3Pb↓
14. Исключение из правил 1 и 2:
ИСКЛЮЧЕНИЕ ИЗ ПРАВИЛ 1 И 2:1. Металлы, расположенные до Al в водных растворах кислот и
солей взаимодействуют с водой и вытесняют из неё водород:
2Na + 2H2O = 2NaOH + H2↑
Ca + 2H2O = Ca(OH)2 + H2 ↑
Можно ли получить
хлорид
натрия
с помощь реакций:
Закончить
уравнения
реакций:
Li + H2O =
Na + HCl =
Ba + H2O =
Na + ZnCl
2 =
Li, K, Ca, Na, Mg, Al, Mn, Zn, Fe, Pb, H2, Cu, Ag, Au
15. Вопросы.
ВОПРОСЫ.1.5.СКакие
какимметаллы
типом реакций
по
признаку
пассивирует
4.Какие
Правило
вытеснения
металлов
из из
3.
металлы
вытесняют
водород
6.
Какие
металлы
способны
вытеснять
2. Дать
определение
реакции веществ
замещения.
«число
и состав исходных
и
солей.
концентрированная
серная
кислота?
кислот?
водород
из
воды?
продуктов реакции» вы познакомились?
16. Домашнее задание:
ДОМАШНЕЕ ЗАДАНИЕ:§ 31
Упр. 2, 3,4
Дополнительное задание:
презентация на тему
«Применение различных видов
химических реакций в
повседневной жизни».
Уделить особое внимание
наглядности выступления.
17. Литература
ЛИТЕРАТУРА1. Габриелян О.С. Программа курса химии для 8 – 11
классов общеобразовательных учреждений. – М.: ДРОФА
2006.
2. Габриелян О.С. Химия 8 класс: учебник для
общеобразовательных учреждений. – М.: ДРОФА. 2005.
3. Горковенко М.Ю. Химия 8 класс: Поурочные
разработки к учебникам О.С.Габриеляна, Л.С.Гузея,
В.В.Сорокина, Р.П.Суровцевой; Г.Е.Рудзитиса,
Ф.Г.Фельдмана. – М.: ВАКО, 2004.
















 Химия
Химия








