Похожие презентации:
Типы реакций алканов
1.
ГБОУ «Морская школа»учитель химии
Смирнова Надежда Александровна
2.
Типы реакций алканов.1. Замещение
-галогенирование
-нитрование
2. Окисление
-горение (при высоких температурах)
-О2 воздуха с катализатором
3. Термические превращения
-крекинг
-дегидрирование
-дегидроциклизация
-изомеризация
3.
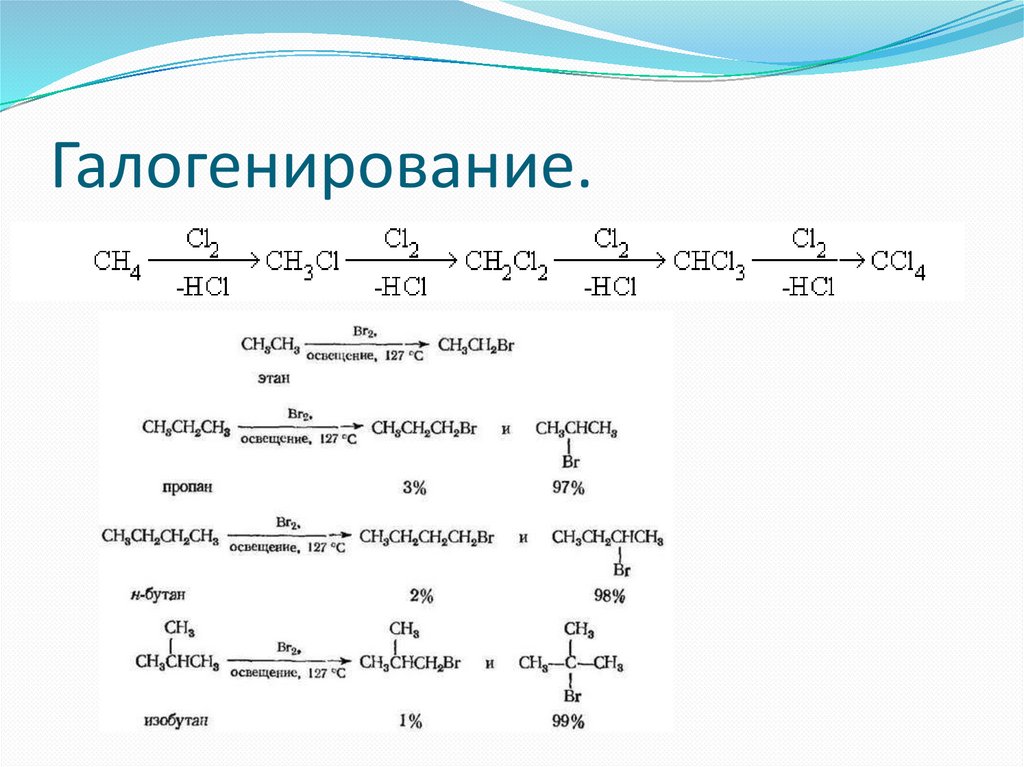
Галогенирование.4.
Нитрование. Реакция Коновалова5.
Окисление кислородом привысоких температурах.
Избыток кислорода
СH4 + 2O2 → CO2 + 2H2O
Недостаток кислорода
2CH4 + 3O2 → 2CO + 4H2O
CH4 + O2 →C + 2H2O
6.
Окисление кислородом скатализатором.
CH4 +O2 kat,t→ 2CH3OH (метанол)
7.
Термический крекинграсщепление при температуре.8.
Дегидрирование.CH4 →t=12000 → C + 2H2
9.
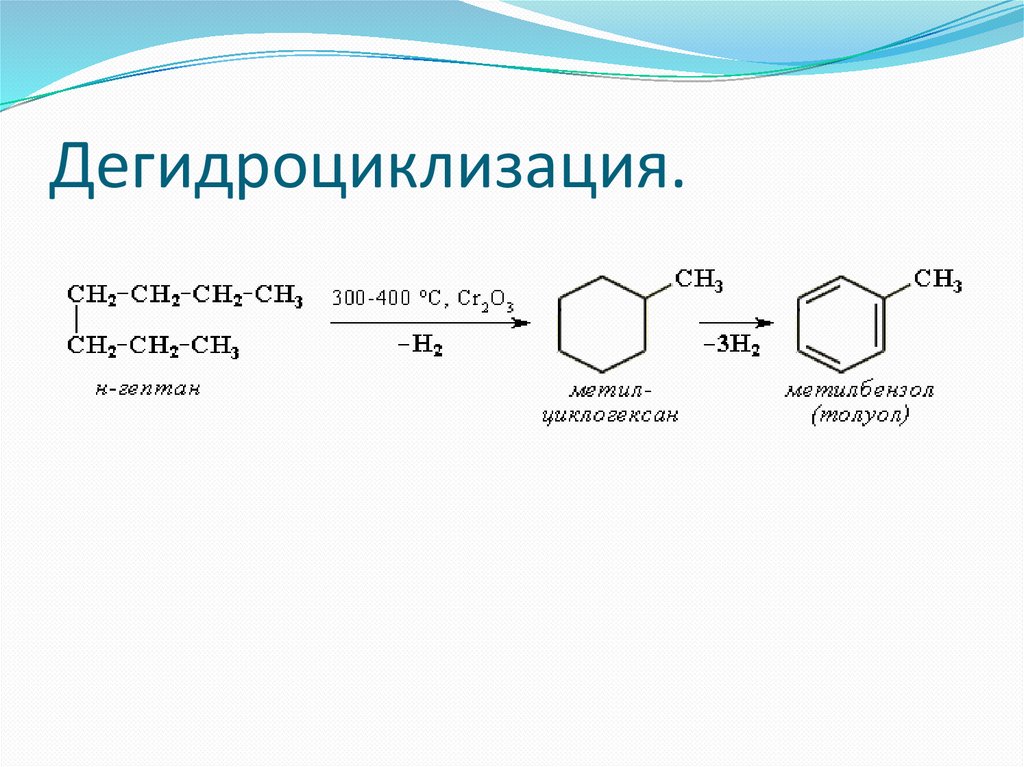
Дегидроциклизация.10.
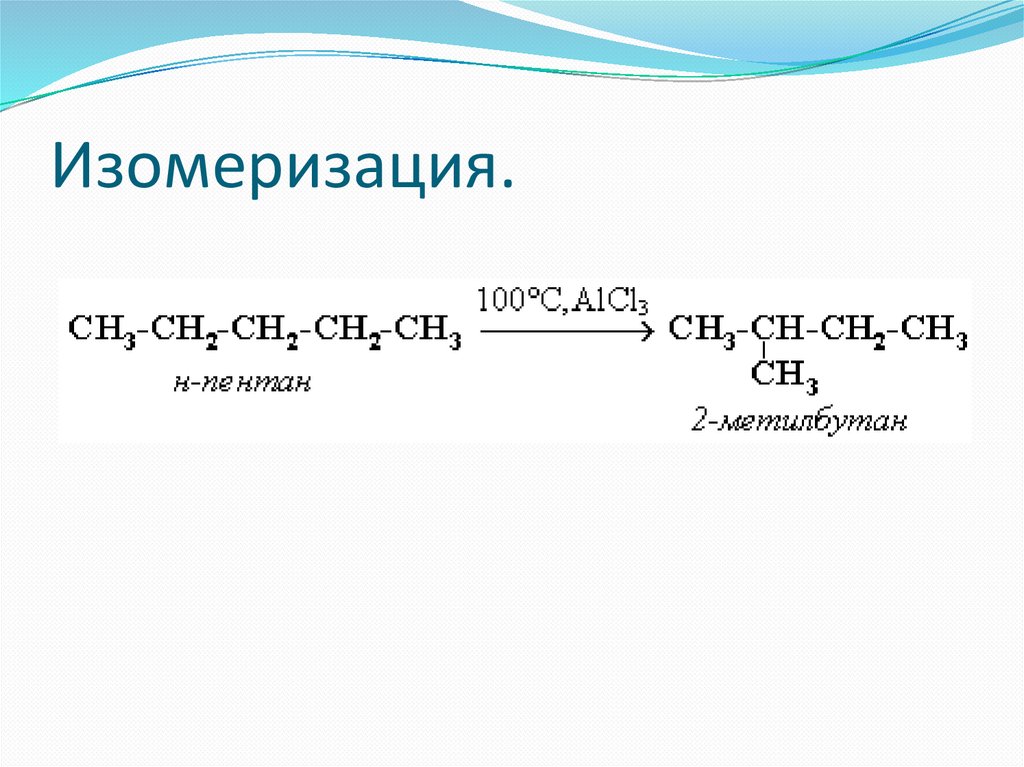
Изомеризация.11.
Типы реакций алкенов.Присоединение
-гидрирование
-галогенирование
-гидрогалогенирование
-гидратация
Окисления
-горение
-О2 воздуха с катализатором
-с KMnO4
Полимеризации
12.
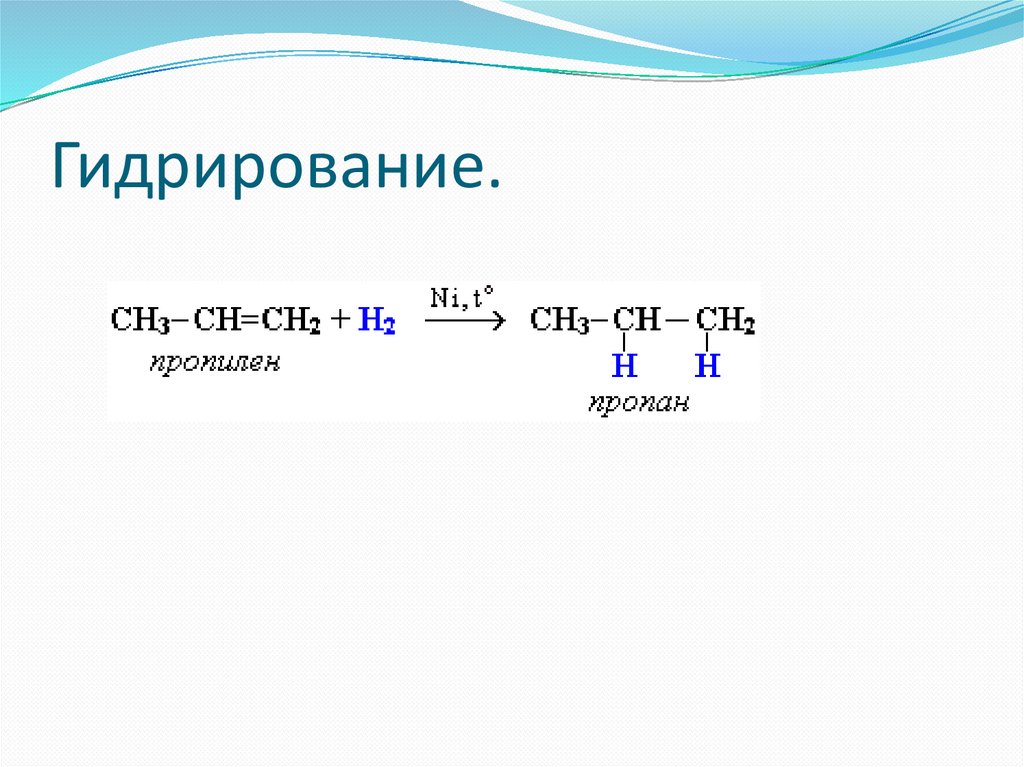
Гидрирование.13.
Галогенирование. Качественная реакцияна двойную связь. Обесцвечивание бромной воды.
14.
Гидрогалогенирование.Правило Марковникова (несимметричный
алкен).
15.
Гидратация.Тоже по правилу Марковникова,
обязательно при температуре.
16.
Горение.Полное (избыток О2)
С2H4 +3O2→ᵗ 2CO2 + 2H2O
Неполное (недостаток О2)
С2H4 +2O2→ᵗ 2CO + 2H2O
С2H4 +O2→ᵗ 2C + 2H2O
17.
О2 воздуха с катализатором.18.
Окислитель KMnO4Реакция Вагнера.
Качественная реакция на непредельные
УВ, обесцвечивание раствора.
19.
Полимеризация.Обязательно температура и давление.
20.
Типы реакций алкадиенов.Присоединения
-галогенирование
-гидрирование
Полимеризация
21.
Галогенирование.Обесцвечивание бромной воды.
При недостатке брома
При избытке брома
22.
Гидрирование.23.
Полимеризация.24.
Типы реакций алкинов.Присоединение
-гидрирование
-галогенирование
-гидрогалогенирование
-гидратация
Окисление
-горение
-с KMnO4
Полимеризация
Замещение атома водорода на металл
25.
Гидрирование. Температура 150С26.
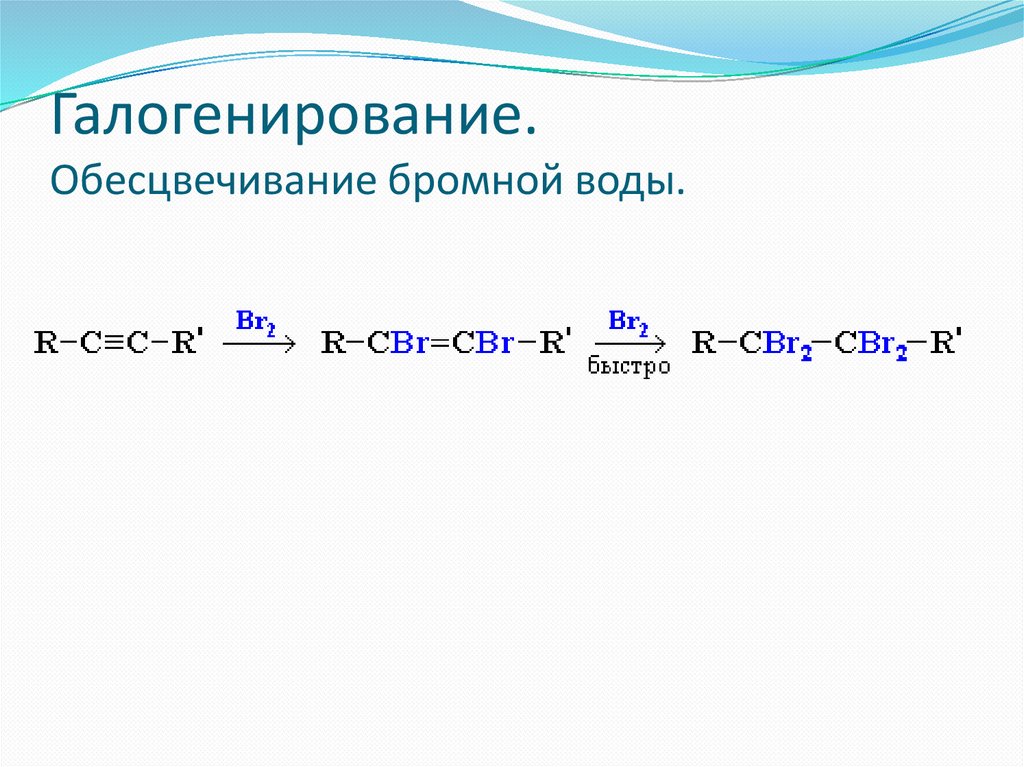
Галогенирование.Обесцвечивание бромной воды.
27.
Гидрогалогенирование.28.
Гидратация. Реакция Кучерова.29.
Горение (полное окисление).30.
Окисление KMnO4Качественная реакция, обесцвечивание
раствора.
CH3-C≡CH3 +8KMnO4 + 4H2O → CH3COOH + HCOOH +8MnO2 + 8KOH
этановая кислота+ метановая кислота
31.
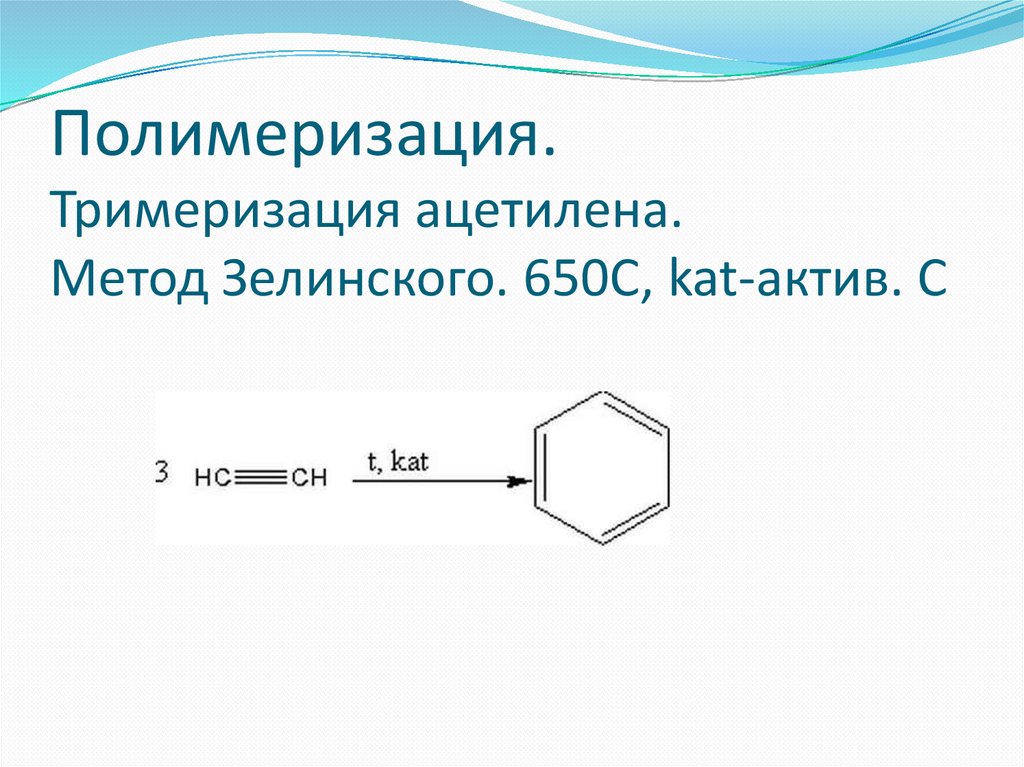
Полимеризация.Тримеризация ацетилена.
Метод Зелинского. 650С, kat-актив. С
32.
Замещение атомов водорода наметалл.
33.
Типы реакций бензола.Присоединение
-гидрирование
-хлора (др. галогены не вступают в реакцию)
Замещения
-галогенирования
-нитрование
-сульфирование
-алкилирование
Окисление
-горение
-с KMnO4 не вступает в реакцию
34.
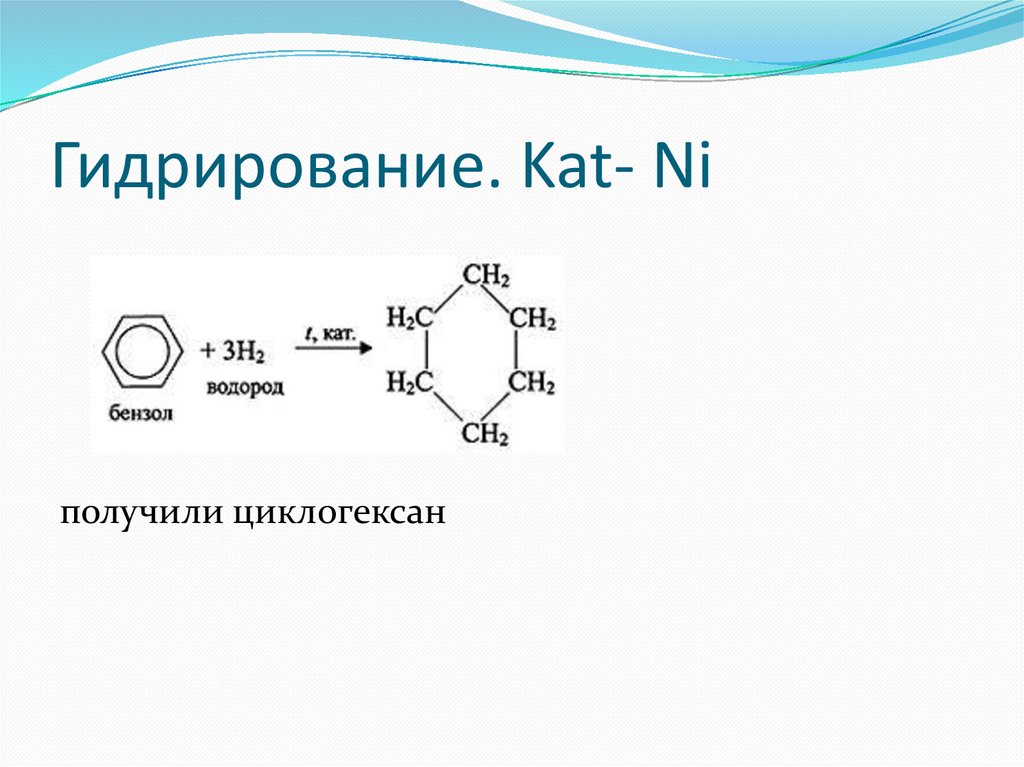
Гидрирование. Kat- Niполучили циклогексан
35.
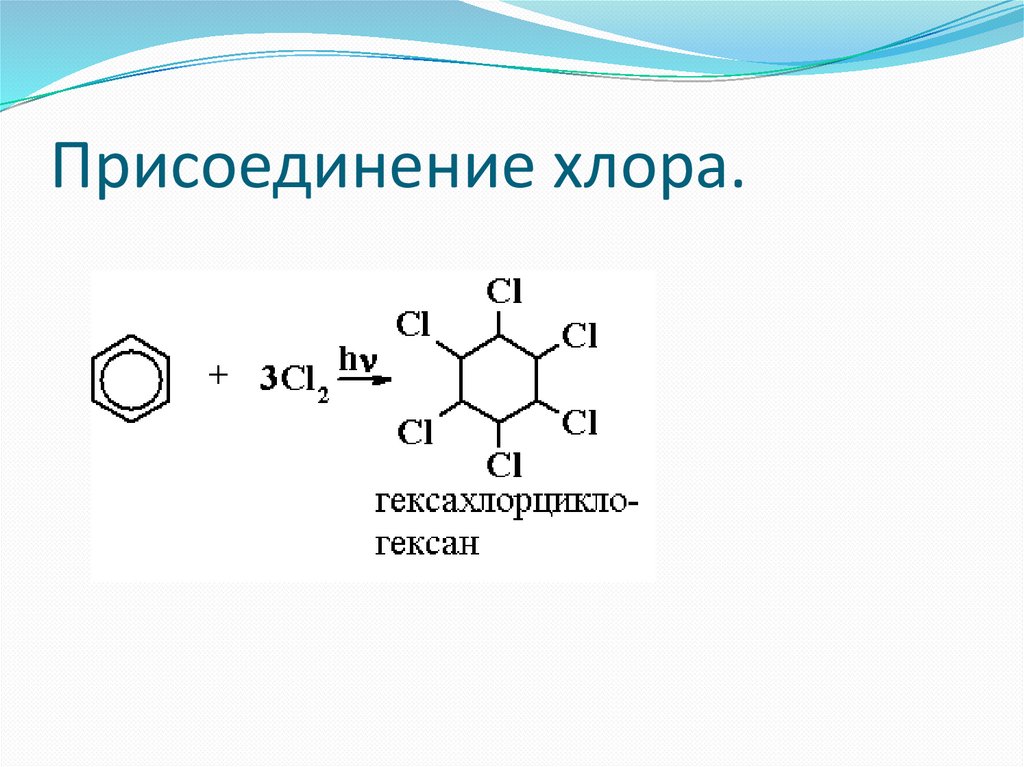
Присоединение хлора.36.
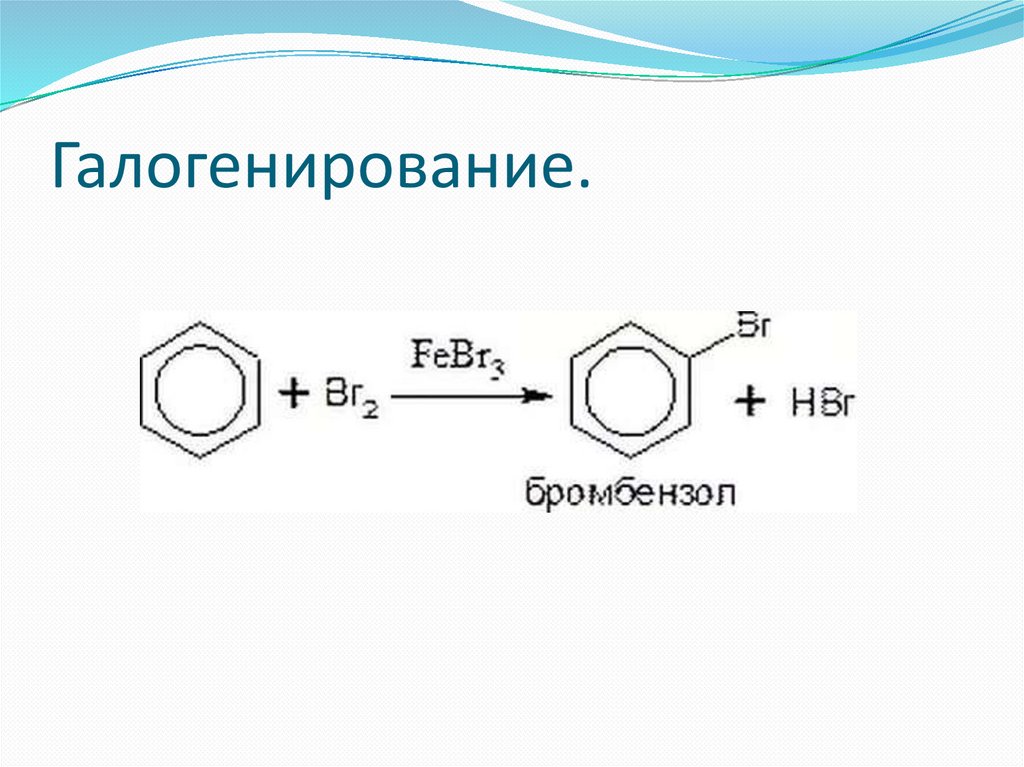
Галогенирование.37.
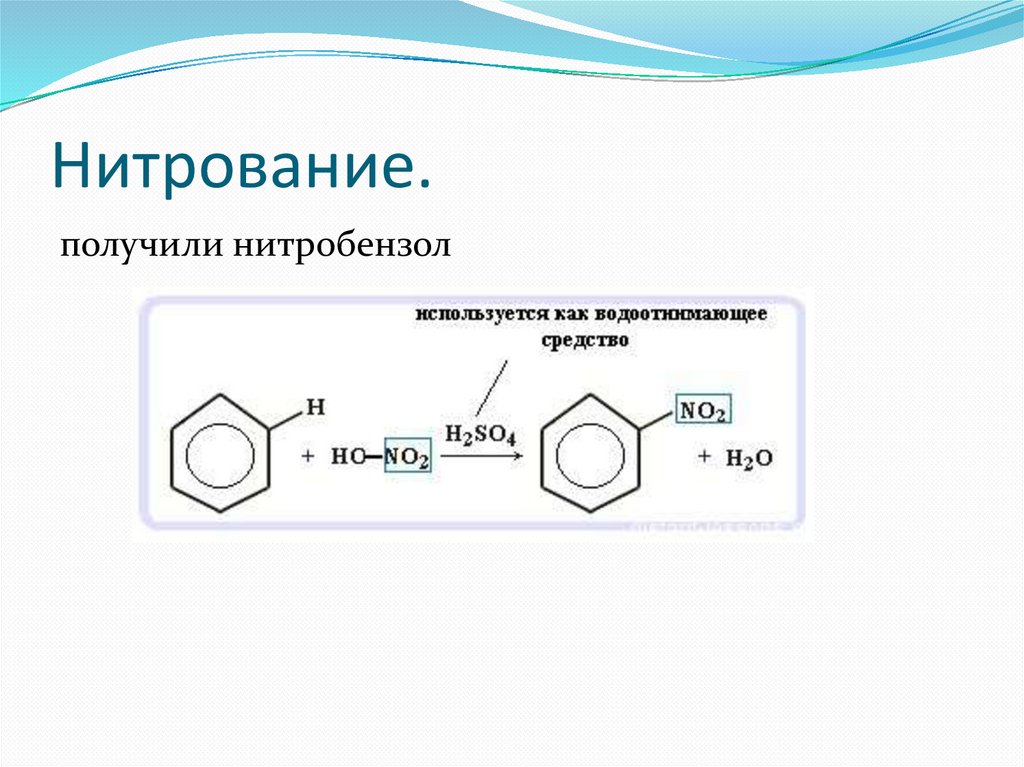
Нитрование.получили нитробензол
38.
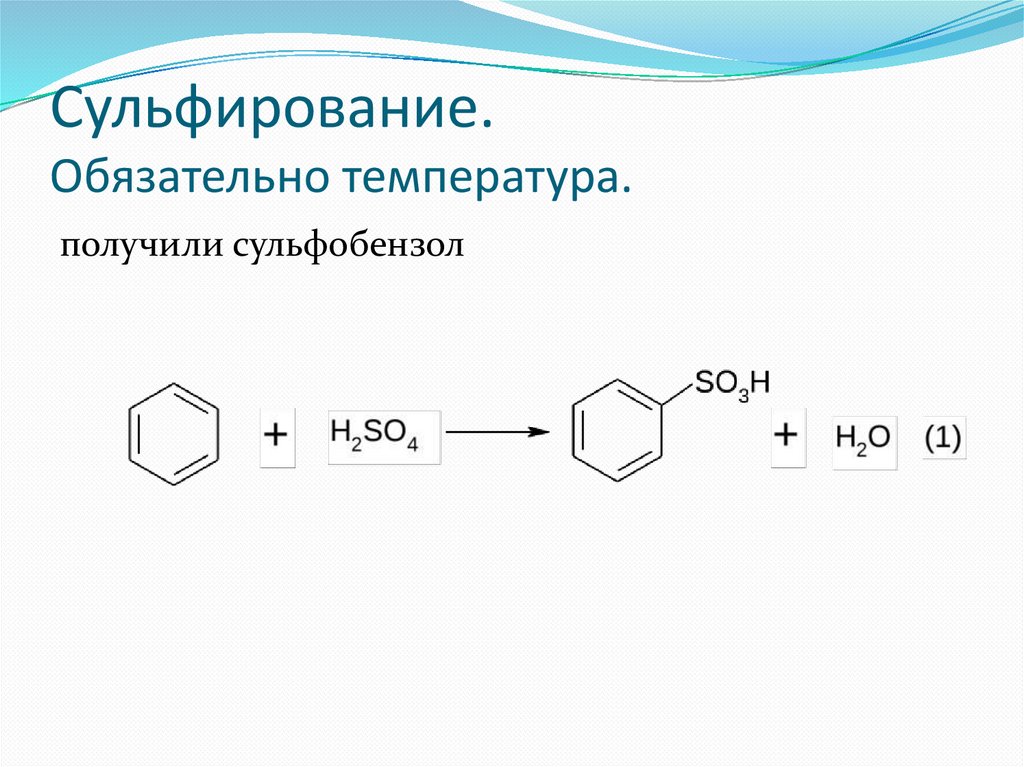
Сульфирование.Обязательно температура.
получили сульфобензол
39.
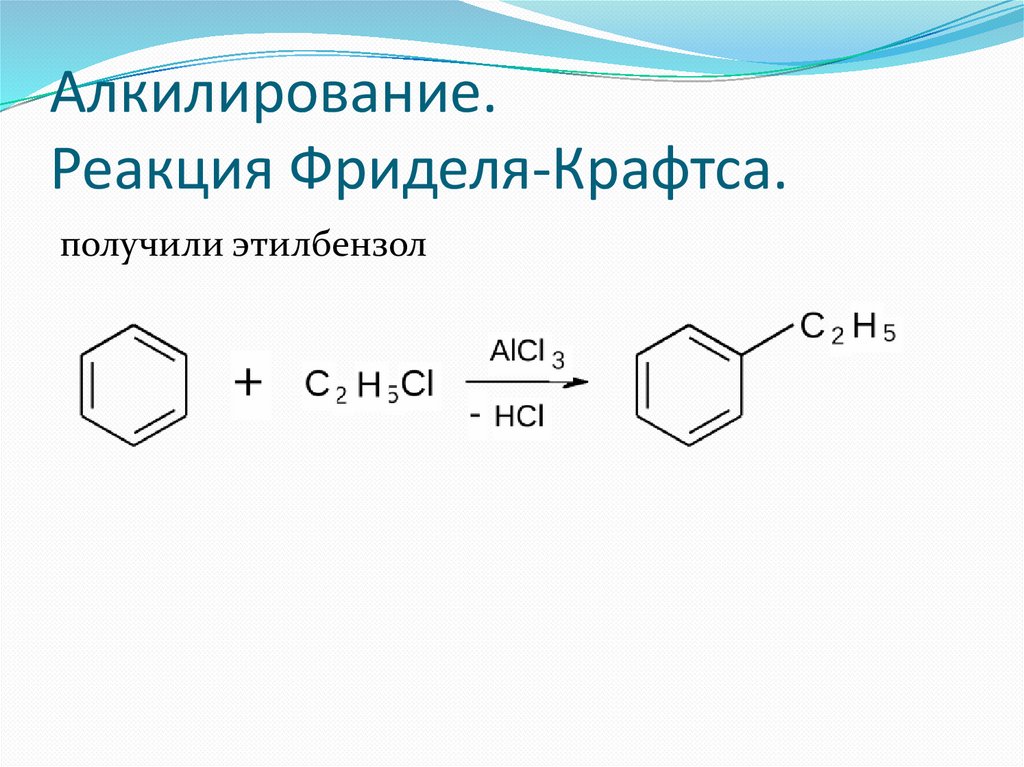
Алкилирование.Реакция Фриделя-Крафтса.
получили этилбензол
40.
Горение.41.
Типы реакций толуола.Реакции с участием бензольного кольца.
-галогенирование (бензольное кольцо, боковая цепь)
-нитрование
-сульфирование
-алкилирование
Присоединение (гидрирование)
Окисление
-горение
-с KMnO4
42.
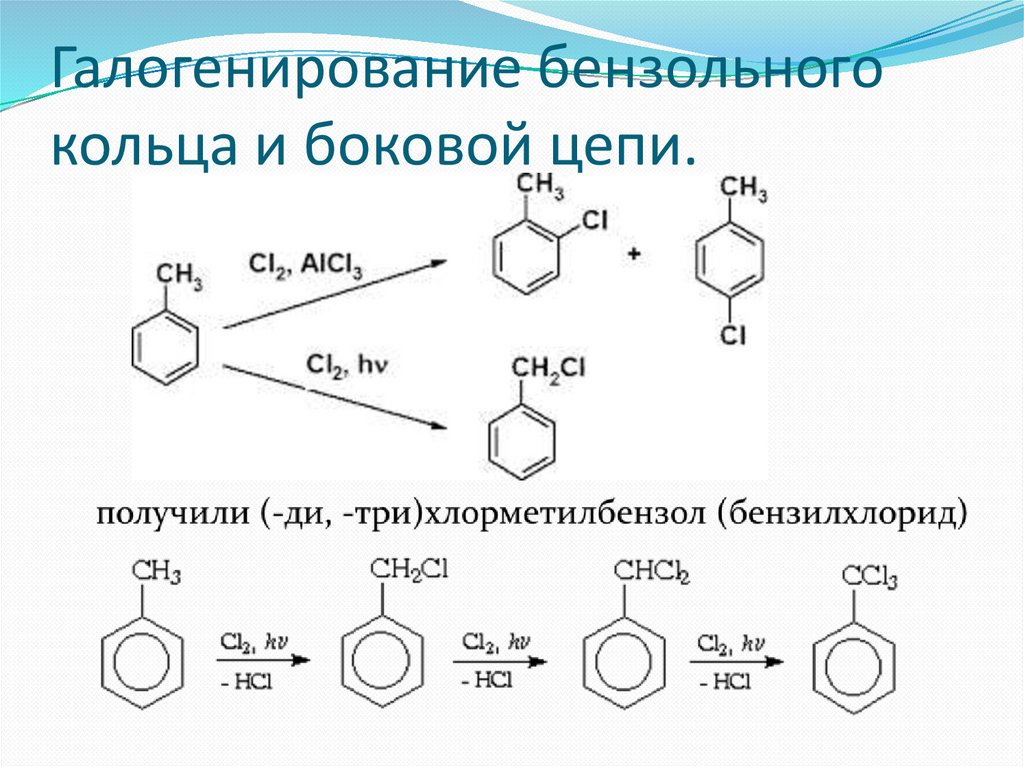
Галогенирование бензольногокольца и боковой цепи.
43.
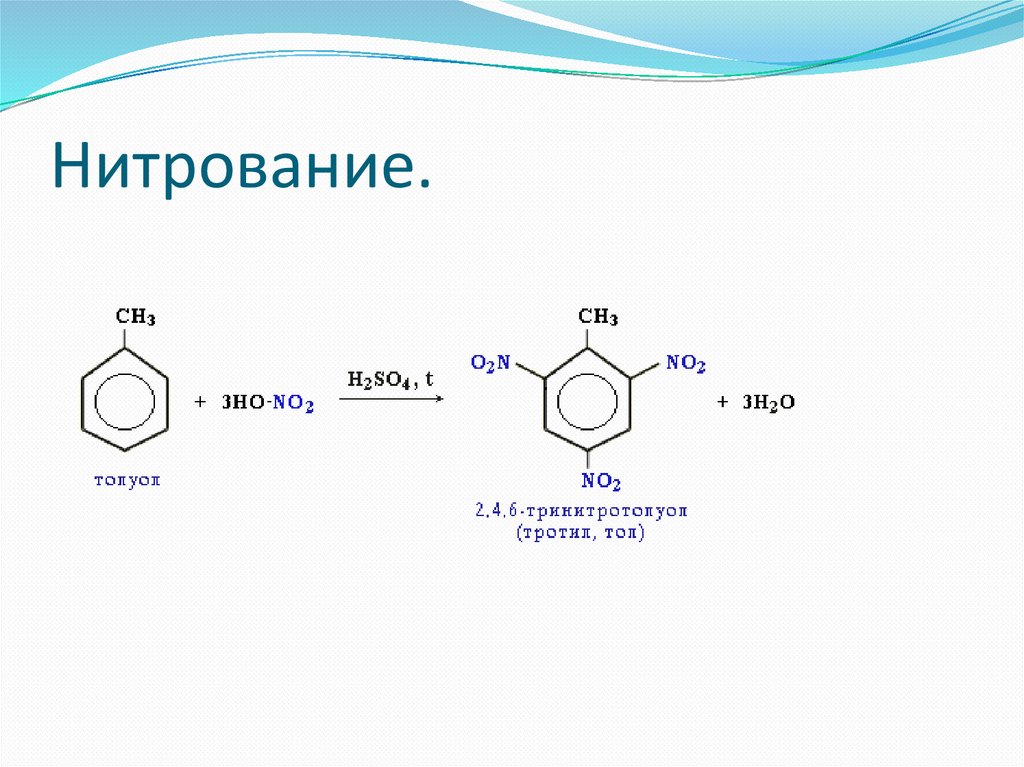
Нитрование.44.
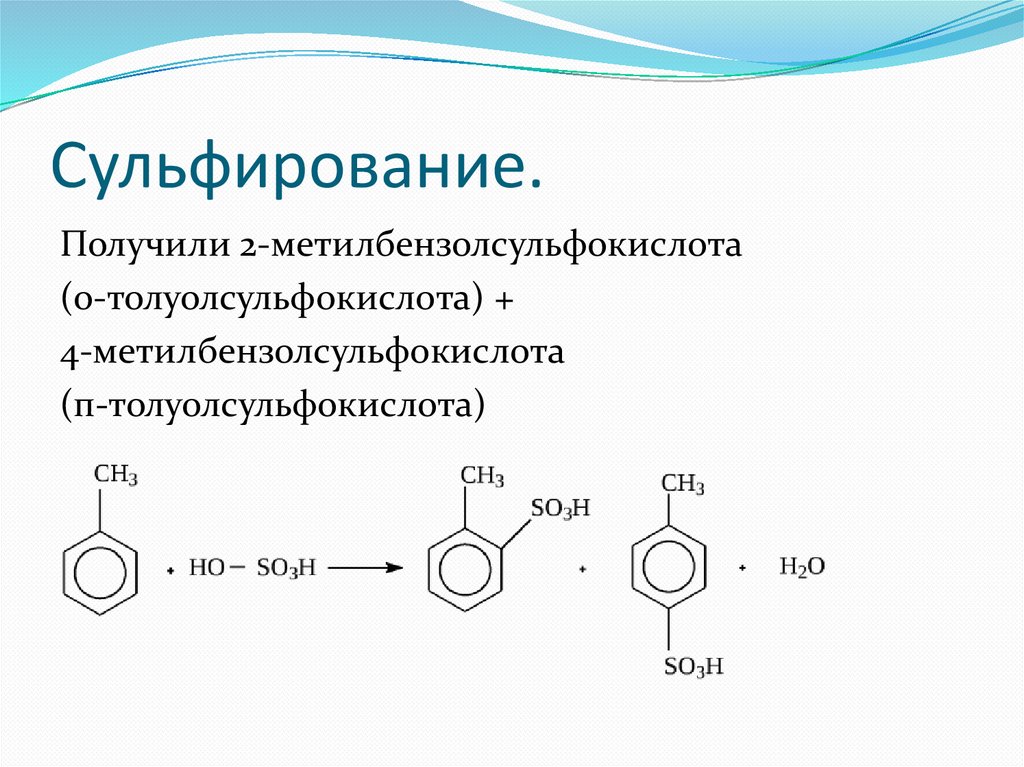
Сульфирование.Получили 2-метилбензолсульфокислота
(о-толуолсульфокислота) +
4-метилбензолсульфокислота
(п-толуолсульфокислота)
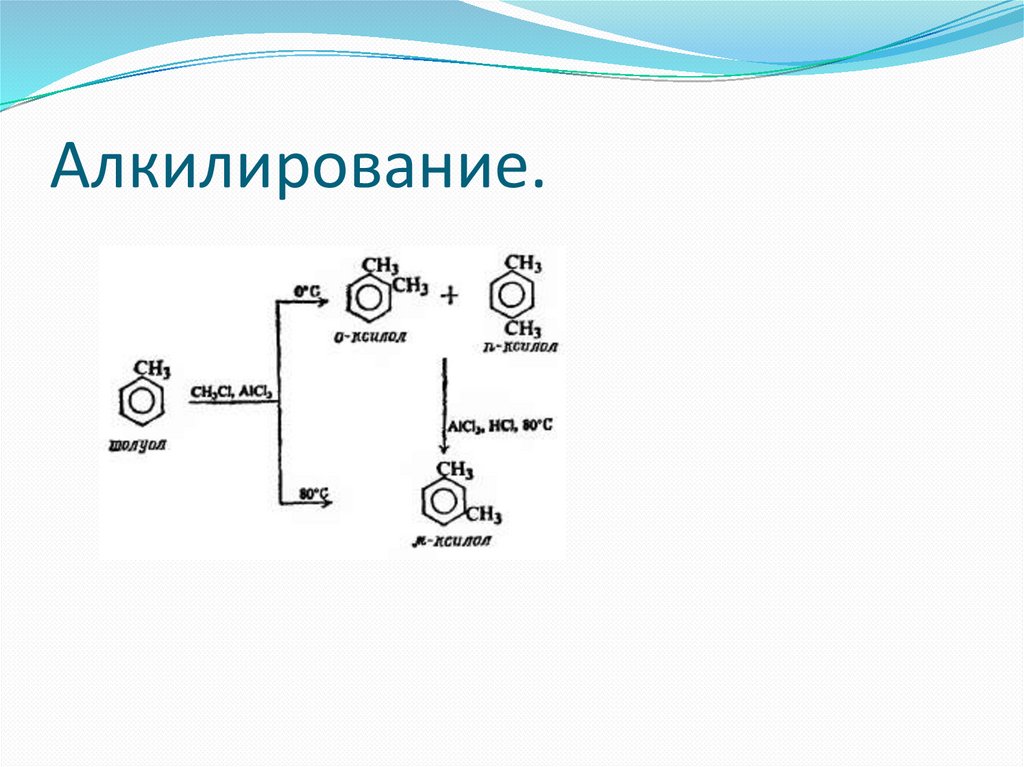
45.
Алкилирование.46.
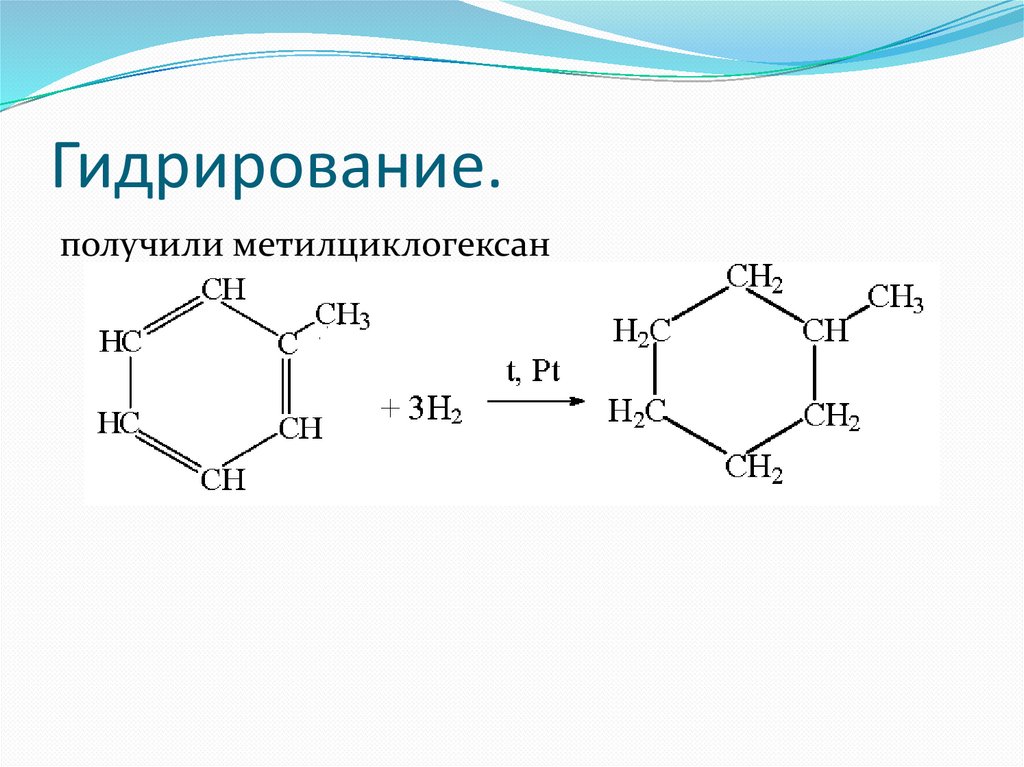
Гидрирование.получили метилциклогексан
47.
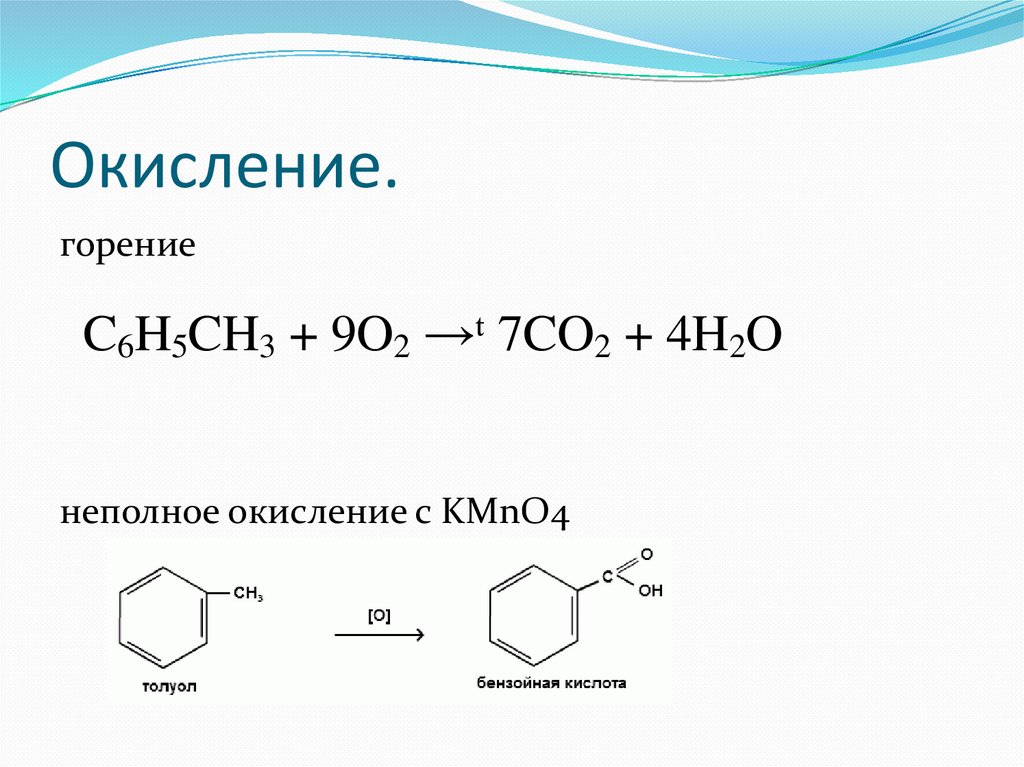
Окисление.горение
C6H5CH3 + 9O2 →ᵗ 7CO2 + 4H2O
неполное окисление с KMnO4
48.
Типы реакцийодноатомных спиртов.
Замещение
-с металлами
-с кислотами
-с галогенводородами
-с аммиаком
Отщепление
-дегидратация
-дегидрирование
Окисление
-горение
-неполное с KMnO4
49.
С металламиполучили этанолят натрия
50.
С кислотами- это реакцияэтерификации.
51.
С галогенводородами притемпературе.
получили бромэтан
52.
С аммиаком.53.
Дегидратация.54.
Дегидрирование.55.
ГорениеC2H5OH + 3O2→ᵗ 2CO2 + 3H2O
56.
Окисление KMnO457.
Типы реакциймногоатомный спиртов.
С щелочными металлами
С гидроксидами металлов
С кислотами
С галогенводородами
58.
С щелочными металлами.Получили тринатрийглицерат
59.
С гидроксидами металлов.Качественная реакция на многоатомные
спирты.
60.
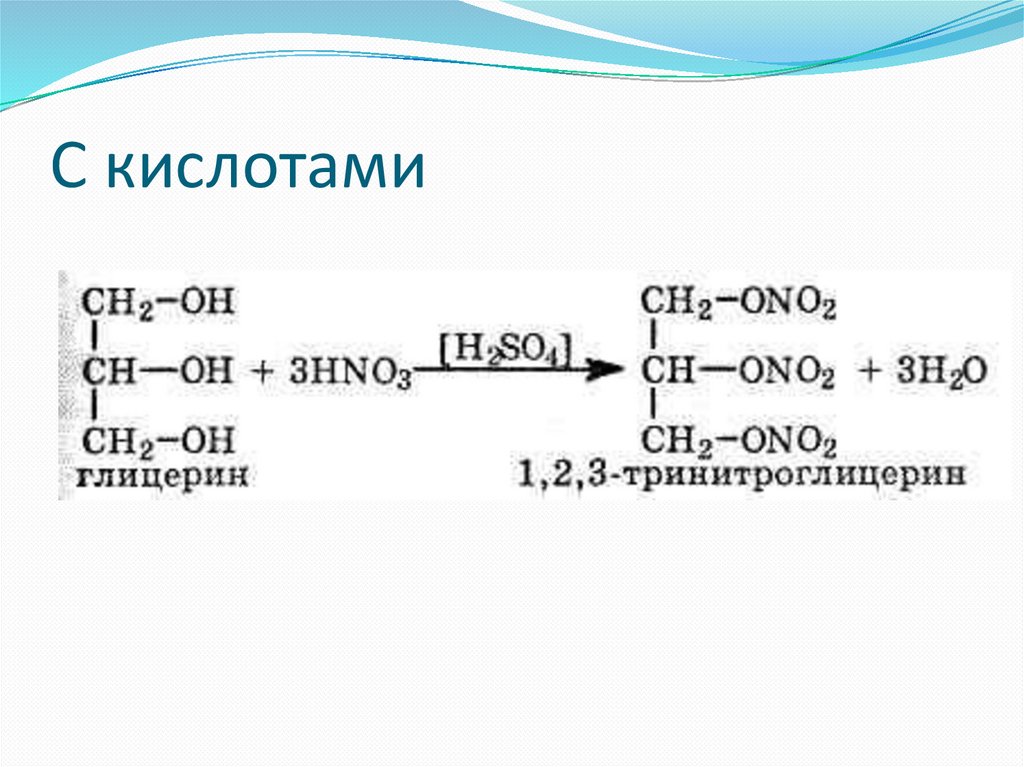
С кислотами61.
Типы реакций фенола.С участием гидроксильной группы
-с активными металлами
-с щелочами
С участием бензольного кольца
-замещение (галогенирование, нитрование,
сульфирование)
-присоединение (гидрирование)
62.
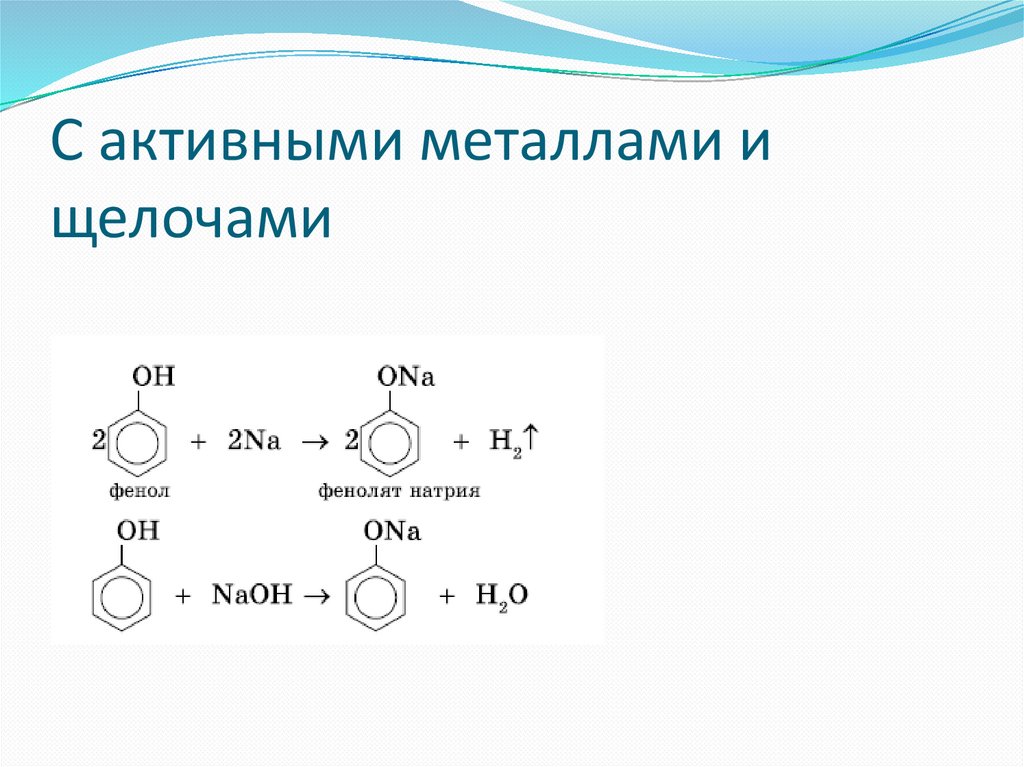
С активными металлами ищелочами
63.
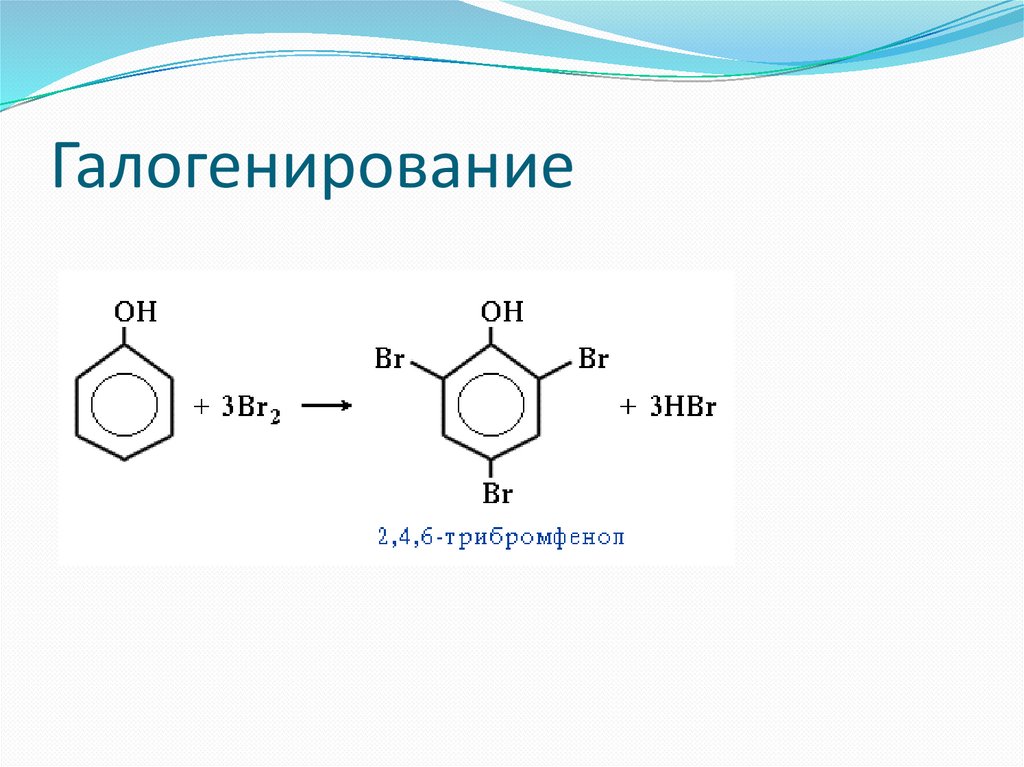
Галогенирование64.
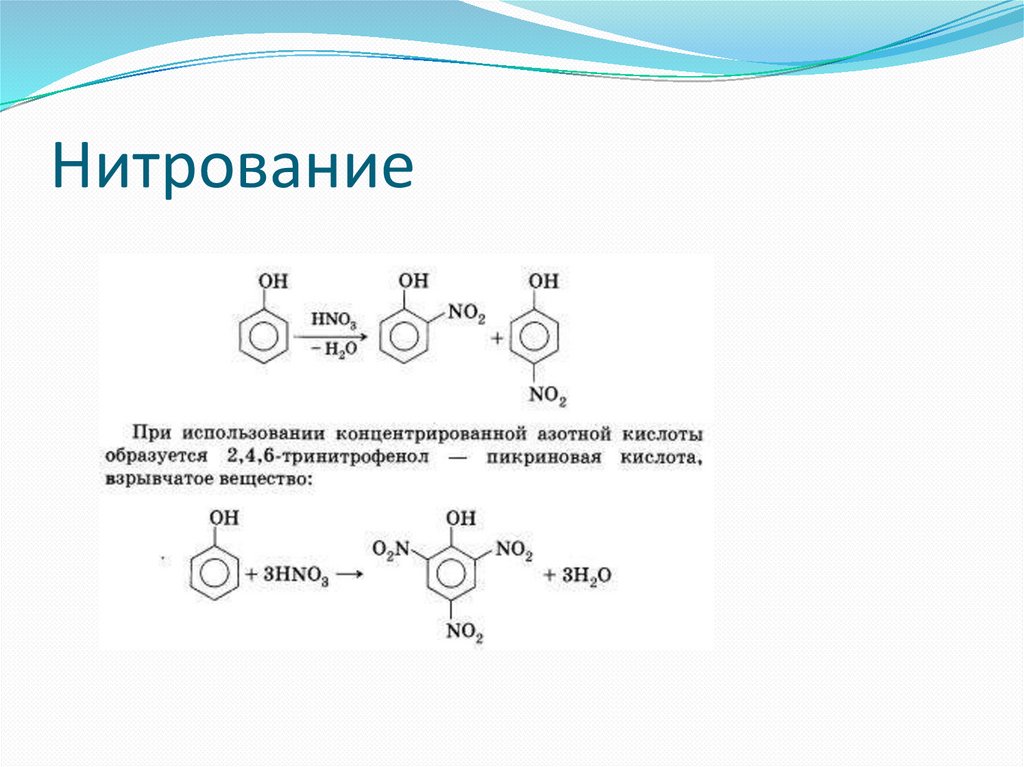
Нитрование65.
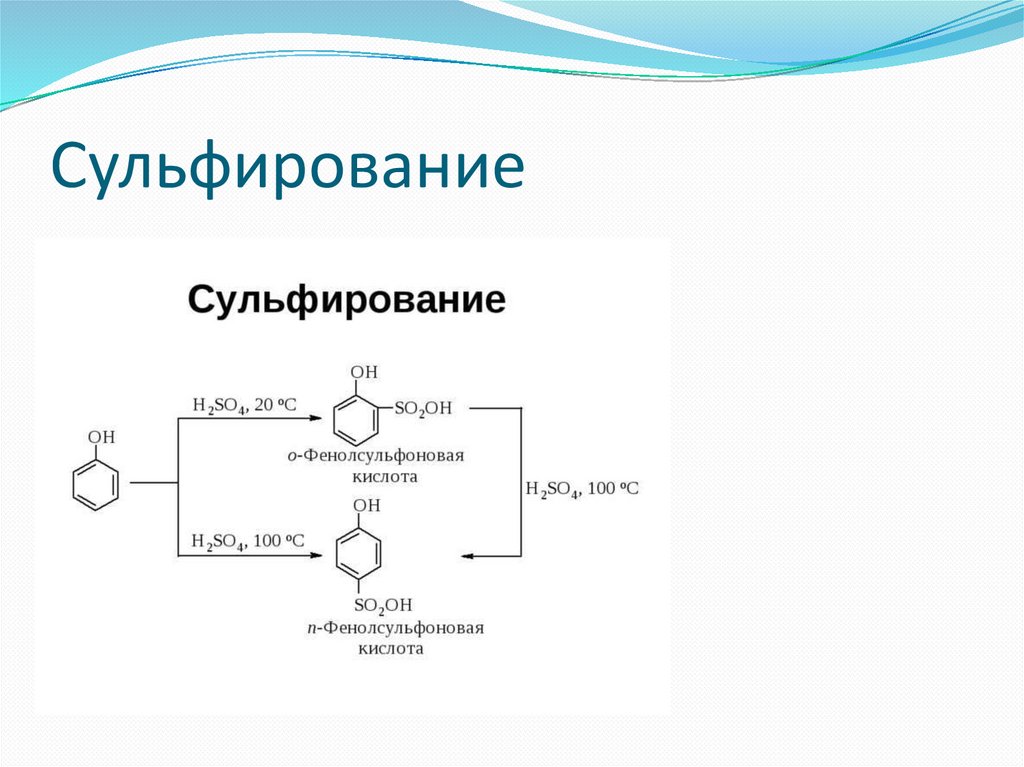
Сульфирование66.
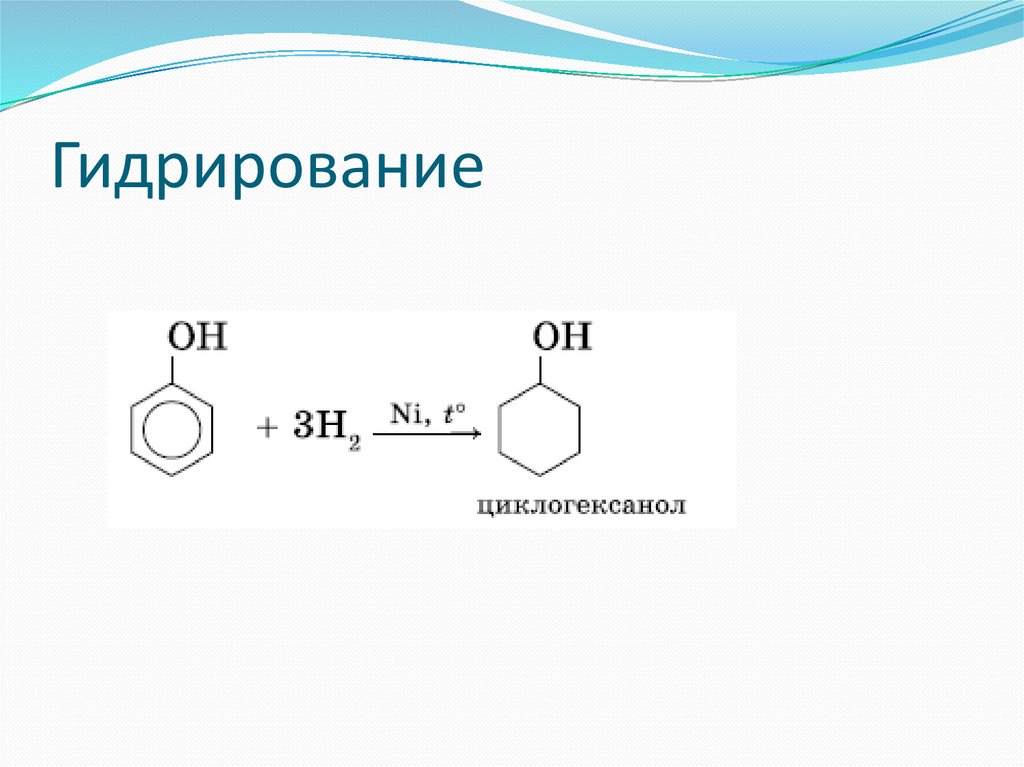
Гидрирование67.
Типы реакций альдегидов.Присоединение
-гидрирование
Окисление
-«серебряное зеркало»
-с Cu(OH)2
Полимеризация
Поликонденсация
68.
Гидрирование69.
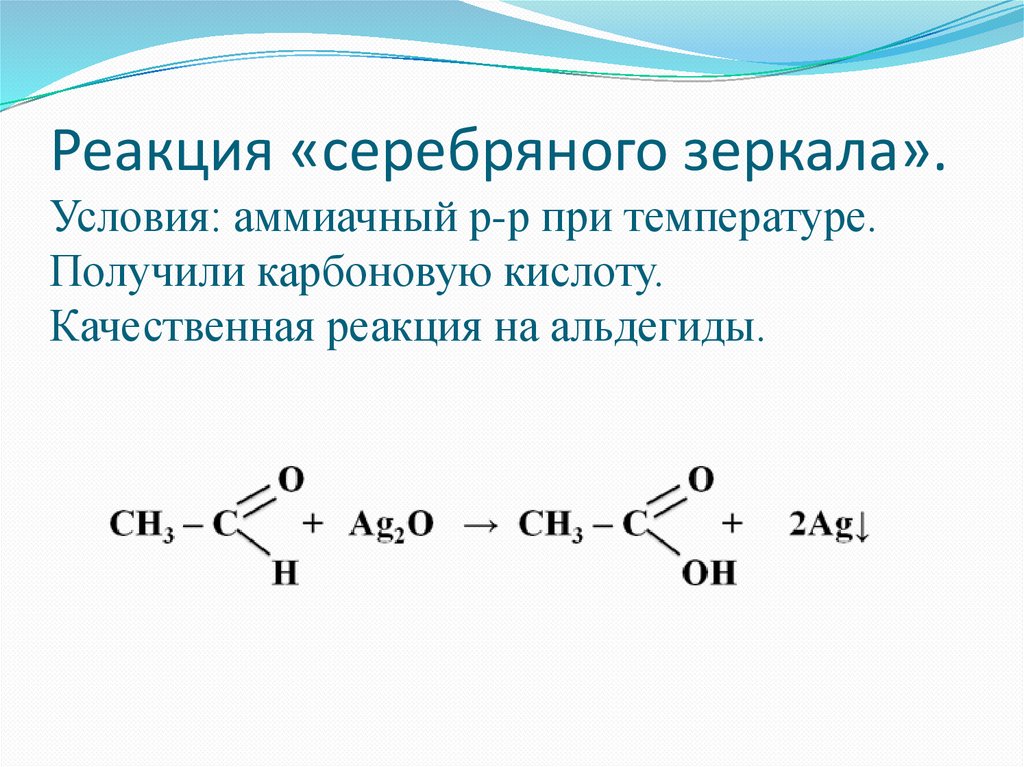
Реакция «серебряного зеркала».Условия: аммиачный р-р при температуре.
Получили карбоновую кислоту.
Качественная реакция на альдегиды.
70.
C Cu(OH)2Качественная реакция на альдегиды.
71.
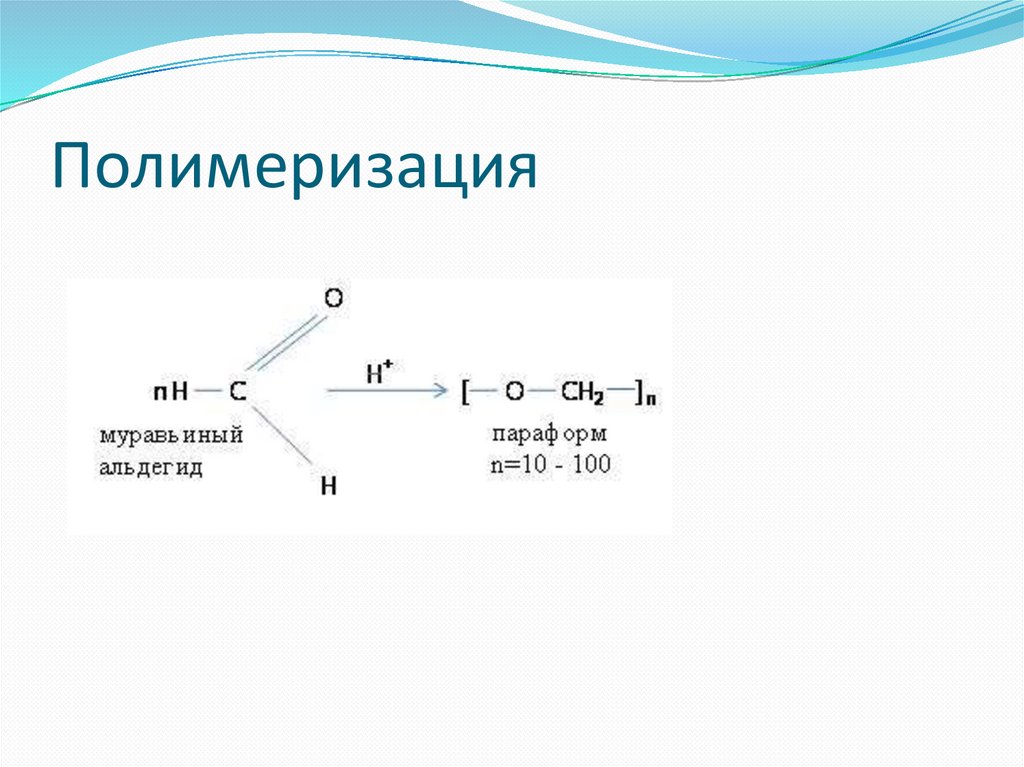
Полимеризация72.
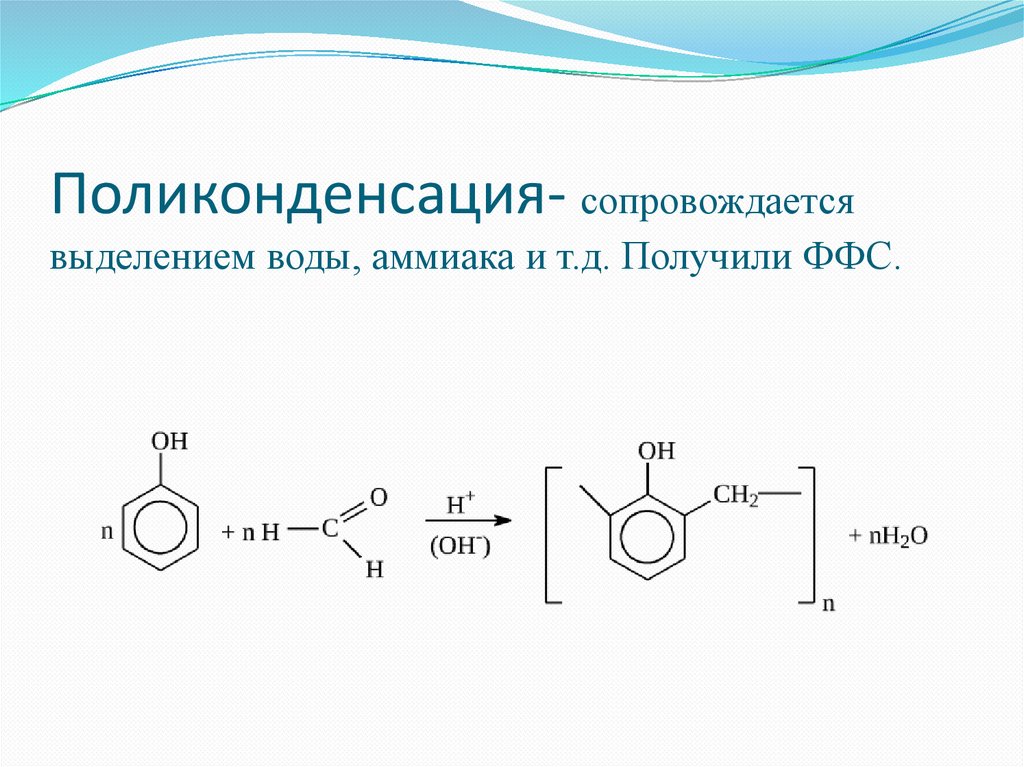
Поликонденсация- сопровождаетсявыделением воды, аммиака и т.д. Получили ФФС.
73.
Типы реакций карбоновыхкислот.
С активными металлами
С основными оксидами
С щелочами
С солями (карбонатами)
С аммиаком
Со спиртами
Межмолекуярная дегидротация.
74.
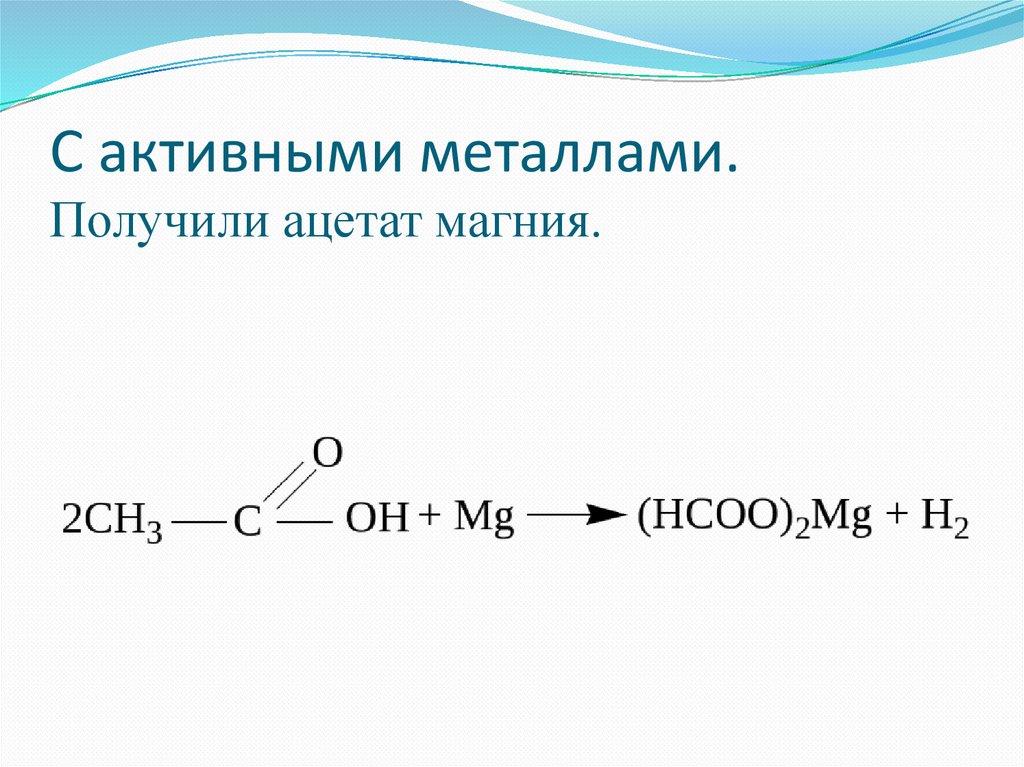
С активными металлами.Получили ацетат магния.
75.
С основными оксидами.2CH3COOH + CaO → (CH3COO)2Ca + H2O
ацетат кальция
76.
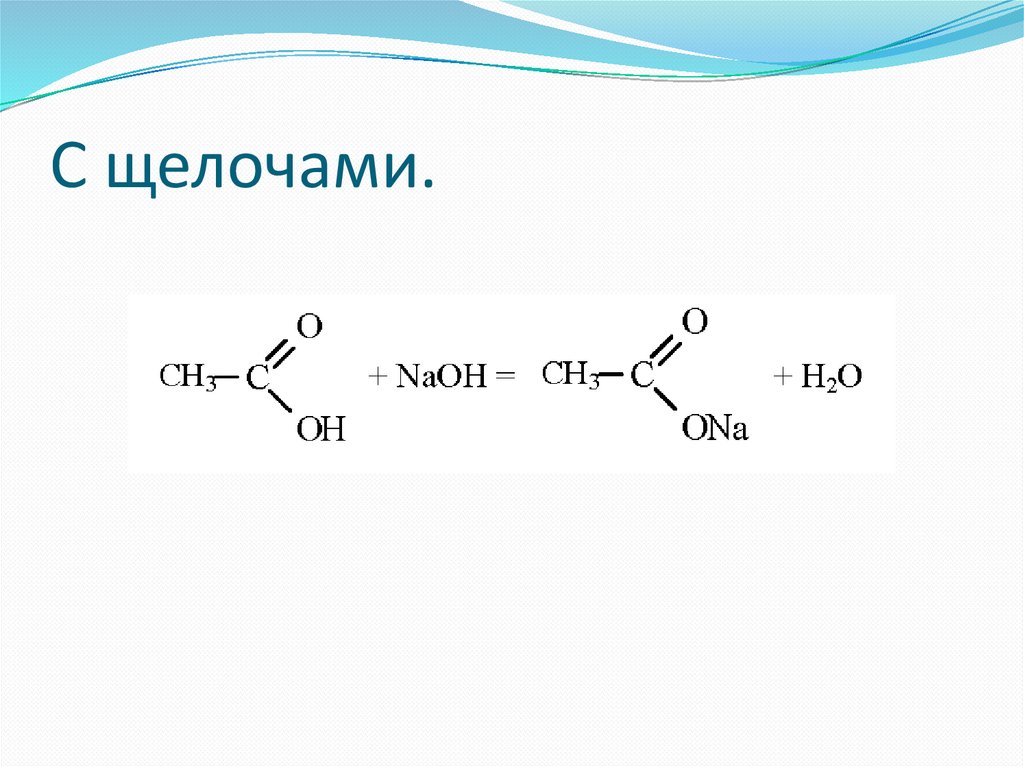
С щелочами.77.
С солями (карбонатами).2CH3COOH + Na2CO3 → 2CH3COONa + CO2↑ + H2O
ацетат натрия
78.
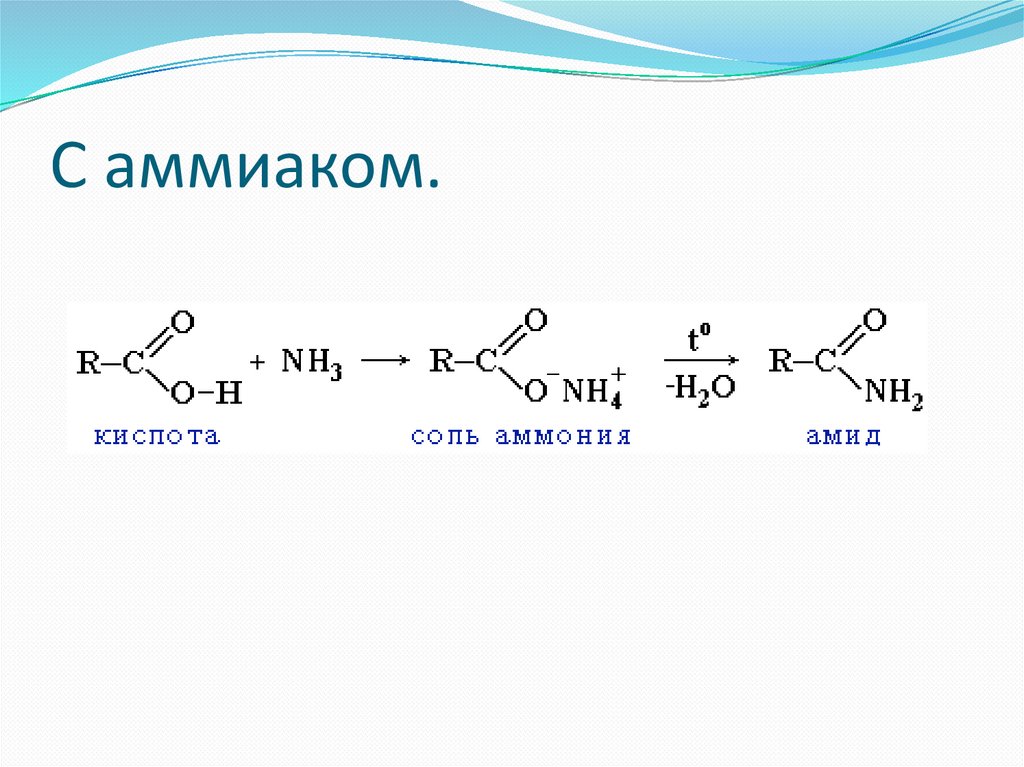
С аммиаком.79.
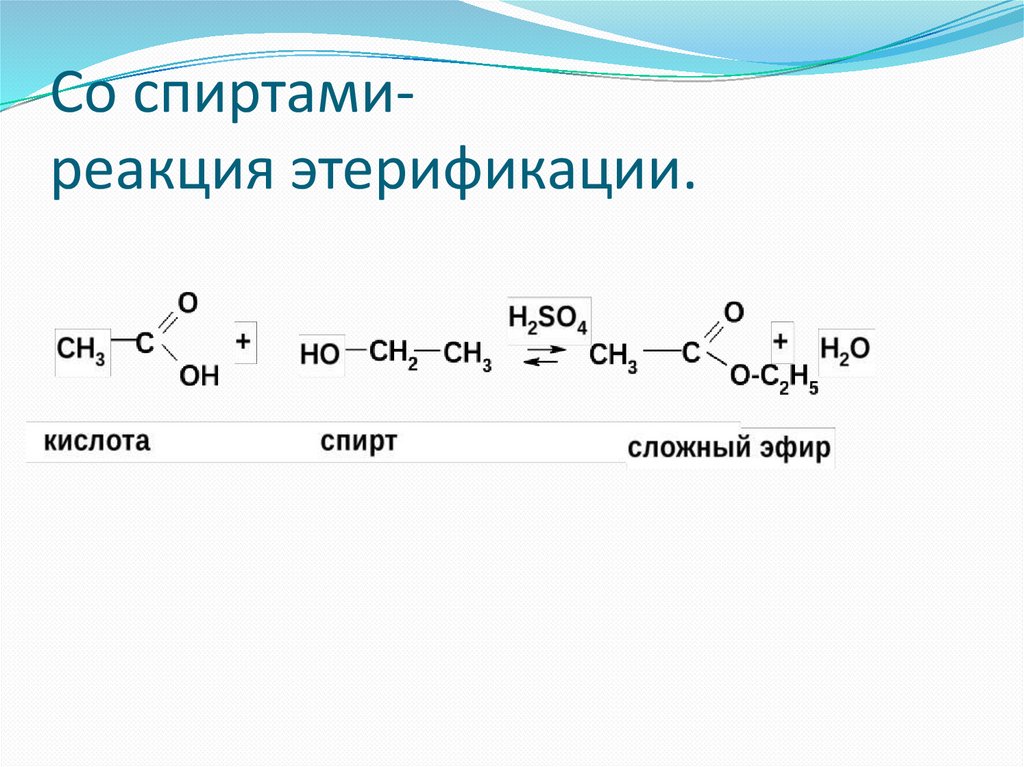
Со спиртамиреакция этерификации.80.
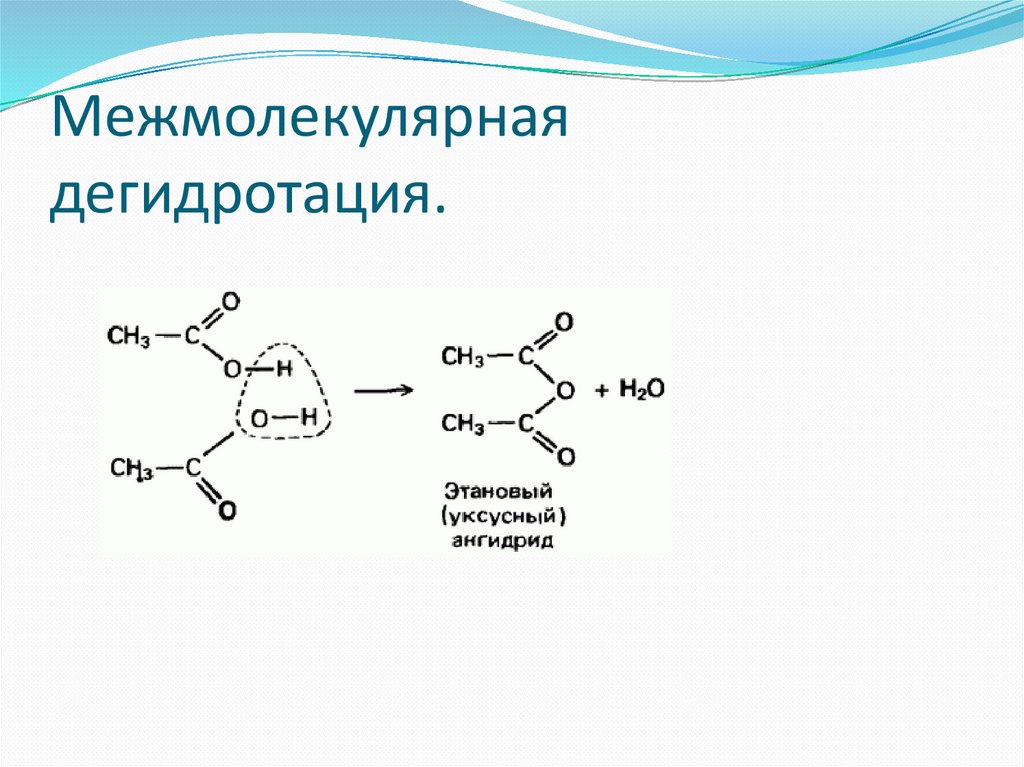
Межмолекулярнаядегидротация.

















































 Химия
Химия








