Похожие презентации:
Определите к какому классу относится оксид
1.
Давайте вспомним!2.
Работа с партнером по лицу (Опроспо карточкам)
3.
Определите к какому классуотносится оксид
Работа в группе
4.
25
5.
6.
7.
38.
9.
Тема и цель урока(видео)10.
Тема: ОснованияЦель:
Иметь знания по теме
основания;
Уметь выделять основания
среди других классов и
называть их
11.
Изучение нового материалаРабота с текстом с партнером по плечу
12.
Вопросы к текстуЗадания:
• Прочитайте текст.
• Ответьте на вопросы (устно в паре с партнером по
плечу):
• Что такое основания?
• Чем отличается щелочь от основания?
• Какое название является синонимом основанию?
• Как правильно назвать основание?
• Какие два типы оснований выделены в тексте?
• Какое агрегатное состояние характерно для оснований?
• В чем особенность амфотерных гидроксидов?
13.
ТЕКСТ ДЛЯ РАБОТЫ В ПАРЕОснования (гидроксиды) – сложные вещества, молекулы которых в своём составе имеют
одну или несколько гидроксо-групп (OH). Чаще всего основания состоят из атома
металла и группы OH. Например, NaOH – гидроксид натрия, Ca(OH)2 – гидроксид
кальция и др.
Названия оснований формируются следующим образом: Сначала необходимо указать
название класса: гидроксид, а затем название металла в родительном падеже.
Существует основание – гидроксид аммония, в котором гидрокси-группа присоединена не к
металлу, а к иону NH4+ (катиону аммония). Гидроксид аммония образуется при
растворении аммиака в воде (реакции присоединения воды к аммиаку):
NH3 + H2O = NH4OH (гидроксид аммония).
Степень окисления гирокси-группы – 1. Число гидроксильных групп в молекуле основания
зависит от степени окисления металла и равно ей. Например, NaOH, LiOH, Al (OH)3,
Ca(OH)2, Fe(OH)3 и т.д.
Все основания – твёрдые вещества, которые имеют различную окраску. Некоторые
основания хорошо растворимы в воде (NaOH, KOH и др.). Однако большинство из них в
воде не растворяются.
Растворимые в воде основания называются щелочами. Растворы щелочей «мыльные»,
скользкие на ощупь и довольно едкие. К щелочам относят гидроксиды щелочных и
щелочноземельных металлов (KOH, LiOH, RbOH, NaOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2 и
др.). Остальные являются нерастворимыми.
Нерастворимые основания – это амфотерные гидроксиды(т.е. проявляют свойства, как
кислот, так и оснований), которые при взаимодействии с кислотами выступают как
основания, а со щёлочью ведут себя, как кислоты.
14.
Закрепим15.
Лабораторная работа16.
Для работы в группеХод работы:
Положите перед собой таблицу № 7 и бланк для проведения лабораторной работы.
Опыт № 1.
Выберите 4 любые пробирки с веществами ( пронумерованные № 1,2,3,4)
Возьмите склянку с лакмусом и добавьте в каждую из трех пробирок по 5-7 капель индикатора.
Зафиксируйте изменение цвета раствора в бланке для проведения лабораторной работы
Опыт № 2.
Выберите 4 любые пробирки с веществами ( пронумерованные № 1,2,3,4)
Возьмите склянку с Фенолфталеином и добавьте в каждую из трех пробирок по 5-7 капель индикатора.
Зафиксируйте изменение цвета раствора в бланке для проведения лабораторной работы
Опыт № 3.
Выберите 4 любые пробирки с веществами ( пронумерованные № 1,2,3,4)
Возьмите склянку с метиловым оранжевым и добавьте в каждую из трех пробирок по 5-7 капель
индикатора.
Зафиксируйте изменение цвета раствора в бланке для проведения лабораторной работы
Опыт № 4.
Выберите 4 оставшиеся пробирки с веществами ( пронумерованные № 1,2,3,4)
Возьмите 4 универсальные индикаторные бумажки и опустите в каждую из пробирок
зафиксируйте изменение цвета индикаторной бумаги в бланке для проведения лабораторной работы
17.
Как я поработал(а)?18.
СПАСИБО ЗА УРОК!!!Желаю успехов в изучении химии



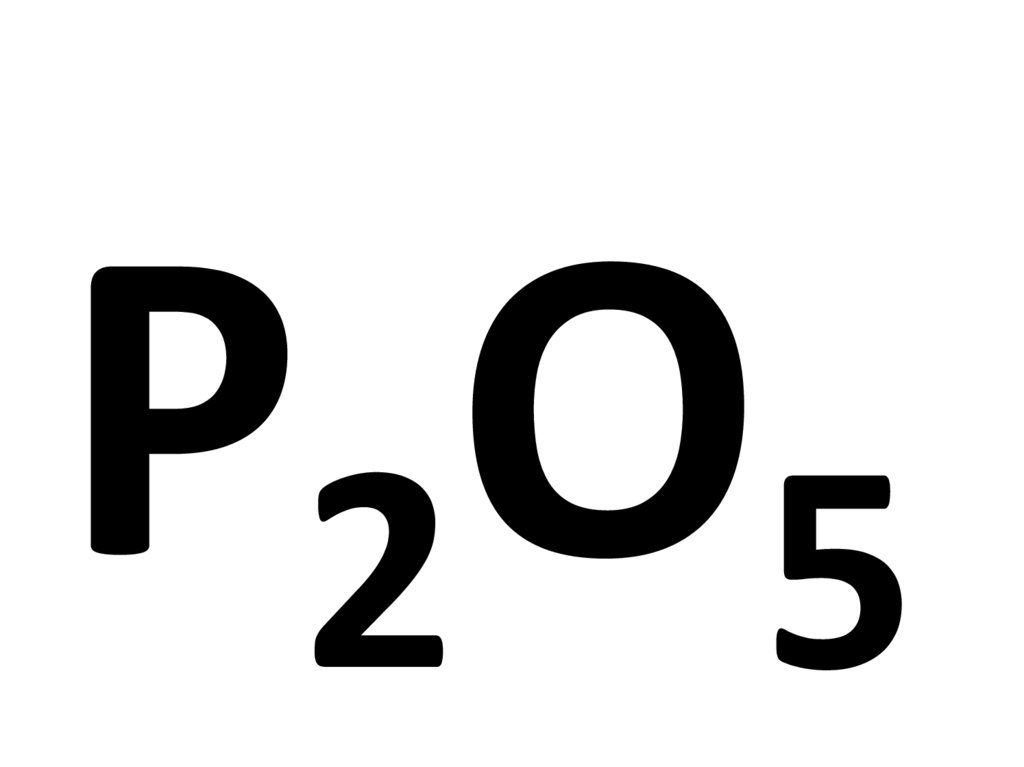


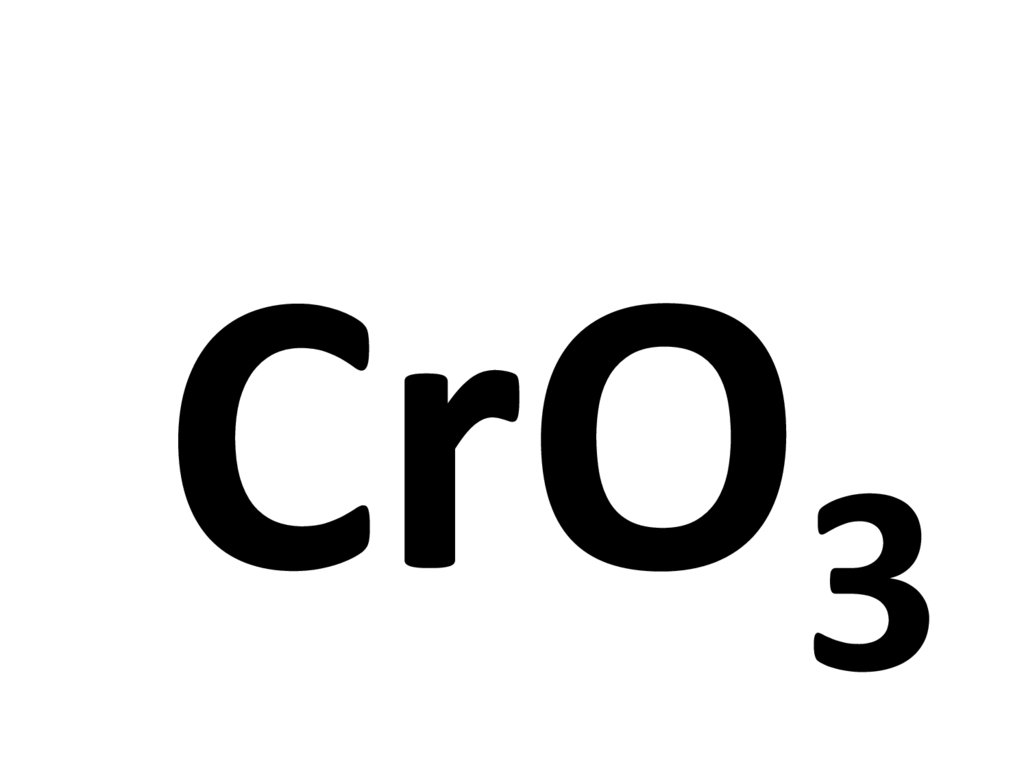











 Химия
Химия








