Похожие презентации:
Алкены - непредельные ациклические углеводороды
1.
Алкены2.
Алкены – непредельные ациклические углеводородынепредельные
ациклические
углеводороды
3.
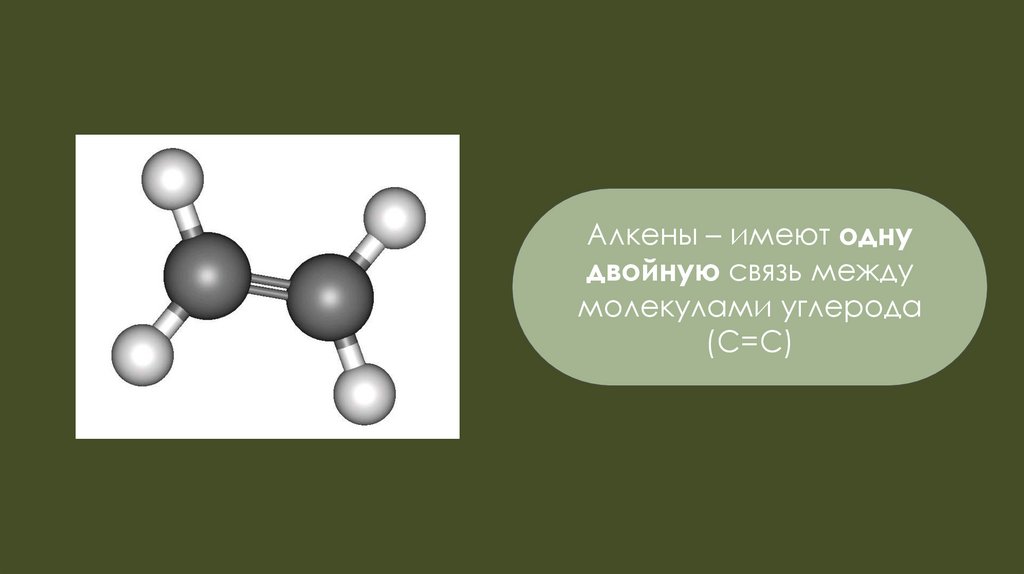
Алкены – имеют однудвойную связь между
молекулами углерода
(С=С)
4.
Общая формула алкенов:CnH2n
5.
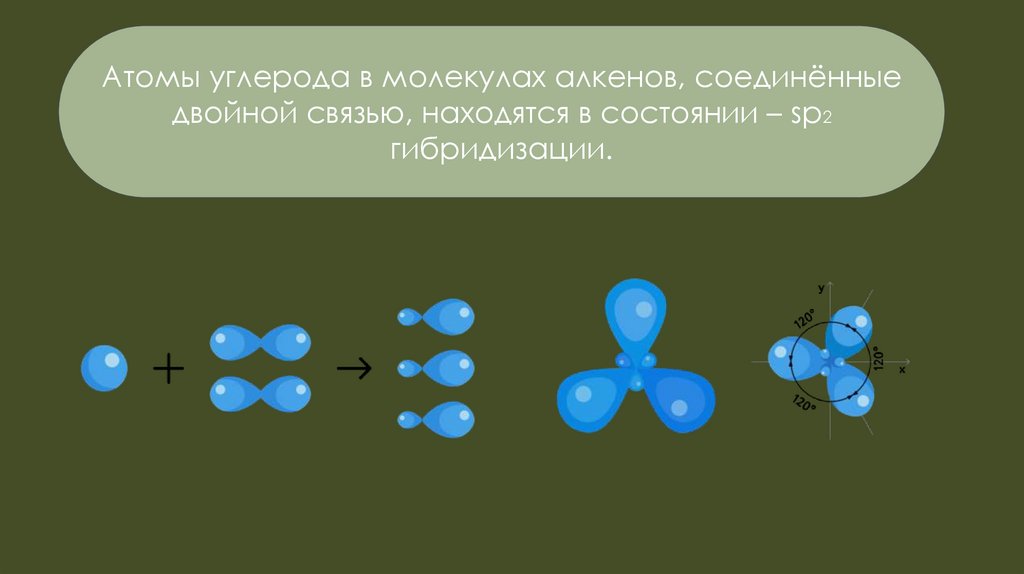
Атомы углерода в молекулах алкенов, соединённыедвойной связью, находятся в состоянии – sp2
гибридизации.
6.
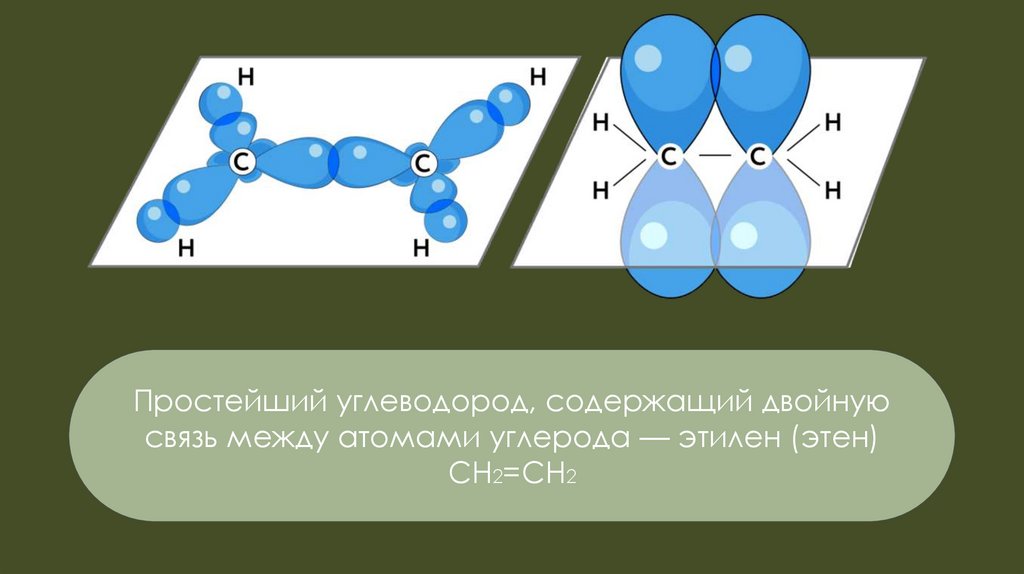
Простейший углеводород, содержащий двойнуюсвязь между атомами углерода — этилен (этен)
CH2=CH2
7.
Номенклатура алкенов:При составлении
названий алкенов по
международной
номенклатуре следует
придерживаться
следующих правил:
Название алкена
происходит от
названия
соответствующего
алкана, путём замены
суффикса –ан на –ен
8.
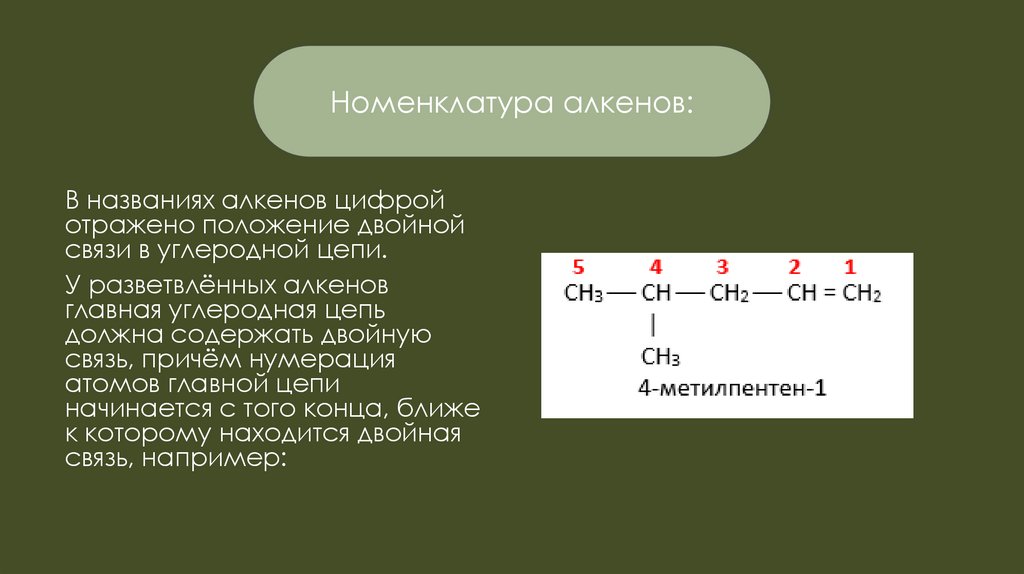
Номенклатура алкенов:В названиях алкенов цифрой
отражено положение двойной
связи в углеродной цепи.
У разветвлённых алкенов
главная углеродная цепь
должна содержать двойную
связь, причём нумерация
атомов главной цепи
начинается с того конца, ближе
к которому находится двойная
связь, например:
9.
ИзомерыВещества, имеющие одинаковую
молекулярную формулу, но разное
строение и разные физические и
химические свойства
10.
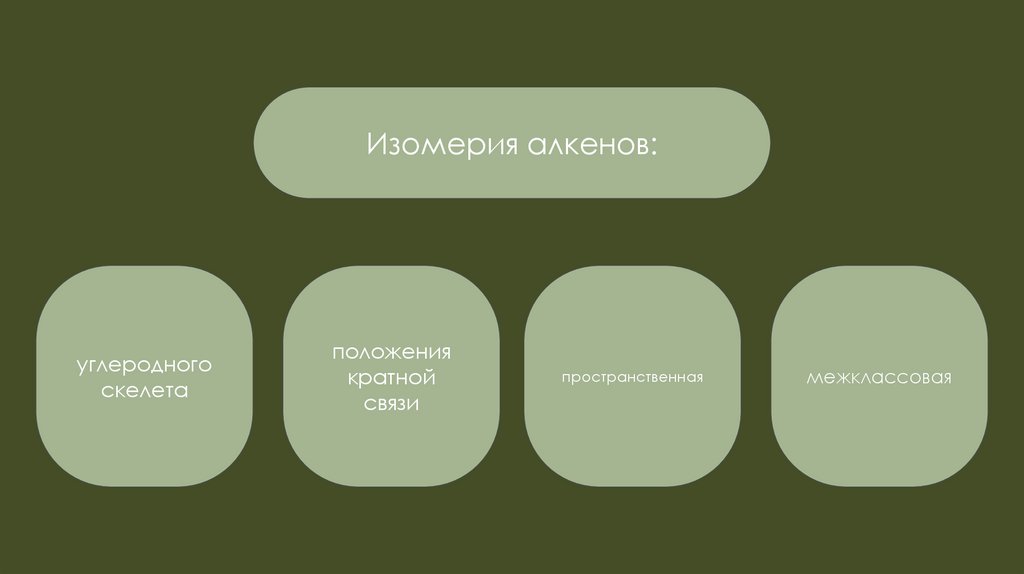
Изомерия алкенов:углеродного
скелета
положения
кратной
связи
пространственная
межклассовая
11.
Изомерия углеродного скелета:Изменение
углеродной цепи
вещества
12.
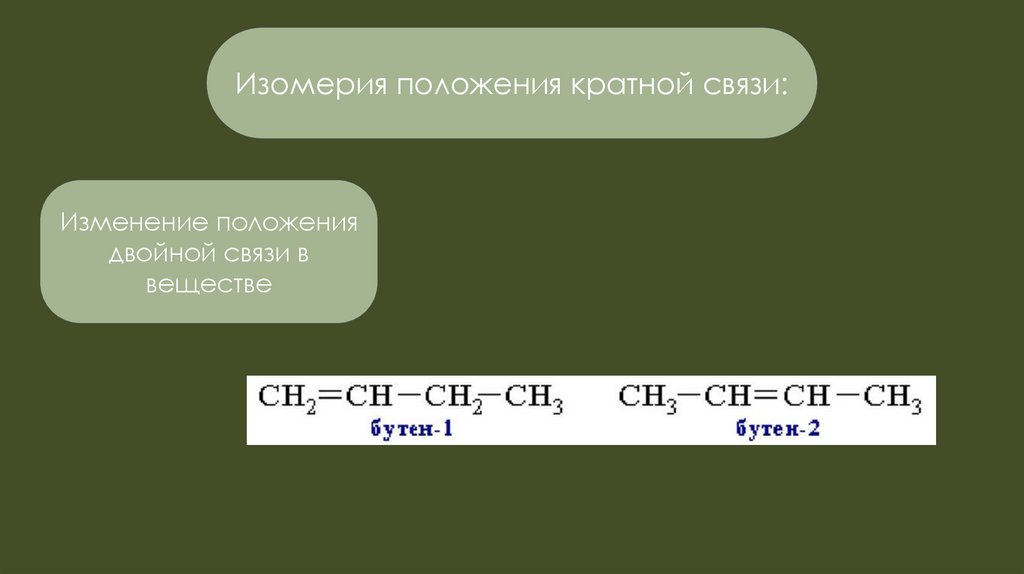
Изомерия положения кратной связи:Изменение положения
двойной связи в
веществе
13.
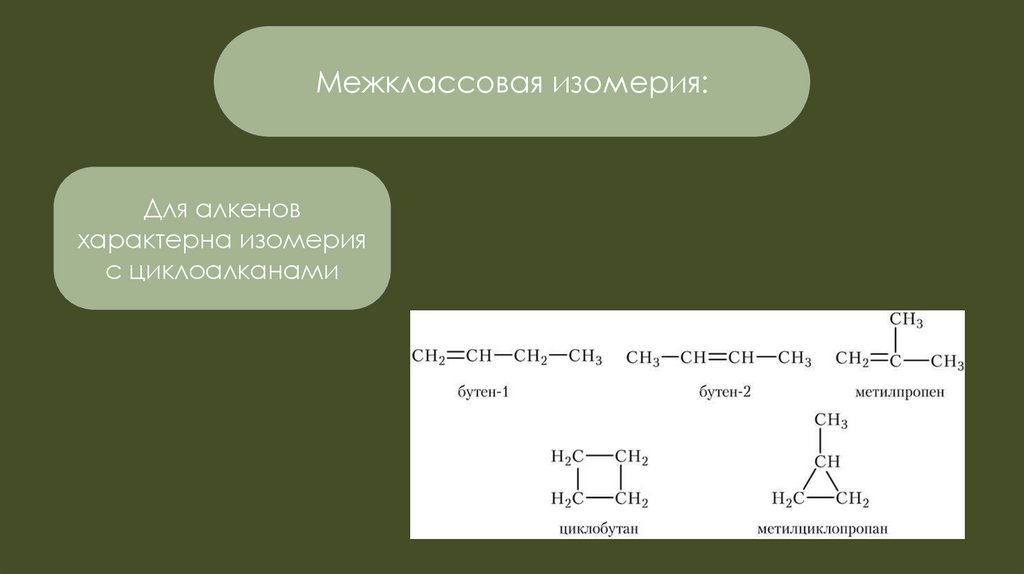
Межклассовая изомерия:Для алкенов
характерна изомерия
с циклоалканами
14.
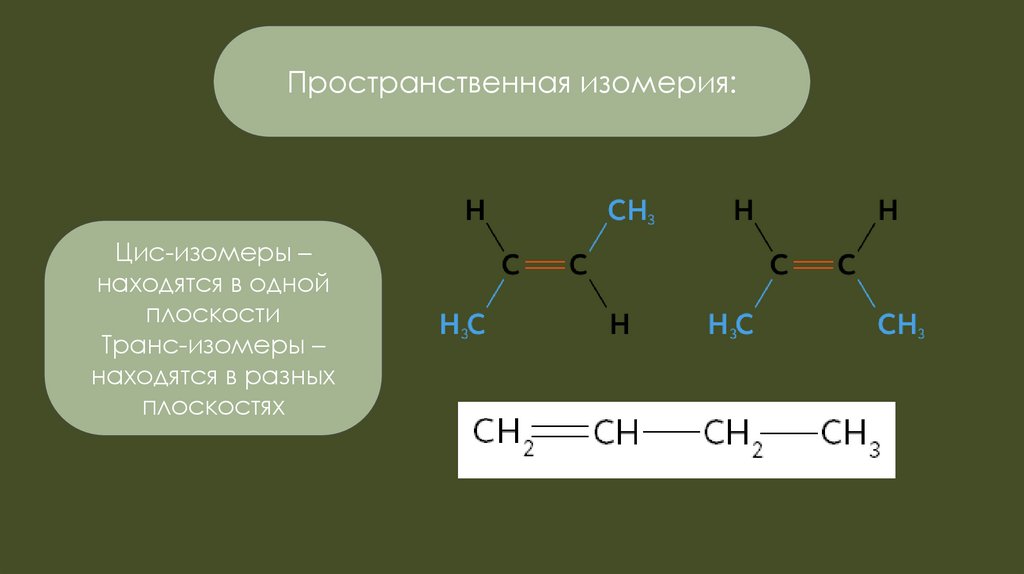
Пространственная изомерия:Цис-изомеры –
находятся в одной
плоскости
Транс-изомеры –
находятся в разных
плоскостях
15.
Физические свойства алкенов:По физическим свойствам алкены похожи на алканы:
при обычных условиях первые представители алкенов
— С2Н4 – С4Н8 — газы,
— С5Н10 – С17Н34 — жидкости,
алкены с большим числом атомов углерода — твёрдые
вещества.
Температура кипения алкенов неразветвлённого строения выше,
чем у их изомеров с разветвлённой цепью. Температуры
плавления транс-изомеров, как правило, выше, чем цисизомеров.
Все алкены бесцветны, жидкие имеют неприятный запах; алкены
практически нерастворимы в воде, но хорошо растворимы в
органических растворителях.
16.
Полиэтилен как крупнотоннажныйпродукт химического производства.
Полиэтилен — это крупнотоннажный продукт химического
производства.
Его основное использование:
• упаковочные материалы (пакеты, плёнки, прокладки, бутылки,
контейнеры);
• канализационные и дренажные трубы;
• электроизоляция;
• термоклей;
• бронепанели для бронежилетов;
• корпуса (лодки, бытовые предметы, детали аппаратуры);
• теплоизоляторы (из вспененного полиэтилена);
• обеспечение защиты от нейтронного излучения.
Ежегодно в мире производится более 100 миллионов тонн
полиэтилена. На производство этого полимера приходится
более трети общего объёма рынка пластмасс.
17.
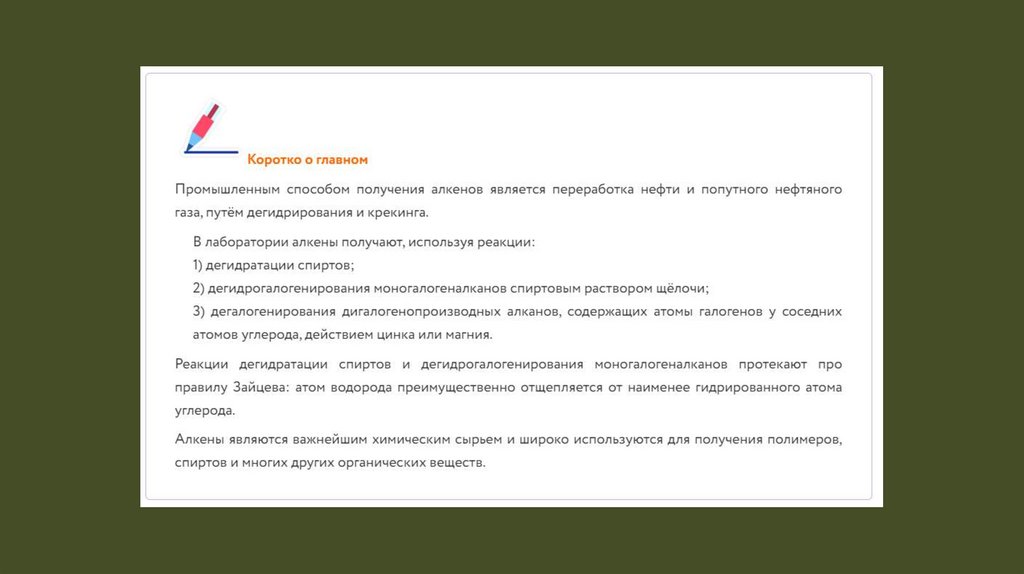
Промышленные способыполучения алкенов
Промышленным способом
получения алкенов является
переработка нефти и
попутного нефтяного газа
путём дегидрирования.
Отщепление водорода
(дегидрирование) от алканов
при нагревании в присутствии
катализатора:
18.
Промышленные способыполучения алкенов
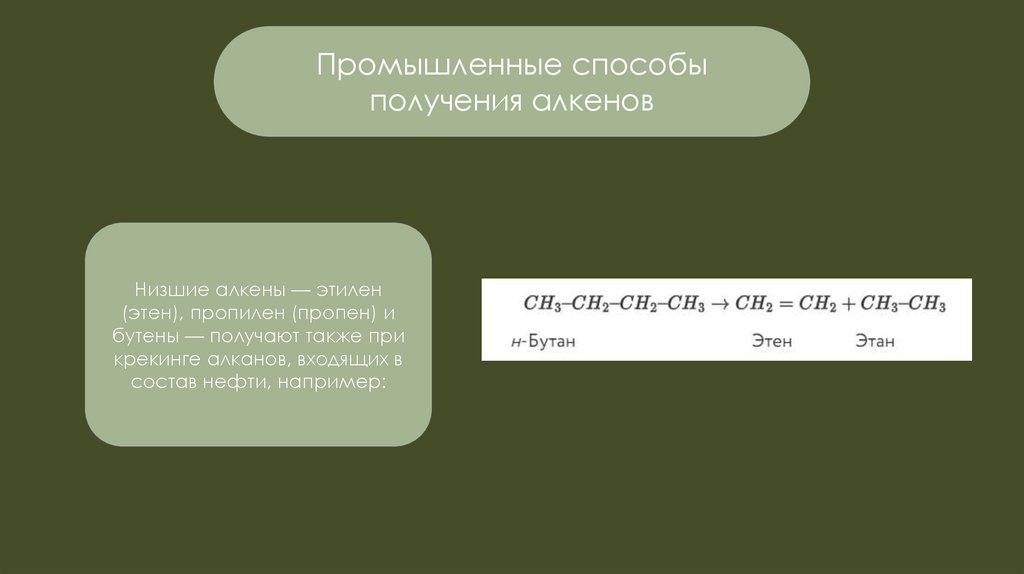
Низшие алкены — этилен
(этен), пропилен (пропен) и
бутены — получают также при
крекинге алканов, входящих в
состав нефти, например:
19.
Промышленные способыполучения алкенов
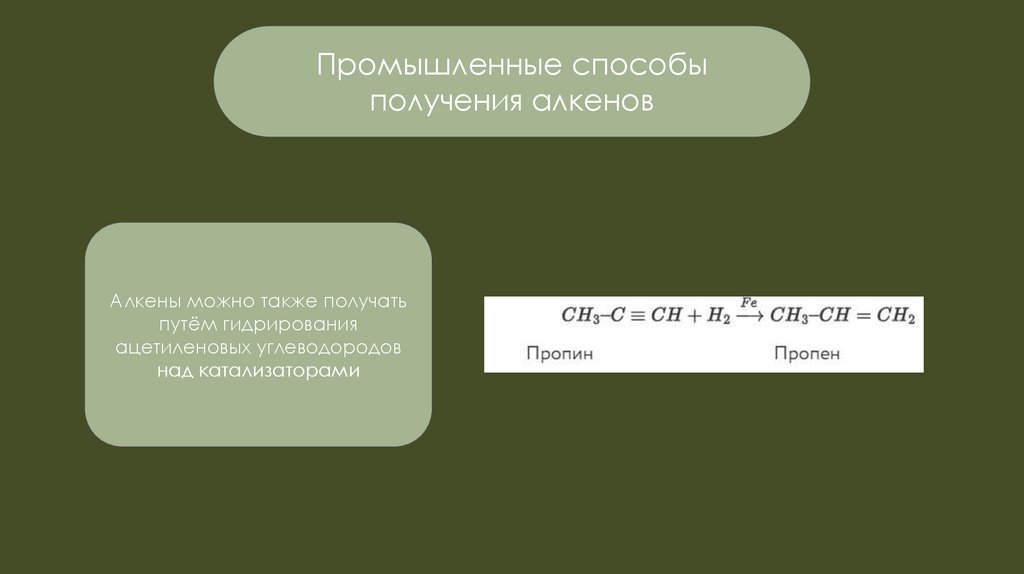
Алкены можно также получать
путём гидрирования
ацетиленовых углеводородов
над катализаторами
20.
Лабораторные способы полученияалкенов
Внутримолекулярная
дегидратация (отщепление
воды) спиртов при
температуре (170-180)
действием концентрированной
серной кислоты или в
присутствии катализатора
21.
Лабораторные способы полученияалкенов
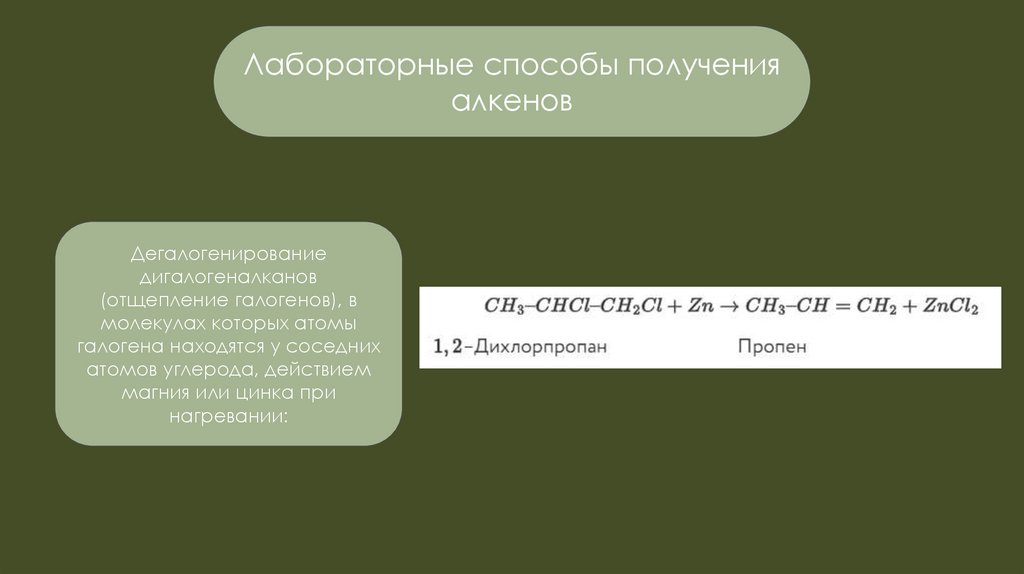
Дегалогенирование
дигалогеналканов
(отщепление галогенов), в
молекулах которых атомы
галогена находятся у соседних
атомов углерода, действием
магния или цинка при
нагревании:
22.
Лабораторные способы полученияалкенов
Дегидрогалогенирование
моногалогеналканов
(отщепление
галогеноводородов)
спиртовым раствором
щёлочи при нагревании. Как и
в случае дегидратации
спиртов, реакция протекает
по правилу Зайцева, т. е.
водород преимущественно
отщепляется от наименее
гидрированного атома
углерода.
23.
Применение алкеновАлкены являются важнейшим
химическим сырьем и широко
используются для получения
полимеров, спиртов и многих
других органических веществ.
24.
ЭтенЭтен используется для производства целого ряда химических
соединений: винилхлорида, этиленгликоля, этиленоксида,
этаноламинов, этанола, диоксана, дихлорэтана, уксусного альдегида и
уксусной кислоты и др.
Полимеризацией этилена и его производных получают полиэтилен,
поливинилацетат, поливинилхлорид, каучуки и смазочные масла.
Взаимодействием этилена с бензолом получают этилбензол, а из него
— стирол (винилбензол), полимеризация которого приводит к
образованию полистирола — полимера, используемого для получения
упаковочного материала.
Известно, что этилен образуется в растениях и способен ускорять
созревание плодов. Это свойство этилена позволяет использовать его,
например, для ускорения созревания зелёных неспелых бананов,
поступающих в продажу после долгой перевозки из тропических стран,
где их выращивают. Для этого бананы перед поступлением в продажу
выдерживают в атмосфере, содержащей этилен.
25.
ПропенПропен в промышленности применяется, в основном,
для синтеза полипропилена, используемого для
получения прочного синтетического волокна. Из него
также получают изопропанол, кумол, оксид пропилена,
глицерин, масляный альдегид, а также акрилонитрил,
используемый для синтеза бутадиен-нитрильного
каучука.
26.
Бутены применяют для производства бутадиена, изопрена,полиизобутилена, бутилкаучука, метилэтилкетона и др.
Изобутен — сырьё для получения бутилкаучука, изопрена,
трет-бутанола. используется для алкилирования фенолов
при синтезе ПАВ. Его сополимеры с бутенами применяют
как присадки к маслам и герметики.
Высшие алкены применяют при синтезе ПАВ, а также для
получения высших спиртов.
27.
28.
Обучающий ролик:https://youtu.be/rF9ztbOYu7
E
29.
ДЗ:• Повторить материал лекции
• Подготовить доклад/презентацию по
теме: «Использование алкенов»















 Химия
Химия








