Похожие презентации:
Сложные эфиры. Номенклатура сложных эфиров
1.
Сложныеэфиры
2.
Сложные эфиры —это функциональные производные
карбоновых кислот, в которых
гидроксильная группа замещена
остатком спирта или фенола.
Сложные
эфиры
R
R и R1 −
алкильные
группы.
-R1
3.
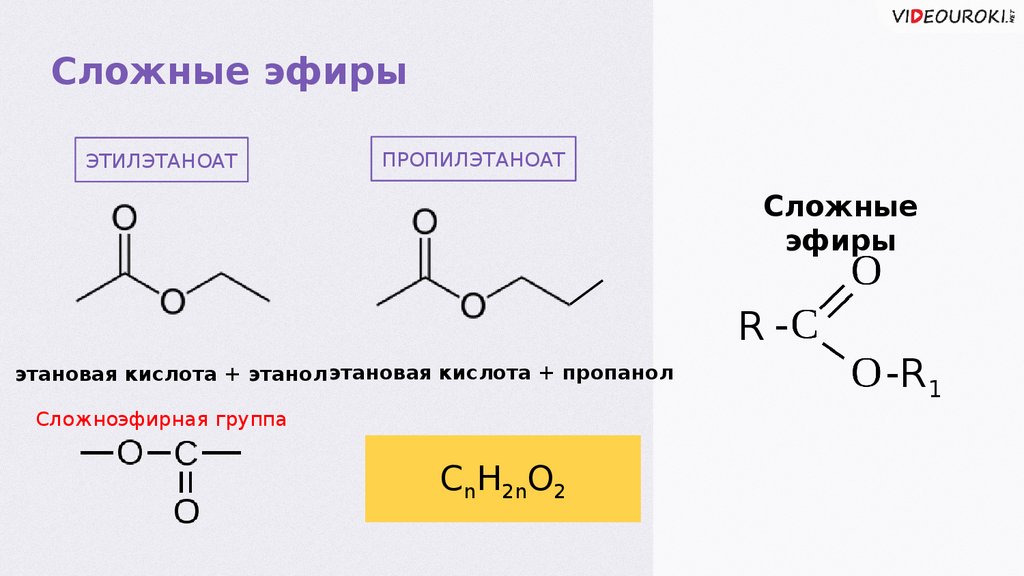
Сложные эфирыЭТИЛЭТАНОАТ
ПРОПИЛЭТАНОАТ
Сложные
эфиры
R
этановая кислота + этанол этановая кислота + пропанол
Сложноэфирная группа
CnH2nO2
-R1
4.
Номенклатура сложных эфировПри названии сложных эфиров сначала указывают
алкильную группу спирта, а потом кислоту,
заменяя суффикс -овая- на суффикс -оат-.
Допускаются и названия сложных эфиров, когда
сначала называется спирт, затем записывают
слово «эфир» и далее название кислоты.
5.
Номенклатура сложных эфировCH3 – COOCH2 – CH2 – CH3
Пропилэтаноат
(пропиловый эфир уксусной
кислоты)
H – COOCH2 – CH3
Этилметаноат
(этиловый эфир муравьиной
кислоты)
6.
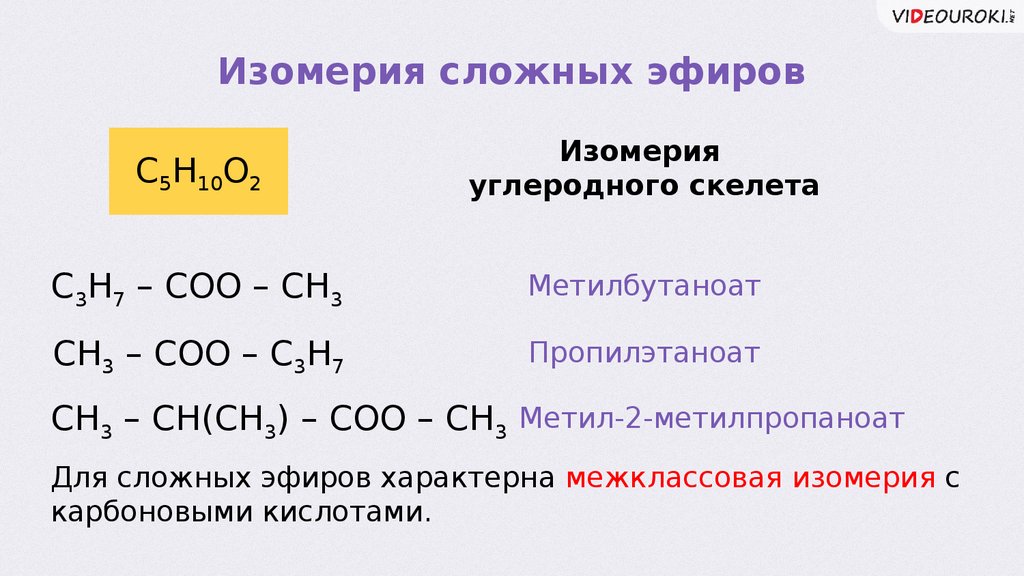
Изомерия сложных эфировС5Н10О2
Изомерия
углеродного скелета
C3H7 – COO – CH3
Метилбутаноат
CH3 – COO – C3H7
Пропилэтаноат
CH3 – CH(CH3) – COO – CH3 Метил-2-метилпропаноат
Для сложных эфиров характерна межклассовая изомерия с
карбоновыми кислотами.
7.
Физические свойстваСложные эфиры, в составе которых
низшие карбоновые кислоты и
спирты, − летучие малорастворимые и
практически нерастворимые в воде
жидкости.
Сложные эфиры хорошо растворимы в
органических растворителях.
Сложные
эфиры
R
-R1
8.
C3H7COOC4H9Бутиловый эфир
бутановой кислоты
9.
CH3COOCH2CH2CH(CH3)2Изоамиловый эфир
этановой кислоты
10.
CH3COOCH2C6H5Бензиловый эфир
этановой кислоты
11.
HCOOCH2C6H5Бензиловый эфир
метановой кислоты
12.
Получение сложных эфировРеакции карбоновых кислот и спиртов
H+
CH3COOH + C2H5OH ↔ CH3COOC2H5 + H2O
Этилэтаноат
(этиловый эфир
уксусной кислоты)
Реакция этерификации
13.
ШеелеКарл Вильгельм
(1742–1786 гг.)
Впервые использовал термин
«эфир» в конце 18 века.
14.
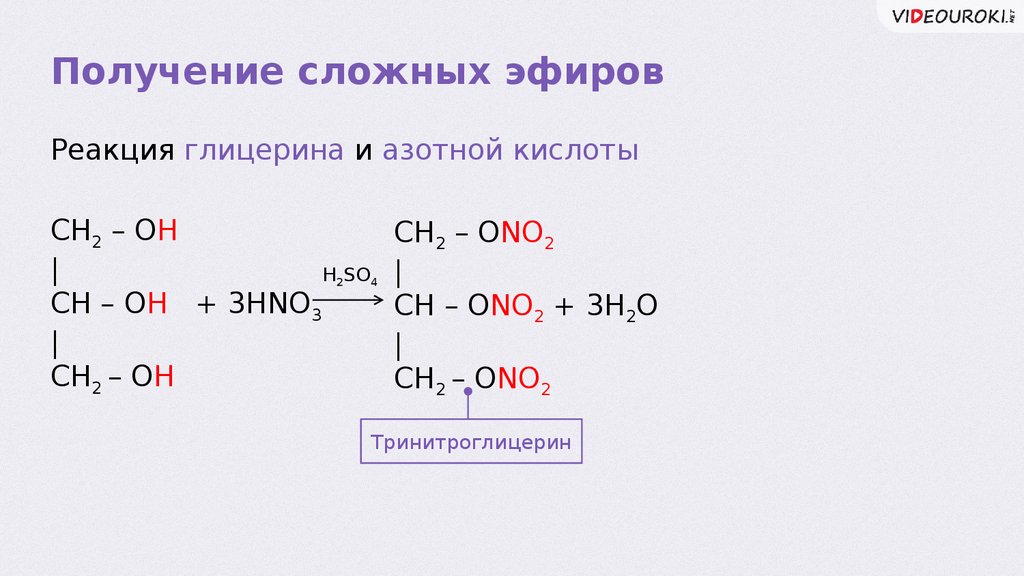
Получение сложных эфировРеакция глицерина и азотной кислоты
CH2 – OH
|
H SO
CH – OH + 3HNO3
|
CH2 – OH
2
4
CH2 – ONO2
|
CH – ONO2 + 3H2O
|
CH2 – ONO2
Тринитроглицерин
15.
Химические свойства сложных эфировРеакция горения
Вода
HCOOCH3 + 2O2 → 2CO2↑ + 2H2O
Углекислый газ
16.
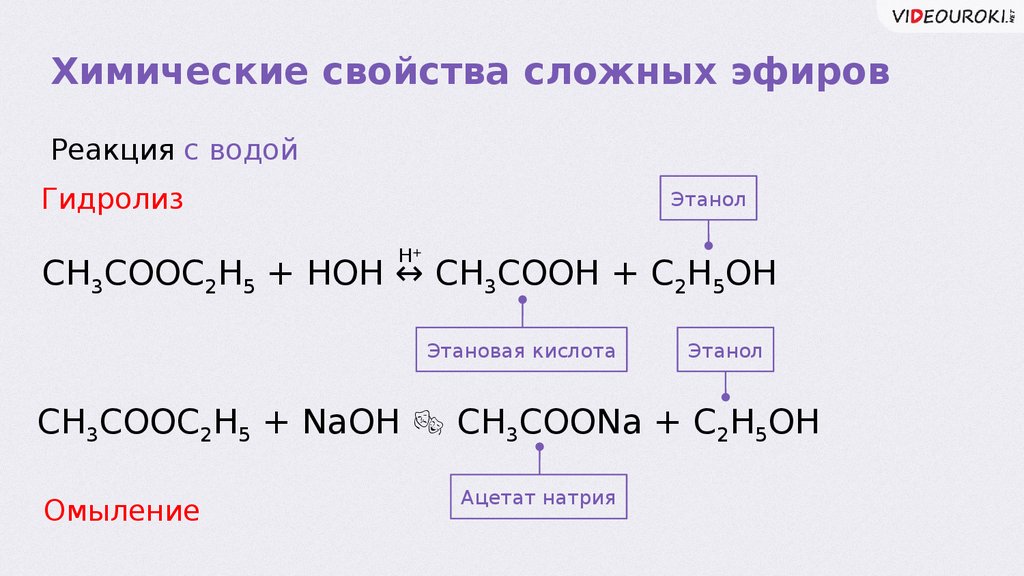
Химические свойства сложных эфировРеакция с водой
Гидролиз
Этанол
H+
CH3COOC2H5 + HOH ↔ CH3COOH + C2H5OH
Этановая кислота
Этанол
CH3COOC2H5 + NaOH CH3COONa + C2H5OH
Омыление
Ацетат натрия
17.
Сложные эфирыЭфирные масла
Жиры
Воски
18.
Воски —это сложные эфиры высших
карбоновых кислот и высших спиртов.
Воски
19.
Пчелиный воск состоитиз пальмитиновой кислоты
и миристилового спирта.
20.
Древняя техника восковойживописи – энкаустика.
Восковые краски не боятся
сырости, не
растрескиваются.
Фаюмские
портреты
21.
Применение воскаПолитуры
Смазки
Пропиточные
составы
22.
Применение воскаКремы
Мази
23.
Применение сложных эфировПроизводство
духов
Производство
бытовой химии
Приготовление
фруктовых вод
24.
Применение сложных эфировПриготовление
кондитерских
изделий
Применяют как
растворители
Производство
полимерных
материалов
25.
Применение сложных эфировВ лакокрасочной
промышленности
Производство
искусственных
волокон
Производство
лекарственных
средств
26.
Сложные эфиры – основаорганического стекла.
27.
Сложные эфиры – это функциональные производные
карбоновых кислот, у которых гидроксильная группа
замещена на остаток спирта.
Сложные эфиры широко распространены в природе.
Сложные эфиры образуются в реакциях между спиртами
и кислородсодержащими кислотами.
Сложные эфиры гидролизуются растворами
минеральных кислот и щелочей.
Сложные эфиры применяются во многих областях
промышленности.























 Химия
Химия








