Похожие презентации:
Подготовка к контрольной работе по теме «Строение атома», «Строение вещества» (11 класс)
1.
ПОДГОТОВКА К КОНТРОЛЬНОЙРАБОТЕ ПО ТЕМЕ «СТРОЕНИЕ
АТОМА», «СТРОЕНИЕ ВЕЩЕСТВА»
11 КЛАСС.
ПРЕЗЕНТАЦИЯ ХАРИТОНОВОЙ Е.В.
УЧИТЕЛЯ ХИМИИ ГБОУ №66 ПРИМОРСКОГО Р-НА СПБ
2.
ЧТО БУДЕТ ВХОДИТЬ К К.Р.• 1. СТРОЕНИЕ АТОМА
• 2. ИЗМЕНЕНИЕ СВОЙСТВ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ ПО ПЕРИОДУ И
ПО ГРУППЕ.
• 3. ТИПЫ ХИМИЧЕСКИХ СВЯЗЕЙ И КРИСТАЛЛИЧЕСКИХ РЕШЁТОК.
• 4. СМЕСИ.
• 5. ЗАДАЧА НА РАСЧЁТ МАССОВОЙ ДОЛИ ЭЛЕМЕНТА В ВЕЩЕСТВЕ.
• 6. ЗАДАЧА НА СМЕСИ (МАССОВАЯ, ОБЪЁМНАЯ ДОЛЯ ВЕЩЕСТВА
(ЭЛЕМЕНТА) В СМЕСИ (ВЕЩЕСТВЕ).
3.
ФОРМА КОНТРОЛЬНОЙ РАБОТЫ:• ЧАСТЬ 1 – ТЕСТОВАЯ
• ЧАСТЬ 2 – С РАЗВЁРНУТЫМ ВАРИАНТОМ ОТВЕТА.
4.
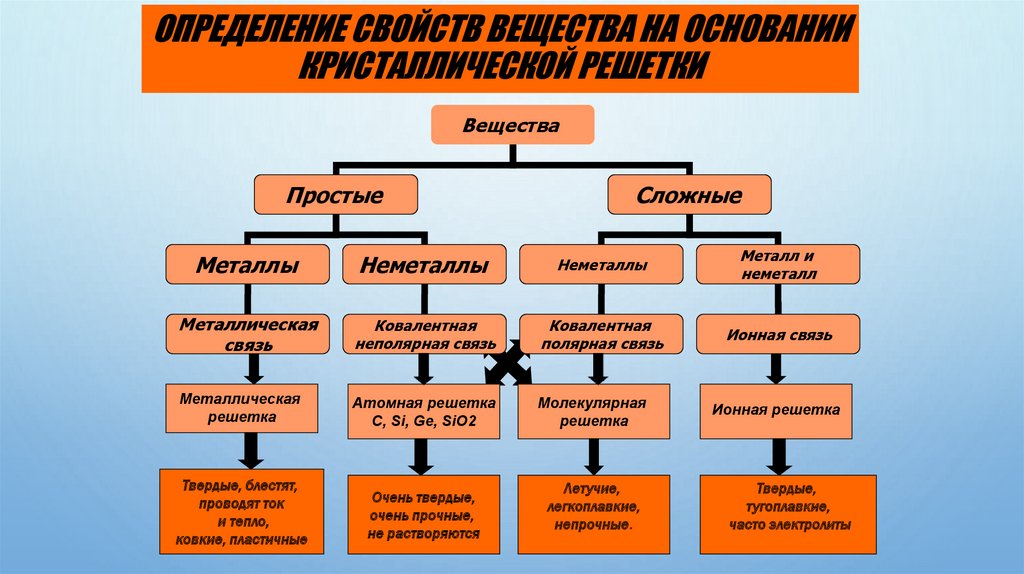
ОПРЕДЕЛЕНИЕ СВОЙСТВ ВЕЩЕСТВА НА ОСНОВАНИИКРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
Вещества
Простые
Сложные
Металлы
Неметаллы
Неметаллы
Металл и
неметалл
Металлическая
связь
Ковалентная
неполярная связь
Ковалентная
полярная связь
Ионная связь
Металлическая
решетка
Атомная решетка
C, Si, Ge, SiO2
Молекулярная
решетка
Твердые, блестят,
проводят ток
и тепло,
ковкие, пластичные
Очень твердые,
очень прочные,
не растворяются
Летучие,
легкоплавкие,
непрочные.
Ионная решетка
Твердые,
тугоплавкие,
часто электролиты
5.
ХИМИЧЕСКАЯ СВЯЗЬ В МОЛЕКУЛЕКИСЛОРОДА
1) КОВАЛЕНТНАЯ ПОЛЯРНАЯ
2) КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ
3) ИОННАЯ
4) МЕТАЛЛИЧЕСКАЯ
6.
В ОКСИДЕ КАЛЬЦИЯ ХИМИЧЕСКАЯ СВЯЗЬ1) МЕТАЛЛИЧЕСКАЯ
2) ИОННАЯ
3) КОВАЛЕНТНАЯ ПОЛЯРНАЯ
4) КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ
7.
КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ СВЯЗЬХАРАКТЕРНА ДЛЯ
1) KCl 2) HBr 3) P4 4) CaCl2
8.
ПРИ ИОННОЙ СВЯЗИ1) ВНЕШНИЕ НЕПАРНЫЕ ЭЛЕКТРОНЫ ПЕРЕХОДЯТ ОТ
ОДНОГО АТОМА К ДРУГОМУ
2) ВНЕШНИЕ НЕПАРНЫЕ ЭЛЕКТРОНЫ ВСЕХ АТОМОВ
ОБЩИЕ
3) ВНЕШНИЕ НЕПАРНЫЕ ЭЛЕКТРОНЫ СОСЕДНИХ АТОМОВ
ОБЩИЕ
4) ВСЕ ЭЛЕКТРОНЫ АТОМОВ ОБЩИЕ
9.
ПРИ ОБРАЗОВАНИИ КАКОЙ СВЯЗИ ПРОИСХОДИТОБОБЩЕСТВЛЕНИЕ ВСЕХ ЭЛЕКТРОНОВ ВНЕШНЕГО
ЭНЕРГЕТИЧЕСКОГО УРОВНЯ
1) КОВАЛЕНТНОЙ ПОЛЯРНОЙ
2) КОВАЛЕНТНОЙ НЕПОЛЯРНОЙ
3) ИОННОЙ
4) МЕТАЛЛИЧЕСКОЙ
10.
КАКОЙ ИЗ ПЕРЕЧИСЛЕННЫХ ЭЛЕМЕНТОВ ИМЕЕТНАИБОЛЬШУЮ ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ
1) АЗОТ
2) СЕЛЕН
3) БОР
4) КИСЛОРОД
11.
КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ СВЯЗЬХАРАКТЕРНА ДЛЯ
1) KCl 2) HBr 3) P4 4) CaCl2
12.
В КАКИХ ВЕЩЕСТВАХ АТОМЫ ХИМИЧЕСКИХЭЛЕМЕНТОВ СВЯЗАНЫ КОВАЛЕНТНОЙ ПОЛЯРНОЙ
ХИМИЧЕСКОЙ СВЯЗЬЮ?
• NaOH
• H2
• CO2
• NaCl
• Zn
13.
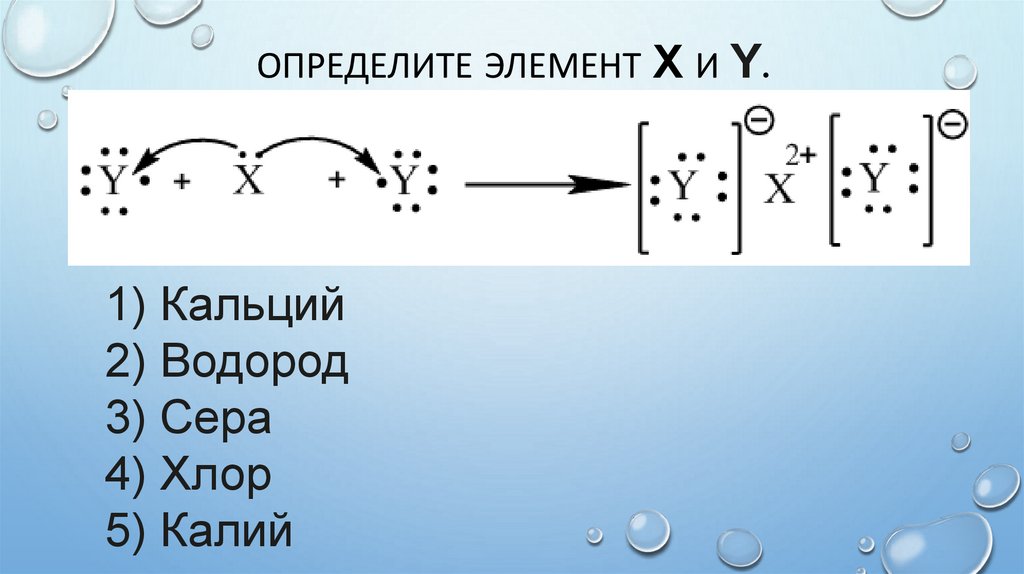
ОПРЕДЕЛИТЕ ЭЛЕМЕНТ X И Y.1) Кальций
2) Водород
3) Сера
4) Хлор
5) Калий
14.
СТЕПЕНЬ ОКИСЛЕНИЯ ХЛОРА В CLO2РАВНА
1) -4
2) -1
3) +1
4) +4
15.
НАИБОЛЬШУЮ СТЕПЕНЬ ОКИСЛЕНИЯАЗОТ ПРОЯВЛЯЕТ В СОЕДИНЕНИИ
1) NH3 2) N2 3) N2O5 4) Na3N
16.
РАСПРЕДЕЛЕНИЮ ЭЛЕКТРОНОВ В АТОМЕ ХИМИЧЕСКОГОЭЛЕМЕНТА, КОТОРЫЙ РАСПОЛОЖЕН В III ПЕРИОДЕ, IАГРУППЕ, СООТВЕТСТВУЕТ РЯДУ ЧИСЕЛ:
1) 2,8,2
2) 2,8,1
3) 2,8,8,1
4) 2,1
17.
РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОНОВ ПОЭНЕРГЕТИЧЕСКИМ УРОВНЯМ 2,8,5 В АТОМЕ
1) УГЛЕРОДА
2) АЗОТА
3) ФОСФОРА
4) СЕРЫ
18.
ХИМИЧЕСКОМУ ЭЛЕМЕНТУ СООТВЕТСТВУЕТ ВЫСШИЙОКСИД СОСТАВА R2O7 .ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ
ВНЕШНЕГО ЭНЕРГЕТИЧЕСКОГО УРОВНЯ АТОМА ЭТОГО
ЭЛЕМЕНТА
2
4
2
3
2
5
1) ns np 2) ns np 3) ns np 4)
19.
ПО ПЕРИОДУ СЛЕВА НАПРАВОУМЕНЬШАЕТСЯ (-ЮТСЯ)
1) АТОМНЫЙ РАДИУС ЭЛЕМЕНТОВ
2) ЧИСЛО ВАЛЕНТНЫХ ЭЛЕКТРОНОВ В АТОМАХ
3) ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ
4) НЕМЕТАЛЛИЧЕСКИЕ СВОЙСТВА
20.
В РЯДУ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ LI – BEМЕТАЛЛИЧЕСКИЕ СВОЙСТВА
1) ОСЛАБЕВАЮТ
2) УСИЛИВАЮТСЯ
3) НЕ ИЗМЕНЯЮТСЯ
4) ИЗМЕНЯЮТСЯ ПЕРИОДИЧЕСКИ
–B–C
21.
РАСПОЛОЖИТЕ НАЗВАНИЯ ХИМИЧЕСКИХЭЛЕМЕНТОВ В ПОРЯДКЕ УСИЛЕНИЯ
МЕТАЛЛИЧЕСКИХ СВОЙСТВ.
• МЫШЬЯК
• КИСЛОРОД
• АЗОТ
• БЕРИЛЛИЙ
• ЦЕЗИЙ
• СТРОНЦИЙ
22.
ИОН К+ ИМЕЕТ ЭЛЕКТРОННУЮКОНФИГУРАЦИЮ ВНЕШНЕГО СЛОЯ
1) 3S23P5
2) 3S23P6
3) 4S1
4) 4S24P6
23.
СВЯЗЬ В СОЕДИНЕНИИ, ОБРАЗОВАННОМАТОМАМИ ВОДОРОДА И ЭЛЕМЕНТОМ,
РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОНОВ В АТОМЕ КОТОРОГО
2,8,6
1) ИОННАЯ
2) КОВАЛЕНТНАЯ ПОЛЯРНАЯ
3) КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ
4) ВОДОРОДНАЯ
24.
РАСЧЁТ МАССОВОЙ ДОЛИ ХИМИЧЕСКОГОЭЛЕМЕНТА В СОЕДИНЕНИИ
25.
Н2О26.
27.
ЗАДАЧКАРАССЧИТАЙТЕ МАССОВЫЕ ДОЛИ ЭЛЕМЕНТОВ
В МЕТАНЕ.
28.
29.
ЗАДАЧА• НАЙТИ МАССУ АЛЮМОСИЛИКАТА
AL2O3*2SIO2*2H2O В 80 Г КАОЛИНИТА,
СОДЕРЖАЩЕГО 15% ПРИМЕСЕЙ
30.
31.
ДОМАШНЕЕ ЗАДАНИЕ• 1. ВЫЧИСЛИТЕ МАССОВЫЕ ДОЛИ ЭЛЕМЕНТОВ В АНИЛИНЕ С6Н5NH2.
• 2. В 200 Г ВОДЫ РАСТВОРИЛИ 15 ГРАММ САХАРА. ВЫЧИСЛИТЕ МАССОВУЮ
ДОЛЮ САХАРА В ПОЛУЧЕННОМ РАСТВОРЕ.
• 3. НАЙТИ ОБЪЕМ КИСЛОРОДА В 55Л ВОЗДУХА, ЕСЛИ СОДЕРЖАНИЕ ЕГО В
ВОЗДУХЕ СОСТАВЛЯЕТ 21%.
• 4. НАЙТИ МАССУ ЦИНКА В 24 Г ТЕХНИЧЕСКОГО ЦИНКА, СОДЕРЖАЩЕГО
15% ПРИМЕСЕЙ.





























 Химия
Химия








