Похожие презентации:
Валентность (8 класс)
1.
Валентность2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
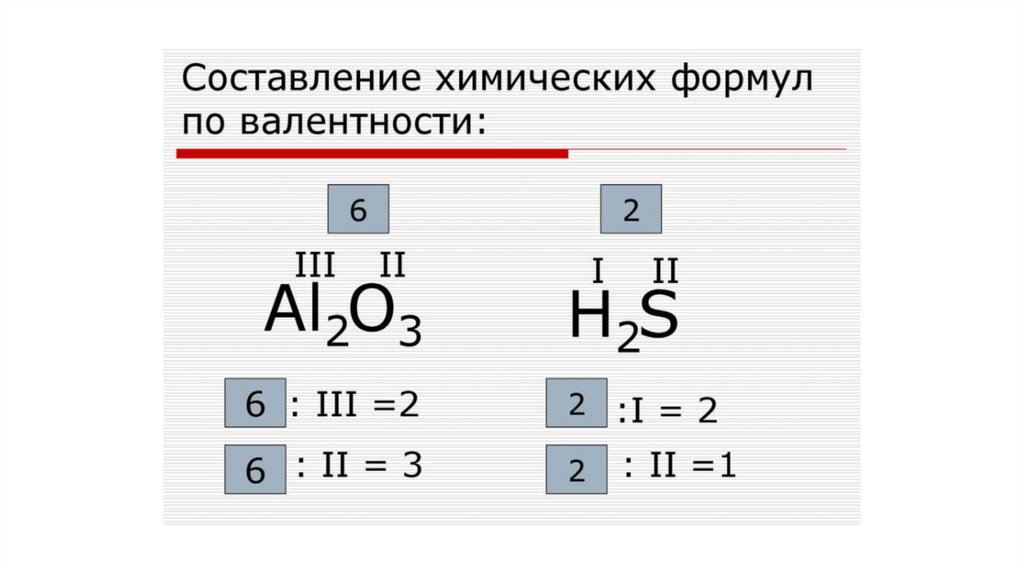
Составление химических формул1.
2.
3.
4.
5.
Кислородное соединение свинца (IV)
Кислородное соединение хлора (V)
Соединение кремния (IV) с хлором (I)
Соль железа (III) и серы (II)
Соль меди (II) и фтора
Ответы: PbO2, Cl2O5, SiCl4, Fe2S3, CuF2
13.
Закон сохранения массы веществА. Лавуазье (1789)
«Масса веществ, вступивших в реакцию, равна массе продуктов
этой реакции»
14.
Химические уравненияC + O2 CO2
реакция горения угля
Стрелочка = процесс превращения
Левая часть – исходные вещества (реагенты)
Правая часть - продукты
15.
Согласно закону сохранения масс: сколько атомов в реакциювступило, столько и должно образоваться в продуктах!
Ca + O2 CaO
Ca + O2 2CaO
коэффициент перед всей формулой! Не внутри!
2Ca + O2 2CaO (итоговое уравнение реакции)
16.
P + O2 P2O3Находим НОК между числом атомов кислорода слева и справа: 6
Разделим НОК на число атомов – получаем коэффициенты
6/2 = 3 коэффициент перед кислородом
6/3=2 коэффициент перед P2O3
P + 3O2 2P2O3
4P + 3O2 2P2O3
17.
Домашка• Зад. 1,2,4,5,7 стр. 60
• Параграф 18-19 читать
• Зад. 2 стр. 62
• Зад. 3 стр. 65 + тест
• Параграф 20 конспект!!
• Зад. 3-5 стр. 68 + тест
18.
Расставьте коэффициенты в схемах реакций1)
2)
3)
4)
5)
6)
7)
8)
Mg + O2 MgO
Fe + Cl2 FeCl3
N2 + H2 NH3
Na + O2 Na2O
Fe2O3 + C Fe + CO2
KOH + H2SO4 K2SO4 + H2O
KMnO4 K2MnO4 + MnO2 + O2
Na + H2O NaOH + H2
19.
Расставьте коэффициенты в схемах реакций1)
2)
3)
4)
5)
6)
7)
8)
2Mg + O2 2MgO
2Fe + 3Cl2 2FeCl3
N2 + 3H2 2NH3
4Na + O2 2Na2O
2Fe2O3 + 3C 4Fe + 3CO2
2KOH + H2SO4 K2SO4 + 2H2O
2KMnO4 K2MnO4 + MnO2 + O2
2Na + 2H2O 2NaOH + H2
20.
Типы химических реакций• Соединения
• Разложения
• Замещения
• Обмена
1)
2)
3)
4)
KClO3 KClO4 + O2
NaI + Pb(NO3)2 PbI2 + NaNO3
H2 + O2 H2O
Fe + CuSO4 Cu + FeSO4
1) AB + CD AC + BD
2) ABC AB + C
3) A + B AB
4) A + BC AB + C
21.
Реакции соединения• Из двух или нескольких более простых веществ получается одно
сложное
1) P + O2 P2O3
2) CaCO3 + CO2 + H2O Ca(HCO3)2
3) MgO + SiO2 MgSiO3
22.
Реакции разложения• Из одного сложного вещества образуются два или несколько
более простых веществ
1) Fe(OH)3 Fe2O3 + H2O
2) NaCl Na + Cl2
3) AgNO3 Ag + NO2 + O2
23.
Реакции замещения• Реакция между простым и сложным веществом, когда атомы
простого вещества замещают атомы одного из элементов в
сложном веществе
1) Cl2 + NaI NaCl + I2
2) K + HOH KOH + H2
3) Fe + H2SO4 FeSO4 + H2
24.
Реакции обмена• Два сложных вещества обмениваются составными частями
1) NaCl + AgNO3 AgCl + NaNO3
2) FeCl3 + KOH KCl + Fe(OH)3
25.
Домашка1. Параграф 20-21 читать
2. Зад. 2-3 стр. 71
3. Найти в Интернете/учебнике и выписать четыре реакции (по
одной каждого типа)
4. Подготовиться к проверочной работе по теме «Валентность.
Химические реакции»
26.
1 вариант2 вариант
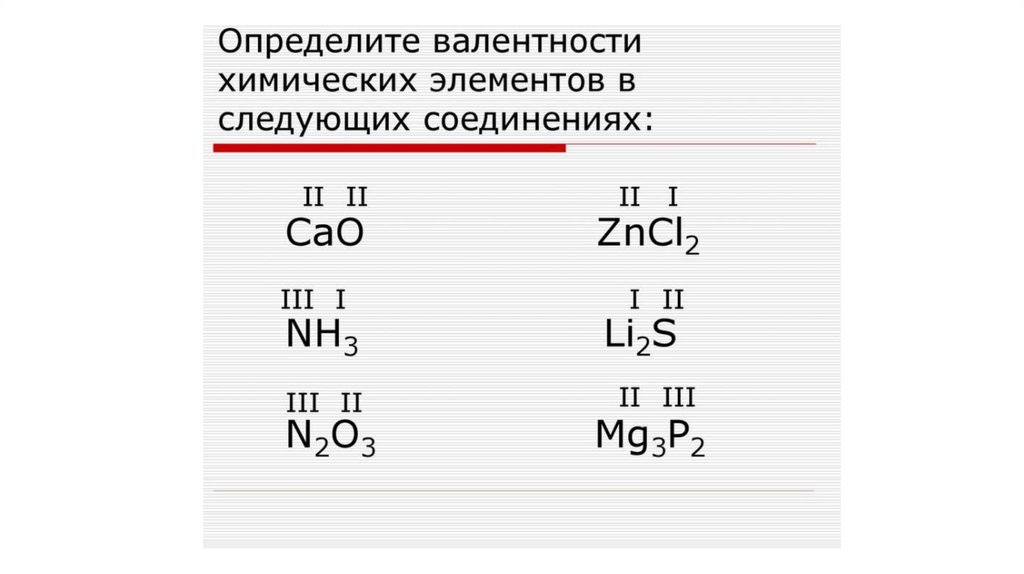
1. Расставьте валентности у
элементов в соединениях:
K2S, MnF2, SO3, SO2, NO2, Cl2O5, NH3,
CH4, SiF4, HCl, Al4C3
2. Установите формулы соединений:
AgIClI, FeIIIOII, CrIIBrI, NIOII, ClVIIOII,
BaIIHI, CdIIBrI, PVClI
3. Расставьте коэффициенты в
схемах реакций, определите тип:
1. Расставьте валентности у элементов в
соединениях:
SF6, PH3, Ca3N2, NO, CrO3, Cl2O3, SiO2, Na2S,
AlCl3, HI, P2O5
2. Установите формулы соединений:
MnIVOII, BIIIHI, SnIIFI, AsIIIClI, CIVOII, BrVOII, IVIIOII,
BaIIHI
3. Расставьте коэффициенты в схемах
реакций, определите тип:
1) Cr + O2 Cr2O3
2) Fe2O3 + HCl FeCl3 + H2O
3) N2 + H2 NH3
1) P + O2 P2O5
2) Cu(NO3)2 + NaOH NaNO3 + Cu(OH)2
3) KMnO4 K2MnO4 + MnO2 + O2
27.
3 вариант4 вариант
1. Расставьте валентности у
элементов в соединениях:
Cu2O, NaCl, NO2, NH3, Mn2O3, SO3,
CaC2, FeF3, OF2, CH4
2. Установите формулы соединений:
FeIIClI, NIIOII, VIIIOII, SIVBrI, PVClI, CrIIISII,
MnIVOII, CaIINIII
3. Расставьте коэффициенты в
схемах реакций, определите тип:
1. Расставьте валентности у элементов в
соединениях:
MnO2, BH3, SnF2, CO2, Br2O5, BaH2, I2O7, AlI3,
SeO2, Fe2O3
2. Установите формулы соединений:
SVIClI, PIIIHI, NIIIOII, CrVIOII, FeIIISII, SiIVClI, NaISII,
PVOII
3. Расставьте коэффициенты в схемах
реакций, определите тип:
1) P + Cl2 PCl5
2) Fe + HCl FeCl2 + H2
3) Al(OH)3 + HBr AlBr3 + H2O
1) NO2 N2 + O2
2) Ca(NO3)2 + Na2S CaS + NaNO3
3) Fe + Cl2 FeCl3

























 Химия
Химия








