Похожие презентации:
Поверхностные явления. Адсорбция
1.
Лекция«Поверхностные явления.
Адсорбция»
1
2.
Поверхностные явления (П.Я.) - этопроцессы, происходящие в гетерогенных
системах на границе раздела фаз и
обусловленные особенностями состава и
строения поверхностного слоя (П.С.).
2
3.
Поверхностный слой может бытьмономолекулярнымтолщиной в
диаметр одной
молекулы
полимолекулярным толщиной в
диаметр
нескольких молекул
3
4.
Поверхность раздела фаз может бытьподвижной
ж/г (H2O/CO2)
ж/ж (H2O/ масло)
неподвижной
т/г (Fe/O2)
т/ж (С/ CH3COOH)
т/т (Fe/S)
4
5.
Живые системы это гетерогенныесистемы с очень сильно развитой
поверхностью раздела :
1. кожные покровы;
2. поверхность кровеносных сосудов;
3. поверхность клеточных мембран...
Поверхность тела взрослого человека
1,5-1,6м2, поверхность эритроцитов 25003800м2, альвеол 1000 м2.
5
6.
Большинствобиологически
важных процессов в организме идут на
клеточных
мембранах
и
для
понимания их механизмов необходимо
знать основные понятия и
законы,
которым
подчиняются
поверхностные явления.
6
7.
ОСНОВНЫЕ ПОНЯТИЯПоверхностная энергия- это энергия
возникающая из-за взаимодействия
молекул П.С. находящихся в особых
условиях, по сравнению с молекулами
находящимися внутри раствора
7
8.
Каждая из «глубинных» молекул жидкостипритягивается друг к другу.Молекулы,
находящиеся на поверхности, испытывают
особенно сильное притяжение друг к другу.
8
9.
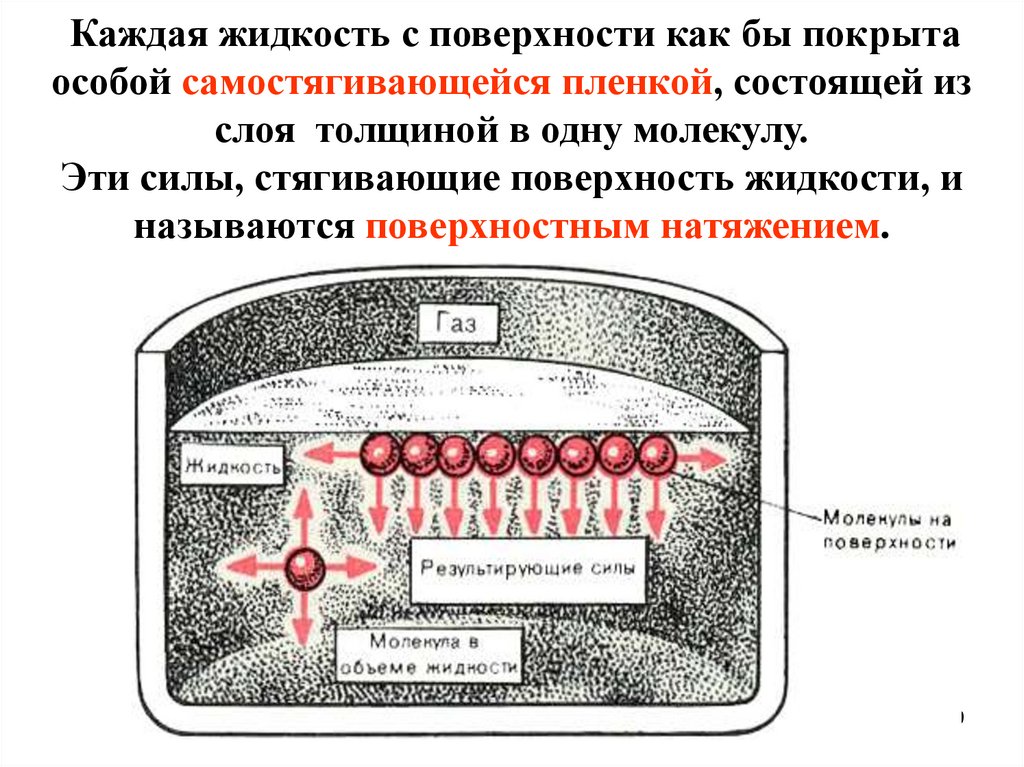
Каждая жидкость с поверхности как бы покрытаособой самостягивающейся пленкой, состоящей из
слоя толщиной в одну молекулу.
Эти силы, стягивающие поверхность жидкости, и
называются поверхностным натяжением.
9
10.
Поэтому капля жидкости всегда шарообразная,а поверхность жидкости в широком сосуде всегда
идеально гладкая.
Эти силы, стягивающие поверхность жидкости,
и называются поверхностным натяжением
σ- сигма
Чем больше силы сцепления между молекулами,
тем больше σ.
Значения σ
Этанол –22.75 эрг/см2
Вода – 72.75 эрг/см2
Ртуть – 480.3 эрг/см2
10
11.
Поверхностное натяжение (σ) – это величина, измеряемаяэнергией Гиббса (G) приходящейся на единицу площади
поверхности раздела фаз (S):
σ = G/ S
σ зависит:
1)от температуры, например у воды при t =100o C
2) от природы растворенного вещества
3)от давления в газовых системах
σ=0
σ влияет на:
1) деление клеток и проницаемость клеточных мембран
2) с возрастом σ плазмы крови уменьшается
3) при раке σ сильно изменяется и поэтому может
использоваться для диагностики рака
11
12.
ВЕЩЕСТВАгидрофильные -
гидрофобные -
сод-щие ионогенные
не сод-щие ионогенные
группы способные
и не способные
взаимод-ть с Н2О.
взаимод-ть с Н2О .
Имеющие сродство
Не имеющие сродства
к воде.
к воде.
12
13.
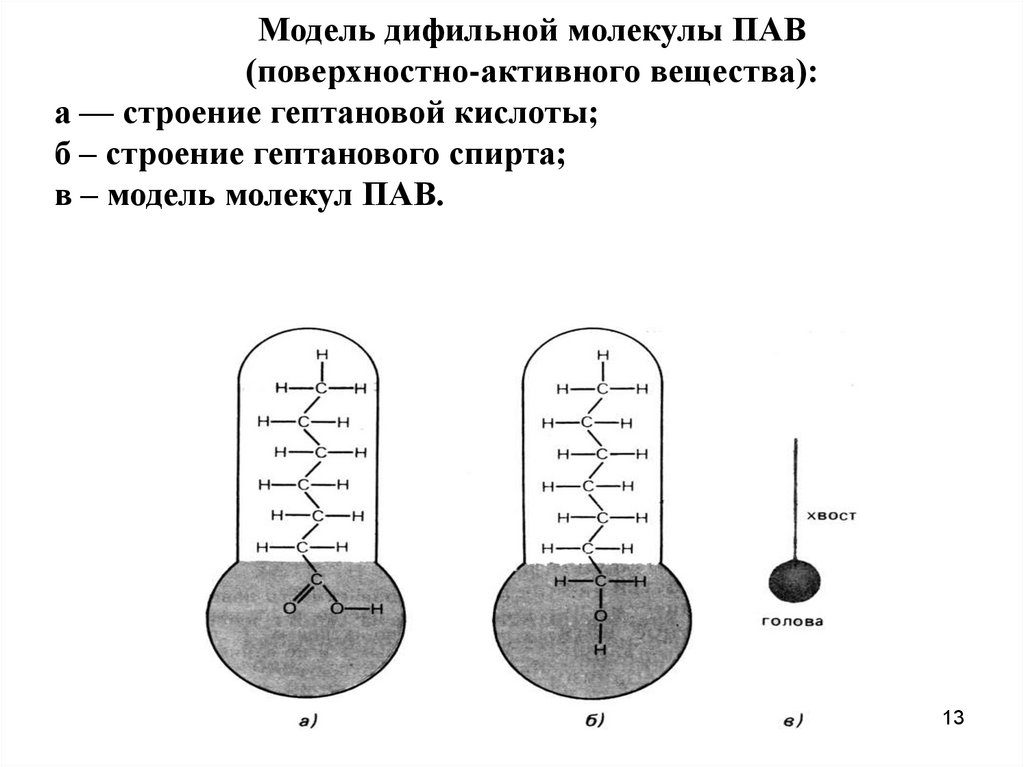
Модель дифильной молекулы ПАВ(поверхностно-активного вещества):
а — строение гептановой кислоты;
б – строение гептанового спирта;
в – модель молекул ПАВ.
13
14.
Дифильное строение в организме имеюттакие молекулы ПАВ как :
фосфатидные
кислоты, кефалины, лецитины…, которые
строят клеточные мембраны.
Поверхностная активность их зависит от
длины гидрофобной части молекулы, т. е. от
длины углеродной цепи
14
15.
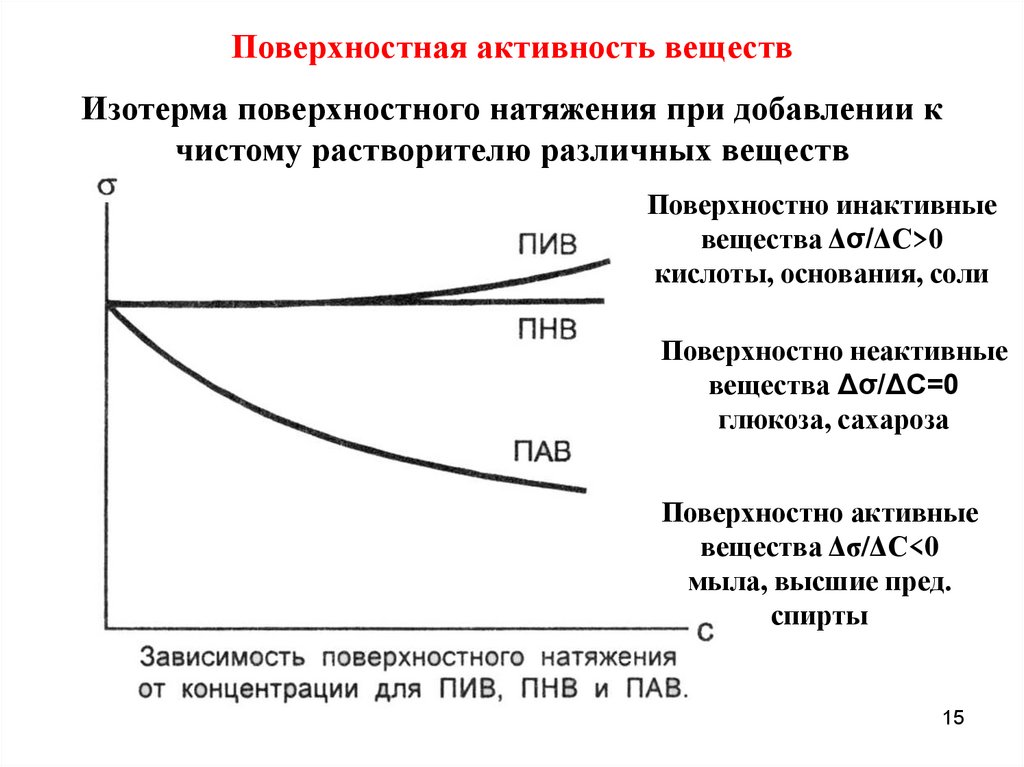
Поверхностная активность веществИзотерма поверхностного натяжения при добавлении к
чистому растворителю различных веществ
Поверхностно инактивные
вещества Δσ/ΔС>0
кислоты, основания, соли
Поверхностно неактивные
вещества Δσ/ΔС=0
глюкоза, сахароза
Поверхностно активные
вещества Δσ/ΔС<0
мыла, высшие пред.
спирты
15
16.
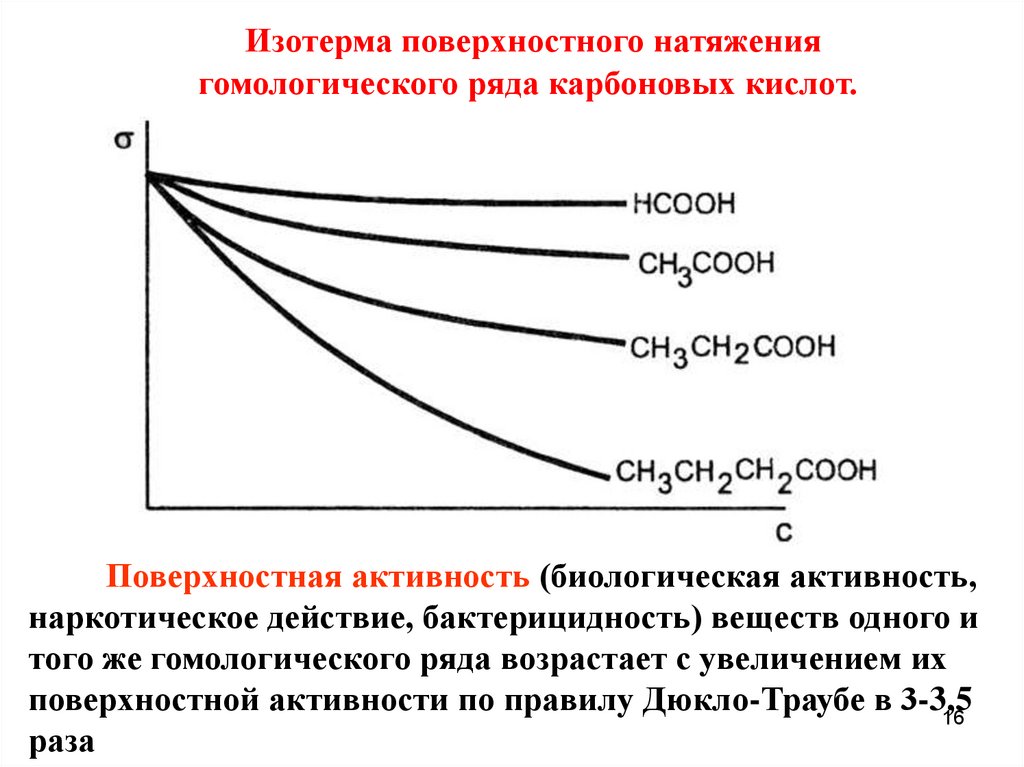
Изотерма поверхностного натяжениягомологического ряда карбоновых кислот.
Поверхностная активность (биологическая активность,
наркотическое действие, бактерицидность) веществ одного и
того же гомологического ряда возрастает с увеличением их
поверхностной активности по правилу Дюкло-Траубе в 3-3,5
16
раза
17.
ПАВоказывают
антимикробное
действие.
Это
связывают с их влиянием на
проницаемость клеточных мембран,
а также подавляющим действием на
ферментативные
системы
микроорганизмов
и
поэтому
применяются в хирургии в качестве
антисептиков.
17
18.
СТАБИЛИЗАЦИЯ ГЕТЕРОГЕННЫХ СИСТЕМт.к. σ = G/ S или G = σ S
то стабилизация может происходить двумя путями:
1) За счет уменьшения S путем укрупнения частиц,
что характерно для процессов идущих вне живого
(in vitro), когда ΔG = σ ΔS
Например: при выпадении осадков, при
свертывании крови…
2) За счет уменьшения σ путем поглощения
(сорбции ) молекул растворенного вещества из
окружающей среды, что характерно для живых
систем, т.е. для процессов идущих in vivo, когда
ΔG = Δ σ S
18
19.
СОРБЦИОННЫЕ ЯВЛЕНИЯэто сложные физико-химические процессы, которыеможно рассматривать как сумму более простых
процессов:
1. АДСОРБЦИЯ – процесс самопроизвольного перераспределения компонентов системы между поверхностным
слоем и объёмной фазой или это
самопроизвольное
увеличение концентрации вещества на границе раздела фаз.
В процессе участвуют : адсорбент – вещество на котором
накапливаются другие вещества – адсорбтивы. ΔG = σ ΔS
2) АБСОРБЦИЯ- процесс поглощения вещества
(абсорбтива) всей массой абсорбента
3) ДЕСОРБЦИЯ – процесс обратный адсорбции.
19
20.
4.ХЕМОСОРБЦИЯ- процесс, когда адсорбция
сопровождается химическим взаимодействием
между адсорбентом и адсорбтивом.
Обычно в этом процессе участвует
поверхностный слой адсорбента, т.е. на границе
раздела , например AI / O2 идет реакция
4 AI + 2O2
2 AI2О3
образующаяся оксидная пленка предохраняет
металл от дальнейшего разрушения
20
21.
5. Если оксидная пленка не предохраняет металл отдальнейшего разрушения, то кислород проникает
вглубь металла, в нем образуются узкие поры, в
которых из окружающей среды конденсируется
вода, а в ней растворяются газы и начинается т.н.
капиллярная конденсация, которая может
сопровождаться хемосорбцией.
Это происходит с железом, которое в конце
концов превращается в ржавчину.
21
22.
Адсорбция идет на активных центрах участках с большой поверхностной энергией. Этопики и углубления, которые есть на любой
поверхности.
На неполярном адсорбенте ( С, Fe ) адсорбция
идет за счет сил ван-дер-ваальса. Это т.н.
физическая адсорбция и она идет за счет
межмолекулярного притяжения.
Скорость адсорбции зависит от температуры,
давления в случае газов и природы адсорбента и
адсорбтива, а также удельной поверхности
адсорбента.
22
23.
Ребиндер Петр Александрович(3.10.1898 – 12.07.1972)
Правило Ребиндера
В первую очередь из растворов
адсорбируются вещ-ва полярность (ε)
которых ближе к полярности
адсорбента
ε угля = 1 < ε уксусной к-ты = 6 < ε воды = 81
H2O
CH 3COOH
уголь
растворитель
растворенное вещество
адсорбент
23
24.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ АДСОРБЦИИГИББС Джозайя Уиллард
(11.02.1839-28.04.1903)
Заложил основы термодинамики
поверхностных явлений
Уравнение Гиббса
с р
RT c
ср - равновесная концентрация вещества, моль/л или кмоль/м3;
Т - абсолютная температура;
Δσ/Δс - поверхностная активность, Дж/м2 или Н/м);
R - универсальная газовая постоянная
(8.31·103 Дж/кмоль·град).
24
25.
Изотермы адсорбции1. Изотерма Ленгмюра
Г Г
Ср
К Ср
Ирвинг Ленгмюр
(31.01.1881 – 16.08.1957)
25
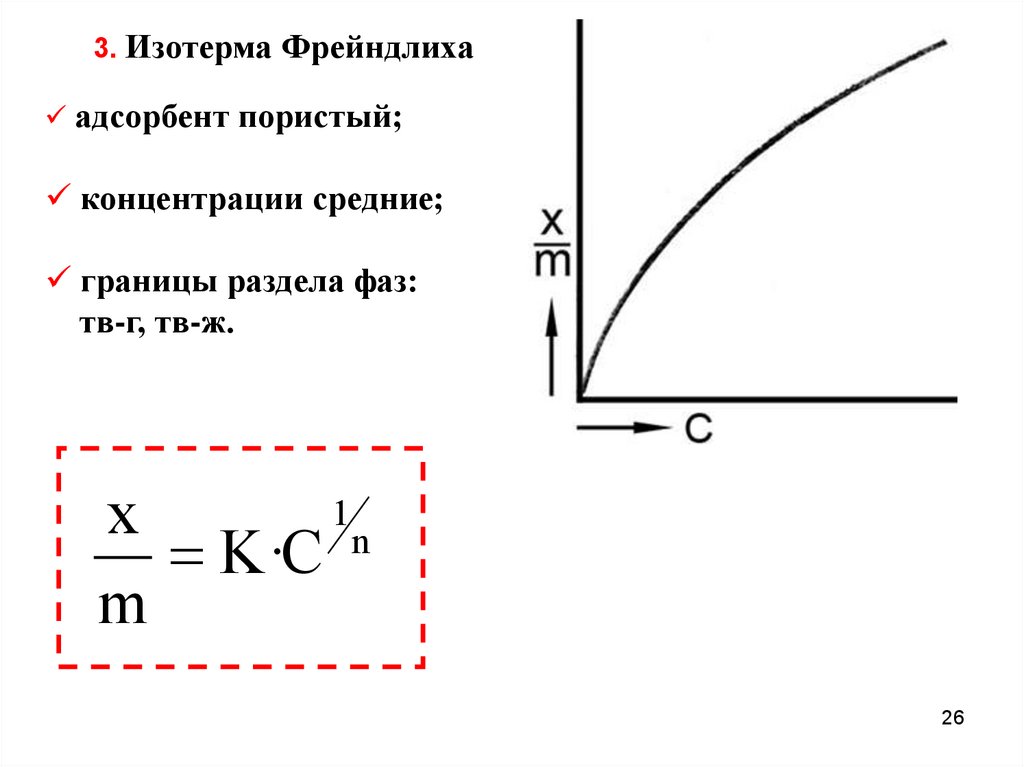
26.
3. Изотерма Фрейндлихаадсорбент пористый;
концентрации средние;
границы раздела фаз:
тв-г, тв-ж.
1
x
K·C n
m
26
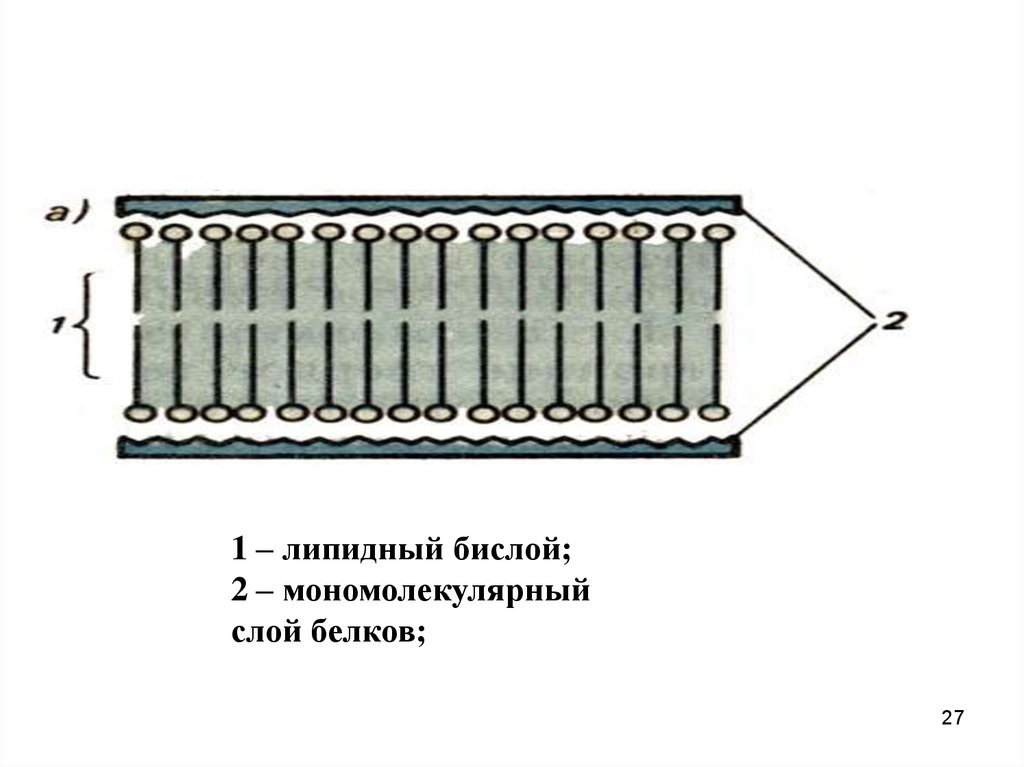
27.
1 – липидный бислой;2 – мономолекулярный
слой белков;
27
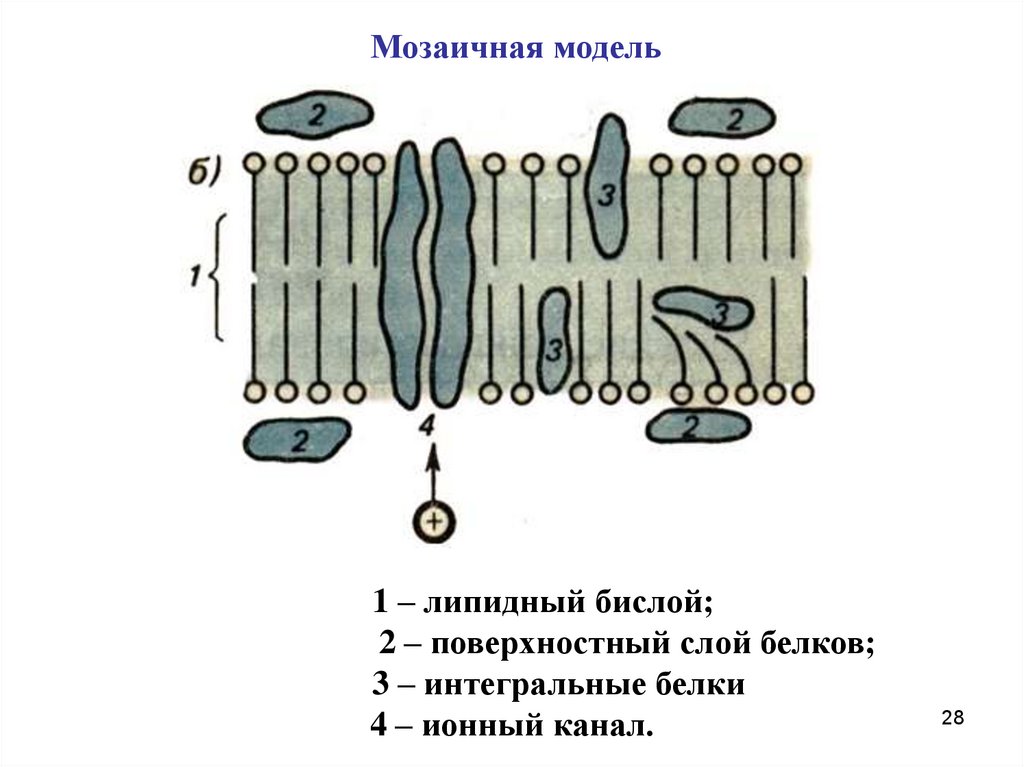
28.
Мозаичная модель1 – липидный бислой;
2 – поверхностный слой белков;
3 – интегральные белки
4 – ионный канал.
28
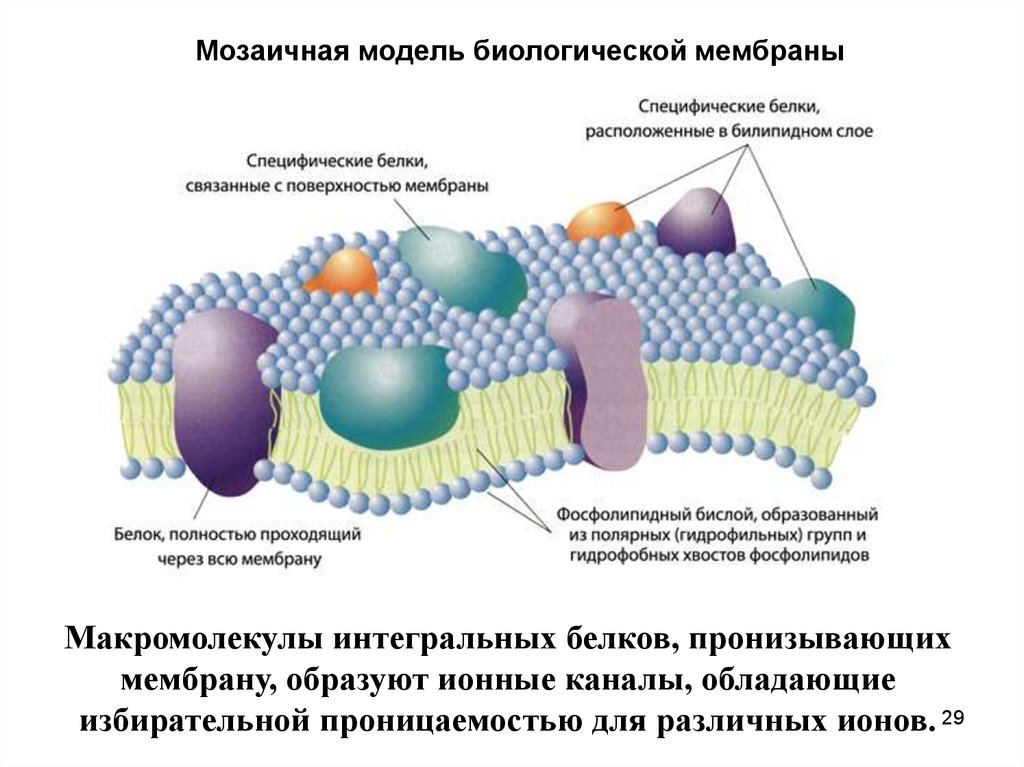
29.
Мозаичная модель биологической мембраныМакромолекулы интегральных белков, пронизывающих
мембрану, образуют ионные каналы, обладающие
избирательной проницаемостью для различных ионов. 29
30.
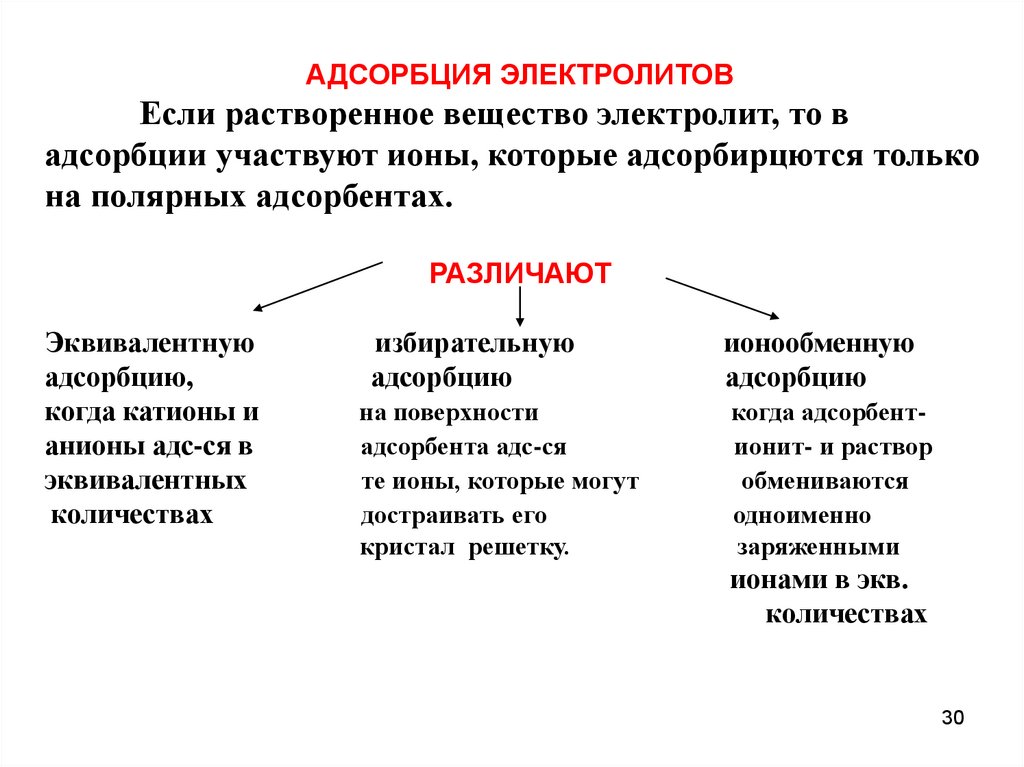
АДСОРБЦИЯ ЭЛЕКТРОЛИТОВЕсли растворенное вещество электролит, то в
адсорбции участвуют ионы, которые адсорбирцются только
на полярных адсорбентах.
РАЗЛИЧАЮТ
Эквивалентную
адсорбцию,
когда катионы и
анионы адс-ся в
эквивалентных
количествах
избирательную
адсорбцию
ионообменную
адсорбцию
на поверхности
адсорбента адс-ся
те ионы, которые могут
достраивать его
кристал решетку.
когда адсорбентионит- и раствор
обмениваются
одноименно
заряженными
ионами в экв.
количествах
30
31.
Правило Панета-ФаянсаВ первую очередь из
растворов адсорбируются
те ионы, которые входят в
состав кристаллической
решетки адсорбента
31
32.
KClZn(NO3)2
Zn 2+
+
K
NO3
AgCl
Cl-
-
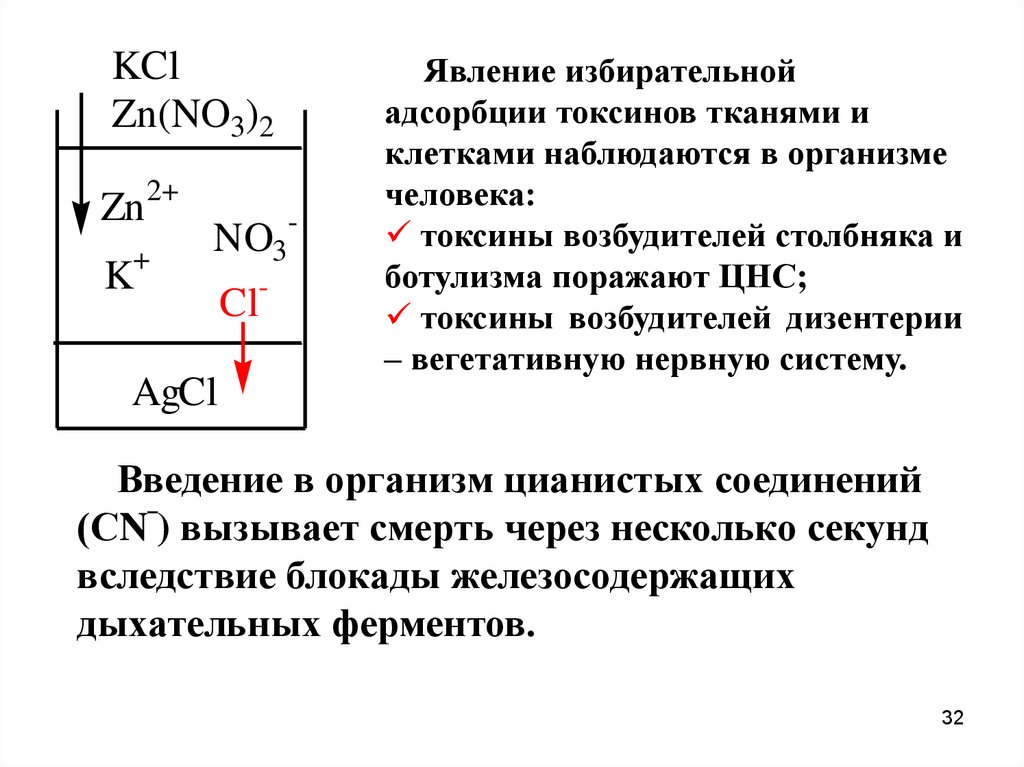
Явление избирательной
адсорбции токсинов тканями и
клетками наблюдаются в организме
человека:
токсины возбудителей столбняка и
ботулизма поражают ЦНС;
токсины возбудителей дизентерии
– вегетативную нервную систему.
Введение в организм цианистых соединений
(СN‾) вызывает смерть через несколько секунд
вследствие блокады железосодержащих
дыхательных ферментов.
32
33.
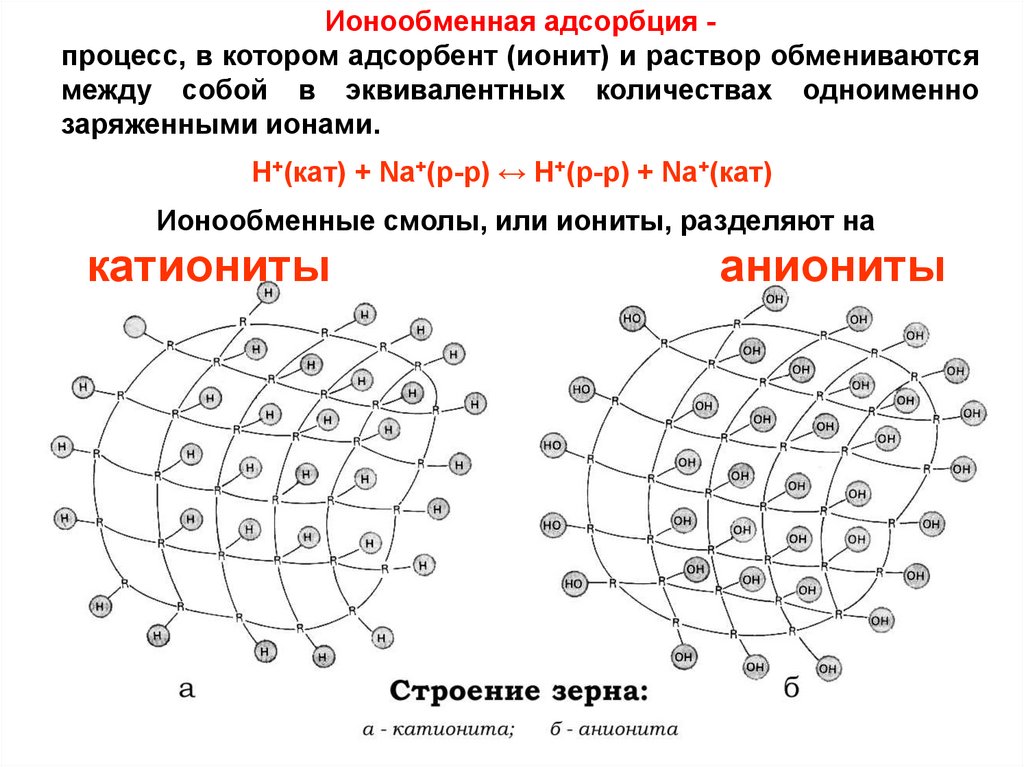
Ионообменная адсорбция процесс, в котором адсорбент (ионит) и раствор обмениваютсямежду собой в эквивалентных количествах одноименно
заряженными ионами.
Н+(кат) + Nа+(р-р) ↔ Н+(р-р) + Nа+(кат)
Ионообменные смолы, или иониты, разделяют на
катиониты
аниониты
33
34.
Применение ионитов1. Разделение и очистка аминокислот и белков
2. Консервирование крови
3. Изменение солевого состава молока
34
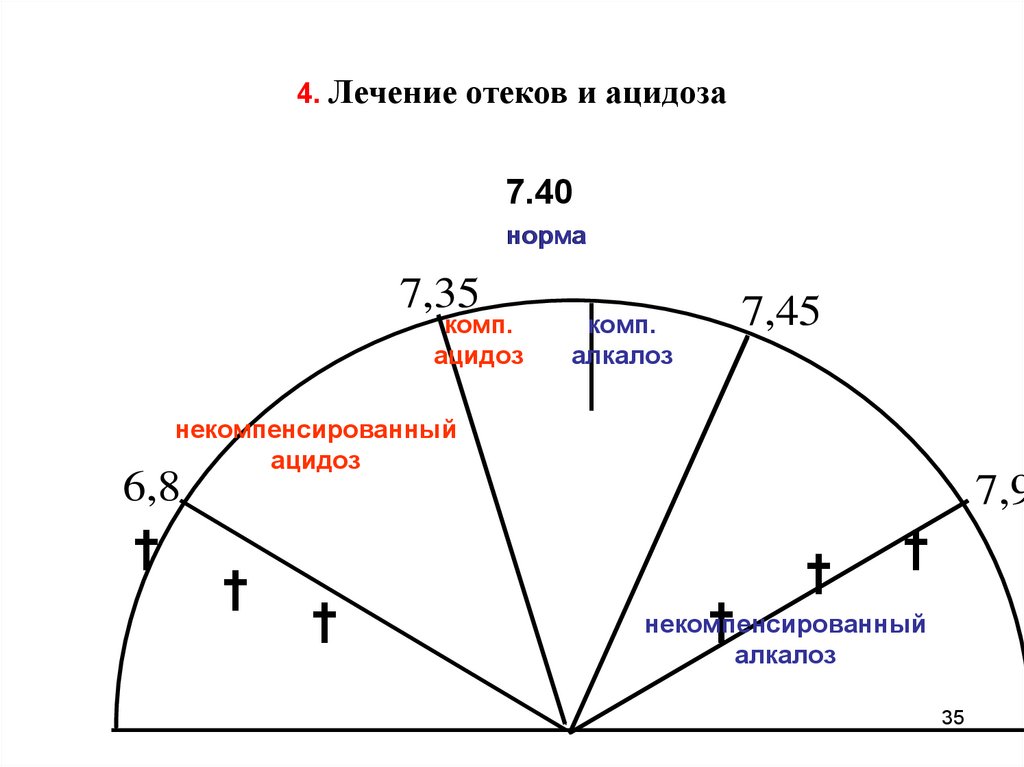
35.
4. Лечение отеков и ацидоза7.40
норма
7,35
комп.
ацидоз
7,45
комп.
алкалоз
некомпенсированный
ацидоз
6,8
†
7,9
†
†
†
†
†
некомпенсированный
алкалоз
35
36.
Для удаления токсических веществ избиологических жидкостей через
адсорбент пропускают:
кровь –
гемосорбция (гемоперфузия)
плазму –
плазмосорбция (плазмоперфузия);
лимфу –
лимфосорбция (лимфоперфузия).
36
























 Химия
Химия








