Похожие презентации:
Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп
1.
Vita brevis, ars longa –життя коротке, наука обширна
2. План
ПЛАН1.
2.
3.
4.
5.
6.
Класифікація органічних сполук за будовою вуглецевого
скелету та природою функціональних груп.
Основні принципи будови назв органічних сполук за
номенклатурою ІЮПАК.
Електронна будова хімічних зв’язків. Типи хімічних зв’язків в
органічних сполуках. Види гібридизації атомних орбіталей
вуглецю. Важливі характеристики σ- та π - зв’язків (довжина,
енергія, помірність, здатність до поляризації).
Взаємний вплив атомів в органічних сполуках. Індуктивний
ефект. Супряжені системи з відкритими та замкненими
ланцюгами, види супряжень
Електронодонорні і електроноакцепторні замісники.
Загальна характеристика реакцій органічних сполук.
3. Предмет органічної хімії
ПРЕДМЕТ ОРГАНІЧНОЇХІМІЇ
Органічна хімія — це хімія сполук атома
Карбону та інших елементів ПС
Елементи Н, О, N, S, галогени –
називають органогенами.
Органічна хімія — це хімія вуглеводнів і
їх похідних
4. Основні положення теорії будови органічних сполук (1861)
ОСНОВНІ ПОЛОЖЕННЯ ТЕОРІЇ БУДОВИОРГАНІЧНИХ СПОЛУК (1861)
БУТЛЕРОВ
Олександр Михайлович
3(15) вересня 1828 р. –
5(17) серпня 1886 р.
5.
Основні положення теорії будови органічнихсполук (1861)
1. Атоми, що входять до складу молекули
органічних сполук, зв’язані між собою в
суворо визначеному порядку, згідно з їх
валентністю.
Послідовність
зв’язування
атомів у молекулі називається хімічною
будовою.
2. Властивості речовини залежать не тільки
від того, які атоми і в якій кількості входять
до складу її молекули, але й від того, в якій
послідовності вони зв’язані між собою, тобто
від хімічної будови молекули.
6.
Основні положення теорії будови органічнихсполук (1861)
Атоми або групи атомів, які утворюють
молекулу, як зв’язані безпосередньо, так і
зв’язані через інші атоми, взаємно впливають
одні на других, від чого залежить реакційна
здатність молекули.
4. Вивчаючи реакційну здатність речовини,
можна встановити її будову, і навпаки, за
будовою речовини можна судити про її
властивості.
3.
7.
СКЛАД – БУДОВА – ВЛАСТИВОСТІСучасне трактування:
Властивості складних речовин залежать від
якісного і кількісного складу і від хімічної
будови, а також від взаємного впливу атомів в
молекулі.
Значення теорії будови органічних сполук
Зв’язок між будовою і властивостями стверджує
пізнаваність органічних речовин і відкриває широку
дорогу до вивчення синтезу і структури речовин. Дійсно,
з основного положення теорії випливає, що вивчення
властивостей речовин дає можливість знати будову і
навпаки.
8.
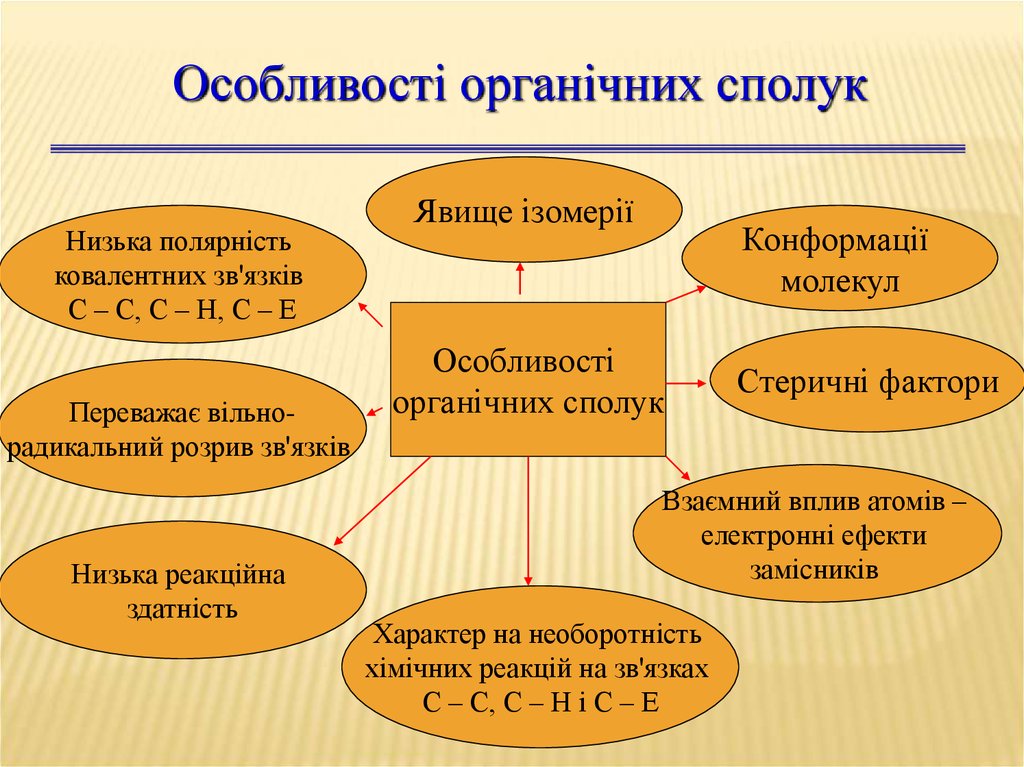
Особливості органічних сполукНизька полярність
ковалентних зв'язків
С – С, С – Н, С – Е
Переважає вільнорадикальний розрив зв'язків
Низька реакційна
здатність
Явище ізомерії
Конформації
молекул
Особливості
органічних сполук
Стеричні фактори
Взаємний вплив атомів –
електронні ефекти
замісників
Характер на необоротність
хімічних реакцій на зв'язках
С – С, С – Н і С – Е
9.
Основні положення теорії будови органічнихсполук (1861)
Структурна формула — це зображення
послідовності зв'язування атомів в молекулі.
Брутто-формула – СН4О або CH3OH
Структурна формула
H
H C O H
H
CH3OH
Спрощені формули будови
називають раціональними
іноді
10.
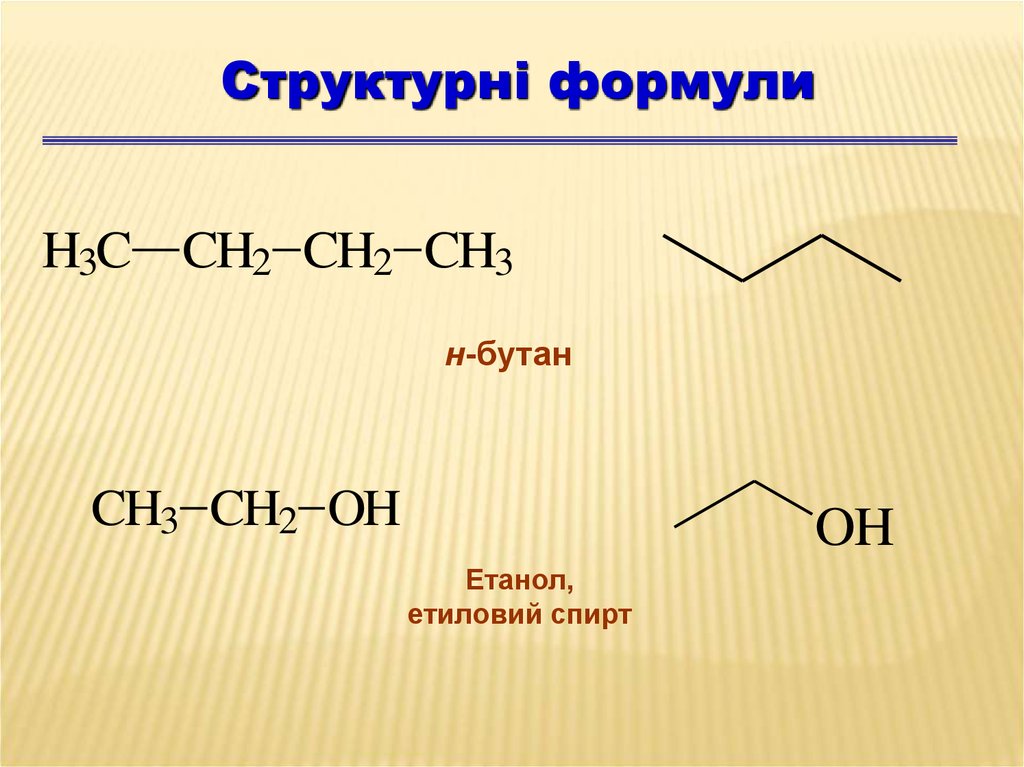
Структурні формулиH3C CH2 CH2 CH3
н-бутан
CH3 CH2 OH
OH
Етанол,
етиловий спирт
11.
Класифікація органічнихсполук
12. Классификация органических соединений
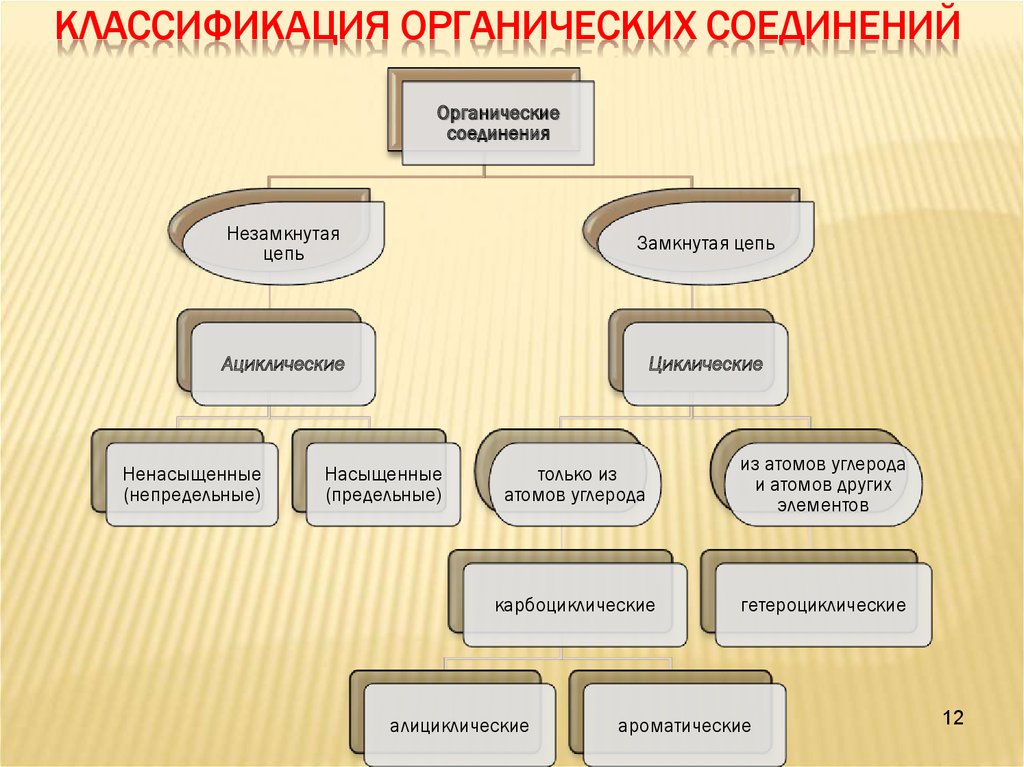
КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙОрганические
соединения
Незамкнутая
цепь
Замкнутая цепь
Ациклические
Циклические
Ненасыщенные
(непредельные)
Насыщенные
(предельные)
только из
атомов углерода
из атомов углерода
и атомов других
элементов
карбоциклические
гетероциклические
алициклические
ароматические
12
13.
Функціональна групаФункціональна група – це атом або група
певним чином зв'язаних атомів, наявність
якої в молекулі органічної речовини надає їх
характерних властивостей і визначає його
приналежність до того чи іншого класу
сполук
O
O
O
C
OH H2N CH2 C
CH3 C
OH
OH
ацетатна кислота
бензоатна кислота
гліцин (амінокислота)
14.
* Классификация органических соединенийФункциональная группа
Название класса
Общая
формула
класса
-F, -Cl, -Br, -I(Hal)
Галогены
Галогенпроизводные
R-Hal
-OH
Гидроксильная
Спирты, фенолы
R-OH
-OR
Алкоксильная
Простые эфиры
R-OR
-SH
Тиольная
Тиолы (тиоспирты,
меркаптаны)
R-SH
-SR
Алкилтиольная
Тиоэфиры (сульфиды)
R-SR
- SО3Н
Сульфоновая
Сульфокислоты
-SО3Н
-NH2; >NH; >N-
Амины
R-NH2; R2NH;
15.
* Классификация органических соединенийФункциональная группа
Название класса
Общая формула
класса
-NО2
Нитро
Нитросоединения
R-NО2
-С≡N
Циано
Нитрилы
R-С≡N
Альдегиды
Кетоны
Карбонильная
Карбоновые кислоты
Карбоксильная
Сложные эфиры
Алкоксикарбонильная
Амиды
16.
Класифікація органічнихсполук
Сполуки можуть містити не одну, а декілька
функціональних груп. Якщо ці групи
однакові, то такі сполуки називаються
поліфункціональними.
CHCl3
CH2 CH CH2
OH OH OH
хлороформ
гліцерин
17.
Класифікація органічнихсполук
Сполуки, що містять різні функціональні
групи, називаються гетерофункціональними.
CH3 CH COOH
CH2 CH2
OH
NH2 OH
молочна кислота
коламін
18.
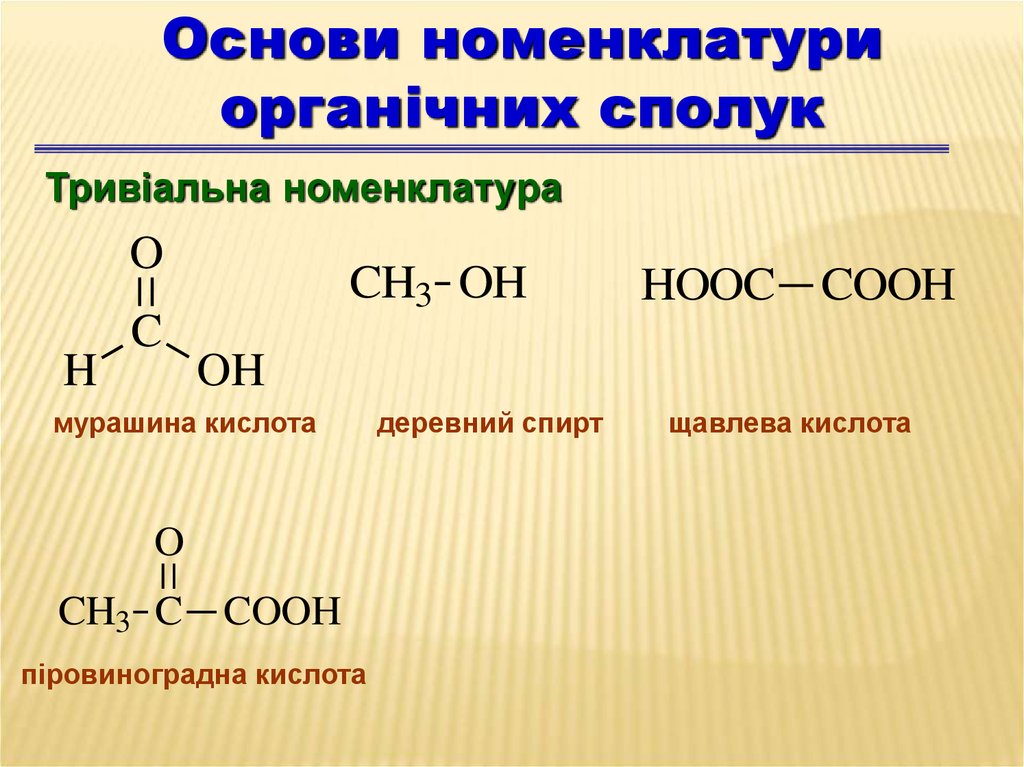
Основи номенклатуриорганічних сполук
Тривіальна номенклатура
O
H
C
CH3 OH
HOOC COOH
OH
мурашина кислота
O
CH3 C COOH
піровиноградна кислота
деревний спирт
щавлева кислота
19.
Основи номенклатуриорганічних сполук
Тривіальна номенклатура
O
O
HN
NH
O
Барбітурова кислота
31.10.1835 – 20.08.1917
Іоганн Фрідріх Вільгельм Адольф фон Байєр
20.
Основи номенклатуриорганічних сполук
Раціональна номенклатура
H3C
C C CH3
диметилацетилен
H3C
CH
CH
H3C
CH3
диметилетилен
CH3
OH
CH3 CH2 C CH2 CH2 CH3
CH
H3C
C C
O
OH
CH3
CH3
етилпропілізопропілкарбінол
триметилоцтова кислота
21.
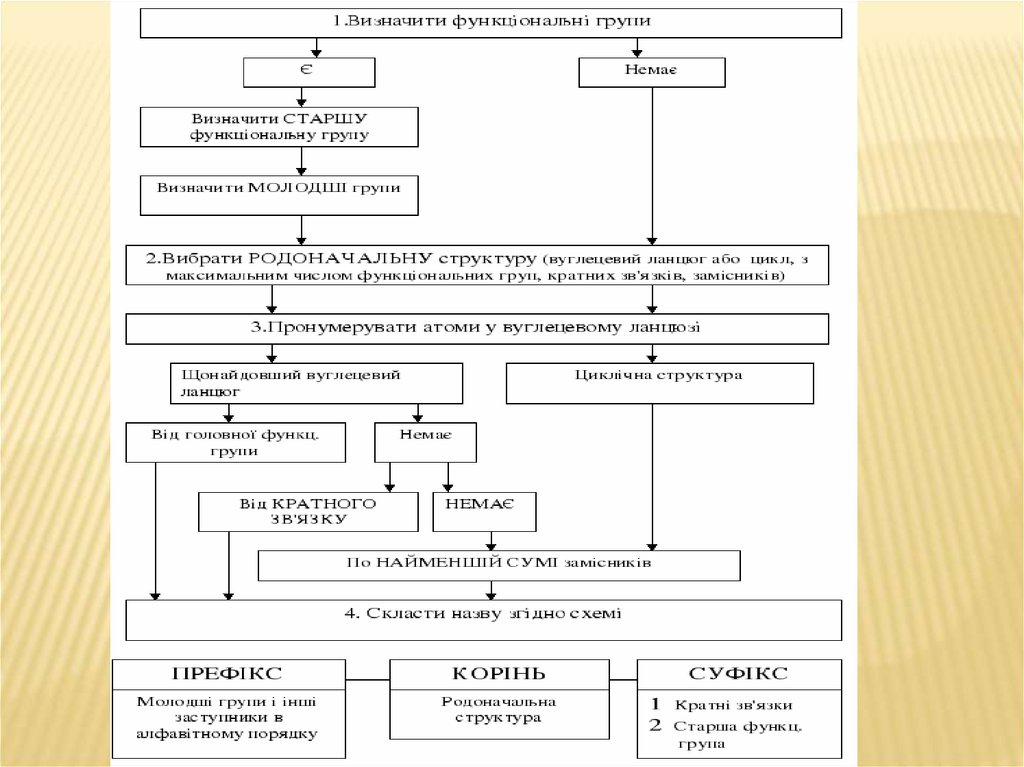
Основи номенклатуриорганічних сполук
Систематична номенклатура ІЮПАК
ІЮПАК [від англійської назви Міжнародного союзу
чистої і прикладної хімії — International Union of Pure
and Applied Chemistry (IUPAC)]
Систематичні назви складені
зі слів, спеціально створених або
вибраних для опису структурних
особливостей сполук.
замісникова
та
радикальнофункціональна
22.
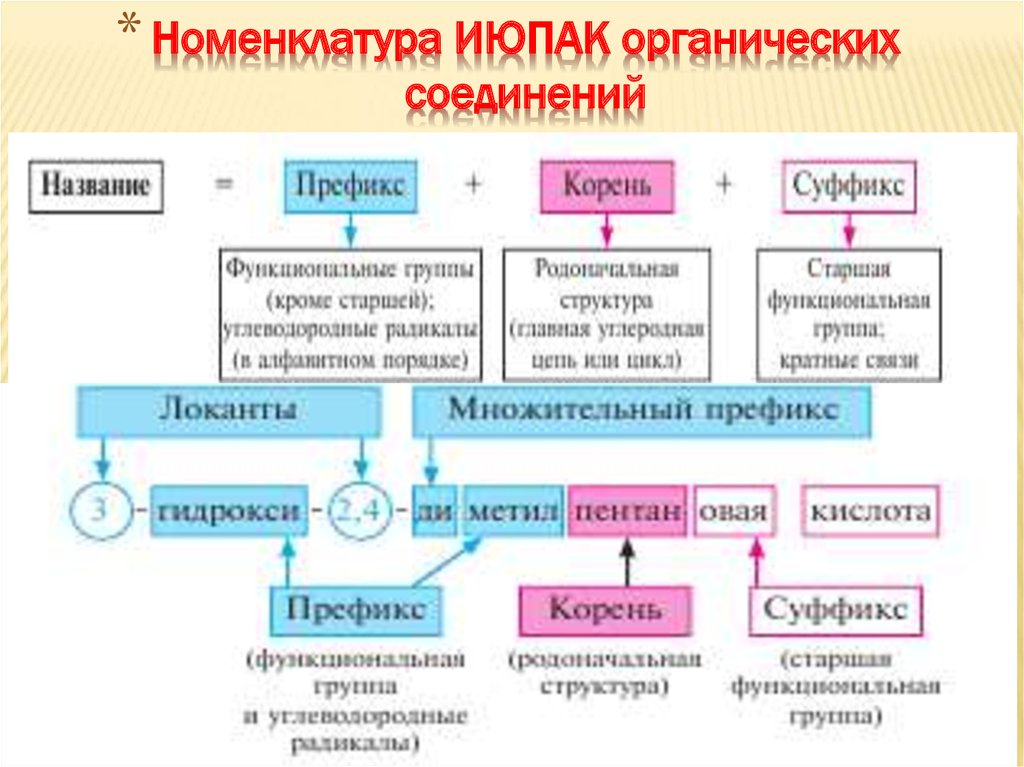
23.
* Номенклатура ИЮПАК органическихсоединений
23
24.
Основи номенклатуриорганічних сполук
Систематична номенклатура ІЮПАК
Характеристична група
—(C)OOH
Префікс
Суфікс
—
-ова кислота
карбокси-
-карбонова кислота
сульфо-
-сульфокислота
—(C)H=O
оксо-
-аль
—CH=O
форміл-
-карбальдегід
оксо-
-он
—OH
гідрокси-2
-ол
—SH
меркапто-
-тіол
—NH2
аміно-
-амін
—NO2
нітро-
—
—COOH
—SO3H
25.
У випадку наявності в сполуці декількох функціональних груп, то саместарша функціональна група визначає приналежність до класу, а замісники
позначають літерами грецького алфавіту , , , і т. д., причому літерою
позначається перший атом від функціональної групи, а для назви родоначальної
структури використовують тривіальну назву:
O
H
H3C C
C
NH2
H
H3C C
O
C
2
H
H3C C
NH2
-амінопропіонова кислота (радикально-функціональна)
OH
NH2
3
OH
аланін (тривіальна назва)
1
O
C
OH
2-амінопропанова кислота (замісникова ІЮПАК)
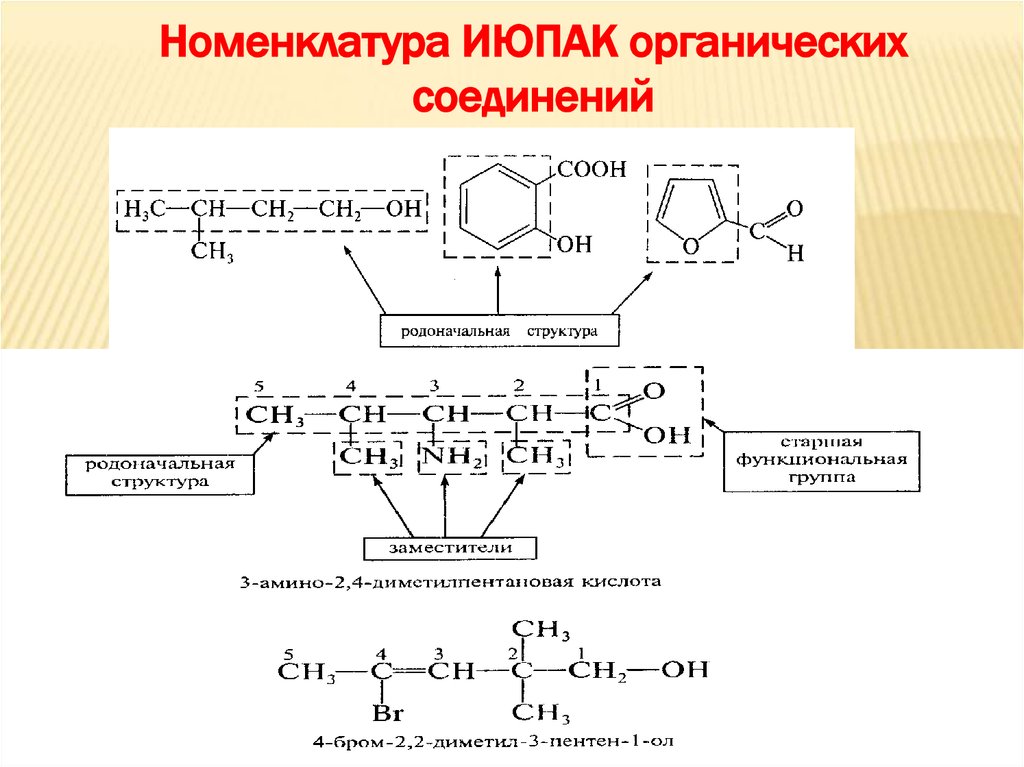
26.
Номенклатура ИЮПАК органическихсоединений
27.
Ізомерія ОСІзомери — це речовини, які мають
однаковий якісний і кількісний
склад (молекулярну формулу), але
різну хімічну будову і, тому,
володіють різними
властивостями.
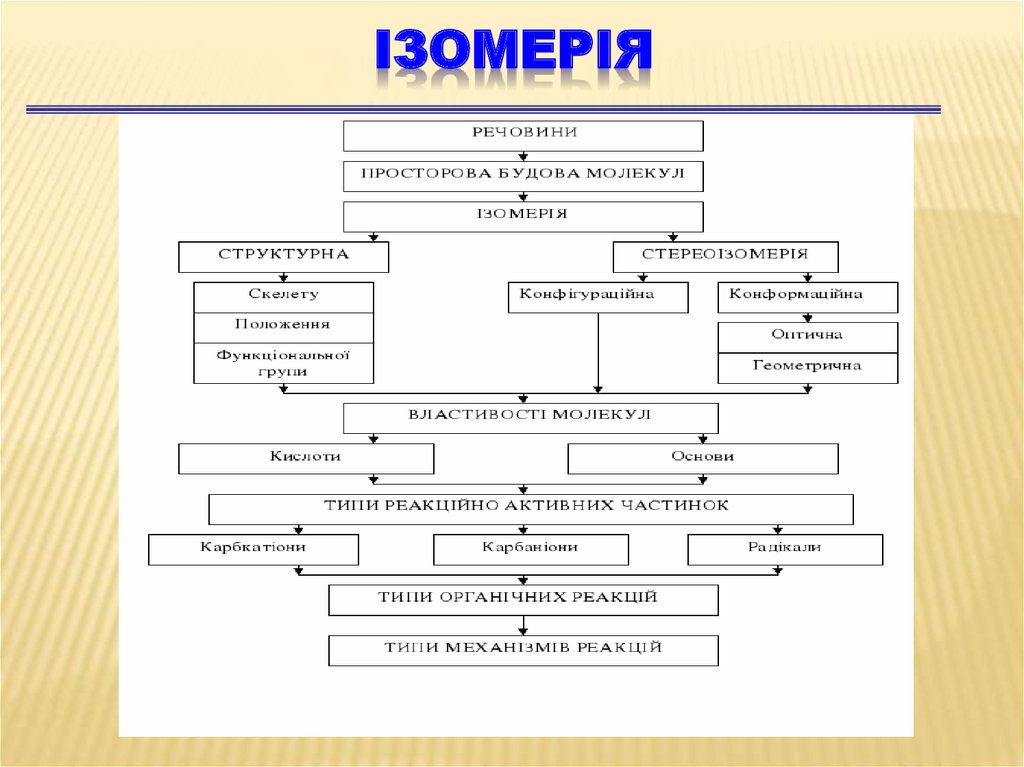
28. Ізомерія ОС
ІЗОМЕРІЯ ОСІзомерія
Структурна
Статична
1. Ізомерія
вуглецевого
скелету
2. Ізомерія
положення
функціональної
групи
3. Ізомерія
самих функціональних груп
(метамерія)
Динамічна
(таутомерія)
Просторова (Стереоізомерія)
Конфігураційна Конформаційна
(поворотна)
Оптична
Геометрична
1. Енантіомерія
2. Діастереомерія
29.
ІЗОМЕРІЯ30.
ІзомеріяС2Н6О
H H
H C C O H
H H
етиловий спирт
Ткип= 78 С
H
H
H C O C H
H
H
диметиловий ефір
Ткип= -24 С
31.
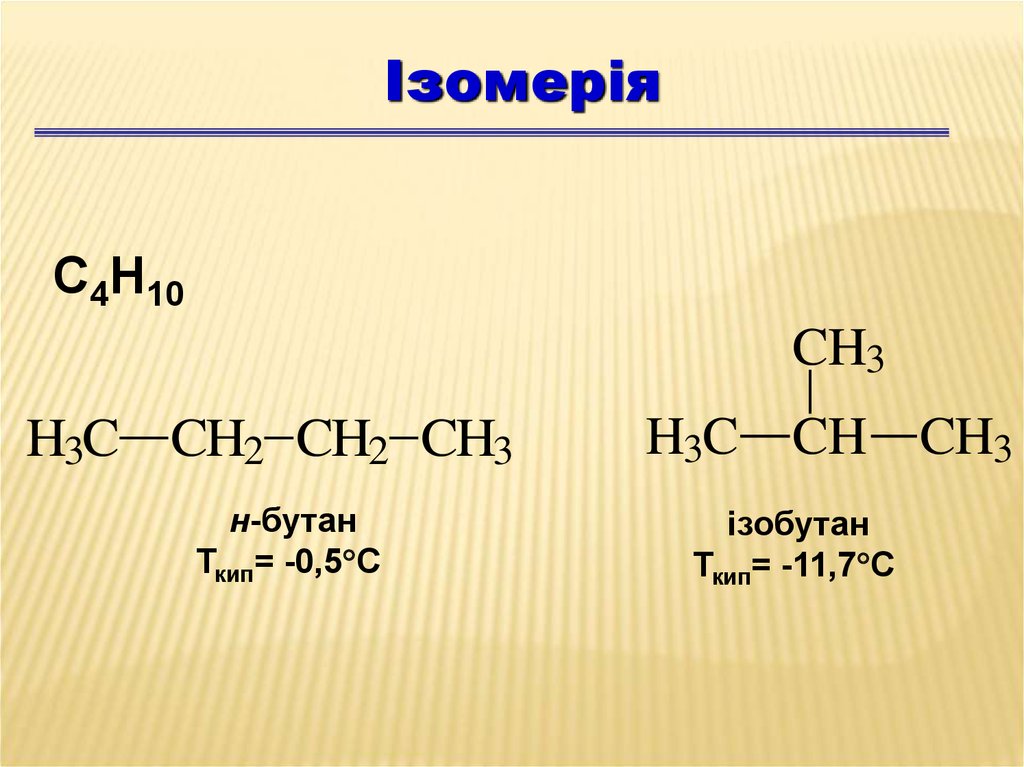
ІзомеріяС4Н10
CH3
H3C CH2 CH2 CH3
н-бутан
Ткип= -0,5 С
H3C
CH CH3
ізобутан
Ткип= -11,7 С
32.
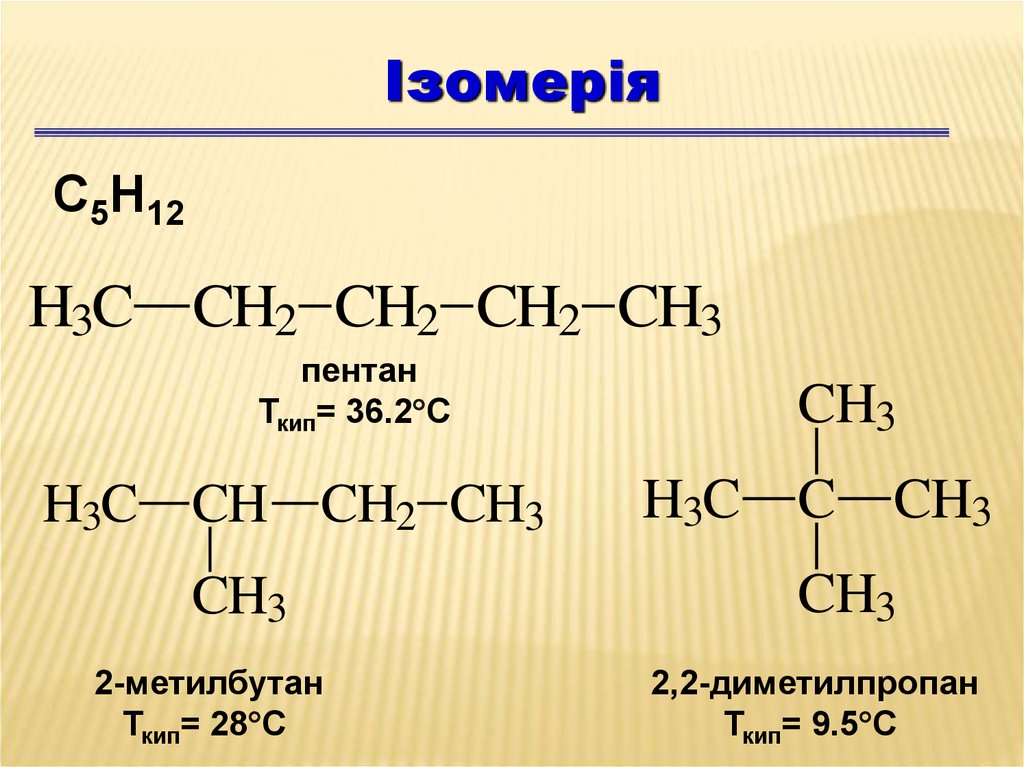
ІзомеріяС5Н12
H3C CH2 CH2 CH2 CH3
пентан
Ткип= 36.2 С
H3C CH CH2 CH3
CH3
2-метилбутан
Ткип= 28 С
CH3
H3C
C
CH3
CH3
2,2-диметилпропан
Ткип= 9.5 С
33.
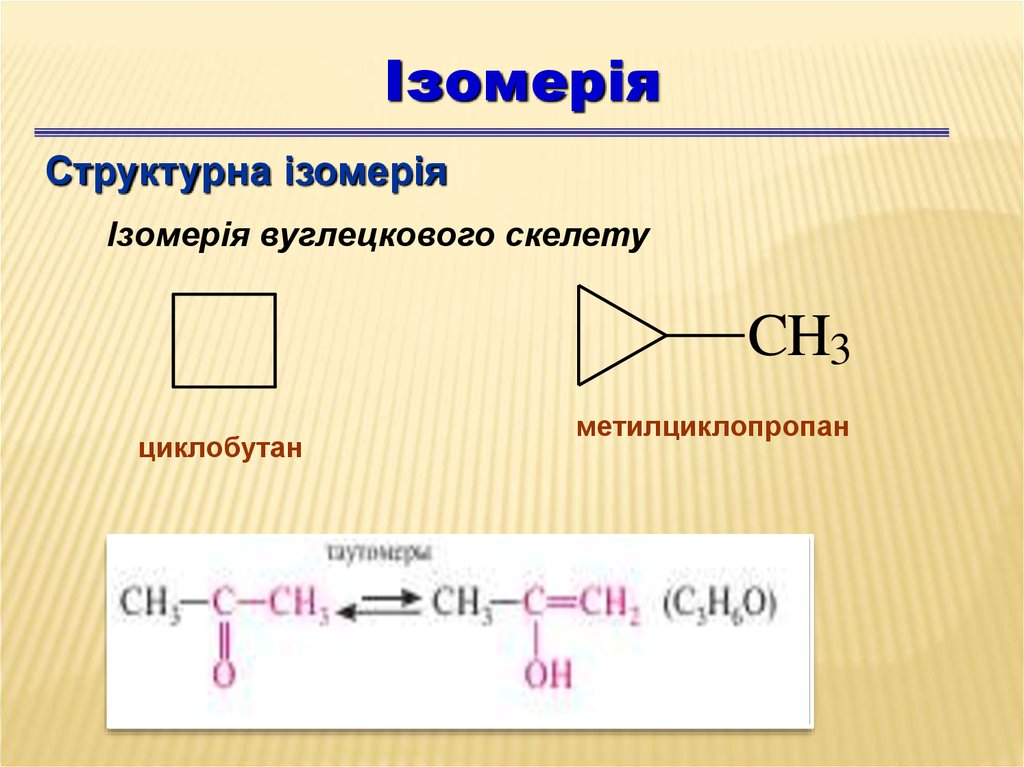
ІзомеріяСтруктурна ізомерія
Ізомерія вуглецкового скелету
CH3
циклобутан
метилциклопропан
34.
ІзомеріяСтруктурна ізомерія
Ізомерія положення функціональної групи
CH3CH2CH2CH2OH
CH3CHCH2CH3
OH
бутанол-1
бутанол-2
CH2 CHCH3CH3
CH3CH CHCH3
бутен-1
бутен-2
35.
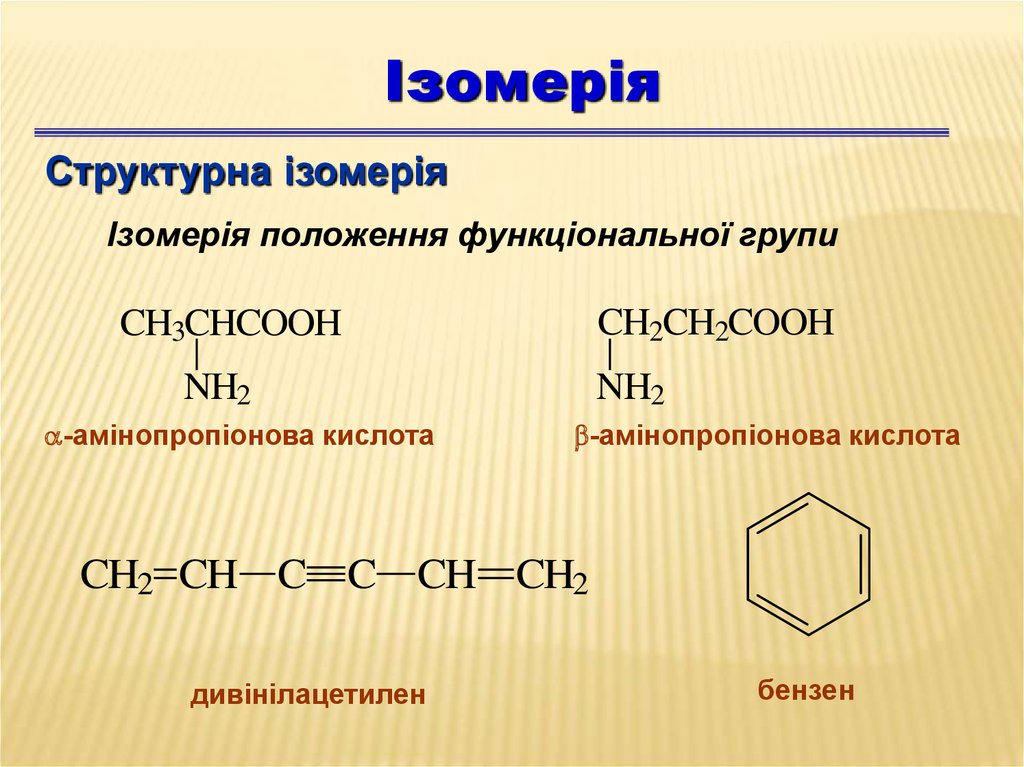
ІзомеріяСтруктурна ізомерія
Ізомерія положення функціональної групи
CH2CH2COOH
CH3CHCOOH
NH2
NH2
-амінопропіонова кислота
-амінопропіонова кислота
CH2 CH C C CH CH2
дивінілацетилен
бензен
36.
ГомологиГрупи органічних сполук однотипної
структури з однаковими функціональними
групами, що відрізняються один від одного
на одну або декілька груп CH2 у вуглецевому
ланцюгу, складають гомологічний ряд.
Гомологічний ряд метана
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
37.
ГомологиГомологічний ряд ізобутану
CH3
CH3CHCH3
CH3
CH3CHCH2CH3
CH3
CH3CHCH2CH2CH3
CH3
CH3CHCH2CH2CH2CH3
Гомологічний ряд метанолу
CH3OH
CH3CH2OH
CH3CH2CH2CH2OH
CH3CH2CH2OH
38. Електронна структура атома Карбону в органічних сполуках
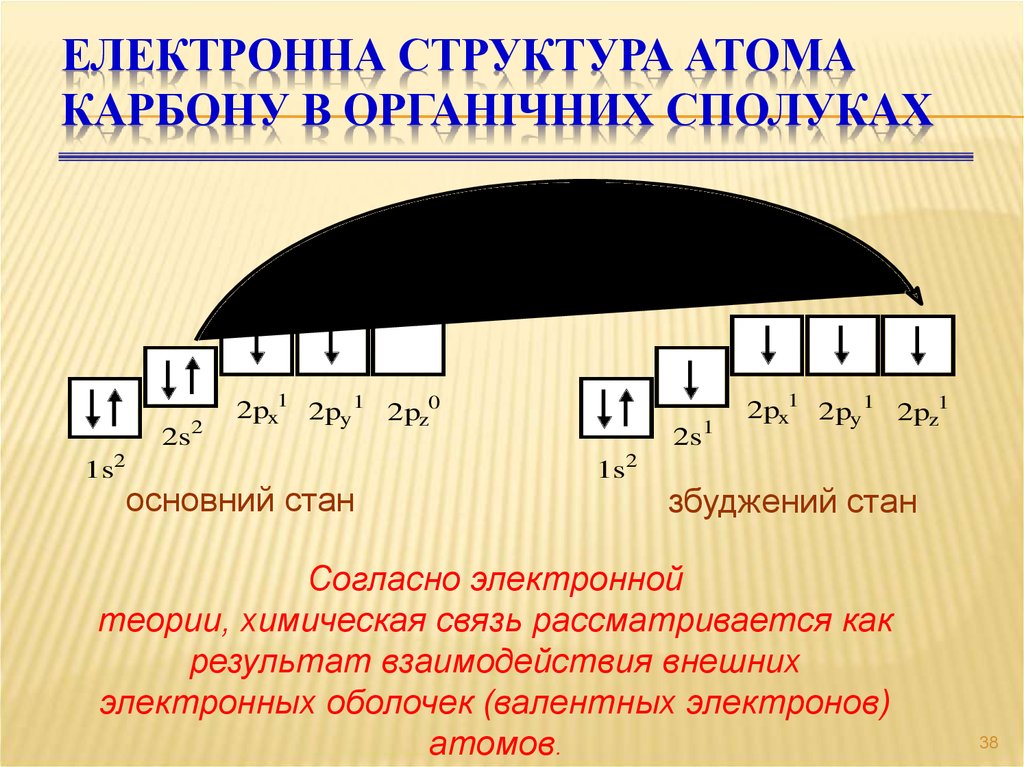
ЕЛЕКТРОННА СТРУКТУРА АТОМАКАРБОНУ В ОРГАНІЧНИХ СПОЛУКАХ
2s2
1s2
2px1 2py 1 2pz0
основний стан
2s1
1s2
2px1 2py 1 2pz1
збуджений стан
Согласно электронной
теории, химическая связь рассматривается как
результат взаимодействия внешних
электронных оболочек (валентных электронов)
атомов.
38
39. Типи хімічних зв'язків
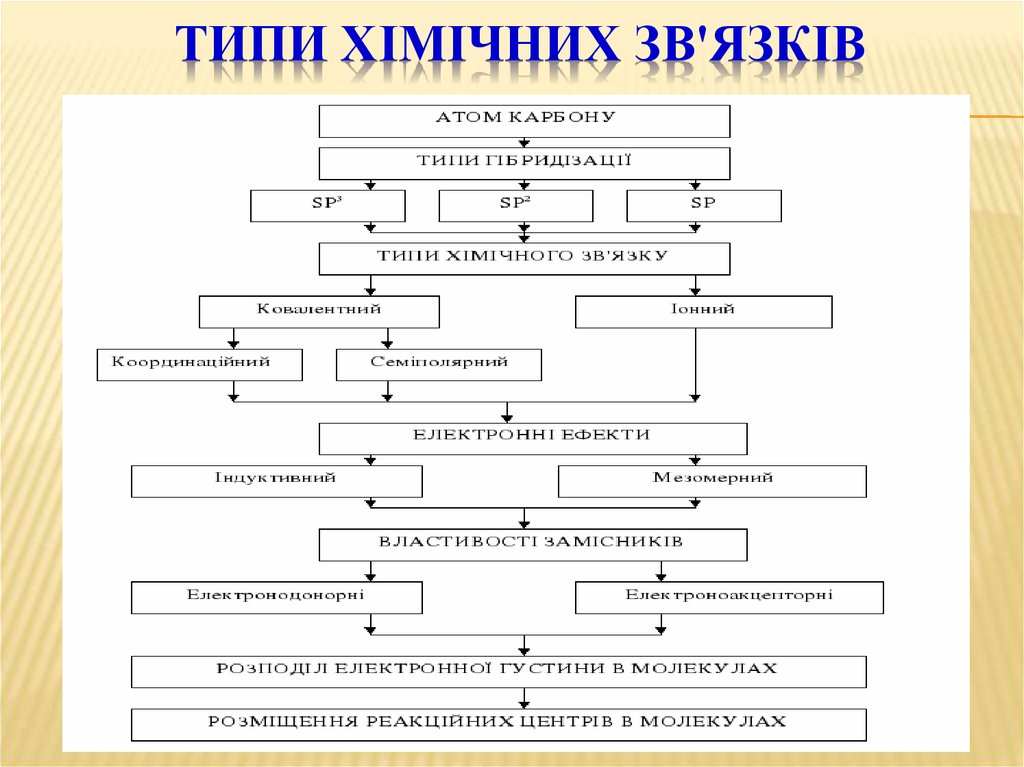
ТИПИ ХІМІЧНИХ ЗВ'ЯЗКІВ40.
Электронное строение химических связейорганических соединений
41. Гібридизація
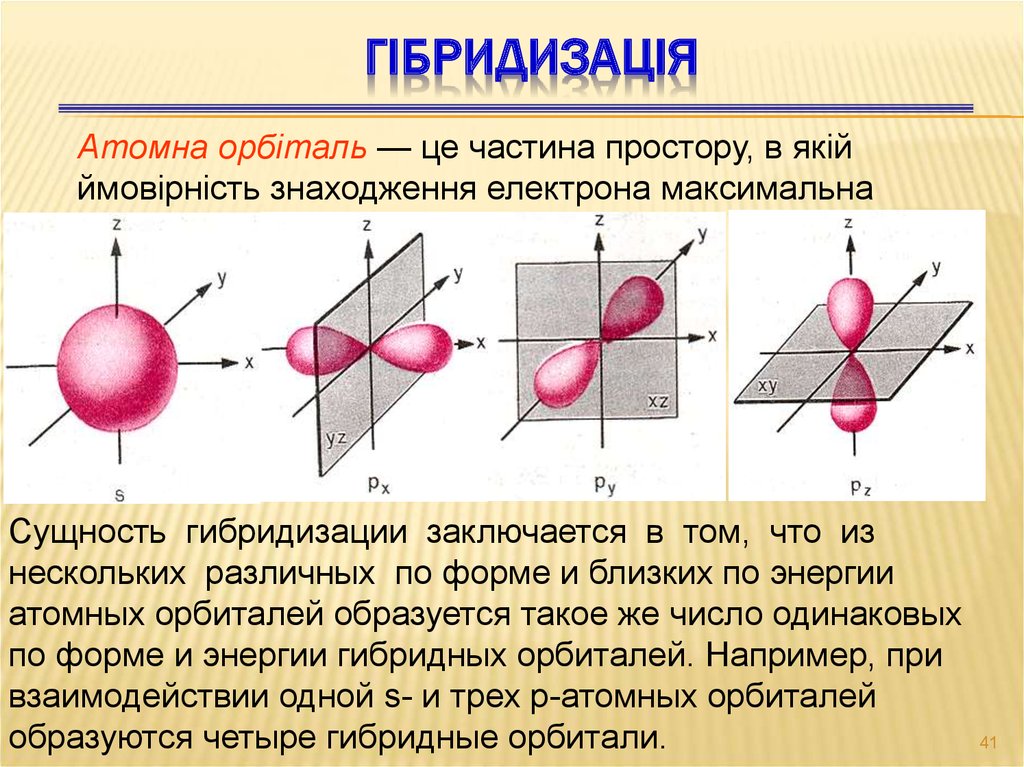
ГІБРИДИЗАЦІЯАтомна орбіталь — це частина простору, в якій
ймовірність знаходження електрона максимальна
Сущность гибридизации заключается в том, что из
нескольких различных по форме и близких по энергии
атомных орбиталей образуется такое же число одинаковых
по форме и энергии гибридных орбиталей. Например, при
взаимодействии одной s- и трех р-атомных орбиталей
образуются четыре гибридные орбитали.
41
42.
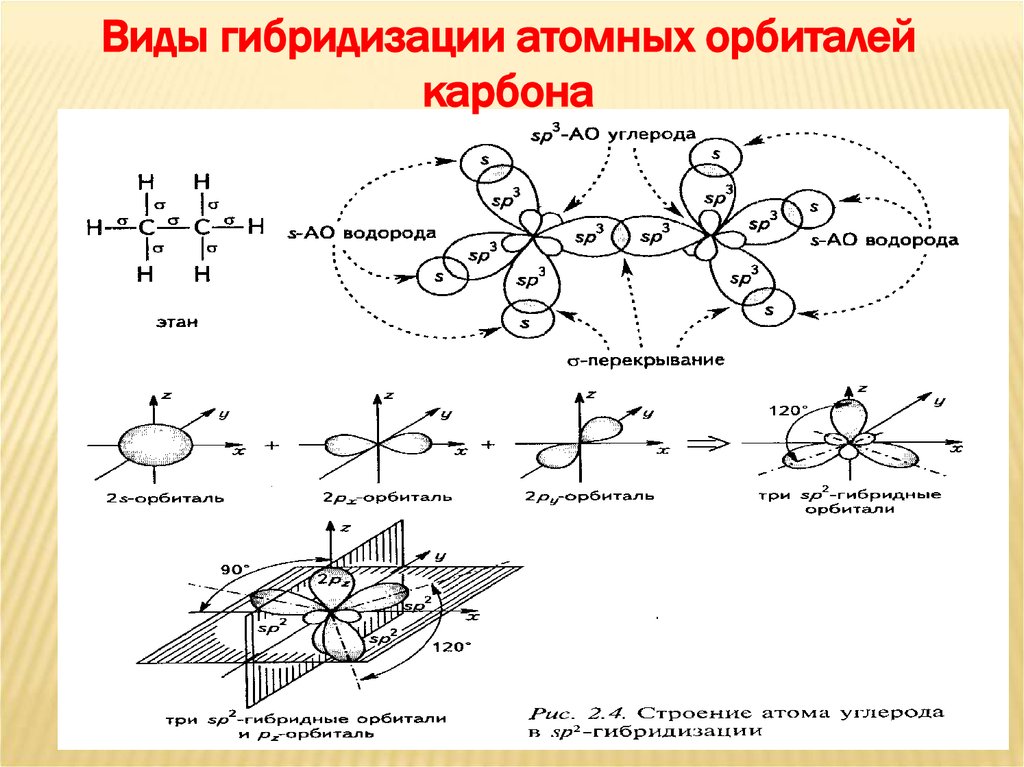
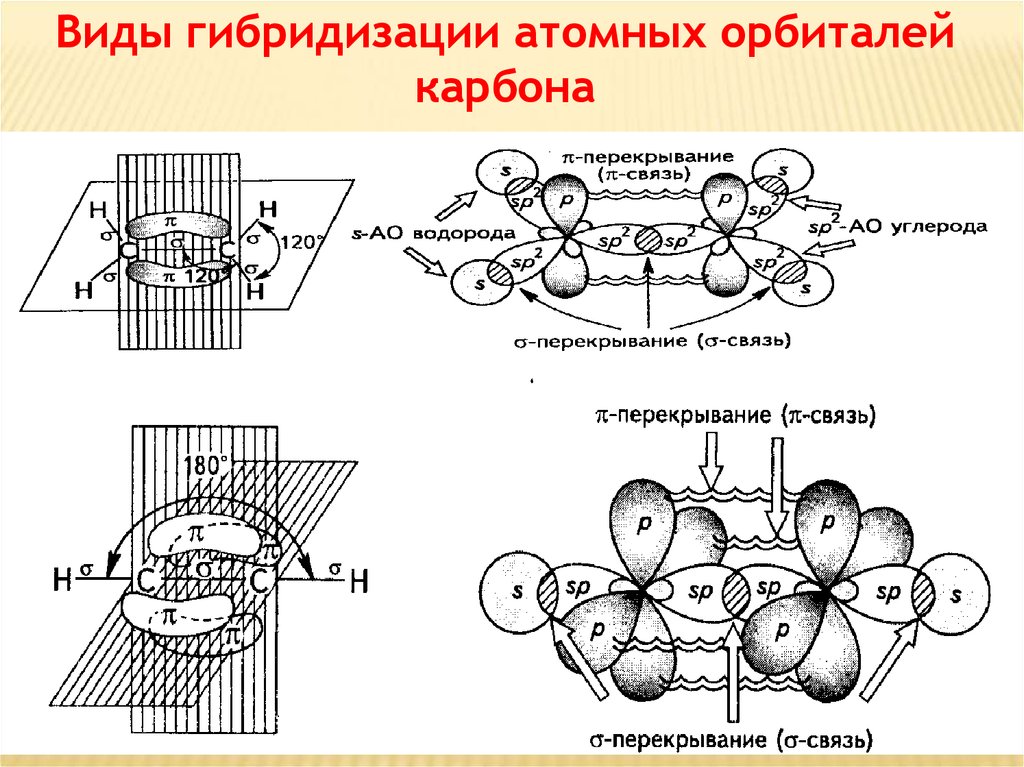
Виды гибридизации атомных орбиталейкарбона
42
43.
Виды гибридизации атомных орбиталейкарбона
43
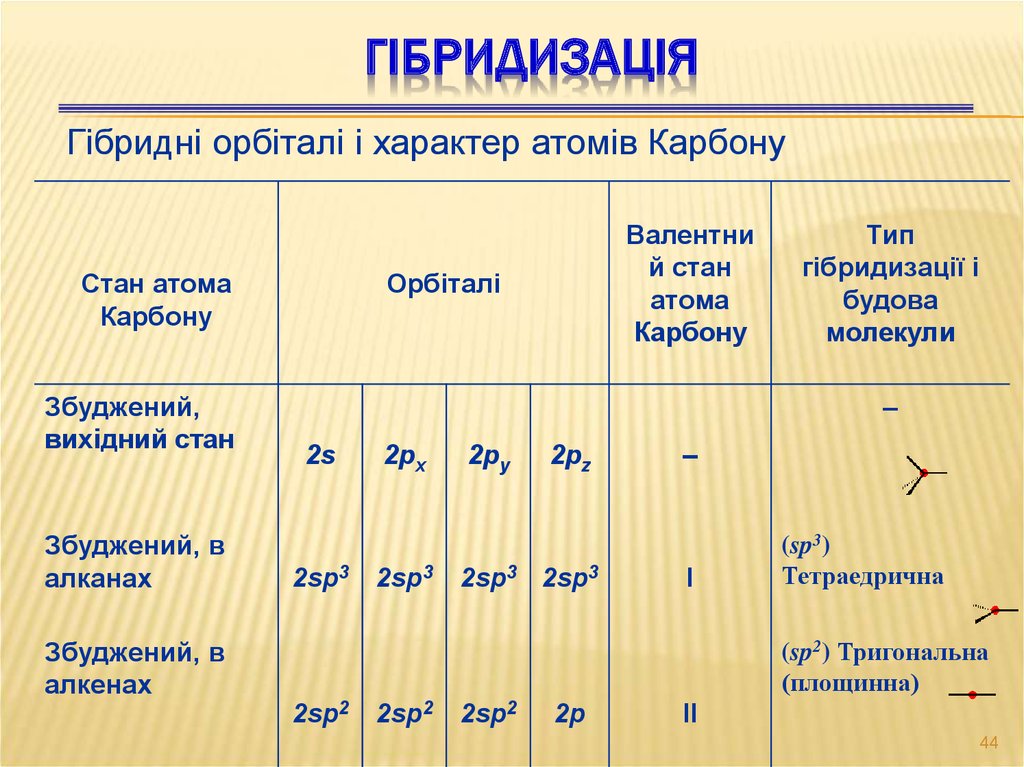
44. Гібридизація
ГІБРИДИЗАЦІЯГібридні орбіталі і характер атомів Карбону
Стан атома
Карбону
Збуджений,
вихідний стан
Збуджений, в
алканах
Валентни
й стан
атома
Карбону
Орбіталі
Тип
гібридизації і
будова
молекули
–
2s
2sp3
2px
2sp3
2py
2pz
2sp3 2sp3
–
I
Збуджений, в
алкенах
(sp3)
Тетраедрична
(sp2) Тригональна
(площинна)
2sp2
2sp2
2sp2
2p
II
44
45. Різні види перекривання орбіталей
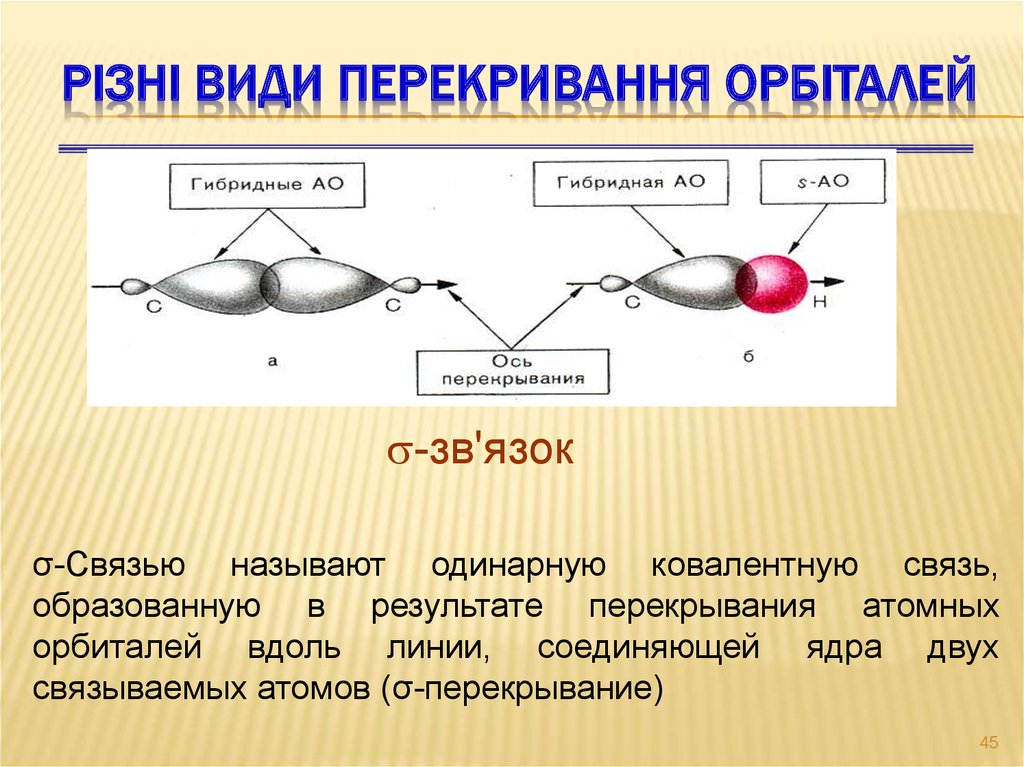
РІЗНІ ВИДИ ПЕРЕКРИВАННЯ ОРБІТАЛЕЙ-зв'язок
σ-Связью называют одинарную ковалентную связь,
образованную в результате перекрывания атомных
орбиталей вдоль линии, соединяющей ядра двух
связываемых атомов (σ-перекрывание)
45
46. Різні види перекривання орбіталей
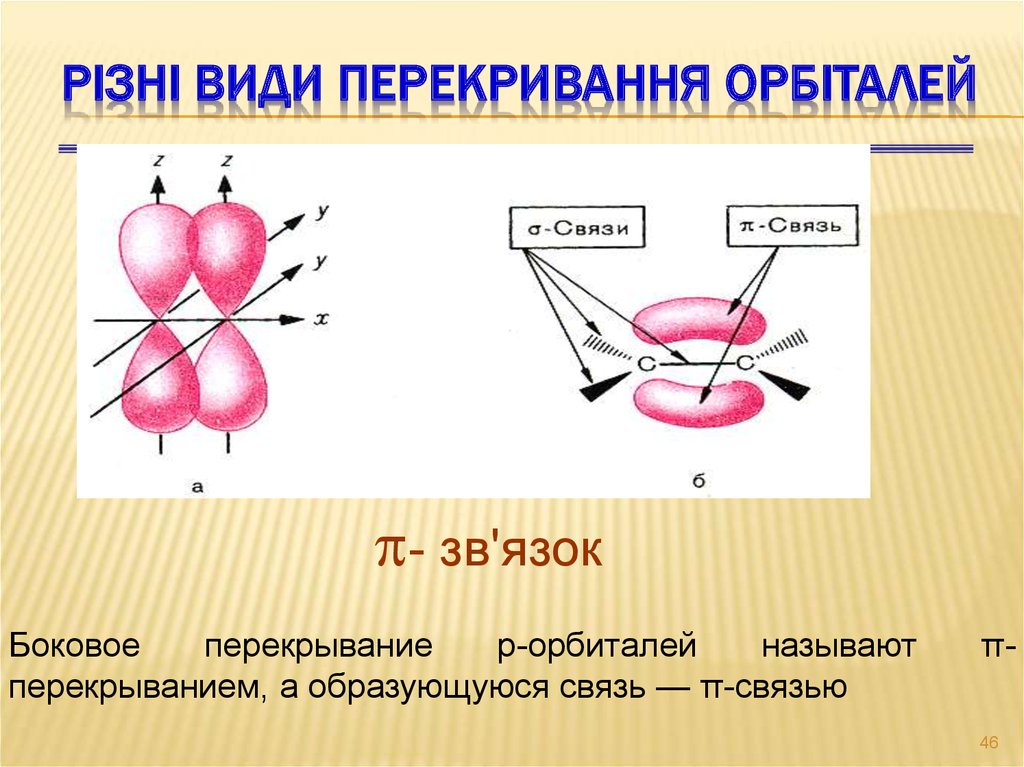
РІЗНІ ВИДИ ПЕРЕКРИВАННЯ ОРБІТАЛЕЙ- зв'язок
Боковое
перекрывание
р-орбиталей
называют
перекрыванием, а образующуюся связь — π-связью
π46
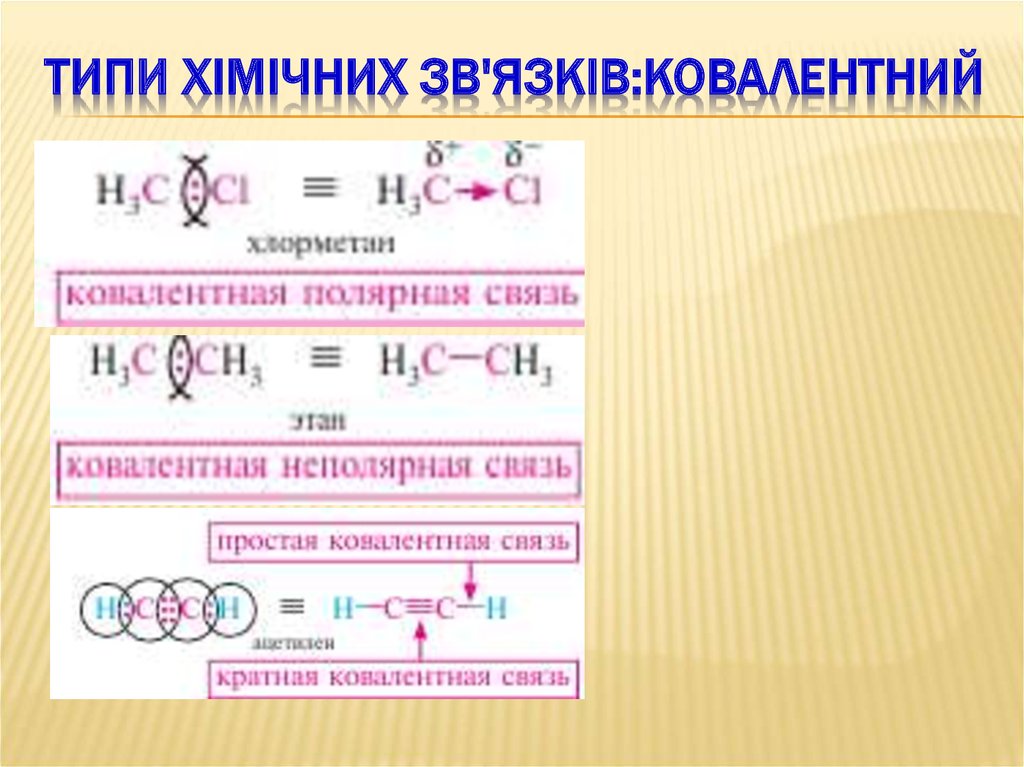
47. Типи хімічних зв'язків:КОВАЛЕНТНИЙ
ТИПИ ХІМІЧНИХ ЗВ'ЯЗКІВ:КОВАЛЕНТНИЙ48. Типи хімічних зв'язків: КОВАЛЕНТНИЙ
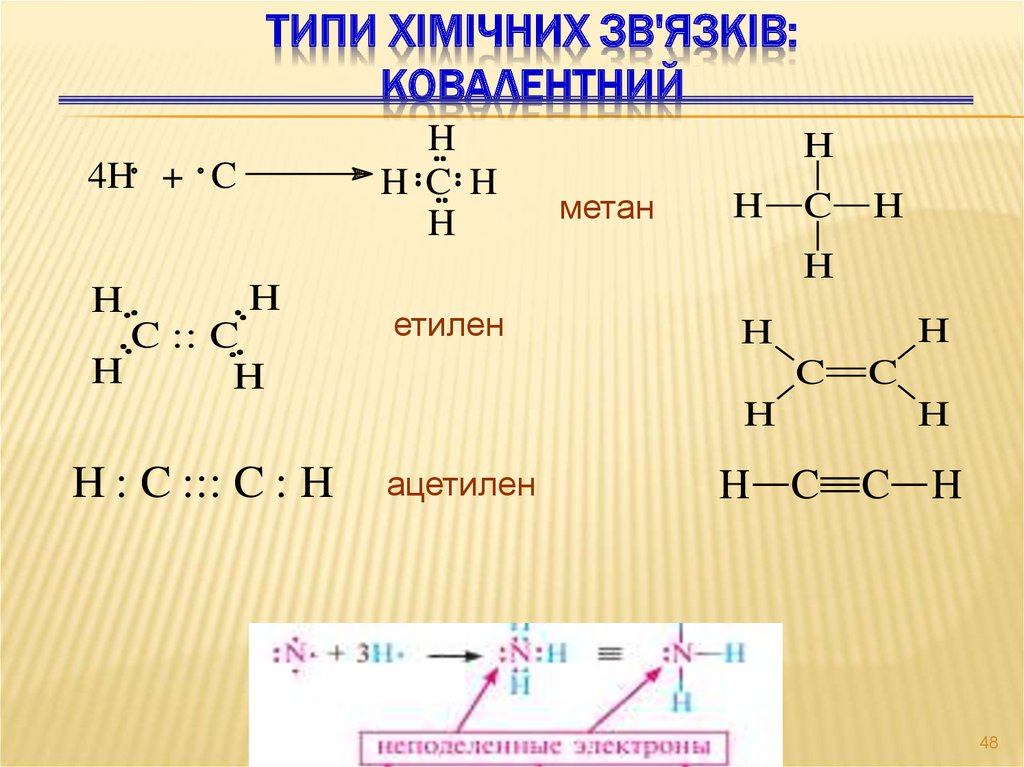
ТИПИ ХІМІЧНИХ ЗВ'ЯЗКІВ:КОВАЛЕНТНИЙ
H
H C H
H
4H + C
H
H
C :: C
H
H
H
метан
H
H
H
етилен
H
H
C
H
H : C ::: C : H
C
ацетилен
C
H
H C C H
48
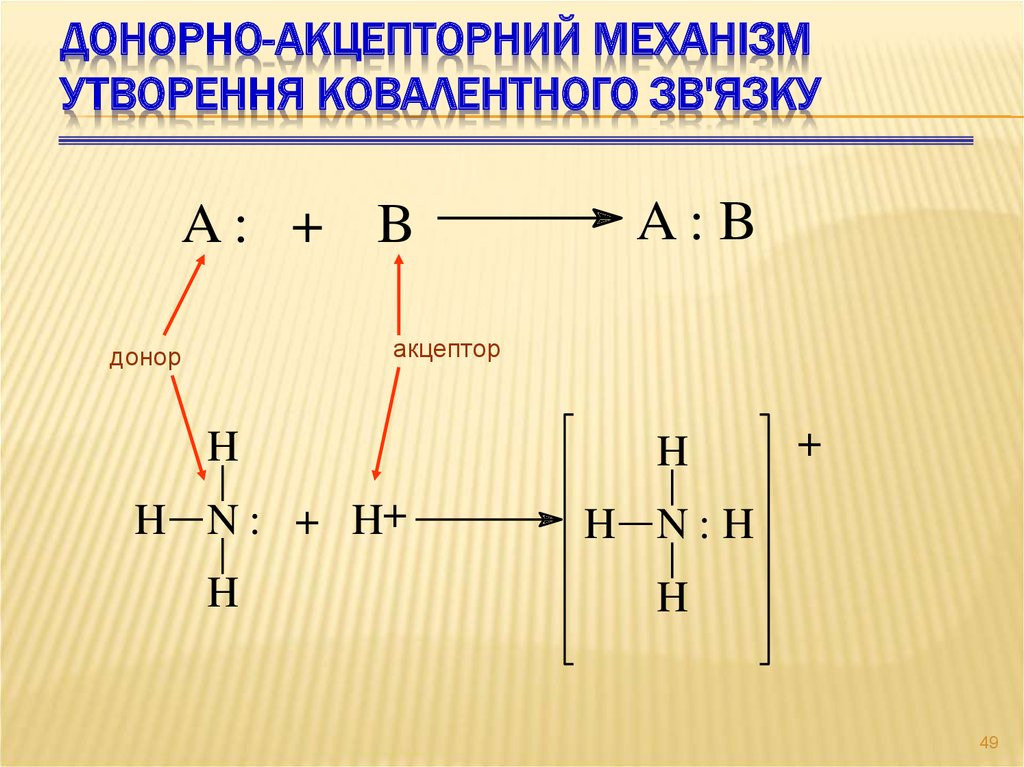
49. Донорно-акцепторний механізм утворення ковалентного зв'язку
ДОНОРНО-АКЦЕПТОРНИЙ МЕХАНІЗМУТВОРЕННЯ КОВАЛЕНТНОГО ЗВ'ЯЗКУ
A: + B
A: B
акцептор
донор
H
H N : + H+
H
H
+
H N:H
H
49
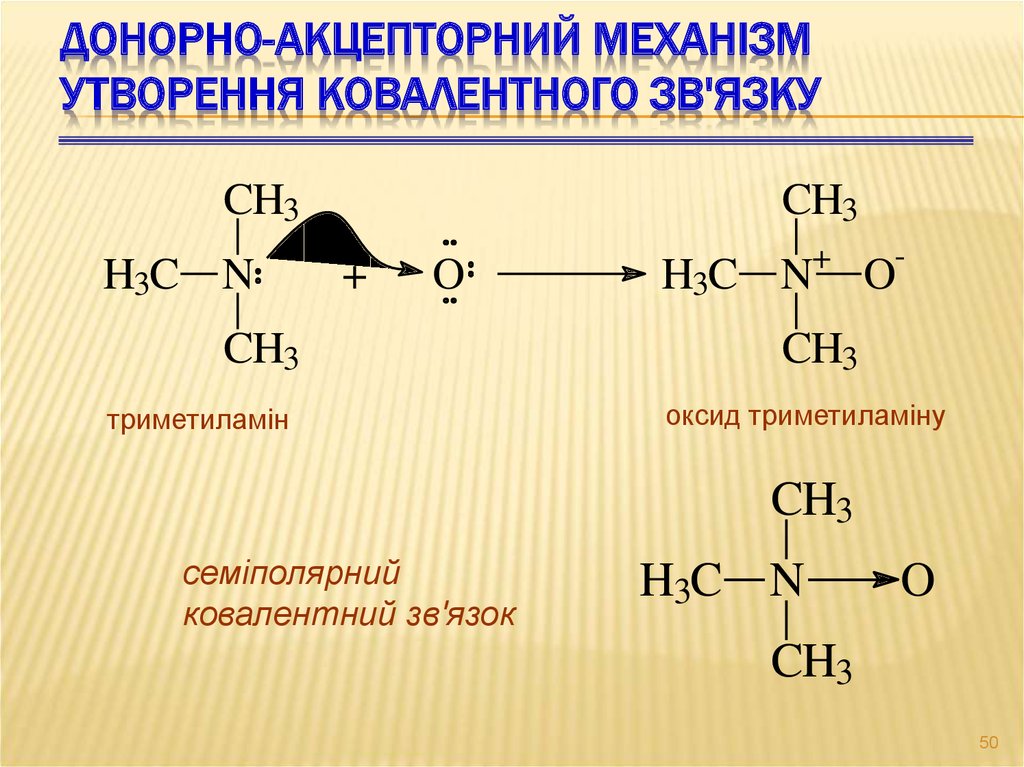
50. Донорно-акцепторний механізм утворення ковалентного зв'язку
ДОНОРНО-АКЦЕПТОРНИЙ МЕХАНІЗМУТВОРЕННЯ КОВАЛЕНТНОГО ЗВ'ЯЗКУ
CH3
H3C N
CH3
+
O
CH3
триметиламін
+
H3C N
-
O
CH3
оксид триметиламіну
CH3
семіполярний
ковалентний зв'язок
H3C N
O
CH3
50
51. Властивості ковалентного зв'язку
ВЛАСТИВОСТІ КОВАЛЕНТНОГО ЗВ'ЯЗКУКовалентний зв'язок характеризується
такими параметрами: насиченістю,
полярністю, поляризованістю,
довжиною, енергією і направленістю в
просторі (кутами між зв'язками).
51
52. Полярність
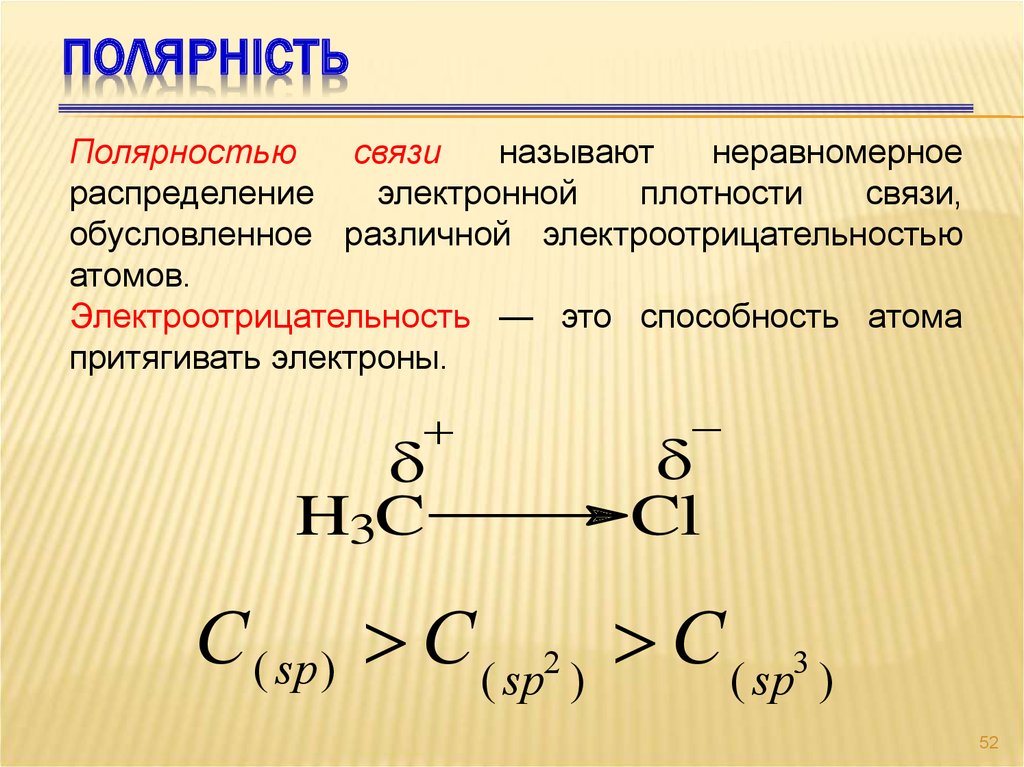
ПОЛЯРНІСТЬПолярностью
связи
называют
неравномерное
распределение
электронной
плотности
связи,
обусловленное различной электроотрицательностью
атомов.
Электроотрицательность — это способность атома
притягивать электроны.
H3C
Cl
С ( sp) C ( sp2 ) C ( sp3 )
52
53. Довжина зв҆язку і енергія
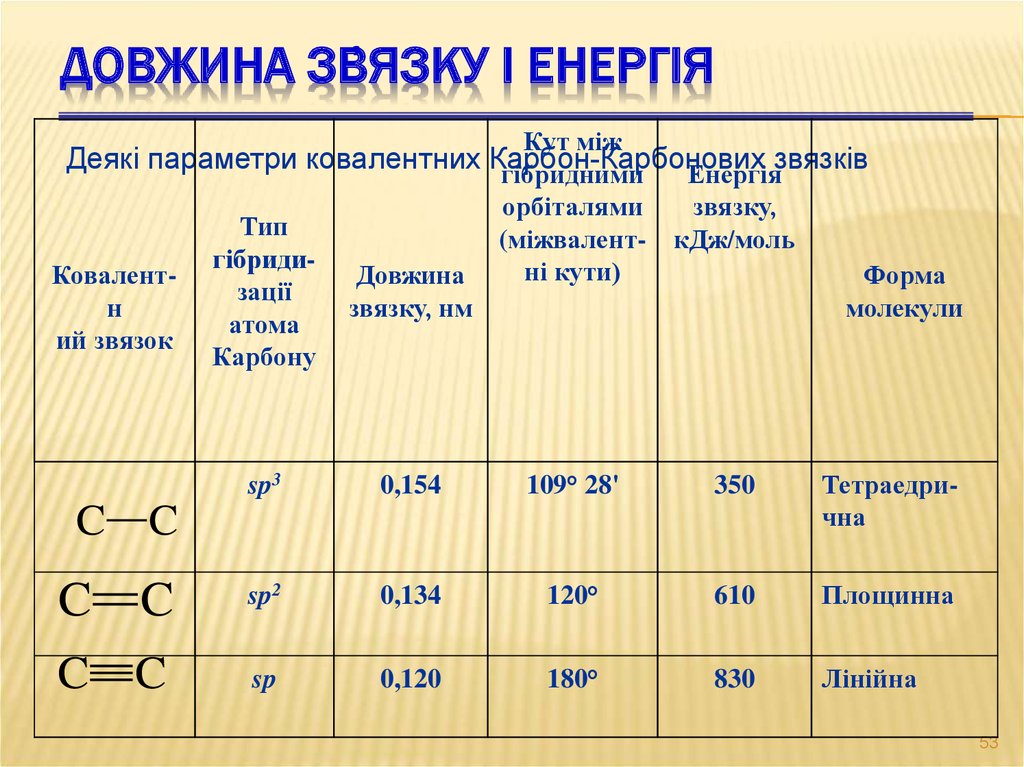
ДОВЖИНА ЗВ҆ЯЗКУ І ЕНЕРГІЯКут між
Деякі параметри ковалентних Карбон-Карбонових
звязків
гібридними
Енергія
орбіталями
звязку,
(міжвалент- кДж/моль
ні кути)
Тип
гібридизації
атома
Карбону
Довжина
звязку, нм
sp3
0,154
109° 28'
350
Тетраедрична
C C
sp2
0,134
120°
610
Площинна
C C
sp
0,120
180°
830
Лінійна
Ковалентн
ий звязок
C C
Форма
молекули
53
54. Направленість ковалентного зв'язку
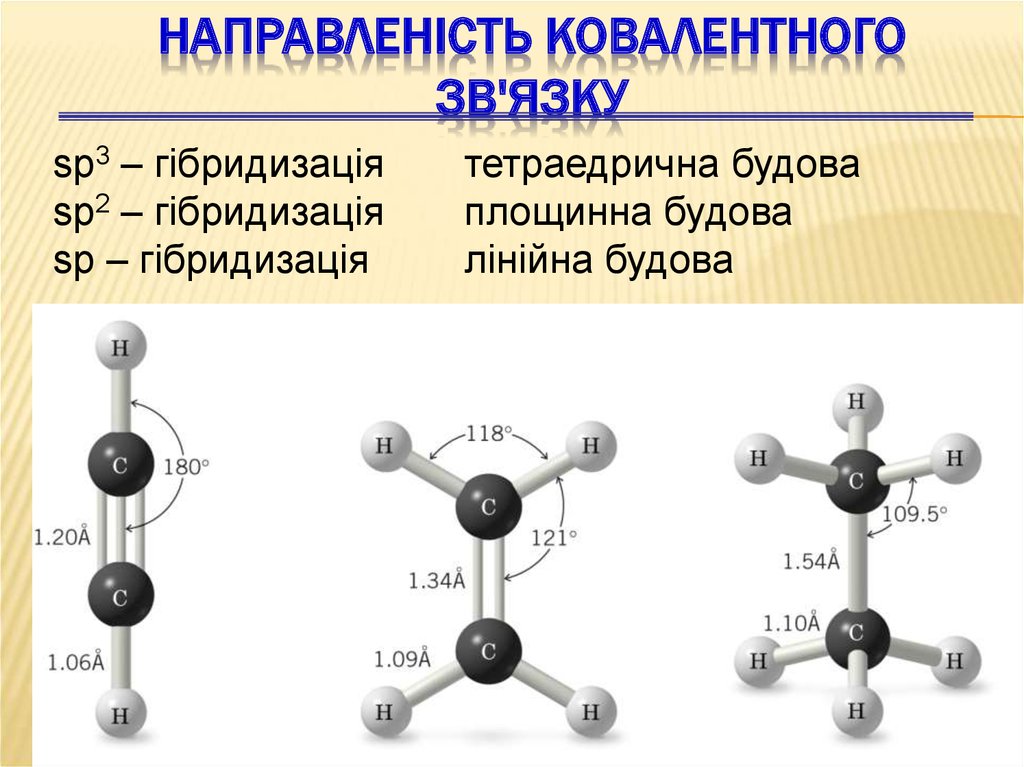
НАПРАВЛЕНІСТЬ КОВАЛЕНТНОГОЗВ'ЯЗКУ
sp3 – гібридизація
sp2 – гібридизація
sp – гібридизація
тетраедрична будова
площинна будова
лінійна будова
54
55. Типи хімічних зв'язків: Водневий зв'язок
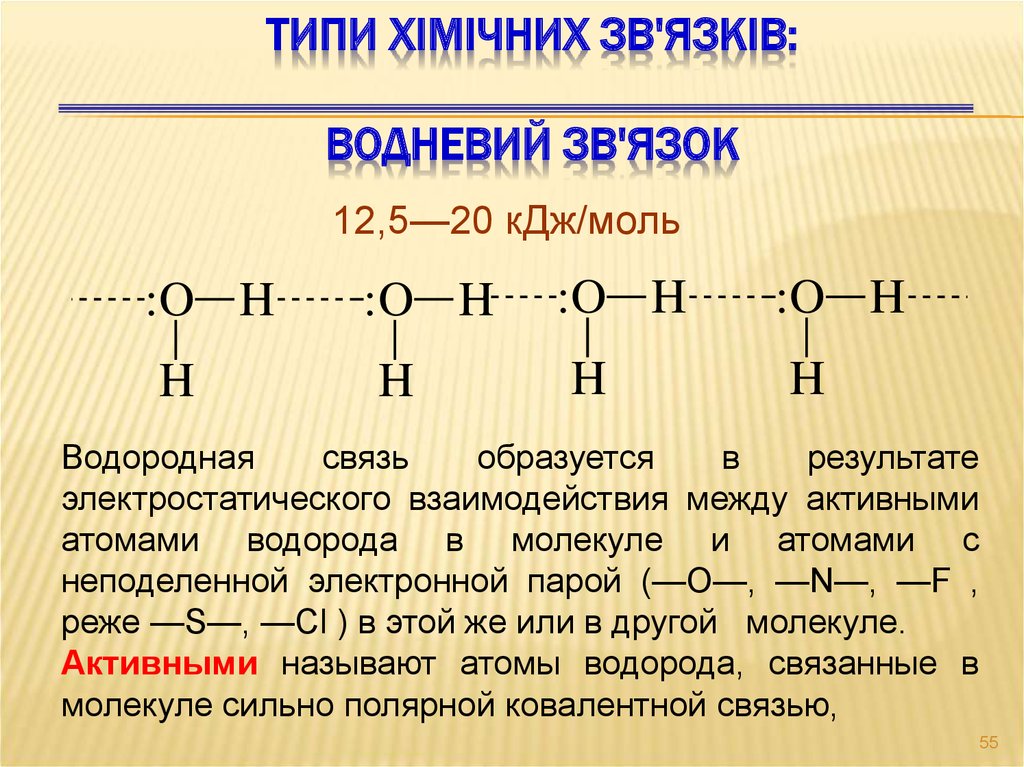
ТИПИ ХІМІЧНИХ ЗВ'ЯЗКІВ:ВОДНЕВИЙ ЗВ'ЯЗОК
12,5—20 кДж/моль
:O H
:O H
:O H
:O H
H
H
H
H
Водородная
связь
образуется
в
результате
электростатического взаимодействия между активными
атомами водорода в молекуле и атомами с
неподеленной электронной парой (—O—, —N—, —F ,
реже —S—, —Cl ) в этой же или в другой молекуле.
Активными называют атомы водорода, связанные в
молекуле сильно полярной ковалентной связью,
55
56.
Вчення про взаємний впливатомів у молекулі
В органических соединениях
различают
два
вида
электронных смещений:
смещение
электронной
плотности по цепи σ-связей —
индуктивный эффект;
смещение по системе π-связей
— мезомерный эффект.
Бутлеров Олександр Михайлович
1828–1886
57. Взаємний вплив атомів в молекулі
ВЗАЄМНИЙ ВПЛИВ АТОМІВ В МОЛЕКУЛІІндуктивний ефект
+
H3C Cl
CH3 H
метан
Зв'язок C–H
малополярний
хлорметан
+
H3C
-
OH
метанол
Зв'язок C–Cl полярний Зв'язок C–O полярний
Зміщення електронної густини по лінії зв'язків називається індуктивним ефектом і
позначається буквою I.
57
58. Взаємний вплив атомів в молекулі
ВЗАЄМНИЙ ВПЛИВ АТОМІВ В МОЛЕКУЛІІндуктивний ефект
Електроноакцепторні замісники – це атом або
група атомів, що зміщують електронну густину звязку від атома Карбону, проявляють негативний
індуктивний ефект (-I-ефект).
Електронодонорні замісники – це атом або група
атомів, що зміщують електронну густину -звязку
до атома Карбону, проявляють позитивний
індуктивний ефект (+I-ефект).
58
59. Взаємний вплив атомів в молекулі
ВЗАЄМНИЙ ВПЛИВ АТОМІВ В МОЛЕКУЛІІндуктивний ефект
1. Индуктивный эффект проявляется всегда при
наличии в молекуле атомов
с различной электроотрицательностью.
2. Индуктивный эффект распространяется только
через σ-связи и всегда
в одном направлении.
3. Индуктивный эффект затухает в цепи через 3—4 σсвязи.
59
60. Взаємний вплив атомів в молекулі
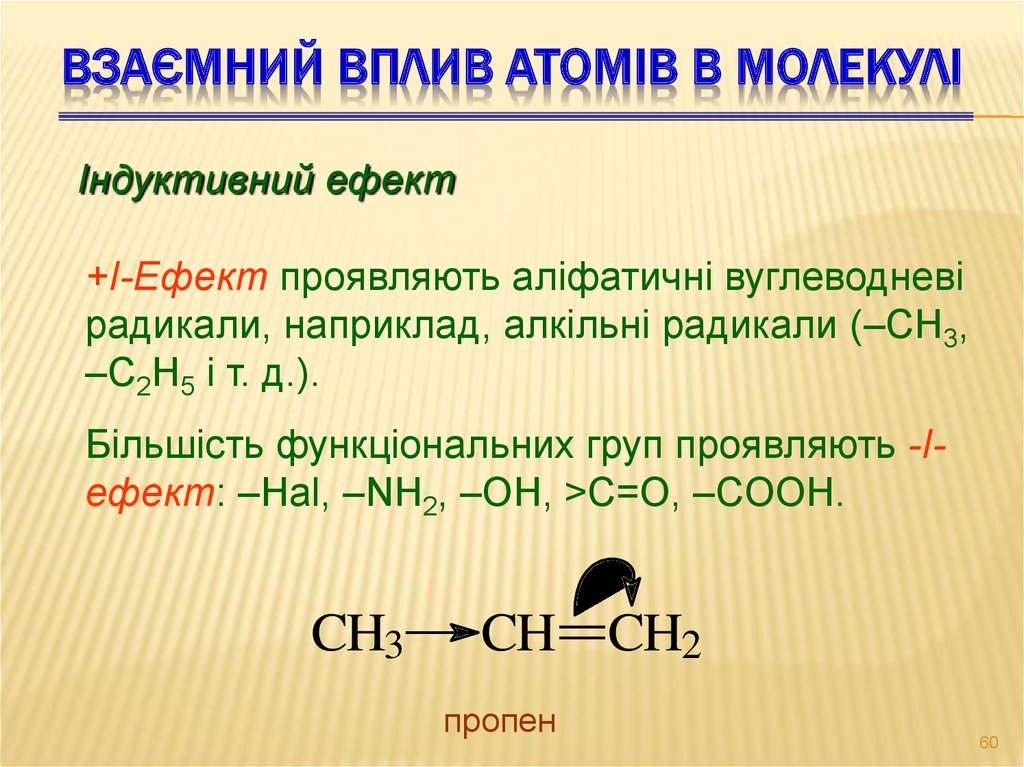
ВЗАЄМНИЙ ВПЛИВ АТОМІВ В МОЛЕКУЛІІндуктивний ефект
+I-Ефект проявляють аліфатичні вуглеводневі
радикали, наприклад, алкільні радикали (–CH3,
–C2H5 і т. д.).
Більшість функціональних груп проявляють -Iефект: –Hal, –NH2, –OH, >С=O, –COOH.
CH3
CH CH2
пропен
60
61.
Индуктивный эффект61
62. Взаємний вплив атомів в молекулі
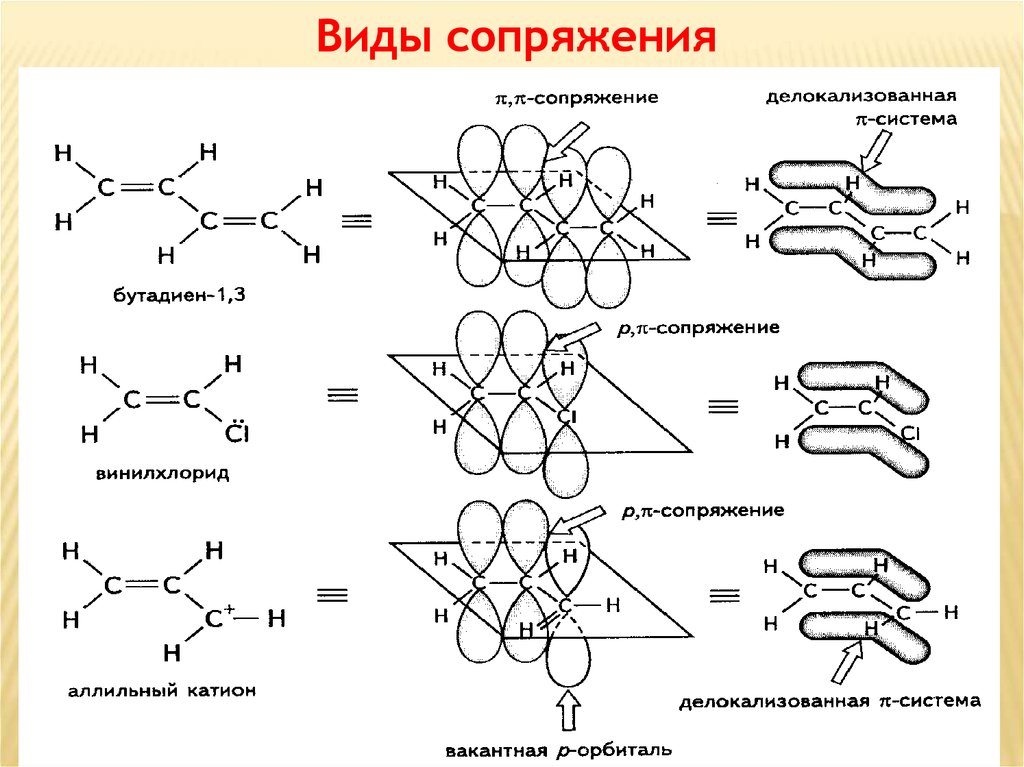
ВЗАЄМНИЙ ВПЛИВ АТОМІВ В МОЛЕКУЛІМезомерний ефект (ефект спряження)
Сопряженной
называют
систему,
состоящую
из
чередующихся простых и кратных связей, или же когда
рядом с углеродным атомом, образующим кратную связь,
находится атом, р-АО которого заполнена одним
электроном, двумя или вакантна.
Сопряжение связей обусловливает образование единого
делокализованного электронного облака.
Делокалізований зв'язок
O
CH3 C
O -
-
O
-
O
CH3 C
O
CH3 C
O
62
63.
Виды сопряжения63
64.
Замкнутые сопряженные системыМолекула бензена
65.
Мезомерный эффектПроцесс передачи электронного влияния заместителя по
сопряженной системе π-связей называют мезомерным
эффектом (М) или эффектом сопряжения (С).
66. Дякую за увагу!
ДЯКУЮ ЗА УВАГУ!67.
Кислотність і основністьорганічних сполук
Кислоти та основи по Бренстеду-Лоурі
Согласно теории Брёнстеда кислотой называют любое
вещество, способное отдавать протон (донор протона), а
основанием — вещество, способное присоединять протон
(акцептор протона).
А—Н + B
кислота
=
А–
основание cопряженное
основание
+
В+—Н
сопряженная кислота
67
68.
Кислотність і основність органічнихсполук
Кислотний центр
Центр протонування
68
69.
Кислотність і основність органічнихсполук
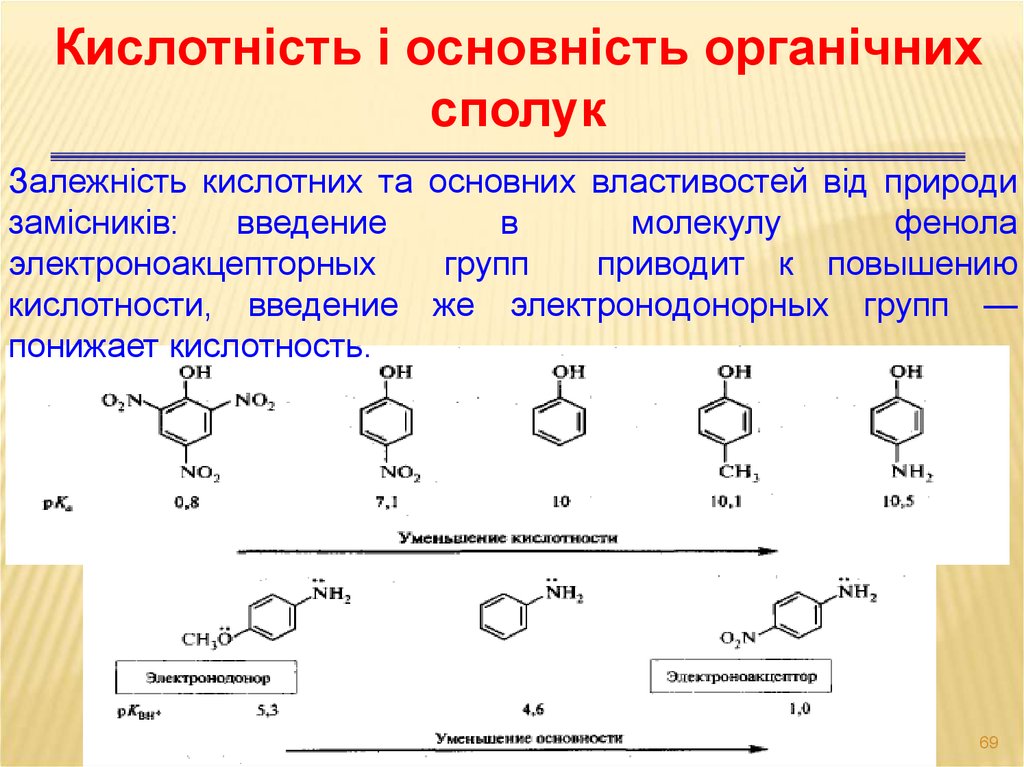
Залежність кислотних та основних властивостей від природи
замісників:
введение
в
молекулу
фенола
электроноакцепторных
групп
приводит к повышению
кислотности, введение же электронодонорных групп —
понижает кислотность.
69
70.
Кислотність і основність органічнихсполук
Типы органических кислот
он
- кислоты: карбоновые кислоты, спирты, фенолы, вода
и др.
Sн -кислоты: тиолы, тиоловые кислоты и др.
Nн -кислоты: амины, амиды кислот, имиды и др.
сн -кислоты: соединения, содержащие сильно полярные
С—Н-связи.
Сила кислотності:
-SH > -OH > -NH > -CH
70
71. Кислотність і основність органічних сполук
КИСЛОТНІСТЬ І ОСНОВНІСТЬ ОРГАНІЧНИХСПОЛУК
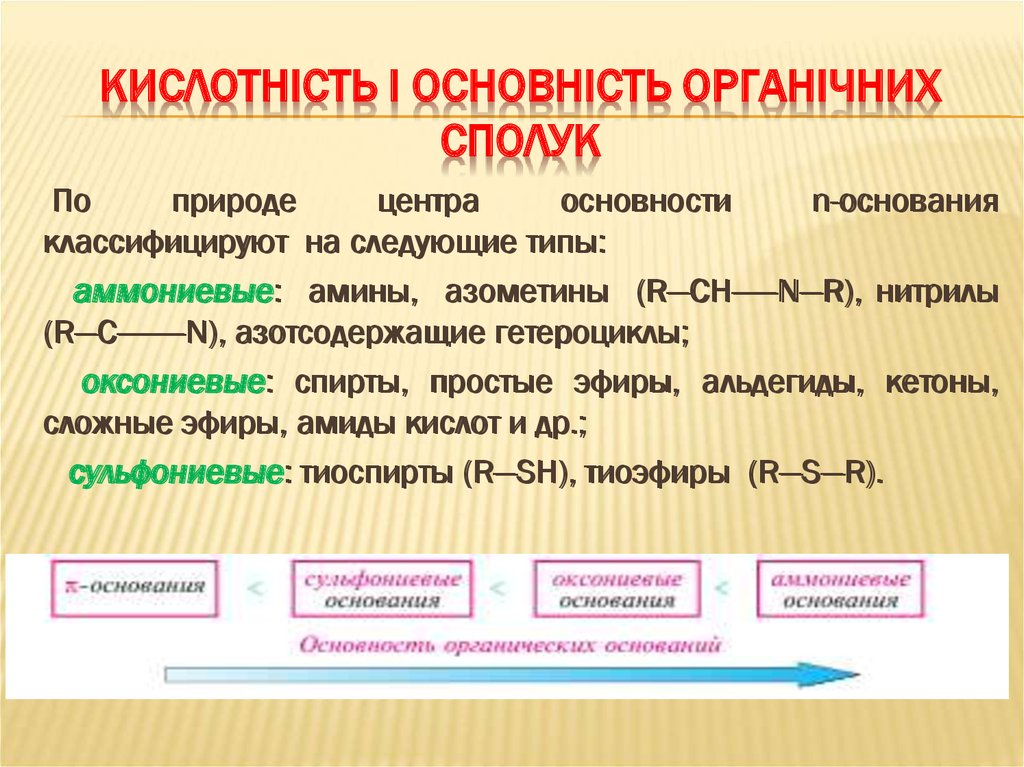
По
природе
центра
основности
n-основания
классифицируют на следующие типы:
аммониевые: амины, азометины (R—CH——N—R), нитрилы
(R—C———N), азотсодержащие гетероциклы;
оксониевые: спирты, простые эфиры, альдегиды, кетоны,
сложные эфиры, амиды кислот и др.;
сульфониевые: тиоспирты (R—SH), тиоэфиры (R—S—R).
72.
Кислотність і основність органічнихсполук
Кислоти та основи Льюїса
основание — любая частица (атом, молекула или
анион), способная отдавать электронную пару
для образования ковалентной связи, а кислота —
любая частица (атом, молекула, катион), способная
принимать пару электронов с образованием
ковалентной связи
72
73.
Основание по теории Льюиса является донором, акислота — акцептором пары электронов
74.
Кислотність і основність органічнихсполук
Легкость протекания кислотно-основной реакции определяется силой
кислоты и основания, а также жесткостью или мягкостью кислоты и
основания. Представление о жестких и мягких кислотах и основаниях
(ЖМКО), введено Р. Пирсоном
74
75.
Загальна характеристика реакційорганічних сполук
Реакції нуклеофільного заміщення
(S
)
N
Ізобутилйодид
Основна реакція:
Хлорацетамід
Основна реакція:
75
76.
Реакція нуклеофільного заміщення(SN)
Феноксиацетатна кислота
Основна реакція:
2,4-Динітрофенілгідразин
Основна реакція:
76
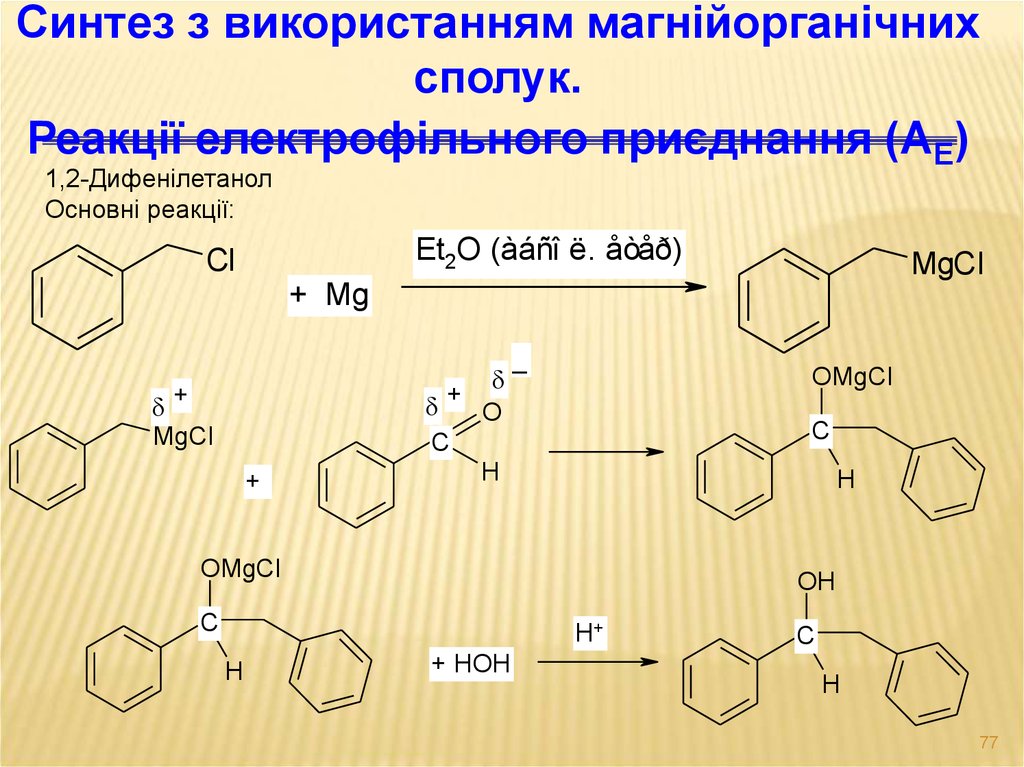
77.
Синтез з використанням магнійорганічнихсполук.
Реакції електрофільного приєднання (АЕ)
1,2-Дифенілетанол
Основні реакції:
Et2O (àáñî ë. åòåð)
Cl
MgCl
+ Mg
+
MgCl
+
+
O
C
H
_
OMgCl
C
H
OMgCl
OH
C
H+
H
+ HOH
C
H
77
78.
Реакції електрофільного приєднання(АЕ)
Дибром-пара-хлоркорична кислота
Основна реакція:
78
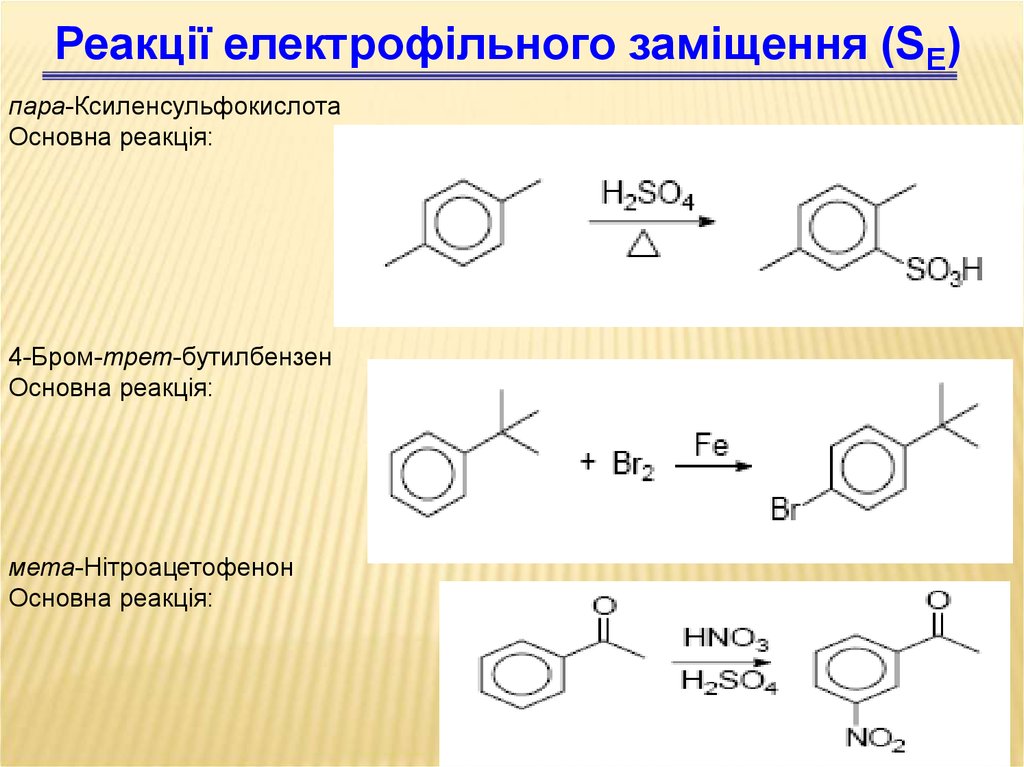
79.
Реакції електрофільного заміщення (SЕ)пара-Ксиленсульфокислота
Основна реакція:
4-Бром-трет-бутилбензен
Основна реакція:
мета-Нітроацетофенон
Основна реакція:
79
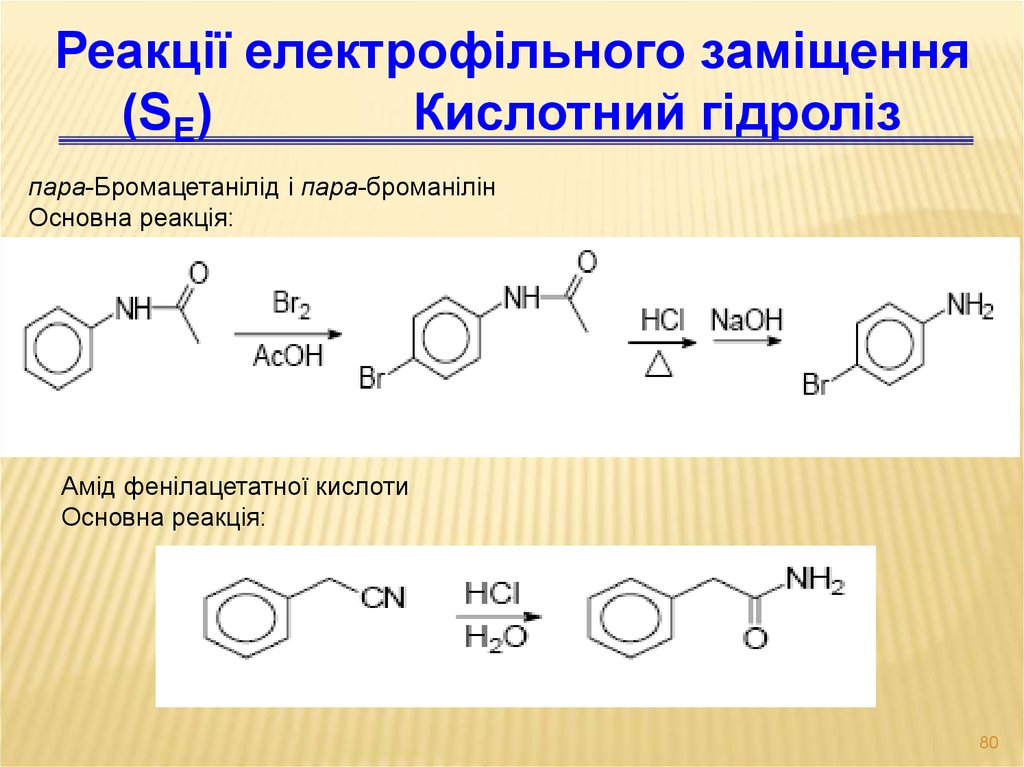
80.
Реакції електрофільного заміщення(SЕ)
Кислотний гідроліз
пара-Бромацетанілід і пара-броманілін
Основна реакція:
Амід фенілацетатної кислоти
Основна реакція:
80
81.
Реакції елімінування (відщеплення)(Е1 та Е2)
транс-Стільбен
Основна реакція:
81
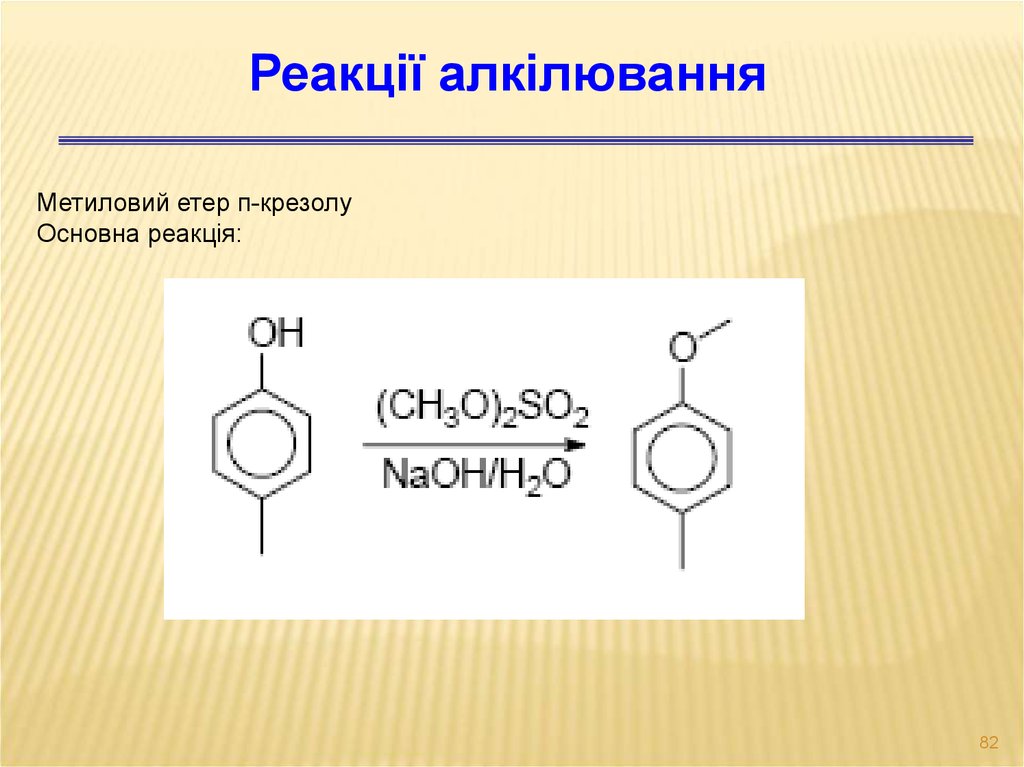
82.
Реакції алкілюванняМетиловий етер п-крезолу
Основна реакція:
82
83.
Реакції ацилюванняАцетилсаліцилова кислота
Основна реакція:
83
84.
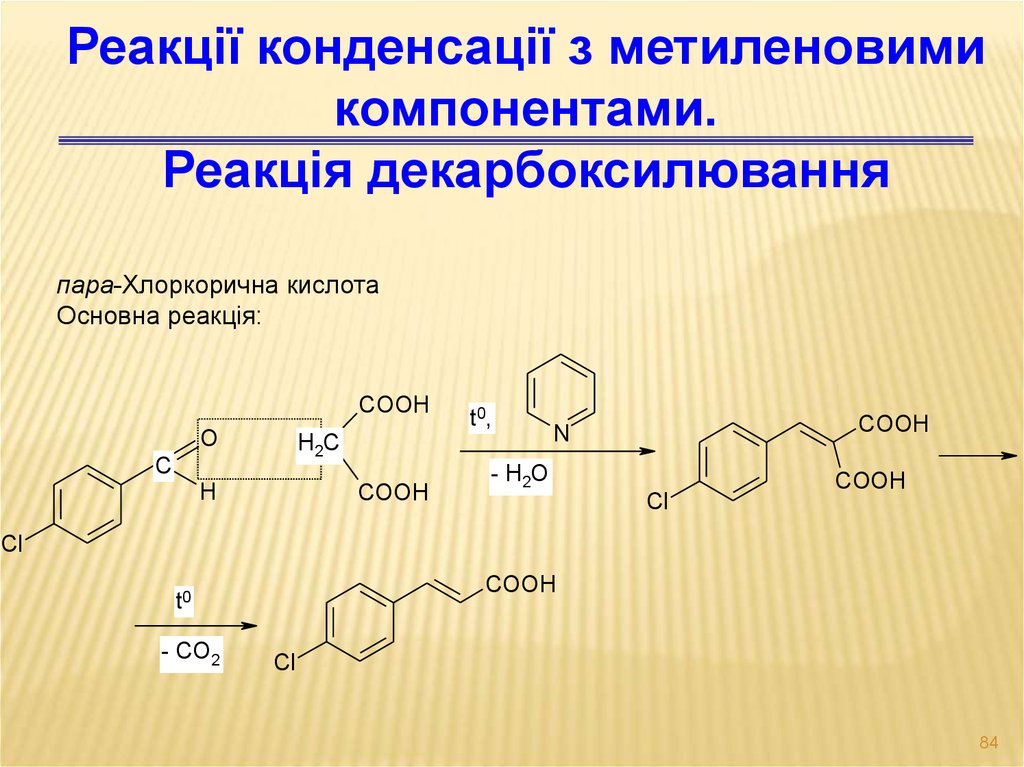
Реакції конденсації з метиленовимикомпонентами.
Реакція декарбоксилювання
пара-Хлоркорична кислота
Основна реакція:
COOH
O
t0,
H2C
C
H
COOH
COOH
N
- H2O
Cl
COOH
Cl
COOH
t0
- CO2
Cl
84
85.
Реакції приєднання-відщепленнякарбонільних сполук зі сполуками, що
містять фрагмент H2N-X
2,4-Динітрофенілгідразон циклогексанону
Основна реакція:
85
86.
Реакція діазотування.Реакція Зандмейєра
(з виділенням азогрупи)
COOH
NH2
NaNO2
COOH
HCl
+
N
KI
_
N Cl
COOH
- N2, - KCl
I
86
87.
Реакція діазотування. РеакціяМеєрвейна (з виділенням азогрупи)
COOH
NH2
NaNO2
COOH
HCl
+
N
O
+
_
CH2=CH
C
+ NaSCN
NH2
N Cl
COOH
+ N2 + NaCl
O
C CH
H2
NCS
C
NH2
87
88.
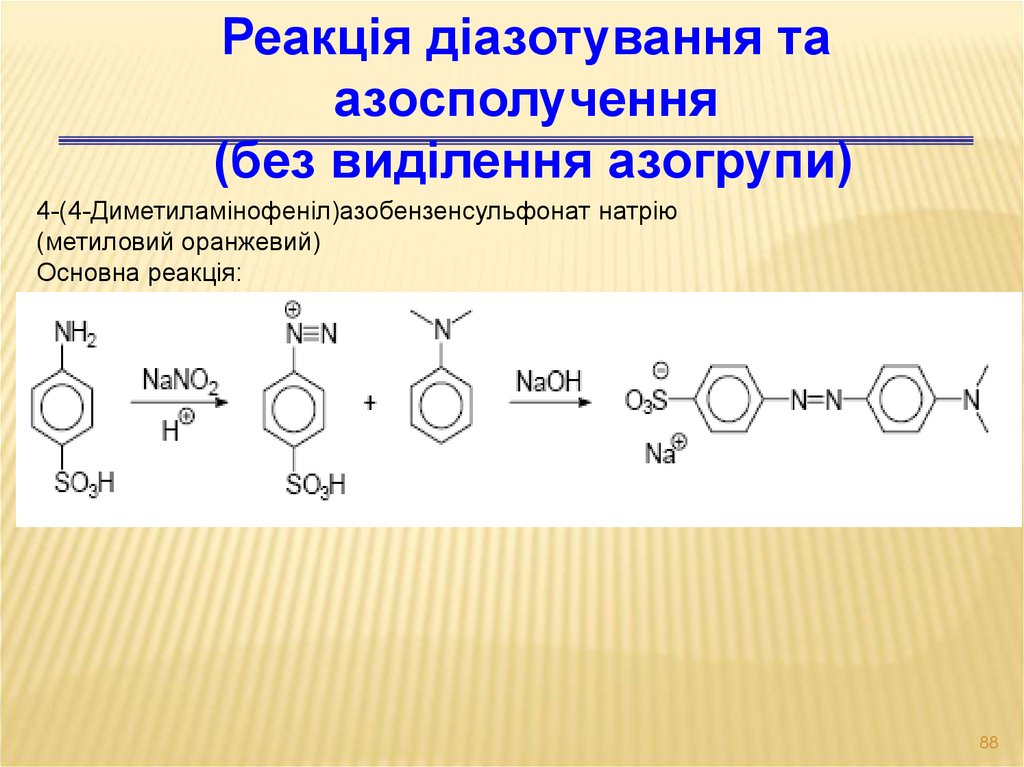
Реакція діазотування таазосполучення
(без виділення азогрупи)
4-(4-Диметиламінофеніл)азобензенсульфонат натрію
(метиловий оранжевий)
Основна реакція:
88
89.
Реакція відновлення та окиснення89
90.
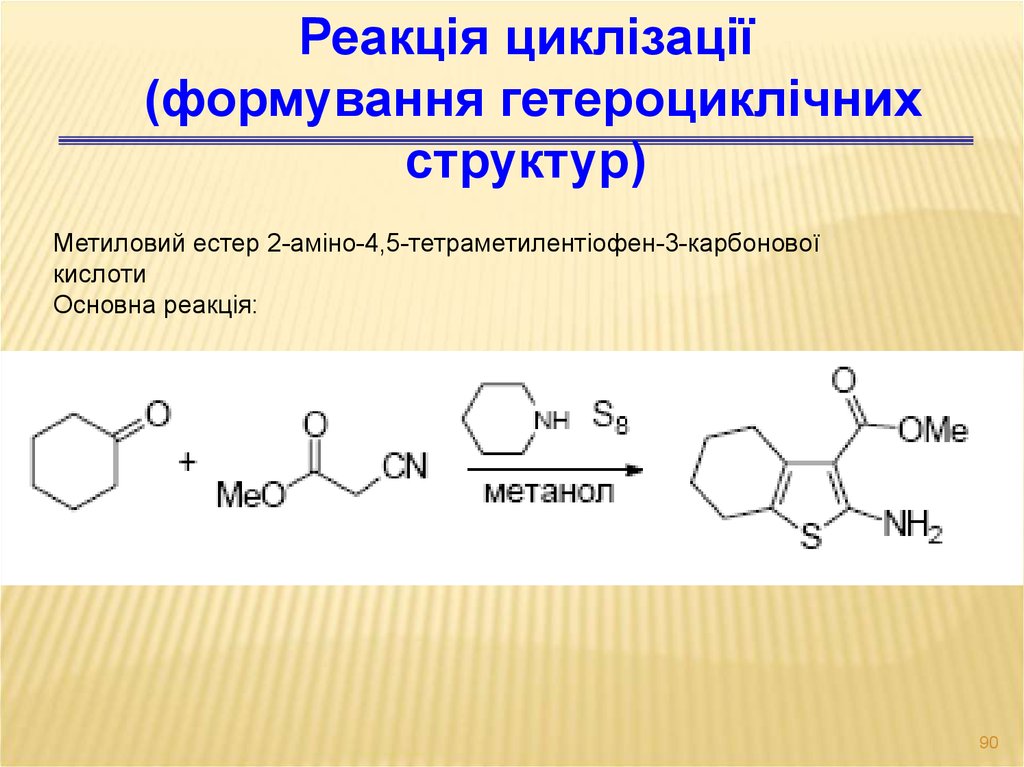
Реакція циклізації(формування гетероциклічних
структур)
Метиловий естер 2-аміно-4,5-тетраметилентіофен-3-карбонової
кислоти
Основна реакція:
90




















































 Химия
Химия








