Похожие презентации:
Коррозия металлов в природных и технологических средах
1.
КОРРОЗИЯ МЕТАЛЛОВ ВПРИРОДНЫХ
И ТЕХНОЛОГИЧЕСКИХ СРЕДАХ
2.
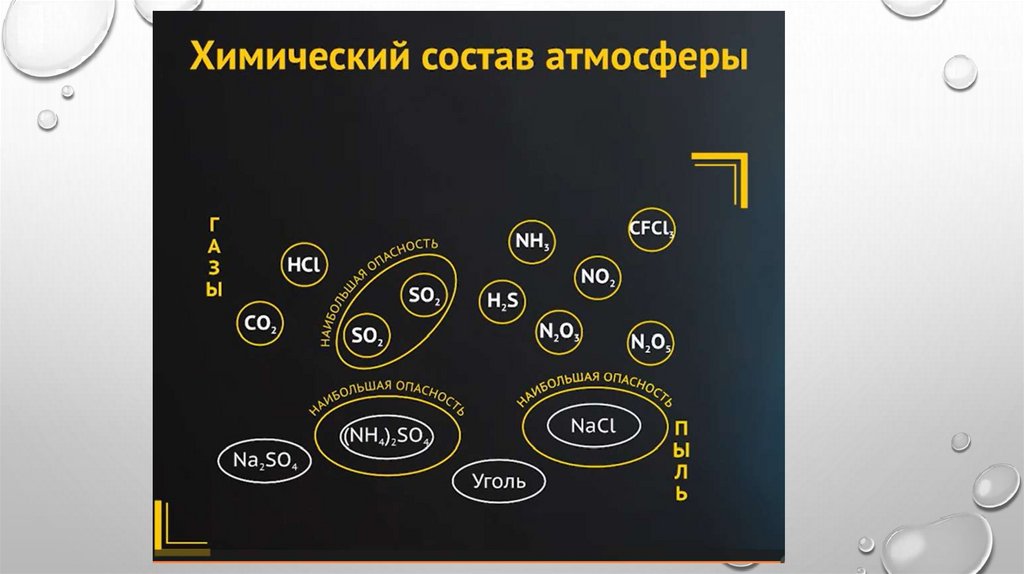
Коррозия металлов в природных средахАтмосферная коррозия металлов
Атмосферная коррозия — это коррозия сооружений и оборудования,
эксплуатирующихся в нормальной земной атмосфере.
СУХАЯ
ВЛАЖНАЯ
МОКРАЯ
3.
4.
5.
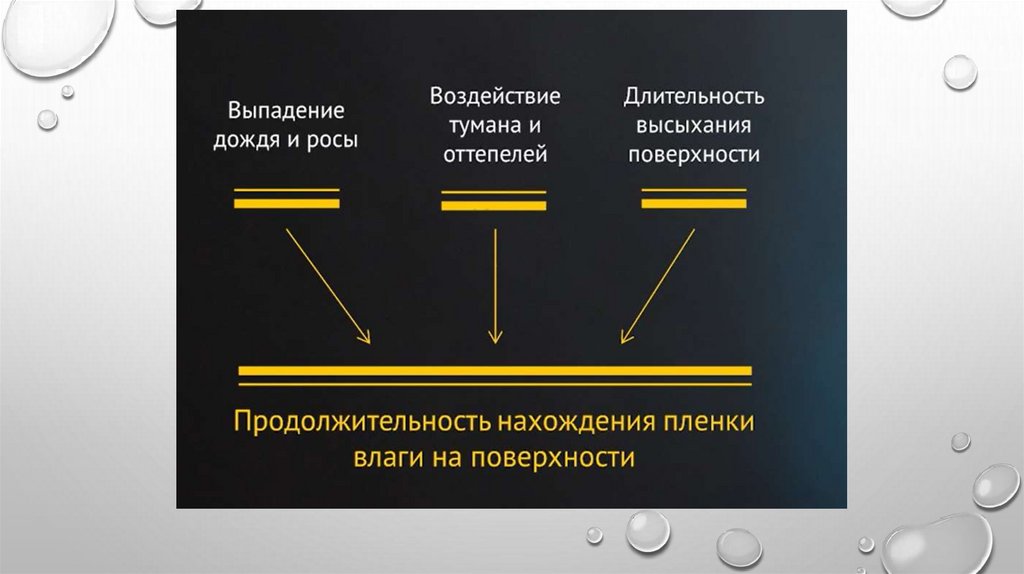
Основным стимулирующим фактором атмосферной коррозии являетсявода. При относительной влажности воздуха до 60 % следы
влаги на поверхности металла отсутствуют. В этом случае коррозия
протекает по химическому механизму.
Образующиеся на поверхности оксидные пленки обладают защитными
свойствами и тормозят развитие коррозионных разрушений .
6.
При относительной влажности воздуха, равной 60-70%, начинаетсяконденсация влаги и на поверхности металла появляется адсорбционная
пленка воды.
Относительная влажность, при которой начинается конденсация влаги на
поверхности металла, называется критической влажностью. Она зависит
от состояния металла и от степени загрязнения воздуха.
7.
При образовании адсорбционного слоя влаги(толщиной порядка нескольких молекулярных
слоев) на поверхности металла появляется
электролит.
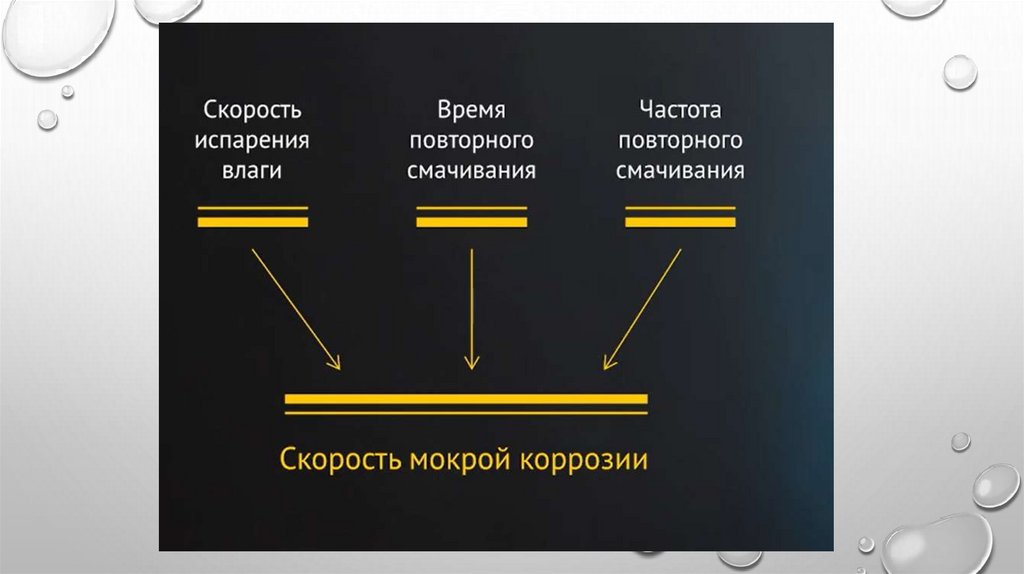
В этих условиях реализуется
электрохимический механизм и скорость
коррозии значительно возрастает.
Пленка влаги имеет небольшую толщину,
кислород проникает через нее
беспрепятственно и катодный процесс не
затруднен.
8.
Критическую влажностьснижают частицы
адсорбированных
загрязнителей,
притягивающих влагу из
воздуха (природные или
антропогенные)
Например сульфат
аммония (уменьшают
критическую влажность с
70 до 50%)или даже
продукты коррозии
9.
При относительной влажности,близкой к 100 %, или при
непосредственном увлажнении
металла (дождь, туман), на
поверхности происходит
образование видимых фазовых
слоев воды.
10.
Процесс коррозии несколькозатрудняется по сравнению с
влажной коррозией.
При образовании фазовых пленок
в области мокрой коррозии
затруднятся доставка кислорода и
наблюдается катодное
торможение процесса.
11.
12.
13.
14.
15.
16.
17.
• ДЛЯ ИЗОЛЯЦИИ МЕТАЛЛА ОТ ОКРУЖАЮЩЕЙ СРЕДЫ НАНЕГО НАНОСЯТ РАЗЛИЧНОГО РОДА ПОКРЫТИЯ: ЛАКИ,
КРАСКИ,
МЕТАЛЛИЧЕСКИЕ
ПОКРЫТИЯ.
НАИБОЛЕЕ
РАСПРОСТРАНЕННЫМИ
ЯВЛЯЮТСЯ
ЛАКОКРАСОЧНЫЕ
ПОКРЫТИЯ, ОДНАКО ИХ МЕХАНИЧЕСКИЕ СВОЙСТВА
ЗНАЧИТЕЛЬНО НИЖЕ, ЧЕМ У МЕТАЛЛИЧЕСКИХ.
• ПОСЛЕДНИЕ ПО ХАРАКТЕРУ ЗАЩИТНОГО ДЕЙСТВИЯ МОЖНО
РАЗДЕЛИТЬ НА АНОДНЫЕ И КАТОДНЫЕ
18.
Если металлическое покрытие изготовлено изметалла с более отрицательным потенциалом
(более активный) , чем защищаемый, то оно
называется анодным покрытием.
Пример анодного покрытия может служить –
хром, нанесенный на железо. В случае нарушения
целостности покрытия при контакте с влажным
воздухом будет работать гальванический элемент:
А (–) Cr H2O, O2 Fe (+) К
на аноде: Cr – 2e → Cr2+
на катоде: 2 H2O + O2 + 4e → 4 OH–
Cr2+ + 2 OH– → Cr(OH)2
Гидроксид хрома (II) окисляется кислородом
воздуха до Cr(OH)3:
4 Cr(OH)2 + 2H2O + O2 → 4 Cr(OH)3
Таким образом, в результате электрохимической
коррозии разрушается анодное покрытие.
19.
20.
Неметаллические покрытия.Такие
покрытия
могут
быть
неорганические
(цементный
раствор,
стекловидная
масса)
и
органические
(высокомолекулярные
соединения,
лаки, краски, битум).
Химические покрытия.
В этом случае защищаемый металл подвергают
химической обработке с целью образования на
поверхности пленки его соединения, устойчивой к
коррозии. Сюда относятся:
оксидирование – получение устойчивых оксидных
пленок (Al2O3, ZnO и др.);
фосфатирование – получение защитной пленки
фосфатов (Fe3(PO4)2, Mn3(PO4)2);
21.
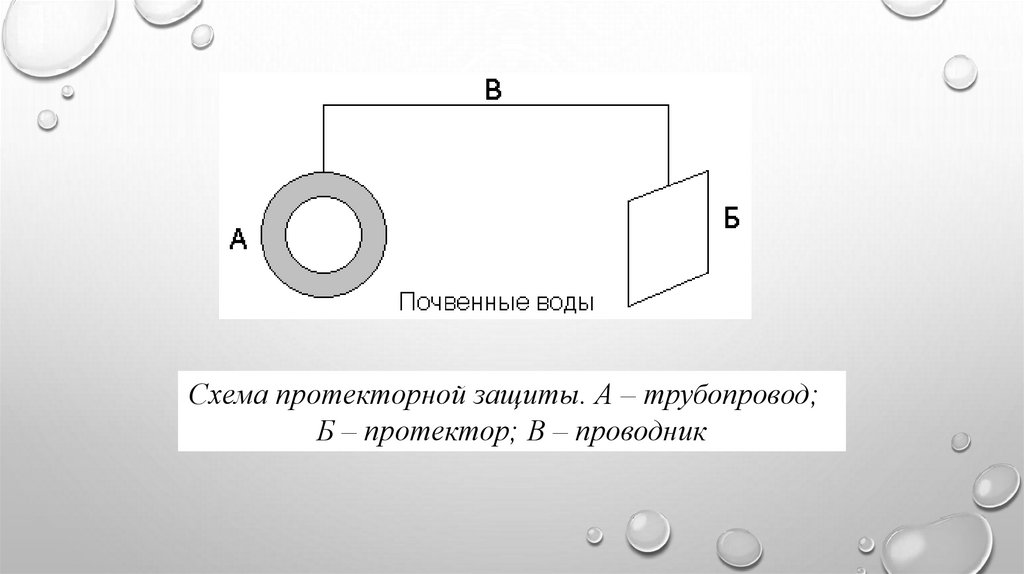
Протекторная защита. Защищаемое откоррозии изделие соединяют с металлическим
ломом
из
более
электроотрицательного
металла (протектора).
Это равносильно созданию гальванического
элемента, в котором протектор является анодом
и будет разрушаться.
Например, для защиты подземных сооружений
(трубопроводов) на некотором расстоянии от
них закапывают металлолом (протектор),
присоединив его к сооружению
22.
Схема протекторной защиты. А – трубопровод;Б – протектор; В – проводник
23.
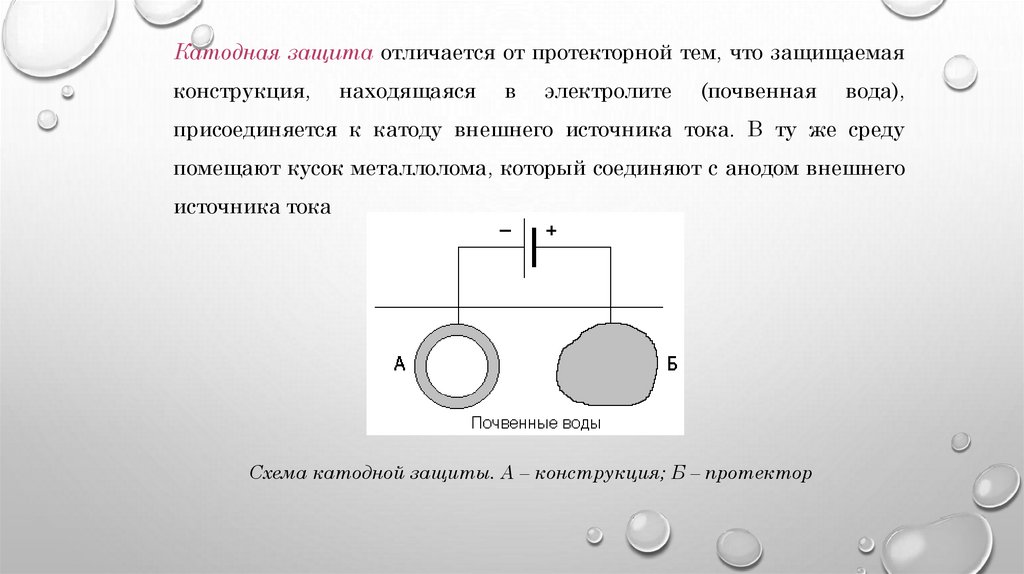
Катодная защита отличается от протекторной тем, что защищаемаяконструкция,
находящаяся
в
электролите
(почвенная
вода),
присоединяется к катоду внешнего источника тока. В ту же среду
помещают кусок металлолома, который соединяют с анодом внешнего
источника тока
Схема катодной защиты. А – конструкция; Б – протектор
24.
25.
26.
Ингибиторы коррозии- химические соединенияили их композиции , присутствие которых в
небольшом количестве в агрессивной среде
замедляет
коррозию
металлов,
например
неорганические:NaNO3, K2CrO4, органические :
уротропин, диэтиламин они адсорбируются на
поверхности металлов, образуя тонкие пленки.
Летучие
(атмосферные ингибиторы) (серии
ИФХАН);
Ингибиторы
применяются при химической
очистке от накипи паровых котлов, снятиии
окалины с обработанных изделий, при хранении
и перевозке соляной кислоты в стальной таре.
27.
В качестве ингибиторов коррозии используют как органические, так инеорганические вещества различного химического состава.
Различные ингибиторы действуют разными способами:
• либо, адсорбируясь на поверхности металла, влияют на электродные
процессы локальных микроэлементов, тормозя их дальнейшее
действие;
• либо же, вследствие своего окисляющего действия, образуют на
поверхности металла плотную, хорошо защищающую его оксидную
пленку
Принцип действия значительного числа ингибиторов
заключается в адсорбции ингибитора на корродирующей
поверхности и последующем торможении катодных или анодных
процессов электрохимической коррозии.
28.
Летучиеингибиторы
атмосферной
коррозии
самопроизвольно
адсорбируются
на
поверхности изделия, находятся при нормальной
температуре в летучем состоянии. Воздействуют на
кинетику электродных реакций.
• К ним относятся соли слабых неорганических и
органических кислот, аминов (бензоаты, нитриты,
фосфаты, нитрофеноляты, нитробензоаты и др.)
• Летучие
ингибиторы
атмосферной
коррозии
адсорбируются на поверхности защищаемого
металла
тонким
мономолекулярным
слоем,
происходит его взаимодействие с металлом.
29.
Анодные ингибиторы чаще всего используют в нейтральных средахпри коррозии с кислородной деполяризацией.
К таким ингибиторам относятся неорганические вещества-окислители:
хроматы, бихроматы, нитриты, молибдаты, вольфраматы щелочных
металлов
Ингибирующее действие фосфатов, полифосфатов, боратов,
силикатов, солей бензойной кислоты проявляется только при
наличии в электролите растворенного кислорода, который и играет
роль пассиватора.
Эти вещества способствуют адсорбции кислорода на поверхности
металла,переводя его в пассивное состояние. Помимо этого, они
тормозят анодный процесс растворения металла за счет
образования труднорастворимых защитных пленок самого
разнообразного характера.
30.
• В зависимости от класса ингибирующегосоединения
оно может ускорять катодную
реакцию (переводит поверхность металла в
пассивное состояние), либо тормозить анодную и
катодную.
• Действие ингибитора зависит от его строения и
состава,
механизма
испарения,
давления
насыщенного пара, адсорбционных свойств
поверхности, самого ингибитора, способности
изменять кинетику процесса.
• Для защиты металлов от атмосферной коррозии
во время перевозки, хранения и консервации
очень
часто
используют
ингибированную
антикоррозионную бумагу. При производстве
ингибированной бумаги, основным ее активным
элементом является ингибирующее вещество.
31.
Антикоррозионные смазкиВ
качестве
таких
смазок
используются
нефтяные
масла,
вазелин,
воск.
Нефтяные
смазки
относительно
дешевы,
не
взаимодействуют с защищаемым металлом, достаточно стабильны при
хранении и применении, их легко наносить, удалять, возобновлять.
Применение
таких
смазок
не
требует
тщательной
подготовки
поверхности
защищаемого
изделия
Слой смазки, нанесенный на металлическую поверхность, препятствует
проникновению воды и кислорода воздуха к металлу и тем самым
затрудняет протекание коррозионных процессов.
Консистентные смазки наносят только на сухую поверхность. Для усиления
защитных свойств смазок в них дополнительно вводят ингибиторы коррозии.
Консистентные ингибированные смазки применяют для консервации
наружных поверхностей машин, станков и механизмов.
Наряду с маслами в качестве защитных смазок используется воск


























 Химия
Химия








