Похожие презентации:
Физико-химические основы перегонки. Законы Коновалова. Перегонка с водяным паром
1.
Физико-химические основы перегонки.Законы Коновалова. Перегонка с водяным
паром
1
2.
Первый закон Коновалова: пар по сравнению с жидкостью,находящейся с ней в равновесии, богаче тем компонентом,
добавление которого к жидкости повышает общее давление пара (или
понижает температуру кипения раствора при заданном давлении).
Уравнение математически выражает первый закон Коновалова.
Если РА°>РВ°, то
и, следовательно, парообразная фаза в этом случае обогащена более
летучим компонентом А.
Можно дать более простую формулировку первого закона
Коновалова: парообразная фаза по сравнению с жидкой обогащена
более летучим компонентом, то есть компонентом, температура кипения
которого ниже.
2
3.
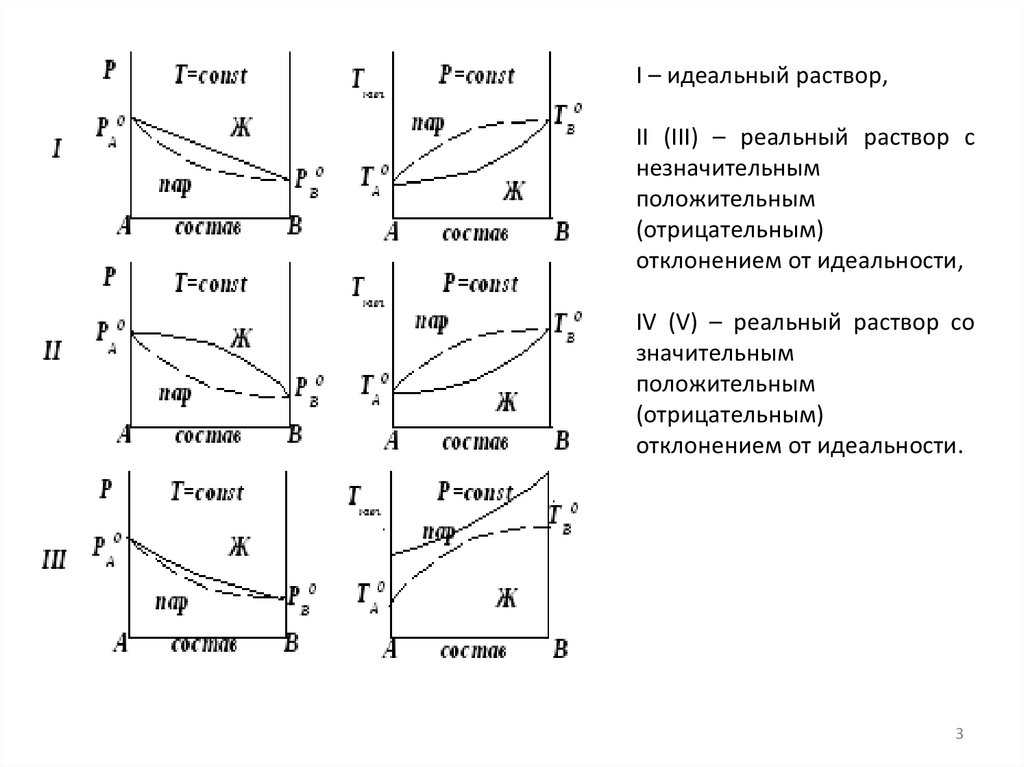
I – идеальный раствор,II (III) – реальный раствор с
незначительным
положительным
(отрицательным)
отклонением от идеальности,
IV (V) – реальный раствор со
значительным
положительным
(отрицательным)
отклонением от идеальности.
3
4.
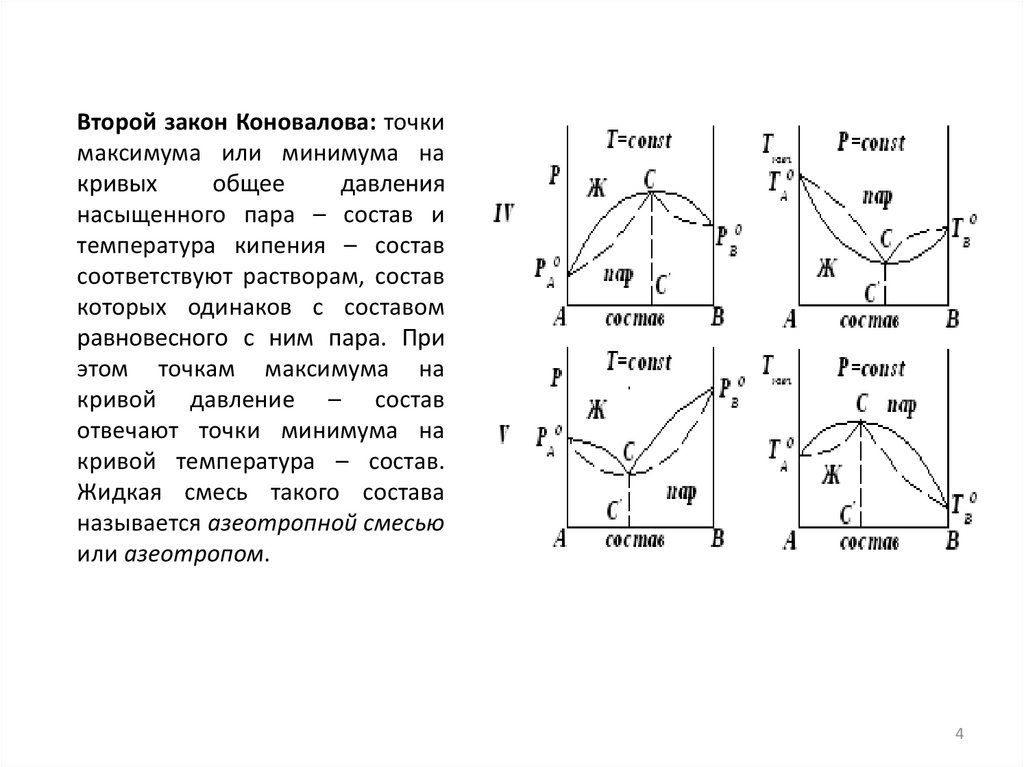
Второй закон Коновалова: точкимаксимума или минимума на
кривых
общее
давления
насыщенного пара – состав и
температура кипения – состав
соответствуют растворам, состав
которых одинаков с составом
равновесного с ним пара. При
этом точкам максимума на
кривой давление – состав
отвечают точки минимума на
кривой температура – состав.
Жидкая смесь такого состава
называется азеотропной смесью
или азеотропом.
4
5.
Первый закон Вревского имеет следующую формулировку: приповышении температуры раствора его насыщенный пар обогащается тем
компонентом, у которого парциальная мольная теплота испарения Qiuсп
больше.
Второй закон Вревского характеризует влияние внешних условий на
состав двойных азеотропных растворов. Смещение азеотропного состава
определяется следующим правилом: в смеси с минимумом температуры
кипения (максимумом давления пара) при повышении температуры
возрастает относительное содержание компонента с большей
парциальной мольной теплотой испарения, в противоположном случае —
наоборот.
Третий закон Вревского также описывает влияние температуры и
давления на состав пара в азеотропных системах и по существу является
следствием двух предыдущих законов. Содержание третьего закона
формулируется следующим образом: при изменении температуры
(давления) в системе с максимумом на кривой упругости пара Р(х) состав
пара и состав азеотропной смеси смещаются в одном направлении, в
системе с минимумом давления — в противоположных направлениях.
5
6.
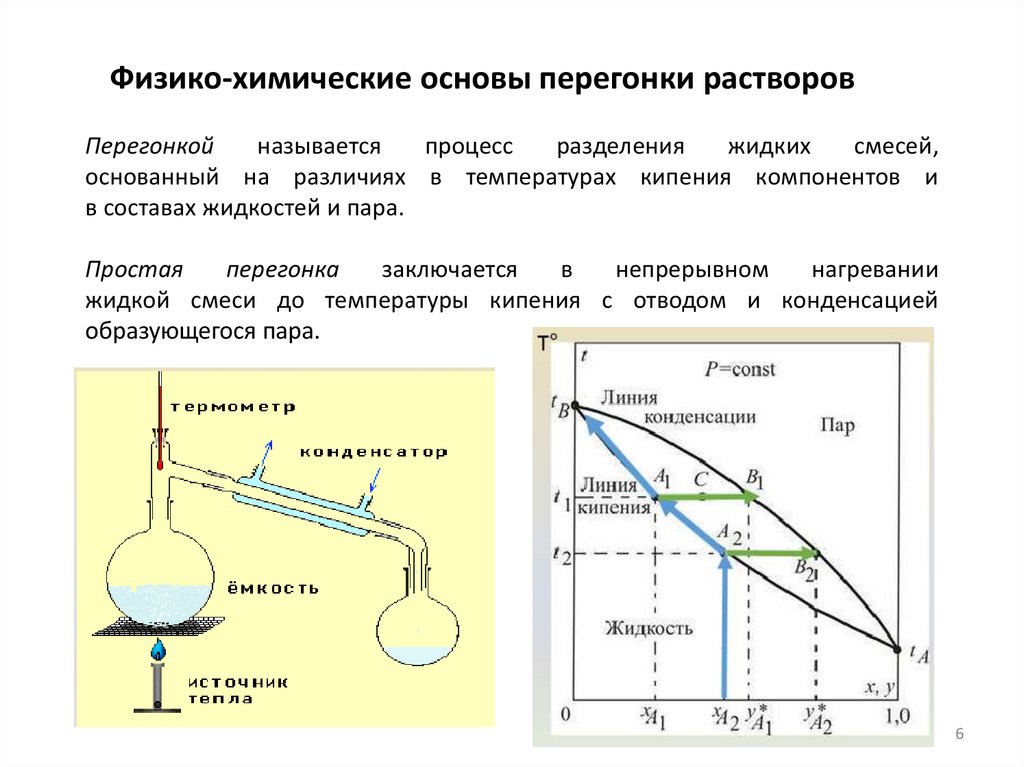
Физико-химические основы перегонки растворовПерегонкой
называется
процесс
разделения
жидких
смесей,
основанный на различиях в температурах кипения компонентов и
в составах жидкостей и пара.
Простая
перегонка
заключается
в
непрерывном
нагревании
жидкой смеси до температуры кипения с отводом и конденсацией
образующегося пара.
6
7.
Более эффективным методом разделения веществ является фракционнаяперегонка, которая состоит в многократном повторении процессов
испарения и конденсации.
При этом соблюдается следующая последовательность операций:
нагревание исходной жидкой смеси до кипения для получения
некоторого количества пара определённого состава;
конденсация полученного пара;
испарение конденсата для получения пара нового состава.
7
8.
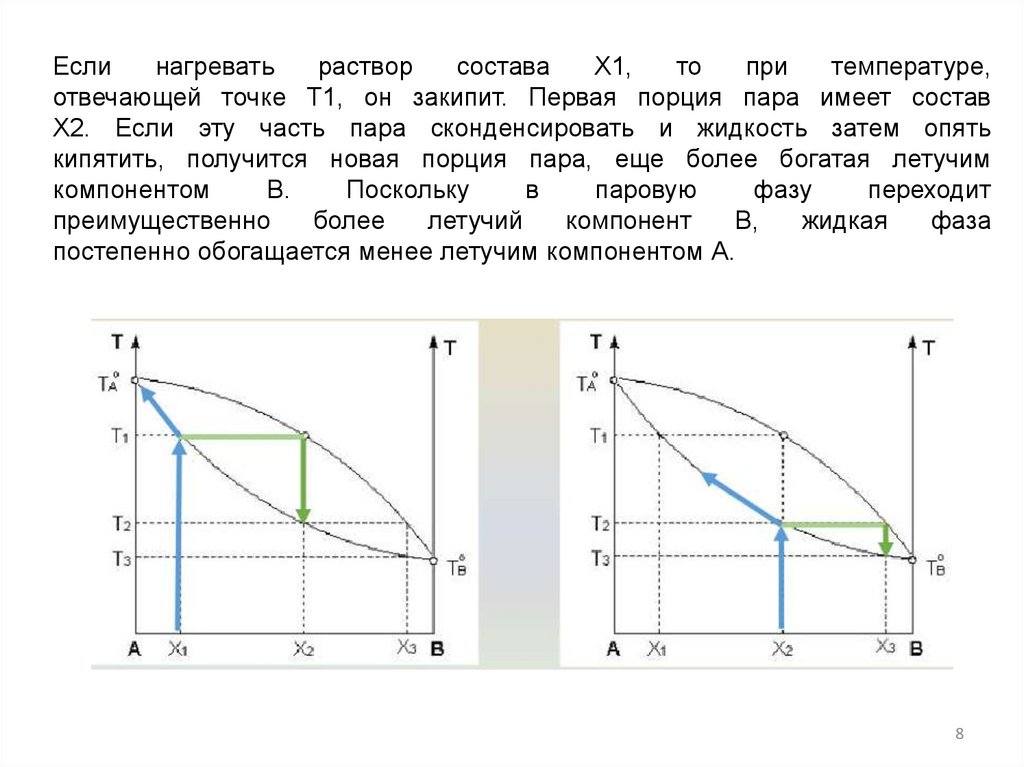
Еслинагревать
раствор
состава
X1,
то
при
температуре,
отвечающей точке T1, он закипит. Первая порция пара имеет состав
X2. Если эту часть пара сконденсировать и жидкость затем опять
кипятить, получится новая порция пара, еще более богатая летучим
компонентом
В.
Поскольку
в
паровую
фазу
переходит
преимущественно
более
летучий
компонент
В,
жидкая
фаза
постепенно обогащается менее летучим компонентом А.
8
9.
Продолжая многократно процессы испарения и конденсации, можнодостигнуть того, что пар будет представлять собой практически чистый
компонент В, а жидкость – чистый компонент А. В промышленности и в
лабораторной практике обычно используется процесс, в котором
многократные стадии испарения и конденсации совмещены в одном
аппарате, называемом ректификационной колонной.
Этот процесс разделения жидких смесей называется ректификацией.
В процессе ректификации жидкий раствор, стекающий вниз по тарелкам
ректификационной колонны, встречается с паром, поднимающимся
вверх. При этом часть менее летучего компонента конденсируется из
пара в жидкость, а за счет выделившейся теплоты конденсации часть
более летучего компонента из жидкости переходит в пар.
Если жидкая смесь обладает малыми положительными отклонениями от
закона Рауля, она может быть путем ректификации полностью
разделена на компоненты.
9
10.
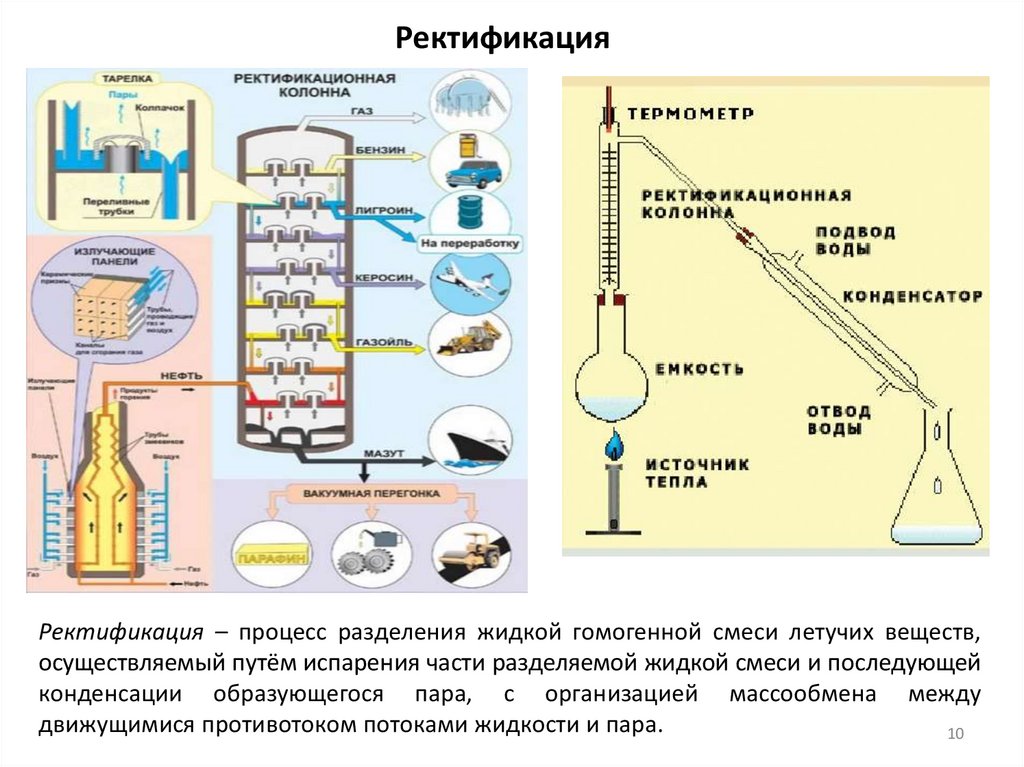
РектификацияРектификация – процесс разделения жидкой гомогенной смеси летучих веществ,
осуществляемый путём испарения части разделяемой жидкой смеси и последующей
конденсации образующегося пара, с организацией массообмена между
движущимися противотоком потоками жидкости и пара.
10
11.
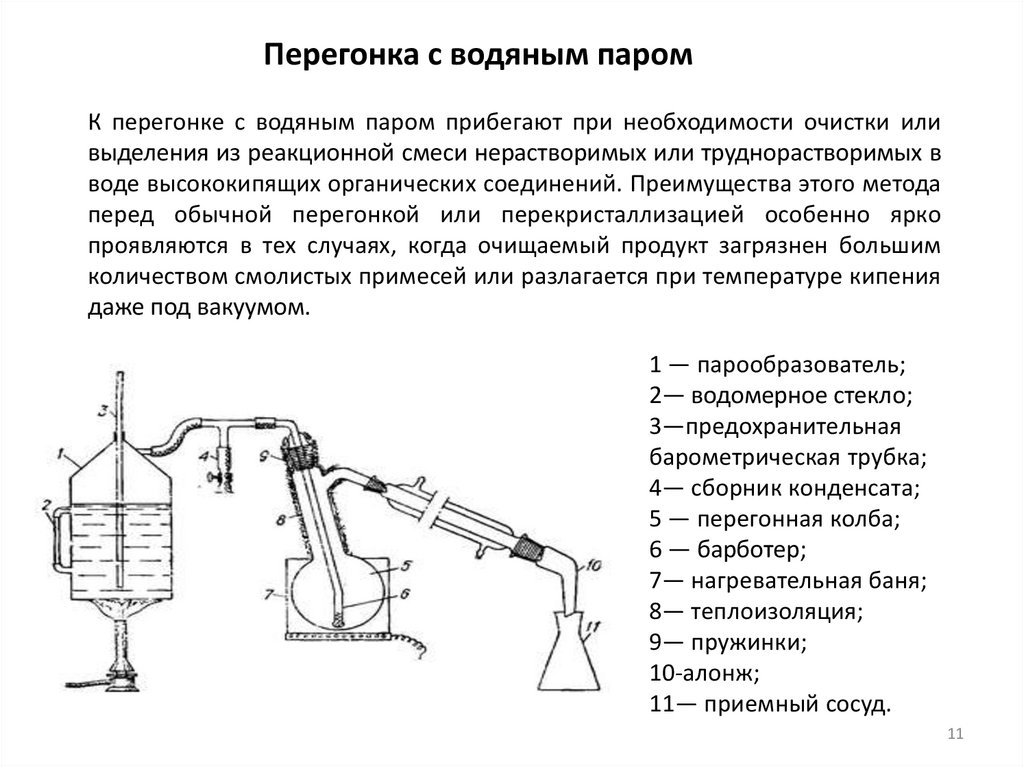
Перегонка с водяным паромК перегонке с водяным паром прибегают при необходимости очистки или
выделения из реакционной смеси нерастворимых или труднорастворимых в
воде высококипящих органических соединений. Преимущества этого метода
перед обычной перегонкой или перекристаллизацией особенно ярко
проявляются в тех случаях, когда очищаемый продукт загрязнен большим
количеством смолистых примесей или разлагается при температуре кипения
даже под вакуумом.
1 — парообразователь;
2— водомерное стекло;
3—предохранительная
барометрическая трубка;
4— сборник конденсата;
5 — перегонная колба;
6 — барботер;
7— нагревательная баня;
8— теплоизоляция;
9— пружинки;
10-алонж;
11— приемный сосуд.
11





 Химия
Химия








