Похожие презентации:
Полимеры и материалы на их основе. Тема № 20
1.
ТЕМА № 20:ПОЛИМЕРЫ И МАТЕРИАЛЫ НА ИХ ОСНОВЕ
2.
Полимером называют химическое вещество, имеющеебольшую молекулярную массу и состоящее из большого числа
периодически
повторяющихся
фрагментов,
связанных
химическими связями. Эти фрагменты называются элементарными
звеньями или мономерами.
Признаки полимеров
1. очень большая молекулярная масса (десятки и сотни тысяч а. е.)
2. цепное строение молекул (чаще встречаются простые связи).
Быстрое расширение производства
полимеров привело к тому, что их
пожароопасность (все они горят
лучше,
чем
дерево)
стала
национальным бедствием для многих
стран.
При горении и разложении полимеров
образуются различные токсичные для
человека вещества, представляющие также
угрозу для экологии.
3.
Полимеры труднорастворимы;нелетучи; не имеют точной
Тпл.; существуют только в
двух агрегатных состояниях –
твёрдом и жидком; имеют
очень большую вязкость;
смачиваемость зависит от
наличия гидрофильных групп
(-NH-, -COOH).
Применение полимеров:
•полимеры
биологического
и
медицинского назначения
•ионно- и электронно-обменные
материалы
•тепло- и термостойкие пластики
•изоляторы
•строительные и конструкционные
материалы
ПАВы и материалы, стойкие к
агрессивной среде.
Классификация полимеров по составу основной
макромолекул (наиболее распространенная):
цепи
I. Карбоцепные ВМС – основные полимерные цепи построены
только из углеродных атомов
II. Гетероцепные ВМС – основные полимерные цепи, помимо
атомов углерода, содержат гетероатомы (кислород, азот,
фосфор, серу)
III. Элементоорганические полимерные соединения – основные
цепи макромолекул содержат элементы, не входящие в состав
природных органических соединений (Si, Al, Ti, B, Pb, Sb, Sn и
др.)
4.
I Карбоцепные ВМСа) полимеры с насыщенными цепями: полипропилен
[-CH2-CH-]n,
полиэтилен – [-CH2-CH2-]n
I
CH3
б) полимеры с ненасыщенными цепями: полибутадиен
[-CH2-CH=CH-CH2-]n
в) галогензамещенные полимеры: тефлон [-CF2-CF2-]n,
ПВХ [-CH2-CHCl-]n;
г) полимерные спирты:
поливиниловый спирт
– [-CH2-CH-]n;
I
OH
д) производных
спиртов:
поливинилацетат –
[-CH2-CH-]n;
I
OCOCH3
е) полимерные альдегиды и
кетоны: полиакролеин
[-СН2-СН-]n;
I
з) полимерные нитрилы: ПАН – [-СН2-СН-]n;
Н-С=О
Полиакрилонитрил
I
ж) полимеры карбоновых
CN
кислот: полиакриловая и) полимеры ароматических углеводородов:
кислота
полистирол
[-СН2-СН-]n;
I
– [-СН2-СН-]n.
СООН
I
С 6Н5
5.
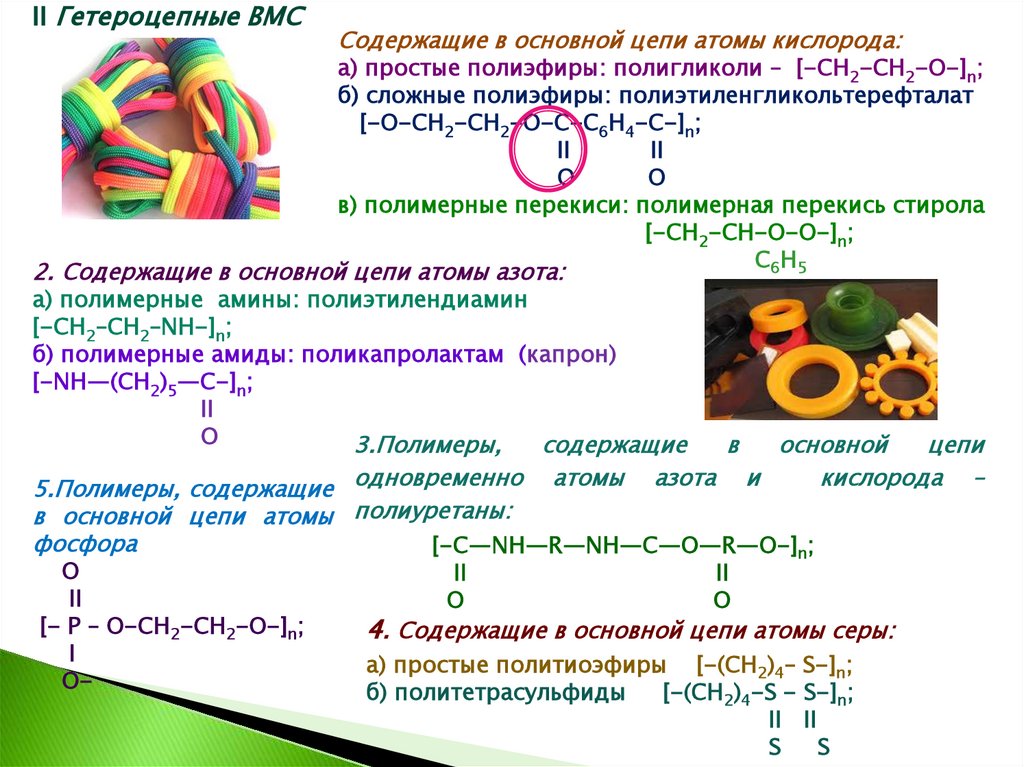
II Гетероцепные ВМССодержащие в основной цепи атомы кислорода:
а) простые полиэфиры: полигликоли – [-СН2-СН2-О-]n;
б) сложные полиэфиры: полиэтиленгликольтерефталат
[-О-СН2-СН2-О-С-С6Н4-С-]n;
II
II
O
O
в) полимерные перекиси: полимерная перекись стирола
[-СН2-СН-О-О-]n;
С6Н 5
2. Содержащие в основной цепи атомы азота:
а) полимерные амины: полиэтилендиамин
[-СН2–СН2–NН-]n;
б) полимерные амиды: поликапролактам (капрон)
[-NН—(СH2)5—С-]n;
II
O
3.Полимеры,
содержащие
в
основной
цепи
и
кислорода –
5.Полимеры, содержащие одновременно атомы азота
в основной цепи атомы полиуретаны:
фосфора
[-С—NН—R—NН—С—О—R—О-]n;
O
II
[- P – O-CH2-CH2-O-]n;
I
O-
II
O
II
О
4. Содержащие в основной цепи атомы серы:
а) простые политиоэфиры [-(СН2)4– S-]n;
б) политетрасульфиды
[-(СН2)4-S - S-]n;
II II
S
S
6.
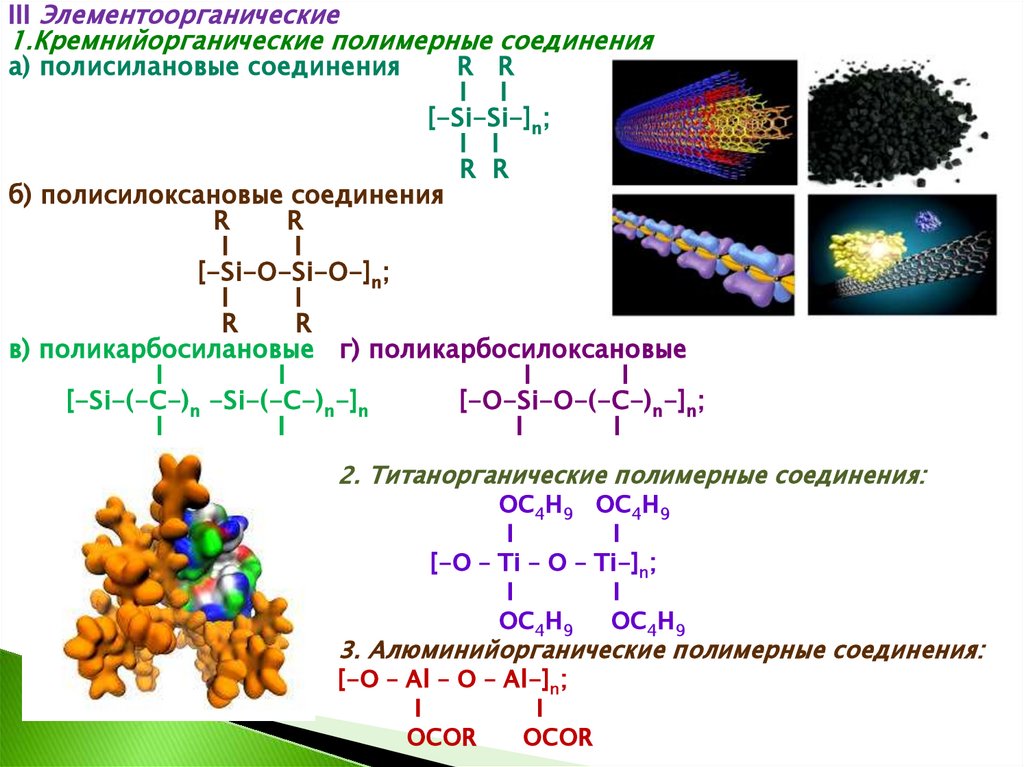
III Элементоорганические1.Кремнийорганические полимерные соединения
а) полисилановые соединения
R R
I I
[-Si-Si-]n;
I I
R R
б) полисилоксановые соединения
R
R
I
I
[-Si-O-Si-O-]n;
I
I
R
R
в) поликарбосилановые г) поликарбосилоксановые
I
I
I
I
[-Si-(-C-)n -Si-(-C-)n-]n
[-O-Si-O-(-C-)n-]n;
I
I
I
I
2. Титанорганические полимерные соединения:
OC4H9 OC4H9
I
I
[-O – Ti – O – Ti-]n;
I
I
OC4H9
OC4H9
3. Алюминийорганические полимерные соединения:
[-O – Al – O – Al-]n;
I
I
OCOR
OCOR
7.
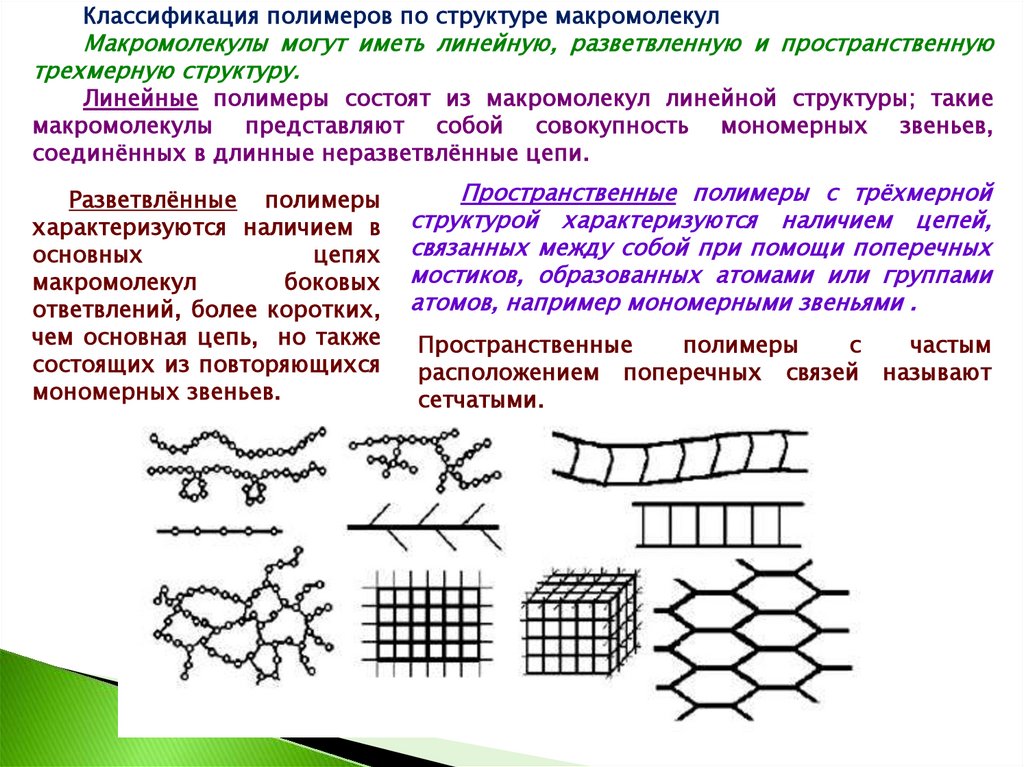
Классификация полимеров по структуре макромолекулМакромолекулы могут иметь линейную, разветвленную и пространственную
трехмерную структуру.
Линейные полимеры состоят из макромолекул линейной структуры; такие
макромолекулы представляют собой совокупность мономерных звеньев,
соединённых в длинные неразветвлённые цепи.
Разветвлённые полимеры
характеризуются наличием в
основных
цепях
макромолекул
боковых
ответвлений, более коротких,
чем основная цепь, но также
состоящих из повторяющихся
мономерных звеньев.
Пространственные полимеры с трёхмерной
структурой характеризуются наличием цепей,
связанных между собой при помощи поперечных
мостиков, образованных атомами или группами
атомов, например мономерными звеньями .
Пространственные
полимеры
с
частым
расположением поперечных связей называют
сетчатыми.
8.
Отдельные звенья макромолекул могут самостоятельновступать в химические реакции; свойства полимера
зависят от геометрической
формы макромолекул;
появление водородных связей между макромолекулами
значительно повышает прочность полимера.
9.
Классификация по поведению при нагреваниитермопластичные - полимеры, свойства которых
обратимы
при
многократном
нагревании
и
охлаждении;
термореактивные - полимеры, макромолекулы
которых при нагревании в результате происходящих
между ними химических взаимодействий соединяются
друг с другом; при этом образуются пространственные
сетчатые структуры за счёт прочных химических связей.
После прогрева термореактивные полимеры обычно
становятся неплавкими и нерастворимыми –
происходит процесс их необратимого отверждения.
Классификация по горючести
Воспламенение и горение материалов зависят не только от природы
материала, но и от температуры источника зажигания, условий воспламенения,
формы изделия или конструкций и т.д.
Полимерные материалы делят на горючие, трудногорючие и негорючие. Из
сгораемых материалов выделяют трудновоспламеняемые и трудносгораемые самозатухающие.
Сгораемые полимеры: полиэтилен, полистирол, полиметилметакрилат,
поливинилацетат, эпоксидные смолы, целлюлоза и т.д.
Трудносгораемые полимеры: ПВХ, тефлон, фенолформальдегидные и
мочевиноформальдегидные смолы.
10.
Классификация по способуполучения (происхождения)
- природные (белки, нуклеиновые
кислоты, природные смолы,
целлюлоза) животного и
растительного происхождения;
- синтетические (полиэтилен,
полипропилен и т.д.)
- искусственные (химическая
Органические
и
модификация природных
неорганические полимеры
полимеров – эфиры целлюлозы)
Неорганические: кварц,
силикаты, алмаз, графит,
корунд, карбин, карбид бора
и т. д.
Органические: каучуки,
целлюлоза, крахмал,
органическое стекло и т. д.
11.
Реакции синтеза полимеров Полимеризация – это процессполучения ВМС, при котором молекула полимера образуется путём
последовательного
присоединения
молекул
мономера
(низкомолекулярные вещества) и активному центру на конце растущей
цепи
nM Mn' ; где n-число отдельных молекул; n’-степень
полимеризации; М – молекулярная масса мономера.
Степень полимеризации указывает количество звеньев, входящих в
макромолекул: n= М полимера / М мономера, n 100-10000 и более.
Полимеризация
бывает
радикальной
и
ионной.
Радикальная полимеризация протекает с участием свободных радикалов.
Стадии: инициирования, роста цепи, обрыва цепи.
Инициирование:
нагреванием (термическая активация):
t
t
(С6Н5СОО)2 2 [С6Н5СОО ]= 2R
перекись бензоила
СН2=СН2 СН2-СН2 бирадикал
введением специальных инициаторов:
Далее СН2=СН2 + СН2-СН2 +СН2=СН2 Далее R + CH =CH R-CH -CH и
2
2
2
2
т.д.
СН2-(СН2)4-СН2 и т.д.
Обрыв цепи:
радиационный способ активации:
CН2=СН2
h
СН2-СН2
R—(CH2)n + (CH2)n–R'
R—(CH2)n—(CH2)n –R
12.
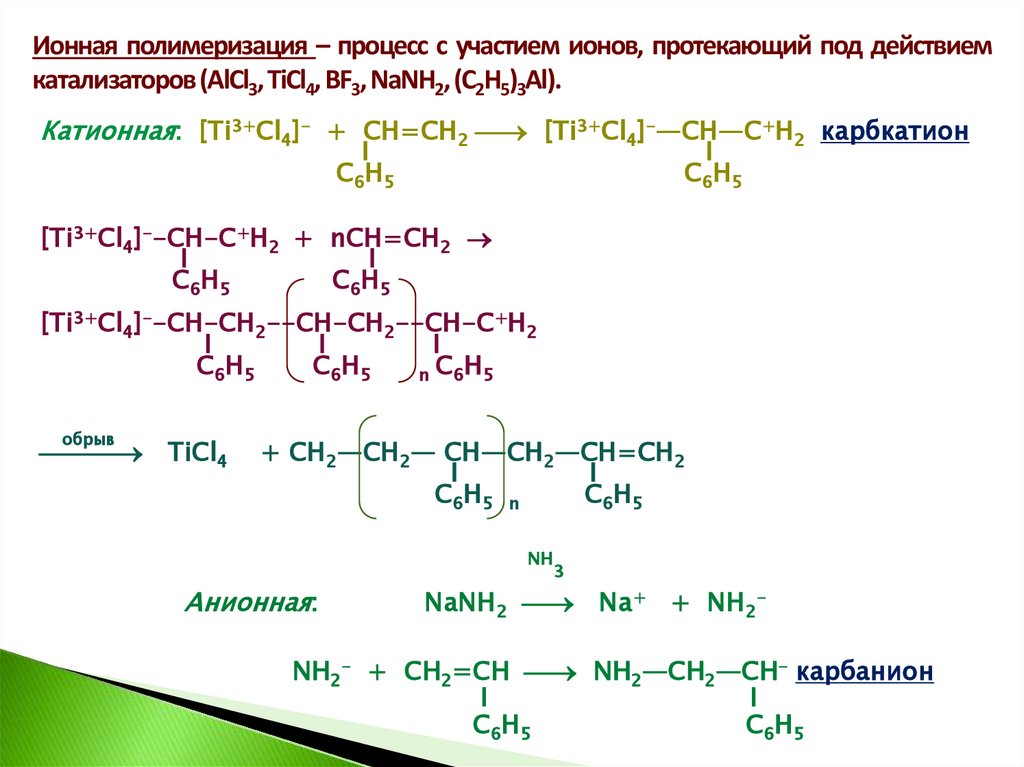
Ионная полимеризация – процесс с участием ионов, протекающий под действиемкатализаторов (AlCl3, TiCl4, BF3, NaNH2, (C2H5)3Al).
Катионная: [Ti3+Cl4]- + CH=CH2 [Ti3+Cl4]-—CH—C+H2 карбкатион
I
C 6H5
I
C6H5
[Ti3+Cl4]--CH-C+H2 + nCH=CH2
I
I
C 6H5
C 6H5
[Ti3+Cl4]--CH-CH2--CH-CH2--CH-C+H2
I
I
I
C 6 H5
C 6H5
n C 6H5
обрыв
TiCl4
+ CH2—CH2— CH—CH2—CH=CH2
I
I
C 6H5 n
C6H5
NH
Анионная:
3
NaNH2 Na+ + NH2-
NH2- + CH2=CH NH2—CH2—CH- карбанион
I
I
C 6H5
C 6H5
13.
Мономерами для полимеризации могут быть вещества,содержащие кратные связи или циклы, раскрывающиеся в
результате реакции.
Мономеры: этилен СН2=СН2; стирол СН2=СН; капролактам
NH2-(CH2)5COOH,
C6H5
метилметакрилат СН2= С-СООСН3, изопрен СН2=С-СН=СН2,
I
I
CH3
CH3
CI
I
бутадиен
СН2=СН-СН=СН2,
хлоропрен
СН2=С-СН=СН2;
винилхлорид СH2=CHCl; акрилонитрил CH2=CH—CN и другие.
Если в процессе участвует несколько видов мономеров,
то происходит сополимеризация (бутадиеннитрильный,
бутадиенстирольный каучуки и т.д.)
14.
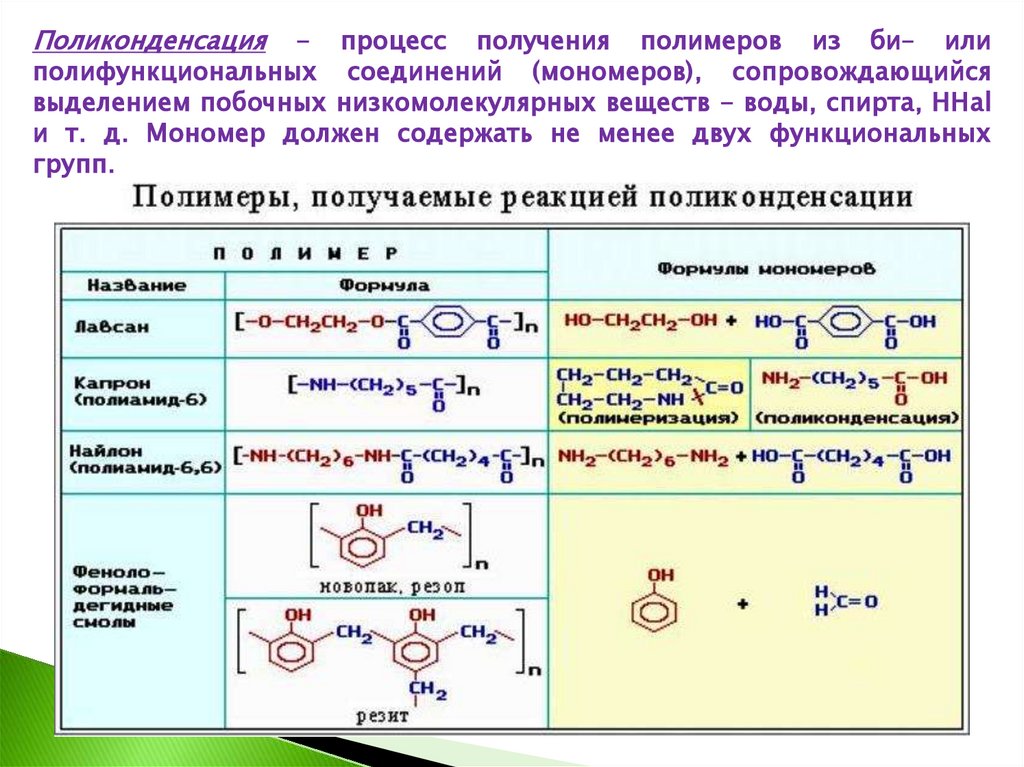
Поликонденсация- процесс получения полимеров из би– или
полифункциональных соединений (мономеров), сопровождающийся
выделением побочных низкомолекулярных веществ - воды, спирта, ННal
и т. д. Мономер должен содержать не менее двух функциональных
групп.
15.
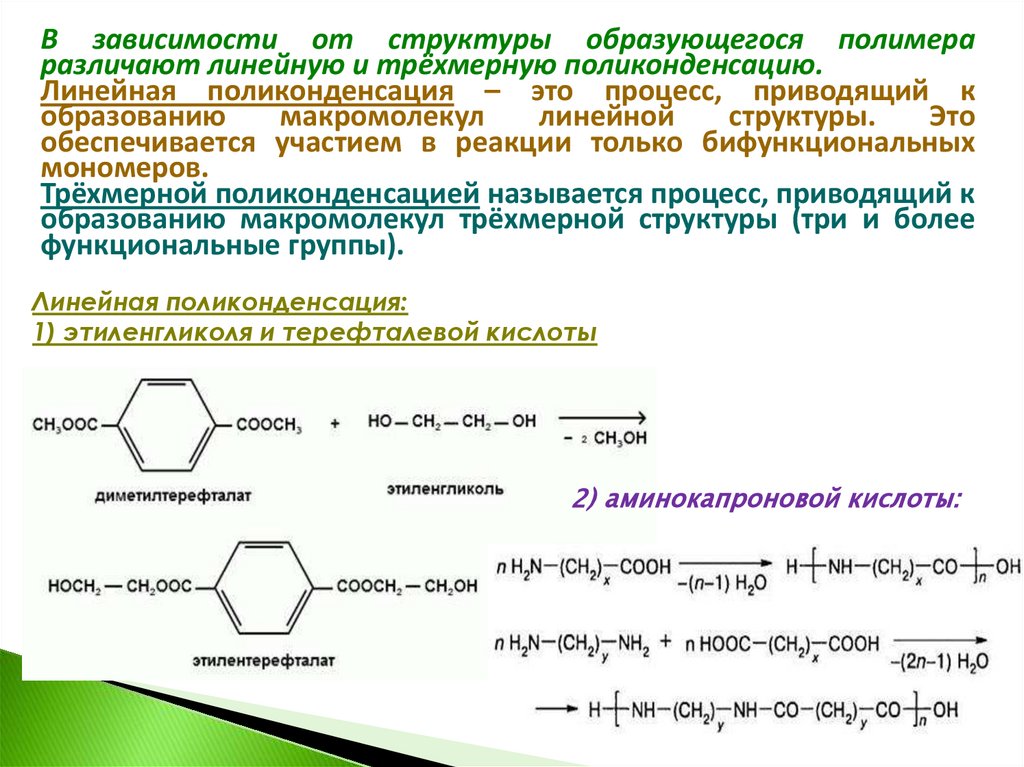
В зависимости от структуры образующегося полимераразличают линейную и трёхмерную поликонденсацию.
Линейная поликонденсация – это процесс, приводящий к
образованию
макромолекул
линейной
структуры.
Это
обеспечивается участием в реакции только бифункциональных
мономеров.
Трёхмерной поликонденсацией называется процесс, приводящий к
образованию макромолекул трёхмерной структуры (три и более
функциональные группы).
Линейная поликонденсация:
1) этиленгликоля и терефталевой кислоты
2) аминокапроновой кислоты:
16.
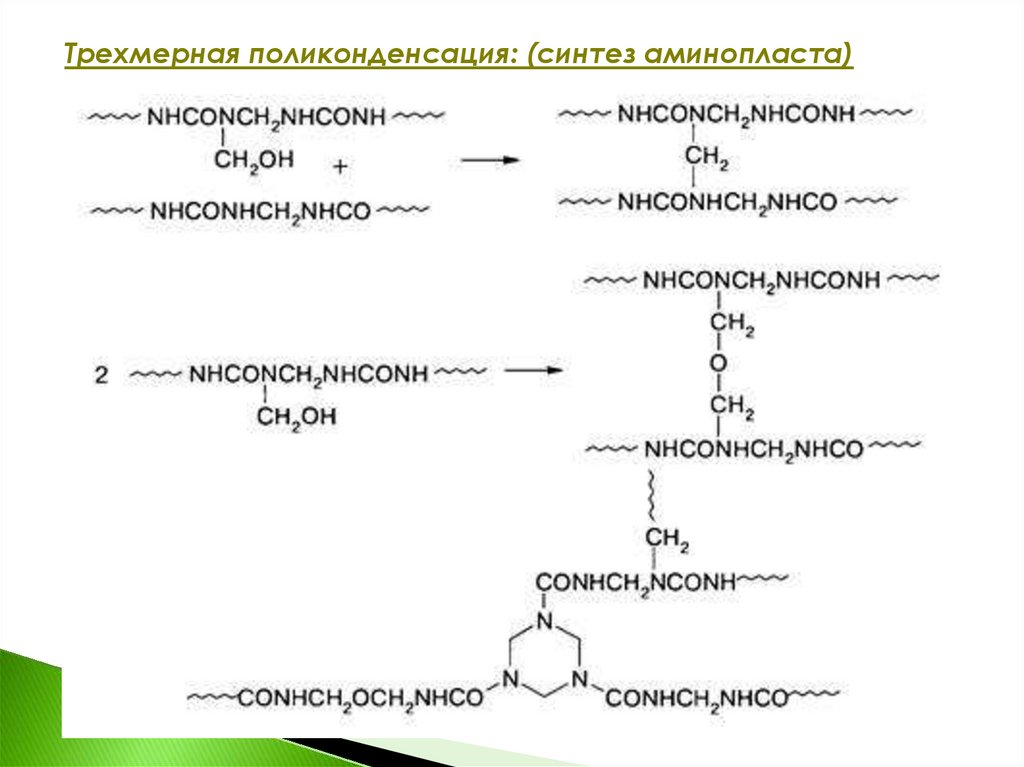
Трехмерная поликонденсация: (синтез аминопласта)17.
Особенности горения полимеровДля сгорания единицы веса полимера требуются большие объёмы
воздуха (в 1.5 – 2 раза больше, чем для древесины - 4.5 м3/кг);
Образуются большие объемы продуктов горения;
Значительный недожог – образуется обильный плотный дым;
В дыму содержится много токсичных продуктов недожога (CO, NO2,
HCl, HCN, CO2 и т.д.);
Плавление и растекание горящих полимеров – происходит
распространение пожара по всем направлениям;
Высокая температура горения – 1100 – 1300 оC и более (до 2500 оC);
Высокая излучательная способность пламени с передачей
воспламеняющего светового импульса на большие расстояния.
Горение полимеров – это многостадийный (в
пространстве и времени) многофазный циклический
самоподдерживающийся процесс со взаимосвязанным
тепломассопереносом.
Разрыв цикла горения может быть осуществлен как в газовой, так и в
конденсированной фазе, и на поверхности раздела фаз (расплав/газ).
Как правило, необходимо замедлить тепломассоперенос в системе и
уменьшить долю возвращенной теплоты на разогрев и расплавление
твердой фазы и снизить выход горючих газов.
18.
Способы защиты полимеров от огня:а) обработка полимера растворами неорганических солей – инертный
способ, соль не гасит огонь, а лишь препятствует его распространению
от одного волокна к другому, образуя корку.
б) обработка полимера веществом, разлагающимся под действием
огня с выделением негорючих газов либо твердой коксовой пленки
(антипиреном). Над поверхностью
материала
либо
образуется
защитная газовая подушка либо прекращается доступ кислорода в зону
горения.
При введении в материал огнезащитных добавок (антипиренов)
изменяется состав и структура материала, что зачастую приводит к
снижению горючести.
Антипирены снижают горючесть различным образом:
1) ингибируют реакцию горения;
2) изменяют долю возвращённой теплоты горения;
3) приводят к получению менее горючих продуктов пиролиза или
снижают долю газов при деструкции;
4) снижают скорость диффузии горючих продуктов пиролиза к фронту
пламени.
Антипиренами могут быть вещества, которые содержат фосфор,
галогены, азот, сурьму в своём составе. К этой категории могут быть
причислены гидроокись алюминия и магния, соединения бора, силикаты,
карбонаты.
Наиболее
эффективными
и
практически
универсальными
антипиренами являются фосфор - и галогенсодержащие соединения.
19.
Основныеполимеров
реакции
термического
разложения
и
горения
Виды деструкции:
• химическая (+Н2О, + кислоты, + щёлочи и т. д.);
• механическая (необратимая деформация под действием нагрузки);
• термоокислительная (О2 + нагрев);
• термическая;
• фотохимическая (h );
• радиационная (n, , , - излучения);
• биологическая (нитраты целлюлозы, ряд каучуков разлагаются под
действием микроорганизмов).
При разложении полимеров образуется твердые (коксовый остаток),
жидкие и газообразные вещества. Жидкие и газообразные вещества
называются "летучими". Выделение летучих веществ – признак
разложения полимеров.
Температура, при которой начинают выделяться летучие вещества температура начала разложения.
Конечными продуктами разложения сложного вещества (полимеров)
являются простые вещества (C2H2 – C, H2 , капрона – C, O2, H2, N2).
Распад на простые вещества возможен при Т ~ 3000 оС.
На пожаре Т 1500 оС состав выделяющихся веществ сложный (H2, CO, C2H4, C2H6, СН4, СО2, О2, НСN, NН3 и т.д.)
20.
При воздействии сравнительно низких температур (до 500-600 оС) наполимер, летучие вещества в своём составе будут содержать больше
смолистых и меньше газообразных веществ. С повышением температуры
образование газообразных веществ увеличивается.
В зависимости от того, разложение полимеров идёт в присутствии или
отсутствии О2 воздуха, различают термическое и термоокислительное
разложение.
Под
термическим
разложением
понимают
распад
полимерного материала под действием температуры в отсутствии
окислителя (относительное движение составляющих приводит к
разрушению связей). Термическая деструкция обычно идёт по
радикальному
механизму.
При
этом
происходит
деполимеризация, т.е. отщепление мономеров.
При 300 оС полистирол деполимеризуется на 60-70%,
органическое стекло – на 90-95 %:
CH3
CH3
CH3
CH3
CH3
CH3
I
I
I
I
I
I
—CH2 – C—CH2—C—CH=C –CH2—C—CH2 + C—CH=C
I
I
I
I
I
I
COOCH3
COOCH3 COOCH3
COOCH3 COOCH3 COOCH3
21.
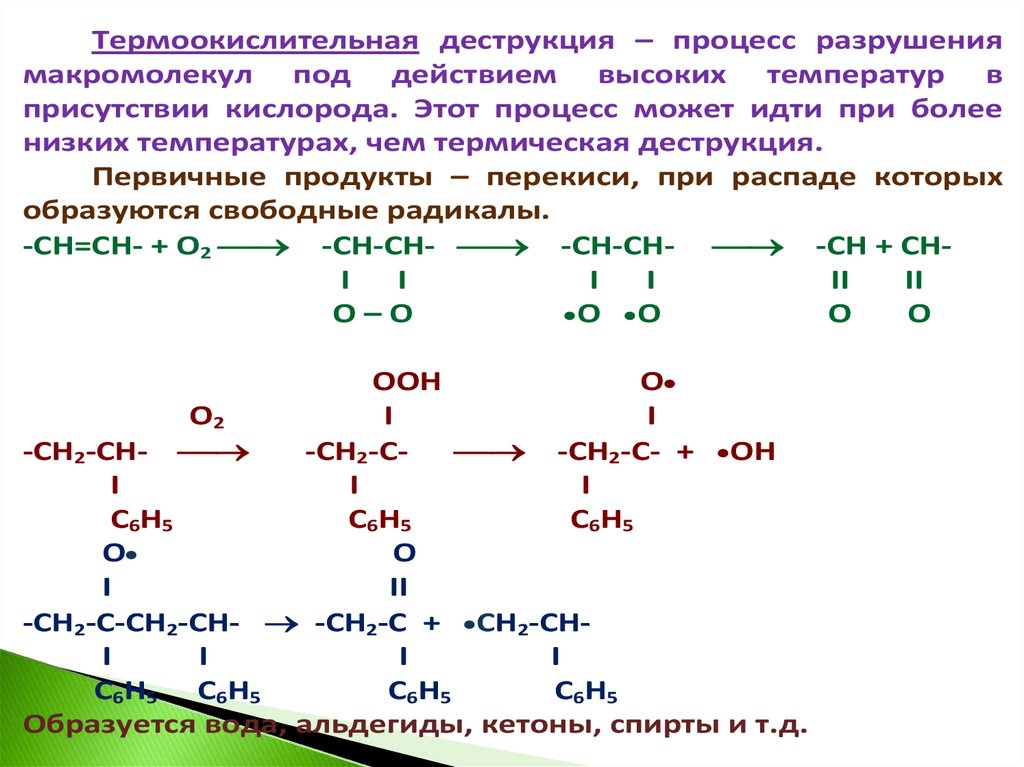
Термоокислительная деструкция – процесс разрушениямакромолекул под действием высоких температур в
присутствии кислорода. Этот процесс может идти при более
низких температурах, чем термическая деструкция.
Первичные продукты – перекиси, при распаде которых
образуются свободные радикалы.
-CH=CH- + O2 -CH-CH- -CH-CH- -CH + CHI
I
I
I
II
II
O–O
O O
O
O
OOH
O
O2
I
I
-CH2-CH-
-CH2-C -CH2-C- + ОН
I
I
I
С6Н5
С6Н5
С6Н5
O
O
I
II
-CH2-C-CH2-CH- -CH2-C + CH2-CHI
I
I
I
С6Н5 С6Н5
С6Н5
С6Н5
Образуется вода, альдегиды, кетоны, спирты и т.д.
22.
Токсичность продуктов горения и разложения полимеровГазообразные продукты (NH3, HCI, CI2, SO2, HCN), растворимые в воде,
поглощаются носовой полостью.
Нерастворимые в воде (СО) продукты проникают в лёгкие, где происходит
интенсивный газообмен с кровью.
Твёрдые продукты горения проникают также в дыхательные пути (бронхи,
лёгкие).
Токсичные продукты горения: СО, СО2, NH3, Br2, CI2, COCI2, HCN, H2S, SO2,
HCI, HBr, HF, COF2, CH3CI, C2H5Br, CH2=CHCI, HCOH, CH3COH.
Их токсичное действие увеличивается при понижении концентрации О2,
которое всегда наблюдается при техногенных пожарах.
Нормальное содержание кислорода- в воздухе 21 %, при 14 % - ощущается
головокружение, головная боль, утомляемость; при 6 % - наступает смерть в
течении 6-8 минут.
СО2
(в воздухе 0,05-0,04 %). Наркотическое действие. При высокой
концентрации – химические ожоги. При 9 % - через 4 часа падение
давления и смерть.
СО – мало растворим в воде. Получается при неполном сгорании органики.
СО легко проникает через пористые материалы. Связь гемоглобина с СО
прочнее, чем с О2. Вдыхание 5 % СО составе воздушной смеси в течении
5-10 минут - смертельно.
HCl - резкий запах, хорошо растворим в воде. Вызывает раздражение
слизистых оболочек глаз, носа. Образуется при сгорании Cl – содержащих
полимеров. Вызывает коррозию металлов, разрушение бетона, цемента.
HF - резкий запах, хорошо растворим в воде (плавиковая кислота).
Образуется при сгорании фторсодержащих полимеров. Сильно раздражает
верхние дыхательные пути человека. Вызывает коррозию металлов.
23.
Н2S – запах тухлых яиц. Скапливается на дне ям колодцев и т.д. Горюч ивзрывоопасен. Образуется при горении шерсти, резины и т. д. В небольших
количествах вызывает жжение, слезотечение, светобоязнь. В больших
концентрациях – судороги и смерть от остановки дыхания. Углеводороды
усиливают его действие.
SO2 – характерный острый запах. Раздражает слизистые, травмирует лёгкие.
Сухой кашель, жжение и боль в горле, слезотечение, кровотечение.
HCN – бесцветная очень подвижная жидкость. Ткип. =25,7 оС. Легче воздуха.
Хорошо растворима в воде, горюча. Хорошо проникает через кожный и
легочный барьер, действует на нервную систему, парализует дыхательный
центр.
NO – образуется при сгорании азотсодержащих полимеров. Разрушает
гемоглобин.
NO2 - бурый газ. Раздражение слизистых, химические ожоги, отёк лёгких.
NH3 – образуется при сгорании азотсодержащих полимеров. Обладает
резким запахом. Хорошо растворим в воде. Горюч. Оказывает раздражающее
действие на слизистые оболочки.
COCI2
– запах прелых фруктов или сена. Тяжелее воздуха. Хорошо
растворяется в органике, плохо в холодной воде. При нагревании может
разлагаться: COCI2=CO+CI2. Боевое ОВ; запрещен после 1 мировой войны.
Хлор – поражает лёгкие, вызывает отек Квинке, легочные кровотечения.
Обычно на человека действует смесь продуктов горения.
Повышение температуры и влажности, понижение парциального
давления О2 усиливают токсичное действие ядов.
24.
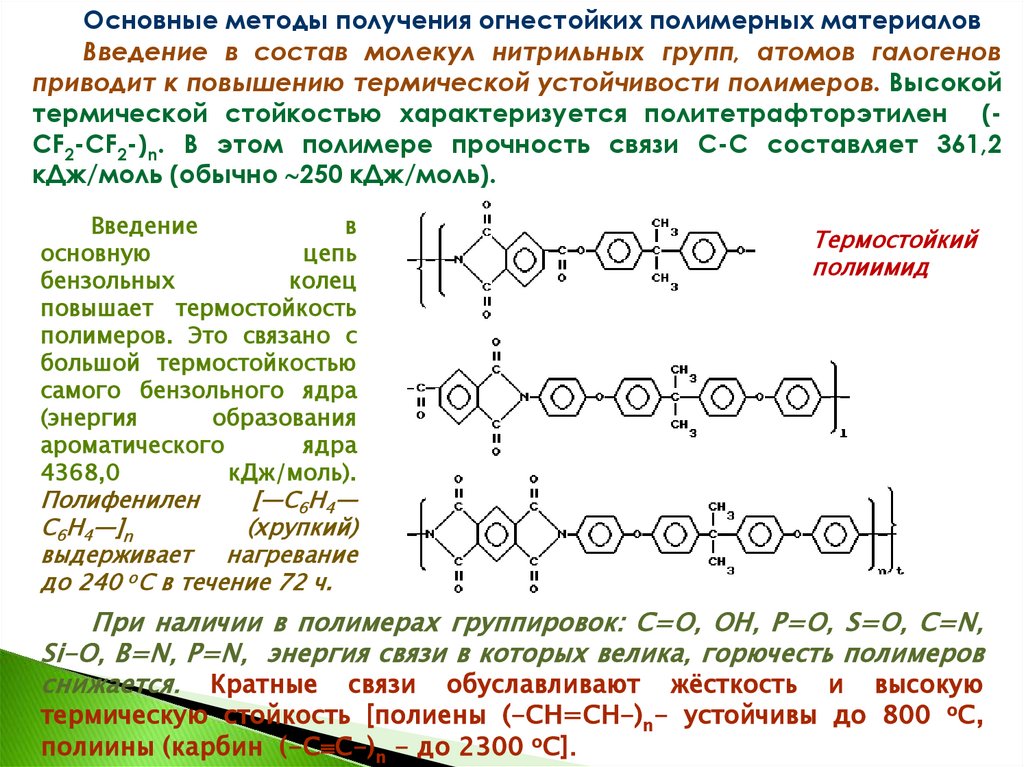
Основные методы получения огнестойких полимерных материаловВведение в состав молекул нитрильных групп, атомов галогенов
приводит к повышению термической устойчивости полимеров. Высокой
термической стойкостью характеризуется политетрафторэтилен (CF2-CF2-)n. В этом полимере прочность связи С-С составляет 361,2
кДж/моль (обычно 250 кДж/моль).
Введение
в
основную
цепь
бензольных
колец
повышает термостойкость
полимеров. Это связано с
большой термостойкостью
самого бензольного ядра
(энергия
образования
ароматического
ядра
4368,0
кДж/моль).
Термостойкий
полиимид
Полифенилен
[—С6Н4—
С6Н4—]n
(хрупкий)
выдерживает нагревание
до 240 оС в течение 72 ч.
При наличии в полимерах группировок: С=О, ОН, Р=О, S=O, C=N,
Si-О, B=N, P=N, энергия связи в которых велика, горючесть полимеров
снижается. Кратные связи обуславливают жёсткость и высокую
термическую стойкость [полиены (-CH=CH-)n- устойчивы до 800 оС,
полиины (карбин (-С С-)n - до 2300 оС].
25.
Зависимость пожарной опасности полимеров от их химическогостроения
Оргстекло
Деполимеризация: при 300 оС – на 90-95 %. При термоокислительной деструкции
образуются и другие продукты. При пламенном горении в основном образуется СО2 и
Н2О.
Полистирол
До 400 оС происходит деполимеризация При пожаре - пеплообразование,
растекание, чёрный дым.
ПВХ материалы
Распад начинается уже при температуре 160-180 оС. Образуются HCI (до
95 % хлора) и COCl2.
Хлоропреновый каучук и резина
Повышенная термическая устойчивость (наличие галогена). Выделение
НСI начинается при 200-250 оС и заканчивается при 400 оС. Из готовой
резины выделяется SO2, SO3, H2S и много сажи.
Тефлон
Устойчив термически до 400 оС. Способен к горению только в среде,
обогащенной кислородом. В условиях пожара разлагается до мономера
С 2 F4 .
Капрон, нитрон, шерсть
Продукты горения: СО, СО2, Н2О, СnН2n+2, HCN, NO, NO2, NH3 и другие
(для шерсти – SO2, H2S, S – в виде жёлтого дыма). Комбинированное
отравляющее действие.
26.
Пластические массыПластическими массами называют материалы, полученные на
основе полимеров, содержащие различные добавки и способные
под влиянием температуры и давления становиться пластичными.
В состав пластмасс, кроме полимера, входят наполнители,
пластификаторы,
стабилизаторы,
красители,
отвердители,
смазывающие вещества и другие.
В качестве наполнителей применяют порошкообразные,
волокнистые и листообразные горючие и негорючие вещества.
Содержание наполнителя в пластмассах 30 - 70 %.
Порошкообразные наполнители – кварцевая мука, мел, тальк
и другие измельчённые материалы. Эти наполнители придают
пластмассе
твёрдость.
теплостойкость,
кислотостойкость,
увеличивают
Волокнистые наполнители – асбестовое волокно, хлопковое
очесы, древесное волокно, стеклянное волокно – также
увеличивают механическую прочность пластмасс и снижают их
хрупкость, повышают теплостойкость.
Листообразными наполнителями для пластмасс является
бумага, х/б и стеклоткани, асбестокартон и т. д.
27.
улучшают свойства полимеров: эластичность,морозостойкость, огнестойкость, стойкость к действию Уф-света, а также
облегчают условия переработки. В качестве пластификаторов в
пластмассах применяют главным образом сложные эфиры различных
кислот, а также низкомолекулярные полиэфиры.
Пластификаторы
Стабилизаторы – вещества, которые вводят в пластмассы для
повышения их стойкости к действию тепла, света, кислорода воздуха и
т. д., т. е. замедления разрушения полимера, протекающего при
переработке и эксплуатации. В качестве стабилизаторов применяют
большое количество органических и металлоорганических соединений.
Красители и пигменты придают пластмассам определённый цвет.
Они должны иметь живые тона, не давать грязноватого оттенка,
обладать химической стабильностью. В качестве красителей применяют
нитрозин, пигмент жёлтый, хризондин, в качестве пигментов - охру,
сурик, умбру, ультрамарин, окись хрома, белила.
Отвердители вводят в некоторые полимеры для перевода их в
неплавкое и нерастворимое соединение. В качестве отвердителей
применяют различные перекиси и гидроперекиси, третичные амины,
ангидриды различных кислот и др. В ряде случаев для сокращения
времени отверждения применяют ускорители отверждения.
Смазывающие вещества вводят в пластмассы для предотвращения
прилипания к пресс-формам (олеиновая кислота, стеарин и другие).
28.
Пластмассы на основе полиэтилена устойчивы к действию растворителейи концентрированных кислот; хорошие диэлектрики Тпл. ~ 300 оC. Горят
светящимся пламенем. Твоспл. – 300 оС, Твсп.- 400 оС. При нагревании идёт
деполимеризация с образованием горючих смесей [трубы, плёнка,
электроизоляция].
Пластмассы на основе полистирола – твёрдые, прозрачные, хрупкие
вещества, растворимые в бензоле, толуоле, диэлектрики. С целью
уменьшения хрупкости проводят сополимеризацию полистирола с каучуком.
В этом случае получают ударопрочное вещество. Тпл. и Твоспл. – 200 оС, Твсп. –
400 оС. Горит сильно коптящим пламенем. Пыль пожаровзрывоопасна.
[ванны, раковины, детали холодильников, облицовочная плитка, пенопласты
и т. д.].
Пластмассы на основе ПВХ – твёрдые, прозрачные
вещества. Не растворяются в кислотах, щелочах, в
большинстве
органических
растворителей.
Диэлектрики. Т размягчения
80-100 оС. При
оС
температуре
120-150
разлагаются.
При
нагревании
вспучиваются,
обугливаются
с
о
выделением НСI. Т воспл. = 1100 С. Пыль
взрывоопасна. Без пластификатора – винипласт, с
пластификатором – пластикат.
[Линолеум,
искусственная
кожа,
декоративная
плёнка, моющиеся обои, трубы, пищевая упаковка,
оконные рамы, травильные ванны, и т. д.].
29.
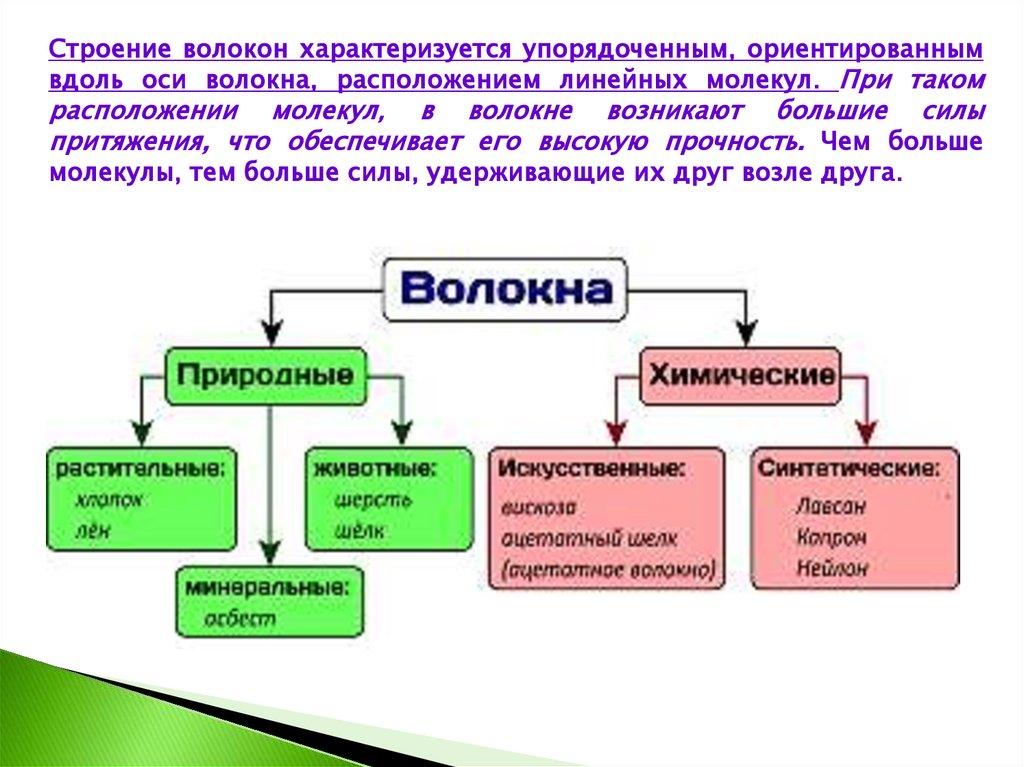
Строение волокон характеризуется упорядоченным, ориентированнымвдоль оси волокна, расположением линейных молекул. При таком
расположении молекул, в волокне возникают большие силы
притяжения, что обеспечивает его высокую прочность. Чем больше
молекулы, тем больше силы, удерживающие их друг возле друга.
30.
Капроновые волокна химически малостойкие. Под действием кислот ищелочей они растворяются. Плотность их 140 кг/м3. Тпл.=208-215 оС,
при 300 оС волокно начинает разлагаться с выделением различных
продуктов разложения.
Волокно легко воспламеняется, в расплавленном состоянии интенсивно
горит с выделением большого количества дыма, в котором содержатся
много опасных продуктов разложения (HCN, NO2, NH3) К тепловому
самовозгоранию волокно не склонно.
Применение: добавки в шерстяные изделия, искусственные меха,
капроновые корды в шинной промышленности, тяжёлые транспортные
ленты, приводные ремни, спасательные верёвки, рыболовные снасти.
31.
применение полиамидных полимеров в строительствеи автомобильной промышленности
32.
Лавсан(полиэтилентерефталат) по своим свойствам близок к
натуральной шерсти. Он имеет самую высокую прочность, изделия из
него не сминаются. Из всех видов синтетических волокон волокно
лавсан наиболее термически стойкое. Оно может работать в диапазоне
температур от –70 до +1750С. Изделия из лавсана имеют высокую
светостойкость. Диэлектрик.
Лавсан относится к химически устойчивым волокнам. Он стоек к
действию органических и минеральных кислот. Твоспл.=390 оС. В
расславленном состоянии интенсивно горит ярким, сильно коптящим
пламенем. К тепловому возгоранию волокно не склонно.
Применение: одежда, утеплители, набивка мягкой мебели, гибкие
рукава, корд, транспортные ленты, приводные ремни, заменитель
шерстяного волокна.
Волокно нитрон легко воспламеняется под действием пламени (Твоспл =
200 о С). При 220-230 оС оно размягчается и одновременно разлагается.
Горит ярким, коптящим пламенем. К тепловому самовозгоранию не
склонно.
В химическом отношении нитрон менее стоек, чем лавсан, но более
стоек, чем капрон. По внешнему виду напоминает шерсть. Нитрон
дешевле капрона и лавсана.
Применение: верхний трикотаж, технические изделия и ткани:
специальная одежда, плетеные рукава и т. д.
33.
Полиэфирные материалы в мировой химической и текстильной промышленностизанимают доминирующую позицию:
Кордовые нити
и ленты для
шин
Геосетки для
выравнивания дорог
Тара бытовая,
техническая,
медицинская
Конвеерные ленты
Строповые и
такелажные ленты,
канаты
Носители информации
34.
Текстильные нити ,шнуры
Игрушки
Лаки, смолы, клеи,
шпатлевки
Гардинно-тюлевые
изделия
Ткани , трикотаж, лечебное белье,
искусственный мех
Наполнители подушек, матрасов, утеплители одежды:
синтепон, файбертек, холлофайбер , спанбонд и.т.д.
Отделочные и
строительные
материалы
35.
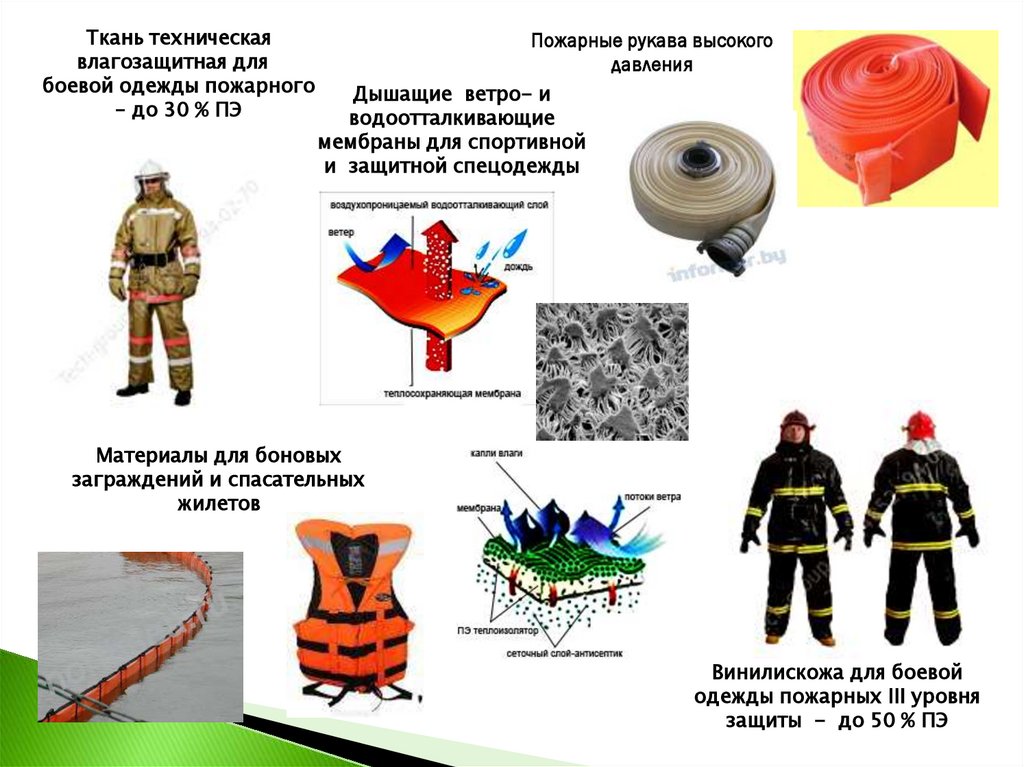
Ткань техническаявлагозащитная для
боевой одежды пожарного
– до 30 % ПЭ
Пожарные рукава высокого
давления
Дышащие ветро- и
водоотталкивающие
мембраны для спортивной
и защитной спецодежды
Материалы для боновых
заграждений и спасательных
жилетов
Винилискожа для боевой
одежды пожарных III уровня
защиты - до 50 % ПЭ
36.
применяется в резиновой, кабельной, обувнойпромышленности. Из него готовят мягкие и эбонитовые изделия,
резиновую обувь, наружные оболочки различных кабелей и т. д. Резины
из БК содержат до 60 % сажи, хорошо сопротивляются тепловому
сгоранию и многократным деформациям.
Бутадиеновый каучук
Бутадиен-стирольный каучуки. Хорошо растворяются в углеводородах и
хлорированных углеводородах, петролейном эфире, бензине. Горят
ярким, сильно коптящим пламенем. При определённых условиях
склонны к самовозгоранию.
Резины из БСК по морозостойкости в большинстве случаев уступают
натуральным, но по износостойкости, сопротивлению тепловому,
озоновому и естественному старению, пароводонепроницаемости
превосходят натуральные. Работоспособность шин из них на 10 %
больше, чем из других эмульсионных каучуков общего назначения.
Хлоропреновые каучуки Каучуки типа наирит в основном горючи. Резины
на основе наирита свето- и озоностойкие хорошо сопротивляются
истиранию, некоторые из них не горючи и имеют повышенную масло
стойкость.
Применение: резиновая и кабельная промышленность (ремни,
транспортные
ленты, рукава, формовые изделия, наружные оболочки
кабелей, специальные озоно- и маслостойкие изделия).


























 Химия
Химия








