Похожие презентации:
Патология клетки
1.
Патология клеткиБрилль
Игорь Ефимович
Профессор
кафедры патофизиологии им. А.А. Богомольца,
доктор медицинских наук,
академик Всемирной Академии Биомедицинских Технологий
(WABT, UNESCO), академик Лазерной Академии Наук (ЛАН РФ),
академик Российской Академии Естествознания (РАЕ),
Соросовский профессор
2.
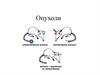
АльтерацияПовреждающий агент действует на различные
типы клеток
Специфические
клетки ткани
Клетки
соединительной
ткани (тучные)
Клетки крови
(нейтрофилы,
моноциты)
Клетки стенки
сосудов
Нервные
клетки
3.
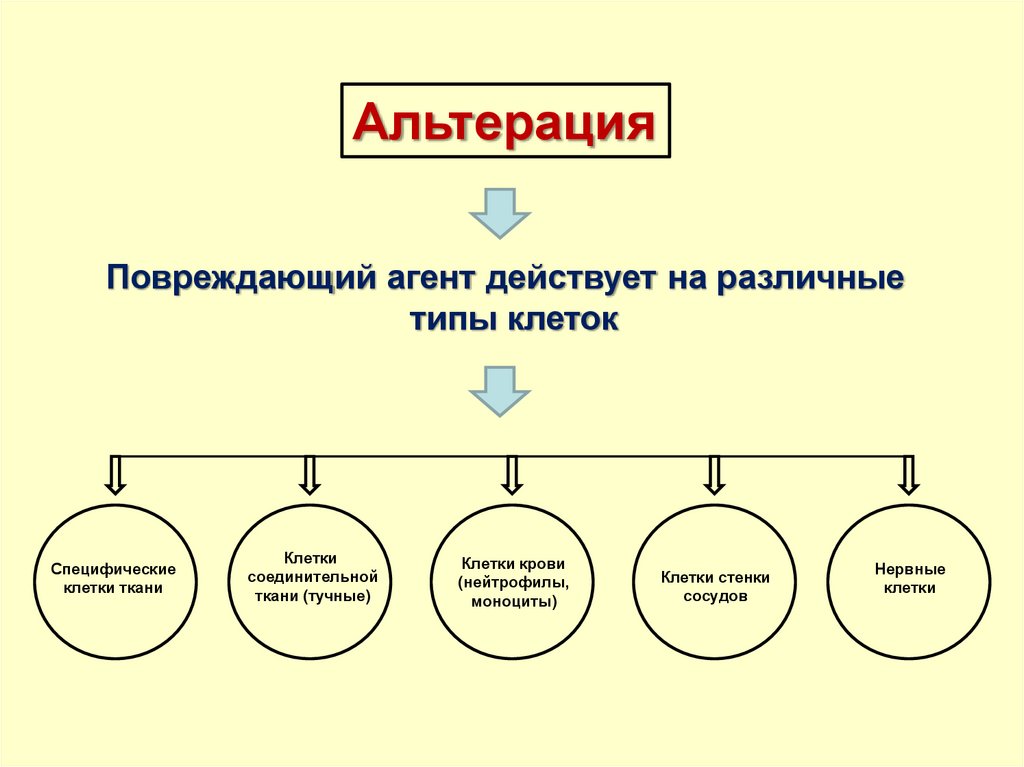
Клеточные органеллыЦилия
Центриоли
Рибосомы
4.
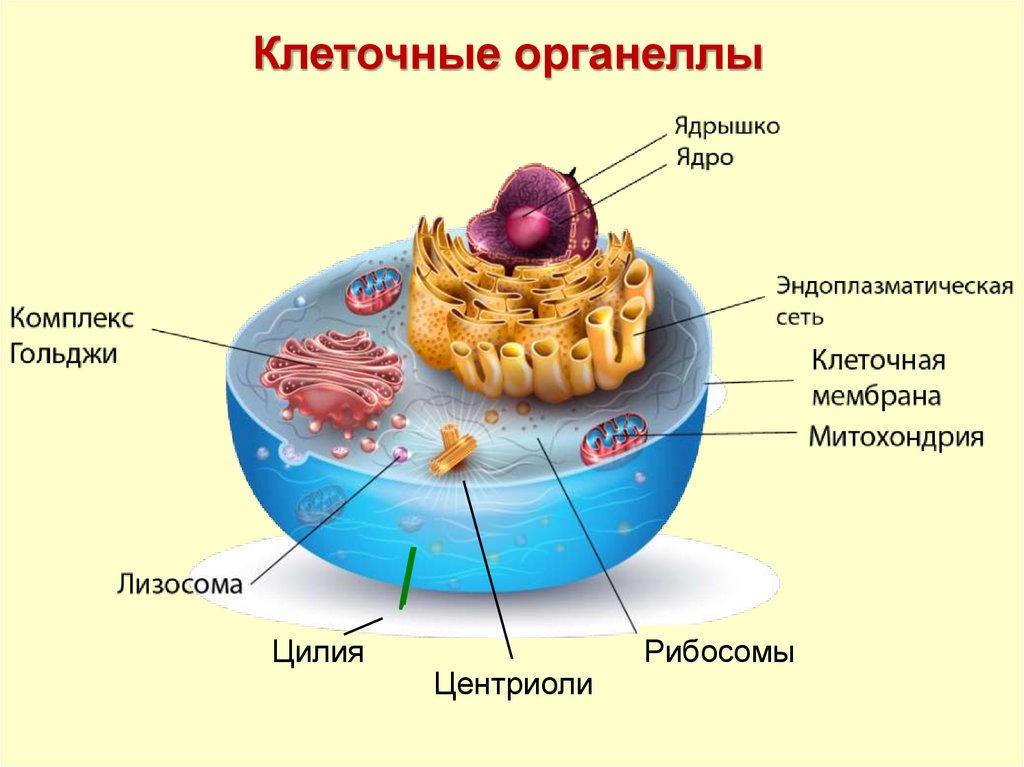
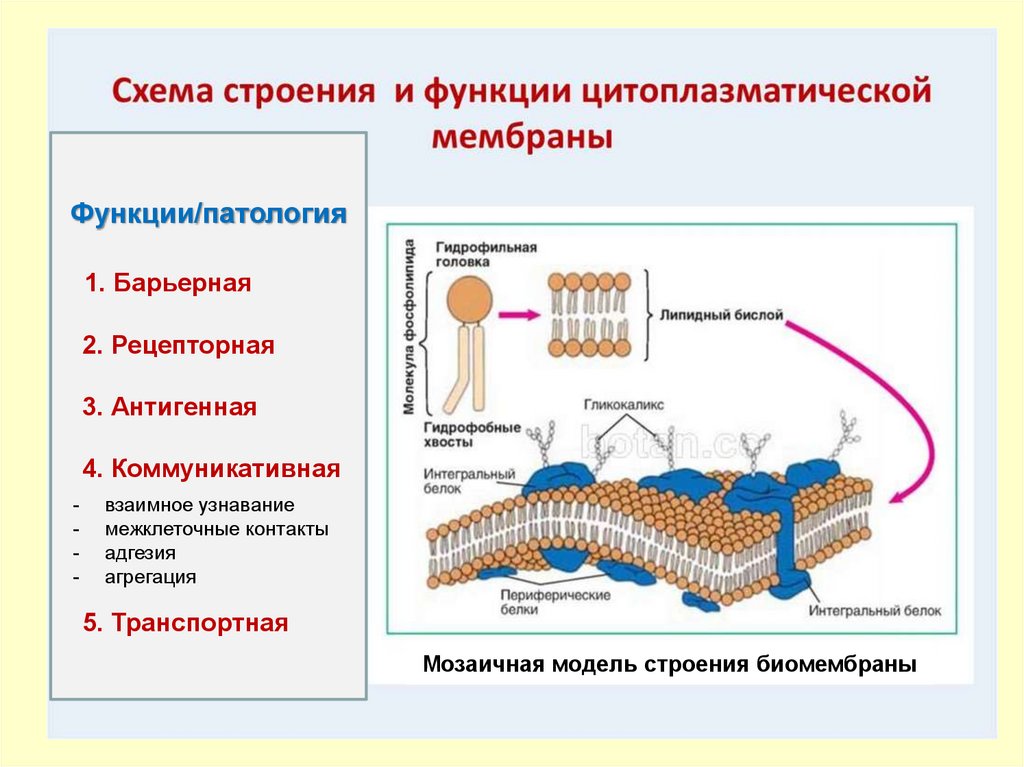
Структура наружной цитоплазматическоймембраны
5.
Функции/патология1. Барьерная
2. Рецепторная
3. Антигенная
4.4. Коммуникативная
Антигенная
взаимное узнавание
5.-- Коммуникативная
межклеточные контакты
-
адгезия
агрегация
5. Транспортная
Мозаичная модель строения биомембраны
6.
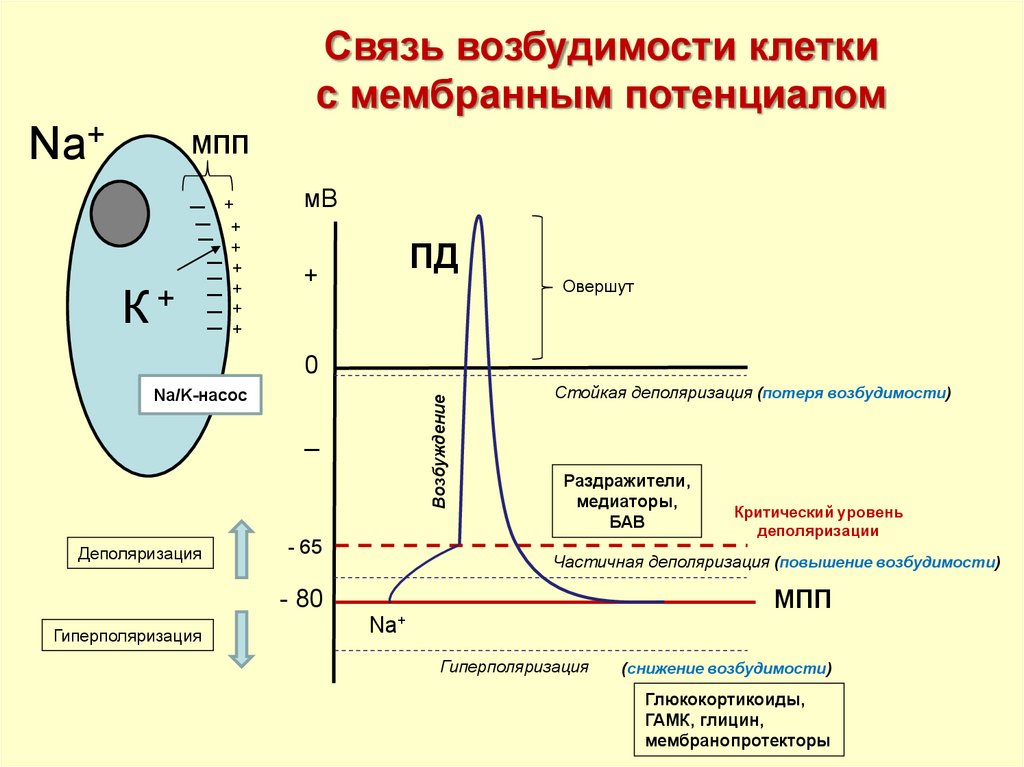
Связь возбудимости клеткис мембранным потенциалом
Na+
МПП
К
_ +
_ +
_
_+
_ +
_
+ _ ++
_ +
мВ
ПД
+
Овершут
0
Возбуждение
Na/K-насос
̶
Деполяризация
- 65
Стойкая деполяризация (потеря возбудимости)
Раздражители,
медиаторы,
БАВ
Частичная деполяризация (повышение возбудимости)
МПП
- 80
Гиперполяризация
Критический уровень
деполяризации
Na+
Гиперполяризация
(снижение возбудимости)
Глюкокортикоиды,
ГАМК, глицин,
мембранопротекторы
7.
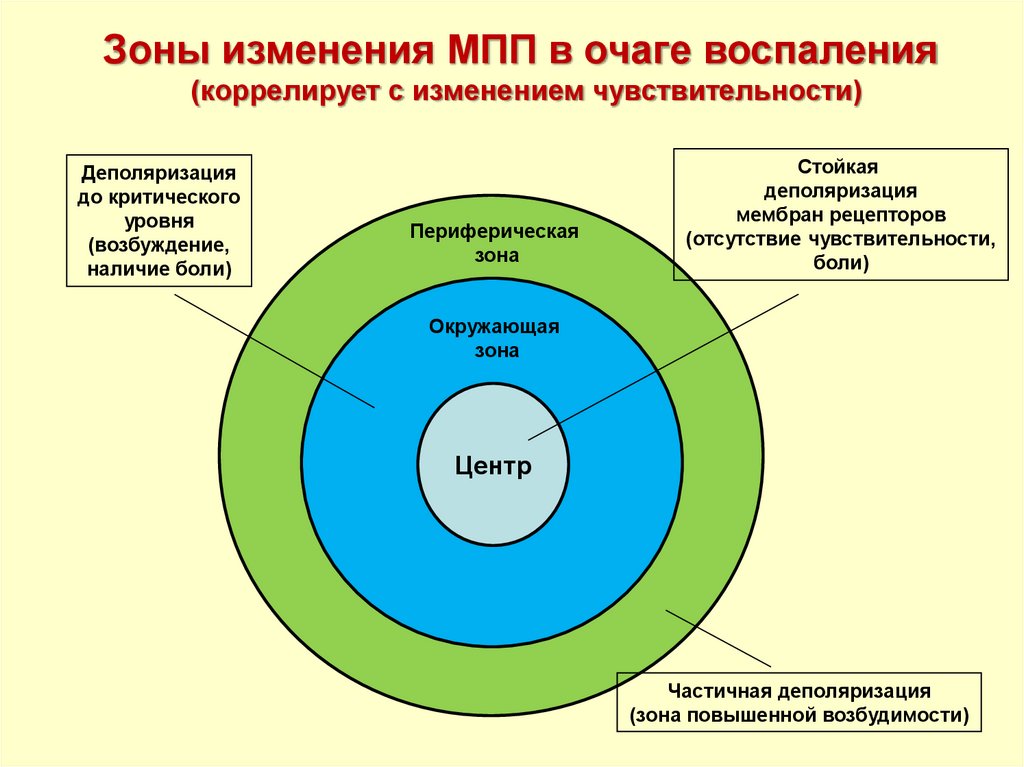
Зоны изменения МПП в очаге воспаления(коррелирует с изменением чувствительности)
Деполяризация
до критического
уровня
(возбуждение,
наличие боли)
Периферическая
зона
Стойкая
деполяризация
мембран рецепторов
(отсутствие чувствительности,
боли)
Окружающая
зона
0
Центр
Частичная деполяризация
(зона повышенной возбудимости)
8.
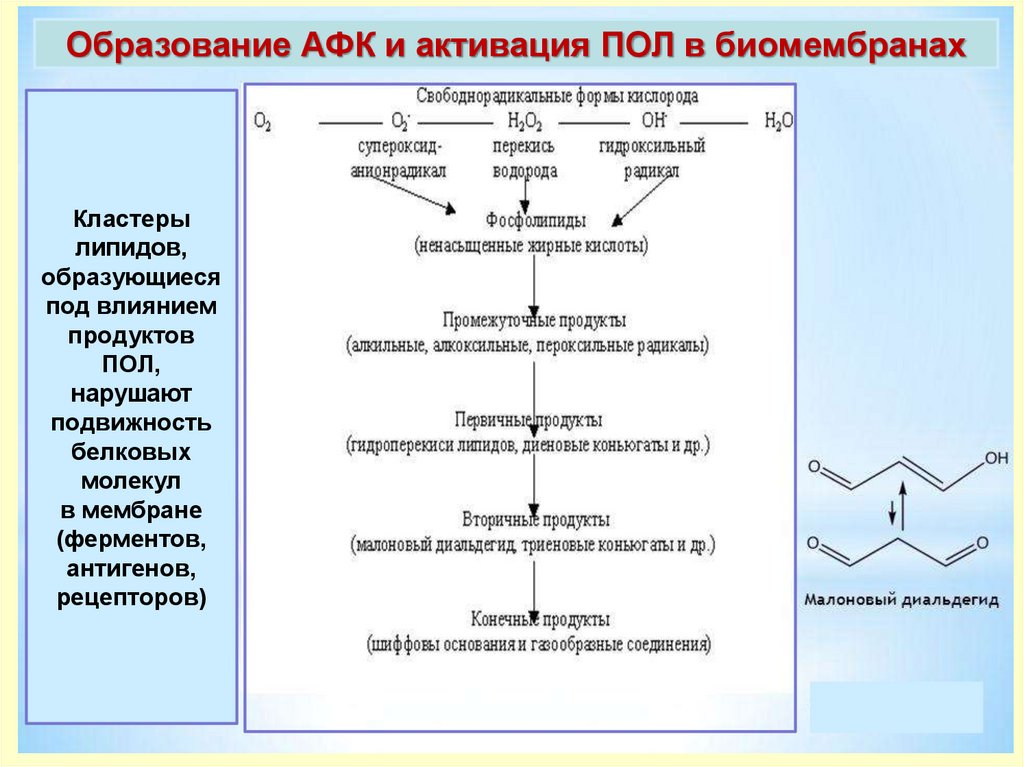
Образование АФК и активация ПОЛ в биомембранахКластеры
липидов,
образующиеся
под влиянием
продуктов
ПОЛ,
нарушают
подвижность
белковых
молекул
в мембране
(ферментов,
антигенов,
рецепторов)
9.
Регуляция процессов ПОЛ• Восстановленный глютатион
10.
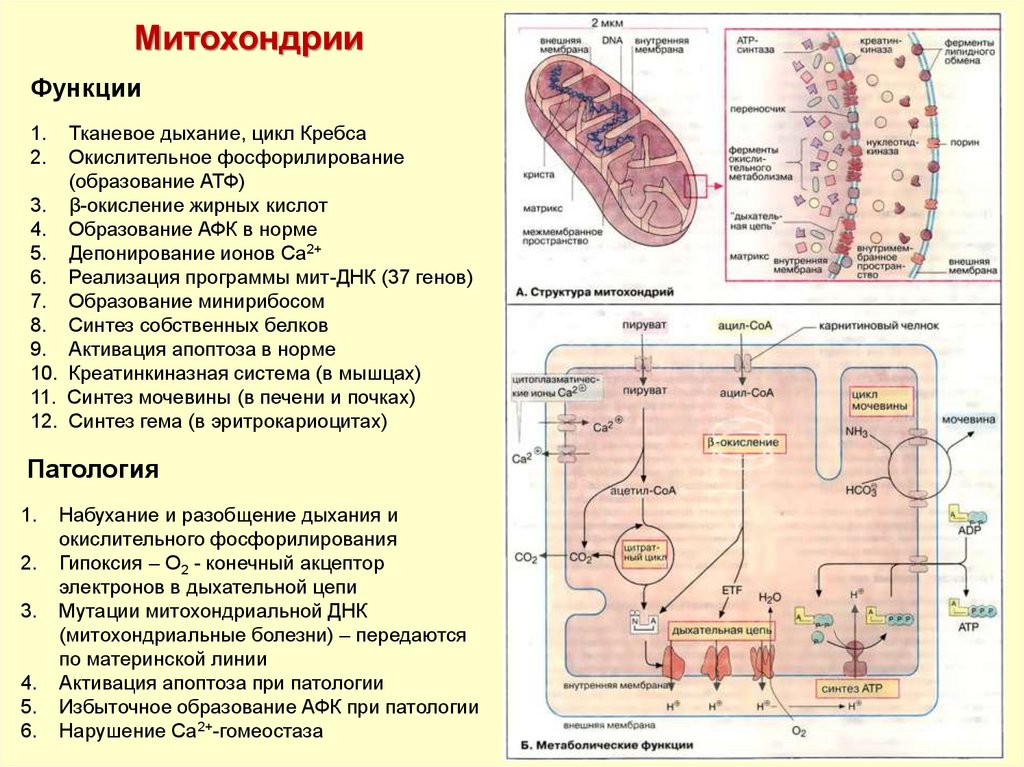
МитохондрииФункции
Тканевое дыхание, цикл Кребса
Окислительное фосфорилирование
(образование АТФ)
3. β-окисление жирных кислот
4. Образование АФК в норме
5. Депонирование ионов Са2+
6. Реализация программы мит-ДНК (37 генов)
7. Образование минирибосом
8. Синтез собственных белков
9. Активация апоптоза в норме
10. Креатинкиназная система (в мышцах)
11. Синтез мочевины (в печени и почках)
12. Синтез гема (в эритрокариоцитах)
1.
2.
Патология
1.
2.
3.
4.
5.
6.
Набухание и разобщение дыхания и
окислительного фосфорилирования
Гипоксия – О2 - конечный акцептор
электронов в дыхательной цепи
Мутации митохондриальной ДНК
(митохондриальные болезни) – передаются
по материнской линии
Активация апоптоза при патологии
Избыточное образование АФК при патологии
Нарушение Са2+-гомеостаза
11.
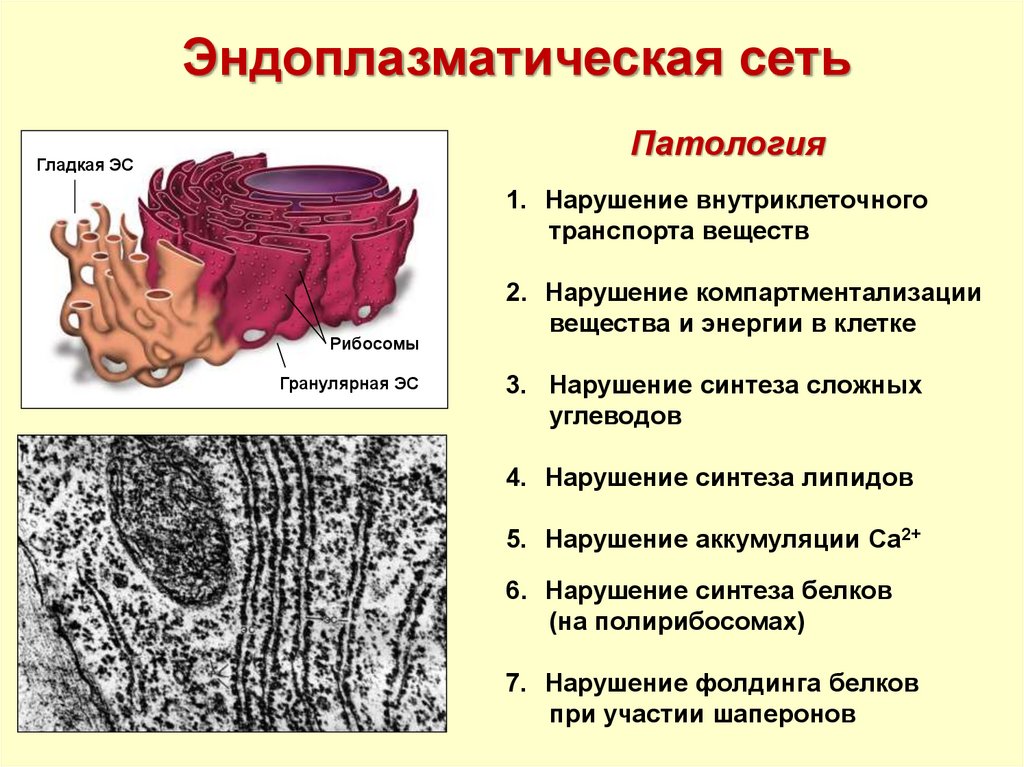
Эндоплазматическая сетьПатология
Гладкая ЭС
1. Нарушение внутриклеточного
транспорта веществ
Рибосомы
Гранулярная ЭС
2. Нарушение компартментализации
вещества и энергии в клетке
3. Нарушение синтеза сложных
углеводов
4. Нарушение синтеза липидов
5. Нарушение аккумуляции Са2+
6. Нарушение синтеза белков
(на полирибосомах)
7. Нарушение фолдинга белков
при участии шаперонов
12.
ЛизосомыПокрытые однослойной мембраной «мешки с ферментами».
Содержат более 60 гидролаз.
При неконтролируемом повышении проницаемости мембраны лизосом –
аутолиз клетки (некроз ткани).
В патологии лизосом нарушаются следующие функции:
1. Внутриклеточное пищеварение
2. Разрушение (переваривание) фагоцитированных объектов
3. Процессы внутриклеточной репаративной регенерации
4. Процессы лимитированного протеолиза (активации БАВ)
5. Уничтожение белков с нарушенным фолдингом
Стабилизируют мембрану лизосом - глюкокортикоиды
(противовоспалительное действие).
Лабилизируют мембрану лизосом – любая альтерация, гипоксия, ацидоз.
Лизосомальные болезни (болезни накопления) – наследственные
заболевания, связанные с недостаточностью какого-то из лизосомальных
ферментов вследствие генетического дефекта (гликогенозы, мукополисахаридозы).
13.
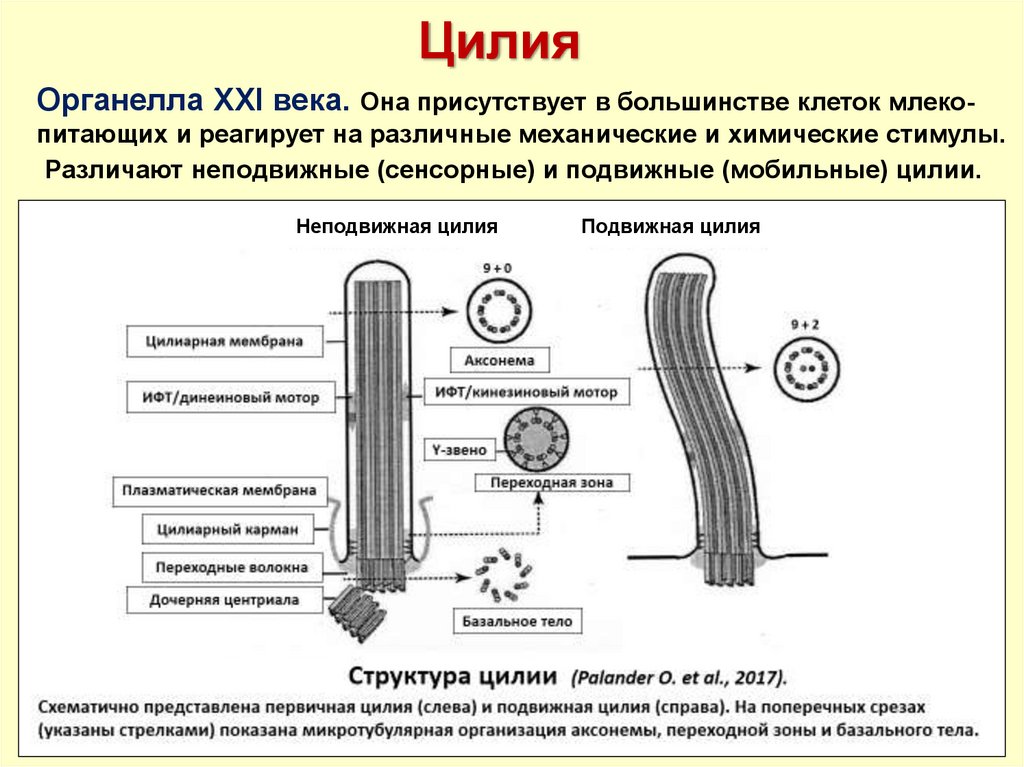
ЦилияОрганелла XXI века. Она присутствует в большинстве клеток млекопитающих и реагирует на различные механические и химические стимулы.
Различают неподвижные (сенсорные) и подвижные (мобильные) цилии.
Неподвижная цилия
Подвижная цилия
14.
Функции цилииНеподвижные реснички существуют на поверхности всех клеток в
единственном экземпляре (monocilia). Они функционируют в качестве
сенсорных антенн и улавливают звук, свет, запах, движение жидкости,
функционируют как механо-, хемо- и осморецепторы. Они обнаружены
на сосудистом эндотелии, в сердце, почечных канальцах и т.д. С верхушки
цилии могут освобождаться внеклеточные везикулы (эктосомы), которые
выполняют сигнальные функции.
Подвижные цилии существуют в виде нескольких ресничек (multicilia)
и присутствует на специализированных клетках. Они расположены на
клетках верхних и нижних дыхательных путей (мукоцилиарная система),
среднего уха, желудочков мозга, фаллопиевых труб и сперматозоидов.
В патологии – цилиопатии (1 на 20 000 новорожденных). Известно уже
более 127 цилиопатий. Список цилиопатий будет быстро расти, учитывая
наличие около 1000 цилиарных генов.
15.
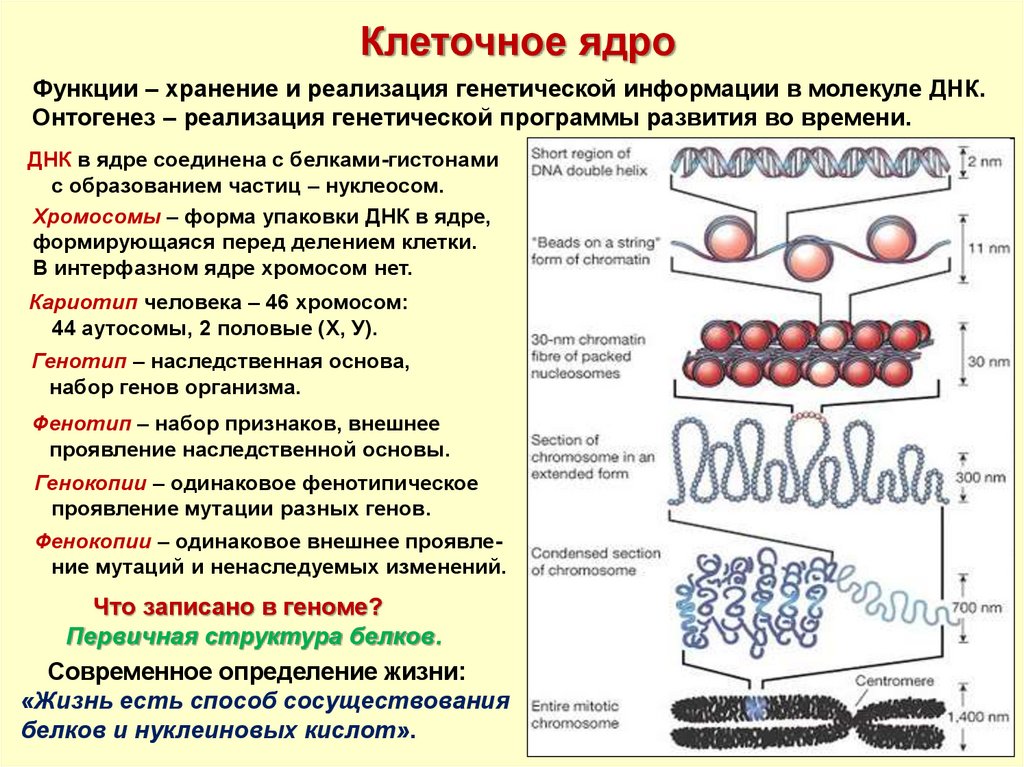
Клеточное ядроФункции – хранение и реализация генетической информации в молекуле ДНК.
Онтогенез – реализация генетической программы развития во времени.
ДНК в ядре соединена с белками-гистонами
с образованием частиц – нуклеосом.
Хромосомы – форма упаковки ДНК в ядре,
формирующаяся перед делением клетки.
В интерфазном ядре хромосом нет.
Кариотип человека – 46 хромосом:
44 аутосомы, 2 половые (Х, У).
Генотип – наследственная основа,
набор генов организма.
Фенотип – набор признаков, внешнее
проявление наследственной основы.
Генокопии – одинаковое фенотипическое
проявление мутации разных генов.
Фенокопии – одинаковое внешнее проявление мутаций и ненаследуемых изменений.
Что записано в геноме?
Первичная структура белков.
Современное определение жизни:
«Жизнь есть способ сосуществования
белков и нуклеиновых кислот».
16.
МутацииМутация – изменение структуры ДНК, незапрограммированное
в геноме. Последняя добавка – поскольку есть транспозоны
и мигрирующие нуклуотидные последовательности.
Геномные – полиплоидия, анеуплоидия
Хромосомные – делеция, дубликация, инверсия, транслокация
Генные – выпадения, вставки, замены оснований (транзиции,
трансверсии)
Жесткие, со «сдвигом рамки»
Мягкие
Мутации в соматических клетках - ведут к мозаицизму, канцерогенезу,
активации клеточного старения, аутоиммунным заболеваниям.
Мутации в половых клетках - ведут к развитию
наследственного заболевания (генетический дефект, который
проявляется в любых условиях среды), или
наследственного предрасположения (генетический дефект,
который проявляется только в определенных условиях среды).
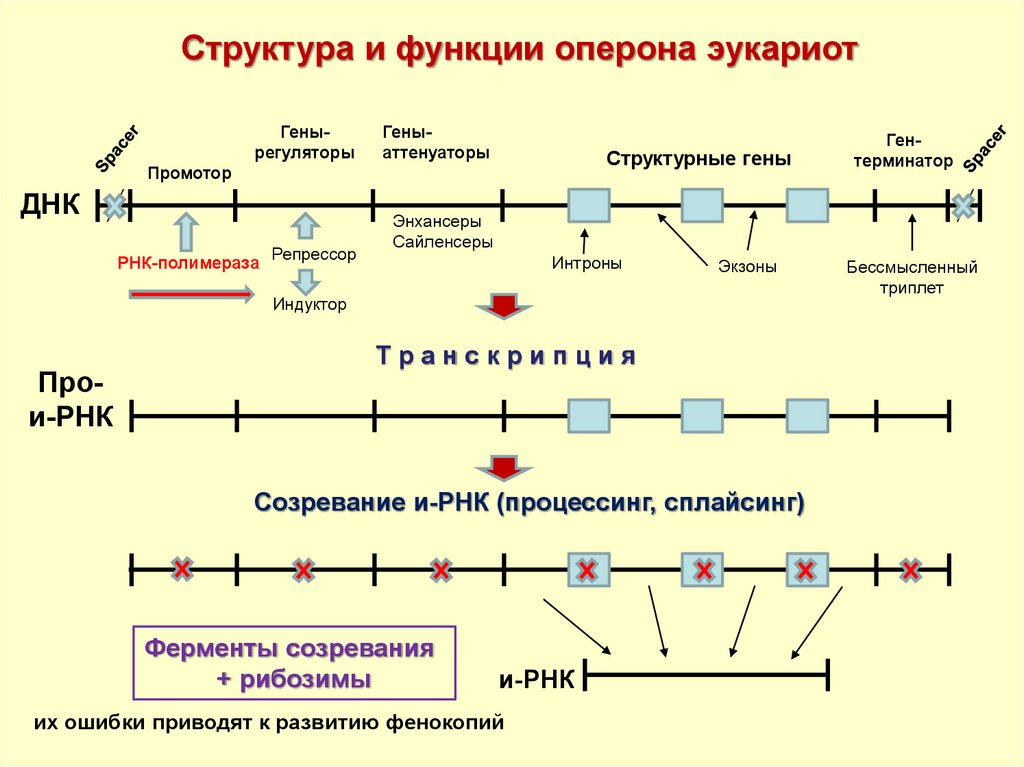
17.
Структура и функции оперона эукариотГенырегуляторы
Геныаттенуаторы
Структурные гены
Промотор
ДНК
РНК-полимераза
Репрессор
Энхансеры
Сайленсеры
Интроны
Экзоны
Индуктор
Прои-РНК
Гентерминатор
Транскрипция
Созревание и-РНК (процессинг, сплайсинг)
Ферменты созревания
+ рибозимы
и-РНК
их ошибки приводят к развитию фенокопий
Бессмысленный
триплет
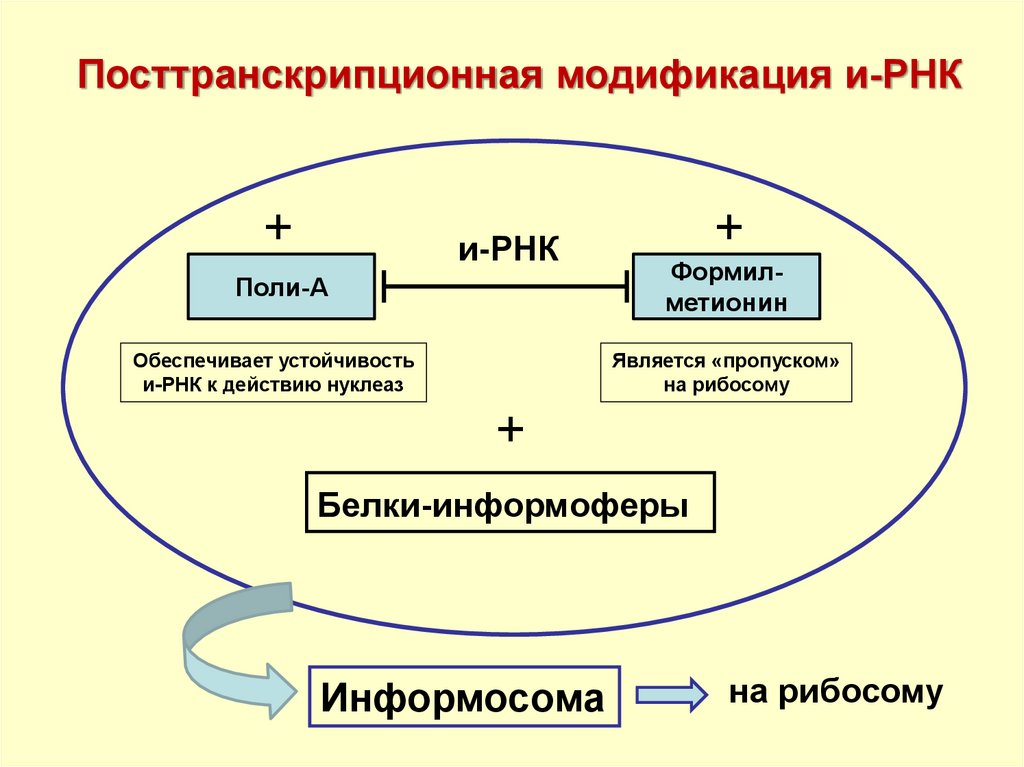
18.
Посттранскрипционная модификация и-РНК+
и-РНК
+
Поли-А
Формилметионин
Обеспечивает устойчивость
и-РНК к действию нуклеаз
Является «пропуском»
на рибосому
+
Белки-информоферы
Информосома
на рибосому
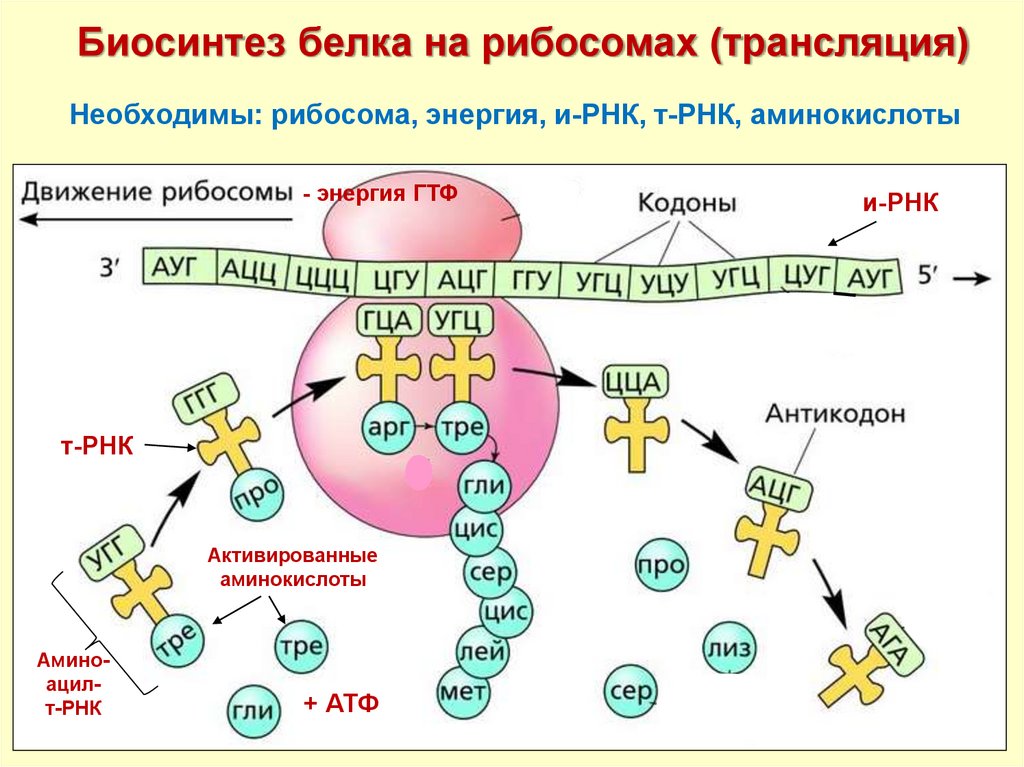
19.
Биосинтез белка на рибосомах (трансляция)Необходимы: рибосома, энергия, и-РНК, т-РНК, аминокислоты
- энергия ГТФ
т-РНК
Активированные
аминокислоты
Аминоацилт-РНК
+ АТФ
и-РНК
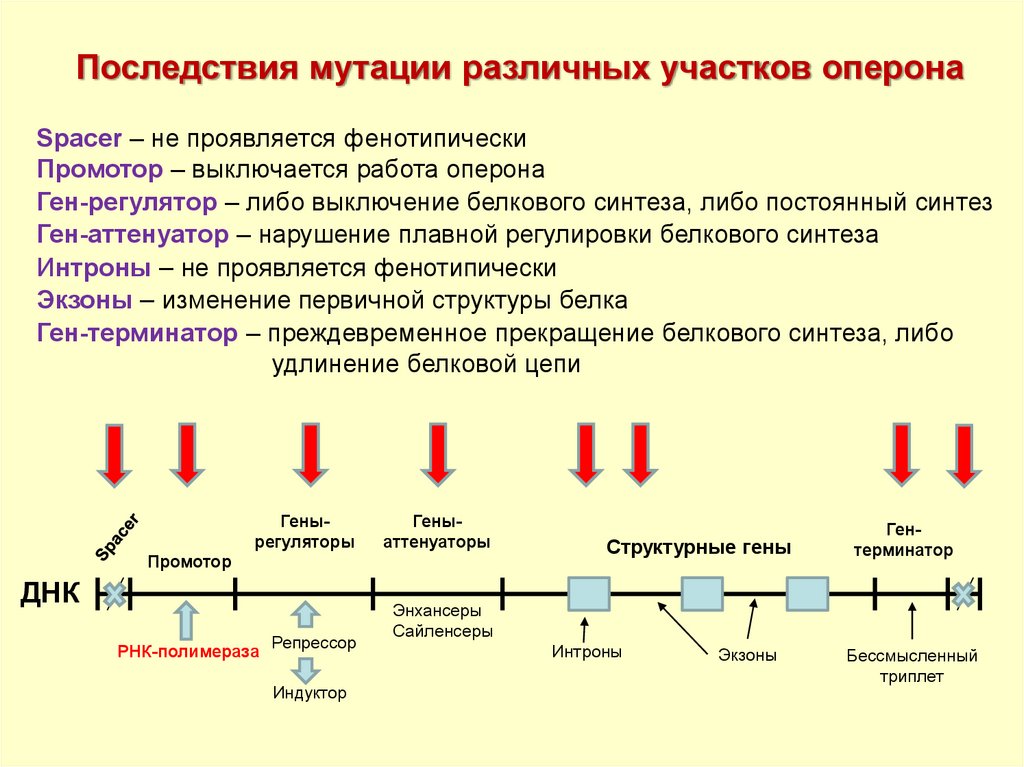
20.
Последствия мутации различных участков оперонаSpacer – не проявляется фенотипически
Промотор – выключается работа оперона
Ген-регулятор – либо выключение белкового синтеза, либо постоянный синтез
Ген-аттенуатор – нарушение плавной регулировки белкового синтеза
Интроны – не проявляется фенотипически
Экзоны – изменение первичной структуры белка
Ген-терминатор – преждевременное прекращение белкового синтеза, либо
удлинение белковой цепи
Генырегуляторы
Геныаттенуаторы
Промотор
ДНК
РНК-полимераза
Репрессор
Индуктор
Структурные гены
Гентерминатор
Энхансеры
Сайленсеры
Интроны
Экзоны
Бессмысленный
триплет
21.
Некоторые нерешёные вопросы1. Непонятна «избыточность» ДНК в геноме. Для кодирования всех белков
и регуляторов нужно лишь 5% ДНК. Зачем нужны остальные 95%?
2. Излишняя шумиха поднята вокруг якобы расшифровки генома человека.
Но мы узнали только последовательность нуклеотидов в цепи ДНК.
Принцип работы большинства участков генома пока остается неясным.
3. Первичная структура белка лишь создает основу для последующей
модификации его активности с участием протеинкиназ, гормонов и т.п.
Неясно, как координируются различные уровни регуляции.
4. Неясна организация обратной связи между белком и ДНК.
Резюмируя вышеизложенное, можно заключить, что
«о работе генома человека мы сегодня по-прежнему
ничего не знаем, … но на более высоком уровне».
22.
Спасибо за внимание!23.
Механизмы канцерогенезаБрилль
Игорь Ефимович
Профессор
кафедры патофизиологии им. акад. А.А. Богомольца
доктор медицинских наук, академик WABT (UNESCO),
академик РАЕ, академик ЛАН Российской Федерации,
Соросовский профессор
24.
СтатистикаРак занимает второе место как причина смертности населения
в экономически развитых странах после сердечно-сосудистых
заболеваний.
В России рак ежегодно уносит жизни более 300 тысяч
пациентов.
В последние годы отмечаются две тревожные тенденции:
1. увеличение частоты рака
2. омоложение рака
25.
Опухоль – это избыточное, некоординируемоеорганизмом, потенциально беспредельное
разрастание ткани, состоящей из качественно
изменённых клеток, характеризующихся
морфологическим, биохимическим
и функциональным атипизмом.
Атипизм – нетипичность, необычность.
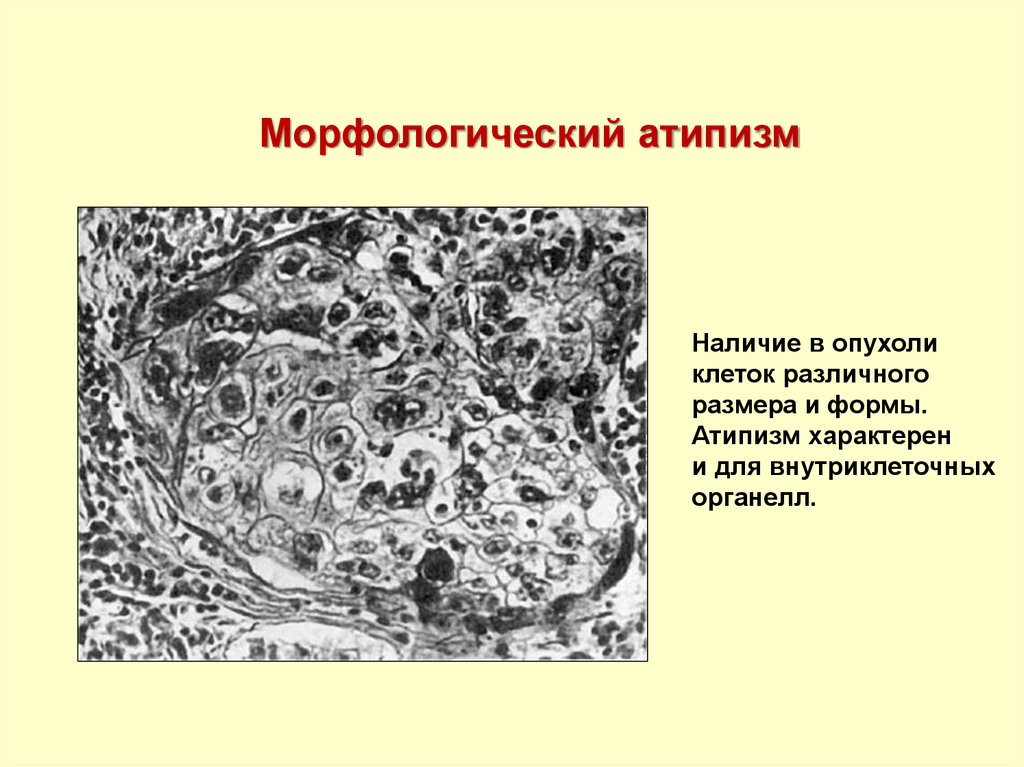
26.
Морфологический атипизмНаличие в опухоли
клеток различного
размера и формы.
Атипизм характерен
и для внутриклеточных
органелл.
27.
Биохимический атипизм(углеводный метаболизм)
1. Раковая клетка – ловушка глюкозы (ключевые
ферменты гликолиза вынесены на наружную цитоплазматическую
мембрану)
2. Отсутствие эффекта Пастера – дыхание не тормозит
гликолиз. Наличие эффекта Крэбтри – гликолиз тормозит
дыхание.
3. Активирован гликолиз анаэробный обмен
метаболический ацидоз
4. Гексокиназа не регулируется гормонами
(автономность)
5. Пентозный цикл не регулируется эстрогенами
(автономность)
28.
Биохимический атипизм(белковый метаболизм)
1. Опухолевая клетка – ловушка азота (аминокислот)
2. Характерна анаболическая направленность обмена
(т.е. преобладает синтез белка)
3. Синтез белка происходит преимущественно для
внутренних нужд клетки
4. Интенсивно синтезируются аминокислоты
29.
Биохимический атипизм(жировой метаболизм)
1. Раковая клетка – ловушка жиров
2. Использует липиды для построения органелл
и клеточных мембран
30.
Биохимический атипизм(обмен нуклеиновых кислот)
1. Высока активность ДНК- и РНК-полимеразы
2. Низка активность нуклеаз
3. Интенсивно синтезируются азотистые основания
(пурины и пиримидины)
31.
Поведенческий (функциональный) атипизм1. Бессмертие (иммортализация) раковых клеток
Учеными замечено, что нормальные дифференцированные
клетки в культуре долго не живут. Через некоторое время
отмечаются признаки старения и культура погибает.
Закон Хейфлика – в генетическом аппарате каждой
нормальной дифференцированной клетки
запрограммировано определенное число делений.
Когда клетка превышает этот предел, включаются
механизмы апоптоза и клетка погибает.
Для фибробластов ограничение Хейфлика ~ 50 делений.
32.
Пример бессмертия раковых клетокКультура раковых клеток HeLa.
Она была получена в 1951 году в США из раковой
опухоли шейки матки пациентки по имени Генриетта
Лакс.
Эта культура уже 70 лет прекрасно растёт во многих
лабораториях мира.
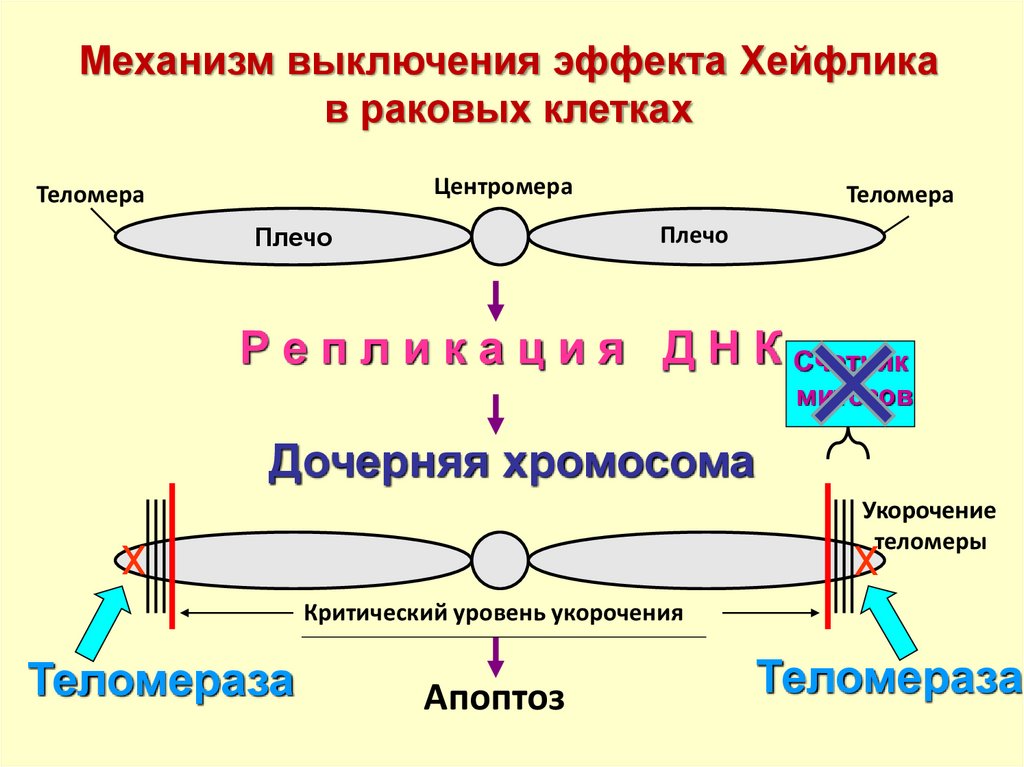
33.
Механизм выключения эффекта Хейфликав раковых клетках
Центромера
Теломера
Плечо
Теломера
Плечо
Р е п л и к а ц и я Д Н К Счетчик
митозов
Дочерняя хромосома
Укорочение
теломеры
Х
Х
Критический уровень укорочения
Теломераза
Апоптоз
Теломераза
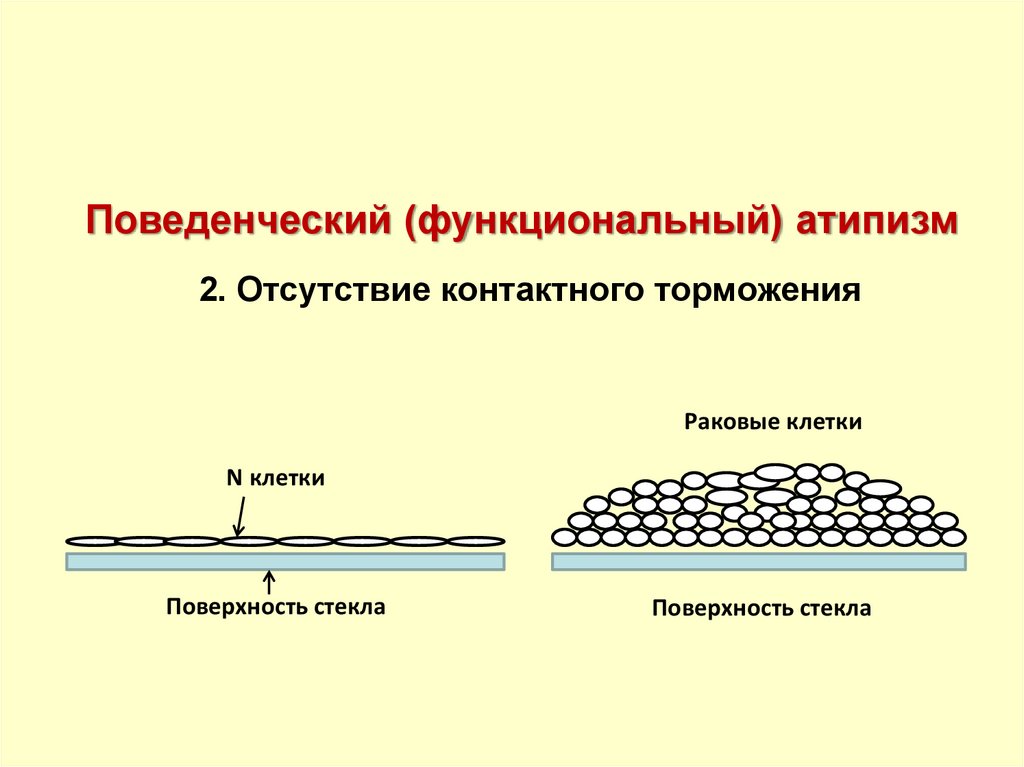
34.
Поведенческий (функциональный) атипизм2. Отсутствие контактного торможения
Раковые клетки
N клетки
Поверхность стекла
Поверхность стекла
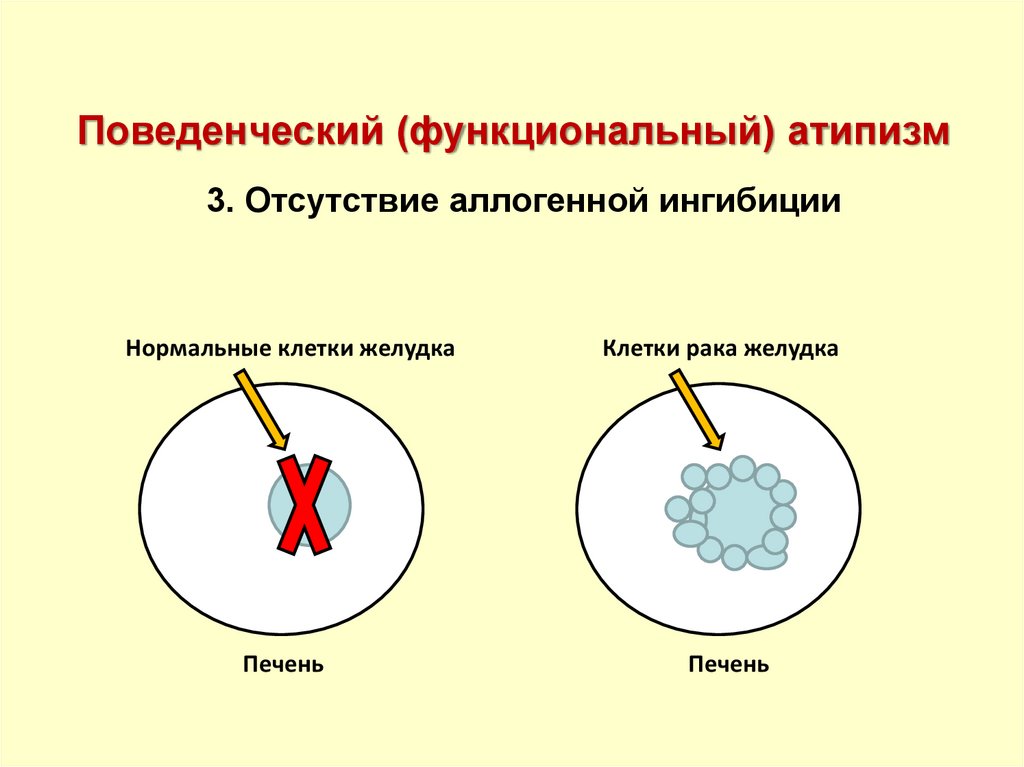
35.
Поведенческий (функциональный) атипизм3. Отсутствие аллогенной ингибиции
Нормальные клетки желудка
Клетки рака желудка
Печень
Печень
36.
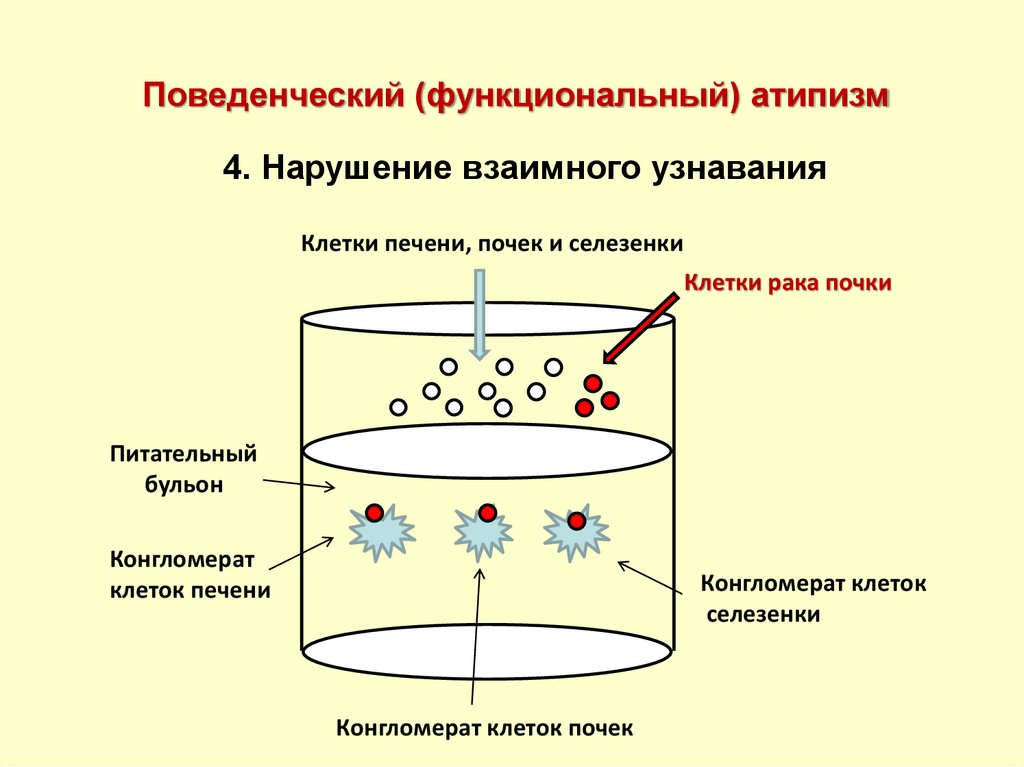
Поведенческий (функциональный) атипизм4. Нарушение взаимного узнавания
Клетки печени, почек и селезенки
Клетки рака почки
Питательный
бульон
Конгломерат
клеток печени
Конгломерат клеток
селезенки
Конгломерат клеток почек
37.
Вывод:раковые клетки неразборчивы
в связях (межклеточных)
38.
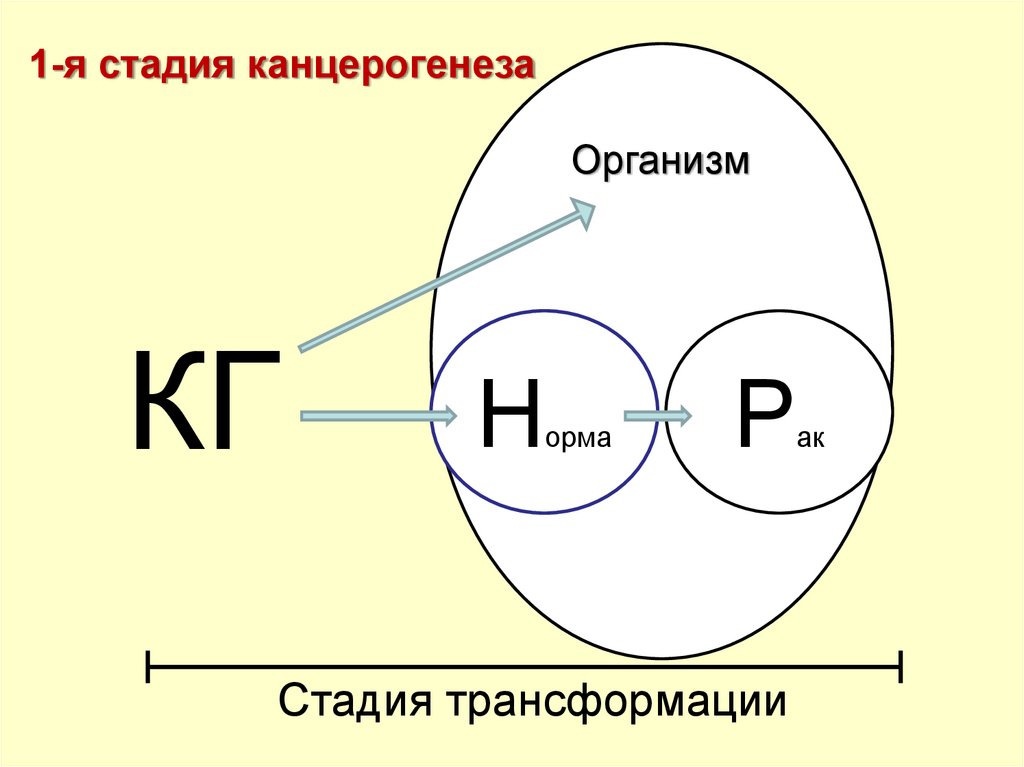
Стадии канцерогенеза39.
1-я стадия канцерогенезаОрганизм
КГ
Н
орма
Р
Стадия трансформации
ак
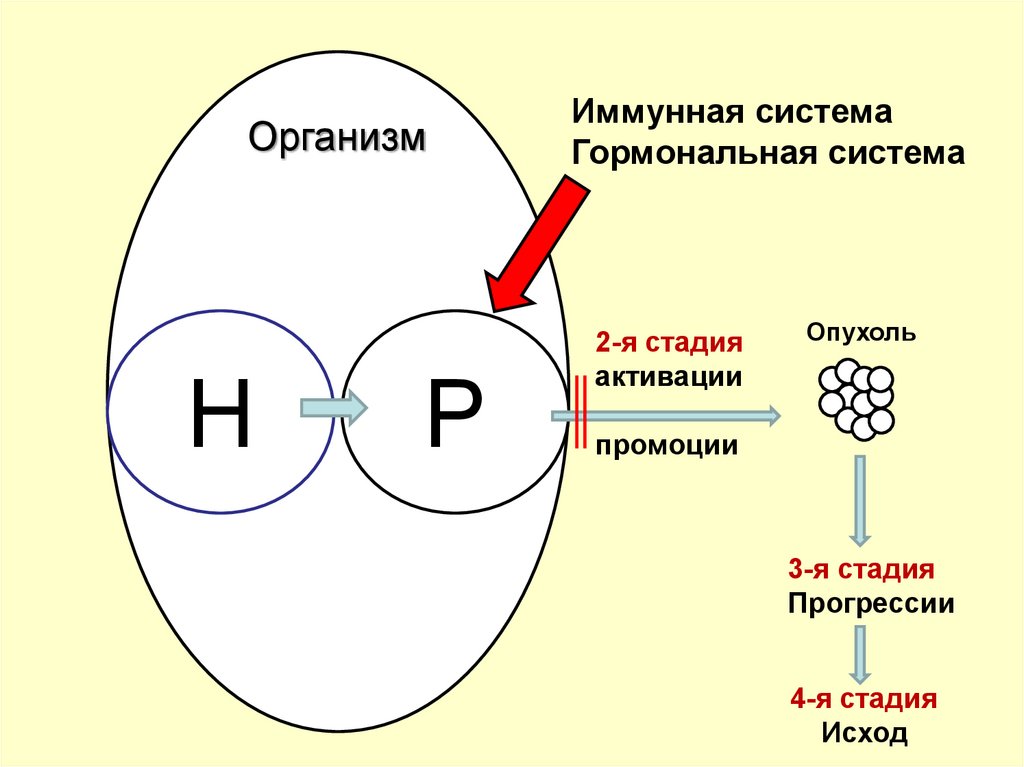
40.
ОрганизмН
Р
Иммунная система
Гормональная система
2-я стадия
активации
Опухоль
промоции
3-я стадия
Прогрессии
4-я стадия
Исход
41.
Канцерогены – агенты, вызывающиепревращение нормальной клетки в
раковую.
Классификация канцерогенов
1. Физические
2. Химические
3. Биологические
4. Социальные (?)
42.
Физические канцерогены1. Ионизирующее излучение
2. Ультрафиолетовая радиация
3. Пластмассовый канцерогенез
43.
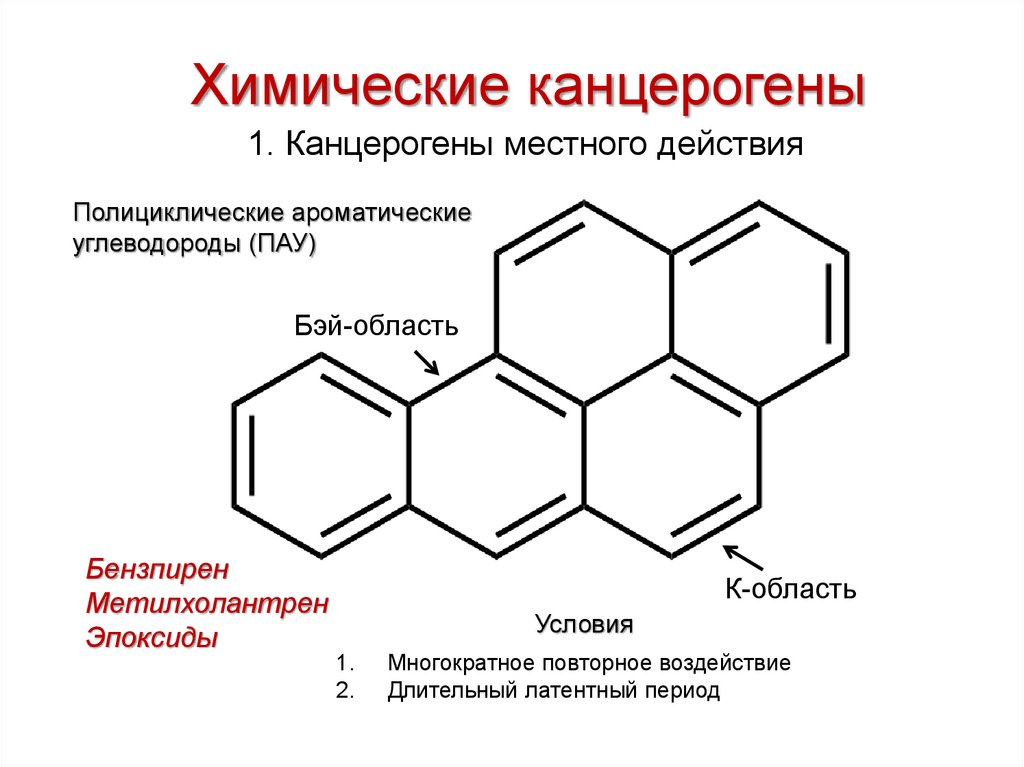
Химические канцерогены1. Канцерогены местного действия
Полициклические ароматические
углеводороды (ПАУ)
Бэй-область
Бензпирен
Метилхолантрен
Эпоксиды
К-область
Условия
1.
2.
Многократное повторное воздействие
Длительный латентный период
44.
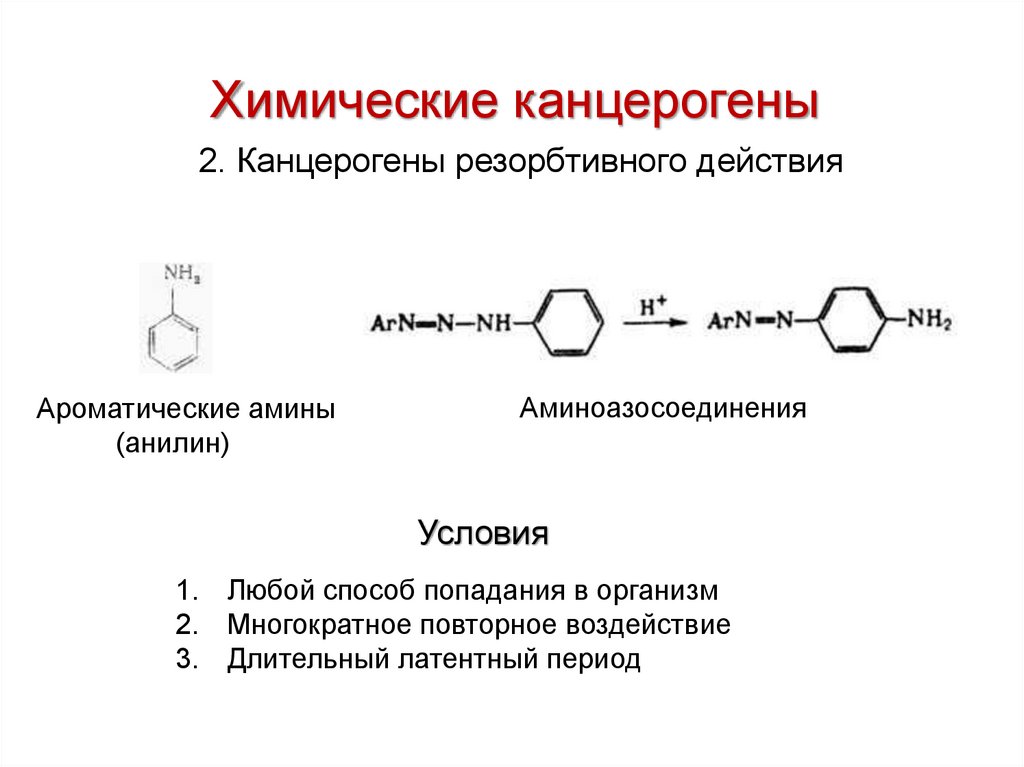
Химические канцерогены2. Канцерогены резорбтивного действия
Ароматические амины
(анилин)
Аминоазосоединения
Условия
1. Любой способ попадания в организм
2. Многократное повторное воздействие
3. Длительный латентный период
45.
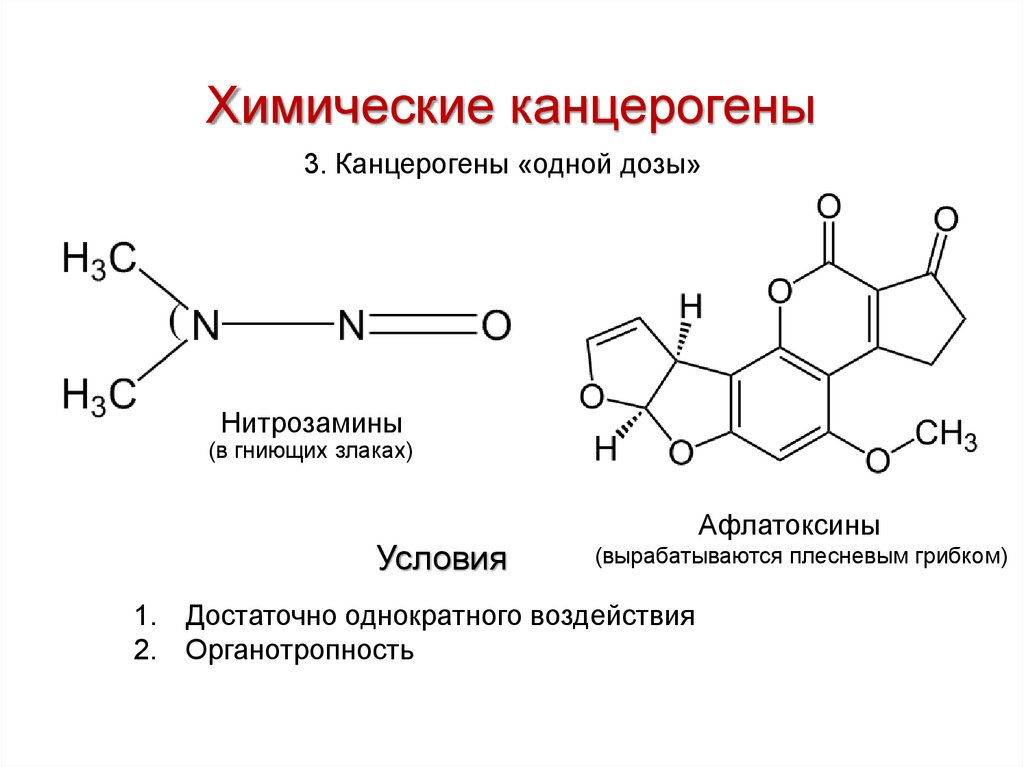
Химические канцерогены3. Канцерогены «одной дозы»
Нитрозамины
(в гниющих злаках)
Условия
Афлатоксины
(вырабатываются плесневым грибком)
1. Достаточно однократного воздействия
2. Органотропность
46.
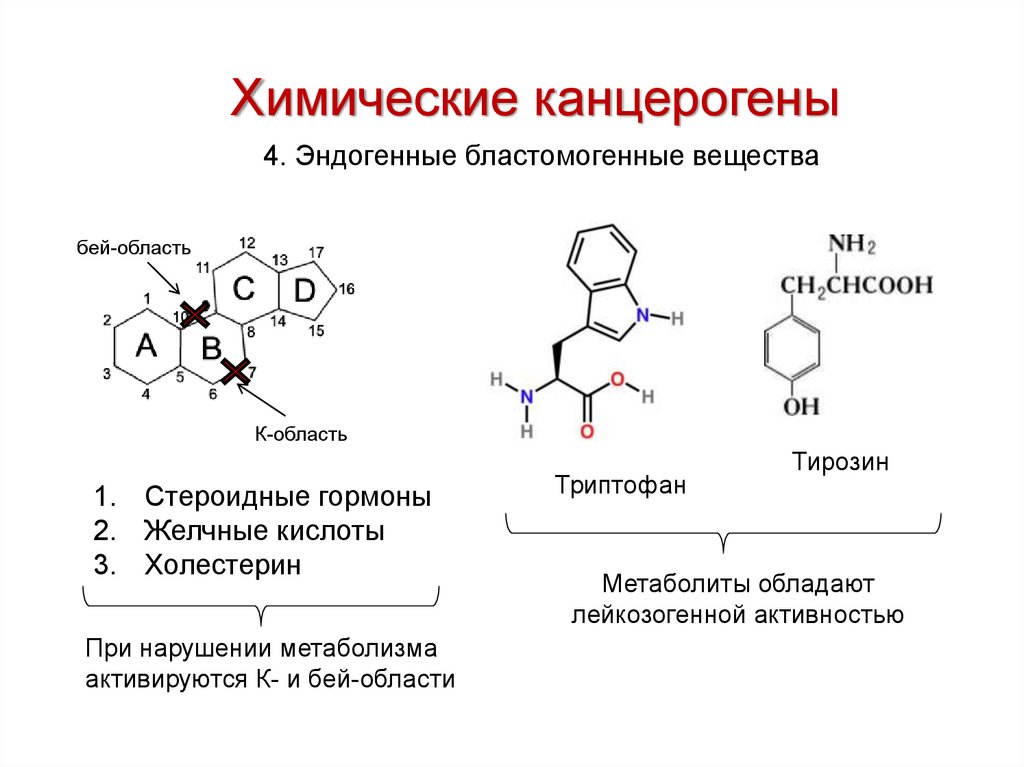
Химические канцерогены4. Эндогенные бластомогенные вещества
бей-область
К-область
1. Стероидные гормоны
2. Желчные кислоты
3. Холестерин
При нарушении метаболизма
активируются К- и бей-области
Триптофан
Тирозин
Метаболиты обладают
лейкозогенной активностью
47.
Биологические канцерогеныОнкогенные вирусы животных
РНК-содержащие (ретровирусы, онкоРНАвирусы) – более 100 типов
ДНК-содержащие вирусы – около 50 типов
1. Вирус саркомы Рауса у кур
2. Вирус саркомы Шоупа у кроликов
3. Вирус Биттнера – вызывает рак молочной железы у мышей
Особенности вирусного канцерогенеза у животных
1. Возможность прямого заражения – контагиозность
2. Возможность вертикальной передачи рака от родителей через
половые клетки
48.
Биологические канцерогеныОнкогенные вирусы человека
I. ДНК-онкогенные вирусы
Вирус простого герпеса 2 типа (HHV-2) – рак шейки матки
Вирус простого герпеса 8 типа (HHV-8) – саркома Капоши
Вирус Эпштейна-Барр – лимфома Беркитта, лимфома Ходжкина
Вирус папилломы человека – бородавки
II. РНК-онкогенные вирусы (онкорнавирусы)
НТLV-1 – Т-клеточный лейкоз
НТLV-2 – волосовидный лейкоз
Автор вирусо-генетической теории рака
– академик Лев Александрович Зильбер
Возникают закономерные вопросы:
1. вирусные формы рака у человека заразны или нет?
2. почему вирусный грипп заразен, а рак нет?
49.
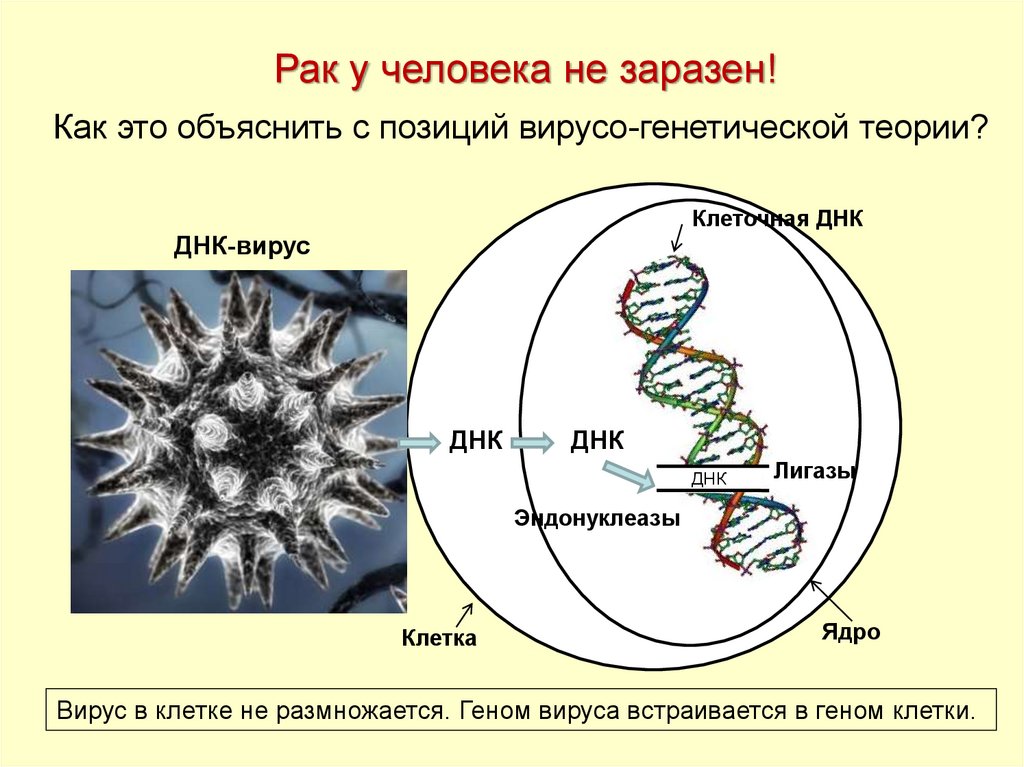
Рак у человека не заразен!Как это объяснить с позиций вирусо-генетической теории?
Клеточная ДНК
ДНК-вирус
ДНК
ДНК
ДНК
ДНК
Лигазы
Эндонуклеазы
Клетка
Ядро
Вирус в клетке не размножается. Геном вируса встраивается в геном клетки.
50.
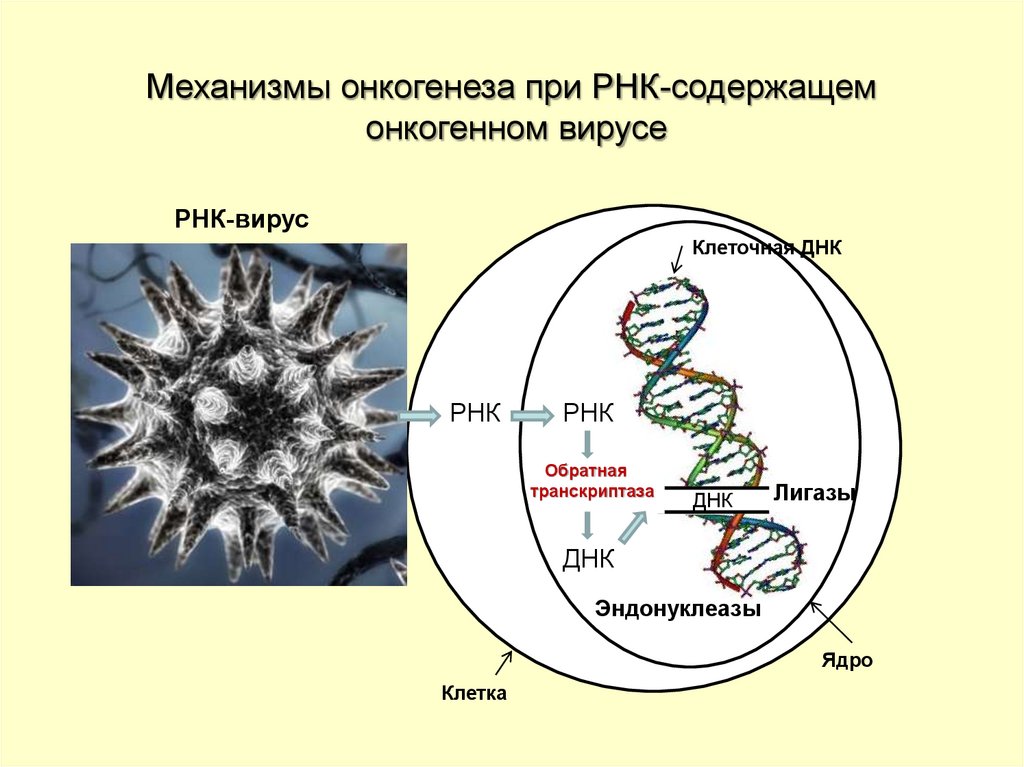
Механизмы онкогенеза при РНК-содержащемонкогенном вирусе
РНК-вирус
Клеточная ДНК
РНК
РНК
Обратная
транскриптаза
ДНКДНК
Лигазы
ДНК
Эндонуклеазы
Ядро
Клетка
51.
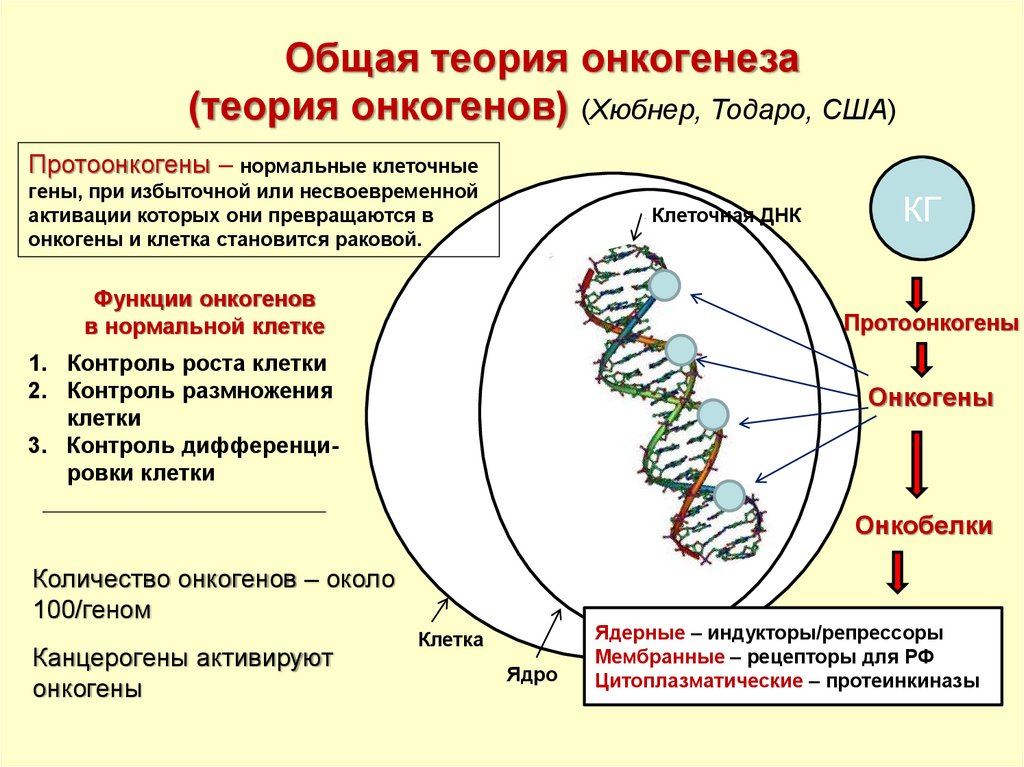
Общая теория онкогенеза(теория онкогенов) (Хюбнер, Тодаро, США)
Протоонкогены – нормальные клеточные
гены, при избыточной или несвоевременной
активации которых они превращаются в
онкогены и клетка становится раковой.
Клеточная ДНК
Функции онкогенов
в нормальной клетке
КГ
Протоонкогены
1. Контроль роста клетки
2. Контроль размножения
клетки
3. Контроль дифференцировки клетки
Онкогены
Онкобелки
Количество онкогенов – около
100/геном
Канцерогены активируют
онкогены
Клетка
Ядро
Ядерные – индукторы/репрессоры
Мембранные – рецепторы для РФ
Цитоплазматические – протеинкиназы
52.
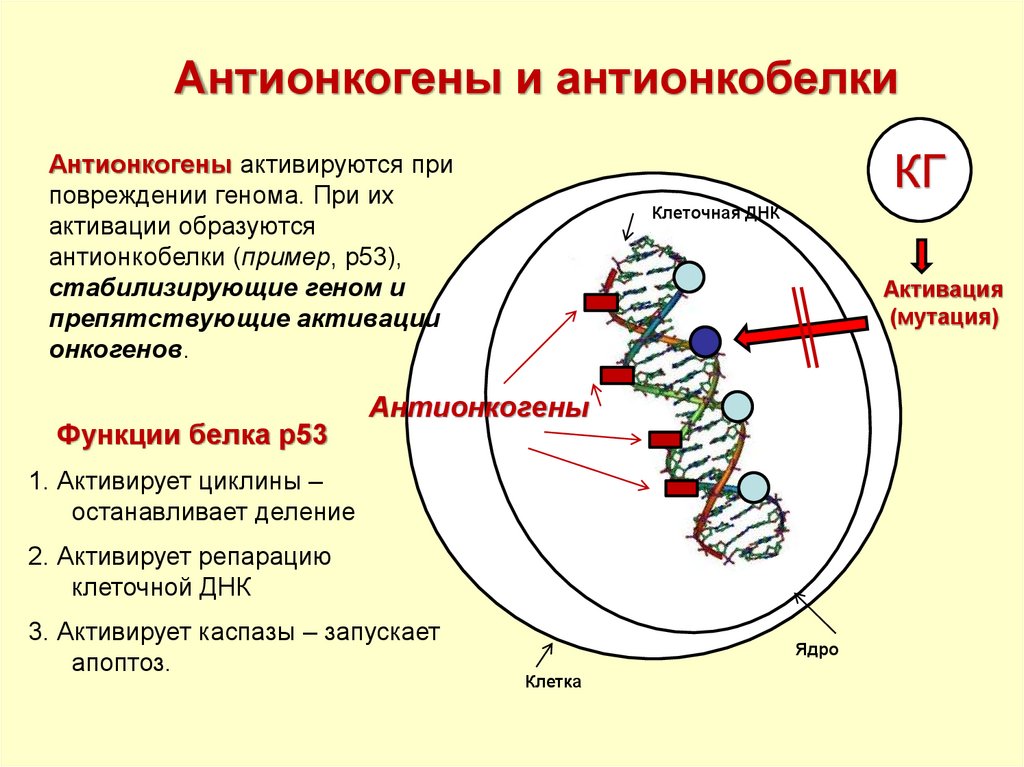
Антионкогены и антионкобелкиКГ
Антионкогены активируются при
повреждении генома. При их
активации образуются
антионкобелки (пример, р53),
стабилизирующие геном и
препятствующие активации
онкогенов.
Функции белка р53
Клеточная ДНК
Активация
(мутация)
Антионкогены
1. Активирует циклины –
останавливает деление
2. Активирует репарацию
клеточной ДНК
3. Активирует каспазы – запускает
апоптоз.
Ядро
Клетка
53.
Рак – многостадийный процессКанцерогенезу способствуют:
1. наличие канцерогенов
2. мутации антионкогенов – повышают нестабильность генома
3. мутации онкогенов – ведут к опухолевой трансформации
4. иммунодефицитное состояние – снимается иммунный надзор
5. гормональный дисбаланс – нарушается контроль клеточного цикла
54.
Опухолевая прогрессия - приобретениеопухолевыми клетками в процессе роста новых
качеств и свойств и потеря старых.
Принцип Фулдса – принцип независимой прогрессии отдельных
свойств опухоли.
Генеральные направления прогрессии
1. в сторону большей злокачественности
2. в сторону большей автономности
3. в сторону метастазирования
Метастазирование – образование вторичных удаленных очагов
опухолевого роста.
Основные пути метастазирования – гематогенный,
лимфогенный
Стадии метастазирования
инвазия
транспорт
(проникновение в сосуд)
(кровью или лимфой)
имплантация
(осаждение на чужом поле)
активация
(размножение на чужом поле)
55.
Механизмы системного действия опухоли1. Кахексия
2. Активация ГГНС
3. Иммунодепрессия
4. Геморрагии и тромбозы
5. Тромбоцитопения
6. Анемия
7. Отёки
8. Продукция эктопических гормонов
9. Дефицит факторов антиоксидантной защиты
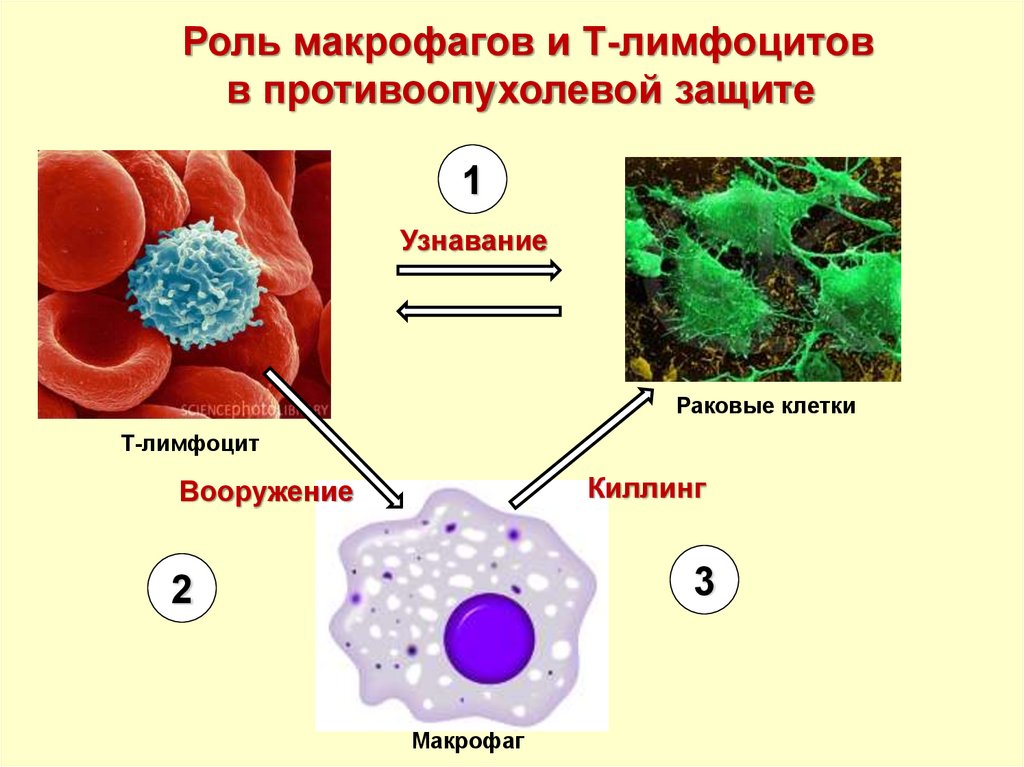
56.
Роль макрофагов и Т-лимфоцитовв противоопухолевой защите
1
Узнавание
Раковые клетки
Т-лимфоцит
Киллинг
Вооружение
3
2
Макрофаг


























 Медицина
Медицина