Похожие презентации:
Синтез полимеров
1. Синтез полимеров
2.
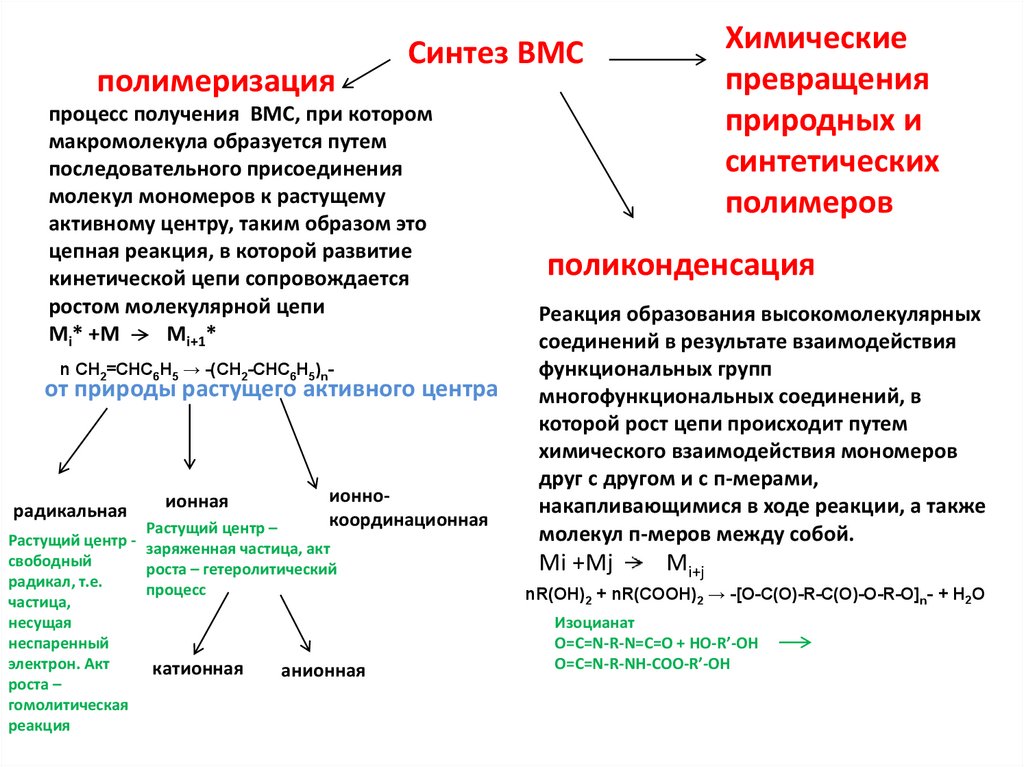
полимеризацияпроцесс получения ВМС, при котором
макромолекула образуется путем
последовательного присоединения
молекул мономеров к растущему
активному центру, таким образом это
цепная реакция, в которой развитие
кинетической цепи сопровождается
ростом молекулярной цепи
Mi* +M
Mi+1*
n СН2=СНС6Н5 → -(СН2-СНС6Н5)n-
от природы растущего активного центра
радикальная
ионная
ионнокоординационная
Растущий центр –
Растущий центр - заряженная частица, акт
свободный
роста – гетеролитический
радикал, т.е.
процесс
частица,
несущая
неспаренный
электрон. Акт
катионная
анионная
роста –
гомолитическая
реакция
Химические
превращения
природных и
синтетических
полимеров
Синтез ВМС
поликонденсация
Реакция образования высокомолекулярных
соединений в результате взаимодействия
функциональных групп
многофункциональных соединений, в
которой рост цепи происходит путем
химического взаимодействия мономеров
друг с другом и с п-мерами,
накапливающимися в ходе реакции, а также
молекул п-меров между собой.
Mi +Mj
Mi+j
nR(OH)2 + nR(COOH)2 → -[O-C(O)-R-C(O)-O-R-O]n- + Н2О
Изоцианат
O=C=N-R-N=C=O + НО-R’-OH
O=C=N-R-NH-COO-R’-OH
3.
Полимеризация – цепной процесс4.
Поликонденсация – ступенчатый процесс5.
Основные особенности процессов полимеризации и поликонденсации1
2
Особенность процесса
Характер образования
цепи
Полимеризация
Цепной
Продуктом процесса является
макромолекула
Зависимость средней
степени полимеризации
от числа реакций,
составляющих стадию
образования
макромолекул
Арифметическая прогрессия
i – число актов взаимодействия
3
Число реакционных
центров в ходе процесса
Постоянно
Поликонденсация
Ступенчатый
Нарастание длины макромолекулы
происходит по «ступеням» различной
величины
Геометрическая прогрессия
Чем более глубоко проходит процесс,
тем более сильно будет изменяться
молекулярная масса в процессе
поликонденсации
В каждом акте число реакционных
центров уменьшается на 2 (модель
дубликации)
6.
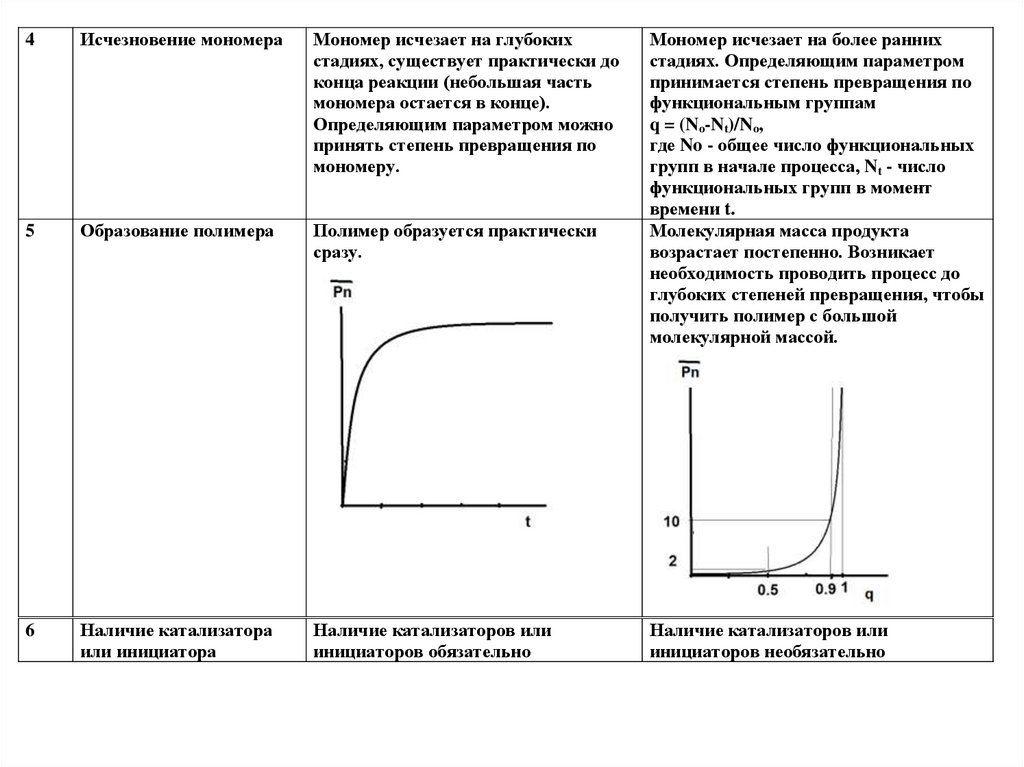
4Исчезновение мономера
Мономер исчезает на глубоких
стадиях, существует практически до
конца реакции (небольшая часть
мономера остается в конце).
Определяющим параметром можно
принять степень превращения по
мономеру.
5
Образование полимера
Полимер образуется практически
сразу.
6
Наличие катализатора
или инициатора
Наличие катализаторов или
инициаторов обязательно
Мономер исчезает на более ранних
стадиях. Определяющим параметром
принимается степень превращения по
функциональным группам
q = (No-Nt)/No,
где No - общее число функциональных
групп в начале процесса, Nt - число
функциональных групп в момент
времени t.
Молекулярная масса продукта
возрастает постепенно. Возникает
необходимость проводить процесс до
глубоких степеней превращения, чтобы
получить полимер с большой
молекулярной массой.
Наличие катализаторов или
инициаторов необязательно
7.
ПОЛИМЕРИЗАЦИЯ8.
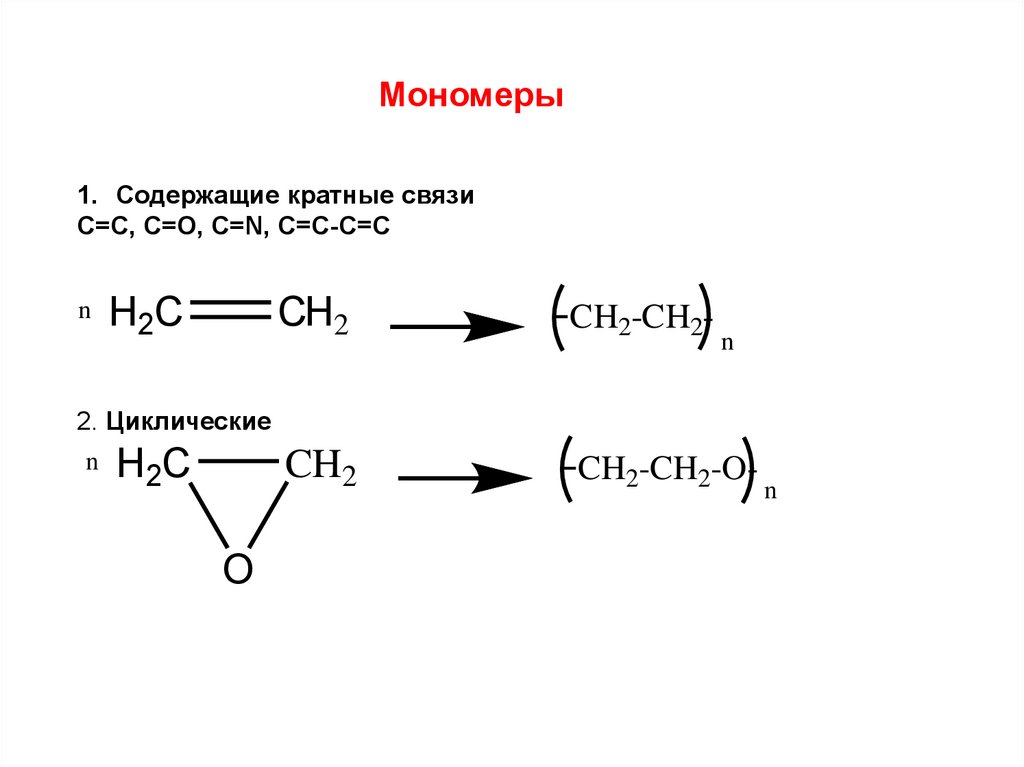
Мономеры1. Содержащие кратные связи
С=С, С=О, С=N, C=C-C=C
n H C
2
CH2
-CH2-CH2- n
CH2
-CH2-CH2-O- n
2. Циклические
n H C
2
O
9.
Как правило мономеры – устойчивые соединения и самопроизвольно не полимеризуются.Способность к полимеризации зависит от термодинамических и кинетических (природа
катализатора или инициатора, давление, температура, концентрация ) факторов.
Термодинамический фактор
В большинстве случаев полимеризация – экзотермический процесс, т.е. ∆Q > 0, а т.к. ∆H = ∆Q, то поэтому ∆H < 0. Таким образом, изменение энтальпии способствует протеканию
полимеризации, и чем больше по абсолютной величине ∆Q, тем меньше ∆G, т.е. процесс
термодинамически более выгоден.
10.
∆11.
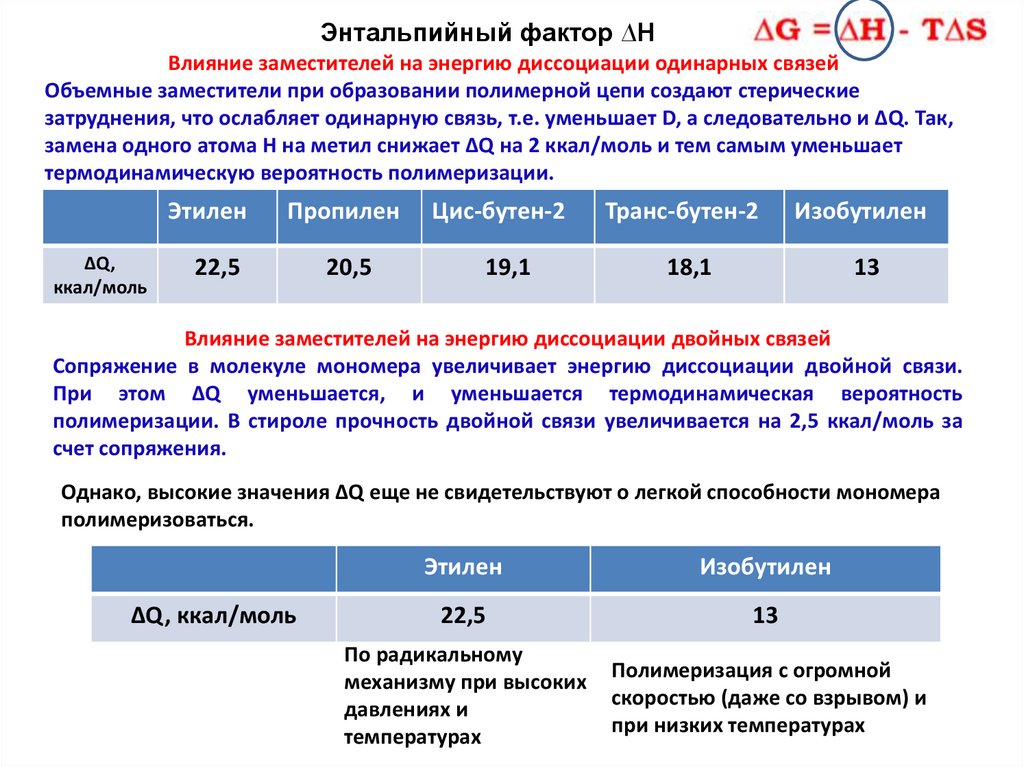
Энтальпийный фактор ∆НВлияние заместителей на энергию диссоциации одинарных связей
Объемные заместители при образовании полимерной цепи создают стерические
затруднения, что ослабляет одинарную связь, т.е. уменьшает D, а следовательно и ∆Q. Так,
замена одного атома Н на метил снижает ∆Q на 2 ккал/моль и тем самым уменьшает
термодинамическую вероятность полимеризации.
∆Q,
ккал/моль
Этилен
Пропилен
Цис-бутен-2
Транс-бутен-2
Изобутилен
22,5
20,5
19,1
18,1
13
Влияние заместителей на энергию диссоциации двойных связей
Сопряжение в молекуле мономера увеличивает энергию диссоциации двойной связи.
При этом ∆Q уменьшается, и уменьшается термодинамическая вероятность
полимеризации. В стироле прочность двойной связи увеличивается на 2,5 ккал/моль за
счет сопряжения.
Однако, высокие значения ∆Q еще не свидетельствуют о легкой способности мономера
полимеризоваться.
∆Q, ккал/моль
Этилен
Изобутилен
22,5
13
По радикальному
механизму при высоких
давлениях и
температурах
Полимеризация с огромной
скоростью (даже со взрывом) и
при низких температурах
12.
Энтропийный фактор ∆S13.
Рассмотрим возможные изменения ∆G как функции температурыэкзотермические реакции
Тпр – предельная температура, ниже этой температуры нет термодинамических
препятствий для полимеризации.
14.
эндотермические реакции15.
Кинетический фактор16.
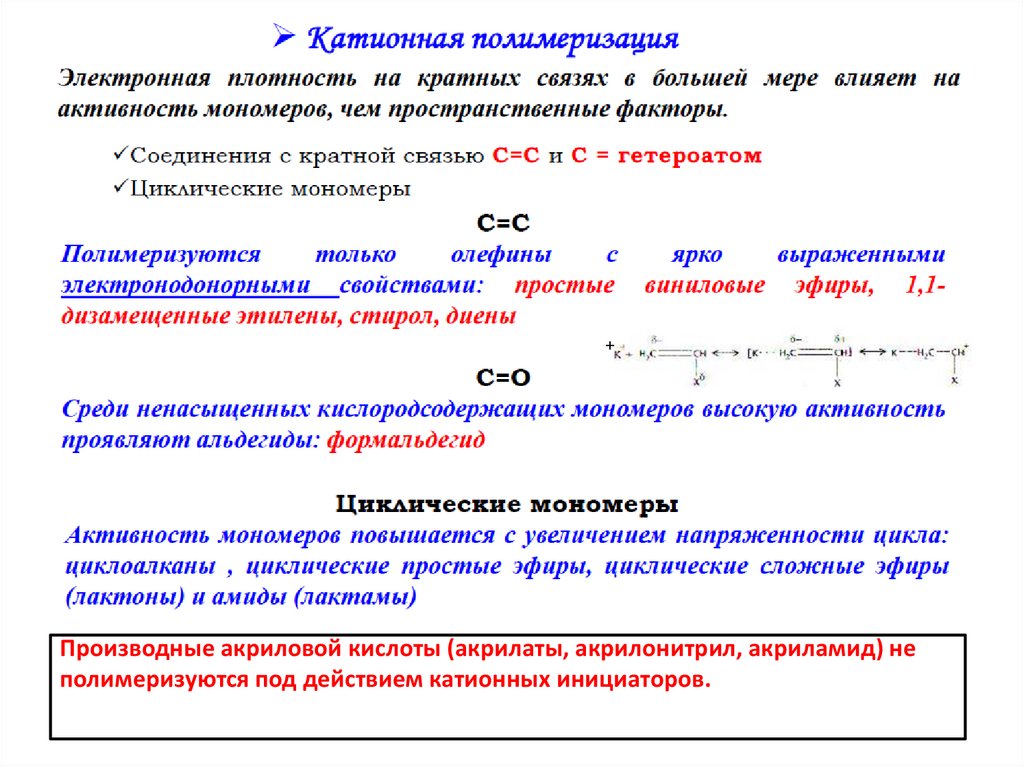
+Производные акриловой кислоты (акрилаты, акрилонитрил, акриламид) не
полимеризуются под действием катионных инициаторов.
17.
Винилкарбазол и винилпирролидон не полимеризуются под действиеманионных инициаторов.
18.
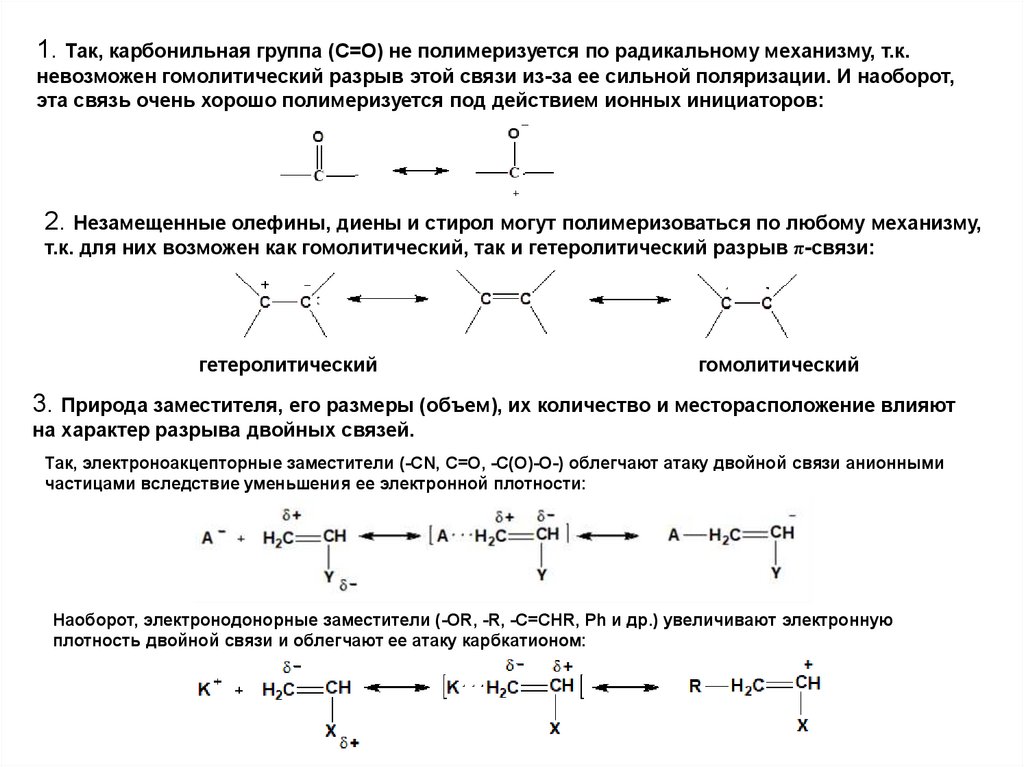
1. Так, карбонильная группа (С=О) не полимеризуется по радикальному механизму, т.к.невозможен гомолитический разрыв этой связи из-за ее сильной поляризации. И наоборот,
эта связь очень хорошо полимеризуется под действием ионных инициаторов:
2. Незамещенные олефины, диены и стирол могут полимеризоваться по любому механизму,
т.к. для них возможен как гомолитический, так и гетеролитический разрыв π-связи:
гетеролитический
гомолитический
3. Природа заместителя, его размеры (объем), их количество и месторасположение влияют
на характер разрыва двойных связей.
Так, электроноакцепторные заместители (-CN, C=O, -C(O)-O-) облегчают атаку двойной связи анионными
частицами вследствие уменьшения ее электронной плотности:
Наоборот, электронодонорные заместители (-OR, -R, -C=CHR, Ph и др.) увеличивают электронную
плотность двойной связи и облегчают ее атаку карбкатионом:
19.
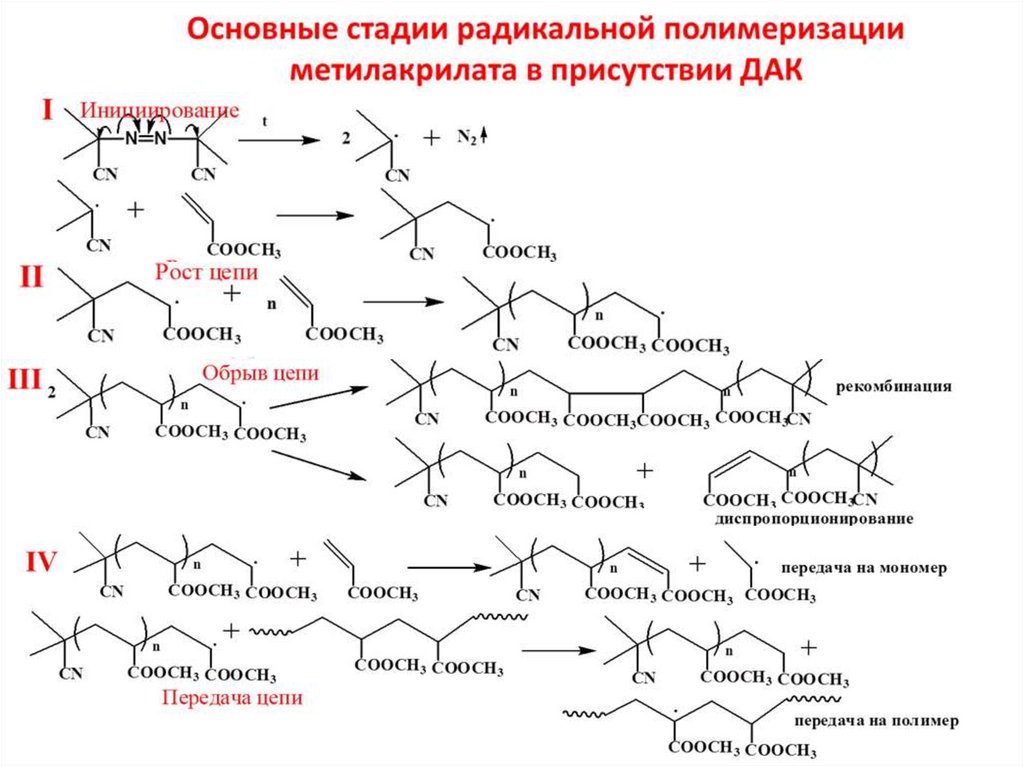
Основные стадии процесса полимеризации1. Инициирование – превращение небольшого числа молекул мономера в
активные центры, способные присоединять новые молекулы мономера. Для создания
таких условий в систему вводят специальные вещества (инициаторы или
катализаторы), либо подвергают ее воздействию ионизирующего излучения, света,
электрического тока, тепла.
R* + M
RM*
K+ + M
KM+
A- + M
AMсостоит из ряда многократно повторяющихся реакций
присоединения молекул мономера к растущему активному центру. Реакция роста в
принципе обратима, поэтому наряду с присоединением мономера может происходить
его отщепление.
3. Обрыв цепи – это гибель растущих макроцепей в результате их
взаимодействия с другим активным центром ( только радикальная), посторонним
веществом или вследствие молекулярной перестройки.
4. Передача цепи: активный центр растущей молекулы переходит на какуюнибудь частицу S, начинающую рост новой макромолекулы. Различают передачу цепи
на мономер, растворитель, полимер, компоненты каталитической системы, примеси и
стенки реакционного сосуда.
реакции ограничения роста цепи
2. Рост цепи
20.
Допущения для вывода кинетического уравнения полимеризации:1. Реакционная способность растущих полимерных цепей не
зависит от их длины, т.е. для кинетического описания
достаточно учесть влияние последнего звена растущей цепи.
2. При образовании макромолекул с высокой ММ скорость
полимеризации,
т.е.
скорость
расхода
мономера,
равна
скорости реакции роста, т.е. мономер расходуется только на
стадии реакции роста.
3. В общем случае, когда время жизни активных центров
(растущих цепей) меньше времени процесса, используют
принцип стационарности, т.е. скорость инициирования =
скорости обрыва.
21. Радикальная полимеризация - Это цепной процесс, в котором макроцепи являются растущими свободными радикалами, а акт роста –
Радикальная полимеризация Это цепной процесс, в котором макроцепи являются растущимисвободными радикалами, а акт роста – гомолитической реакцией,
т.е. химической реакцией, сопровождающейся разрывом
некоторых существующих двухэлектронных связей и образованием
новых электронных пар.
22.
(а)(б)
23.
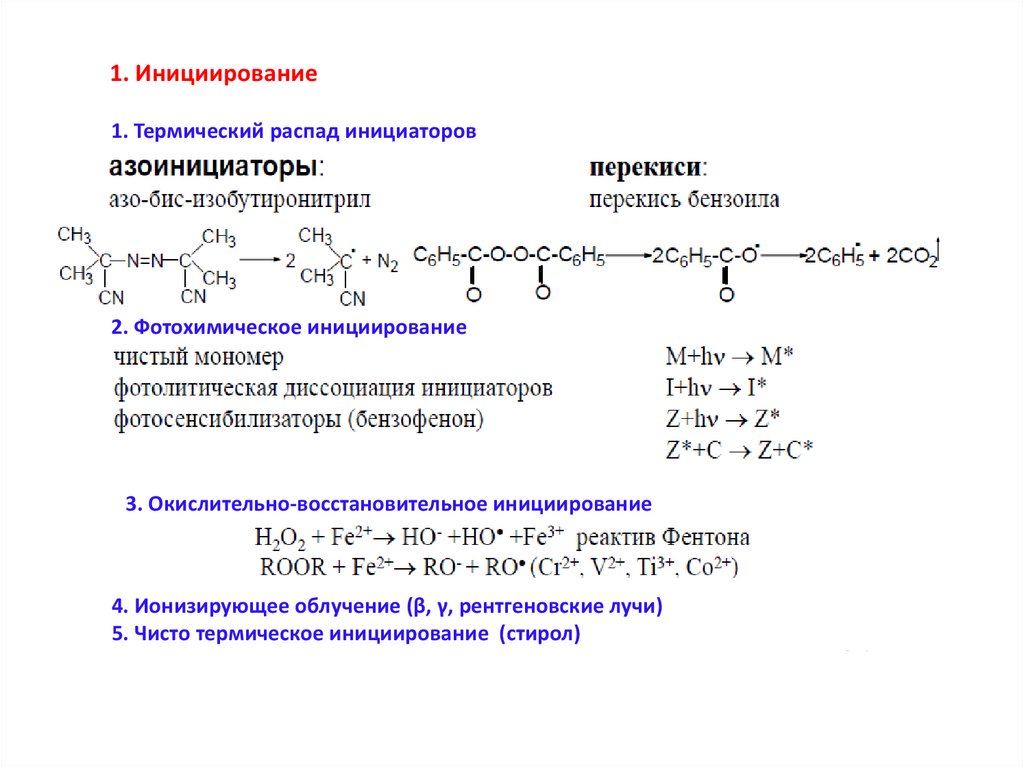
1. Инициирование1. Термический распад инициаторов
2. Фотохимическое инициирование
3. Окислительно-восстановительное инициирование
4. Ионизирующее облучение (β, γ, рентгеновские лучи)
5. Чисто термическое инициирование (стирол)
О-
24.
25.
(ТЕМПО)26.
С увеличением степени конверсии вязкость реакционной системы в отсутствиерастворителя (например, при полимеризации в блоке) возрастает, что препятствует
свободному перемещению растущих макрорадикалов.
В результате скорость
эффективных соударений растущих макрорадикалов уменьшается, поэтому падает
вероятность обрыва (ko). Благодаря этому падению скорости обрыва резко возрастает
время жизни макрорадикалов и, следовательно, ММ. Однако, увеличение вязкости
реакционной системы не оказывает влияния на скорость движения молекул мономера,
т.е. kр, поэтому скорость роста не уменьшается. Вот почему общая скорость реакции
(kр/ko) растет, и наступает «автокатализ» или «гель-эффект».
Для устранения «гель-эффекта»:
1. используют методы повышения скорости
инициирования, применяя
высокоэффективные инициаторы
2. Снижают скорость полимеризации на
стадии «гель-эффекта» путем, например,
добавления системы RSH+ алкилнитриты
3. Снижают тепловыделение на стадии
«гель-эффекта» путем сополимеризации с
соединениями, полимеризующимися с
поглощением тепла, или добавления
веществ, которые разлагаются с
выделением веществ, ингибирующих
полимеризацию
27.
˅На инициатор˅На различные примеси, добавки, стенки реакционного сосуда
28.
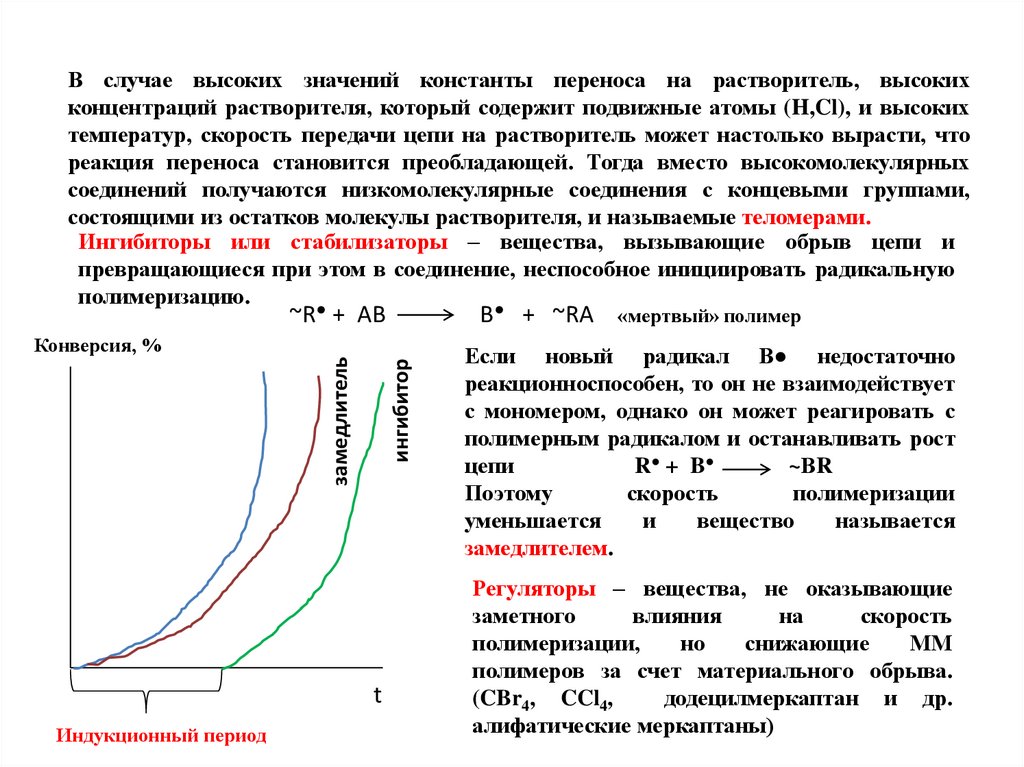
В случае высоких значений константы переноса на растворитель, высокихконцентраций растворителя, который содержит подвижные атомы (H,Cl), и высоких
температур, скорость передачи цепи на растворитель может настолько вырасти, что
реакция переноса становится преобладающей. Тогда вместо высокомолекулярных
соединений получаются низкомолекулярные соединения с концевыми группами,
состоящими из остатков молекулы растворителя, и называемые теломерами.
Ингибиторы или стабилизаторы – вещества, вызывающие обрыв цепи и
превращающиеся при этом в соединение, неспособное инициировать радикальную
полимеризацию.
~R + AB
B
ингибитор
замедлитель
Конверсия, %
t
Индукционный период
+ ~RA
«мертвый» полимер
Если новый радикал В● недостаточно
реакционноспособен, то он не взаимодействует
с мономером, однако он может реагировать с
полимерным радикалом и останавливать рост
цепи
R● + B
~ВR
Поэтому
скорость
полимеризации
уменьшается
и
вещество
называется
замедлителем.
Регуляторы – вещества, не оказывающие
заметного
влияния
на
скорость
полимеризации,
но
снижающие
ММ
полимеров за счет материального обрыва.
(CBr4, CCl4,
додецилмеркаптан и др.
алифатические меркаптаны)
29.
Вводится допущение о стационарномсостоянии, в котором концентрация
радикалов сначала увеличивается, а
потом очень быстро
достигает
постоянной величины, т.е. скорость
изменения концентрации радикалов
равна 0, т.е. Vи=Vo
Реакция радикальной полимеризации подчиняется первому порядку по мономеру и
половинному – по инициатору. Половинный порядок по инициатору является следствием
бимолекулярного механизма обрыва растущих цепей.
30.
31.
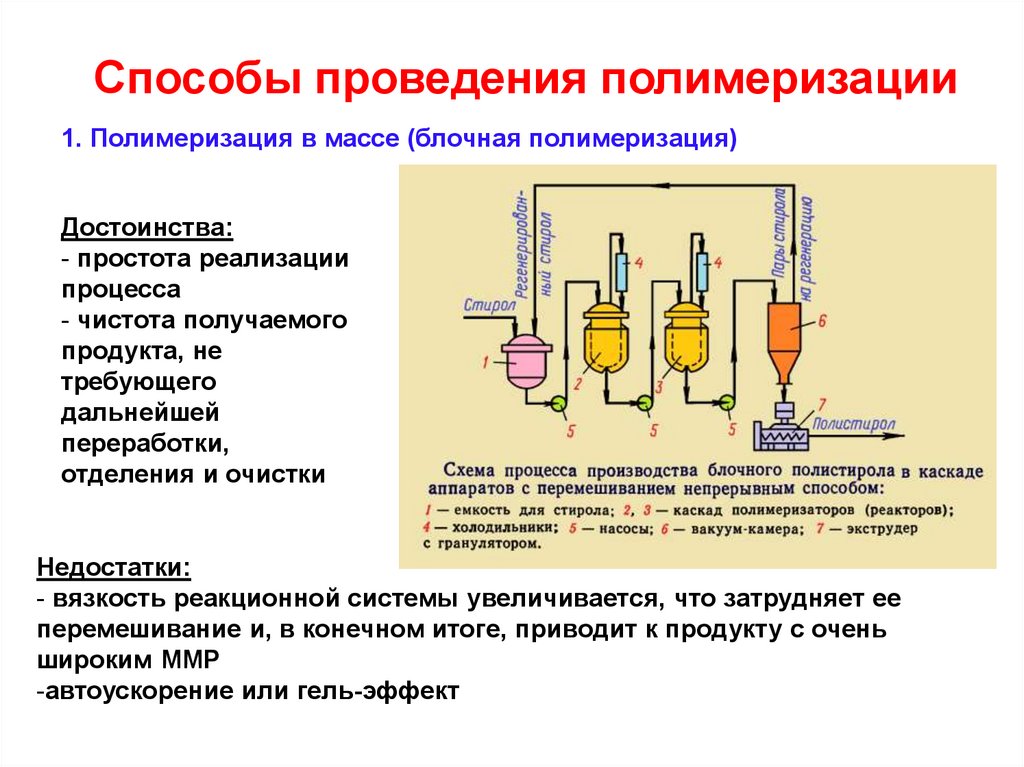
Способы проведения полимеризации1. Полимеризация в массе (блочная полимеризация)
Достоинства:
- простота реализации
процесса
- чистота получаемого
продукта, не
требующего
дальнейшей
переработки,
отделения и очистки
Недостатки:
- вязкость реакционной системы увеличивается, что затрудняет ее
перемешивание и, в конечном итоге, приводит к продукту с очень
широким ММР
-автоускорение или гель-эффект
32.
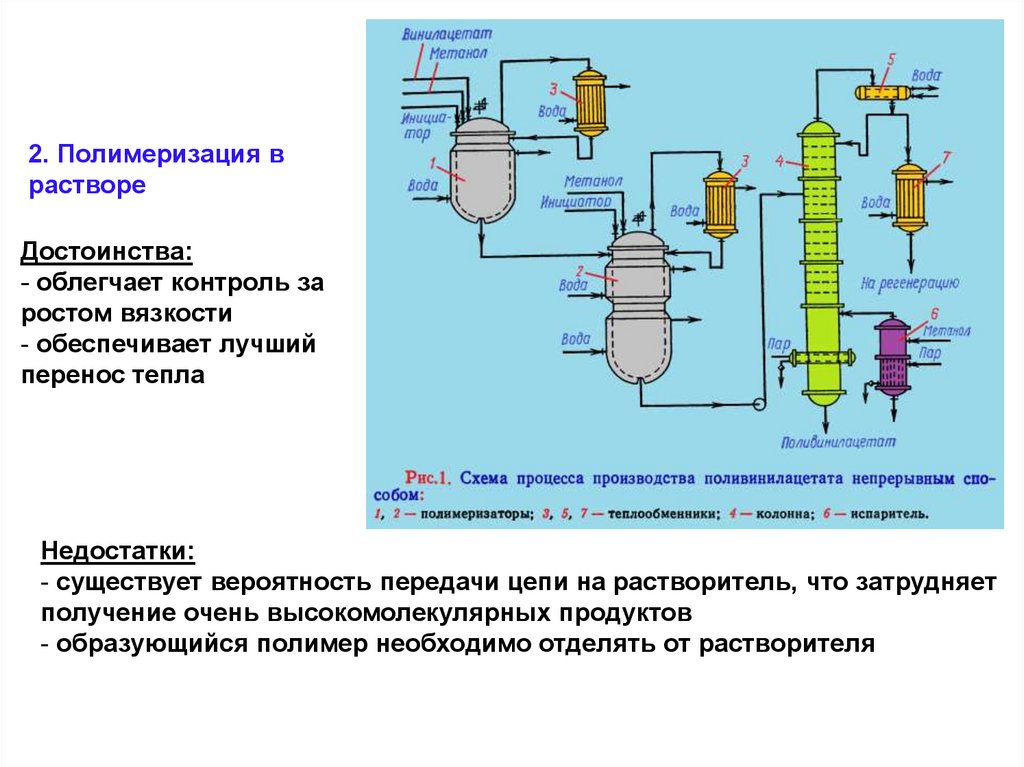
2. Полимеризация врастворе
Достоинства:
- облегчает контроль за
ростом вязкости
- обеспечивает лучший
перенос тепла
Недостатки:
- существует вероятность передачи цепи на растворитель, что затрудняет
получение очень высокомолекулярных продуктов
- образующийся полимер необходимо отделять от растворителя
33.
3. Суспензионная полимеризация (гранульная, бисерная, жемчужная)Достоинства:
- контроль за длиной
кинетических цепей (неширокое
ММР) и высокая ММ
- эффективный перенос тепла
- легкость отделения от воды
- простота переработки готового
продукта
Недостатки:
- ограниченность использования
- возможность загрязнения стабилизатором
1. При полимеризации в суспензии мономер диспергируют в воде в виде мелких капель.
2. Устойчивость дисперсии достигается механическим перемешиванием и введением в
реакционную систему специальных добавок – стабилизаторов. (гидрофильные
полимеры, такие как поливиниловый спирт, полиакриловая кислота, крахмал, а также оксид
алюминия, тальк, тонкодисперсная глина). Стабилизаторы адсорбируются на поверхности
капель, образующихся при перемешивании, и препятствуют их слиянию. Капли относительно
большие (диаметр от 0,1 до 5 мм)
3. Инициаторы обычно не растворимы в воде, но растворимы в мономере. Полимеризация
протекает самостоятельно в каждой капле, являющейся своеобразным «резервуаром»
мономера. Образуется полимер в виде шарообразных частиц (гранул, бисер) с высокой
молекулярной массой, которые не растворимы в воде и легко оседают без специальной
коагуляции при прекращении перемешивания.
Суспензионная полимеризация представляет собой, по существу, разновидность блочной
полимеризации, так как гранулы являются как бы «микроблоками».
34.
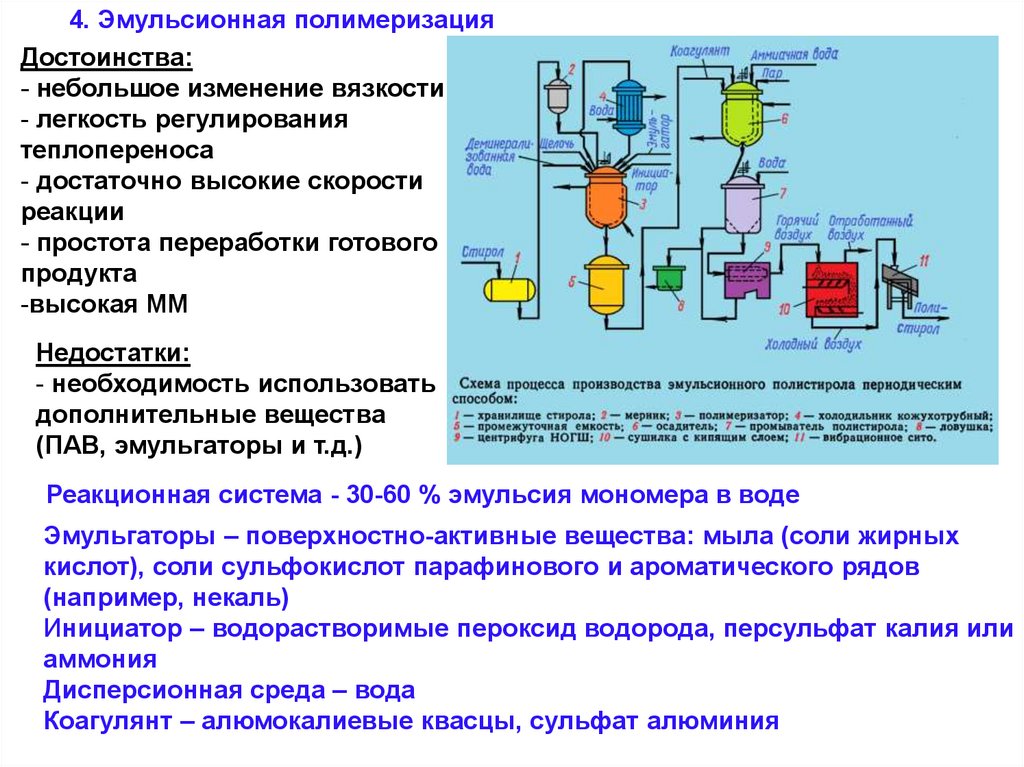
4. Эмульсионная полимеризацияДостоинства:
- небольшое изменение вязкости
- легкость регулирования
теплопереноса
- достаточно высокие скорости
реакции
- простота переработки готового
продукта
-высокая ММ
Недостатки:
- необходимость использовать
дополнительные вещества
(ПАВ, эмульгаторы и т.д.)
Реакционная система - 30-60 % эмульсия мономера в воде
Эмульгаторы – поверхностно-активные вещества: мыла (соли жирных
кислот), соли сульфокислот парафинового и ароматического рядов
(например, некаль)
Инициатор – водорастворимые пероксид водорода, персульфат калия или
аммония
Дисперсионная среда – вода
Коагулянт – алюмокалиевые квасцы, сульфат алюминия
35.
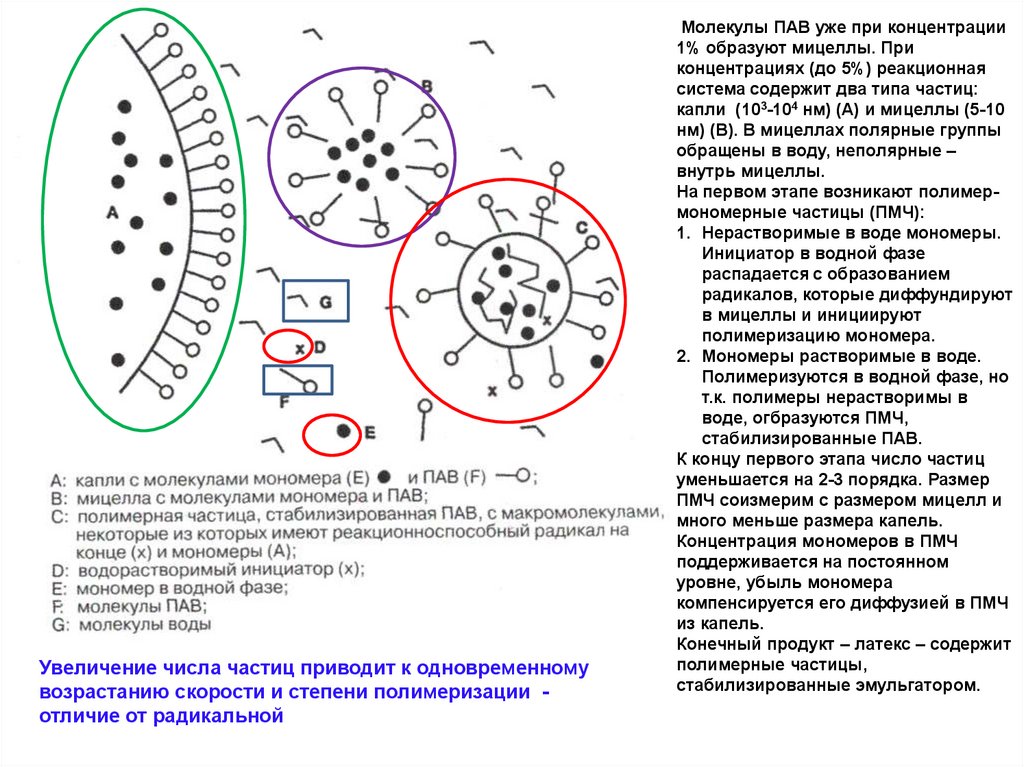
Увеличение числа частиц приводит к одновременномувозрастанию скорости и степени полимеризации отличие от радикальной
Молекулы ПАВ уже при концентрации
1% образуют мицеллы. При
концентрациях (до 5%) реакционная
система содержит два типа частиц:
капли (103-104 нм) (А) и мицеллы (5-10
нм) (В). В мицеллах полярные группы
обращены в воду, неполярные –
внутрь мицеллы.
На первом этапе возникают полимермономерные частицы (ПМЧ):
1. Нерастворимые в воде мономеры.
Инициатор в водной фазе
распадается с образованием
радикалов, которые диффундируют
в мицеллы и инициируют
полимеризацию мономера.
2. Мономеры растворимые в воде.
Полимеризуются в водной фазе, но
т.к. полимеры нерастворимы в
воде, огбразуются ПМЧ,
стабилизированные ПАВ.
К концу первого этапа число частиц
уменьшается на 2-3 порядка. Размер
ПМЧ соизмерим с размером мицелл и
много меньше размера капель.
Концентрация мономеров в ПМЧ
поддерживается на постоянном
уровне, убыль мономера
компенсируется его диффузией в ПМЧ
из капель.
Конечный продукт – латекс – содержит
полимерные частицы,
стабилизированные эмульгатором.
36.
ПСЕВДОЖИВАЯ РАДИКАЛЬНАЯ ПОЛИМЕРИЗАЦИЯПри псевдоживой радикальной полимеризации растущие цепи часть времени (большую) являются
неактивными, другую часть времени (значительно меньшую) - активными, т.е. участвуют в реакции
роста. Это происходит благодаря периодическим актам обратимого ингибирования.
Впервые псевдоживая радикальная полимеризация была реализована в начале 1980-х годов с
использованием инифертеров. Это название происходит от сокращения английских слов initiator transfer - termination - agent, оно обозначает соединения, выполняющие в радикальной полимеризации
функции инициатора, а также участвующие в реакциях обрыва и передачи цепи.
В качестве инифертеров применяются главным образом серосодержащие соединения: дитиокарбаматы,
дитиокарбонаты, различного рода дисульфиды и трифенилметильные производные. Такие соединения,
как правило, диссоциируют с образованием активного и неактивного радикалов:
где R• - активный радикал, способный инициировать полимеризацию, X• -неактивный радикал,
обрывающий растущие цепи:
Для реализации режима псевдоживой полимеризации важно, чтобы скорость бимолекулярного обрыва
радикалов роста была существенно меньше скорости их обрыва с участием X•. Тогда большая часть
макромолекул будет способна к реинициированию в результате гомолитического распада аддукта Р-Х. В
результате ММ полимера должна возрастать по ходу полимеризации, что подтверждается
экспериментально. Недостатком псевдоживой полимеризации в присутствии инифертеров является
широкое ММР, т.е. значительная полидисперсность получаемого полимера. В данном случае эту
нежелательную особенность полимеризации связывают с возможностью инициирования полимеризации
радикалом X•.
37.
В 83-84-х гг. XX в. были предложены варианты псевдоживой полимеризации, лишенные недостатков,присущих полимеризации в присутствии инифертеров, т.е. приводящие к образованию полимеров с
узким ММР. Наибольшее распространение получили два метода:
1. Полимеризация с обратимым ингибированием комплексами переходных металлов и
стабильными радикалами при температурах, превышающих 100 °С. В англоязычной
научной и учебной литературе этот метод обозначается как SFRP (stable free radical
polymerization).
Примером «идеальной» считается псевдоживая
полимеризация стирола, обратимо ингибируемая
2,2',6,6'-тетраметилпиперидиноксилом-1 (далее
ТЕМПО или Т):
ТЕМПО и подобные ему нитроксильные
радикалы чаще используются в виде аддуктов,
т.е. алкоксиаминов.
При нагревании стирола в присутствии алкоксиаминов выше 100°С протекают следующие элементарные
реакции. Распад алкоксиаминов:
где Р• - макрорадикал со степенью полимеризации n.
Последняя реакция приводит к увеличению
концентрации свободного нитроксильного
радикала. Благодаря этому скорость
обратимого ингибирования возрастает
настолько, что по сравнению с ней скорость
бимолекулярного обрыва становится
пренебрежимо малой.
38.
2. Полимеризация с переносом атома галогена или ATRP (atom transfer radicalpolymerization).
Типичным примером является псевдоживая радикальная полимеризация стирола при 110 °С в
присутствии растворимых комплексов CuBr с лигандом L:
в которой растущие цепи обратимо реагируют с сильным ингибитором CuBr. В данном случае
обратимая окислительно-восстановительная реакция ингибирования сопровождается переносом
атома брома.
1. Первый порядок скорости
по концентрации мономера.
2. Линейная зависимость
степени полимеризации от
конверсии.
3. Узкое ММР полимера:
параметр полидисперсности
колеблется в пределах 1,05 <
Кд < 1,2. При обычной
радикальной полимеризации
1,5 ≤ Кд ≤ 2,0. Такая ситуация
характерна лишь для
начальных конверсий.
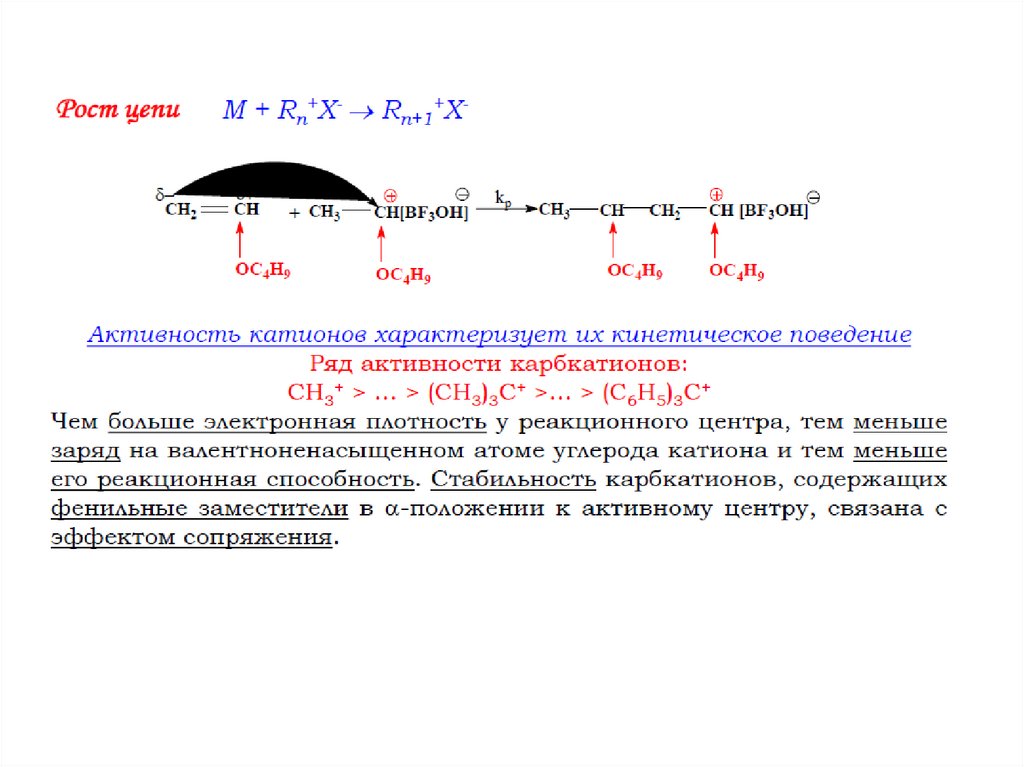
39. Катионная полимеризация – это цепной процесс, происходящий путем последовательного присоединения молекул мономера к
положительнозаряженному растущему активному центру (карбкатиону),
причем акт роста является гетеролитической реакцией.
40.
41.
Катионная полимеризация42.
ИнициированиеА) инициирование протонными кислотами (кислотами Бренстеда)
H+A- + CH2=CHR
CH3-CHR+ AH3PO4, HClO4, H2SO4
Б) Апротонные кислоты (кислоты Льюиса, катализаторы
Фриделя-Крафтса)
MeXn (BF3, SnCl4, AlCl3, AlR3, SbCl5 ) c HA или Rhal
+M
MeXn + HA ↔ H+[MeXnA]H-M+[MeXnA]+M
MeXn + RHal ↔ R+[MeXnHal]R-M+[MeXnHal]B) Другие способы инициирования
- Молекулярный иод
- Стабильные соли карбония
- Излучение высоких энергий
- Фотоинициирование
43.
44.
45.
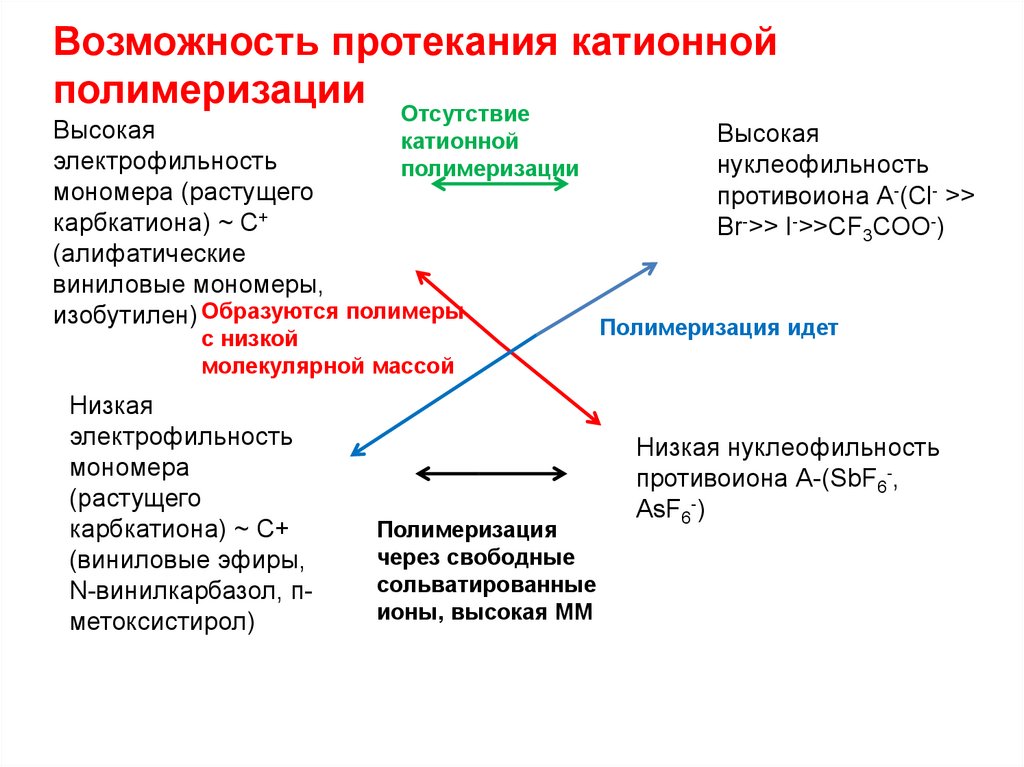
Возможность протекания катионнойполимеризации Отсутствие
Высокая
Высокая
катионной
электрофильность
нуклеофильность
полимеризации
мономера (растущего
противоиона А-(Cl- >>
карбкатиона) ~ С+
Br->> I->>CF3COO-)
(алифатические
виниловые мономеры,
изобутилен) Образуются полимеры
Полимеризация идет
с низкой
молекулярной массой
Низкая
электрофильность
мономера
(растущего
карбкатиона) ~ С+
(виниловые эфиры,
N-винилкарбазол, пметоксистирол)
Полимеризация
через свободные
сольватированные
ионы, высокая ММ
Низкая нуклеофильность
противоиона А-(SbF6-,
AsF6-)
































 Химия
Химия








