Похожие презентации:
Химические формулы. Относительная молекулярная масса
1. Тема урока: «Химические формулы. Относительная молекулярная масса»
2.
“В природе ничего другого нет,Ни здесь, ни там, в космических
глубинах.
Все от песчинок малых до планет
Из элементов состоит единых”
Степан Щипачев
Работу выполнила Романова Н.Н,
учитель химии и биологии
МБОУ «Сизябская СОШ»
2016 год
3.
ПРОВЕРОЧНЫЙ ТЕСТЗадание : подбери соответствие.
1.Аргентум
2.Аурум
3.Гидраргирум
4.Силициум
5.Натрий
6.Плюмбум
7.Фосфор
8.Кальций
9.Купрум
10.Феррум
а) Ag
б) Cu
в) Fe
г) Cа
д) Na
е) Hg
ж) Pb
з) Р
и) Si
к) Au
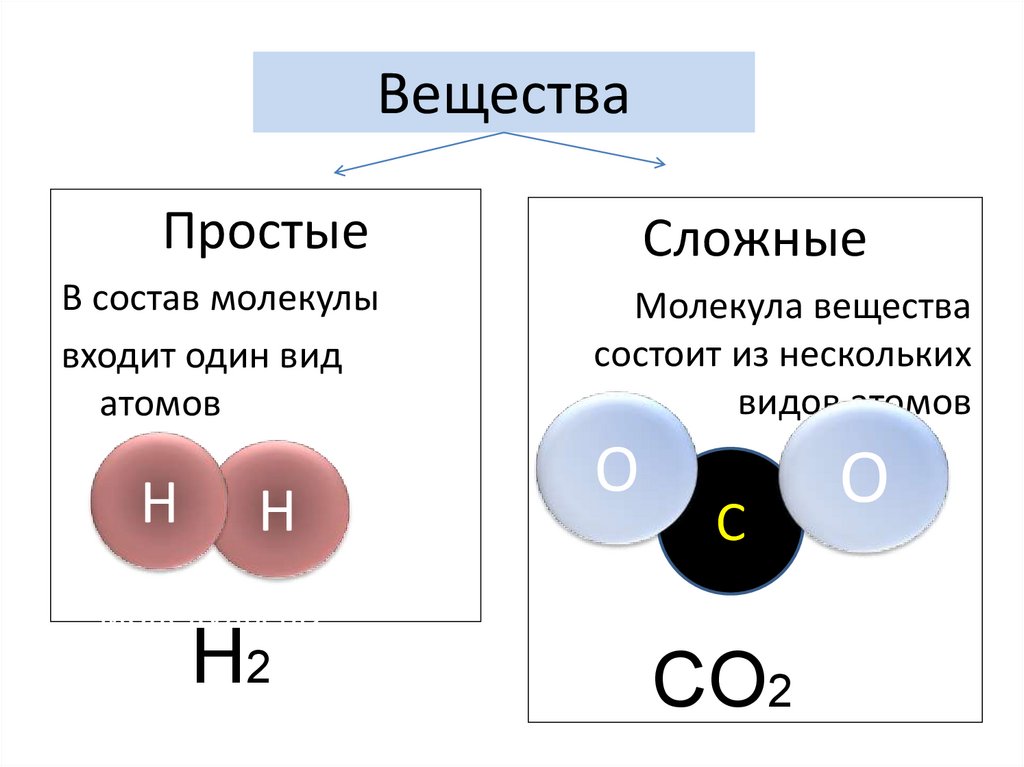
4. Вещества
ПростыеВ состав молекулы
входит один вид
атомов
H молекулы
H
• в состав
веществв состав
молекулы вD
• ещества 2
входит один
вид атомов
H
Сложные
Молекула вещества
состоит из нескольких
видов атомов
O
C
CO2
O
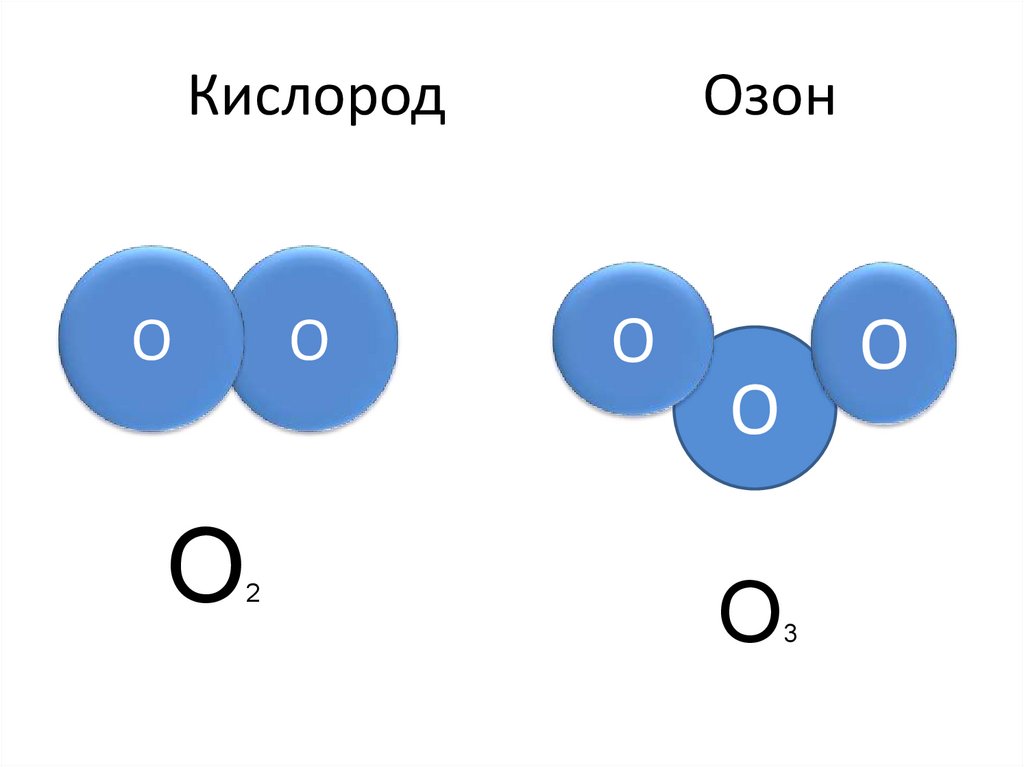
5. Кислород Озон
КислородO
O
O
2
Озон
O
O
O
O
3
6.
Просмотрите видеоурокhttps://yandex.ru/video/preview/6051390452954790091
• Химическая формула – это
условная запись состава
вещества, посредствам
химических знаков и символов.
7.
5H2СO3Индекс – показывает число
атомов в молекуле.
Знаки химических элементов.
Коэффициент - показывает число
молекул или атомов
8.
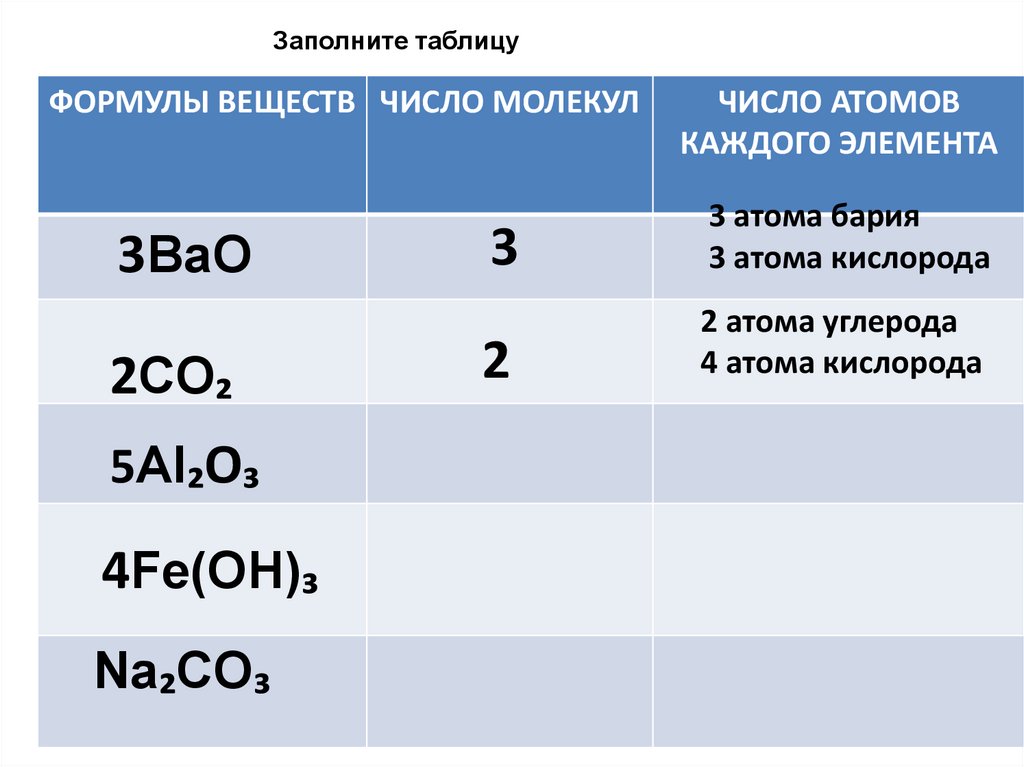
Заполните таблицуФОРМУЛЫ ВЕЩЕСТВ ЧИСЛО МОЛЕКУЛ
3BaO
2CO₂
5Al₂O₃
4Fe(OH)₃
Na₂CO₃
ЧИСЛО АТОМОВ
КАЖДОГО ЭЛЕМЕНТА
3
3 атома бария
3 атома кислорода
2
2 атома углерода
4 атома кислорода
9. Относительная масса атома
• mат (Н) = 0,000 000 000 000 000 000 000 001674 г = 0,1674∙10-23 г• mат (О) = 0,000 000 000 000 000 000 000 026667 г = 2,6667∙10-23 г
• mат (C) = 0,000 000 000 000 000 000 000 01993 г = 1,993∙10-23 г
-Ar – относительная атомная масса
1 а.е.м. – величина равная 1/12 массы атома углерода.
1 а.е.м. = mат(C)/12 = 1,674 ∙ 10-24г
1а.е.м. = = 1,993∙10-23 г/ 12 = 1,674 ∙ 10-24г
• Относительная атомная масса – это величина,
показывающая, во сколько раз масса атома больше
1/12 массы атома углерода
10.
mат (Н) = 0,000 000 000 000 000 000 000 001674 г = 0,1674∙10-23 гmат (О) = 0,000 000 000 000 000 000 000 026667 г = 2,6667∙10-23 г
mат (C) = 0,000 000 000 000 000 000 000 01993 г = 1,993∙10-23 г
2,6667 10 г
16
Аr(О) =
- 23
0,1674 10 г
-23
1,993 10-23 г
12
Аr(C) =
- 23
0,1674 10 г
11.
II. Нахождение Ar с помощью периодическойсистемы.
Правила округления:
- если после запятой стоит цифра меньше 5, то число остается без
изменения.
- если после запятой стоит цифра 5 или больше 5 , то число
увеличивается на единицу.
Пример:
Fe
Ar(Fe)=56
55,847
Cu
63,546
Pb
Ar(Pb)=207
207,19
Ar(Fe)=64
Ag
107,868
Ar(Ag)=108
12.
Мr(Н2О) = 2∙Ar(H) + A r(O) = 2∙1 + 16 = 18Мr(Н2SО4) = ?
Мr(Ca(OH)2 = 40 + 2(16 +1) = 74
Mr(Ca(OH)2 = 40 + 16 ∙2 +1 ∙2 =74
Мr(СuOH)2CO3 = ?
Мr(HNO3) = ?
13.
Составь формулу1. 2 атома кислорода
2. 4 атома водорода
3. 5 молекул воды, каждая из которых
состоит из двух атомов водорода и одного
атома кислорода
4 .Молекула глюкозы, которая состоит
из 6 атомов углерода, 12 атомов водорода
и 6 атомов кислорода
5.Молекула уксусной кислоты состоит
из 2 атомов углерода,4 атомов водорода и
2 атомов кислорода
1 3O
4H
2
3 5H2O
4 C6H12O6
5 CHO
2
4
2
14.
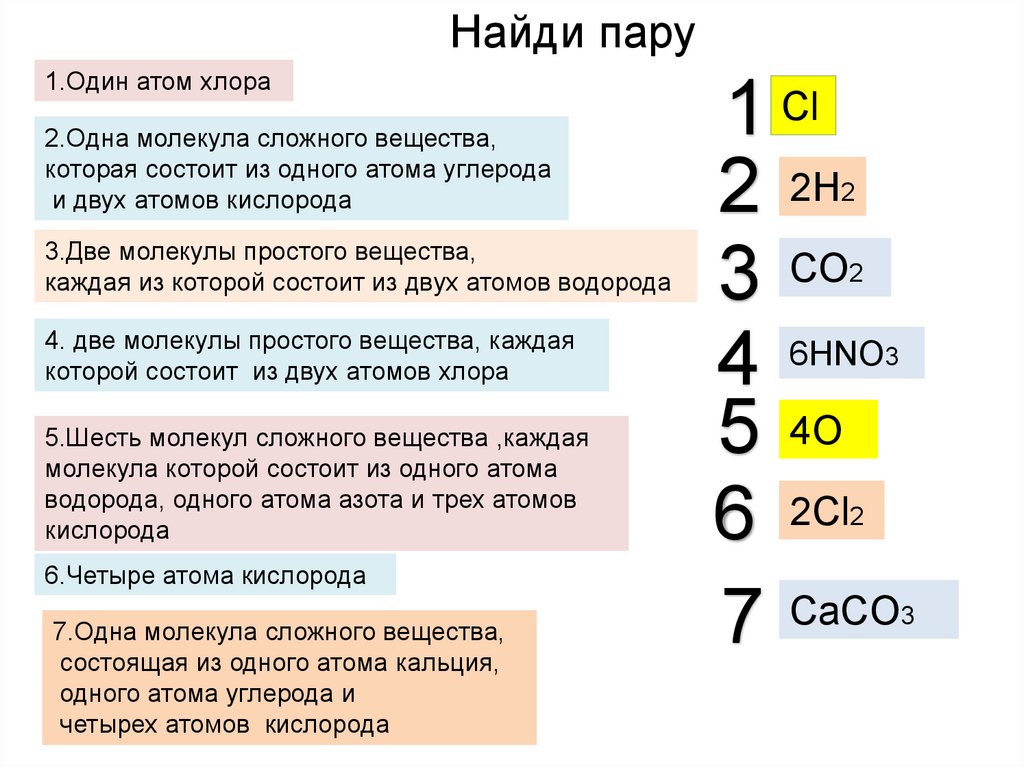
Найди пару1.Один атом хлора
2.Одна молекула сложного вещества,
которая состоит из одного атома углерода
и двух атомов кислорода
3.Две молекулы простого вещества,
каждая из которой состоит из двух атомов водорода
4. две молекулы простого вещества, каждая
которой состоит из двух атомов хлора
5.Шесть молекул сложного вещества ,каждая
молекула которой состоит из одного атома
водорода, одного атома азота и трех атомов
кислорода
6.Четыре атома кислорода
7.Одна молекула сложного вещества,
состоящая из одного атома кальция,
одного атома углерода и
четырех атомов кислорода
1 Cl
2 2H
3 CO
4 6HNO
5 4O
6 2Cl
7 CaCO
2
2
3
2
3
15. Домашнее задание
• 1.Прочитать § 6, 7• 2.Найти относительную
молекулярную массу молекулы
белка мела:
Мr (Са2CO3)-?
16. Вопросы
• 1.Я узнал много нового• 2.На уроке было над чем подумать
• 3.Думаю,что мне это пригодится в жизни
• 4.На все возникшие вопрос я получил(а)
ответы
• 5.Я поработал(а) добросовестно












 Химия
Химия








