Похожие презентации:
Химические формулы. Относительная молекулярная масса вещества
1.
2.
ПРОВЕРОЧНЫЙ ТЕСТЗадание : подбери соответствие.
1.Аргентум
2.Аурум
3.Гидраргирум
4.Силициум
5.Натрий
6.Плюмбум
7.Фосфор
8.Кальций
9.Купрум
10.Феррум
а)
б)
в)
г)
д)
е)
ж)
з)
и)
к)
Ag
Cu
Fe
Cа
Na
Hg
Pb
Р
Si
Au
3. ОТВЕТЫ
• 1-а• 2-к
• 3-е
• 4-и
• 5-д
• 6-ж
• 7-з
• 8-г
• 9-б
• 10-в
4.
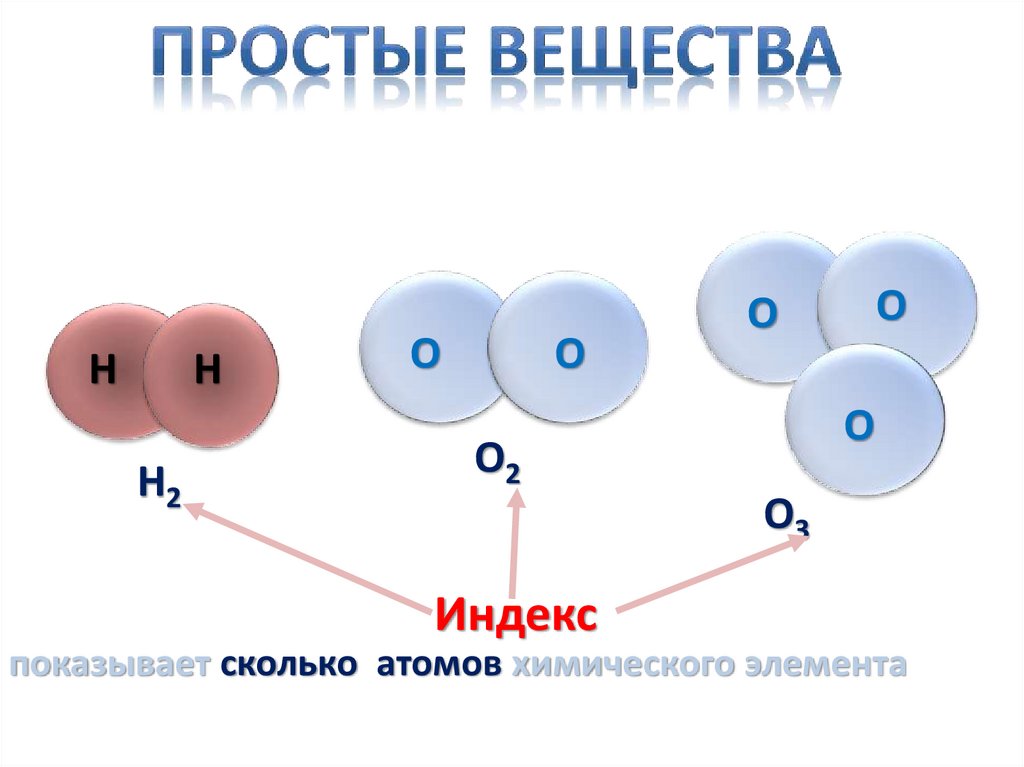
НН
Н2
О
О
О
О
О
O2
O3
Индекс
показывает сколько атомов химического элемента
5.
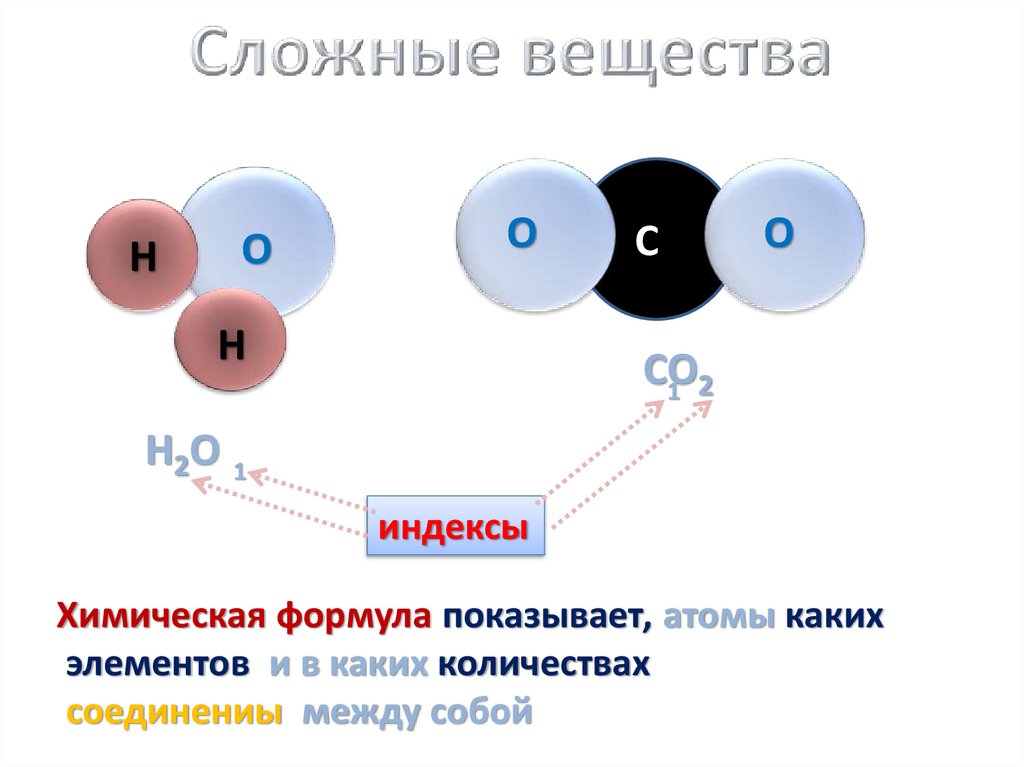
НО
О
Н
С
О
СО
1 2
Н2О 1
индексы
Химическая формула показывает, атомы каких
элементов и в каких количествах
соединениы между собой
6.
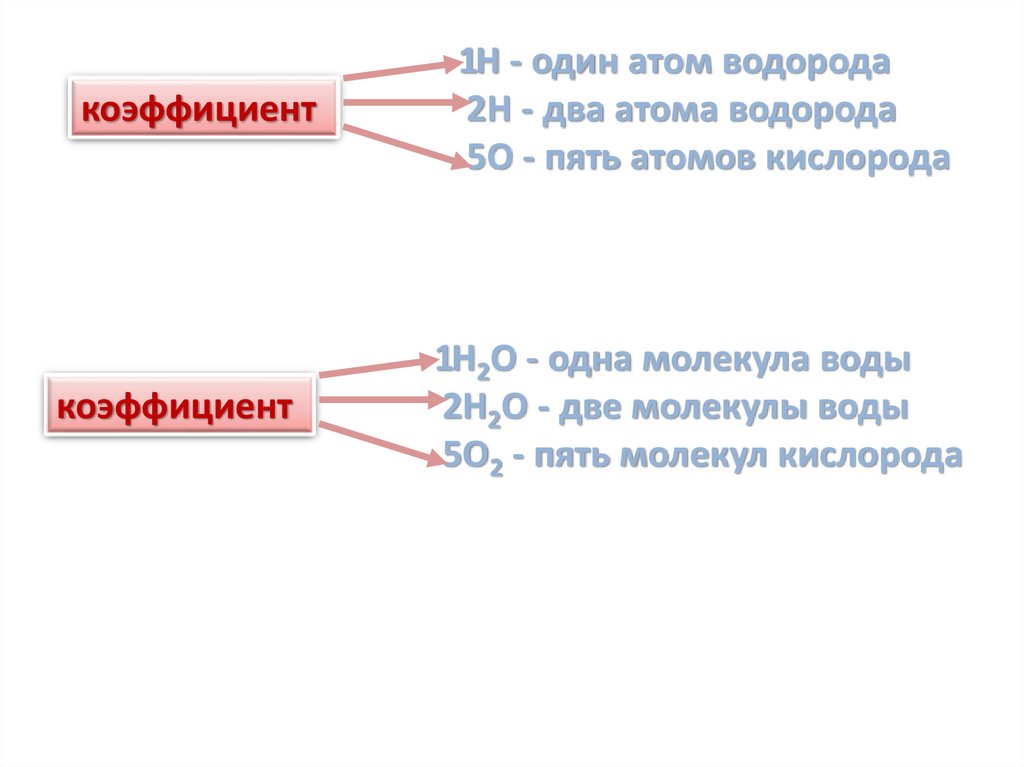
коэффициенткоэффициент
1Н - один атом водорода
2Н - два атома водорода
5О - пять атомов кислорода
1Н2О - одна молекула воды
2Н2О - две молекулы воды
5О2 - пять молекул кислорода
7.
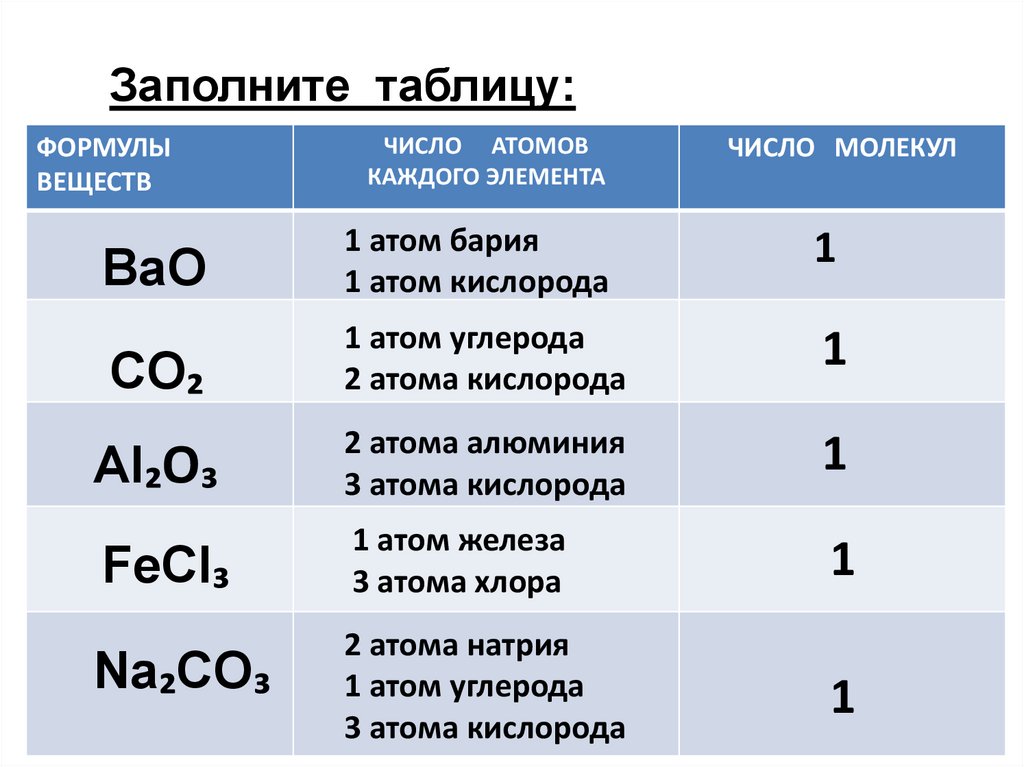
Заполните таблицу:ФОРМУЛЫ
ВЕЩЕСТВ
ЧИСЛО АТОМОВ
КАЖДОГО ЭЛЕМЕНТА
ЧИСЛО МОЛЕКУЛ
BaO
1 атом бария
1 атом кислорода
1
CO₂
1 атом углерода
2 атома кислорода
1
Al₂O₃
2 атома алюминия
3 атома кислорода
1
FeCl₃
1 атом железа
3 атома хлора
1
Na₂CO₃
2 атома натрия
1 атом углерода
3 атома кислорода
1
8.
ФОРМУЛЫ ВЕЩЕСТВ ЧИСЛО МОЛЕКУЛЧИСЛО АТОМОВ
КАЖДОГО ЭЛЕМЕНТА
3BaO
3
3 атома бария
3 атома кислорода
2CO₂
2
2 атома углерода
4 атома кислорода
5Al₂O₃
5
10 атомов алюминия
15 атомов кислорода
4FeCl₃
4
Na₂CO₃
1
4 атома железа
12 атомов хлора
2 атома натрия
1 атом углерода
3 атома кислорода
9.
mат (Н) = 0,000 000 000 000 000 000 000 001674 г = 0,1674∙10-23 гmат (О) = 0,000 000 000 000 000 000 000 026667 г = 2,6667∙10-23 г
mат (C) = 0,000 000 000 000 000 000 000 01993 г = 1,993∙10-23 г
2,6667 10-23 г
Аr(О) =
16
- 23
0,1674 10 г
Аr(C) =
1,993 10-23 г
12
- 23
0,1674 10 г
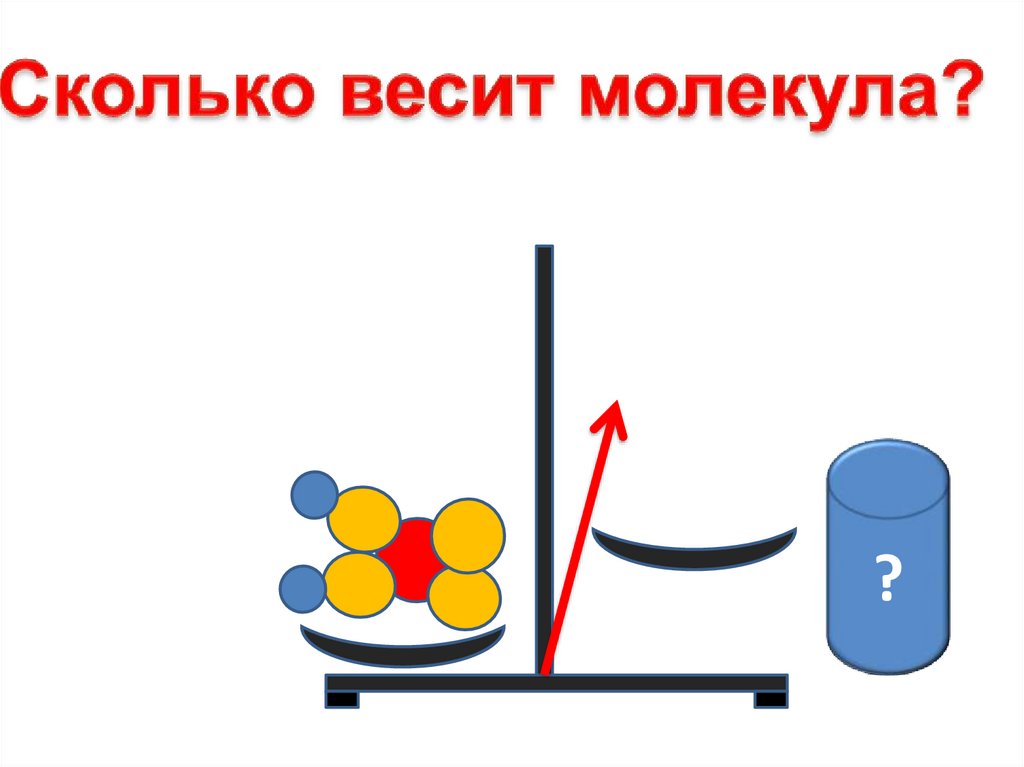
10.
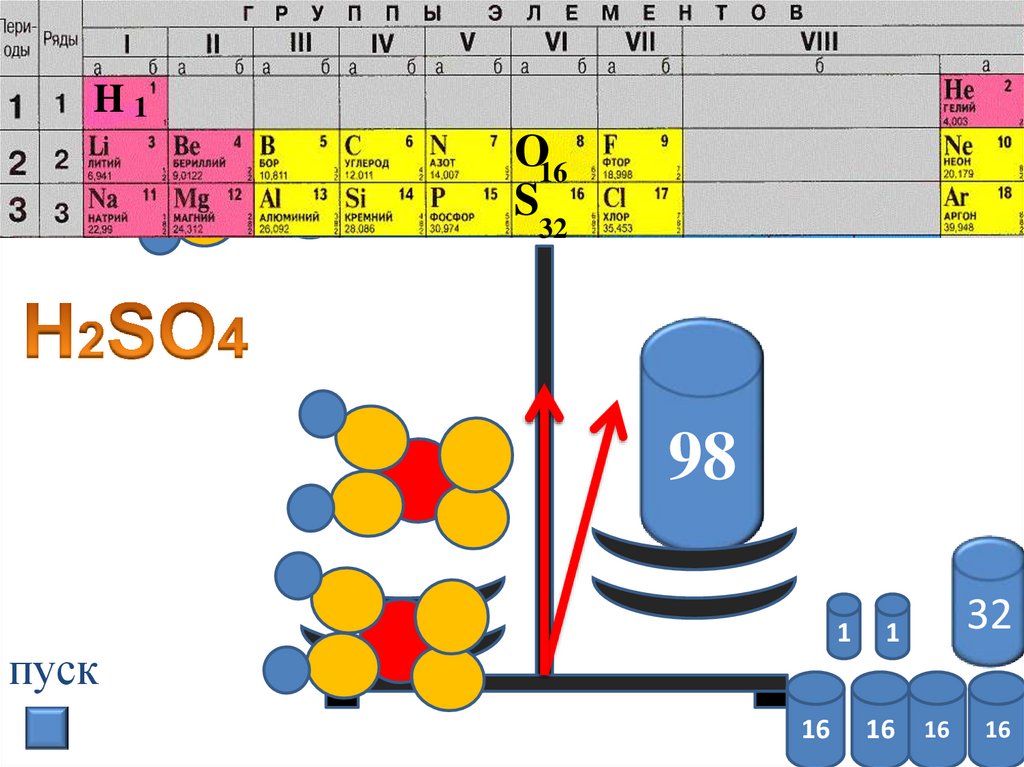
?11.
H1О16
S
32
98
1
пуск
16
32
1
16
16
16
12.
Масса молекулярнаяПонятие относительное.
Смысл её физический
Совсем не удивительный.
Массу чтоб молекулы быстренько сравнить,
Нужно на двенадцатую часть углерода разделить.
Mr
m (в-ва)
Mr (в-ва)= -----------------1/12 m (C)
Ты молекулярную
Массу рассчитай:
Атомные массы
Вместе все слагай
И на число атомов
При этом умножай.
13.
Mr(Na₂O) = 2 · Ar(Na) + Ar(O) = 2 · 23 + 16 = 62Mr(H₂SO₄) = 2 · 1 + 32 + 4 · 16 = 98
?
?
?
РАСЧИТАЙТЕ
ОТНОСИТЕЛЬНЫЕ
МОЛЕКУЛЯРНЫЕ МАССЫ :
Mr( H₂O) = ?
Mr(H₂O) = 2 · 1 + 16 = 18
Mr( NaCl) = ?
Mr(NaCl) = 23 + 35,5 = 58,5
14.
Мr(Н2О) = 2∙Ar(H) + A r(O) = 2∙1 + 16 = 18Мr(Н2SО4) = 2∙1 + 32 + 16·4 = 98
Мr(Al2О3) = 2∙27 + 3∙16 = 102
Мr(CO2) = 12 + 16·2 = 44
Мr(N2O) = 2∙14 + 16 = 44
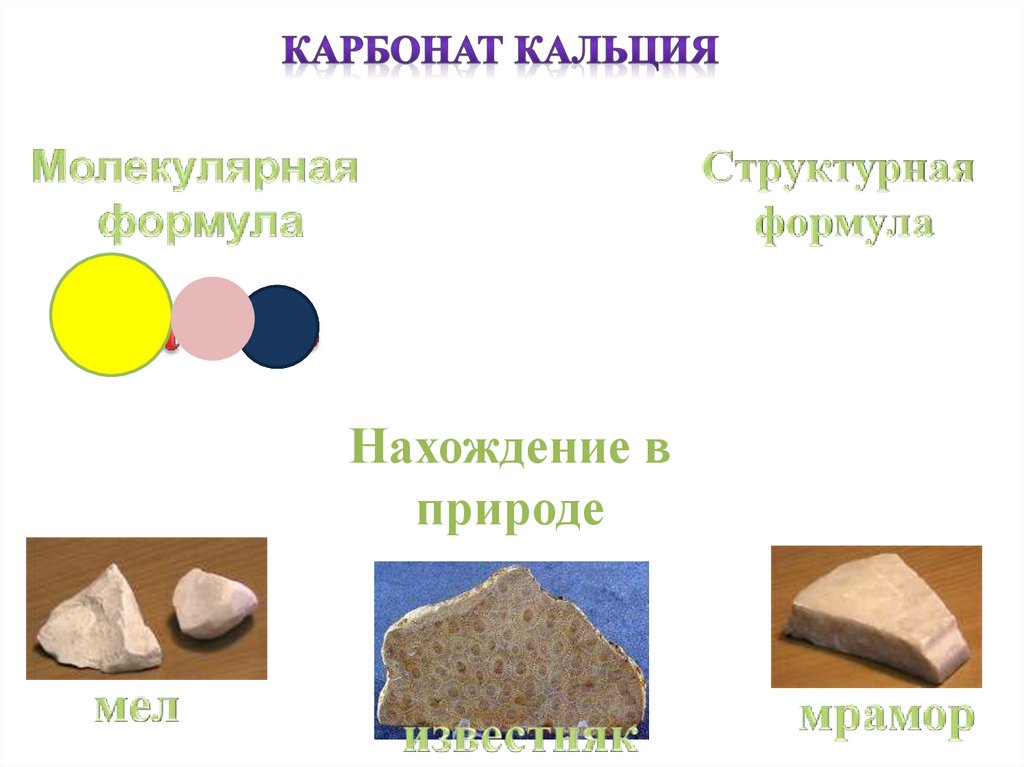
15.
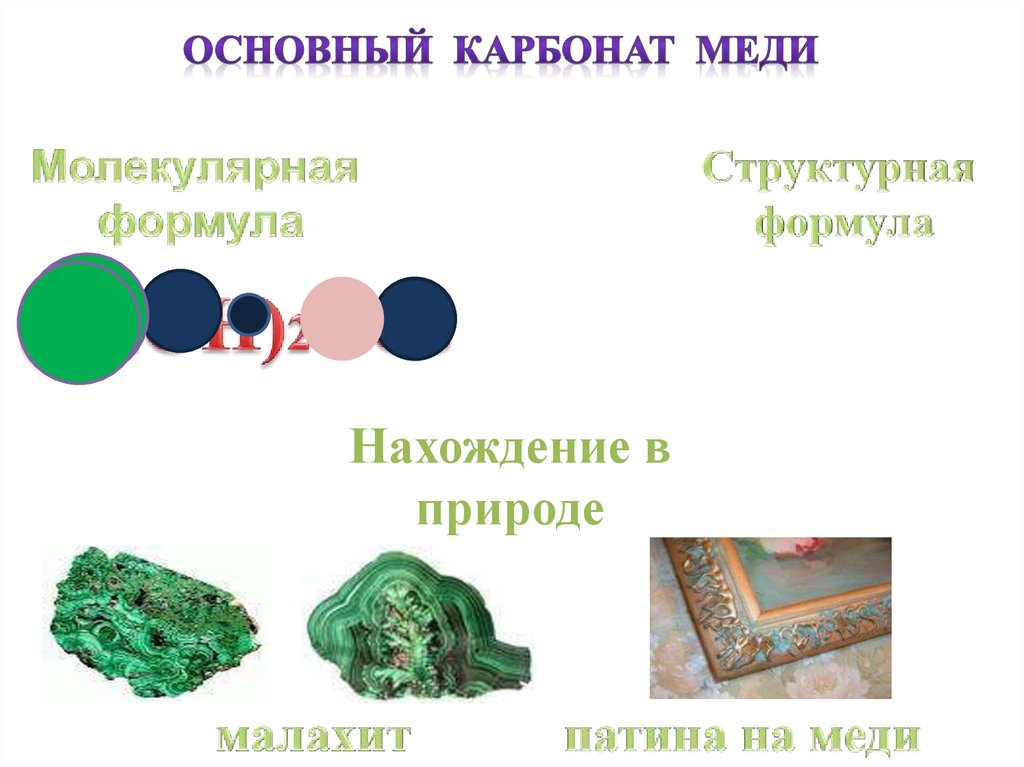
Нахождение вприроде
16.
4040
32
28 31
27
24
16
12 14
7
1
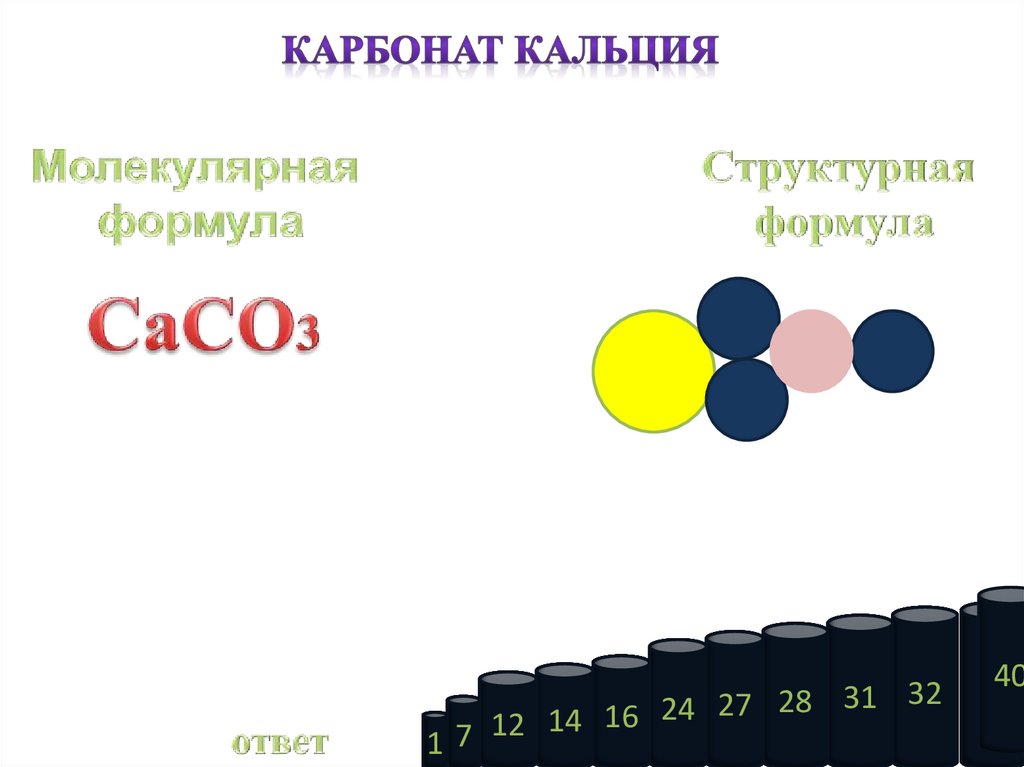
17.
Mr CaCO340 12 16·3
18.
Нахождение вприроде
19.
31 32 4028
27
24
16
16
14
12
17
64
64
20.
Mr CuOH16·3
или так
Mr CuOH
+1·2
O3
O3
64 16+1) ·2
64·2 16 ·5
21.
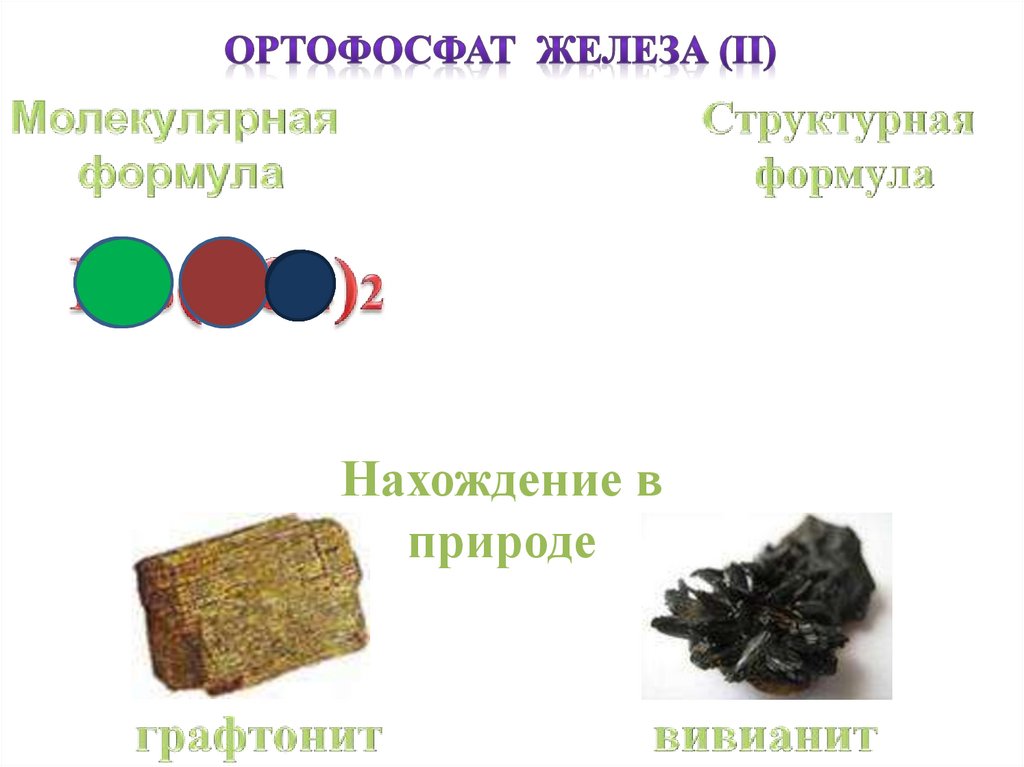
Нахождение вприроде
22.
31 32 4028
27
24
16
16
16
14
12
17
56
23.
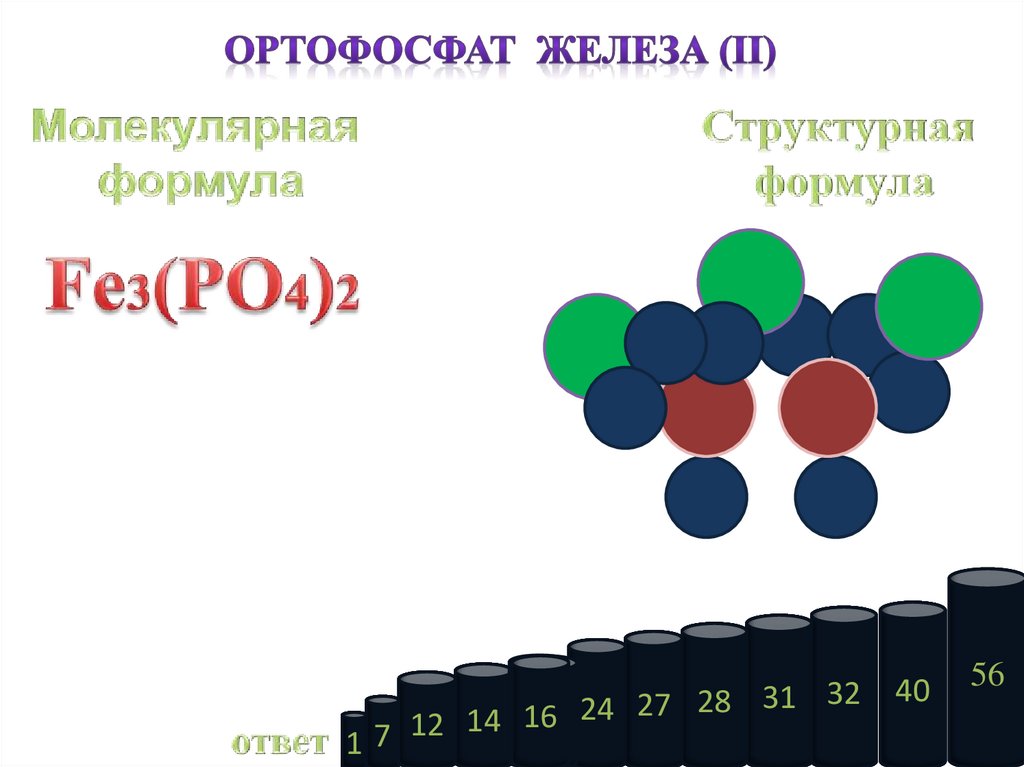
Mr Fe3 PO456·3+ 31 16·4) ·2
или так
Mr Fe3 PO4
56·3+31·2 16·8








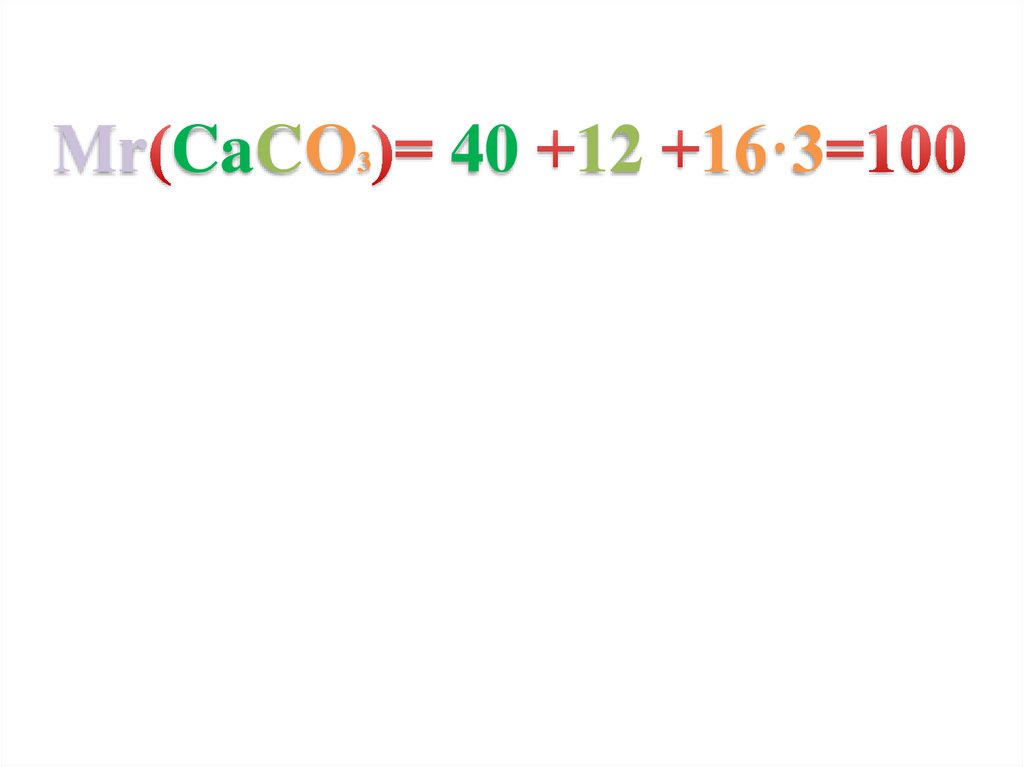

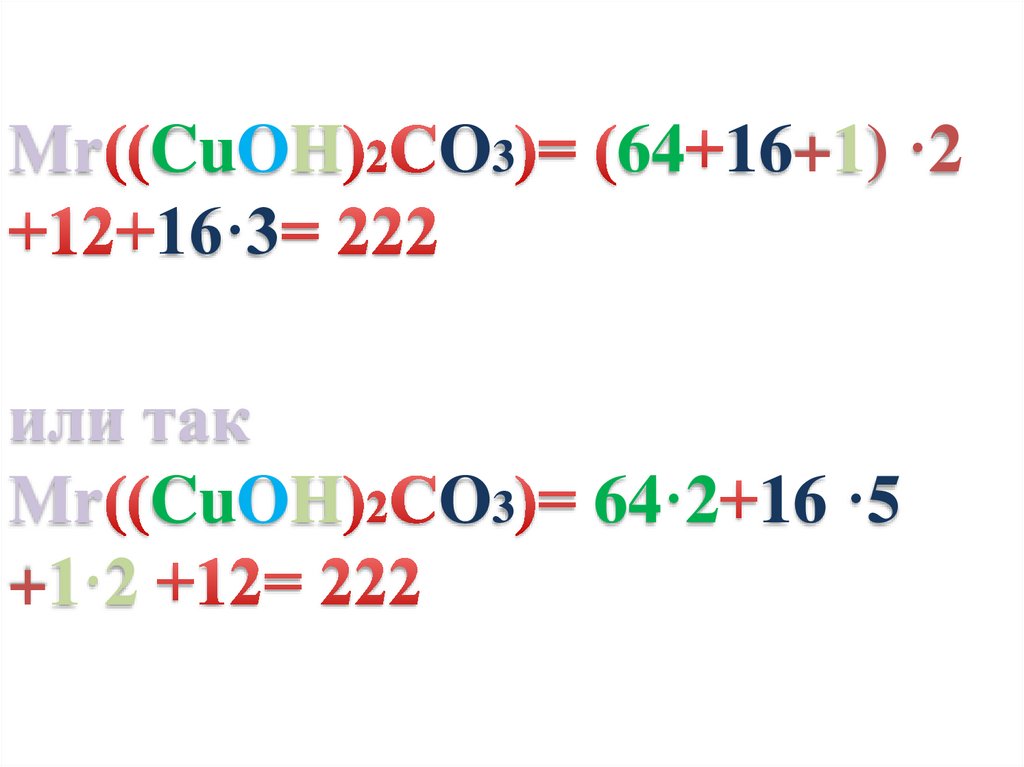


 Химия
Химия








