Похожие презентации:
Классификация веществ. Урок химии в 11 классе
1. Классификация веществ
Урок химии в 11 классеМуртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
2. Цели урока
Обобщить знания учащихся о классахнеорганических и органических
соединений.
Продолжить формирование умений
сравнивать, анализировать, делать
выводы.
Установить взаимосвязь строения и
свойств веществ.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
3.
Самая простая классификкация вешествзаключается в том, что все известные
вещества делят на неорганические и
органические.
К органическим веществам относят все
углеводороды и их производные.
Все остальные вещества –
неорганические вещества.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
4. Классификация неорганических веществ
Неорганическиевещества
Простые вещества
09.10.2024
Сложные вещества
Муртузалиев А.М. МКОУ
"Некрасовская СОШ"
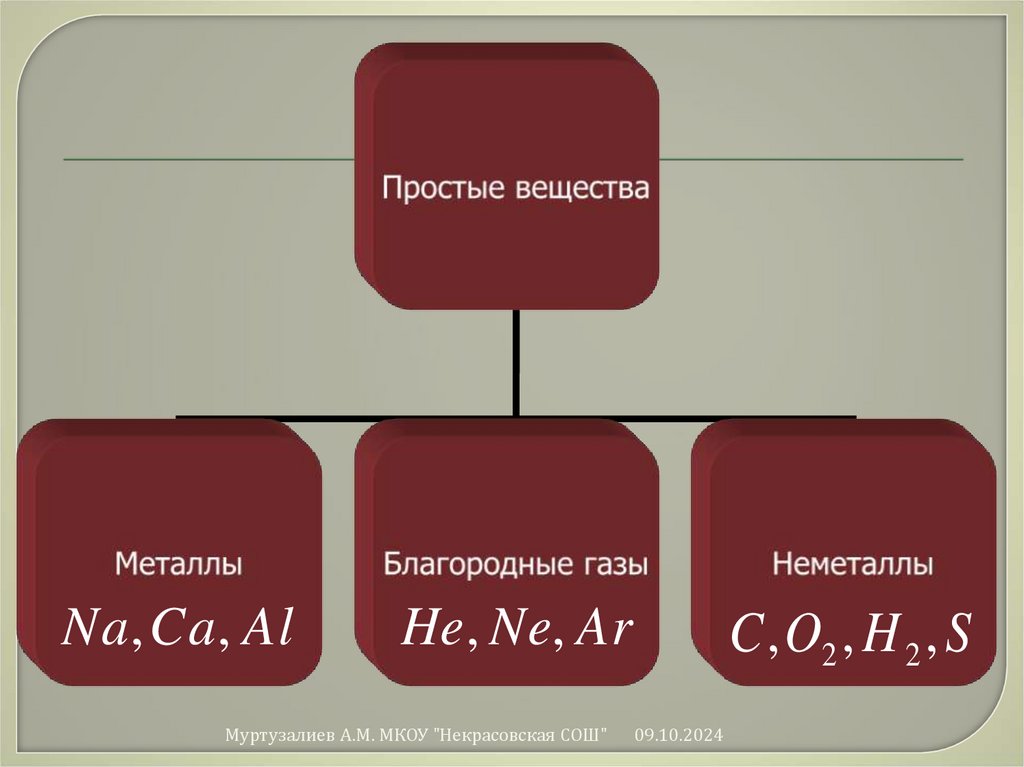
5.
Простые вещества состоят из атомоводного химического элемента и
подразделяются на металлы,
неметаллы и благородные (инертные)
газы.
Сложные вещества состоят из
атомов разных элементов,
химически связанных
друг с другом.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
6.
Na , Ca , AlHe , Ne, Ar
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
C , O2 , H 2 , S
09.10.2024
7.
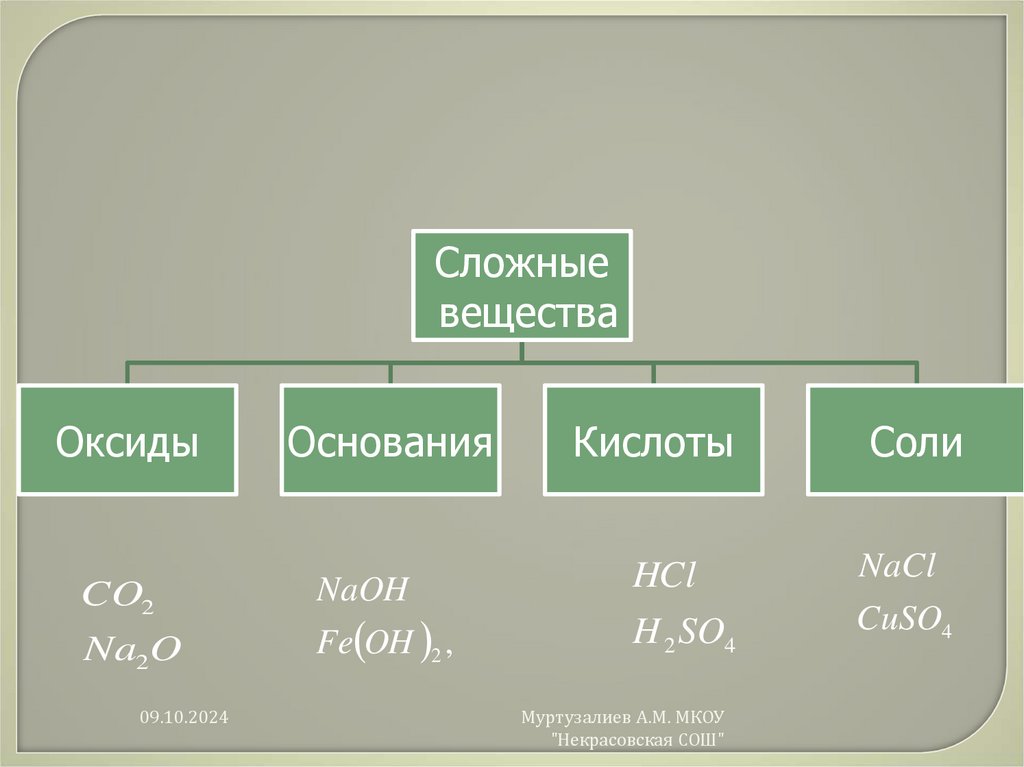
Сложныевещества
Оксиды
CO2
Na2O
09.10.2024
Основания
NaOH
Fe OH 2 ,
Кислоты
Соли
HCl
H 2 SO4
NaCl
CuSO4
Муртузалиев А.М. МКОУ
"Некрасовская СОШ"
8.
Оксиды- этоОксиды
сложные вещества,
состоящие из двух
элементов, один из
которых кислород в
степени окисления - Несолеобразующие
2.
Общая формула: Э O
Солеобразующие
m n
Основные
09.10.2024
Амфотерные
Муртузалиев А.М. МКОУ
"Некрасовская СОШ"
Кислотные
9. Оксиды ЭаОс - ?
ОсновныеКислотные
Амфотерные
СаО
СО2
Al2O3
К2О
Р2О5
ZnO
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
10.
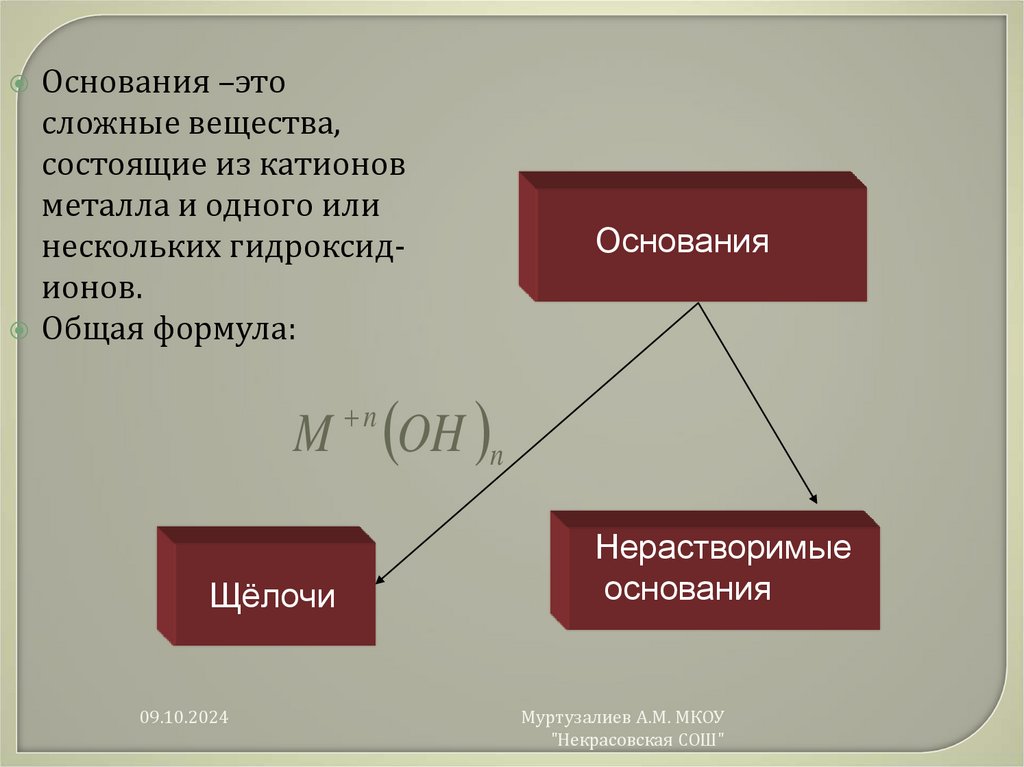
Основания –этосложные вещества,
состоящие из катионов
металла и одного или
нескольких гидроксидионов.
Общая формула:
M
Щёлочи
09.10.2024
n
Основания
OH n
Нерастворимые
основания
Муртузалиев А.М. МКОУ
"Некрасовская СОШ"
11. Основания М(ОН)x - ?
Растворимые(щелочи,10)
Нерастворимые
NaOH
Cu(OH)2
Ba(OH)2
Cr(OH)2
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
12.
Амфотерные гидроксиды проявляют исвойства кислот и оснований, поэтому
можно записывать в двух видах:
Zn(OH)2 или H2ZnO2 –гидроксид цинка
Be(OH)2 или H2BeO2 – гидроксид
бериллия
AL(OH)3 или H3AlO3 – гидроксид
алюминия
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
13.
Кислоты -это сложныевещества, состоящие из
атомов водорода,
способных замещаться
на атомы металла, и
кислотных остатков.
Кислоты
Общая формула:
x
H Ac
x
,
гдеAc кислотный
остаток
09.10.2024
Бескислородные
Муртузалиев А.М. МКОУ
"Некрасовская СОШ"
Кислородсодержащие
14. Кислоты НxАс -?, Ас- кислотный остаток(acid-кислота)
КислотыКислородсодержащие
H2SO4
Бескислородные
HCl, HF
HNO3
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
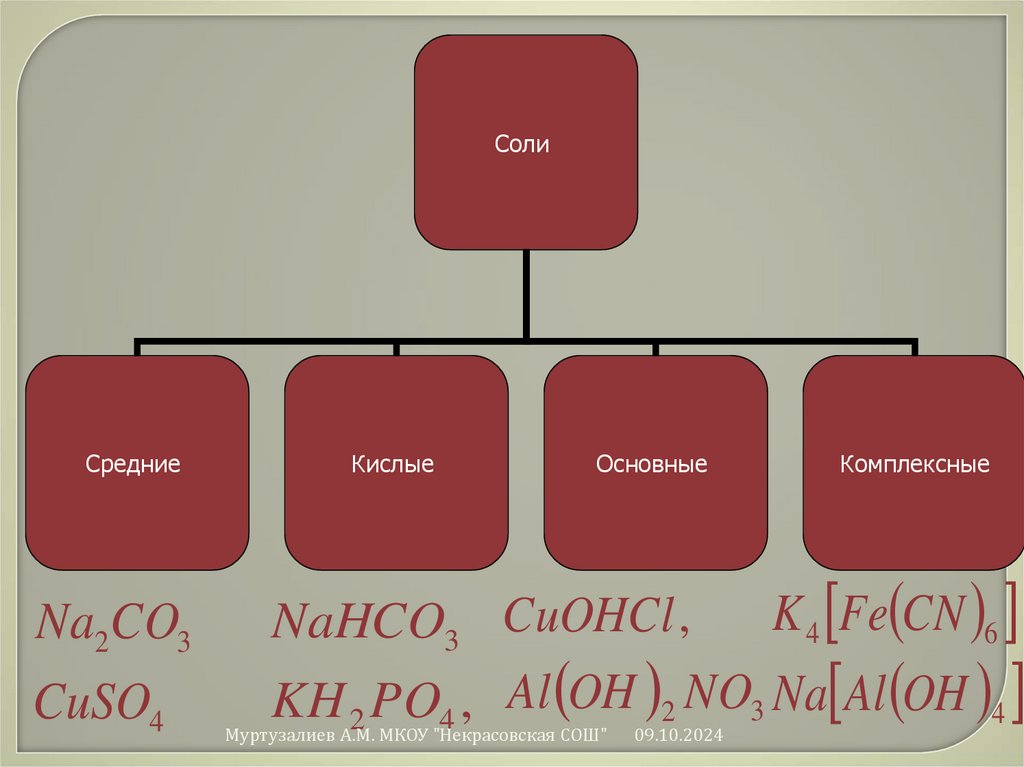
15. Соли
Средние соли- это сложные вещества, состоящие изкатионов металла и анионов кислотных остатков.
Средние соли – это продукты полного замещения
атомов водорода в молекуле кислоты атомами металла
или полного замещения гидроксигрупп в молекуле
основания кислотными остатками.
Кислые соли- это сложные вещества, состоящие из
катионов металла и водорода и анионов кислотного
остатка.
Основные соли- это сложные вещества, состоящие из
катионов металла и анионов кислотного остатка и
гидроксильной группы
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
16.
СолиСредние
Na2CO3
CuSO4
Кислые
Основные
Комплексные
K 4 Fe CN 6
NaHCO3 CuOHCl ,
KH 2 PO4 , Al OH 2 NO3 Na Al OH 4
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
17. Соли Мx(Ас)y -?
СредниеКислые
Основные
BaSO4
NaHSO3
CuOHCl
Al(NO3)3
Ca(HCO3)2
Al(OH)2Br
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
18. Классификация неорганических веществ
ВеществаСложные
Простые
основные
оксиды
несолеобразующие
амфотерные
солеобразующие
кислотные
основания
Растворимые(щелочи)
Амфотерные
гидроксиды
нерастворимые
кислоты
соли
металлы
Благородные
газы
бескислородные
кислородсодержащие
основные
средние
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
кислые
неметаллы
комплексные
09.10.2024
19. Классификация органических веществ
УглеводородыКислородсодержащие соединения
Азотсодержащие соединения
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
20.
УГЛЕВОДОРОДЫАциклические
(алифатические)
алканы
циклические
Карбоцикличес
кие соединения
Гетероцикличе
ские
алкенны
алициклические
ароматические
алкины
алкадиены
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
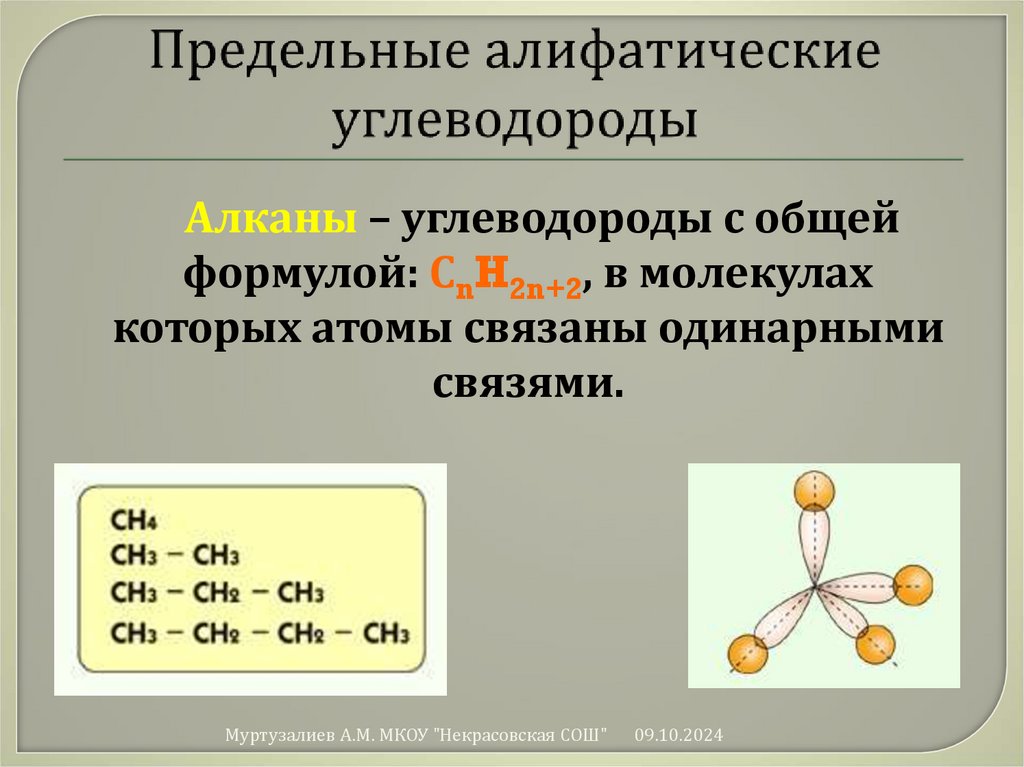
21. Предельные алифатические углеводороды
Алканы – углеводороды с общейформулой: СnH2n+2, в молекулах
которых атомы связаны одинарными
связями.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
22. Непредельные алициклические углеводороды
Алкены (этиленовые углеводороды,олефины) – непредельные
алифатические углеводороды, молекулы
которых содержат двойную связь.
Общая формула ряда алкенов СnH2n
С2Н4
С3Н6
С4Н8
СН2=СН2
этилен
(этен)
СН2=СН–СН3 СН2=СН–СН2–СН3
пропилен
(пропен)
бутилен-1
(бутен-1)
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
23.
Алкадиены – это соединения с двумядвойными связями. Общая формула
алкадиенов - СnН2n-2, причем n>3.
СН2=СН–СН=СН2
бутадиен-1,3
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
24.
Алкины – непредельные углеводороды собщей формулой CnH2n-2 . В их молекулах
одна тройная связь между атомами
углерода.
Простейший представитель –ацетилен
С2Н2
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
25.
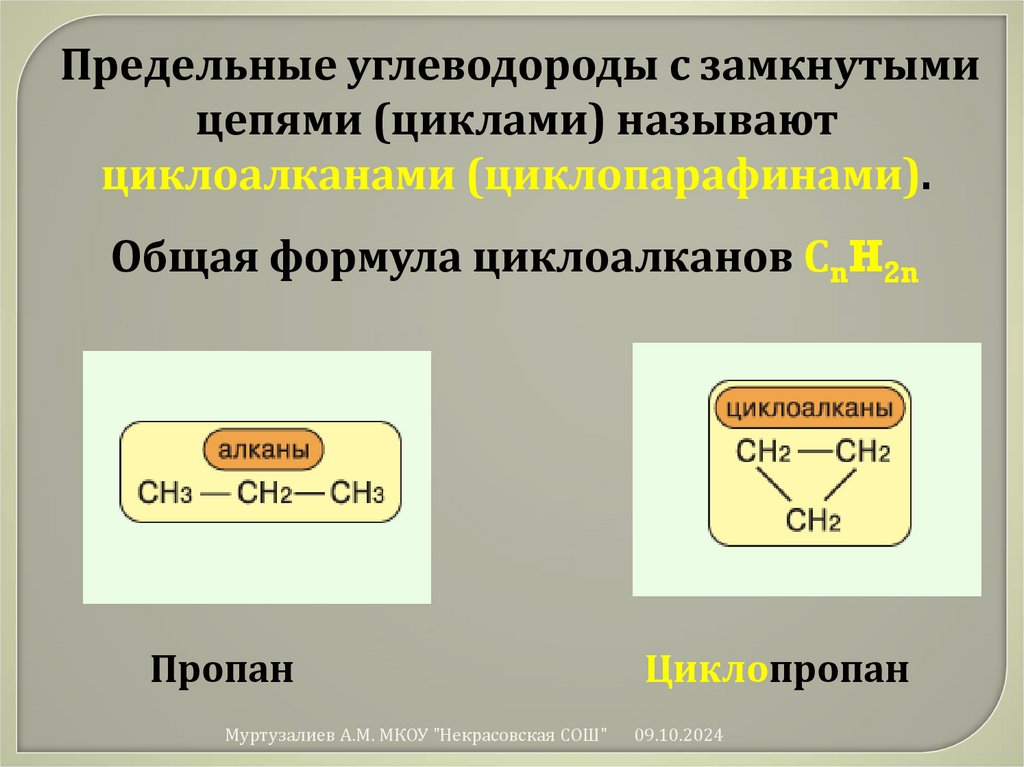
Предельные углеводороды с замкнутымицепями (циклами) называют
циклоалканами (циклопарафинами).
Общая формула циклоалканов СnH2n
Пропан
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
Циклопропан
09.10.2024
26. Бензол С6Н6 – родоначальник ароматических углеводородов.
Общая формулагомологического ряда
бензола СnH2n-6 ,
(n не менее 6).
Гомологи бензола –
соединения, образованные
заменой одного или
нескольких атомов
водорода в молекуле
бензола на углеводородные
радикалы
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
27.
Спиртами называют производные углеводородов,в молекулах которых один или несколько атомов
водорода замещены гидроксильными группами.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
28.
По числу гидроксильных групп спиртыподразделяются на одноатомные (одна группа -ОН) и
многоатомные (две и более групп -ОН). Современное
название многоатомных спиртов - полиолы (диолы,
триолы ит.д).
двухатомный спирт – этиленгликоль (этандиол-1,2)
HO–СH2–CH2–OH
трехатомный спирт – глицерин (пропантриол-1,2,3)
HO–СH2–СН(ОН)–CH2–OH
По строению радикалов, связанных с атомом кислорода
различают спирты:
предельные, или алканолы (например, СH3CH2–OH)
непредельные, или алкенолы (CH2=CH–CH2–OH)
ароматические (C6H5CH2–OH).
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
29.
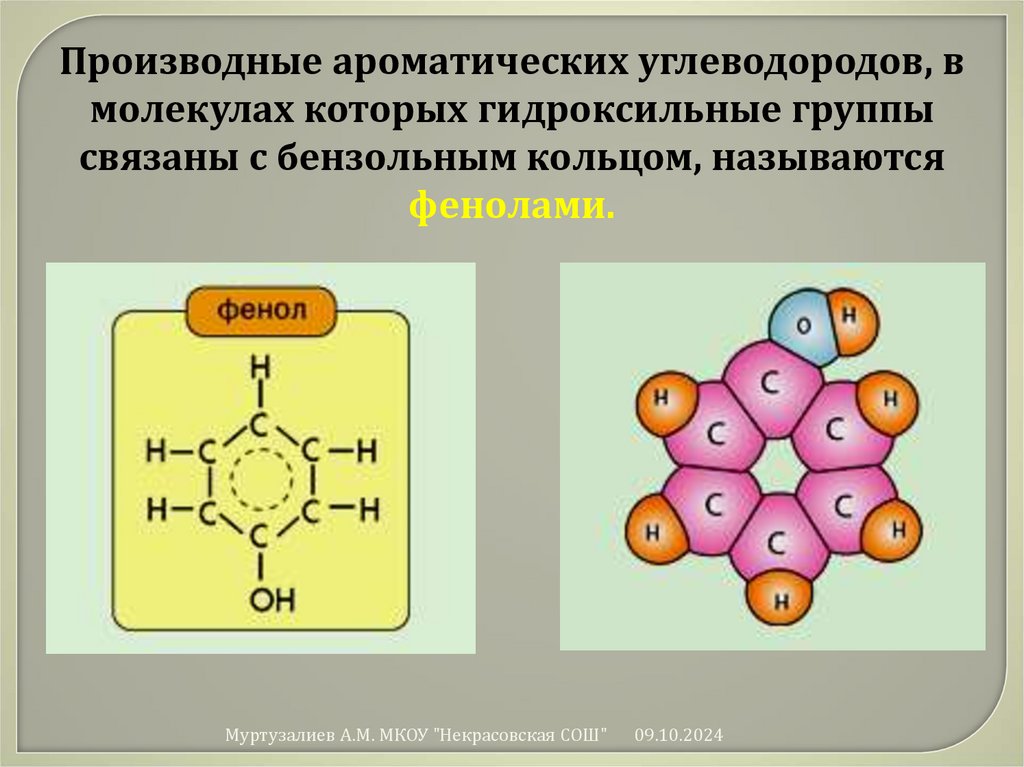
Производные ароматических углеводородов, вмолекулах которых гидроксильные группы
связаны с бензольным кольцом, называются
фенолами.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
30.
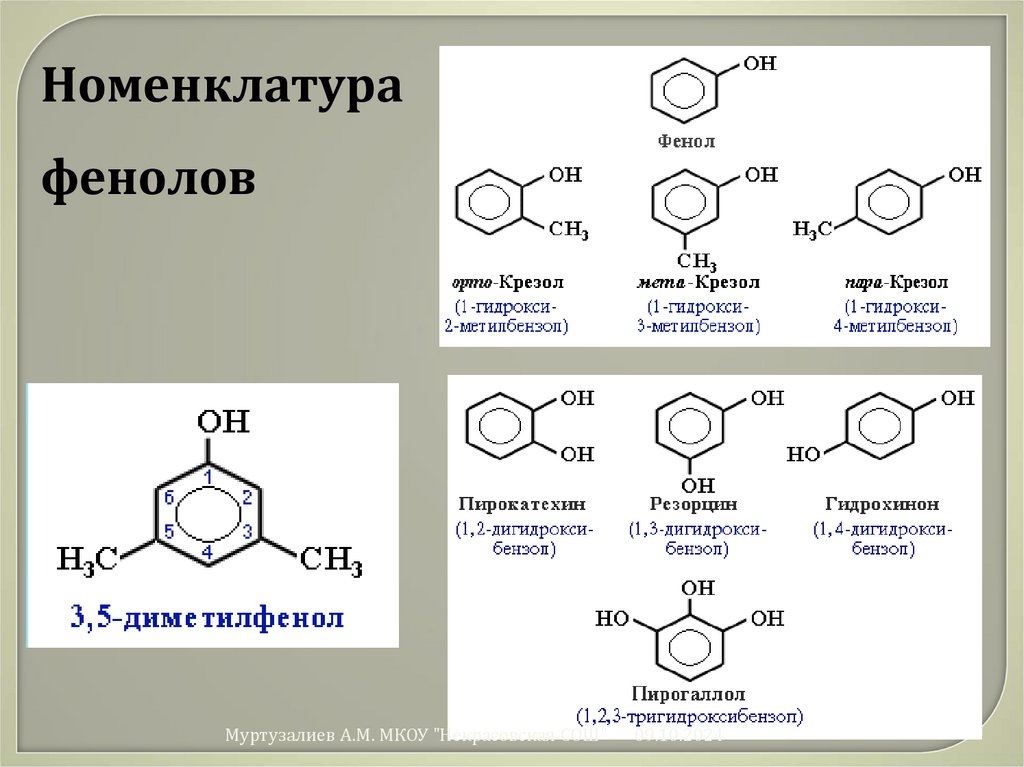
Номенклатурафенолов
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
31.
Альдегиды - это карбонильные производныеуглеводородов, в молекулах которых
присутствует альдегидная группа:
Простейшим альдегидом является муравьиный
альдегид, или формальдегид.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
32.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
33.
Межклассовыми изомерами альдегидовявляются кетоны:
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
34.
Карбоновые кислоты – это сложные органическиевещества, в которых углеводородный радикал соединён
с одной или несколькими карбоксильными группами.
Кислоты классифицируют
По радикалу:
По количеству
карбоксильных групп
•Предельные
- одноосновные
•Непредельные
- двухосновные
•Ароматические
- многоосновные
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
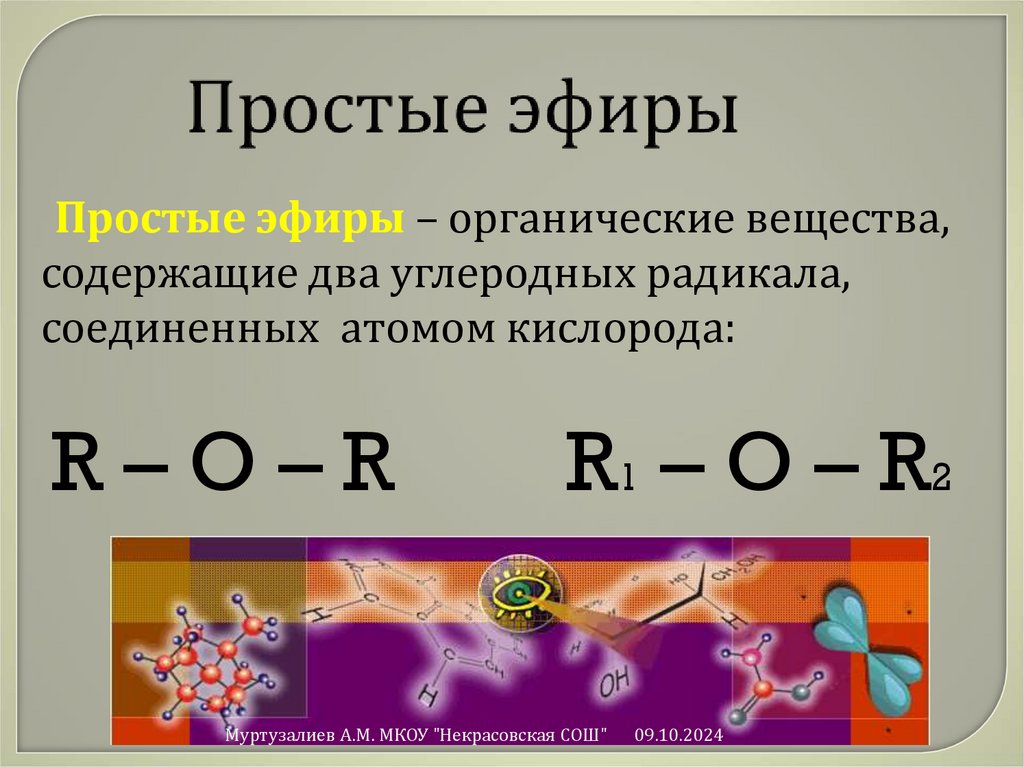
35. Простые эфиры
– органические вещества,содержащие два углеродных радикала,
соединенных атомом кислорода:
R–O–R
R1 – O – R2
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
36.
Сложными эфирами называются производныекислородосодержащих кислот, в которых
гидроксогруппы замещены остатками спирта
или фенола. Общая формула сложных эфиров:
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
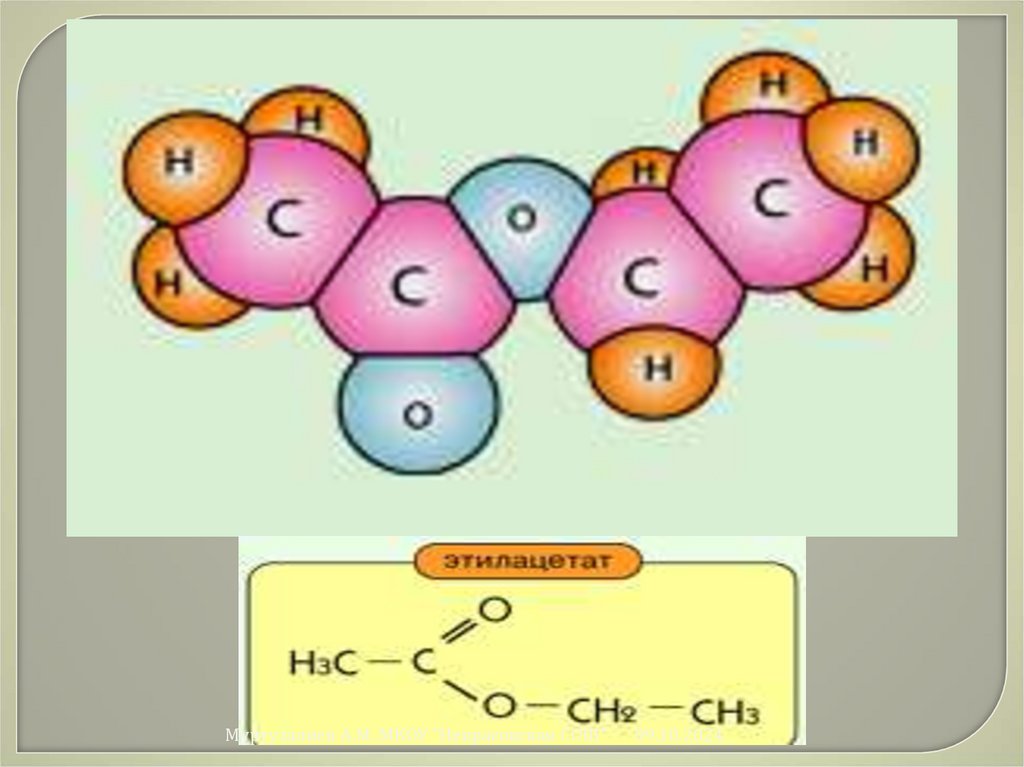
37. Свойства эфиров
Сложные эфиры представляют собойлегковоспламеняющиеся жидкости с невысокими
температурами кипения. Сложные эфиры широко
распространены в природе. Они обеспечивают
ароматы цветов и плодов.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
38.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
39.
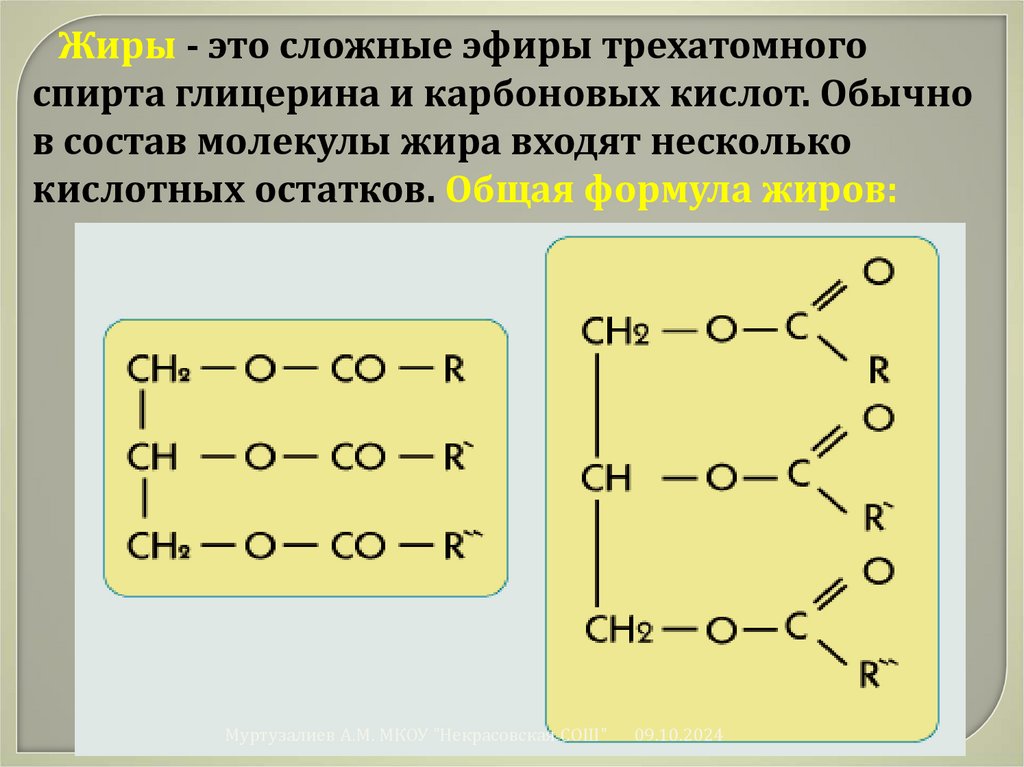
Жиры - это сложные эфиры трехатомногоспирта глицерина и карбоновых кислот. Обычно
в состав молекулы жира входят несколько
кислотных остатков. Общая формула жиров:
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
40.
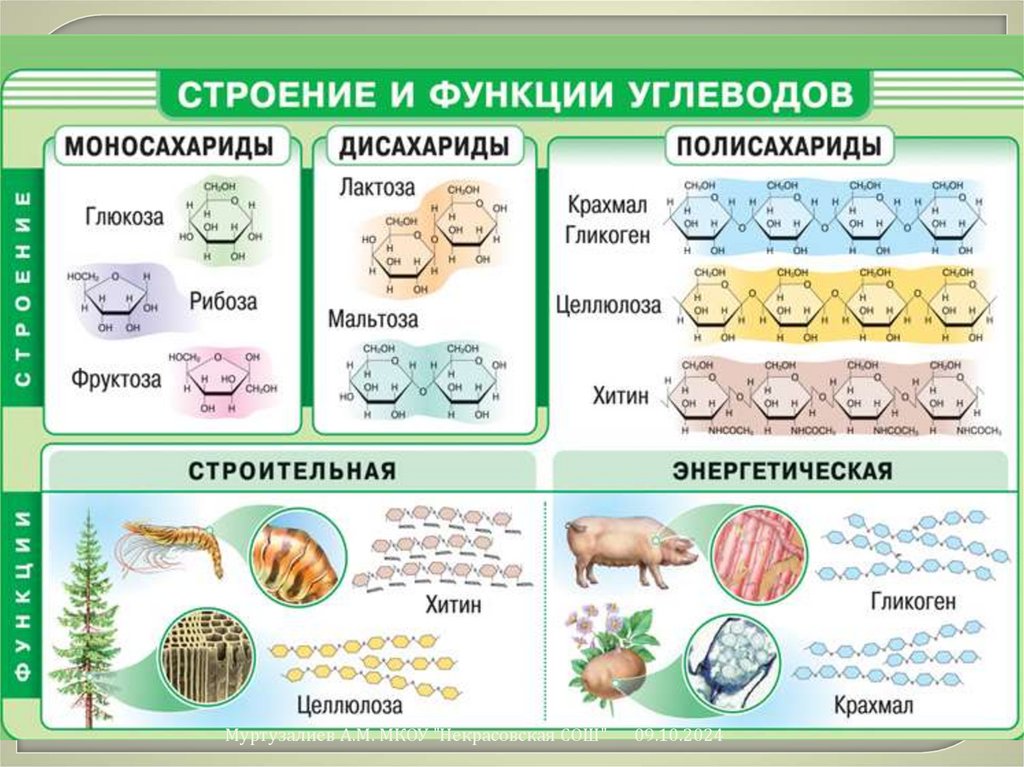
Углеводы (сахара) - органические вещества, составкоторых выражается формулой
Cx(H2O)y, где x и y 3.
По способности к гидролизу углеводы делятся на две
группы:
простые
и сложные
моносахариды;
олигосахариды и полисахариды
Углеводы образуются растениями в процессе фотосинтеза
из углекислого газа и воды.
ФОТОСИНТЕЗ:
xCO2 + yH2O + энергия Cx(H2O)y + xO2
углеводы
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
41.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
42. Азотсодержащие соединения
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
43.
Амины – это производные аммиака, вмолекуле которого один, два или три
атома водорода замещены на
углеводородный радикал.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
44. Номенклатура аминов
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
45.
Аминокислоты - это производныекислот, у которых атом водорода в
радикале замещен на аминогруппу.
Примером аминокислот может
служить 6-амино гексановая кислота.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
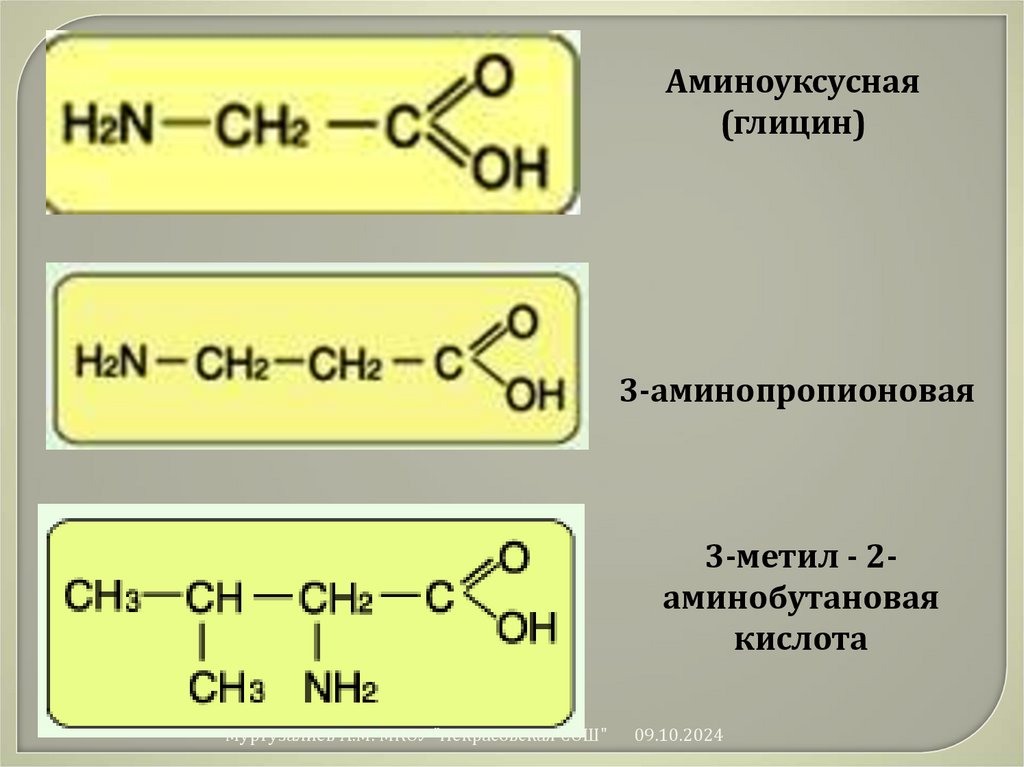
46.
Аминоуксусная(глицин)
3-аминопропионовая
3-метил - 2аминобутановая
кислота
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
47.
В зависимости от положения аминогруппыотносительно карбоксильной группы, различают -, -,
-, - и -аминокислоты. Качественной реакцией на
аминокислоты является появление фиолетовой
окраски в результате реакции с Cu(OH)2.
В состав белков входят только - аминокислоты.
-аминокислоты очень распространены в природе, так
как являются составными частями молекул белка и
основой жизни на Земле.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
48.
Белки (полипептиды) биополимеры, построенные изостатков -аминокислот, соединенных пептидными
связями.
Пептидной связью называют амидную связь –CO–NH–,
образованную при взаимодействии -аминокислот за
счет реакции между аминогруппой - NH2 одной
молекулы и карбоксильной группы -COOH – другой.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
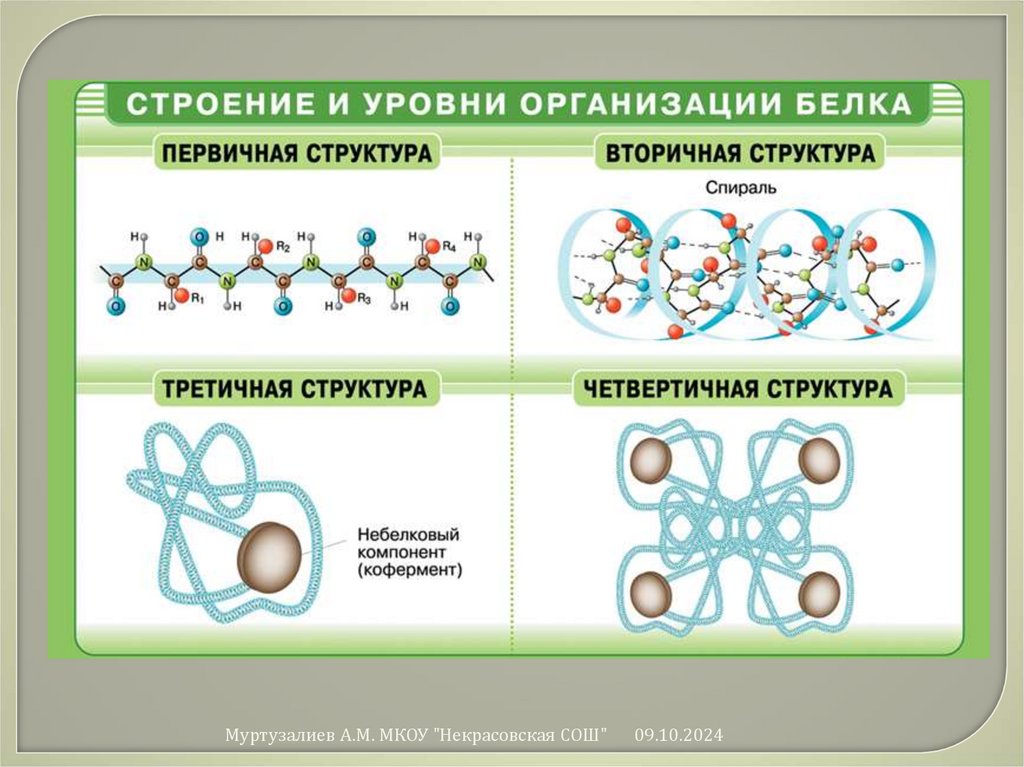
49.
Первичная структура – определенный набор ипоследовательность -аминокислотных остатков в
полипептидной цепи .
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
50.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
51.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
52.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
53.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
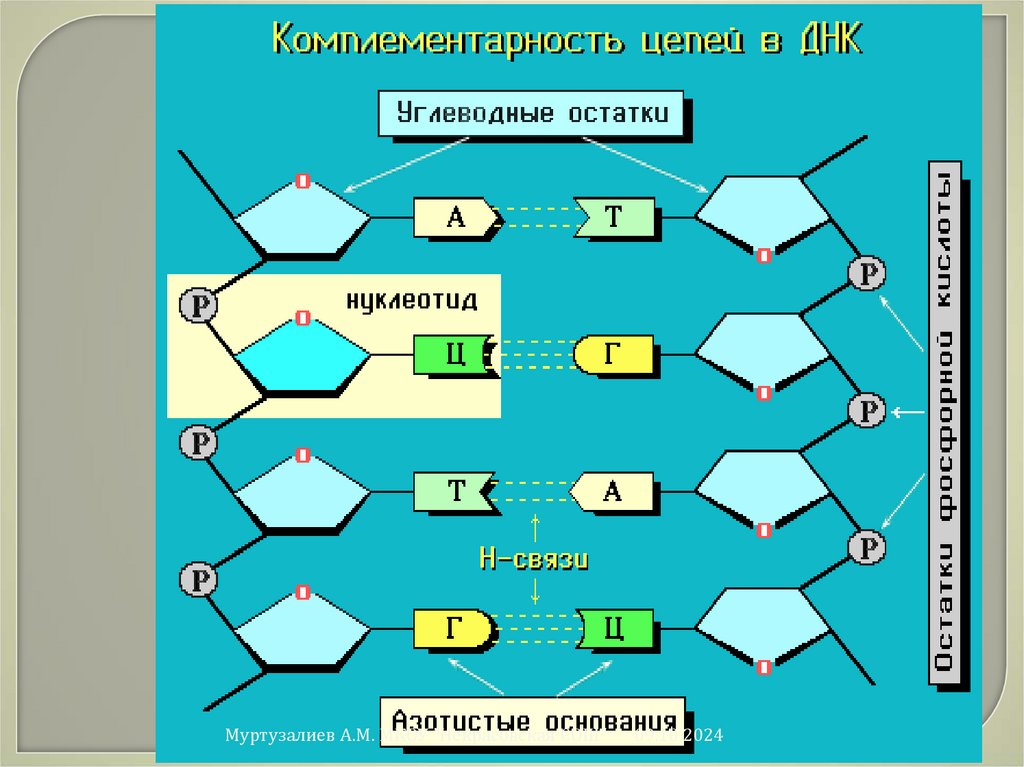
54.
Макромолекула ДНК представляет собойдве параллельные неразветвленные
полинуклеотидные цепи, закрученные
вокруг общей оси в двойную спираль.
Такая пространственная структура
удерживается множеством водородных
связей, образуемых азотистыми
основаниями, направленными внутрь
спирали. Водородные связи возникают
между пуриновым основанием одной
цепи и пиримидиновым основанием другой
цепи.
Эти основания составляют
комплементарные пары (от лат.
complementum - дополнение).
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
55.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"09.10.2024
56.
Способность ДНК не толькохранить, но и использовать
генетическую информацию
определяется следующими ее
свойствами:
1. Молекулы ДНК способны к
репликации (удвоению), т.е.
могут обеспечить
возможность синтеза других
молекул ДНК, идентичных
исходным .
2. Молекулы ДНК могут
направлять совершенно
точным и определенным
образом синтез белков,
специфичных для
организмов данного вида.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
57. Изомерия
Явление изомерии состоит в том, чтомогут существовать несколько разных по
свойствам веществ, имеющих
одинаковый состав молекул, но разное
строение. Эти вещества называются
изомерами.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
58.
Структурная изомерия1. Изомерия положения сопряженных двойных связей:
СН2=СН–СН=СН–СН2–СН3 СН3–СН=СН–СН=СН–СН3
гексадиен-1,3
гексадиен-2,4
2. Изомерия углеродного скелета:
СН2=СН–СН=СН–СН3
пентадиен-1,3
СН2=С–СН=СН2
СН3
2-метилбутадиен-1,3 (изопрен)
3. Межклассовая изомерия с алкинами и циклоалкенами.
Например, формуле С4Н6 соответствуют следующие
соединения:
СН = СН
СН2=СН–СН=СН2
СН С–СН2–СН3
СН2 –СН2
бутадиен-1,3
бутин-1
циклобутен
4.Пространственная изомерия -?
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024
59. Закрепление
1.2.
3.
Напишите структурные формулы
состава С4Н10О.
Какие вещества имеют двойственную
номенклатуру? Привести примеры
таких веществ.
Написать по три примера изомеров и
гомологов 4-метил-2-аминогексановой
кислоты.
Муртузалиев А.М. МКОУ "Некрасовская СОШ"
09.10.2024











































 Химия
Химия








